Клиническая иммунология Основные задачи клинической

































ЛЕКЦИЯ Клиническая иммунология.ppt
- Количество слайдов: 44
 Клиническая иммунология
Клиническая иммунология
 Основные задачи клинической иммунологии 1. Изучение и моделирование функций иммунной системы в норме 2. Оценка иммунного статуса. Мониторинг состояния иммунной системы. 3. Выявление болезней иммунной системы, анализ иммунопатогенеза различных заболеваний 4. Иммунокоррекция 5. Иммунопрофилактика (вакцинация) 6. Иммуноэпидемиология
Основные задачи клинической иммунологии 1. Изучение и моделирование функций иммунной системы в норме 2. Оценка иммунного статуса. Мониторинг состояния иммунной системы. 3. Выявление болезней иммунной системы, анализ иммунопатогенеза различных заболеваний 4. Иммунокоррекция 5. Иммунопрофилактика (вакцинация) 6. Иммуноэпидемиология
 Иммунный статус – комплекс количественных и качественных показателей иммунной системы в данный момент времени. Иммунный статус определяют с помощью стандартных, доступных, общепринятых тестов, позволяющих получить ориентировочные сведения об общих параметрах иммунной системы.
Иммунный статус – комплекс количественных и качественных показателей иммунной системы в данный момент времени. Иммунный статус определяют с помощью стандартных, доступных, общепринятых тестов, позволяющих получить ориентировочные сведения об общих параметрах иммунной системы.
 Сбор иммунологического анамнеза • Одним из важнейших разделов работы врача иммунолога- аллерголога является сбор иммунологического анамнеза, в ходе которого необходимо выявить отдельные виды иммунопатологии. • В дальнейшем от правильного диагноза в многом зависит дальнейший успех в лечении заболеваний
Сбор иммунологического анамнеза • Одним из важнейших разделов работы врача иммунолога- аллерголога является сбор иммунологического анамнеза, в ходе которого необходимо выявить отдельные виды иммунопатологии. • В дальнейшем от правильного диагноза в многом зависит дальнейший успех в лечении заболеваний
 Формула крови человека • Тип клеток процент Кол-во в 1 мкл • • Лейкоциты 100 4300 -9200 • Нейтрофилы 45 -70 2000 -5800 • Моноциты 3 -11 60 -90 • Базофилы 0 -5 0 -300 • Тромбоциты - 2000000 -300000 • Лимфоциты 17 -41 1200 -3000 • ЭРИТРОЦИТЫ - 4 -5 МИЛ.
Формула крови человека • Тип клеток процент Кол-во в 1 мкл • • Лейкоциты 100 4300 -9200 • Нейтрофилы 45 -70 2000 -5800 • Моноциты 3 -11 60 -90 • Базофилы 0 -5 0 -300 • Тромбоциты - 2000000 -300000 • Лимфоциты 17 -41 1200 -3000 • ЭРИТРОЦИТЫ - 4 -5 МИЛ.
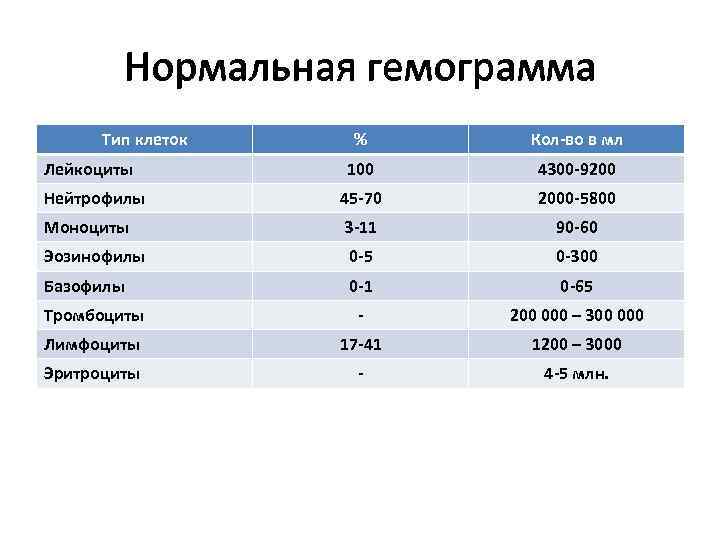
 Нормальная гемограмма Тип клеток % Кол-во в мл Лейкоциты 100 4300 -9200 Нейтрофилы 45 -70 2000 -5800 Моноциты 3 -11 90 -60 Эозинофилы 0 -5 0 -300 Базофилы 0 -1 0 -65 Тромбоциты - 200 000 – 300 000 Лимфоциты 17 -41 1200 – 3000 Эритроциты - 4 -5 млн.
Нормальная гемограмма Тип клеток % Кол-во в мл Лейкоциты 100 4300 -9200 Нейтрофилы 45 -70 2000 -5800 Моноциты 3 -11 90 -60 Эозинофилы 0 -5 0 -300 Базофилы 0 -1 0 -65 Тромбоциты - 200 000 – 300 000 Лимфоциты 17 -41 1200 – 3000 Эритроциты - 4 -5 млн.
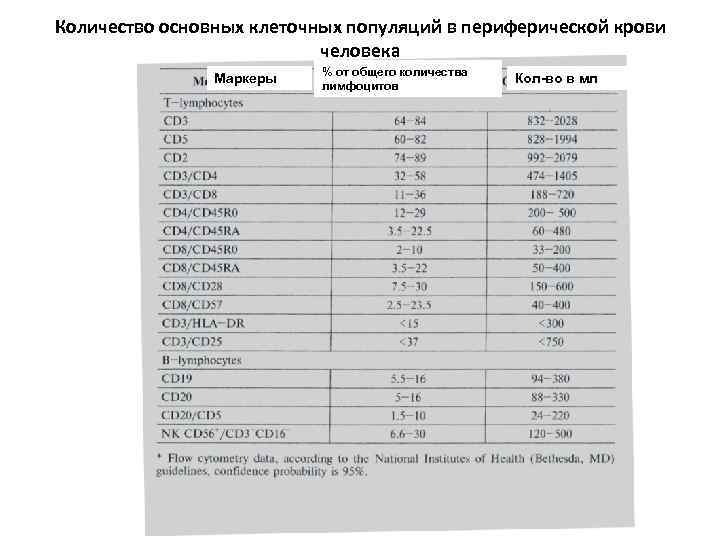
 Количество основных клеточных популяций в периферической крови человека % от общего количества Маркеры лимфоцитов Кол-во в мл
Количество основных клеточных популяций в периферической крови человека % от общего количества Маркеры лимфоцитов Кол-во в мл
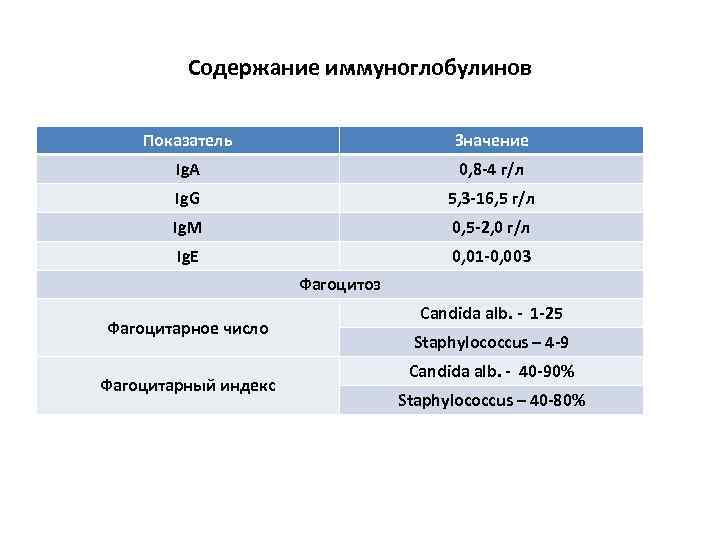
 Содержание иммуноглобулинов Показатель Значение Ig. A 0, 8 -4 г/л Ig. G 5, 3 -16, 5 г/л Ig. M 0, 5 -2, 0 г/л Ig. E 0, 01 -0, 003 Фагоцитоз Candida alb. - 1 -25 Фагоцитарное число Staphylococcus – 4 -9 Candida alb. - 40 -90% Фагоцитарный индекс Staphylococcus – 40 -80%
Содержание иммуноглобулинов Показатель Значение Ig. A 0, 8 -4 г/л Ig. G 5, 3 -16, 5 г/л Ig. M 0, 5 -2, 0 г/л Ig. E 0, 01 -0, 003 Фагоцитоз Candida alb. - 1 -25 Фагоцитарное число Staphylococcus – 4 -9 Candida alb. - 40 -90% Фагоцитарный индекс Staphylococcus – 40 -80%
 Инфекционный синдром • : • Длительный субфебрилитет (повышение температуры до 37, 0 -37, 5 С) или лихорадка; • Лимфадениты (увеличение лимф. узлов); • Бактериальные инфекции кожи и подкожной клетчатки (пиодермии, фурункулез ); • Грибковое поражение ногтей, слизистых оболочек (кандидоз);
Инфекционный синдром • : • Длительный субфебрилитет (повышение температуры до 37, 0 -37, 5 С) или лихорадка; • Лимфадениты (увеличение лимф. узлов); • Бактериальные инфекции кожи и подкожной клетчатки (пиодермии, фурункулез ); • Грибковое поражение ногтей, слизистых оболочек (кандидоз);
 • Частые ОРЗ (более 4 раз в год у взрослых и более 6 раз в год у детей), хронические и часто повторяющиеся инфекции ЛОР- органов (синуситы, отиты ), органов дыхания (бронхиты, пневмонии); • Рецидивирующий герпес (генитальный, опоясывающий лишай); • Хронические инфекции мочеполовой системы (уретриты, пиелонефриты и др. ); • Генерализованные инфекции (сепсис)
• Частые ОРЗ (более 4 раз в год у взрослых и более 6 раз в год у детей), хронические и часто повторяющиеся инфекции ЛОР- органов (синуситы, отиты ), органов дыхания (бронхиты, пневмонии); • Рецидивирующий герпес (генитальный, опоясывающий лишай); • Хронические инфекции мочеполовой системы (уретриты, пиелонефриты и др. ); • Генерализованные инфекции (сепсис)
 Аллергический синдром: • Наличие в анамнезе заболеваний кожи (экзема, крапивница, контактный дерматит), • Лор-органов (аллергический ринит), органов дыхания (бронхиальная астма) аллергического генеза; • Непереносимость пищевых продуктов , лекарств, пыльцы и др.
Аллергический синдром: • Наличие в анамнезе заболеваний кожи (экзема, крапивница, контактный дерматит), • Лор-органов (аллергический ринит), органов дыхания (бронхиальная астма) аллергического генеза; • Непереносимость пищевых продуктов , лекарств, пыльцы и др.
 Аутоиммунный синдром: • Воспаление суставов конечностей , позвоночника, крестцово-подвздошных сочленений: • Поражение кожи (геморрагические высыпания, дискоидные очаги, фотосенсибилизация), алопеция; • Указания на поражение почек (гломерулонефрит) и печени (гепатит); • Цитопения (снижение количества клеток крови)
Аутоиммунный синдром: • Воспаление суставов конечностей , позвоночника, крестцово-подвздошных сочленений: • Поражение кожи (геморрагические высыпания, дискоидные очаги, фотосенсибилизация), алопеция; • Указания на поражение почек (гломерулонефрит) и печени (гепатит); • Цитопения (снижение количества клеток крови)
 • Наследственные заболевания, чаще • выявляются у детей. • Синдром Луизы –Бар: атаксия (расстройство координации произвольных движений )+ телеангиоэктазии (локальное расширение капилляров и мелких концевых артерий)+ участки ди- и гиперпигментации; • Синдром Вискотта-Олдрича: геморрагии +экзема+тромбоцитопения. • синдром Ди Джорджи: судороги+пороки развития лицевого скелета и сердечно-сосудистой системы +гипоплазия тимуса.
• Наследственные заболевания, чаще • выявляются у детей. • Синдром Луизы –Бар: атаксия (расстройство координации произвольных движений )+ телеангиоэктазии (локальное расширение капилляров и мелких концевых артерий)+ участки ди- и гиперпигментации; • Синдром Вискотта-Олдрича: геморрагии +экзема+тромбоцитопения. • синдром Ди Джорджи: судороги+пороки развития лицевого скелета и сердечно-сосудистой системы +гипоплазия тимуса.
 Вторичные иммунодефициты • НАЛИЧИЕ ХРОНИЧЕСКИХ ИЛИ ЧАСТО ВОЗНИКАЮЩИХ ИНФЕКЦИЙ (ОСОБЕННО ВЫЗВАННЫХ УСЛОВНО ПАТОГЕННОЙ МИКРОФЛОРОЙ) • АЛОПЕЦИЯ , ДЕ- И ГИПЕРПИГМЕНТАЦИЯ КОЖИ • САРКОМА КАПОШИ
Вторичные иммунодефициты • НАЛИЧИЕ ХРОНИЧЕСКИХ ИЛИ ЧАСТО ВОЗНИКАЮЩИХ ИНФЕКЦИЙ (ОСОБЕННО ВЫЗВАННЫХ УСЛОВНО ПАТОГЕННОЙ МИКРОФЛОРОЙ) • АЛОПЕЦИЯ , ДЕ- И ГИПЕРПИГМЕНТАЦИЯ КОЖИ • САРКОМА КАПОШИ
 ЛИМФОПРОЛИФЕРАТИВНЫЙ СИНДРОМ • УВЕЛИЧЕНИЕ МНОГИХ ГРУПП ЛУ (ОНИ МОГУТ БЫТЬ СПАЯННЫМИ И НЕСПАЯННЫМИ С ОКРУЖАЮЩИМИ ТКАНЯМИ ) • ХАРАКТЕРНЫЕ ИЗМЕНЕНИЯ В ОБЩЕМ АНАЛИЗЕ КРОВИ (УВЕЛИЧЕНИЕ КОЛ-ВА ЛЦ. , ПОЯВЛЕНИЕ БЛАСТОВ, МАЛОДИФФЕРЕНЦИРОВАННЫХ КЛЕТОК) • СПЛЕНОМЕГАЛИЯ (УВЕЛИЧЕНИЕ СЕЛЕЗЕНКИ). • ЧАСТЫЕ БАКТЕРИАЛЬНЫЕ ИНФЕКЦИИ
ЛИМФОПРОЛИФЕРАТИВНЫЙ СИНДРОМ • УВЕЛИЧЕНИЕ МНОГИХ ГРУПП ЛУ (ОНИ МОГУТ БЫТЬ СПАЯННЫМИ И НЕСПАЯННЫМИ С ОКРУЖАЮЩИМИ ТКАНЯМИ ) • ХАРАКТЕРНЫЕ ИЗМЕНЕНИЯ В ОБЩЕМ АНАЛИЗЕ КРОВИ (УВЕЛИЧЕНИЕ КОЛ-ВА ЛЦ. , ПОЯВЛЕНИЕ БЛАСТОВ, МАЛОДИФФЕРЕНЦИРОВАННЫХ КЛЕТОК) • СПЛЕНОМЕГАЛИЯ (УВЕЛИЧЕНИЕ СЕЛЕЗЕНКИ). • ЧАСТЫЕ БАКТЕРИАЛЬНЫЕ ИНФЕКЦИИ
 ЛЕЙКОЦИТЫ НОРМА И ПРИЧИНЫ ОТКЛОНЕНИЯ ОТ НЕЕ. ЛЕЙКОЦИТАРНАЯ ФОРМУЛА Увеличение показателя (лейкоцитоз): • Бактериальная, вирусная, грибковая инфекции; • Злокачественные новообразования; • Лейкозы; • Действие стероидных гормонов;
ЛЕЙКОЦИТЫ НОРМА И ПРИЧИНЫ ОТКЛОНЕНИЯ ОТ НЕЕ. ЛЕЙКОЦИТАРНАЯ ФОРМУЛА Увеличение показателя (лейкоцитоз): • Бактериальная, вирусная, грибковая инфекции; • Злокачественные новообразования; • Лейкозы; • Действие стероидных гормонов;
 Снижение показателя (лимфопения): • Гипо- и аплазия костного мозга, повреждение его химическими веществами, ионизирующим излучением; • Гиперспленизм (увеличение селезенки); • Острые лейкозы; • Плазмоцитома (опухоли из плазмацитов); • Метастазы, новообразования в костный мозг; • Некоторые инфекции: тиф, корь, краснуха, ветряная оспа, сальмонелез, инфекционный мононуклеоз; • Действие лекарств: сульфаниламиды, некоторые антибиотики, нестероидные противовоспалительные препараты, противоэпилептические препараты;
Снижение показателя (лимфопения): • Гипо- и аплазия костного мозга, повреждение его химическими веществами, ионизирующим излучением; • Гиперспленизм (увеличение селезенки); • Острые лейкозы; • Плазмоцитома (опухоли из плазмацитов); • Метастазы, новообразования в костный мозг; • Некоторые инфекции: тиф, корь, краснуха, ветряная оспа, сальмонелез, инфекционный мононуклеоз; • Действие лекарств: сульфаниламиды, некоторые антибиотики, нестероидные противовоспалительные препараты, противоэпилептические препараты;
 Определение уровня иммуноглобулинов Увеличение концентрации Ig. А, Ig. М, Ig. G: • Острые, хронические, бактериальные, грибковые и паразитарные инфекции; • Хронические заболевания печени; • Системные заболевания соединительной ткани; • Хронический лимфолейкоз; • Миеломная болезнь; • Макроглобулинемия Вальденстрема
Определение уровня иммуноглобулинов Увеличение концентрации Ig. А, Ig. М, Ig. G: • Острые, хронические, бактериальные, грибковые и паразитарные инфекции; • Хронические заболевания печени; • Системные заболевания соединительной ткани; • Хронический лимфолейкоз; • Миеломная болезнь; • Макроглобулинемия Вальденстрема
 Снижение концентрации Ig. А, Ig. М, Ig. G: • Врожденная а- или гипогаммаглобулинемия (снижение или отсутствие синтеза антител); • Новообразования иммунной системы; • Удаленная селезенка; • Потеря белка при заболеваниях почек или кишечника; • Лечение цитостатиками или иммунодепрессантами; • Действие ионизирующего излучения; • Острая вирусная инфекция для Ig. A и хроническая для Ig. M и Ig. G.
Снижение концентрации Ig. А, Ig. М, Ig. G: • Врожденная а- или гипогаммаглобулинемия (снижение или отсутствие синтеза антител); • Новообразования иммунной системы; • Удаленная селезенка; • Потеря белка при заболеваниях почек или кишечника; • Лечение цитостатиками или иммунодепрессантами; • Действие ионизирующего излучения; • Острая вирусная инфекция для Ig. A и хроническая для Ig. M и Ig. G.
 Иммуноанализами называют такие методы, в основе которых лежит взаимодействия антиген-антитело, которые определяются с помощью специальных меток заранее конъюгированных с антигеном или антителом. Используют следующие виды меток: 1. Радионулиды (Н 3 – уридин, Н 3 – тимидин); 2. Ферменты (пероксидаза хрена и др. ); 3. Люминесцентные или флюоресцентные вещества (люминол, флюорисцин изоцианата и др. ).
Иммуноанализами называют такие методы, в основе которых лежит взаимодействия антиген-антитело, которые определяются с помощью специальных меток заранее конъюгированных с антигеном или антителом. Используют следующие виды меток: 1. Радионулиды (Н 3 – уридин, Н 3 – тимидин); 2. Ферменты (пероксидаза хрена и др. ); 3. Люминесцентные или флюоресцентные вещества (люминол, флюорисцин изоцианата и др. ).
 Объекты исследования в клинической иммунолгии: 1. Периферическая кровь (клетки, сыворотка, плазма); 2. Биологические жидкости (слюна, слезы, бронхоальвеолярная жидкость и др. ); 3. Гистологический анализ (иммуногистохимия); 4. Генотипирование (ПЦР, ПЦР в реальном времени). 5. Супернатант с культивируемых in vitro клеток
Объекты исследования в клинической иммунолгии: 1. Периферическая кровь (клетки, сыворотка, плазма); 2. Биологические жидкости (слюна, слезы, бронхоальвеолярная жидкость и др. ); 3. Гистологический анализ (иммуногистохимия); 4. Генотипирование (ПЦР, ПЦР в реальном времени). 5. Супернатант с культивируемых in vitro клеток
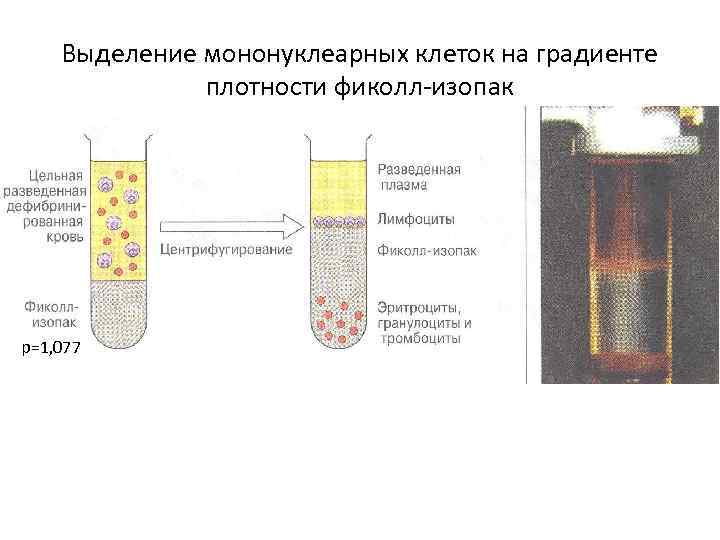
 Выделение мононуклеарных клеток на градиенте плотности фиколл-изопак p=1, 077
Выделение мононуклеарных клеток на градиенте плотности фиколл-изопак p=1, 077
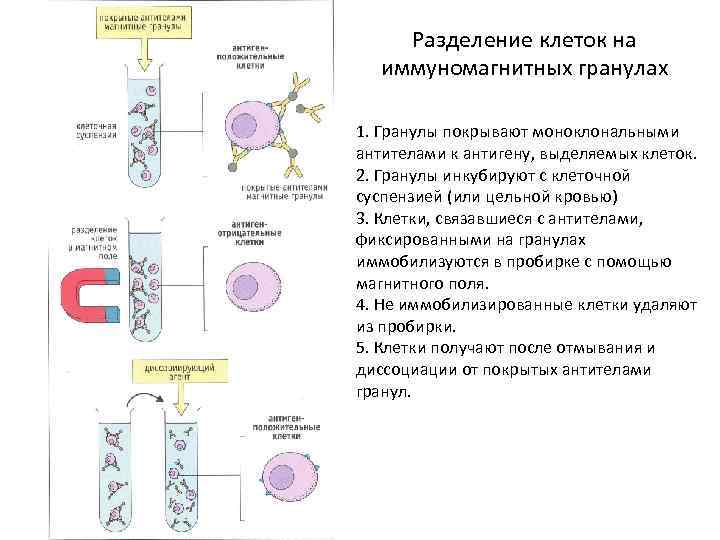
 Разделение клеток на иммуномагнитных гранулах 1. Гранулы покрывают моноклональными антителами к антигену, выделяемых клеток. 2. Гранулы инкубируют с клеточной суспензией (или цельной кровью) 3. Клетки, связавшиеся с антителами, фиксированными на гранулах иммобилизуются в пробирке с помощью магнитного поля. 4. Не иммобилизированные клетки удаляют из пробирки. 5. Клетки получают после отмывания и диссоциации от покрытых антителами гранул.
Разделение клеток на иммуномагнитных гранулах 1. Гранулы покрывают моноклональными антителами к антигену, выделяемых клеток. 2. Гранулы инкубируют с клеточной суспензией (или цельной кровью) 3. Клетки, связавшиеся с антителами, фиксированными на гранулах иммобилизуются в пробирке с помощью магнитного поля. 4. Не иммобилизированные клетки удаляют из пробирки. 5. Клетки получают после отмывания и диссоциации от покрытых антителами гранул.
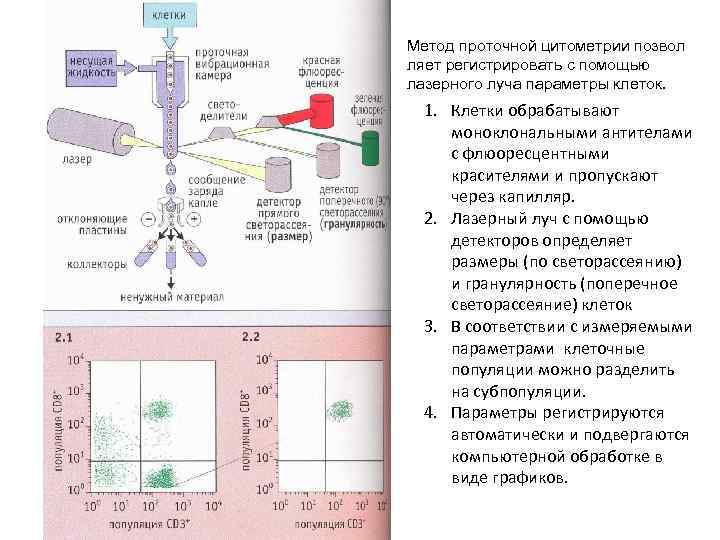
 Метод проточной цитометрии позвол ляет регистрировать с помощью лазерного луча параметры клеток. 1. Клетки обрабатывают моноклональными антителами с флюоресцентными красителями и пропускают через капилляр. 2. Лазерный луч с помощью детекторов определяет размеры (по светорассеянию) и гранулярность (поперечное светорассеяние) клеток 3. В соответствии с измеряемыми параметрами клеточные популяции можно разделить на субпопуляции. 4. Параметры регистрируются автоматически и подвергаются компьютерной обработке в виде графиков.
Метод проточной цитометрии позвол ляет регистрировать с помощью лазерного луча параметры клеток. 1. Клетки обрабатывают моноклональными антителами с флюоресцентными красителями и пропускают через капилляр. 2. Лазерный луч с помощью детекторов определяет размеры (по светорассеянию) и гранулярность (поперечное светорассеяние) клеток 3. В соответствии с измеряемыми параметрами клеточные популяции можно разделить на субпопуляции. 4. Параметры регистрируются автоматически и подвергаются компьютерной обработке в виде графиков.
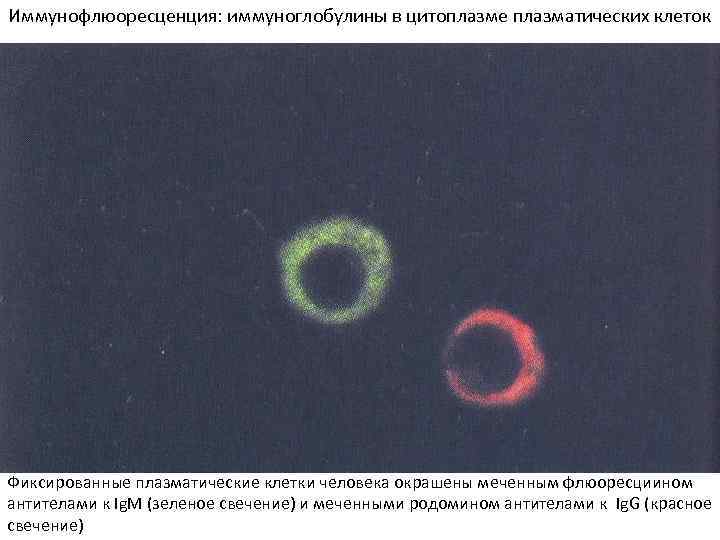
 Иммунофлюоресценция: иммуноглобулины в цитоплазме плазматических клеток Фиксированные плазматические клетки человека окрашены меченным флюоресциином антителами к Ig. M (зеленое свечение) и меченными родомином антителами к Ig. G (красное свечение)
Иммунофлюоресценция: иммуноглобулины в цитоплазме плазматических клеток Фиксированные плазматические клетки человека окрашены меченным флюоресциином антителами к Ig. M (зеленое свечение) и меченными родомином антителами к Ig. G (красное свечение)
 Оценку иммунного статуса можно проводить несколькими способами: 1. По тестам I уровня (ориентировочные, можно провести практически в любой лаборатории); 2. По тестам II уровня (аналитические тесты, используют для углубленного анализа); 3. Патогенетический принцип: оценка отдельных звеньев иммунной системы (распознавание, активация, пролиферация, дифференцировка и регуляция); 4. Оценка состояния врожденного иммунитета (клеток и гуморальных факторов); 5. Оценка состояния адаптивного или приобретенного иммунитета (Т и В – лимфоциты и их субпопуляции).
Оценку иммунного статуса можно проводить несколькими способами: 1. По тестам I уровня (ориентировочные, можно провести практически в любой лаборатории); 2. По тестам II уровня (аналитические тесты, используют для углубленного анализа); 3. Патогенетический принцип: оценка отдельных звеньев иммунной системы (распознавание, активация, пролиферация, дифференцировка и регуляция); 4. Оценка состояния врожденного иммунитета (клеток и гуморальных факторов); 5. Оценка состояния адаптивного или приобретенного иммунитета (Т и В – лимфоциты и их субпопуляции).
 Тесты I уровня • Исследование должно начинаться с определения количества основных клеточных популяций крови(анализ крови): – количество лейкоцитов (абсолютное и относительное); – количество Т-лимфоцитов (CD 3); – количество В-лимфоцитов (CD 19); – фагоцитоз (фагоцитарное число и фагоцитарный индекс). • количество иммуноглобулинов (Ig. M, Ig. A, Ig. G); . Анализ на ВИЧ- инфекцию Тесты I уровня назначаются при подозрении на наличие иммунодефицитов, аутоиммунных, аллергических заболеваний при хронических инфекционных заболеваниях и злокачественных новообразованиях, при обследовании реципиентов до и после аллотрансплантации органов тканей.
Тесты I уровня • Исследование должно начинаться с определения количества основных клеточных популяций крови(анализ крови): – количество лейкоцитов (абсолютное и относительное); – количество Т-лимфоцитов (CD 3); – количество В-лимфоцитов (CD 19); – фагоцитоз (фагоцитарное число и фагоцитарный индекс). • количество иммуноглобулинов (Ig. M, Ig. A, Ig. G); . Анализ на ВИЧ- инфекцию Тесты I уровня назначаются при подозрении на наличие иммунодефицитов, аутоиммунных, аллергических заболеваний при хронических инфекционных заболеваниях и злокачественных новообразованиях, при обследовании реципиентов до и после аллотрансплантации органов тканей.
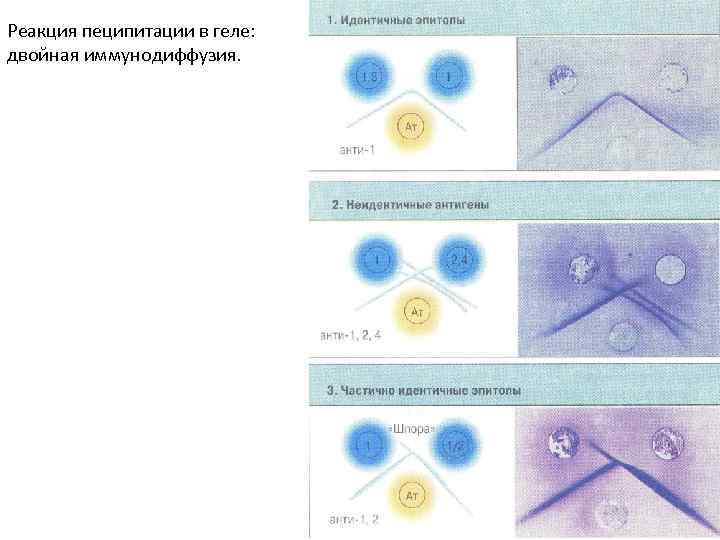
 Реакция пеципитации в геле: двойная иммунодиффузия.
Реакция пеципитации в геле: двойная иммунодиффузия.
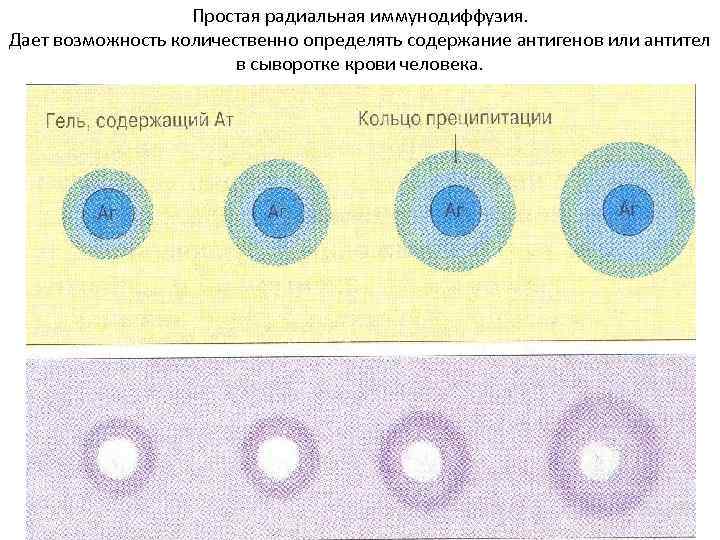
 Простая радиальная иммунодиффузия. Дает возможность количественно определять содержание антигенов или антител в сыворотке крови человека.
Простая радиальная иммунодиффузия. Дает возможность количественно определять содержание антигенов или антител в сыворотке крови человека.
 Тесты II уровня назначаются для уточнения нарушений в функционировании иммунной системы. Важно оценивать данные иммунограммы в комплексе с клинической картиной и данными анамнеза. • Определение субпопуляции Т-лимфоцитов Th 1, Th 2, Th 17, Treg. По маркерам и внутреннему содержанию и выработке цитокинов (ИФН-y, ИЛ-4, ТФР-в) методом проточной цитометрии. • Оценка активности киллерных клеток (ЦТЛ, NK, и др. с определением гранзимов перфорина или выходу радиоактивной метки) • Определение специфических Ig Е (ИФА); • Оценка пролиферативной активности Т-и-В лимфоцитов на митогены, антигены, аллогенные клетки. (РБТЛ). • Экспрессия активационных маркеров (CD 25, CD 69, CD 71, HLA-DR). • Определение различных компонентов комплемента (Манчини, Рокет-ИФА). • Оценка различных этапов фагоцитоза и рецепторного аппарата фагоцитов (Н 2 O 2. О 2 - NВТ-нитросинего тетразоля) • Определение продукции цитокинов (экспрессия рецепторов идр. ). • Анализ генов. Ответственных за экспрессию иммунологически значимых молекул (ПЦР). • Подавление миграции лейкоцитов in vitro в присутствии митогена или специфического для Т-лимфоцитов антигена (МИФ). Комплекс тестов второго уровня может значительно варьировать в зависимости от поставленных врачом задач.
Тесты II уровня назначаются для уточнения нарушений в функционировании иммунной системы. Важно оценивать данные иммунограммы в комплексе с клинической картиной и данными анамнеза. • Определение субпопуляции Т-лимфоцитов Th 1, Th 2, Th 17, Treg. По маркерам и внутреннему содержанию и выработке цитокинов (ИФН-y, ИЛ-4, ТФР-в) методом проточной цитометрии. • Оценка активности киллерных клеток (ЦТЛ, NK, и др. с определением гранзимов перфорина или выходу радиоактивной метки) • Определение специфических Ig Е (ИФА); • Оценка пролиферативной активности Т-и-В лимфоцитов на митогены, антигены, аллогенные клетки. (РБТЛ). • Экспрессия активационных маркеров (CD 25, CD 69, CD 71, HLA-DR). • Определение различных компонентов комплемента (Манчини, Рокет-ИФА). • Оценка различных этапов фагоцитоза и рецепторного аппарата фагоцитов (Н 2 O 2. О 2 - NВТ-нитросинего тетразоля) • Определение продукции цитокинов (экспрессия рецепторов идр. ). • Анализ генов. Ответственных за экспрессию иммунологически значимых молекул (ПЦР). • Подавление миграции лейкоцитов in vitro в присутствии митогена или специфического для Т-лимфоцитов антигена (МИФ). Комплекс тестов второго уровня может значительно варьировать в зависимости от поставленных врачом задач.
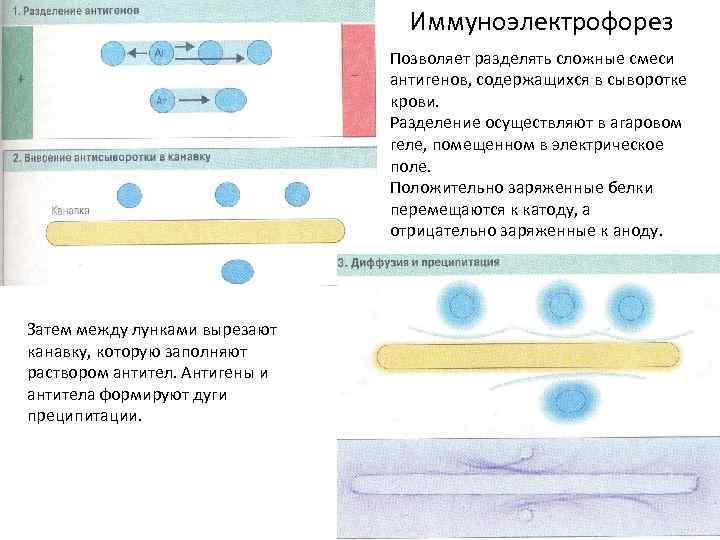
 Иммуноэлектрофорез Позволяет разделять сложные смеси антигенов, содержащихся в сыворотке крови. Разделение осуществляют в агаровом геле, помещенном в электрическое поле. Положительно заряженные белки перемещаются к катоду, а отрицательно заряженные к аноду. Затем между лунками вырезают канавку, которую заполняют раствором антител. Антигены и антитела формируют дуги преципитации.
Иммуноэлектрофорез Позволяет разделять сложные смеси антигенов, содержащихся в сыворотке крови. Разделение осуществляют в агаровом геле, помещенном в электрическое поле. Положительно заряженные белки перемещаются к катоду, а отрицательно заряженные к аноду. Затем между лунками вырезают канавку, которую заполняют раствором антител. Антигены и антитела формируют дуги преципитации.
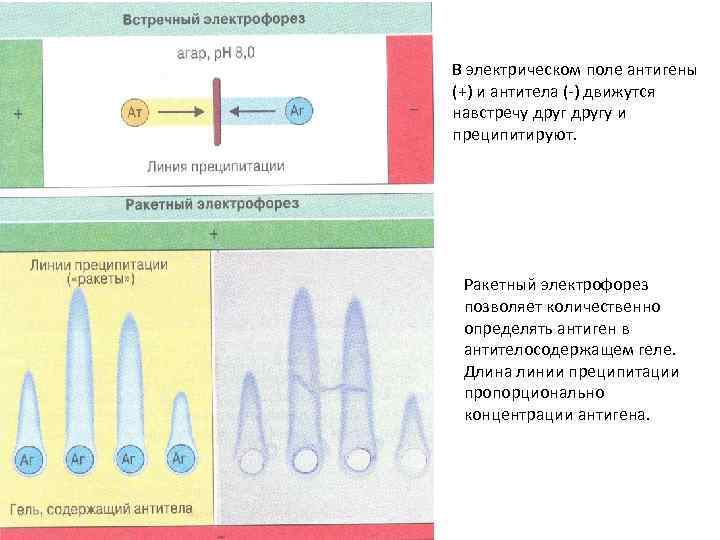
 В электрическом поле антигены (+) и антитела (-) движутся навстречу другу и преципитируют. Ракетный электрофорез позволяет количественно определять антиген в антителосодержащем геле. Длина линии преципитации пропорционально концентрации антигена.
В электрическом поле антигены (+) и антитела (-) движутся навстречу другу и преципитируют. Ракетный электрофорез позволяет количественно определять антиген в антителосодержащем геле. Длина линии преципитации пропорционально концентрации антигена.
 Тесты оценки иммунного статуса по патогенетическому принципу I. Распознаванание – Оценка Т-клеточного рецептора (TCR); – Адгезивные молекулы (интегрины и др. ); – Смешанная культура лимфоцитов; – Генный анализ аллотипов HLA и TCR; – Распознавание цитотоксическими CD 8 лимфоцитами антигенов вирусов, опухолевых клеток и др. II. Активация – Фенотипирование маркеров активации (CD 25, CD 71, HLA- DR и др. ) при стимуляции ФГА, антителами к TCR и CD 2; – Выявление маркеров в крови без стимуляции с использованием двойной метки CD 4+CD 25+; – Выявление вторичных мессенджерова (с. АМР, с. АТР, протеинкиназы и др. ); – Отвечаемость на цитокины (экспрессия рецепторов цитокинов);
Тесты оценки иммунного статуса по патогенетическому принципу I. Распознаванание – Оценка Т-клеточного рецептора (TCR); – Адгезивные молекулы (интегрины и др. ); – Смешанная культура лимфоцитов; – Генный анализ аллотипов HLA и TCR; – Распознавание цитотоксическими CD 8 лимфоцитами антигенов вирусов, опухолевых клеток и др. II. Активация – Фенотипирование маркеров активации (CD 25, CD 71, HLA- DR и др. ) при стимуляции ФГА, антителами к TCR и CD 2; – Выявление маркеров в крови без стимуляции с использованием двойной метки CD 4+CD 25+; – Выявление вторичных мессенджерова (с. АМР, с. АТР, протеинкиназы и др. ); – Отвечаемость на цитокины (экспрессия рецепторов цитокинов);
 III. Пролиферация – Бласттрансформация лимфоцитов на митогены, специфические антигены; – Ответ на факторы роста клеток; IV. Дифференцировка (эффекторная функция) – Продукция иммуноглобулинов; – Цитотоксическая функция Т-клеток (CD 8); – Оценка естественных киллеров (NK-клеток); – Продукция цитокинов; V. Регуляция – Оценка хелперных и супрессорных функций лимфоцитов; – Анализ функциональных свойств Т-хелперов первого и второго типов и продуцируемых ими цитокинов (ИНФγ, ИЛ 4); – Оценка регуляторных свойств моноцитов;
III. Пролиферация – Бласттрансформация лимфоцитов на митогены, специфические антигены; – Ответ на факторы роста клеток; IV. Дифференцировка (эффекторная функция) – Продукция иммуноглобулинов; – Цитотоксическая функция Т-клеток (CD 8); – Оценка естественных киллеров (NK-клеток); – Продукция цитокинов; V. Регуляция – Оценка хелперных и супрессорных функций лимфоцитов; – Анализ функциональных свойств Т-хелперов первого и второго типов и продуцируемых ими цитокинов (ИНФγ, ИЛ 4); – Оценка регуляторных свойств моноцитов;
 Методы оценки цитотоксических клеток • Механизм цитолиза , осуществляемого NК киллерами и цитотоксическими Т- лф, практически идентичны. Характер цитолиза предполагает значительную роль молекул адгезии в установлении контакта между клетками-киллерами и мишенями LFA-1 и ICAM-1. и перфорингранзимный механизм, служащими основными инструментом цитолиза (NK-клетки) CD 8+ лимфоциты используют Fas-Fas. L. • NK-клетки оценивают по способности лизировать трансформированные клетки, предварительно меченные флуорохромами или радионуклеидами. • В качестве клеток-мишеней и пользуются клетки линии эритромиелоидного лейкоза человека К-562, которые предварительно (за 6 часов до конца инкубации) метят 51 Cr или Н 3 -уридин. • Реакцию ставят в круглодонных планшетах, соотношение эффектор-мишень обычно варьирует от 20: 1 до 1; 1 • После инкубации (60 мин при 37 о. С) клеток-мишеней с киллерами собирают надосадок без клеток в пробирки для Y-счетчика. • Мерой лизиса клеток служит выход радиоактивной метки в супернатант • Рассчитывают процент метки, освободившейся из клеток по формуле: • Индекс цитотоксичности (Эксп. -Спонт. /Макс. – Спонт. )Радиоактивность опытных проб / спонтанная. Максимальная- в положительном контроле ( 100% лизис при обработке 2, 5 %раствором тритона Х-100)
Методы оценки цитотоксических клеток • Механизм цитолиза , осуществляемого NК киллерами и цитотоксическими Т- лф, практически идентичны. Характер цитолиза предполагает значительную роль молекул адгезии в установлении контакта между клетками-киллерами и мишенями LFA-1 и ICAM-1. и перфорингранзимный механизм, служащими основными инструментом цитолиза (NK-клетки) CD 8+ лимфоциты используют Fas-Fas. L. • NK-клетки оценивают по способности лизировать трансформированные клетки, предварительно меченные флуорохромами или радионуклеидами. • В качестве клеток-мишеней и пользуются клетки линии эритромиелоидного лейкоза человека К-562, которые предварительно (за 6 часов до конца инкубации) метят 51 Cr или Н 3 -уридин. • Реакцию ставят в круглодонных планшетах, соотношение эффектор-мишень обычно варьирует от 20: 1 до 1; 1 • После инкубации (60 мин при 37 о. С) клеток-мишеней с киллерами собирают надосадок без клеток в пробирки для Y-счетчика. • Мерой лизиса клеток служит выход радиоактивной метки в супернатант • Рассчитывают процент метки, освободившейся из клеток по формуле: • Индекс цитотоксичности (Эксп. -Спонт. /Макс. – Спонт. )Радиоактивность опытных проб / спонтанная. Максимальная- в положительном контроле ( 100% лизис при обработке 2, 5 %раствором тритона Х-100)
 Определение цитолитических CD 8+ Т-клеток • Метод оценки цитотоксических CD 8+клеток по выявлению мембранной экспрессии молекул CD 107 (LAMP-1), которые являются специфическим маркером гранул гранзима-перфорина. • В норме эта молекула отсутствует на клеточной поверхности, но содержится на мембранах лизосом. При активации специфическим антигеном происходит быстрая дегрануляция цитотоксических гранул слияние с цитоплазматической мембраной на поверхности клеток. • Дегранулировавшие CD 8+ клетки выявляют с помощью поверхностной иммунофлуоресцентной окраски на CD 107 а на проточной цитометрии. • Этот метод позволяет выявлять именно цитолитические АГ- специфические CD 8+ Т –клетки. • Метод может применяться в сочетании с внутриклеточной окраской на IFNy для оценки содержания АГ-специфичных CD 8+ Т-клеток памяти, не обладающих немедленной цитолитической функцией • )
Определение цитолитических CD 8+ Т-клеток • Метод оценки цитотоксических CD 8+клеток по выявлению мембранной экспрессии молекул CD 107 (LAMP-1), которые являются специфическим маркером гранул гранзима-перфорина. • В норме эта молекула отсутствует на клеточной поверхности, но содержится на мембранах лизосом. При активации специфическим антигеном происходит быстрая дегрануляция цитотоксических гранул слияние с цитоплазматической мембраной на поверхности клеток. • Дегранулировавшие CD 8+ клетки выявляют с помощью поверхностной иммунофлуоресцентной окраски на CD 107 а на проточной цитометрии. • Этот метод позволяет выявлять именно цитолитические АГ- специфические CD 8+ Т –клетки. • Метод может применяться в сочетании с внутриклеточной окраской на IFNy для оценки содержания АГ-специфичных CD 8+ Т-клеток памяти, не обладающих немедленной цитолитической функцией • )
 • Метод измерения пролиферативного ответа лимфоцитов с помощью моноклональных антител с CD 3 и костимулирующей молекуле CD 28. м. АТ к CD 3, фиксируют на пластике в сочетании с растворимыми антителами к молекуле CD 28, что вызывает поликлональный ответ лф. (вместо митогенов). Добавляют лимфоциты от больного и культивируют 24 -48 часов при 37 о С. Оценивают по включению Н 3 -тимидина в пролиферирующие клетки ( на радиоактивном счетчике). • Функцию Тх1 и Тх2 определяю по синтезу ИНФy и ИЛ-4 на проточном цитофлуориметре. Для этого лф. стимулируют ФМА (активатор РКС) и иономицином (кальциевый ионофор). Клетки обрабатывают брефельдином А, блокирующим синтез, затем обрабатывают сапонином (нарушает клет. мембрану) и инкубируют с моно. АТ к цитокинам, меченными флуорохромом.
• Метод измерения пролиферативного ответа лимфоцитов с помощью моноклональных антител с CD 3 и костимулирующей молекуле CD 28. м. АТ к CD 3, фиксируют на пластике в сочетании с растворимыми антителами к молекуле CD 28, что вызывает поликлональный ответ лф. (вместо митогенов). Добавляют лимфоциты от больного и культивируют 24 -48 часов при 37 о С. Оценивают по включению Н 3 -тимидина в пролиферирующие клетки ( на радиоактивном счетчике). • Функцию Тх1 и Тх2 определяю по синтезу ИНФy и ИЛ-4 на проточном цитофлуориметре. Для этого лф. стимулируют ФМА (активатор РКС) и иономицином (кальциевый ионофор). Клетки обрабатывают брефельдином А, блокирующим синтез, затем обрабатывают сапонином (нарушает клет. мембрану) и инкубируют с моно. АТ к цитокинам, меченными флуорохромом.
 Апоптоз • Оценка клеток, вступивших в апоптоз методом проточной цитофлуорометрии • ( связывания анексина V, меченного флуорохромом с фосфатидилсерином, который появляется на поверхности клетки только при апоптозе).
Апоптоз • Оценка клеток, вступивших в апоптоз методом проточной цитофлуорометрии • ( связывания анексина V, меченного флуорохромом с фосфатидилсерином, который появляется на поверхности клетки только при апоптозе).
 Определение специфических CD 8+ Т-лимфоцитов с использованием МНС-тетрамеров • Антигенный пептид даже в комплексе с МНС, обладает очень низкой аффинностью к ТCR Т-лф. , в связи с этим необходимы подходы, которые помогли бы выявлять специфические цитотоксические Т-лф. • Решение было достигнуто путем создания тетрамеров биотилированных комплексов МНС-пептид • Создают тетрамер молекулы МНС-1 (ПЦР) • Добавляют специфический антиген(пептид). • К МНС-пептидному комплексу добавляют фермент (Bir A –лигаза) и биотин и др. Смесь инкубируют для создания биотилированного комплекса. , к которому хорошо присоединяется авидин (или стрептавидин), меченный флуорохромом (фикоэритрин). К каждой молекуле авидина присоединяется 4 молекулы комплекса МНС- пептид. • СD 8+лф. инкубируют с МНС-пептидом, добавляют м. АТк СD 8+. • Клетки анализируют на проточном цитофлуориметре. Определяют • Одновременно экспрессию меченных тетрамеров и CD 8.
Определение специфических CD 8+ Т-лимфоцитов с использованием МНС-тетрамеров • Антигенный пептид даже в комплексе с МНС, обладает очень низкой аффинностью к ТCR Т-лф. , в связи с этим необходимы подходы, которые помогли бы выявлять специфические цитотоксические Т-лф. • Решение было достигнуто путем создания тетрамеров биотилированных комплексов МНС-пептид • Создают тетрамер молекулы МНС-1 (ПЦР) • Добавляют специфический антиген(пептид). • К МНС-пептидному комплексу добавляют фермент (Bir A –лигаза) и биотин и др. Смесь инкубируют для создания биотилированного комплекса. , к которому хорошо присоединяется авидин (или стрептавидин), меченный флуорохромом (фикоэритрин). К каждой молекуле авидина присоединяется 4 молекулы комплекса МНС- пептид. • СD 8+лф. инкубируют с МНС-пептидом, добавляют м. АТк СD 8+. • Клетки анализируют на проточном цитофлуориметре. Определяют • Одновременно экспрессию меченных тетрамеров и CD 8.
 Оценка функции естественных регуляторных клеток • Регуляторные клетки (CD 4+ CD 25+) инкубируют с магнитными бусами нагруженными антителами (CD 14, CD 56, CD 19, CD 8, CD 54 RA(рец. для LFA-1), CD 235(гликофорин к мембранам эритроцитов). • Несвязавшиеся клетки CD 4 +CD 25+ смешивают с бусами, нагруженными антителами с CD 25+ • Несвязавшиеся CD 4+CD 25 -клетки используют для постановки функционального теста: активируют моноклональными антителами к CD 3, CD 28 и IL-2 и добавляют АПК • CD 4+CD 25 - CD 4+CD 25+ клетки культивируют в 96 -луночных планшетах порознь. • За 18 часов до окончания культивирования добавляли 3 Н-тимидин • оценивают индекс стимуляции и подавления стимуляции (отношение вкл. 3 Н-тимидина в культуре CD 4+ CD 25 - и CD 4+CD 25+) •
Оценка функции естественных регуляторных клеток • Регуляторные клетки (CD 4+ CD 25+) инкубируют с магнитными бусами нагруженными антителами (CD 14, CD 56, CD 19, CD 8, CD 54 RA(рец. для LFA-1), CD 235(гликофорин к мембранам эритроцитов). • Несвязавшиеся клетки CD 4 +CD 25+ смешивают с бусами, нагруженными антителами с CD 25+ • Несвязавшиеся CD 4+CD 25 -клетки используют для постановки функционального теста: активируют моноклональными антителами к CD 3, CD 28 и IL-2 и добавляют АПК • CD 4+CD 25 - CD 4+CD 25+ клетки культивируют в 96 -луночных планшетах порознь. • За 18 часов до окончания культивирования добавляли 3 Н-тимидин • оценивают индекс стимуляции и подавления стимуляции (отношение вкл. 3 Н-тимидина в культуре CD 4+ CD 25 - и CD 4+CD 25+) •
 Оценка внутриклеточного киллинга бактерий • Для исследований используют ФИТЦ-меченый стафилококк (St. aureus), который добавляют к лейкоцитам крови человека в соотношении 1: 5. ( Удаляют несвязавшиеся бактерии центрифугированием с осаждением лейкоцитов и отмыванием ФСБ) • Инкубируют 20 мин при 37 С в 96 луночных круглодонных планшетах • Лейкоциты осаждают и ресуспендируют в 2% растворе сапонина в буфере (р. Н 9, 5). • Высвободившиеся бактерии осаждают центрифугированием и ресуспендируют в ФСБ с пропидиумом иодида ( убитые бактерии позитивны по ПИ) • С помощью проточного цитометра оценивают процент двойных позитивных бактерий (ФИТЦ+ ПИ+) среди ФИТЦ- меченых бактерий
Оценка внутриклеточного киллинга бактерий • Для исследований используют ФИТЦ-меченый стафилококк (St. aureus), который добавляют к лейкоцитам крови человека в соотношении 1: 5. ( Удаляют несвязавшиеся бактерии центрифугированием с осаждением лейкоцитов и отмыванием ФСБ) • Инкубируют 20 мин при 37 С в 96 луночных круглодонных планшетах • Лейкоциты осаждают и ресуспендируют в 2% растворе сапонина в буфере (р. Н 9, 5). • Высвободившиеся бактерии осаждают центрифугированием и ресуспендируют в ФСБ с пропидиумом иодида ( убитые бактерии позитивны по ПИ) • С помощью проточного цитометра оценивают процент двойных позитивных бактерий (ФИТЦ+ ПИ+) среди ФИТЦ- меченых бактерий
 • Современные методы оценки фагоцитоза основаны на проточной цитометрии с применением объектов фагоцитоза (бактерий, частиц и др. ), меченных флуорохромам. • К лейкоцитам крови человека добавляют ФИТЦ-меченный стафилококк в соотношении 1: 5 в объеме 200 мкл в 96 луночных круглодонных планшетах. • Суспензию инкубируют 30 мин. При 37 С. • После инкубации клетки поглотившие бактерии, осаждают центрифугированием. • Лейкоциты ресуспензируют 200 мкл 2% раствора параформальдегида и анализуруют на проточном цитометре. • Оценивают процент клеток среди гранулоцитов и моноцитов положительных по зеленой флуоресценции соответствующей ФИТЦ -меченым бактериям.
• Современные методы оценки фагоцитоза основаны на проточной цитометрии с применением объектов фагоцитоза (бактерий, частиц и др. ), меченных флуорохромам. • К лейкоцитам крови человека добавляют ФИТЦ-меченный стафилококк в соотношении 1: 5 в объеме 200 мкл в 96 луночных круглодонных планшетах. • Суспензию инкубируют 30 мин. При 37 С. • После инкубации клетки поглотившие бактерии, осаждают центрифугированием. • Лейкоциты ресуспензируют 200 мкл 2% раствора параформальдегида и анализуруют на проточном цитометре. • Оценивают процент клеток среди гранулоцитов и моноцитов положительных по зеленой флуоресценции соответствующей ФИТЦ -меченым бактериям.
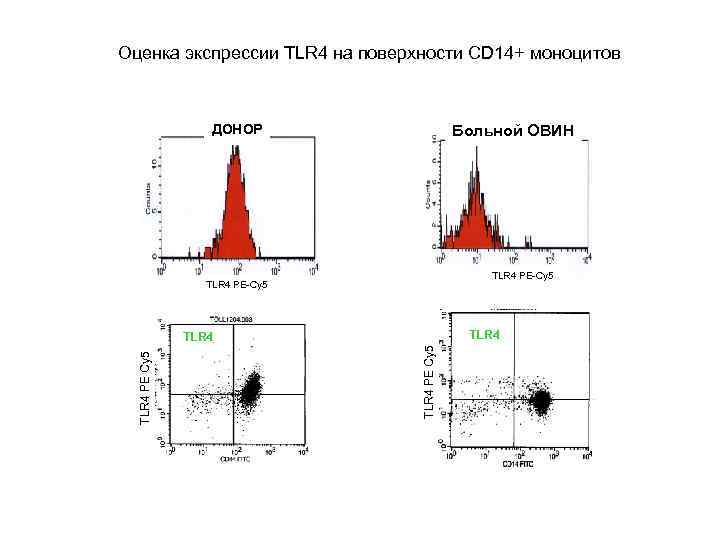
 Оценка врожденного иммунитета • Клетки врожденного иммунитета содержат рецепторы – PPR (pattern recognition receptors). Выявлено три группы рецепторов: TLR (включает 11 рец. ), NOD (8 рец. ), Rig (3 рец. ). • Внеклеточные TLR 2 и TLR 4 распознают пептидогликан клеточной стенки бактерий и ЛПС грамотрицательных бактерий; внутриклеточные TLR 3, 7. 8 – вирусные нукл. к-ты, TLR 9 -Cp. G-мотив бактериальной ДНК. С помощью м. АТ и проточной цитометрии можно оценить интенсивной экспрессии рецепторов. Если мц крови человека, стимулированные ЛПС, синтезируют TNF-a в количествах , соотв. норме, то можно говорить о норм. экспрессии рец. TLR 4.
Оценка врожденного иммунитета • Клетки врожденного иммунитета содержат рецепторы – PPR (pattern recognition receptors). Выявлено три группы рецепторов: TLR (включает 11 рец. ), NOD (8 рец. ), Rig (3 рец. ). • Внеклеточные TLR 2 и TLR 4 распознают пептидогликан клеточной стенки бактерий и ЛПС грамотрицательных бактерий; внутриклеточные TLR 3, 7. 8 – вирусные нукл. к-ты, TLR 9 -Cp. G-мотив бактериальной ДНК. С помощью м. АТ и проточной цитометрии можно оценить интенсивной экспрессии рецепторов. Если мц крови человека, стимулированные ЛПС, синтезируют TNF-a в количествах , соотв. норме, то можно говорить о норм. экспрессии рец. TLR 4.
 Оценка экспрессии TLR 4 на поверхности CD 14+ моноцитов ДОНОР Больной ОВИН TLR 4 PE-Cy 5 TLR 4 PE Cy 5
Оценка экспрессии TLR 4 на поверхности CD 14+ моноцитов ДОНОР Больной ОВИН TLR 4 PE-Cy 5 TLR 4 PE Cy 5

