2014_КЛИНИЧЕСКАЯ ИММУНОЛОГИЯ последняя лекция.ppt
- Количество слайдов: 69

Клиническая иммунология Иммунный статус Иммунодефицитные состояния Аутоиммунные болезни Трансплантационный иммунитет Противоопухолевый иммунитет Иммунокоррекция Шабан Ж. Г.

Клиническая иммунология (КИ) ü раздел иммунологии изучает функционирование ИС у здоровых и больных людей ü разрабатывает методы оценки иммунного статуса, диагностики и коррекции нарушений ü

Задачи КИ ü Изучение функционирования ИС у здоровых людей ü Изучение функционирования ИС при различных заболеваниях (аллергических, аутоиммунных, онкологических и др. ) ü Выявление и изучение первичных ИДС (ПИДС) ü Изучение вторичных ИДС (ВИДС) ü Разработка методов оценки иммунного статуса ü Поиск и разработка иммунотропных препаратов ü Подготовка кадров

Иммунный статус – количественная и функциональная характеристика отдельных звеньев ИС в определённый период онтогенеза или в определённый период заболевания

Методы оценки иммунного статуса: 1. Анамнез 2. Клиническое обследование 3. Лабораторное обследование: - общий анализ крови - иммунологическое обследование

Принципы оценки иммунного статуса 1. 2 уровня оценки 2. Связь количественных показателей и функциональной активности 3. Связь показателей иммунного статуса с клиническим течением заболевания 4. Учёт индивидуальной иммунореактивности 5. Сравнение индивидуальных показателей с показателями нормы 4. Решение вопроса о необходимости иммунокоррекции 5. Иммунологический мониторинг (наблюдение в динамике за показателями иммунного статуса)

Уровни оценки иммунного статуса 1 – ориентировочный: ü обязательный ü выявляет «грубые» дефекты ИС ü включает простые тесты, может быть выполнен в любой клинической лаборатории Если выявлены нарушения на 1 -ом уровне или нет нарушений, но есть клинические проявления, то 2 – аналитический: ü определяет в каком звене и на каком этапе есть нарушение ü включает более сложные тесты ü требует наличия специального оборудования, специалистов и м. б. выполнен только в иммунологической лаборатории

Тесты 1 уровня: Ø Общее число Лф Ø Содержание В-л (относительное и абсолютное) Ø Концентрация Ig. G, Ig. A, Ig. M в сыворотке Ø Содержание Т-л (относительное и абсолютное) Ø ФП, ФЧ и ПЗФ Ø Общая гемолитическая активность системы комплемента (СН 50, АП 50) Ø ИФА – ВИЧ

Тесты 2 уровня: 1. По В-системе лимфоцитов: Ø Ø Ø Субпопуляции В-л Субклассы Ig (Ig. G 1 -4, Ig. М 1 -3, Ig. A 1 -2) Пролиферативная активность (РБТЛ) на В-митогены Антителопродуцирующая активность in vitro Способность отвечать на вакцинацию выработкой АТ

2. По Т-системе лимфоцитов: Ø CD 4+ и CD 8+ субпопуляции, их соотношение (норма – 2, 0) Если > 4, 0 – активация (аутоиммунные процессы; аллергия) Если < 1, 0 – супрессия (хр. инфекции, в т. ч. СПИД; опухоли) Ø Пролиферативная активность (РБТЛ) на Т-митогены (ФГА) Ø Цитотоксическая активность Т-л Ø Продукция цитокинов (ИЛ 2, 3, 4, 5, 6, γ-INF и др. ) Ø Внутрикожные пробы на митогены и анамнестические антигены

3. По фагоцитозу: Ø Расшифровка отдельных этапов: - хемотаксис опсонизация адгезия бактерицидная активность метаболическая активность 4. По системе комплемента: Ø Комплементарный профиль: количественное содержание и функциональная активность отдельных компонентов Ø Уровень фрагментов деградации белков С: С 3 а, С 5 а, С 4 а и др.

Иммунограмма результаты анализа иммунного статуса вносят в бланк, содержащий данные нормальных параметров иммунного статуса лиц соответствующего возраста

Иммунодефицитные состояния (ИДС) Ø нарушения иммунного статуса обусловлены дефектом ( или отсутствие) одного или нескольких звеньев ИС Ø итог – низкая эффективность или полное отсутствие ИО Ø

2 группы ИДС: Ø Первичные (врождённые) – 0, 05% всех ИДС – обусловлены генетически Ø Вторичные – приобретены под влиянием факторов внешней среды

Структура первичных ИДС 1. 2. 3. 4. 5. В-клеточные – 50 % Т-клеточные – 30 % Комбинированные (В- и Т-) – 10 % Дефекты фагоцитоза – 8 % Дефекты системы С – 2 %

В-клеточные ИДС количества В-л, нарушение ГИО, отсутствие или синтеза Ig: ØАгаммаглобулинемия (б-нь Брутона) ØГипогаммаглобулинемия ØДисгаммаглобулинемии Проявления: чувствительность к инфекциям, вызываемым внеклеточными паразитами

Т-клеточные ИДС недоразвитие тимуса и паращитовидных желез, количества и нарушение дифференцировки Т-л, отсутствие или КИО: Ø Аплазия или гипоплазия тимуса (синдром Ди Джорджи) Ø Синдром Незелофа Ø Недостаточность аденозиндезаминазы Проявления: – хр. бактериальные, вирусные и грибковые инфекции – опухоли

Комбинированные ИДС: Ø Тяжёлый комбинированный ИДС Ø Синдром Луи Бар Ø Синдром Вискотт-Олдрича Проявления: организмы нежизнеспособны, погибают в раннем возрасте

Дефекты фагоцитоза Ø Недостаточность ферментов нарушение бактерицидной и переваривающей активности Ø Нарушения хемотаксиса Ø Недостаточность опсонирующих факторов Ø Недостаточная экспрессия рецепторов (С 3 в, Fc- и др. ) на фагоцитах Проявления: чувствительность к гноеродным микроорганизмам

Дефекты комплемента ØДефицит некоторых компонентов: - С 1, 4, 2 – аутоиммунные заболевания - С 3, 5 – рецидивирующие ГВЗ - С 6, 7, 8 – менингококковая и гонококковая инфекции ØДефицит С 1 -ингибитора – наследственный ангионевротический отёк

Причины вторичных ИДС Ø Инфекционные заболевания: - вирусные (СПИД) - бактериальные - протозойные - гельминтозы Ø Соматические заболевания печени, почек, поджелудочной железы Ø Опухоли иммунной системы Ø Гормональный дисбаланс Ø Образ жизни (условия труда, быта, питание и др. ) Ø Экологические факторы Ø Приём лекарственных препаратов: - иммунодепрессантов - некоторых антибиотиков

Вторичные ИДС Ø Т-система - общего числа Т-л - и дисбаланс субпопуляций Ø В-система - В-л как правило, активированы - дисгаммаглобулинемия Ø Фагоцитарная система страдает не всегда Ø Система комплемента изменяется комплементарный профиль

Аутоиммунные болезни (АБ) Ø группа патологических состояний характеризуется агрессией ИС против собственных клеток, их фрагментов или отдельных белков Ø

Ø АБ страдает 6 -8% населения Около 2/3 всех больных – женщины, 20 – 40 лет Ø Аутоиммунный процесс возникает спонтанно (неизвестно, какие факторы и события, инициирующие ИО, приведут к развитию АБ) Ø Риск развития АБ связан с: - некоторыми генами ГКГС (А 1, В 8, В 27 (СКВ), DR 3, DR 4) - факторами окружающей среды

ИММУНОЛОГИЧЕСКИЕ МЕХАНИЗМЫ ПОВРЕЖДЕНИЯ ТКАНЕЙ ПРИ АБ 1. Развитие ИО к АГ собственных тканей 2. Иммунологические механизмы повреждения тканей – реакции гиперчувствительности: - ГНТ 2 -го типа (комплемент-зависимая цитотоксичность) - ГНТ 3 -го типа (иммунокомплексные реакции) - ГНТ 4 -го типа (Т-клеточноопосредованные реакции) 3. Интенсивность иммунологических реакций и доминирующий тип повреждения определяют клиническое течение и основные симптомы АБ

Причины АБ 1. Нарушение гистогематического барьера в результате травмы (глаза) или инфекции (воспаление яичка при эпид. паротите) и выход тканевых АГ забарьерных органов (ЦНС, щитовидной железы, яичников, хрусталика), к которым не вырабатывается естественная ИТ 2. Отмена естественной ИТ с помощью модифицированных АГ или иммунокомпетентных клеток: - появление «запрещённых» клонов Лф (мутации, лимфопролиферативные заболевания) - дерепрессия клонов Лф к собственным АГ - продукции блокирующих АТ

3. Аномальная антигенная стимуляция: - антигенная мимикрия: на поверхности МИО представлены перекрёстные АГ, схожие с АГ хозяина изменение структур организма вирусами, лекарственными препаратами перекрёстные реакции идиотипов АТ 4. Бактериальные и вирусные инфекции: - поликлональная активация Т- и В-л повреждение собственных тканей модификация антигенного состава клеток человека 5. Повреждение тканей и клеток 6. Дисбаланс цитокинов Tх1 или Tх2 типа 7. Недостаточность Т-супрессорной регуляции, которая в норме сдерживает ИО на ауто. АГ
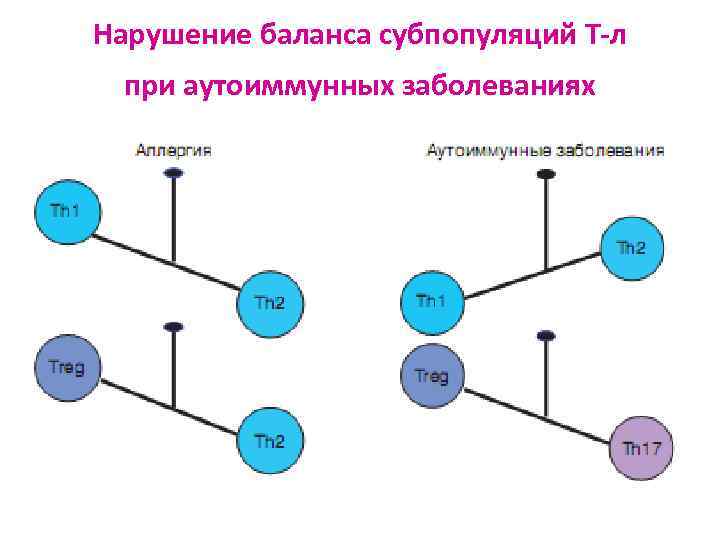
Нарушение баланса субпопуляций Т-л при аутоиммунных заболеваниях

Ауто. АГ – собственные АГ организма, воспринимаются ИС как чужеродные, индуцируют образование аутоиммунных Ат и аутореактивных клонов лимфоцитов Свойства ауто. АГ: Ø Сенсибилизация организма Ø Индукция клонов В-л, синтез и связывание аутоантигенспецифических Ig M, G, A, E Ø Индукция клонов провоспалительных Т-л Ø Активация лейкоцитов (Нф, Эф)
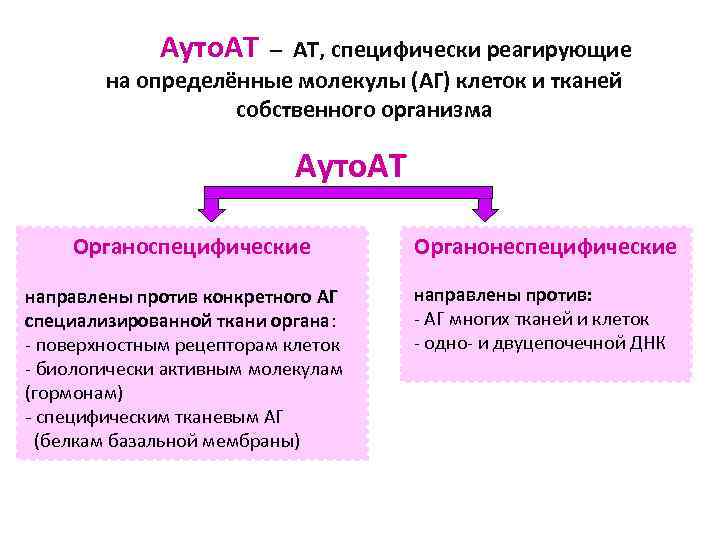
Ауто. АТ – АТ, специфически реагирующие на определённые молекулы (АГ) клеток и тканей собственного организма Ауто. АТ Органоспецифические направлены против конкретного АГ специализированной ткани органа: - поверхностным рецепторам клеток - биологически активным молекулам (гормонам) - специфическим тканевым АГ (белкам базальной мембраны) Органонеспецифические направлены против: - АГ многих тканей и клеток - одно- и двуцепочечной ДНК

Физиологическая роль ауто. АТ Ø «Мусорщики» организма Ø Регуляторы иммунного ответа Патологическая роль ауто. АТ ØАуто. Ат – причина развития воспаления, повреждения клеток и тканей: - ауто. Ат против клеток крови вызывают их повреждение - комплемент, фиксированный на клетке, стимулирует воспаление - антирецепторные ауто. Ат блокируют или специфическую функцию клеток - ауто. Ат к внеклеточным АГ индуцируют воспалительные реакции III типов ГНТ Ø Уровень ауто. Ат в организме и формируемых ими иммунных комплексов определяют степень активности и тяжести иммунопатологического процесса

ИММУНОЛОГИЧЕСКИЕ ОСОБЕННОСТИ СУПЕРАНТИГЕНОВ (САГ) Ø САГ стимулируют сильный первичный КИО Ø - цепь ТКР вовлечена в процесс распознавания САГ Т-л Ø распознавание САГ рецептором Т-л не рестриктировано по молекулам ГКГС Ø САГ связываются с молекулами ГКГС I без предшествующего процессинга АГ Ø Цитокиновый «взрыв» : активация Т-л и Мф сопровождается гиперсекрецией цитокинов Ø Стимулируются обе популяции Т-л (CD 4+ и CD 8+)
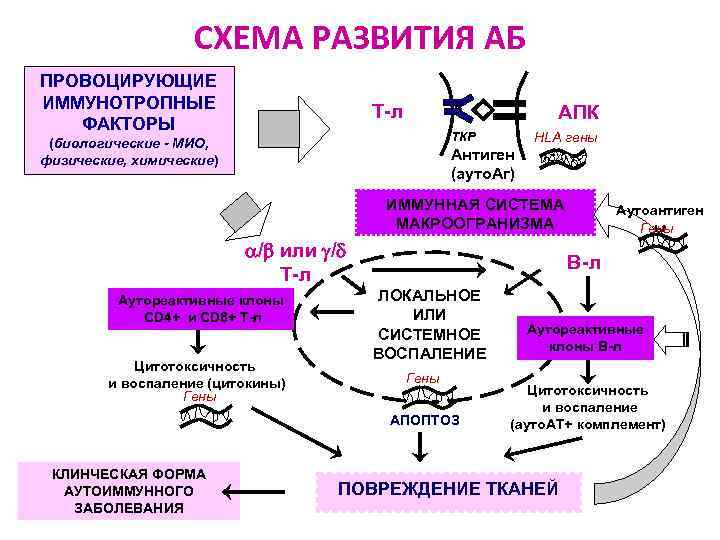
СХЕМА РАЗВИТИЯ АБ ПРОВОЦИРУЮЩИЕ ИММУНОТРОПНЫЕ ФАКТОРЫ Т-л АПК ТКР (биологические - МИО, физические, химические) HLA гены Антиген (ауто. Аг) ИММУННАЯ СИСТЕМА МАКРООГРАНИЗМА / или / Т-л Аутореактивные клоны CD 4+ и CD 8+ Т-л Цитотоксичность и воспаление (цитокины) Гены В-л ЛОКАЛЬНОЕ ИЛИ СИСТЕМНОЕ ВОСПАЛЕНИЕ Гены АПОПТОЗ КЛИНЧЕСКАЯ ФОРМА АУТОИММУННОГО ЗАБОЛЕВАНИЯ Аутоантиген ы Гены Аутореактивные клоны В-л Цитотоксичность и воспаление (ауто. АТ+ комплемент) ПОВРЕЖДЕНИЕ ТКАНЕЙ

АБ развиваются, когда аутореактивные Т- и В-л в достаточной мере активированы или гиперактивированы для развития выраженных и пролонгированных воспалительных реакций

Классификация АБ по локализации процесса 1. Органоспецифические – преимущественная локализация процесса в определённых органах: - эндокринных железах: щитовидной (тиреоидит Хашимото), поджелудочной (сахарный диабет), надпочечниках, семенниках, яичниках - коже (дерматит) - ЖКТ (колит) - клетках крови (гемолитическая анемия) - НС (полиневрит) - глазах (увеит) - сердце (миокардит) - почках (гломерулонефрит) 2. Органонеспецифические (системные) – связаны с появлением АТ к белкам крови, ДНК; распространяются на многие органы и системы: - системная красная волчанка (СКВ) ревматоидный артрит
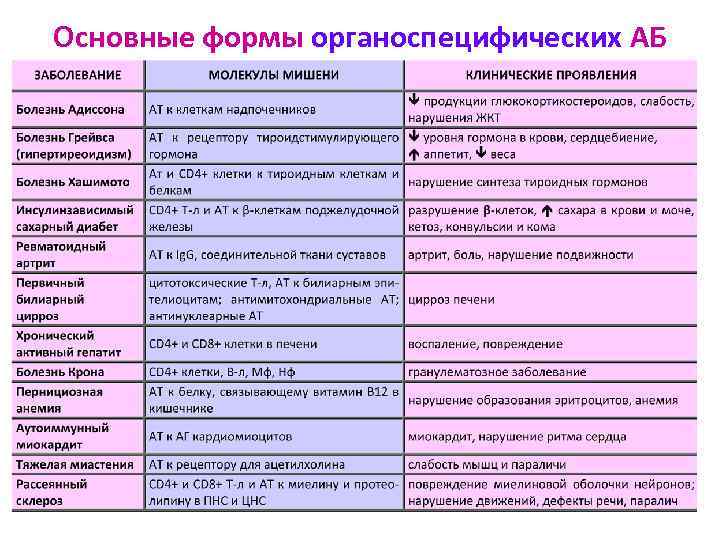
Основные формы органоспецифических АБ

ЭТИОЛОГИЯ АУТОИММУННОГО МИОКАРДИТА
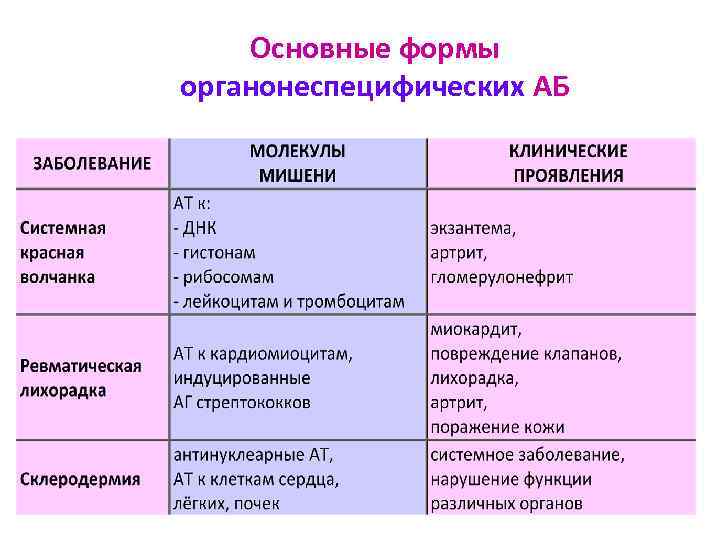
Основные формы органонеспецифических АБ

ИММУНОДИАГНОСТИКА АУТОИММУННЫХ СОСТОЯНИЙ 1. Определение уровней ауто. АТ в сыворотке крови 2. Определение циркулирующих и фиксированных иммунных комплексов 3. Определение продукции эффекторных и регуляторных цитокинов 4. Пролиферативный и цитотоксический ответ Т-л 5. Иммуногенотипирование – гены ГКГС, ФНО, C

ПОДХОДЫ К ИММУНОТЕРАПИИ АБ 1. СИСТЕМНАЯ ИММУНОСУПРЕССИЯ ( ИО против собственных тканей): Иммунодепрессанты (кортикостероиды, азотиоприн) Плазмоферез для удаления из крови ЦИК Цитокины для регуляции функции Т-л (ИЛ 4, ИЛ 10) мк. АТ против CD 18, CD 44, CD 40 L, ФНО Иммуноглобулины для в/в введения для нейтрализации ауто. АТ 2. ИНДУКЦИЯ ЕСТЕСТВЕННОЙ ТОЛЕРАНТНОСТИ Т-л НА ТКАНЕВЫЕ АГ АТ против CD 4+ Т-л 3. МЕТАБОЛИЧЕСКАЯ КОРРЕКЦИЯ ФУНКЦИОНАЛЬНОЙ АКТИВНОСТИ ИКК (избирательная иммунорегуляция): Лазароиды Циклоспорин А Блокаторы ионных каналов

ТРАНСПЛАНТАЦИОННЫЙ ИММУНИТЕТ (ТИ) (лат. transplantatio – пересаживание) n Ответная иммунологическая реакция организма против АГ чужеродной ткани (трансплантата) – РХПТ или ИКК трансплантата против хозяина – РТПХ n Обусловлена содержанием в трансплантате генетически чуждых мембранных гликопротеидов – АГ гистосовместимости (ГКГС, МНС, HLA)

ТИПЫ ТРАНСПЛАНТАТОВ Ø АУТОТРАНСПЛАНТАТЫ – В ДРУГОЙ БИОТОП ОДНОГО ОРГАНИЗМА, ПЕРЕСАДКИ ПОЧТИ ВСЕГДА УСПЕШНЫ (кожа при лечении ожогов) Ø СИНГЕННЫЕ – ГЕНЕТИЧЕСКИ ИДЕНТИЧНЫМ ИНДИВИДАМ (МОНОЗИГОТНЫМ БЛИЗНЕЦАМ ИЛИ ИНБРЕДНЫМ ЖИВОТНЫМ), ПЕРЕСАДКИ ПРАКТИЧЕСКИ ВСЕГДА УСПЕШНЫ Ø АЛЛОГЕННЫЕ – МЕЖДУ ГЕНЕТИЧЕСКИ РАЗЛИЧНЫМИ ИНДИВИДАМИ ОДНОГО ВИДА, ОТЛИЧАЮЩИМИСЯ ПО ИЗОАГ • Иммуносупрессивная терапия позволяет трансплантатам не отторгаться, если Д и Р отличаются только по ГКГС II, но она недостаточна, если имеются различия по ГКГС I • Самая высокая эффективность при отсутствии несовместимых HLA-B и HLA-Dr АГ у Д и Р Ø КСЕНОГЕННЫЕ (гетеротрансплантаты) – между индивидами разных видов, отторгаются в кратчайшие сроки

РХПТ: клеточные реакции: роль Тх Презентация АГ и их распознавание Тх пролиферация и дифференцировка Тх продукция лимфокинов скопление Лф, плазмоцитов, Мф вокруг трансплантата инфильтрация трансплантата ИКК, деструкция клеток трансплантата воспаление и тромбоз сосудов нарушение питания трансплантата гибель и отторжение трансплантата

РХПТ: клеточные реакции: роль Тк Распознавание АГ аллотрансплантата Тк Тк лизируют клетки трансплантата погибшие клетки фагоцитируются Мф

РХПТ: гуморальные реакции Ø В течение 4 дней наблюдается приживление трансплантата, васкуляризация трансплантата происходит за счёт Д Ø Затем прорастают сосуды реципиента Если несовпадение между Д и Р по АГ ГКГС >50% успех маловероятен, т. к. АТ к АГ трансплантата связываются с эндотелиоцитами: 1) активация комплемента о. воспалительная реакция препятствие поступлению крови в трансплантат гибель трансплантата 2) индукция АЗКЦ разрушение трансплантата ПЯЛ и Мф реципиента 3) ГНТ иммунокомплексного типа разрушение трансплантата

ОТТОРЖЕНИЕ ТРАНСПЛАНТАТОВ Ø сверхострое (минуты) – АТ и комплемент Ø ускоренное - 1 -7 дней – Т-л и АТ Ø острое – 7 -21 день – Т-л Ø хроническое – месяцы, годы – Т-л и АТ

ПРЕДУПРЕЖДЕНИЕ ОТТОРЖЕНИЯ Ø ПОДБОР АДЕКВАТНОГО ДОНОРА ПО ТКАНЕВОЙ СОВМЕСТИМОСТИ Банк данных «Евротрасплантат» Ø НЕСПЕЦИФИЧЕСКАЯ ИММУНОСУПРЕССИЯ РЕЦИПИЕНТА С ПОМОЩЬЮ ПРЕПАРАТОВ, ИНГИБИРУЮЩИХ КЛЕТОЧНОЕ ДЕЛЕНИЕ циклоспорин А, меркаптопурин, кортикостероиды, облучение Ø СОЗДАНИЕ ТОЛЕРАНТНОСТИ ПУТЁМ ПЕРЕСАДКИ КЛЕТОК СЕЛЕЗЁНКИ И ККМ ПЛОДУ ИЛИ НОВОРОЖДЕННОМУ – применяется на животных до момента полного созревания ИС ! человек проходит эту стадию в конце II триместра внутриутробного развития

РТПХ: ЕСЛИ АКТИВНОСТЬ ИС Р ОБЛУЧЕНИЕМ, А В ТКАНИ ТРАНСПЛАНТАТА ИМЕЮТСЯ ИКК, ОНИ ОТВЕЧАЮТ НА АГ ХОЗЯИНА Механизм: Тк Д распознают клетки Р как генетически чужеродные и разрушают их Возникает при трансплантации клеток л/у, селезёнки, тимуса, ККМ При пересадке ККМ ч/з 10 -30 дней – дерматит, диарея, желтушный гепатит. Длится несколько суток. Исходы: - смерть или выздоровление в результате возникновения толерантности к Тк реципиента

ПРОБЛЕМЫ ТРАНСПЛАНТАЦИИ Ø ПОТРЕБНОСТИ РАСТУТ Ø ОГРАНИЧЕННЫЕ ВОЗМОЖНОСТИ Ø ПРОБЛЕМА СОВМЕСТИМОСТИ Ø ИДЕАЛЬНЫЙ ДОНОР – только в реанимации: мозг умер, но искусственно поддерживается дыхание, сохраняется температура и равномерное сильное сердцебиение, желателен молодой возраст, есть 30 -40 минут для взятия органа Ø ЭТИЧЕСКИЙ АСПЕКТ Ø ЭКОНОМИЧЕСКИЙ АСПЕКТ

Заключение: анамнез, объективные данные, инструментальные и лабораторные исследования однозначно свидетельствуют о наличии смерти мозга Симптомы смерти головного мозга: А. Отсутствие спонтанного дыхания __________________ Б. Реакция зрачков _________________________ В. Наличие окулоцефального рефлекса ________________ Г. Роговичный рефлекс _______________________ Д. Болевая реакция тройничного нерва ________________ Е. Фаринготрахеальный рефлекс ___________________ Ж. Атония всех мышц ________________________ И. Устойчивая гипотензия ниже 80 мм. рт. ст. (не менее 2 часов) ______ К. Инструментальное подтверждение прекращения мозгового кровотока ___ Л. Характеристика биоэлектрической функции мозга: а. через 12 часов __________________________ б. через 24 часа __________________________ Наличие признаков экзогенной и эндогенной интоксикации _______ гипотермия (ниже 32°С) _____, гиповолемического шока ______

ПЕРЕЧЕНЬ органов и тканей человека, подлежащих трансплантации 1. Почки 2. Печень 3. Сердце 4. Комплекс сердце-лёгкие 5. Костный мозг 6. Фрагменты костей свода и лицевого черепа 7. Твёрдая мозговая оболочка целиком или её фрагменты 8. Головной мозг и его отделы (участки) 9. Нижняя челюсть целиком или её фрагменты 10. Нижний челюстной сустав 11. Слуховые кости 12. Глазное яблоко целиком 13. Склера 14. Роговица 15. Хрусталик 16. Стекловидное тело 17. Позвонки и отделы позвоночника 18. Ключица 19. Лопатка и её фрагменты 20. Таз в целом или его кости 21. Локтевая и лучевая кости или их фрагменты 22. Плечевая кость или её фрагменты 23. Кости предплюсневые 24. Пяточная кость 25. Большеберцовая кость или ееёфрагменты 26. Малоберцовая кость или её фрагменты 27. Бедренная кость или её фрагменты 28. Надколенник 29. Ребра (без хряща) 30. Продольные распилы диафизов плечевой, бедренной и большеберцовой костей 31. Суставные концы локтевой, лучевой, плечевой, бедренной и большеберцовой костей с частью диафиза 32. Суставные хрящи костей верхних и нижних конечностей 33. Полный лучезапястный сустав с диафизами, капсулой и связками 34. Полный локтевой сустав с диафизами, капсулой и связками 35. Полный плечевой сустав с капсулой и связками 36. Полный голеностопный сустав с диафизами, капсулой и связками 37. Полный коленный сустав с диафизами, капсулой и связками 38. Полный тазобедренный сустав с диафизами, капсулой и связками 39. Костная стружка, крошка, порошок 40. Костная деминерализованная пленка 41. Хрящевая ткань 42. Широкая фасция бедра и ее фрагменты 43. Сухожилие костных мышц нижних конечностей 44. Кожные лоскуты 45. Нервы верхних и нижних конечностей 46. Брефоткани 47. Фетонейроны 48. Фрагменты спонгиозной ткани с отмытым костным мозгом 49. Железы внутренней секреции (гипофиз, надпочечники, поджелудочная, щитовидная, паращитовидная, слюнная)

ПАСПОРТ НА БИОТРАНСПЛАНТАТ Проведенные анализы и их результаты: - группа крови: ____________________ - резус-фактор: ____________________ - серологическая реакция на сифилис: __________ - ИФА-ВИЧ: ______________________ - реакция на Нbs-Аg, гепатит С-Аg: ____________ - бакпосев тканей: ___________________

Из ИНСТРУКЦИИ по изъятию тканевых трансплантатов человека Ø Забор органов и тканей у трупа человека не допускается, если учреждению здравоохранения на момент забора стало известно, что человек при жизни, а после его смерти - хотя бы один из его близких родственников (родители, муж, жена, дети) или его законный представитель заявили о своем несогласии на забор его органов и тканей после смерти Ø Изъятие тканевых биотрансплантатов производят до судебно-медицинского или патологоанатомического вскрытия трупа донора не позднее 4 -12 часов с момента смерти Ø Дежурный врач принимает решение о возможности использования трупа в качестве донора в течение часа Ø Перед изъятием тканей берется кровь (из подключичной вены) для последующего определения групповой и резус-принадлежности, постановки серологических реакций (сифилис, ВИЧ, гепатит) Ø После изъятия тканевых биотрансплантатов бригада в случае необходимости обеспечивает восстановительное протезирование трупа донора Ø Изъятые тканевые трансплантаты подвергаются бак. контролю, обработке и упаковке с последующей консервацией

Запрещается использование органов для трансплантации в случаях наличия у донора следующих сопутствующих заболеваний - острые отравления гемолитическими и нефротоксическими ядами - предшествующие заболевания почек, печени, сердца, лёгких (противопоказано для соответствующих органов) - злокачественные опухоли - болезни крови - сахарный диабет - инфекции (явные признаки вирусных заболеваний, туберкулёз) - травма органа, предполагаемого к изъятию - аутоиммунные заболевания - гепатиты - сифилис - ВИЧ-инфекция

ПЕРСПЕКТИВНЫЕ ВЫХОДЫ Ø СОЗДАНИЕ ИСКУССТВЕННЫХ ОРГАНОВ Необходимы материалы: - нейтральные по отношению к тканям - не приводящие к отторжению - поддающиеся обработке - долго служащие - прочные - приемлемые по цене Ø ПЕРЕСАДКА ОРГАНОВ ЖИВОТНЫХ !в организме свиньи могут оказаться латентные вирусы Ø ВЫРАЩИВАНИЕ ТКАНЕЙ И ОРГАНОВ ЧЕЛОВЕКА in vitro (клонирование)

ПРОТИВООПУХОЛЕВЫЙ ИММУНИТЕТ Концепция иммунного надзора (Ф. М. Бернет): контроль со стороны ИС за соматическими клетками Ø элиминация любых клеток, несущих чужеродную генетическую информацию Ø

Уровни иммунного надзора за опухолевыми клетками 1. Немедленный – ЕК, цитотоксические Мн, Мф, Гц, Тк 2. Последующий – специфический ИО с участием цитотоксических Тл, Мф, АТ, INF

Опухолевые АГ Ø Эмбриональные белки: - α-фетопротеин - хорионический гонадотропин - раковоэмбриональный АГ Ø Опухольспецифические АГ: - тканеспецифические (ПСА) - нетканеспецифические - уникальные – продукты мутантных генов (β-катенин)

Механизмы ускользания опухолей от иммунного надзора 1. Низкая экспрессия молекул ГКГС I нарушение распознавания 2. Не экспрессируются CD 80 и CD 86 анергия 3. АТ защищают опухоли от действия Тл (феномен опухолевого роста) 4. Феномен модуляции мембранных АГ (погружение внутрь клетки) 4. Выделение растворимых форм АГ 5. Мутации генов опухолевых клеток 6. Индукция иммуносупрессии: - продукция цитокинов, ИО (трансформирующие факторы α и β, ИЛ 10, простагландин Е 2) - формирование иммунологической толерантности к опухолевому АГ - активация супрессоров

Подходы к активации иммунной защиты от опухолей 1. Применение адъювантов – эффекта не дало 2. Цитокиновая терапия, в т. ч. генная цитокинотерапия 3. Обработка клеток (ЕК, Тк) цитокинами и введение в организм (=адоптивная (воспринимающая) терапия) 4. Создание противоопухолевых вакцин 5. Применение иммунотоксинов

Иммунокоррекция – комплекс мероприятий, позволяющих скорригировать нарушения иммунного статуса

Методы иммунокорригирующей терапии 1. Иммуностимуляция – активация ИС 2. Иммуносупрессия – подавление ИО 3. Иммуномодуляция – восстановление нормального функционирования ИС: стимуляция сниженного и угнетение повышенного иммунитета 4. Замещение недостающих иммунных факторов

Показания для иммунокоррекции Ø Аллергия и аутоиммунные болезни Ø Первичные и вторичные ИДС Ø Опухоли и лимфопролиферативные заболевания Ø Посттрансплантационные реакции Ø Нарушения репродукции

Виды иммунокоррекции Ø Общая и местная Ø Комбинированная и монокоррекция Ø Активная: - стимулирующая - подавляющая Ø Пассивная: - заместительная - подавляющая

Иммуностимуляторы по происхождению Ø Биологические – из тканей живых организмов: Бактериальные: пирогенал, зимозан, рибомунил Растительные: элеутерококк, женьшень Животного происхождения: • из селезёнки: спленин • из тимуса: Т-активин, тималин, вилозен • из костного мозга: миелопид Ø Химические: Природные: интерлейкины , интерфероны Синтетические: дибазол, левамизол Ø Физические: - лучевая терапия - ультразвук - магнитное поле

Иммуностимуляторы по действию Ø Т-лимфоцитов: – препараты тимуса (тактивин, вилозен) – химические препараты (левамизол, диуцифон) – медиаторы ИС (ИЛ-2) Ø В-лимфоцитов: – препараты костного мозга (миелопид) – препараты селезёнки (спленин) Ø Фагоцитов: – полисахариды (зимозан, продигиозан) – нуклеинат натрия

Иммунодепрессанты по происхождению Ø Кортикостероидные гормоны (преднизолон, декаметазон, гидрокортизон) Ø Цитостатики: - антиметаболиты (меркаптопурин, азотиоприн, метотрексат) - алкилирующие соединения (циклофосфан, хлорбутил) Ø Антибиотики (актиномицин Д, циклоспорин А) Ø Алкалоиды (винкристин) Ø Нестероидные противовоспалительные средства Ø Моноклональные АТ

Заместительная иммунокоррекция Ø Пересадка костного мозга Ø Пересадка тимуса и грудины Ø Трансфузия лейкоцитов Ø Введение -глобулина

СПАСИБО ЗА ВНИМАНИЕ!
2014_КЛИНИЧЕСКАЯ ИММУНОЛОГИЯ последняя лекция.ppt