2012 АНТИБИОТИКИ 1.pptx
- Количество слайдов: 100

Клиническая фармакология антибиотиков
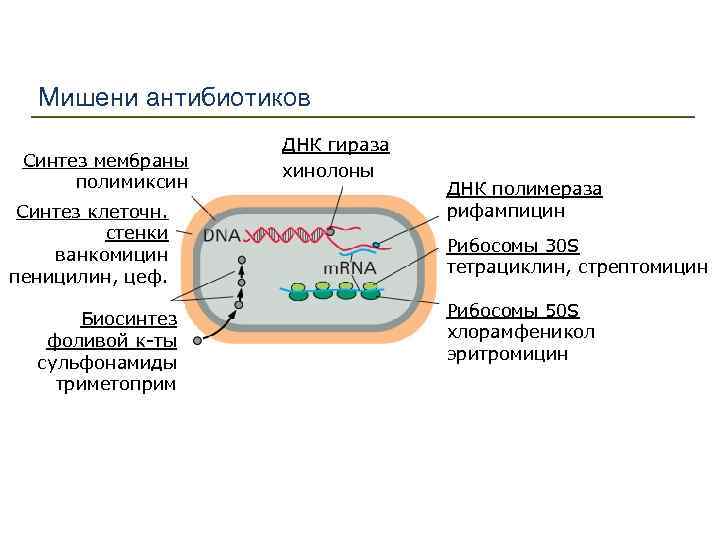
Мишени антибиотиков Синтез мембраны полимиксин Синтез клеточн. стенки ванкомицин пеницилин, цеф. Биосинтез фоливой к-ты сульфонамиды триметоприм ДНК гираза хинолоны ДНК полимераза рифампицин Рибосомы 30 S тетрациклин, стрептомицин Рибосомы 50 S хлорамфеникол эритромицин

Тесты на чувствительность к антибиотикам Метод серийных разведений Диско-диффузионный метод Str Tet 8 4 2 1 0 Тетрациклин (мкг/мл) МПК = 2 мкг/мл Ery Chl Amp
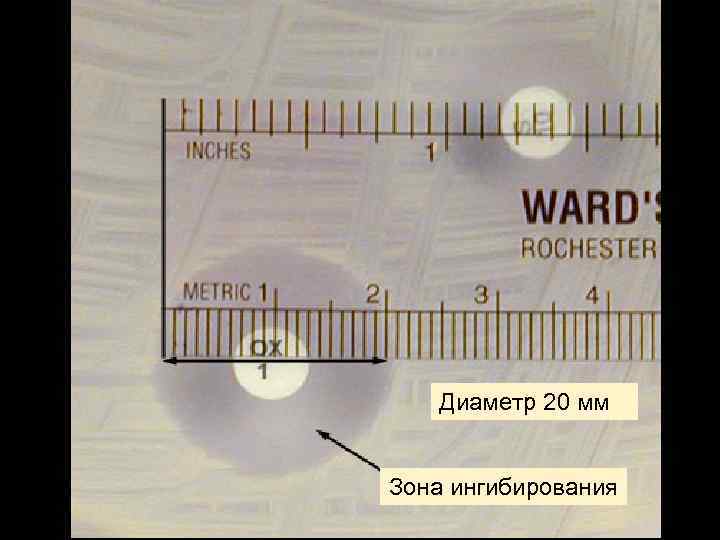
Диаметр 20 мм Зона ингибирования
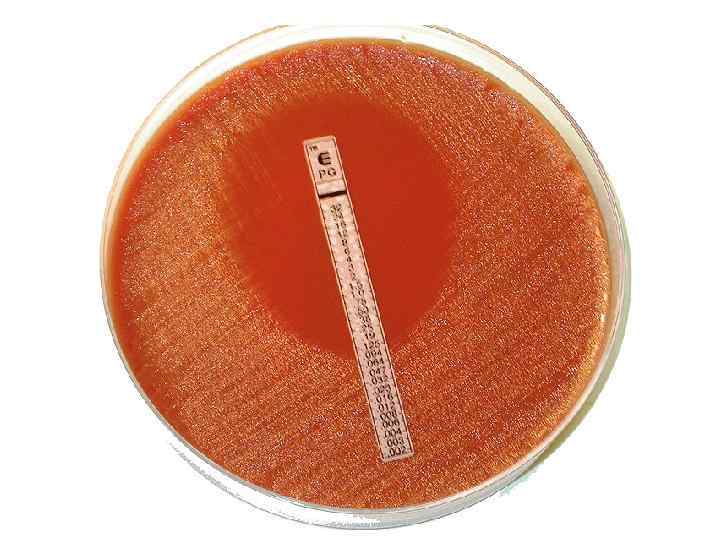
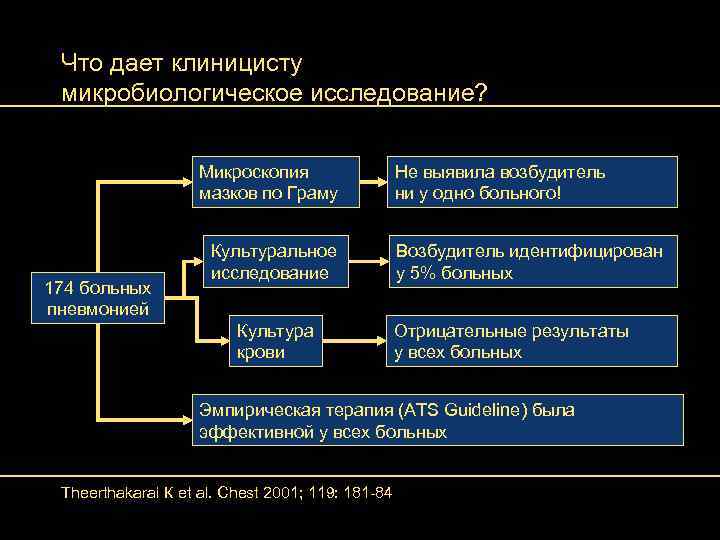
Что дает клиницисту микробиологическое исследование? Микроскопия мазков по Граму 174 больных пневмонией Культуральное исследование Культура крови Не выявила возбудитель ни у одно больного! Возбудитель идентифицирован у 5% больных Отрицательные результаты у всех больных Эмпирическая терапия (ATS Guideline) была эффективной у всех больных Theerthakarai К et al. Chest 2001; 119: 181 -84
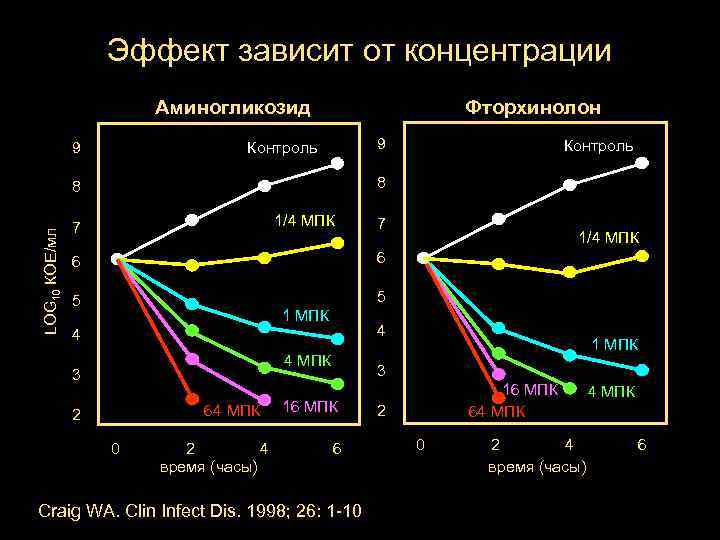
Эффект зависит от концентрации Аминогликозид Фторхинолон 9 Контроль 9 8 8 LOG 10 КОЕ/мл Контроль 1/4 МПК 7 7 6 6 5 1/4 МПК 5 1 МПК 4 4 4 МПК 3 64 МПК 2 0 2 4 время (часы) 1 МПК 3 16 МПК 6 Craig WA. Clin Infect Dis. 1998; 26: 1 -10 16 МПК 64 МПК 2 0 2 4 время (часы) 4 МПК 6
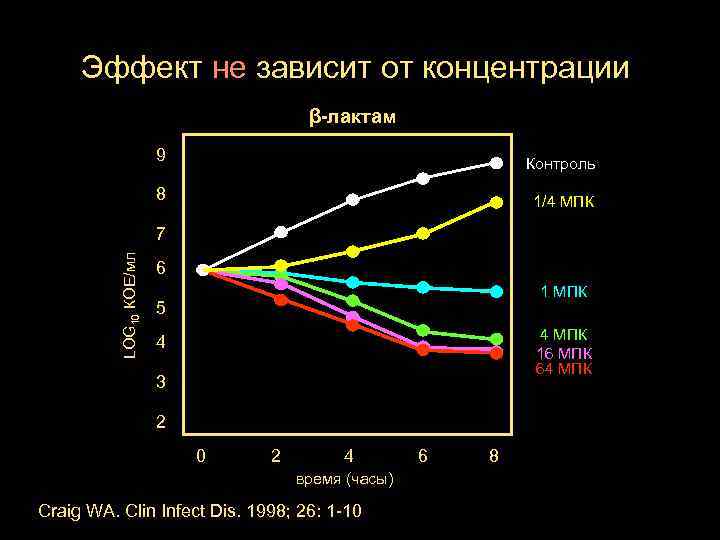
Эффект не зависит от концентрации β-лактам 9 Контроль 8 1/4 МПК LOG 10 КОЕ/мл 7 6 1 МПК 5 4 МПК 16 МПК 64 МПК 4 3 2 0 2 4 время (часы) Craig WA. Clin Infect Dis. 1998; 26: 1 -10 6 8
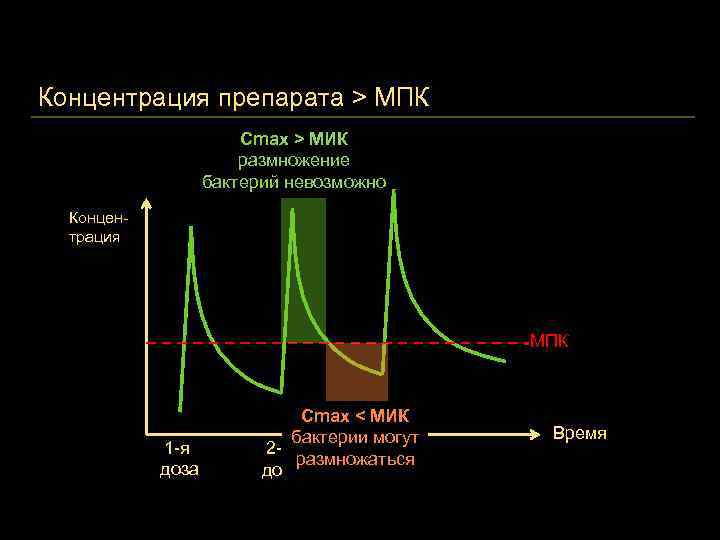
Концентрация препарата > МПК Cmax > МИК размножение бактерий невозможно Концентрация МПК 1 -я доза Cmax < МИК бактерии могут 2 -я 3 -я размножаться доза Время
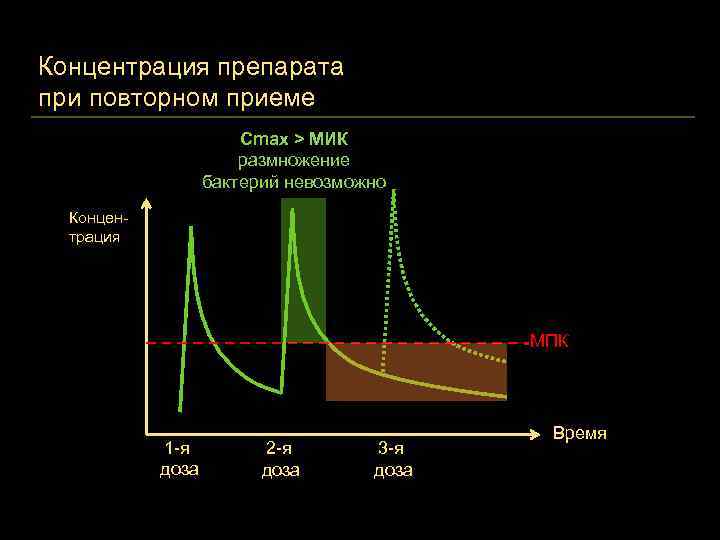
Концентрация препарата при повторном приеме Cmax > МИК размножение бактерий невозможно Концентрация МПК 1 -я доза 2 -я доза 3 -я доза Время
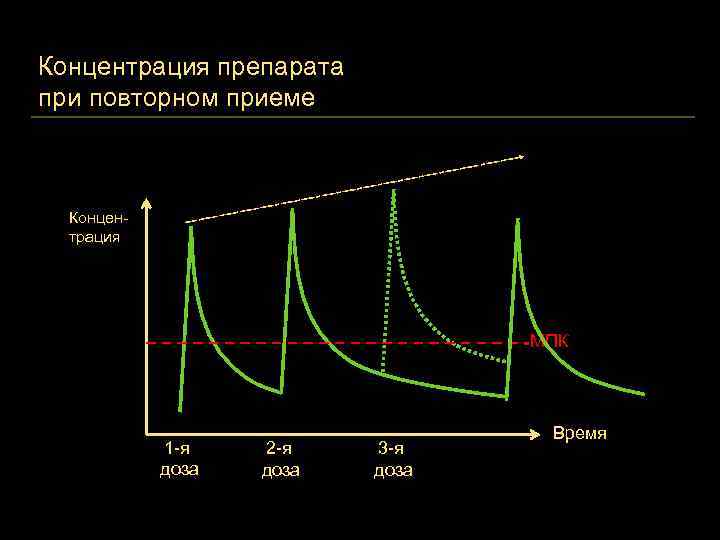
Концентрация препарата при повторном приеме Концентрация МПК 1 -я доза 2 -я доза 3 -я доза Время

Комплайнс l Точно соблюдают врачебные назначения: o на 3 -й день лечения: 44% o на 6 -й день лечения: 29% o на 9 -й день лечения: 18% l Данные мета-анализа 179 РКИ. Комплаентность: o при назначении 4 раза в день – 42 -51% o при назначении 3 раза в день – 52 -65% o при назначении 2 раза в день - 69 -70% o при однократном назначении – 73 -79% Dascher А et al. Acta Paediatr Scand 1975; 64: 105 -08 Bergman A et al. NEMJ 1963; 268: 1334 -38 Greenberg RN. Clin Ther 1984; 6: 592 -99 Claxton AJ et al. Clin Ther 2001; 21; 1296 -310
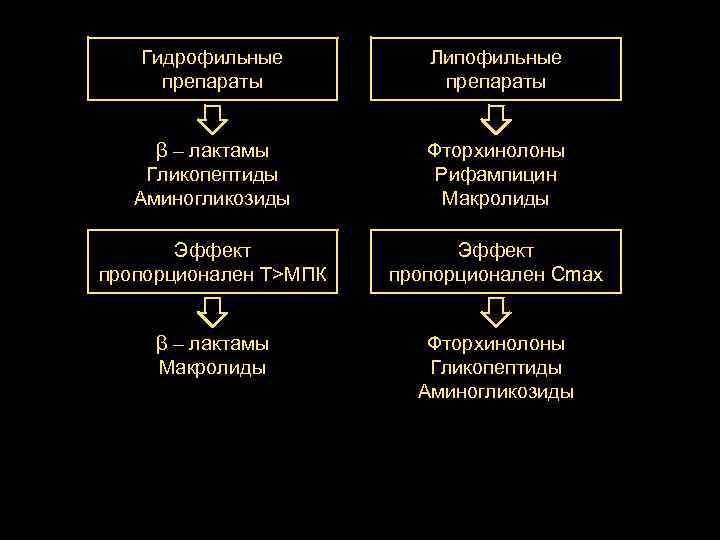
Гидрофильные препараты Липофильные препараты β – лактамы Гликопептиды Аминогликозиды Фторхинолоны Рифампицин Макролиды Эффект пропорционален T>МПК Эффект пропорционален Cmax β – лактамы Макролиды Фторхинолоны Гликопептиды Аминогликозиды

Физические свойства АБ Гидрофильные Липофильные Примеры β – лактамы Гликопептиды Аминогликозиды Фторхинолоны Рифампицин Макролиды Vd Высокий Низкий Максимальная концентрация Плазма, моча, гной Ткани и клетки На концентрацию препарата влияют массивная инфузия, дегидратация, диуретики С осторожностью при: Почечной недостаточности Печеночной недостаточности

«Возможно наступит время, когда пенициллин можно будет купить в магазине. И тогда появится опасность, что невежественный человек сможет принять недостаточную дозу и подвергнет собственные микроорганизмы экспозиции сублетальных концентраций препарата. Это может сделать микробы устойчивыми» Alexander Fleming's Nobel Lecture, 1945
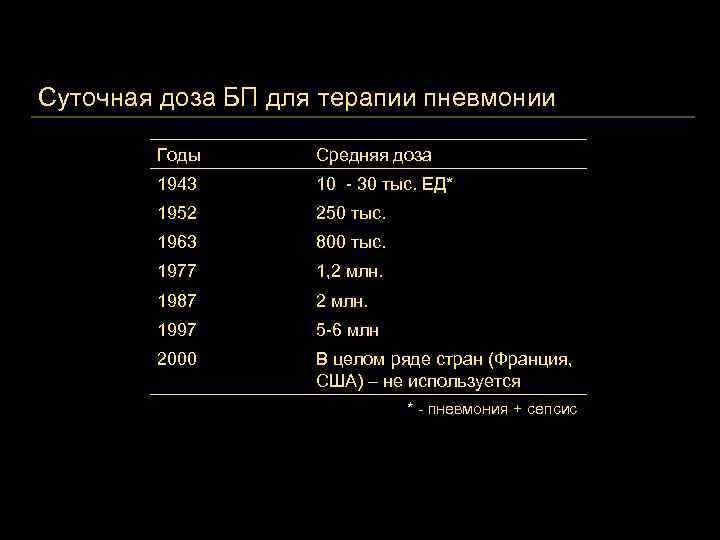
Суточная доза БП для терапии пневмонии Годы Средняя доза 1943 10 - 30 тыс. ЕД* 1952 250 тыс. 1963 800 тыс. 1977 1, 2 млн. 1987 2 млн. 1997 5 -6 млн 2000 В целом ряде стран (Франция, США) – не используется * - пневмония + сепсис
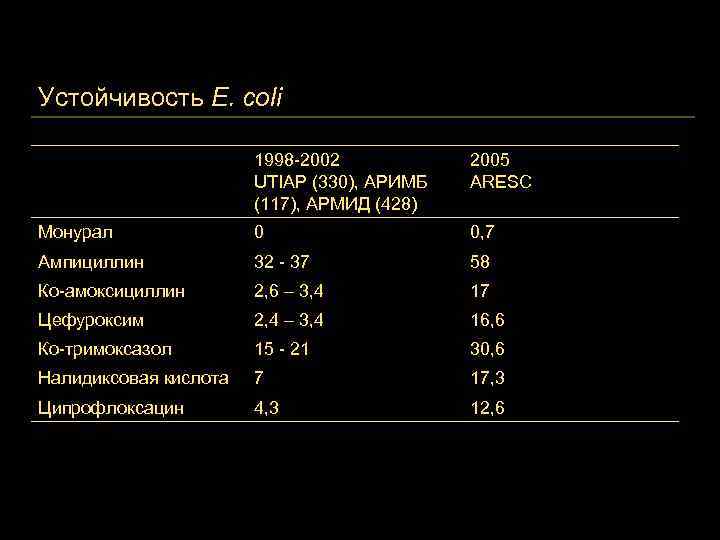
Устойчивость E. coli 1998 -2002 UTIAP (330), АРИМБ (117), АРМИД (428) 2005 ARESC Монурал 0 0, 7 Ампициллин 32 - 37 58 Ко-амоксициллин 2, 6 – 3, 4 17 Цефуроксим 2, 4 – 3, 4 16, 6 Ко-тримоксазол 15 - 21 30, 6 Налидиксовая кислота 7 17, 3 Ципрофлоксацин 4, 3 12, 6

Сельское хозяйство l В мире в год используется 90 -180 млн. кг антибиотиков l В целом, за 50 лет синтезировано 25 млрд. кг (по 4 кг на каждого жителя планеты) l На 1 кг антибиотиков, назначенных врачами, приходится 10 -30 кг в сельском хозяйстве В мире бактерий антибиотики вызывают экологическую катастрофу, так как уничтожают не только отдельного возбудителя, но изменяют всю среду обитания. LEVY, S. B. , 1997: Antibiotic resistance: an ecological imbalance. In: Antibiotic Resistance: Origins, Evolution, Selection and Spread. Ciba Foundation Symposium 207, S. 1 -14, Wiley, Chichester.

Больные l 82% семей имеют антибиотики в домашних аптечках l 54% опрошенных полагают, что антибиотики эффективны при лечении простуды и гриппа l только в 49% случаев опрошенные принимали антибиотики по назначению врача l 52% опрошенных принимали антибиотики в течении последнего года, в том числе, 9, 7% - три раза в год или чаще. Чаще всего опрошенные принимали: o 25% - ампициллин o 10% - ципрофлоксацин o 10% - ко-тримоксазол… l Андреева И. В. , 2003

Врачи l назначение антибиотиков при вирусных инфекциях l неправильный выбор антибиотиков l использование «иммуномодуляторов» , препаратов со спорной эффективностью

Механизмы устойчивости: l l l ферментная инактивация; разрушение и метаболизм; нарушение транспорта в клетку; эффлюкс из клеток; модификация мишеней (мутации генов ПСБ, ДНК-гиразы etc). l МО могут обмениваться генами, определяющими резистентность через бактериофагов. l Обмен плазмидами может происходить даже между различными видами и семействами МО
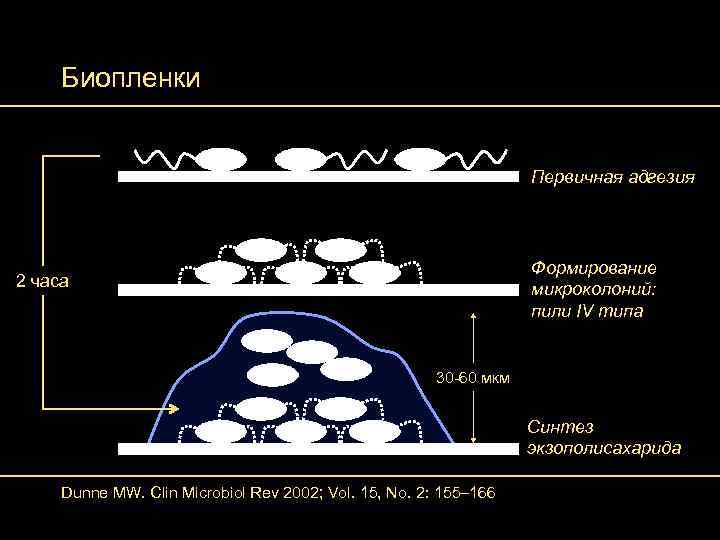
Биопленки Первичная адгезия Формирование микроколоний: пили IV типа 2 часа 30 -60 мкм Синтез экзополисахарида Dunne MW. Clin Microbiol Rev 2002; Vol. 15, No. 2: 155– 166

Биопленки защищают бактерии от действия антибиотиков Ванкомицин 72 часа Рифампицин 72 часа Dunne, W. M. , Jr. , E. O. Mason, Jr. , and S. L. Kaplan. 1993. Diffusion of rifampin and vancomycin through a Staphylococcus epidermidis biofilm. Antimicrob. Agents Chemother. 37: 2522– 2526.
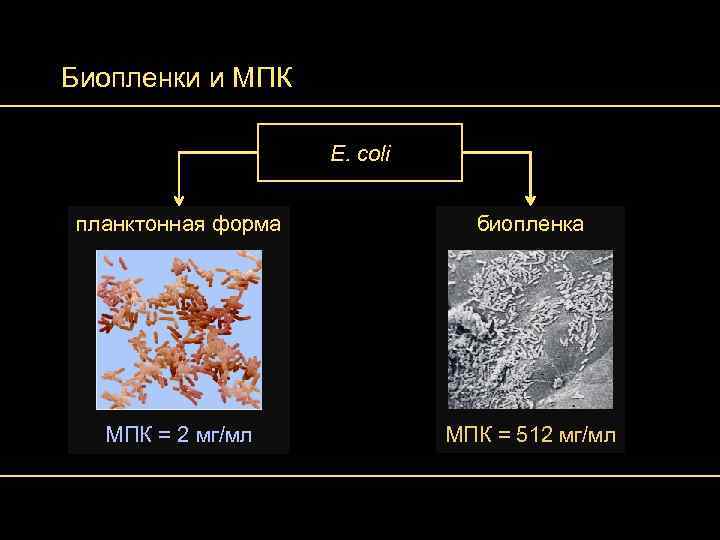
Биопленки и МПК E. coli планктонная форма биопленка МПК = 2 мг/мл МПК = 512 мг/мл
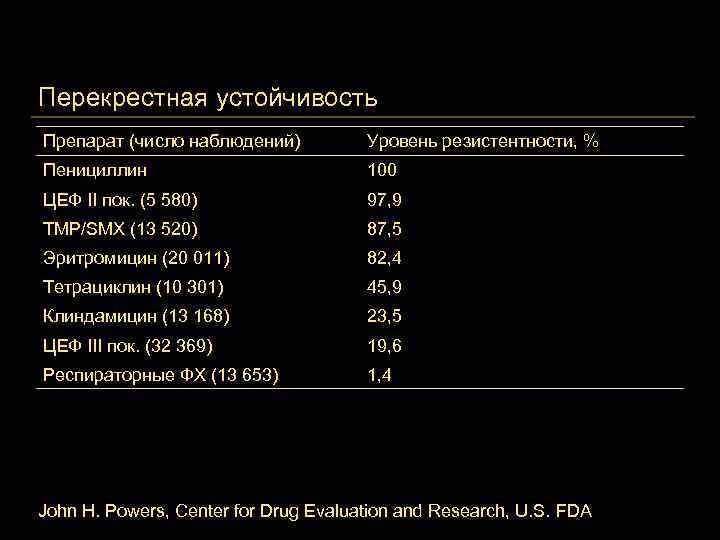
Перекрестная устойчивость Препарат (число наблюдений) Уровень резистентности, % Пенициллин 100 ЦЕФ II пок. (5 580) 97, 9 TMP/SMX (13 520) 87, 5 Эритромицин (20 011) 82, 4 Тетрациклин (10 301) 45, 9 Клиндамицин (13 168) 23, 5 ЦЕФ III пок. (32 369) 19, 6 Респираторные ФХ (13 653) 1, 4 John H. Powers, Center for Drug Evaluation and Research, U. S. FDA

Устойчивость отмечается не только у госпитальных штаммов l Госпитальные штаммы: o MRSA o MDR грамотрицательные МО (eg. P. aeroginosae) o резистентные к ванкомицину энтерококки o ESBL (K. pneumoniae, E. coli) l Внебольничные: o MRSA o PRSP o N. gonorrhea резист. к фторхинолонам

ESBL l K. pneumoniae, E. coli l Гидролизуют Цеф 30 l Часто сочетается с резистентностью к аминогликозидам, тетрациклину, фторхинолонам l В большинстве случаев клавулановая кислота in vitro ингибирует ESBL, но МО вырабатывают ESBL в концентрациях выше, чем концентрация ингибиторов. l Для терапии β-лактамы не назначаются, даже если к ним есть чувствительность in vitro.

классификация микроорганизмов

Г(+) аэробы Кокки (шаровидные) гроздья - Staphylococci пары - S. pneumoniae цепочки – Streptococcus viridans пары и цепочки - Enterococcus spp. Бациллы (палочковидные) Bacillus sp. Corynebacterium sp. Listeria monocytogenes Nocardia sp.

Г(-) аэробы Кокки (шаровидные) Peptococcus sp. Peptostreptococcus sp. Prevotella Veillonella Actinomyces Бациллы (палочковидные) Clostridium perfringens, Clostridium tetani, Clostridium difficile Bacteroides fragilis, Bacteroides disastonis, Bacteroides ovatus, Fusobacterium

Анаэробы «выше диафрагмы» Moraxella catarrhalis Neisseria meningitidis Haemophilus influenzae Pseudomonas aeruginosa* *неферментирующие глюкозу МО «ниже диафрагмы» E. coli, Enterobacter sp. Citrobacter, Klebsiella sp. Proteus sp. , Serratia Salmonella, Shigella Acinetobacter*, Helicobacter Neisseria gonorrhoeae

Другие бактерии l атипичные бактерии: o Legionella pneumophila o Mycoplasma pneumoniae или hominis o Chlamydia pneumoniae или trachomatis l Спирохеты: o Treponema pallidum (сифилис) o Borrelia burgdorferi (болезнь Лайма)
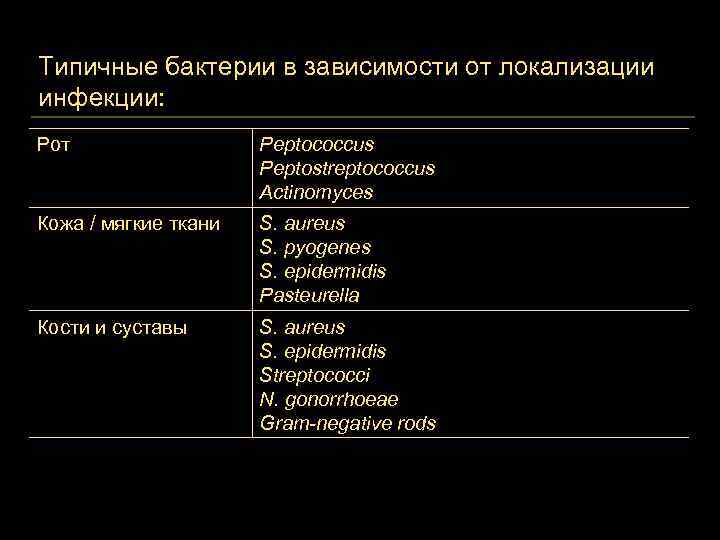
Типичные бактерии в зависимости от локализации инфекции: Рот Peptococcus Peptostreptococcus Actinomyces Кожа / мягкие ткани S. aureus S. pyogenes S. epidermidis Pasteurella Кости и суставы S. aureus S. epidermidis Streptococci N. gonorrhoeae Gram-negative rods

Типичные бактерии в зависимости от локализации инфекции: Верхние дыхательные пути S. pneumoniae H. influenzae M. catarrhalis S. pyogenes Нижние дыхательные пути (внебольничн. ) S. pneumoniae H. influenzae K. pneumoniae Legionella pneumophila Mycoplasma, Chlamydia Нижние дыхательные пути (госпитальн. ) K. pneumoniae P. aeruginosa Enterobacter sp. Serratia sp. S. aureus
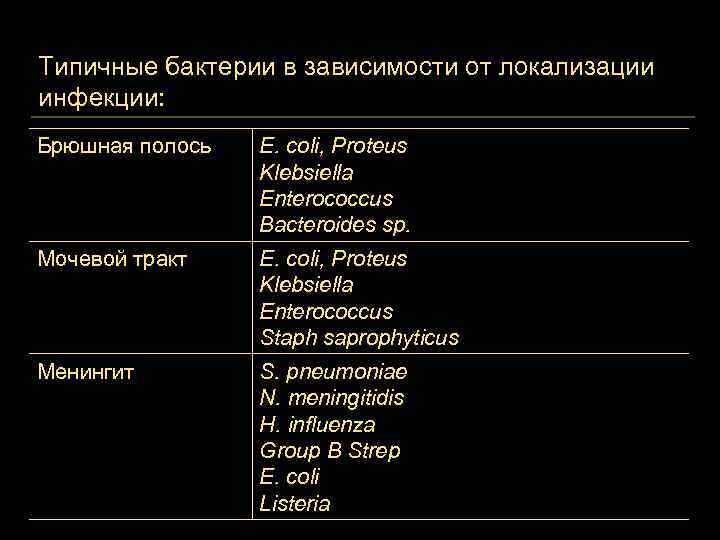
Типичные бактерии в зависимости от локализации инфекции: Брюшная полось E. coli, Proteus Klebsiella Enterococcus Bacteroides sp. Мочевой тракт E. coli, Proteus Klebsiella Enterococcus Staph saprophyticus Менингит S. pneumoniae N. meningitidis H. influenza Group B Strep E. coli Listeria

классы антибиотиков
Выбор эмпирической терапии зависит от: l нозологии l тяжести состояния l эпидемиологии (внебольничная / нозокомиальная инфекция) l состояния иммунитета

Когда можно говорить об иммунодефиците? l l Первичные иммунодефициты ВИЧ Болезни крови Преднизолон 2 и более таб. в день.

Выбор эмпирической терапии зависит от: l нозологии l тяжести состояния l эпидемиологии (внебольничная / нозокомиальная инфекция) l состояния иммунитета l предшествующей терапии Антибактериальная терапия должная быть начата как можно быстрее Материал для микробиологич. исследования целесообразно забрать до начала АБ терапии
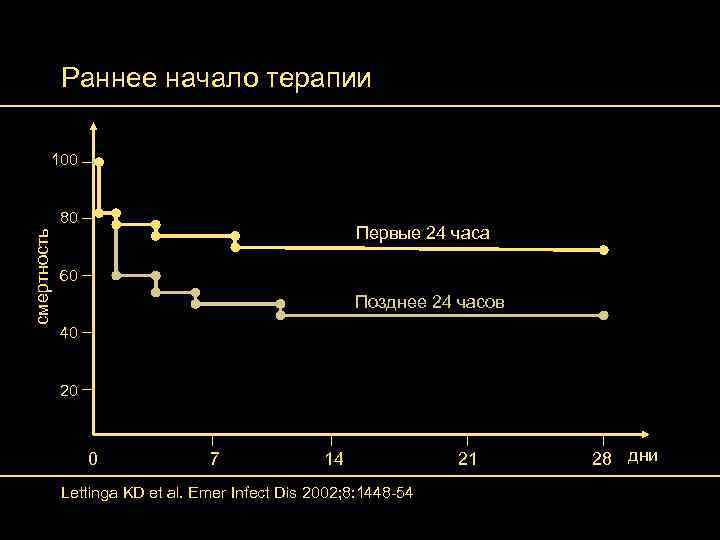
Раннее начало терапии 100 смертность 80 Первые 24 часа 60 Позднее 24 часов 40 20 0 7 14 Lettinga KD et al. Emer Infect Dis 2002; 8: 1448 -54 21 28 дни

Выбор эмпирической терапии зависит от: l нозологии l тяжести состояния l эпидемиологии (внебольничная / нозокомиальная инфекция) l состояния иммунитета l предшествующей терапии l рекомендаций национальных стандартов

Стандарты терапии пневмонии: амбулаторные больные Группа Лечение Нетяжелая ВП нет сопутствующих заболеваний и не принимали АБ последние 3 мес. Амоксициллин или Макролид внутрь. Нетяжелая ВП Амоксициллин/клавуланат есть сопутствующие ± макролид внутрь заболевания или / и Респираторный ФХ (лефо-, принимали АБ последние 3 мес. мокси- или гемифлоксацин) ≥ 2 дней. внутрь РРС & МАКМАХ 2010
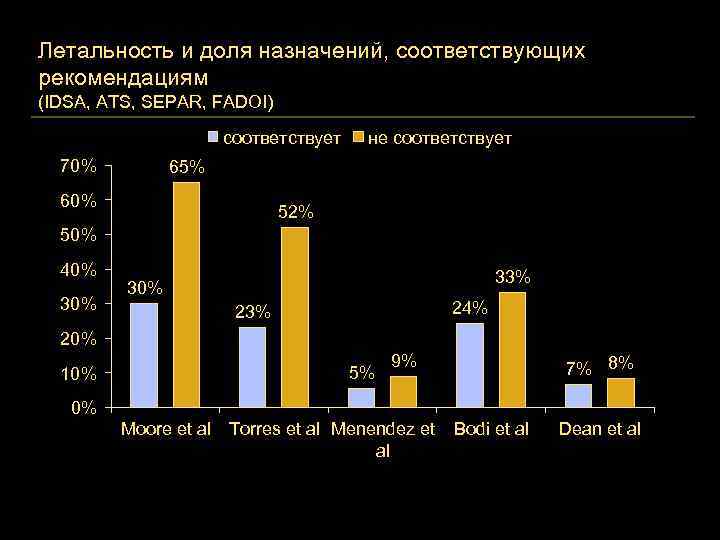
Летальность и доля назначений, соответствующих рекомендациям (IDSA, ATS, SEPAR, FADOI) соответствует 70% не соответствует 65% 60% 52% 50% 40% 33% 30% 24% 23% 20% 5% 10% 9% 7% 8% 0% Moore et al Torres et al Menendez et Bodi et al al Dean et al

β-лактамы l Содержат в своей структуре β-лактамное кольцо l Связываются с ПСБ клеточной стенки – в результате увеличивается проницаемость клеточной стенки l Клетки человека имеют только мембрану – для них пенициллины не опасны l Более активны в отношении Г(+) МО l Бактерицидное действие l Эффект зависит от времени
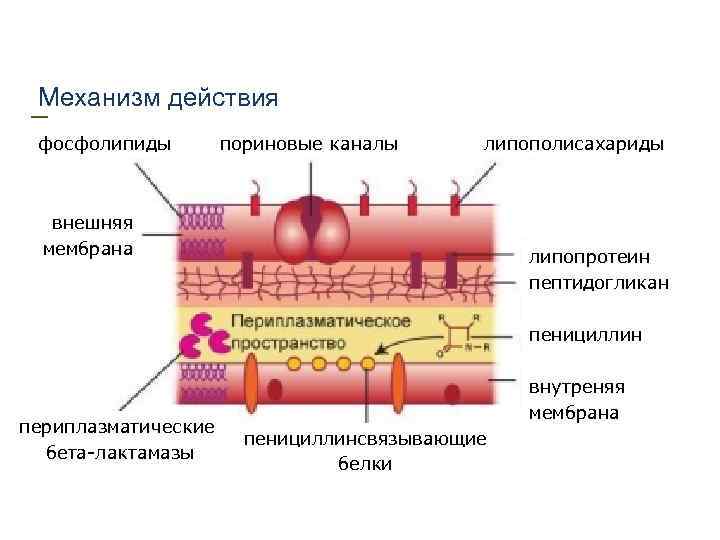
Механизм действия фосфолипиды пориновые каналы липополисахариды внешняя мембрана липопротеин пептидогликан пенициллин периплазматические бета-лактамазы внутреняя мембрана пенициллинсвязывающие белки

β-лактамы Механизм устойчивости l продукция β-лактамаз o самый важный и самое частый механизм o гидролиз бета-лактамного кольца и инактивация антибиотика l снижение проницаемость клеточной стенки для антибиотиков l модификация ПСБ

β-лактамы – пенициллины Бензилпенициллин (пенициллин G) l разрушается кислотой – назначается только парентерально l гидролизуется β-лактамазами l самый активный из пенициллинов l узкий спектр действия: o Strepptococcus pyogenes, o S. pneumoniae, o Neisseria meningitis o N. gonorrhoeae, o трепонемы, o клостридии

β-лактамы – пенициллины Пенициллин V l Феноксиметилпенициллин – устойчив к кислоте l может назначаться внутрь l в остальном сходен с пенициллином G

β-лактамы – пенициллины Ампициллин l в сравнении с пенициллином: o активность ниже o спектр шире: ▪ + Strept. faecalis, ▪ Haemophilus influenza ▪ E. coli, Klebsiella и Proteus l кислотоустойчив l гидролизуется β-лактамазой

β-лактамы – пенициллины Амоксициллин l сходен с пенициллином, но лучше абсорбируется приеме внутрь l обычно назначается в сочетании с клавулановой кислотой l спектр = ампициллину

β-лактамы – пенициллины Антистафилококковые пенициллины l Оксациллин (парентерально) l Флуклоксациллин (внутрь, парентерально) l устойчивы в отношении пенициллиназ стафилококков l применяются при инфекциях, вызванных Staphylococcus aureus

β-лактамы – пенициллины Азлоциллин l назначается только парэнтерально l чувствителен к b-лактамазам l широкий спектр, включая Pseudomonas aeruginosa и Proteus species l назначается ВВ при тяжелых инфекциях и у больных с иммунодефицитом
β-лактамы – пенициллины Карбоксипенициллины l Карбенициллин l Тикарциллин l Активны в отношении резистентных Г(-) бактерий: l Enterobacter spp. l Pseudomonas aeruginosa

β-лактамы – пенициллины Фармакокинетика l Пенициллины гидрофильны и обычно не проходят через ГЭБ, но при воспалении, когда проницаемость ГЭБ повышается пенициллины проникают в ткань мозга и могут применяться для терапии менингитов l Активно выводятся почками в неизмененном виде – при ХПН дозу пенициллина следует уменьшить

β-лактамы – пенициллины НЯ l Аллергия (у 0. 7% - 1. 0% больных). Проявления от крапивницы, до анафилактического шока l Суперинфекция (кандидозы) l Диарея: чаще всего при терапии ампициллином, реже при лечении амоксициллином l Редко: нефрит

β-лактамы – пенициллины Лекарственные взаимодействия l Ампициллин может снижать эффективность пероральных контрацептивов

β-лактамы – цефалоспорины Цефалоспорины l Разделяются на 4 группы – «поколения» l В основе классификации: o спектр активности o чувствительность к β-лактамазам

β-лактамы – цефалоспорины Поколения цефалоспоринов: l 1 -е – ранние препараты, близкие по активности к ампициллину l 2 -е – резистентны к β-лактамазам l 3 -е - резистентны к β-лактамазам + шире спектр и выше активность l 4 -е – более широкий спектр + самая высокая активность

β-лактамы – цефалоспорины Цефалоспорины 10 цефазолин, цефалексин 20 цефуроксим Staph BL- (кр. Еnterococci / кр. MRSA) Г- энтеробактерии (кр. Enterobacter / кр. Рseudomonos)

β-лактамы – цефалоспорины Цефалоспорины третьего поколения l Цефтриаксон и цефотаксим o максимальная активность в отношении Г(+) аэробов, включая пенициллинрезистентные штаммы S. pneumoniae l Цефтазидим и цефоперазон o Pseudomonas aeruginosa l Препараты этой группы могут индуцировать продукцию βлактамаз расширенного спектра

β-лактамы – цефалоспорины Цефепим - цефалоспорин четвертого поколения l Шрокий спектр активности: o Г (+) = цефтриаксон o Г (-) = цефтазидим, включая Pseudomonas aeruginosa и продуцирующие β-лактамазы штаммы Enterobacter sp. l Стабилен в отношении β-лактамаз l Мало индуцирует продукцию β-лактамаз расширенного спектра

β-лактамы – цефалоспорины НЯ l Аллергия (в 10 -20% перекрестная аллергия с пенициллинами) l Острый нефрит и ОПН l Суперинфекция l Дисбактериоз при назначении внутрь l Цефамандол, цефотетан, цефоперазол – гипопротромбинэмия из-за уменьшение продукции витамина К в клетках кишечника l Несовместимы с этанолом

β-лактамы – карбапенемы Карбапенемы l Имипенем активно гидролизуется почками, назначается в сочетании с ингибитором дегиропептидаз циластатином. Может вызывать судорожный синдром (нельзя использовать при лечении менингита) l Меропенем l Дорипенем

β-лактамы – карбапенемы Карбапенемы l Самый широкий спектр антимикробной активности: o Г (+) и Г (-) аэробы и анаэробы o карбапенемы не активны в отношении: MRSA, VRE, коагулазо-негативных staph, C. difficile.

β-лактамы – монобактамы Монобактамы (Азтреонам) l связывается с ПСБ 3 Г(-) аэробов: o E. coli, o K. pneumoniae, o P. mirabilis, o H. influenzae и M. catarrhalis, o Enterobacter, o Citrobacter, o Salmonella, Shigella, o Pseudomonas aeruginosa l не активен в отношении Г(+) и анаэробов

β-лактамы Общие особенности фармакокинетики l Активно выводятся почками в неизмененном виде – при ХПН дозы следует уменьшить l Оксациллин, пиперациллин, цефтриаксон и цефоперазон метаболизируются печенью l все β-лактамы имеют короткий период полувыведения, исключение цефтриаксон l многие препараты выпускаются в виде натриевых солей – это надо учитывать при выборе препаратов для больных ХПН и ХСН

Хинолоны Классификация хинолонов и фторхинолонов l 1 -е поколение (Хинолоны: налидиксовая кислота) применение ограничено мочевой инфекцией (E. coli) l 2 -е поколение (Фторхинолоны: ципрофлоксацин, норфлоксацин) – широкий спектр активности в отношении Г(-) аэробов + синегнойная палочка (ципро-). l 3 -е поколение (Фторхинолоны: левофлоксацин, моксифлоксацин = “респираторные” ФХ) + S pneumonia, но активность в отношении Г(-) аэробов и синегнойной палочки – ниже.

Хинолоны Спектр активности ФХ l Г (-): ципро = лево > мокси l Pseudomonas aeruginosa – ципро и лево l Г (+) – 1 и 2 поколения неактивны, новые “респираторные” ФХ: o метициллин-чувствительные Staphylococcus aureus o Streptococcus pneumoniae (включая устойчивые к пенициллину)

Хинолоны Спектр активности ФХ (продолжение) l все ФХ активно в отношении атипичных МО: o Legionella pneumophila o Chlamydia spp. o Mycoplasma spp. o Ureaplasma urealyticum l Другие МО – Mycobacterium tuberculosis (ципро), Bacillus anthracis

Хинолоны НЯ l ЖКТ – 5 % (тошнота, рвота, диарея) l Центральная нервная система (головная боль, возбуждение, бессонница, головокружение, редко, галлюцинации и эпилептические припадки (пожилые люди) l Гепатотоксичность
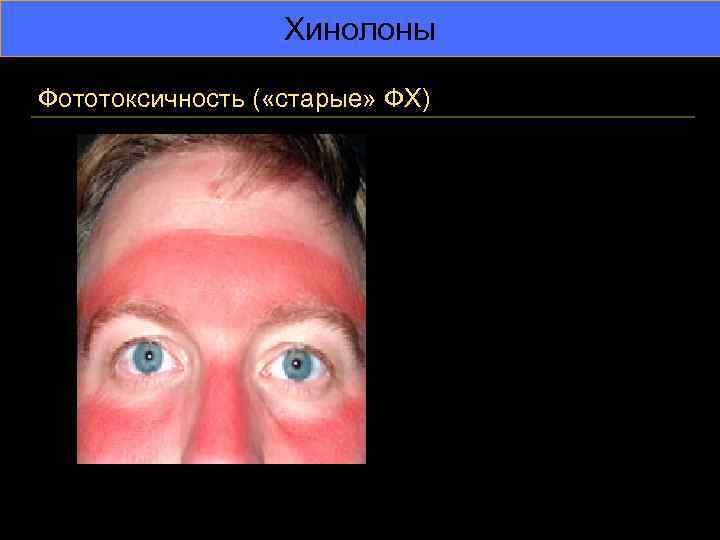
Хинолоны Фототоксичность ( «старые» ФХ)
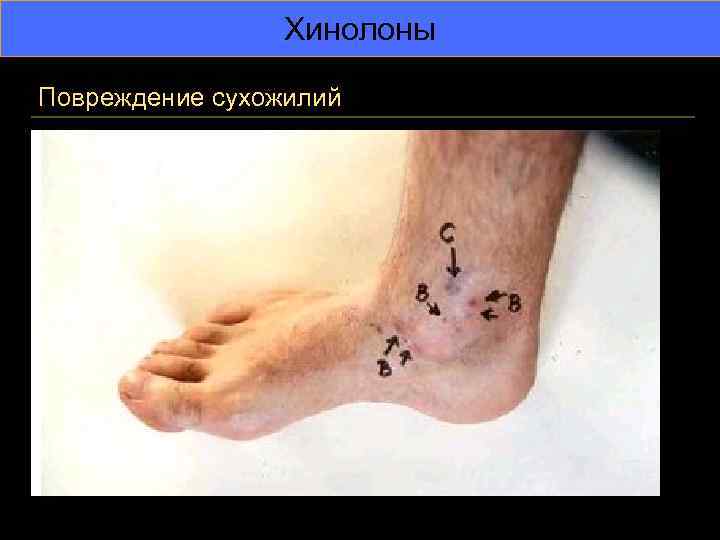
Хинолоны Повреждение сухожилий

Хинолоны Взаимодействия l Хелатные комплексы с двух- и трехвалентными катионами: o солит цинка, железа, кальция, алюминия, магния o антациды, сукральфат, энтеральное питание o пища, богатая кальцием o интервал между приемом ФХ не менее 2 -4 часов l Теофиллин и циклоспорин - ципро тормозит метаболизм, ↑ концентрации и ↑ токсичности l Варфарин l Макролиды и антигистаминные – риск аритмии

Макролиды l Эритромицин – узкий спектр, короткий период выведения, нестабилен в кислой среде, вызывает тромбофлебиты при ВВ инъекциях. l Новые макролиды: кларитромицин и aзитромицин: o шире спектр o лучше показатели фармакокинетики: ▪ выше биодоступность ▪ лучше проникают в ткани и клетки ▪ дольше задерживаются в организме o лучше переносятся

Макролиды l Эритромицин и кларитромицин – эффект зависит от времени l Азитромицин - – эффект зависит от концентрации l У всех макролидов действие бактериостатическое

Макролиды Механизмы резистентности l активный эффлюкс l модификация мишеней l перекрёстная резистентность

Макролиды Спектр активности l Г (+) аэробы: кларитро > эритро > азитро o метициллин-чувствительные Staphylococcus aureus o Streptococcus pneumoniae но только чувствительные к пенициллину o Bacillus spp. , Corynebacterium spp. l Г (-) аэробы: азитро > кларитро o H. influenzae (кроме эритро), o M. catarrhalis, o Neisseria spp. o все макролиды неактивны в отношении Enterobacteriaceae

Макролиды Спектр активности l Анаэробы (верхние дыхательные пути) l Атипичные бактерии: o Legionella pneumophila o Chlamydia spp. o Mycoplasma spp. o Ureaplasma urealyticum l Другие бактерии – Treponema pallidum, Campylobacter, Borrelia, Bordetella, Brucellа

Макролиды Абсорбция l Эритромицин – низкая биодоступность, вариабильная абсорбция (F = 15 -45%); прием пищи может снижать степень абсорбции l Кларитромицин – кислотоустойчив, хорошо абсорбируется (F = 55%) независимо от приема пищи l Азитромицин – кислотоустойчив, прием пищи может снижать степень абсорбции (F = 38%)

Макролиды Распределение l Кларитро и азитромицин хорошо проникают в ткани и клетки. Концентрация в тканях >> концентрации в плазме

Макролиды Элиминация l Кларитромицин частично выводится почками (18% от дозы). l все макролиды метаболизируются в печени l Период полувыведения: o эритромицин 1. 4 часа o кларитромицин 3 – 7 часов o азитромицин - 68 часов

Макролиды НЯ l ЖКТ (до 33 % больных) – тошнота, рвота, диарея (чаще всего при назначении эритромицина l Редко: холестатический гепатит l Другое: ототоксичность, удлинение QTc, аллергия

Макролиды Лекарственные взаимодействия l Эритро и кларитромицин – ингибируют CYP P 450. При одновременном назначении может повышаться концентрация: o теофиллина o дигоксина o варфарина o карбамазепина o и многих др. препаратов

Аминогликозиды Механизм действия l угнетают синтез белка l 30 S рибосомы l бактерицидное действие зависит от концентрации

Аминогликозиды Спектр активности l Г (+) аэробы: oбольшинство штаммов S. aureus и Streptococci o. Enterococcus spp. l Г (+) аэробы (кр. стрептомицина): o. E. coli, K. pneumoniae, Proteus sp. , Acinetobacter, Citrobacter, Enterobacter sp. , Serratia, Salmonella, Shigella l Pseudomonas aeruginosa (амика>торба>гент) l Mycobacteria tuberculosis - стрепто l атипичные МО – стрепто и амикацин

Аминогликозиды Гентамицин l чаще всего применяется l в основном Г(-) аэробы: E. coli, Klebsiella, S. faecalis, Pseudomonas и Proteus spp. l активен в отношении Staphylococcus aureus. l Не активен по отношению к стрептококкам

Аминогликозиды др. препараты l Тобрамицин: при инфекциях, вызванных синегнойной палочной и гентамицинрезистентными МО l Амикацин – самый активный в отношении Pseudomonas l Неомицин – применяется внутрь для деконтаминации ЖКТ

Аминогликозиды Фармакокинетика l не абсорбируются приеме внутрь l в основном распределяются в интерстициальной жидкости l выделяются почками в неизмененном виде (85 -95% от дозы) l при ХПН элиминация резко замедляется – токсические эффекты

Аминогликозиды НЯ l Нефротоксичность o острая почечная недостаточность из-за повреждения проксимальных канальцев o обратима, если вовремя замечено повышене креатинина o фактор риска – пожилые, прием препарат >2 -х нед. l Ототоксичность o повреждение 8 -й пары ЧМН o необратимы o головокружение, атаксия, шум в ушах, снижение слуха

Гликопептиды: Ванкомицин Спектр активности l Г (+) бактерии: o. MSSA и MRSA и коагулазонегативные стафилококки o. Streptococcus pneumoniae (включая PRSP) o. Streptococcus spp. o. Enterococcus spр. o. Сlostridium sp. (включая C. difficile), Peptococcus, Peptostreptococcus l Не активен в отношении Г(-) МО

Гликопептиды: Ванкомицин Фармакокинетика l плохо всасывается приеме внутрь l применяется ВВ l хорошо в ткани и жидкости, в том числе в жировую ткань l выделяется с мочей. Период полувыведения зависит от функции почек

Гликопептиды: Ванкомицин l Препарат для терапии инфекций, вызванным MRSA: o бактериемии, эмпиема, эндокардит, перитонит, пневмония, инфекции кожи и мягких тканейи, остеомиелит l тяжелые инфекции у больных, которые не переносят βлактамы l инфекции, вызванные резистентными бактериями l внутрь при псевдомембранозном коллите (C. difficile)

Гликопептиды: Ванкомицин Синдром красного человека l покраснение, зуд, эритематозная сыпь на лице и верхней части туловища l препарат следует вводить медленно - не менее 60 минут l разрешается спонтанно после прекращения инфузии l профилактическое назначение антигистаминных средств

Гликопептиды: Ванкомицин НЯ l Нефро- и ототоксичность: o редко при монотерапии o часто при назначении других нефротоксичных препаратов l сыпь l тромбофлебиты l нейтропения и тромбоцитопения

Оксазолиды: Линезолид l первый препарат из новой группы антибиотиков, l одобрен в 2000 г l разработан для терапии инфекций, вызванных резистентными возбудителями (MRSA, VRE)

Оксазолиды: Линезолид Спектр активности l Г(+) бактерии o. MSSA, MRSA, VRSA и коагулазонегативные стафилококки o. Streptococcus pneumoniae (включая PRSP), Streptococcus spp. o. Enterococcus faecium и faecalis (включая VRE) l Bacillus. Listeria, Clostridium spp. (кр. C. difficile), l атипичные МО (Mycoplasma, Chlamydia. , Legionella)
Оксазолиды: Линезолид Фармакология l Бактерицидное действие l 100% биодоступность l Быстро проникает в ткани с высоким уровнем кровообращения l Выведение – почти и печень. t½ 4. 4 - 5. 4 часов

Оксазолиды: Линезолид НЯ l ЖКТ – тошнота, рвота, диарея (6 - 8 %) l Головная боль – 6. 5% l тромбоцитопения – 2 to 4% o при длительном (>2 нед. ) назначении o обратима после отмены препарата
2012 АНТИБИОТИКИ 1.pptx