антибиотики.pptx
- Количество слайдов: 81

Клиническая фармакология антибиотиков и принципы антибиотикотерапии в ОИТР к. м. н. Смирнов В. М. отделение анестезиологии и реанимации РНПЦ Онкологии и медицинской радиологии им. Н. Н. Александрова

Определения понятий Инфекция – клинический диагноз, при котором наличие положительного посева из очага инфекции с колонией возбудителя сочетается с клиническими признаками системной воспалительной реакции. Требует назначения антибактериальной терапии. Колонизация – состояние, при котором наличие положительного посева из предполагаемого очага инфекции сочетается с отсутствием клиники воспаления. Не требует назначения антибиотиков. Антибактериальная терапия – применение антибиотиков с лечебной целью при клинически и/или лабораторно доказанной инфекции Эмпирическая антибактериальная терапия – антибактериальная терапия, которая назначается без уточнения материалов микробиологических исследований, на основании мониторинга чувствительности наиболее часто высеваемых в отделении возбудителей. Целенаправленная антибиотикотерапия – антибактериальная терапия, назначаемая по данным чувствительности возбудителя, выделенного из очага инфекции.

Определения понятий Антибиотикопрофилактика – применение антибиотиков при отсутствии инфекции с профилактической целью, длительностью не более 24 часов или в виде однократной суточной дозы. Профилактическая антибиотикотерапия – назначение антибиотиков курсом с лечебной целью при отсутствии клинических и лабораторных признаков инфекции. Резистентность микроорганизма in vitro – устойчивость микроорганизма к антибактериальному препарату, применяемому в стандартных терапевтических дозах. Перекрестная резистентность, индукция резистентности – явление, при котором применение антибактериального препарата вызывает рост устойчивого штамма не только к самому препарату, но и к антибиотикам других групп. Полирезистентность микроорганизма – устойчивость микроорганизма к трем и более классам антибиотиков Панрезистентность – вид полирезистентности, при котором чувствительность отсутствует или сохраняется только к одному АБ.

Клиническая фармакология антибиотиков
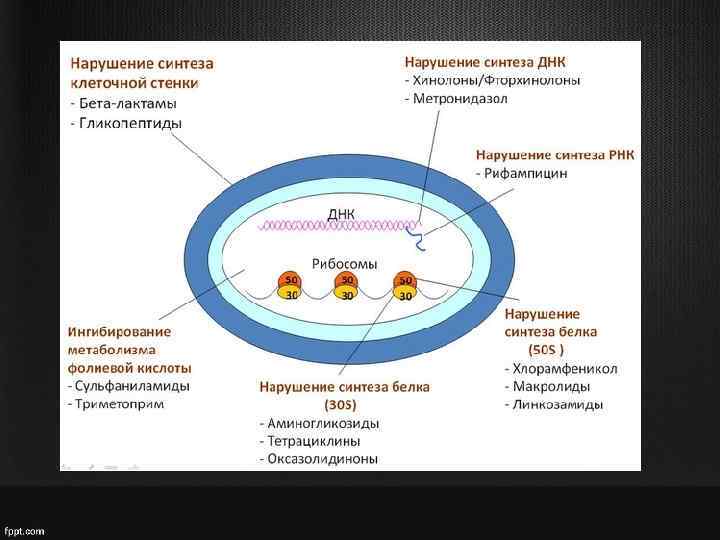
• Синтез и барьерная функция бактериальной стенки; • Синтез нуклеиновых кислот; • Синтез белка.
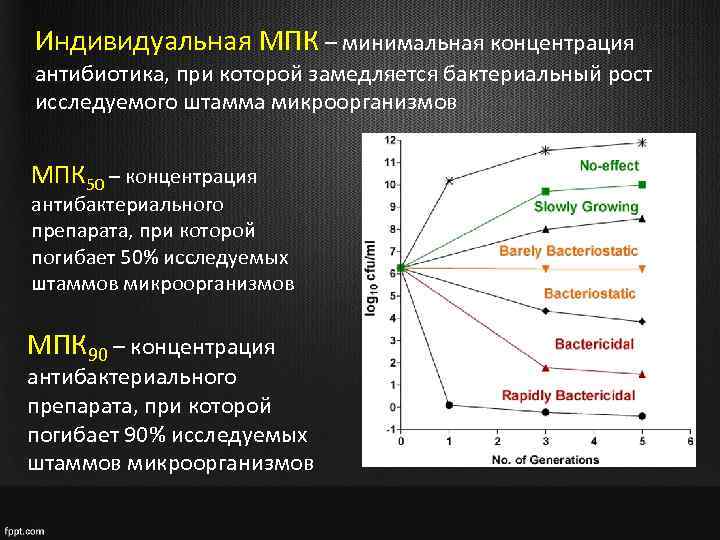
Индивидуальная МПК – минимальная концентрация антибиотика, при которой замедляется бактериальный рост исследуемого штамма микроорганизмов МПК 50 – концентрация антибактериального препарата, при которой погибает 50% исследуемых штаммов микроорганизмов МПК 90 – концентрация антибактериального препарата, при которой погибает 90% исследуемых штаммов микроорганизмов
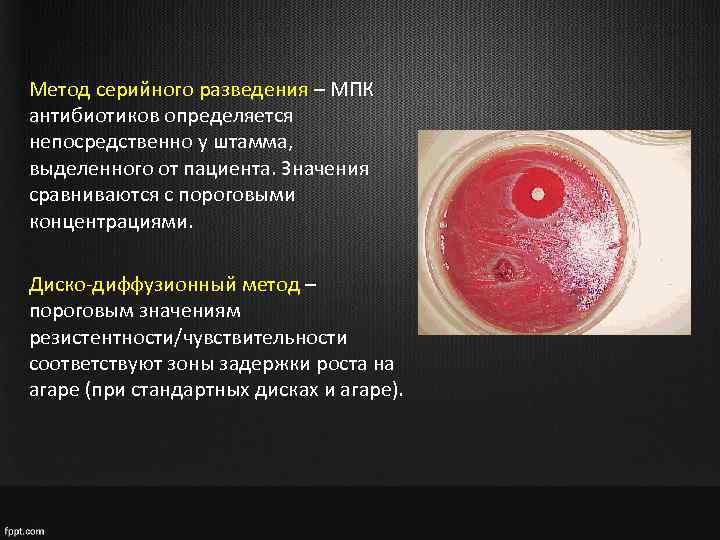
Метод серийного разведения – МПК антибиотиков определяется непосредственно у штамма, выделенного от пациента. Значения сравниваются с пороговыми концентрациями. Диско-диффузионный метод – пороговым значениям резистентности/чувствительности соответствуют зоны задержки роста на агаре (при стандартных дисках и агаре).

Breakpoint (порог чувствительности/резистентности) Стандартное референтное значение, отражающее, в т. ч. концентрацию антибиотика в очаге инфекции применении его в терапевтических дозах. • Разрабатываются FDA и the National Committee on Clinical Laboratory Standards (NCCLS) • Существуют пороги резистентности и пороги чувствительности, на основании которых штаммы относят к чувствительным/резистентным к данному АБ Таким образом, антибиотик может быть признан эффективным только в случае, если МПК исследуемого штамма ниже Breakpoint (соотношения МПК/breakpoint меньше или равно единице )
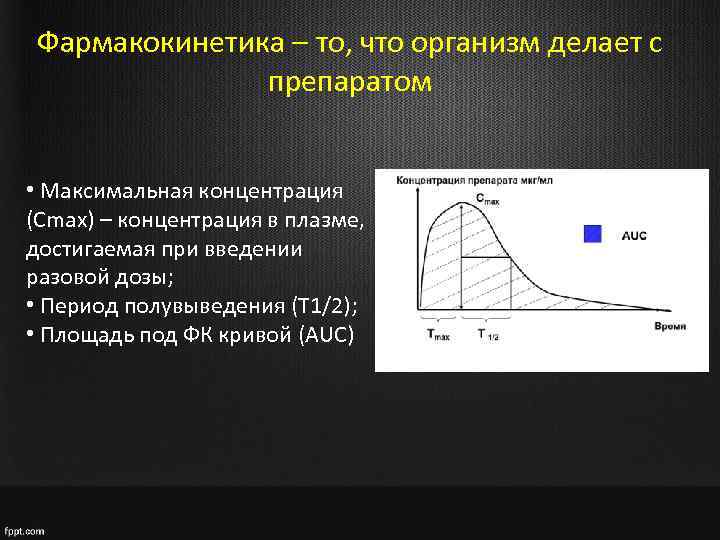
Фармакокинетика – то, что организм делает с препаратом • Максимальная концентрация (Cmax) – концентрация в плазме, достигаемая при введении разовой дозы; • Период полувыведения (T 1/2); • Площадь под ФК кривой (AUC)
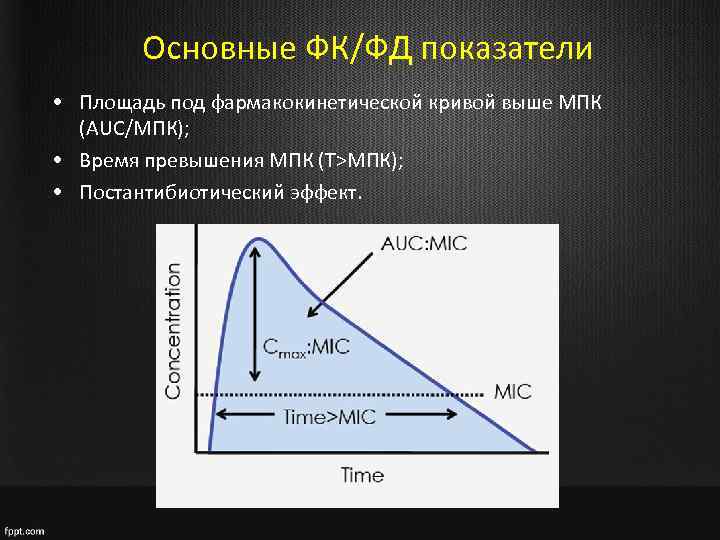
Основные ФК/ФД показатели • Площадь под фармакокинетической кривой выше МПК (AUC/МПК); • Время превышения МПК (T>МПК); • Постантибиотический эффект.

Концентрационно зависимые АБ • Активность зависит от максимальной концентрации и от площади под фармакокинетической кривой выше МПК (Cmax/МПК, AUC/МПК); • Выраженный постантибиотический эффект • Эффективное соотношение AUC/МПК составляет 25 -30 у пациентов без иммунодефицита и 100 -125 у пациентов с иммунодефицитом; • Эффективное Cmax/МПК = 10 -12; • Зная МПК можно рассчитать необходимую Cmax, а зная AUC – требуемое для эффективного лечения МПК • Однократное введение максимальной суточной дозы может повысить эффективность

Время-зависимые АБ • Активность зависит от времени, в течении которого Сmax превышает МПК (T>МПК); • Слабый постантибиотический эффект • Время превышения МПК должно составлять 40 -50% интервала дозирования (20 -30% у препаратов с ПАБЭ); • На основании справочных данных можно вычислить какая концентрация поддерживается 40% длительности интервала дозирования и сравнить с МПК
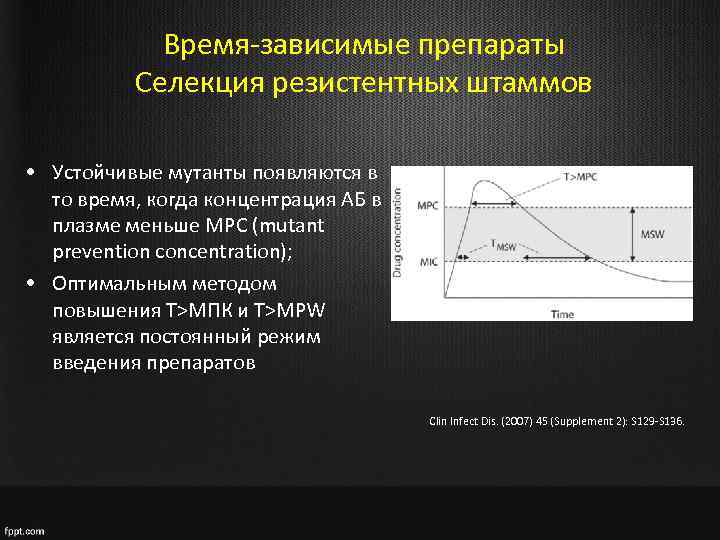
Время-зависимые препараты Селекция резистентных штаммов • Устойчивые мутанты появляются в то время, когда концентрация АБ в плазме меньше MPC (mutant prevention concentration); • Оптимальным методом повышения T>МПК и Т>MPW является постоянный режим введения препаратов Clin Infect Dis. (2007) 45 (Supplement 2): S 129 -S 136.

ФК/ФД группы антибиотиков Концентрационно- зависимые (AUC/МПК, Cmax/МПК) Время-зависимые (T>МПК) Аминогликозиды Бета-лактамы Фторхинолоны Макролиды Метронидазол Кетолиды Даптомицин Хлорамфеникол Колистин Рифампицин Тетрациклины Оксазолидиноны

Что происходит с микроорганизмами?

Как это было • 1941 г. – Альберт Александр – первый пациент, получивший пенициллин • 1942 г. – появление первого резистентного к пенициллину штамма S. aureus. • 1960 г. - введение в клиническую практику метициллина • 1964 г. – зарегистрирован первый случай MRSA • 1980 -е – MRSA становится основным нозокомиальным возбудителем в Европе и США • 1980 -е – БЛРС продуцирующие грамотрицательные бактерии • 1990 -е – зарегистрированы первые штаммы VRE • 2000 -е – зарегистрированы первые случаи VISA и VRSA • 2002 г. – впервые зарегистрированы резистентные к линезолиду стафилококки и энтерококки • 2014 г. – CRAB, MDR P. aeruginosa, CRKP.
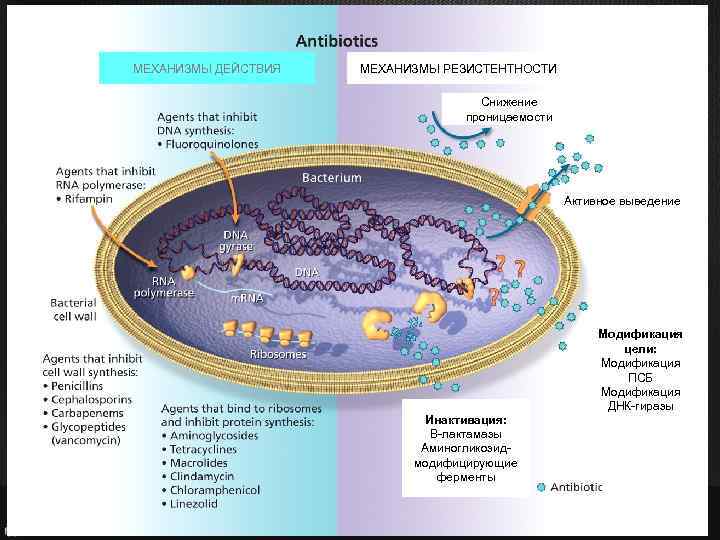
МЕХАНИЗМЫ ДЕЙСТВИЯ МЕХАНИЗМЫ РЕЗИСТЕНТНОСТИ Снижение проницаемости Активное выведение Инактивация: Β-лактамазы Аминогликозидмодифицирующие ферменты Модификация цели: Модификация ПСБ Модификация ДНК-гиразы

Генетические механизмы • • Мутации; Плазмиды; Транспозоны; Интегроны


Проблемы госпитальных инфекций

Почему госпитальные инфекции возникли? • Больные в тяжелом состоянии; • Большое количество инвазивных методик диагностики и лечения • Наиболее сильное давление антибиотиков

Сопутствующие проблемы • Замалчивание и укрывание случаев внутрибольничной инфекции • Неэффективный санитарно-противоэпидемический режим • Безграмотность медперсонала • Отсутствие внимания к проблеме на государственном уровне

Следствия • Специфический набор патогенов; • Высокое распространение устойчивости; • Неэффективность антибактериальной терапии
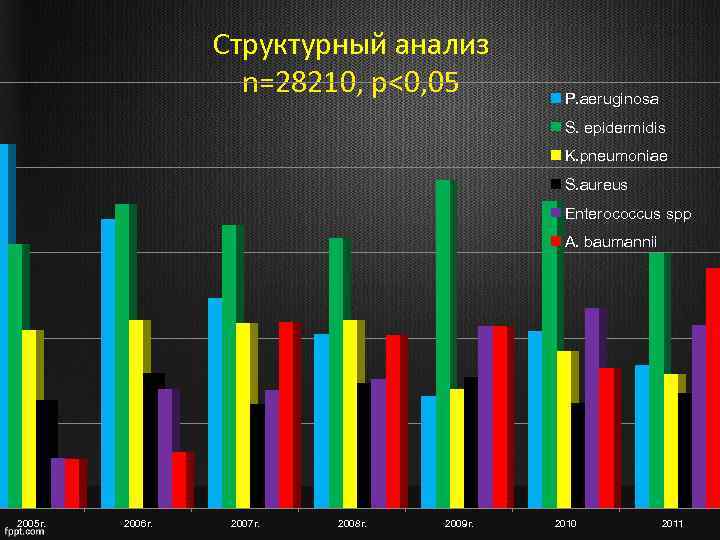
Структурный анализ n=28210, p<0, 05 P. aeruginosa S. epidermidis K. pneumoniae S. aureus Enterococcus spp A. baumannii 2005 г. 2006 г. 2007 г. 2008 г. 2009 г. 2010 2011
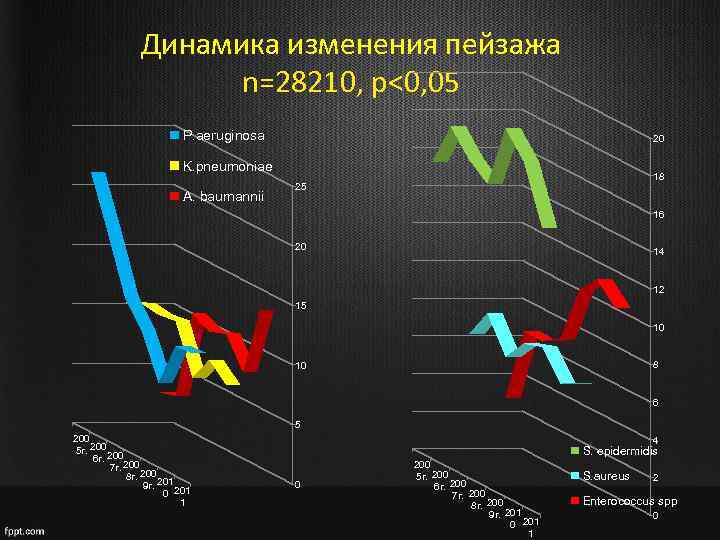
Динамика изменения пейзажа n=28210, p<0, 05 P. aeruginosa 20 K. pneumoniae A. baumannii 18 25 16 20 14 12 15 10 8 10 6 5 200 5 г. 200 6 г. 7 г. 200 8 г. 200 201 9 г. 0 201 1 4 S. epidermidis 0 200 5 г. 200 6 г. 200 7 г. 200 8 г. 200 9 г. 201 0 201 1 S. aureus 2 Enterococcus spp 0
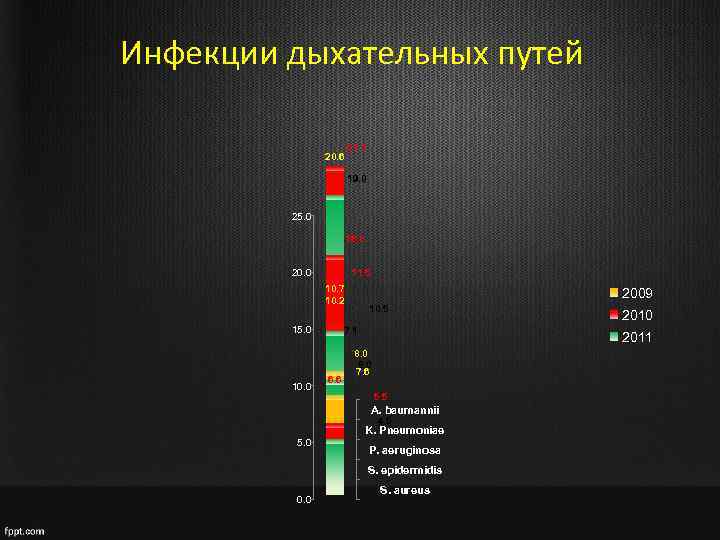
Инфекции дыхательных путей 20. 6 21. 1 19. 0 25. 0 16. 8 20. 0 11. 5 10. 7 10. 2 15. 0 10. 0 2009 10. 5 7. 1 6. 6 2011 8. 0 7. 6 5. 5 A. baumannii 4. 5 K. Pneumoniae 5. 0 P. aeruginosa S. epidermidis 0. 0 2010 S. aureus
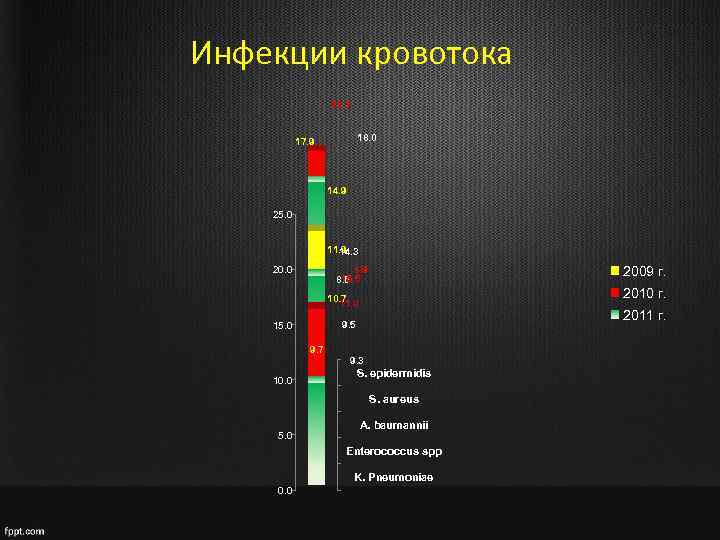
Инфекции кровотока 20. 3 18. 0 17. 9 14. 9 25. 0 11. 9 14. 3 20. 0 2009 г. 8. 9 15. 5 8. 6 2010 г. 10. 7 11. 0 15. 0 8. 2 9. 7 10. 0 2011 г. 9. 5 9. 3 S. epidermidis S. aureus 5. 0 A. baumannii Enterococcus spp K. Pneumoniae 0. 0
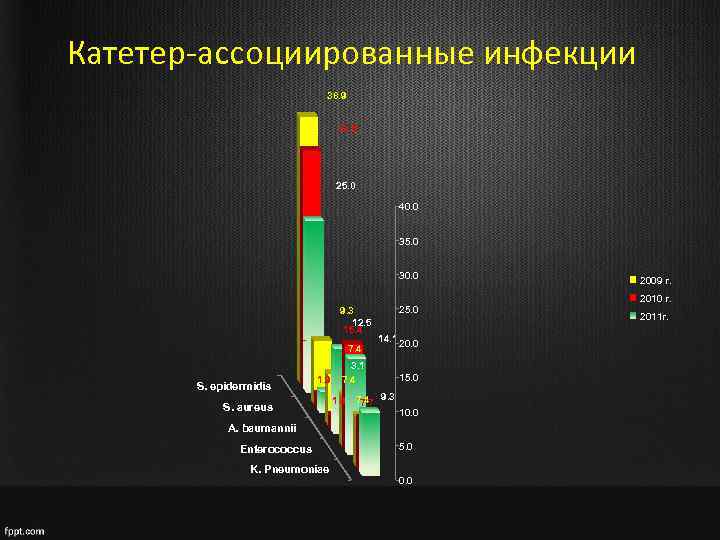
Катетер-ассоциированные инфекции 38. 9 34. 6 25. 0 40. 0 35. 0 30. 0 2009 г. 2010 г. 9. 3 12. 5 15. 4 25. 0 7. 4 S. epidermidis 1. 9 S. aureus 14. 1 20. 0 3. 1 7. 4 15. 0 1. 9 7. 4 9. 3 7. 7 10. 0 A. baumannii Enterococcus K. Pneumoniae 5. 0 0. 0 2011 г.
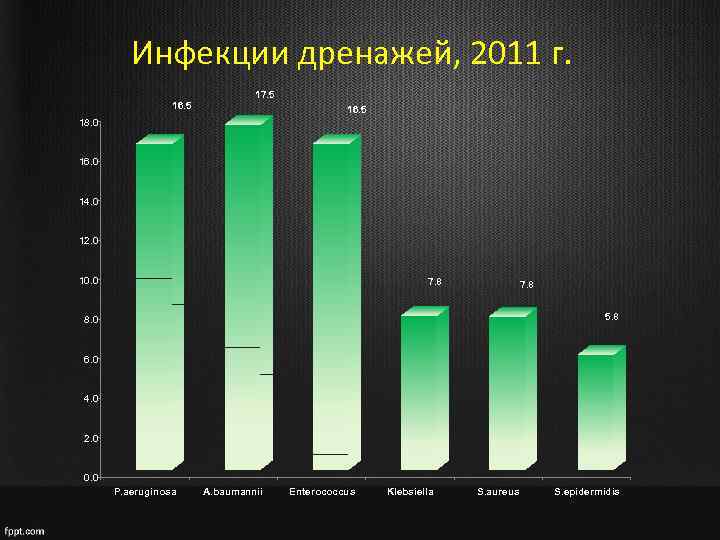
Инфекции дренажей, 2011 г. 16. 5 17. 5 16. 5 18. 0 16. 0 14. 0 12. 0 10. 0 7. 8 5. 8 8. 0 6. 0 4. 0 2. 0 0. 0 P. aeruginosa A. baumannii Enterococcus Klebsiella S. aureus S. epidermidis

Вывод Основные возбудители в ОИТР: • НГОБ (P. aeruginosa, A. baumannii); • Продуценты БЛРС (K. pneumoniae); • Грамположительные кокки (S. aureus, S. epidermidis, Enterococcus)
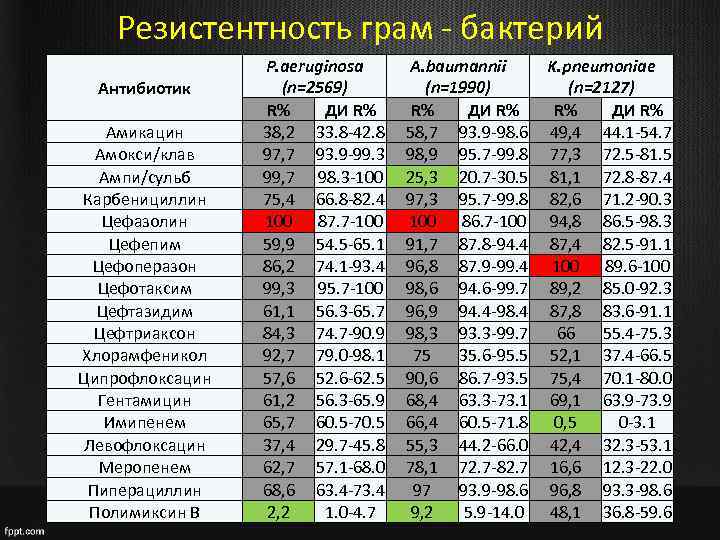
Резистентность грам - бактерий Антибиотик Амикацин Амокси/клав Ампи/сульб Карбенициллин Цефазолин Цефепим Цефоперазон Цефотаксим Цефтазидим Цефтриаксон Хлорамфеникол Ципрофлоксацин Гентамицин Имипенем Левофлоксацин Меропенем Пиперациллин Полимиксин В P. aeruginosa (n=2569) R% ДИ R% 38, 2 33. 8 -42. 8 97, 7 93. 9 -99. 3 99, 7 98. 3 -100 75, 4 66. 8 -82. 4 100 87. 7 -100 59, 9 54. 5 -65. 1 86, 2 74. 1 -93. 4 99, 3 95. 7 -100 61, 1 56. 3 -65. 7 84, 3 74. 7 -90. 9 92, 7 79. 0 -98. 1 57, 6 52. 6 -62. 5 61, 2 56. 3 -65. 9 65, 7 60. 5 -70. 5 37, 4 29. 7 -45. 8 62, 7 57. 1 -68. 0 68, 6 63. 4 -73. 4 2, 2 1. 0 -4. 7 A. baumannii (n=1990) R% ДИ R% 58, 7 93. 9 -98. 6 98, 9 95. 7 -99. 8 25, 3 20. 7 -30. 5 97, 3 95. 7 -99. 8 100 86. 7 -100 91, 7 87. 8 -94. 4 96, 8 87. 9 -99. 4 98, 6 94. 6 -99. 7 96, 9 94. 4 -98. 4 98, 3 93. 3 -99. 7 75 35. 6 -95. 5 90, 6 86. 7 -93. 5 68, 4 63. 3 -73. 1 66, 4 60. 5 -71. 8 55, 3 44. 2 -66. 0 78, 1 72. 7 -82. 7 97 93. 9 -98. 6 9, 2 5. 9 -14. 0 K. pneumoniae (n=2127) R% ДИ R% 49, 4 44. 1 -54. 7 77, 3 72. 5 -81. 5 81, 1 72. 8 -87. 4 82, 6 71. 2 -90. 3 94, 8 86. 5 -98. 3 87, 4 82. 5 -91. 1 100 89. 6 -100 89, 2 85. 0 -92. 3 87, 8 83. 6 -91. 1 66 55. 4 -75. 3 52, 1 37. 4 -66. 5 75, 4 70. 1 -80. 0 69, 1 63. 9 -73. 9 0, 5 0 -3. 1 42, 4 32. 3 -53. 1 16, 6 12. 3 -22. 0 96, 8 93. 3 -98. 6 48, 1 36. 8 -59. 6
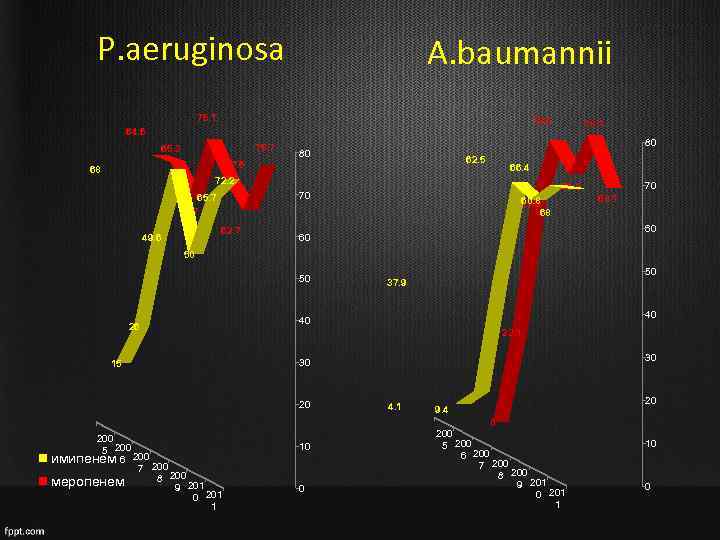
P. aeruginosa A. baumannii 75. 1 72. 4 64. 6 75. 7 65. 3 67. 6 68 80 80 62. 5 66. 4 72. 2 62. 7 49. 6 70 66. 8 70 65. 7 58. 7 78. 1 60. 8 55. 5 68 68. 1 60 60 50 50 26 15 40 40 23. 1 30 30 20 200 5 200 имипенем 6 200 7 8 200 меропенем 9 201 0 201 1 50 37. 9 10 0 4. 1 9. 4 0 200 5 200 6 200 7 200 8 200 9 201 0 201 1 20 10 0
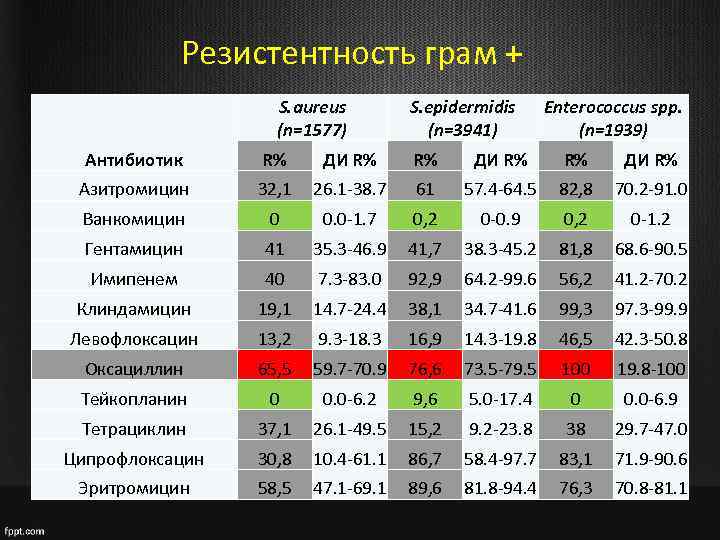
Резистентность грам + S. aureus (n=1577) S. epidermidis (n=3941) Enterococcus spp. (n=1939) Антибиотик R% ДИ R% Азитромицин 32, 1 26. 1 -38. 7 61 57. 4 -64. 5 82, 8 70. 2 -91. 0 Ванкомицин 0 0. 0 -1. 7 0, 2 0 -0. 9 0, 2 0 -1. 2 Гентамицин 41 35. 3 -46. 9 41, 7 38. 3 -45. 2 81, 8 68. 6 -90. 5 Имипенем 40 7. 3 -83. 0 92, 9 64. 2 -99. 6 56, 2 41. 2 -70. 2 Клиндамицин 19, 1 14. 7 -24. 4 38, 1 34. 7 -41. 6 99, 3 97. 3 -99. 9 Левофлоксацин 13, 2 9. 3 -18. 3 16, 9 14. 3 -19. 8 46, 5 42. 3 -50. 8 Оксациллин 65, 5 59. 7 -70. 9 76, 6 73. 5 -79. 5 100 19. 8 -100 Тейкопланин 0 0. 0 -6. 2 9, 6 5. 0 -17. 4 0 0. 0 -6. 9 Тетрациклин 37, 1 26. 1 -49. 5 15, 2 9. 2 -23. 8 38 29. 7 -47. 0 Ципрофлоксацин 30, 8 10. 4 -61. 1 86, 7 58. 4 -97. 7 83, 1 71. 9 -90. 6 Эритромицин 58, 5 47. 1 -69. 1 89, 6 81. 8 -94. 4 76, 3 70. 8 -81. 1

Выбор антибиотика для эмпирической терапии • НГОБ: A. baumanii – ампициллин/сульбактам, цефоперазон/сульбактам, полимиксин В, тигкциклин. P. aeruginosa – колистин • Продуценты БЛРС: K. pneumoniae – карбапенемы • Грам + полирезистентная флора: ванкомицин, линезолид, тигециклин

Цефоперазон/сульбактам или ампициллин/сульбактам Содержание cульбактама Чувствительность A. baumanii Действующее на Acinetobacter в-во Проникновение в очаг Токсичность Цеф/сульб 1: 1 Амп/сульб 1: 0, 5 97, 8% * 70, 8% Сульбактам Хорошее Низкая * Исследование РОСНЕТ, 2003 г.

Ампициллин/сульбактам • Высокие дозы ампициллина/сульбактама (9 г. в/в каждые 8 часов) также эффективны в отношении Acinetobacter, как полимиксин В (Alex P. Betrosian-Efficacy and safety of high-dose ampicillin/sulbactam vs. colistin as monotherapy for the treatment of multidrug resistant Acinetobacter baumannii ventilator-associated pneumonia. Journal of Infection (2008) 56, 432 e 436) • Ампициллин/сульбактам эффективен в отношении устойчивых к карбапенемам штаммов Acinetobacter (Levin AS, Levy CE, Manrique AE, Medeiros EA, Costa SF. Severe nosocomial infections with imipenem-resistant Acinetobacter baumannii treated with ampicillin/sulbactam. Int J Antimicrob Agents 2003; 21: 58– 62. )
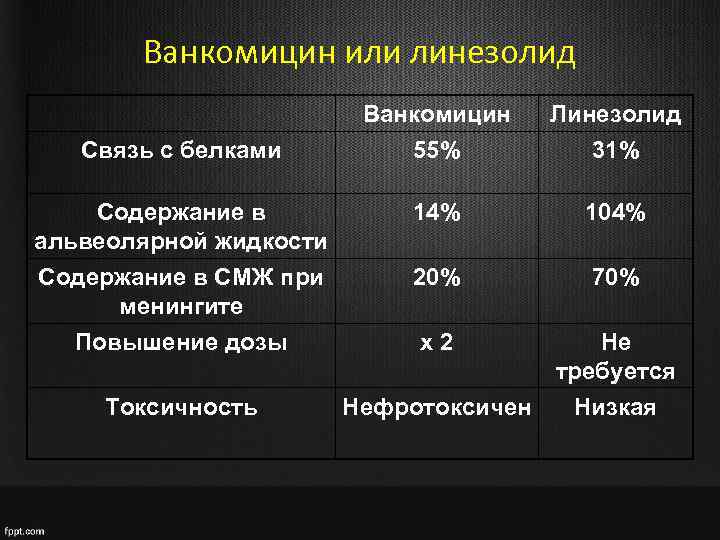
Ванкомицин или линезолид Ванкомицин Линезолид Связь с белками 55% 31% Содержание в альвеолярной жидкости 14% 104% Содержание в СМЖ при менингите 20% 70% Повышение дозы х2 Не требуется Токсичность Нефротоксичен Низкая

Комбинированная терапия для Carbapenem Resistant A. baumannii
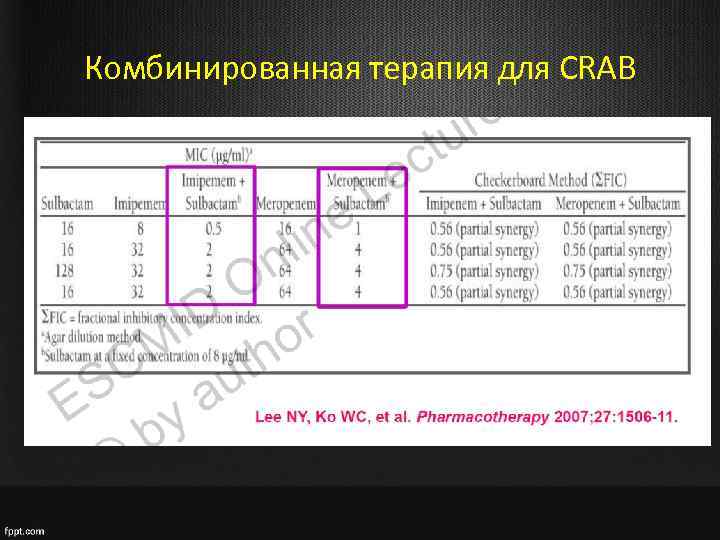
Комбинированная терапия для CRAB
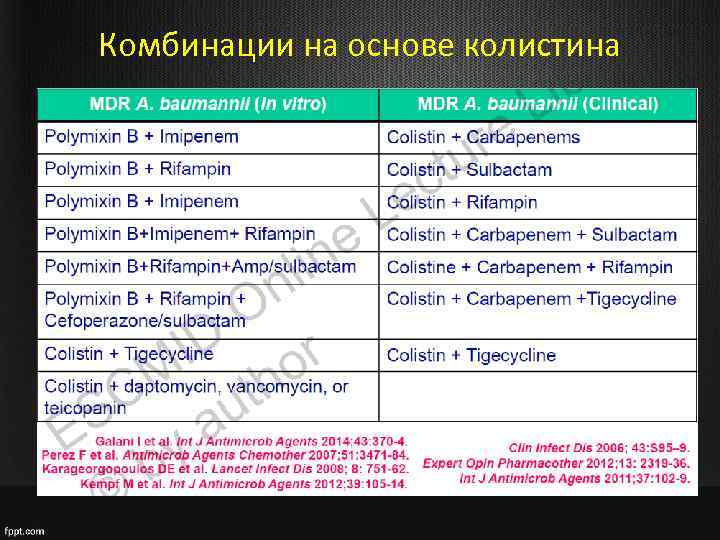
Комбинации на основе колистина

Карбапенем-резистентная K. pneumoniae

MDR P. aeruginosa • Хороший результат лечения достигался оптимизацией фармакологического профиля колистина; • При MIC больше 1 целесообразно использовать комбинацию с карбапенемом;

• Принятые дозы колистина недостаточны, чтобы достичь эрадикации микроорганизмов.

9 млн. ед. загрузочная доза, затем по 4, 5 млн. ед через 12 часов. 100% вылечиваемость ВАП

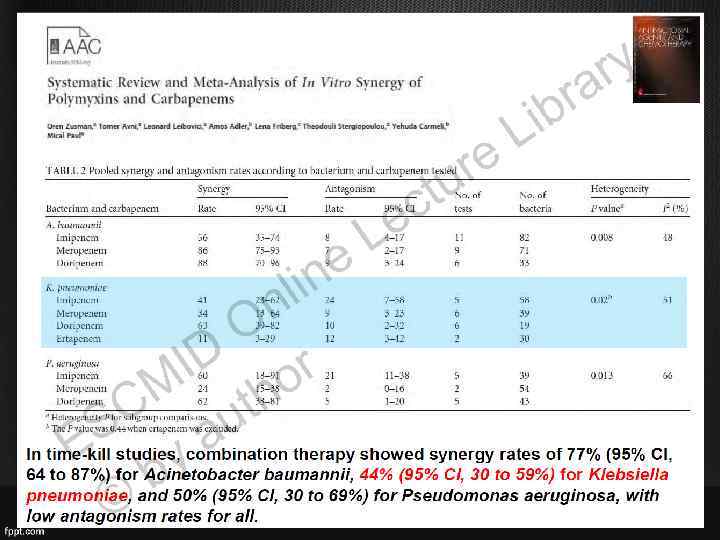
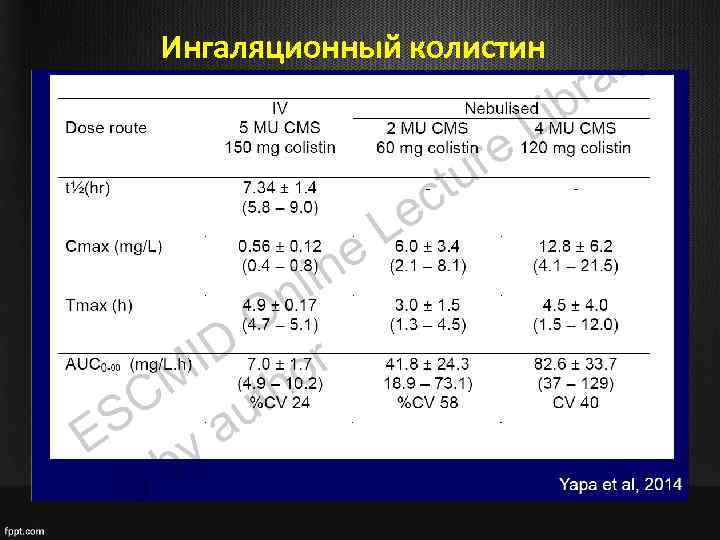
Ингаляционный колистин

Стратегия и тактика антибактериальной терапии в ОИТР НЕЛЬЗЯ ПРОСТО ТАК ВЗЯТЬ И НАЗНАЧИТЬ АНТИБИОТИКИ

Показания к АБТ Наличие клинического диагноза инфекции • Клинические признаки системного воспаления: • гипертермия >38 о. С или <36 о. С; • лейкоцитоз >12 х109 или <4 х109; • подъем СРБ > 20 мг/л в сутки; • Установленный очаг инфекции • Лабораторные признаки (С-реактивный белок, прокальцитонин) • Инструментальные признаки (рентгенологические, КТ и т. д. )

Частный случай - пневмония • Новые или прогрессирующие инфильтраты на рентгенограмме лёгких; • 2 из 3 признаков системного воспаления: гипертермия >38 о. С или <36 о. С; лейкоцитоз >12 х109 или <4 х109; подъем ЦРБ > 20 мг/л в сутки • 1 из локальных признаков воспаления: гнойная мокрота или снижение Pa. O 2/Fi. O 2 на 10% за сутки American Thoracic Society: Guidelines for the management of adults with hospital-acquired, ventilator-associated, and health-care associated pneumonia. Am J Respir Crit Care Med 2005

Шкала CPIS (Clinical Pulmonary Infection Scale) • Создана для облегчения диагностики ВАП и снижения частоты необоснованного назначения АБП • Коррелирует с развитием ВАП при 5 и более баллах • Оптимально использование ее в связке с СРБ и прокальцитонином

Шкала CPIS (Clinical Pulmonary Infection Scale)

Прокальцитонин • Не повышается при вирусной инфекции • Существенно растет при бактеремии • При использовании вместе со CPIS и СРБ (более 200 мг/л) чувствительность и специфичность достигают 100% • Используется для определения срока прекращения АБТ • Cut-off для госпитальной пневмонии составляет 2, 9 нг/мл


Не чеши, где не чешется • АБТ не назначается при отсутствии признаков инфекции • АБТ не назначаются при неинфекционном воспалении (травма, операция и т. д. ) • АБТ не назначается при колонизации (посев < КОЕ× 105) • АБТ не назначается с профилактической целью, поскольку не предотвращает развития инфекций

Почему пациенту после операции не назначены антибиоти…. Никаких антибиотиков без признаков инфекции!

Protective effect of antibiotic prophylaxis against early-onset nosocomial pneumonia in comatose patients J Navellou, C Manzon, M Puyraveau, D Perez, E Laurent, C Patry and G Capellier CHU Jean Minjoz, Besancon, France Critical Care 2007, 11(Suppl 2): P 84 doi: 10. 1186/cc 5244 In our study, antibioprophylaxy did not show a decrease in the incidence of nosocomial pneumonia in medical comatose patients with Glasgow Coma Score < 8 under mechanical ventilation. On the other hand, antibiotics induce a later onset of colonisation and lung infections. Despite a prevention of early-onset nosocomial pneumonia, our data do not support the use of regular prophylactic antibiotics. Профилактическая антибиотикотерапия не показала снижения количества нозокомиальных пневмоний у пациентов на ИВЛ в коме менее 8 баллов по шкале Глазго, таким образом, наши данные не поддерживают необходимость рутинного профилактического использования антибиотиков.

Risk factors for adult nosocomial meningitis after craniotomy: role of antibiotic prophylaxis. Neurosurgery. 2008 Feb; 62 Suppl 2: 532 -9 Korinek AM, Baugnon T, Golmard JL, van Effenterre R, Coriat P, Puybasset L. Perioperative antibiotic prophylaxis, although clearly effective for the prevention of incision infections, does not prevent meningitis and tends to select prophylaxis resistant microorganisms. Периоперационная антибиотикопрофилактика, эффективная для предотвращения раневой инфекции, не предотвращает развития менингитов после краниотомии и способствует селекции полирезистентных штаммов.

A role for prophylactic antibiotics in necrotizing pancreatitis? Why we may never know the answer. . . Critical Care 2008, 12: 195 doi: 10. 1186/cc 7122 Jan J De Waele Conclusion: Until we are able to demonstrate an advantage of antibiotic prophylaxis in a high-risk human population, the absence of proven benefit and potential side effects of this strategy should be acknowledged and the use of antibiotics should be limited to the treatment of documented infection. До тех пор, пока у нас не будет данных, чтобы продемонстрировать преимущество антибиотикопрофилактики , отсутствие доказанного преимущества и возможность развития побочных эффектов должно сдерживать профилактическое применение антибиотиков, и ограничивать их использование только доказанными случаями инфекции.

The influence of empiric antimicrobial therapy on acquired pulmonary infection in patients with a chest injury on ICU I Chytra, E Kasal, R Pradl, J Voborníková and R Sviták Critical Care 2000, 4(Suppl 1): P 98 doi: 10. 1186/cc 818 Empiric antimicrobial therapy in patients with the chest injury on ICU may increase the rate of pulmonary infections, prolong duration of mechanical ventilation and extend the time of ICU stay. There is a need for controlled studies to define the role of antibiotics in empiric therapy in trauma patients. Эмпирическая антимикробная терапия у пациентов ОИТР может повышать частоту легочных инфекций , пролонгировать длительность ИВЛ и продлевать пребывание а ОИТР
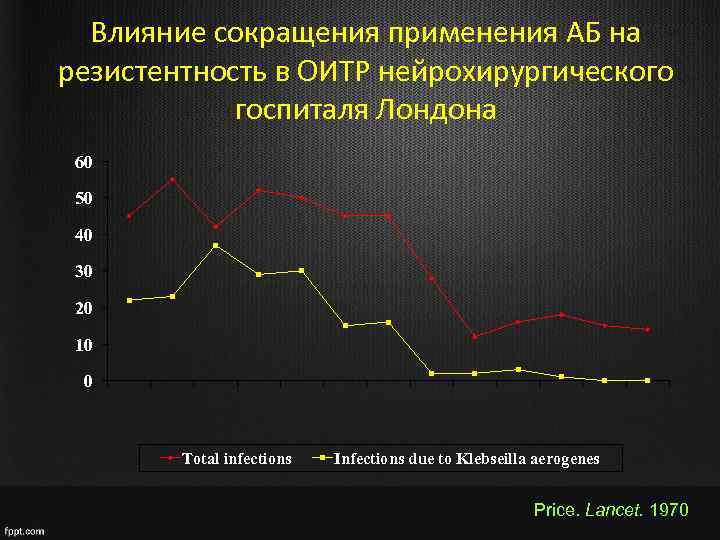
Влияние сокращения применения АБ на резистентность в ОИТР нейрохирургического госпиталя Лондона 60 50 40 30 20 10 0 Total infections Infections due to Klebseilla aerogenes Price. Lancet. 1970
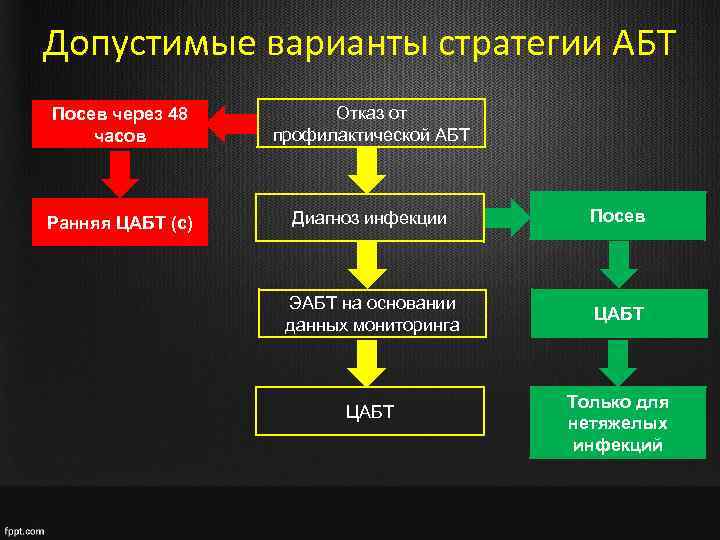
Допустимые варианты стратегии АБТ Посев через 48 часов Отказ от профилактической АБТ Ранняя ЦАБТ (с) Диагноз инфекции Посев ЭАБТ на основании данных мониторинга ЦАБТ Только для нетяжелых инфекций

Результаты необоснованной ЭАБТ • Суперинфекция • Увеличение длительности ИВЛ • Увеличение длительности пребывания в ОИТР • Селекция резистентных штаммов • Колонизация полирезистентными грам штаммами (БЛРС-продуценты, НГОБ), неуправляемая инфекция, повышение летальности
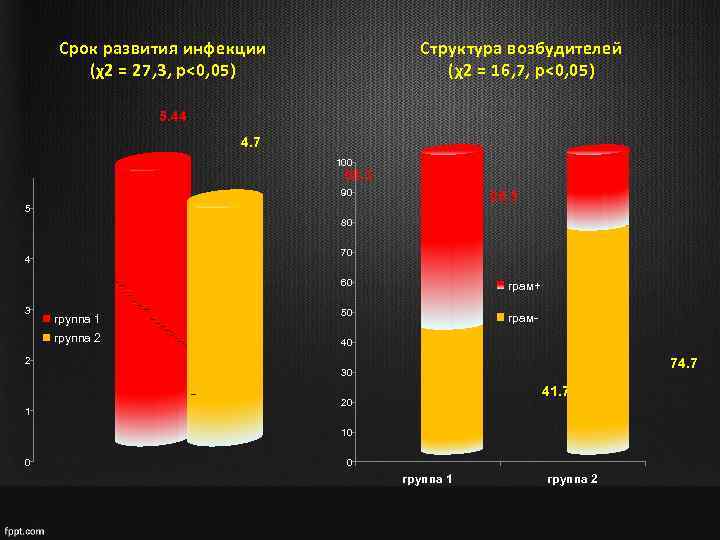
Срок развития инфекции (χ2 = 27, 3, p<0, 05) Структура возбудителей (χ2 = 16, 7, p<0, 05) 5. 44 4. 7 100 58. 3 90 25. 3 5 80 70 4 60 3 группа 1 группа 2 грам+ 50 грам- 40 2 74. 7 30 1 41. 7 20 10 0 0 группа 1 группа 2
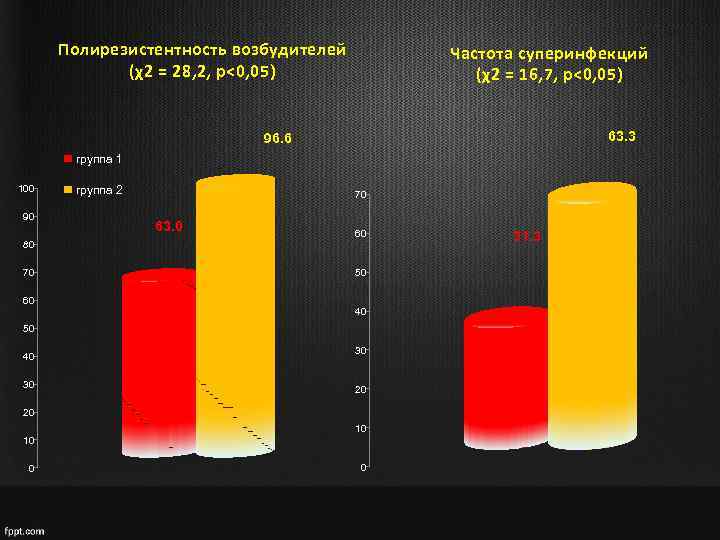
Полирезистентность возбудителей (χ2 = 28, 2, p<0, 05) Частота суперинфекций (χ2 = 16, 7, p<0, 05) 63. 3 96. 6 группа 1 100 90 80 70 60 группа 2 70 63. 0 60 50 40 30 30 20 20 10 10 0 0 31. 3

Что по поводу длительности АБТ? • Короткие курсы антибиотиков так же эффективны, как и длительные; • При сокращении длительности АБТ снижается риск суперинфекции, формирования резистентности • Для сокращения курса АБТ используются маркеры: прокальцитонин, СРБ
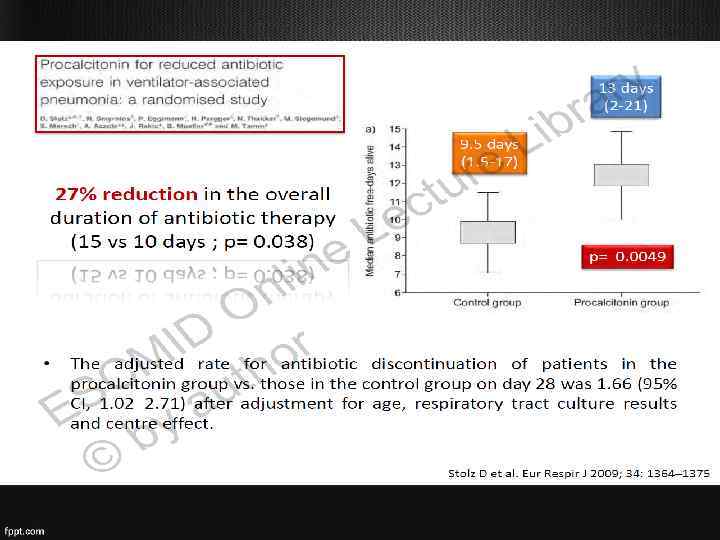
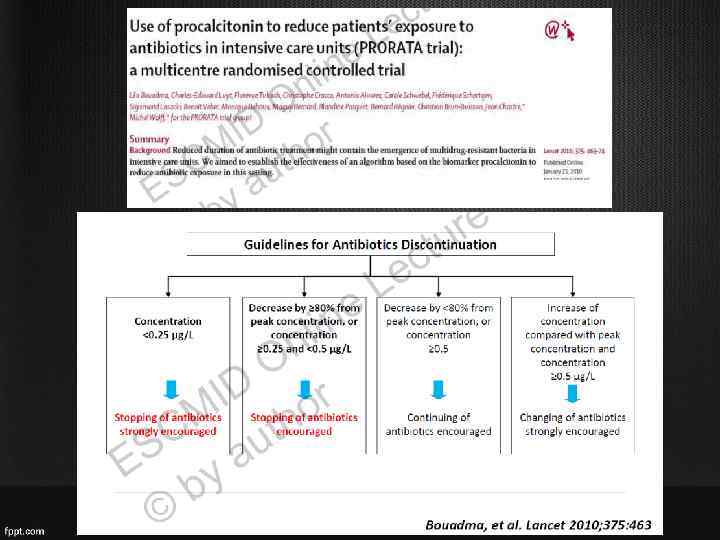
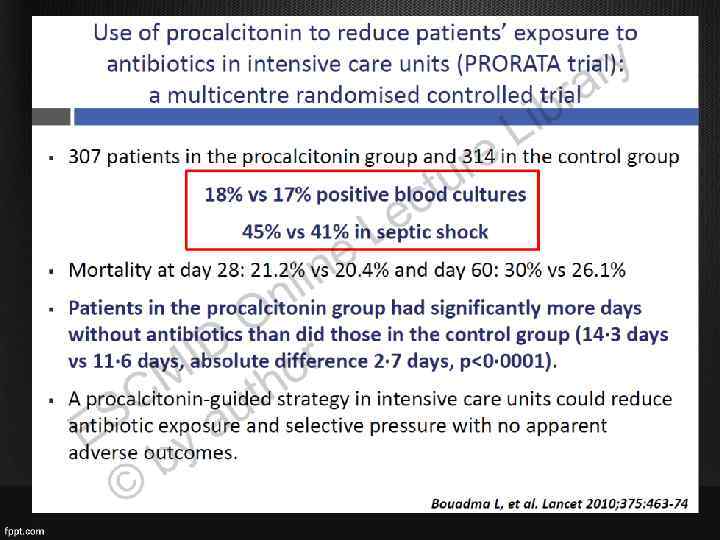

Священные коровы антибиотикотерапии

Миф 1. Курс антибиотиков должен длиться 7 -10 дней • Длительность ЭАБТ составляет время часа до получения результатов посева и антибиотикограммы, после чего проводится ее коррекция. • Короткий курс АБТ (5 сут) так же эффективен, как и стандартный, кроме того он препятствует селекции резистентных штаммов и суперинфекции 1. Политика применения антибиотиков в хирургии, МАКМАХ, 2003) 2. Havey et al. Critical Care 2011, 15: R 267 (http: //ccforum. com/content/15/6/R 267)

Миф 2. Профилактическая АБТ предотвращает развитие инфекций • Инфекционные осложнения развиваются как при отсутствии профилактической терапии, так и с ней. Отличие в том, что в последнем случае они вызваны грамотрицательными полирезистентными микроорганизмами. • Антибиотики не имеют профилактического действия

Миф 3. Антибиотики должны назначаться всегда, если есть теоретические ворота инфекции • Антибиотики не имеют профилактического действия. См. миф 2 • Антибиотики назначаются при документированной инфекции, а не при наличии ворот, тем более теоретических

Миф 4. Антибиотики бывают «сильные» и «слабые» . После «сильного» нельзя назначать «слабый» • Антибиотики бывают соответствующими и не соответствующими чувствительности. • Мы можем назначать АБ в любой последовательности, если микроорганизм к ним чувствителен и это подтверждено антибиотикограммой

Миф 5. Антибиотики не могут повторяться. (Этот пациент получал уже все существующие антибиотики, я не знаю что назначить) • Не важно сколько раз пациент получал курс одного и того же антибиотика, если инфекция персистирует и чувствительность сохранена. Лучше задуматься что приводит к персистированию инфекции на фоне эффективной АБТ: пролонгированное поступление патогена, недостаточное поступление АБ в очаг инфекции, несанированные ворота инфекции.

Миф 6. Антибиотики назначаются всегда при высевании флоры • Антибиотики назначаются при инфекции, что подразумевает наличие клинических, лабораторных и инструментальных признаков инфекции. • Простое выделение МО из очага инфекции называется колонизацией и не требует лечения, поскольку все микроорганизмы, с которыми мы имеем дело - оппортунистические

Миф 7. Антибиотики купируют воспалительную реакцию • Только в случае, если она вызвана инфекционным процессом. • АБ не имеют собственного противовоспалительного действия

Миф 8. Гипертермия и лейкоцитоз являются верными признаками инфекции и показаниями к АБТ • Гипертермия и лейкоцитоз являются признаками ВОСПАЛИТЕЛЬНОЙ РЕАКЦИИ, которая является стандартным патологическим процессом. При отсутствии очага, его причиной могут быть: травма, операция, повреждение диэнцефальной зоны ГМ, инфаркт миокарда, легкого, мозга, отравления и др. • Системное воспаление без очага инфекции не требует АБТ

Миф 9. Цефалоспорины являются хорошей стартовой антибиотикотерапией при неизвестных воротах инфекции • Отсутствие ворот инфекции подразумевает либо неинфекционное воспаление либо недостаточное обследование т. е. отсутствие диагноза инфекции, следовательно АБТ не показана. • Стартовая терапия назначается исходя из возбудителей и их чувствительности на основании мониторинга в конкретном отделении или крупных мониторных исследований • Цефалоспорины, особенно 3 -е поколение, - самый мощный индуктор резистентности по лактамазному и эффлюксному пути. Их исключение из клинической практики чрезвычайно желательно.

• • • Колонизация MDR бактериями Развитие резистентности Цефалоспорины III и IV поколений Хинолоны Карбапенемы Аминогликозиды

Миф 10. Антибиотикопрофилактика, проводимая перед операцией направлена на недопущение развития госпитальных инфекций • Антибиотикопрофилактика, проводимая перед операцией направлена на недопущение развития раневой инфекции, вызванной кожной (внебольничной) флорой. • Профилактикой развития госпитальных инфекций является мероприятия по туалету пациента (обработка раны, дренажей, перевязки), стерилизация и мытье рук медперсоналом и использование одноразовых расходных материалов
антибиотики.pptx