А-биот. Испр. 14.ppt
- Количество слайдов: 68

Клиническая фармакология антибактериальных средств Кафедра клинической фармакологии доцент Черкасова С. П.

Эффективность антибиотика • Определяется минимальной концентрацией, способной подавлять патогенные микроорганизмы, входящие в спектр его активности (МПК) • МПК-50: подавляет рост 50% штаммов • МПК-90: подавляет рост 90% штаммов Эффект инокуляции: снижение активности антибиотика при высокой концентрации бактерий (чувство локтя). Биопленки.

Критерии оценки антибиотика • • терапевтическая эффективность безопасность экономическая эффективность предотвращение селекции штаммов патогенов, устойчивых к антибиотикам резерва • удобство для пациента Управление антибиотикотерапией

Классификация антимикробных средств • С преимущ. действием на Гр+ флору • С преимущ. действием на Гр- флору • Широкого спектра действия Внутри каждой группы – препараты с преимущ. влиянием на аэробов или анаэробов

Связь эффекта антибиотика с временем и концентрацией • «Время / зависимые» антибиотики (В-лактамы, макролиды): уровень в крови выше МПК-90 – не менее 16 часов в сутки • «Концентрация/зависимые» антибиотики (аминогликозиды, фторхинолоны, азалиды): эффект пропорционален высоте концентрации (пусть даже кратковременной)

Стрептококки • БГСА - фарингит, скарлатина, кожные инфекции, ревматизм, эндокардит, гломерулонефрит • Пневмококк – внебольничная пневмония • Альфа-гемолитический (зеленящий) – полость рта • Энтерококки – нозокомиальная инфекция (цефалоспорины неэффективны!). Катетеры

Грампозитивные анаэробы • Клостридии – 80 видов (газовая гангрена, токсикоинфекции, столбняк, ботулизм) • Cl. difficile – псевдомембранозный колит • Актиномицеты: лицо, грудная, брюшная полости • Пептококки, пептострептококки – полость рта

Стафилококки • Патогены: S. aureus, epidermitis, saprophyticus • Обусловливают инфекцию любой области (с-м Лайелла) • Обычная инфекция –эндогенная или нозокомиальная • S. aureus- возможна коагуалазная активность • S. epidermitis: протезы, дренажи, катетеры • S. saprophiticus- гениталии, уретра

Антибиотики с преимущественным влиянием на Гр+ флору • • «Классические» пенициллины Макролиды ЦС- I Линкозамиды Гликопептиды Оксазолидиноны Рифамицины Препараты разных групп

Основные мишени В-лактамов ПСБ: транспептидазы, карбоксипептидазы ПСБ-1: общий рост клетки ПСБ-2: форма клетки ПСБ-3: образование перегородки (деление)

Бензилпенициллин • Бактерициден • Активность против стрептококков (энтерококки – слабо), трепонем, анаэробов • Препарат выбора при тонзиллитах (БГСА), рожистое воспаление • Неактивен против стафилококков ! • Аллергогенен • Парентеральное применение – стационар

Основные возбудители внебольничной пневмонии В половине случаев возбудитель установить не удаётся. В случае идентификации: • Пневмококк - 30 -50% • Гемофильная палочка (ХОБЛ) - 5 -20% • Микоплазма, хламидии - молодые больные -20 -30%, старший возраст - 5% • S. аureus - 5%

Помощь при анафилактическом шоке на БП • Эпинефрин (адреналин) – по 0, 2 мл в 2 -3 участка • ГКС быстрого действия • Плазмозаменители • Антигистаминные 1 поколения Если в анамнезе –анафилактический шок на пенициллин, другие В-лактамы тоже вводить нельзя

Оксациллин • Мишень – стафилококки (ОSSA), при стрептококковых инфекциях нецелесообразен • При ОRSA – бесполезен (как и все остальные В-лактамы) • Антибиотик стационара • Вводить парентерально в больших дозах • Контроль функции печени

Микоплазмы, уреаплазмы, хламидии • • Микоплазмы – 12 видов M. pneumoniae – 20% всех пневмоний, ЦНС M. hominis – урогенитальные инфекции Уреаплазма – негонококковые уретриты (50% у мужчин) Хламидии – только внутриклеточно! Орнитоз C. pneumoniae – пневмонии. Астма? А/склероз? C. trachomatis – трахома, уретриты Все – прокариоты. В-лактамы не работают, нет пептидогликана

Классификация макролидных антибиотиков по химической структуре 14 -членные 15 -членные 16 -членные Природные (азалиды) Природные Полусинтетические эритромицин олеандомицин азитромицин Полусинтетические рокситромицин кларитромицин диритромицин флуритромицин мидекамицин джосамицин спирамицин Полусинтетические мидекамицина ацетат (миокамицин) рокитамицин

Макролиды в комбинированной АБТ ИДП • Внебольничная пневмония (госпитализация): ЦС 2 -3 + МЛ на 2 -5 дней < пребывание в стационаре (J. Trowbridge et al. , 2002) • В сравнении с монотерапией ЦС – при ВП летальность < в 1, 5 раза (P. Gleason et al. , 1999) • Макролиды + цефтриаксон при ВП: на 30 -60% ниже риск летального исхода, на 0, 6 -1, 5 дня – время пребывания в стационаре, на 1800 -3400$ - прямые расходы (R. Brown et al. , 2003)

Бактерицидный и бактериостатический эффекты макролидов Обычно - бактериостатики: большой разрыв между задерживающей рост и подавляющей концентрацией Бактерицидны в отношении: БГСА, пневмококка, возбудителей коклюша и дифтерии Антибиотики «среднетяжелых» инфекций

Дополнительные эффекты макролидов • Противовоспалительный – – Супрессия цитокинов Стимуляция апоптоза Снижение бронхиальной секреции (Cl- каналы) Блок активности NF-каппа фактора • Модификация факторов вирулентности возбудителей, препятств. образованию биопленок • Захват нейтрофилами • Постантибиотический • Суб-МПК • Низкодозовая длительная терапия диффузного панбронхиолита

Внутриклеточное накопление антибиотиков Соотношение внутри/внеклеточной концентрации: МАКРОЛИДЫ > 10 ТЕТРАЦИКЛИНЫ, АМИНОГЛИКОЗИДЫ, ФТОРХИНОЛОНЫ 1 -10 -ЛАКТАМЫ, МЕТРОНИДАЗОЛ <1

Преимущества джозамицина (вильпрафен) • Исключительно хорошая переносимость • Разрешен к применению при беременности и лактации • 16 -ти членные макролиды сохраняют активность в отношении ряда возбудителей, устойчивых к 14 - и 15 -ти членным препаратам • Пища практически не снижает биодоступность • Не влияет на моторику кишечника • Не влияет на метаболизм других препаратов в печени

Резистентность к макролидам • Активное выведение (М-фенотип) – синтез транспортного белка: низкий уровень резистентности • Метилирование аденина в рибосомах: (MLS – фенотип) – высокий уровень резистентности • Точечные мутации – непредсказуемая индивидуальная резистентность к отдельным антибиотикам Диспропорция между растущей резистентностью и сохраненной клинической эффективностью

Принципиальные отличия азалидов (азитромицин) от других макролидов • «Концентрационно-зависимая» эффективность • Более активное поступление в ткани • Высокая активность против H. Influenzae • Лучше всасывается • Длительно действует • Короткий курс лечения

Азитромицин и муковисцидоз • Длительное введение низких доз: – cнижает вирулентность P. aeruginosa Reinert P, 1995 – несколько повышает ОФВ 1 Carr RR, Nahata MC. 2004 – cнижает число обострений Saiman L et al. , 2003 – улучшает качество жизни и < уровень СРП Wolter J et al. , 2002 Требуются дальнейшие исследования

Линкосамиды (линко-, клиндамицин) • • Антианаэробный эффект Хорошо проникают в костную ткань Действуют на ОSSA, стрептококков Более токсичны, чем В-лактамы и макролиды • Часто – псевдомембранозный колит • MLS-резистентность

Гликопептиды (ванкомицин, тейкопланин) • Основной объект - метициллинрезистентный S. aureus (MRSA) - «жизнеспасающий эффект» • Влияние на конечные этапы синтеза пептидогликана • Режим дозирования: 1 г / 500 мл через 12 часов в/в медленно! в течение не менее 1 часа • Желателен контроль концентрации препаратов в крови • Аллергогенность, ото- и нефротоксичность; не сочетать с ото- и нефротоксинами • У беременных, детей до 3 лет – по жизненным показаниям

Ванкомицин – преимущества и ограничения • Большой опыт применения • Низкий уровень развития резистентности (связана с модификацией дипептида клеточной стенки) • Относительно недорогой препарат • Бактериостатический эффект • Аллергогенность, нефротоксичность (особенно в сочетании с аминогликозидами) – ИЭ и почки • Только парентеральный путь • Низкое проникновение в вегетации (эндокардит) (Perry J. et al, 1999) • Нарастание числа VRE (экспрессия оперона Van. D) (Lefort A. et al. , 2003)
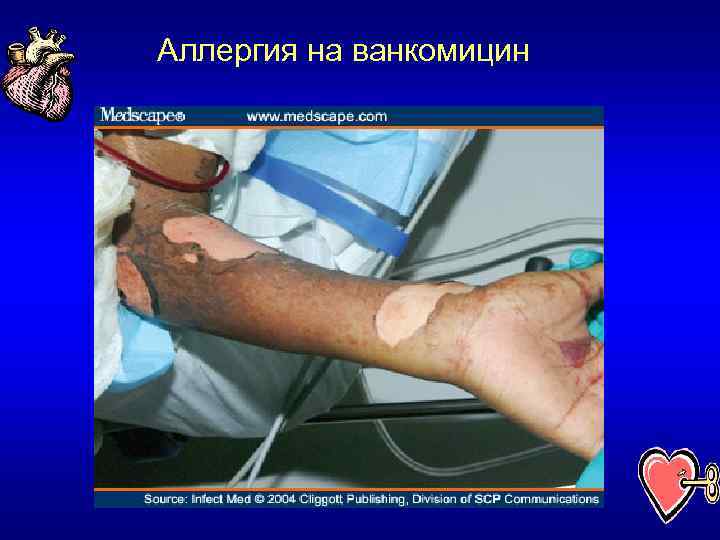
Аллергия на ванкомицин

Рифампицин • Микобактерии (туберкулез, лепра) • Устойчивые стафилококки (ORSA) • Хламидии, микоплазмы, анаэробы • Индуктор микросомальных ферментов

Препараты разных групп • Оксазолидиноны (линезолид) • Стрептограмины (синерцид) • Липопептиды (даптомицин)

Линезолид (зивокс) – преимущества и ограничения • Представитель нового класса (оксазолидиноны) • Оригинальный механизм действия (препятствует образованию комплекса РНК-рибосома) • Эффективен в отношении ампициллин- и ванкомицинрезистентных энтерококков • Простая схема (0, 6 х2), полное всасывание из ЖКТ • Не нужна коррекция при любой степени ПН, метаболизм – без участия цитохрома Р-450 (Garsia Q. et al. , 2003) • Резистентность – с 0 до 17% после 6 месяцев применения в больнице (Raad I. et al. , 2004) • Способен вызывать тромбоцитопению (– вит. В 6), нейропатию (обычно при очень длительном курсе)

Pseudomonas aeruginosa (синегнойная палочка) • «Оппортунистический» патоген • «Мукоидные штаммы» наиболее вирулентны • Ограниченая потребность в питании • Продуцируемый токсин нарушает синтез белков хозяина • Имеющиеся ворсинки способствуют адгезии • Резистрентность к антибиотикам: структура, выработка лактамаз, трансфераз • Резистентность к антисептикам

Антибиотики, преимущественно активные против Гр-- флоры • • Аминогликозиды Фторхинолоны Монобактамы Имидазолы

Аминогликозиды Преимущества Антистафилококковая активность Грам-отрицательные аэробы - основная мишень Выраженная антисинегнойная активность (нозокомиальная флора) Недостатки Анаэробы - активность отсутствует Узкий терапевтический диапазон Выраженный токсический потенциал: - ототоксичность (> амикацин) - нефротоксичность (> гентамицин), нейротоксичность

Позиционирование антибиотиков в стационаре: актуальные потребности Аминогликозиды • Гентамицин – Стафилококки – в сочетании с оксациллином или ванкомицином – Энтерококки – в сочетании с ампициллином или ванкомицином – По другим показаниям исключить • Амикацин – Только ОРИТ ( в других отделениях – исключить) – Основное показание – в сочетании с цефалоспоринами при псевдомонадных инфекциях • Другие аминогликозиды преимуществ не имеют?
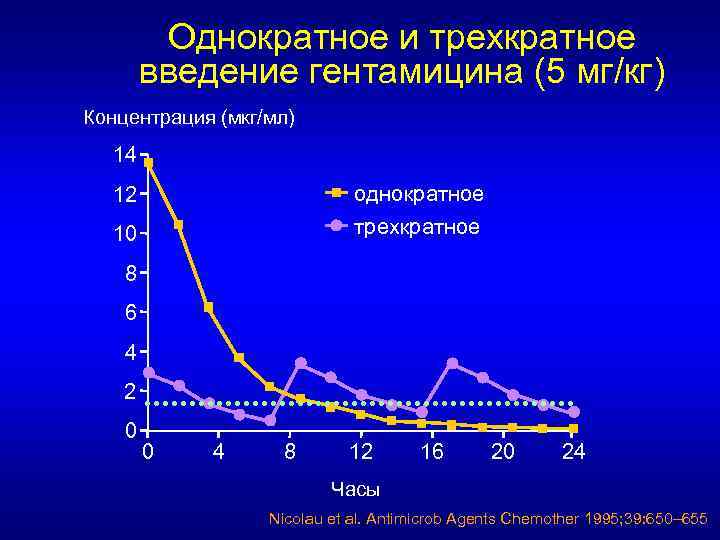
Однократное и трехкратное введение гентамицина (5 мг/кг) Концентрация (мкг/мл) 14 однократное трехкратное 12 10 8 6 4 2 0 0 4 8 12 16 20 24 Часы Nicolau et al. Antimicrob Agents Chemother 1995; 39: 650– 655

Классификация хинолонов/фторхинолонов Поколение Препарат I – нефторированные хинолоны Налидиксовая Г(-) флора (семейство кислота Enterobacteriaceae) Оксолиновая кислота Пипемидовая кислота II – «грамотрицательные» фторхинолоны Норфлоксацин Ципрофлоксацин Пефлоксацин Офлоксацин Ломефлоксацин Г(-) флора, S. aureus, низкая активность против S. pneumoniae и атипичных возбудителей III – «респираторные» фторхинолоны Левофлоксацин Спарфлоксацин Г(+), Г(-), атипичные возбудители IV – «респираторные» + Моксифлоксацин «антианаэробные фторхинолоны Спектр активности Г(+), Г(-), атипичные возбудители + высокая активность против анаэробов
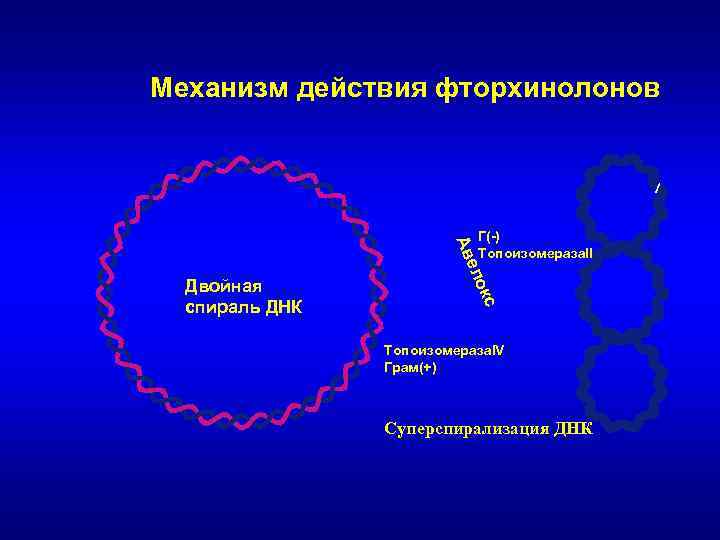
Механизм действия фторхинолонов кс ело Ав Двойная спираль ДНК Г(-) Топоизомераза. II Топоизомераза. IV Грам(+) Суперспирализация ДНК

Позиционирование антибиотиков в стационаре Фторхинолоны Ранние • С антисинегнойной активностью – ципрофлоксацин – Только ОРИТ – Исключить по другим показаниям • Без активности против P. aeruginosa – офлоксацин, пефлоксацин – Вне ОРИТ – Не средства стартовой терапии (ИМВП, пневмония, перитонит) Новые • Моксифлоксацин – тяжелая внебольничная пневмония, нозокомиальная пневмония вне ОРИТ • Левофлоксацин – инфекции Ки. МТ, пневмония вне ОРИТ

Антибиотики ШСД • • • Пеницилллины Цефалоспорины Карбапенемы Тетрациклины Хлорамфеникол

Клинические особенности «базовых» антибиотиков ШСД • Ампициллин: плохо всасывается из ЖКТ, менее активен против H. Influenzae, активен против энтерококков • Амоксициллин: лучше всасывается, активен против Н. influenzae • Аминопенициллины малоактивны в отношении кишечной флоры (но подавляют E. coli) • Частые НЭ – диспепсические расстройства К каждому – высок уровень резистентности

Позиционирование антибиотиков в стационаре: актуальные потребности Пенициллины • Ампициллин – Только внебольничная пневмония и эндокардит • Оксациллин – Только стафилококковые инфекции • Антипсевдомонадные незащищенные – Исключить

Амоксициллин/клавуланат (АК) • По влиянию на анаэробов не уступает метронидазолу и имипенему и превосходит линкозамиды и левофлоксацин Koeth LM, et al. J Antimicrob Chemother. 2004 Jun; 53(6): 1039 -44. • 75% штаммов E. coli, устойчивых к АС, чувствительны к АК, в основном они продуцировали β-лактамазы типа ТЕМ Kaye KS, et al. . Antimicrob Agents Chemother. , 2004 May; 48(5): 1520 -5. • АС: эффективность в отношении Acinetobacter АК: оригинальные и генерические препараты, АС – в основном - генерики

Ампициллин/сульбактам (АС) • Чувствительность до 70% МРСА (устойч. не на продукц. Β-лактамаз) Сидоренко С. В. и др. Антиб химиотер. 1995, 40(3) • Сульбактам > связывание антибиотика с PSP 2α Fasola EL, et al. J Lab Clin Med. 1995 125(2) • При аспирационной пневмонии, абсцессе легкого = цефалоспорин + клиндамицин Allewelt M, et al. Clin Microbiol Infect, 2004; 10(2)

Тикарциллина клавуланат Форма выпуска • Флакон 3, 2 гр № 4 (3 г тикарциллина в форме натриевой соли, 200 мг клавулановой кислоты) • Предназначен для внутривенной инфузии • Эффективен: MSSA, H. infl. , P. aerug. , E. faecalis, St. maltophylia, Enterobact. Spp. , B. fragilis • Применяется в дозе 3, 2 г каждые 6 -8 часов Контроль электролитов, свертывания

ЦС - 1 • Основной препарат – цефазолин • Парентерально: цефпрозил – в России не используют • Перорально: цефалексин, цефадроксил – применяют ограниченно

ЦС-2 • Основной препарат – цефуроксим • Другие : - парентерально: цефотетан, цефокситин, лоракарбеф – реально в России не используются • Перорально - цефаклор – применение ограниченно

ЦС - 3 • Парентерально: • «многоцелевые» - цефотаксим, цефтриаксон; • «антисинегнойные» - цефоперазон, цефтазидим, • «антианаэробный» - латамоксеф • Перорально: цефиксим, цефтибутен, цефпрозил – применение ограниченное

ЦС - 4 • Цефепим (максипим) • Антипсевдомонадная активность • Устойчивость к БЛРС

Позиционирование антибиотиков в стационаре: Цефалоспорины • I-II поколение (цефазолин, цефуроксим) – Предоперационная профилактика • III поколение Цефотаксим, цефтриаксон – Исключить при госпитальных инфекциях – Внебольничные: пневмония, менингит, мочевые Антипсевдомонадные: цефтазидим – Только ОРИТ, только P. aeruginosa • IV поколение (цефепим) – ОРИТ, P. aeruginosa, ротация схем стартовой терапии

Особенности отдельных ЦС • • Цефазолин: АБП, нефротоксичность Цефуроксим: АБП, гемофильная палочка Цефтриаксон: длительность, ЦНС, желчь Цефтазидим, цефоперазон: синегнойная палочка • Цефоперазон-сульбактам: ацинетобактер

Защищенные В-лактамы • Амоксициллин-клавуланат (амоксиклав, аугментин, панклав) • Ампициллин-сульбактам (сультасин, амписид, уназин) • Пиперациллин-тазобактам (тазоцин) • Тикарциллин – клавуланат (тиментин) • Цефоперазон-сульбактам (сульперазон) Расширен спектр действия, снижена приобретенная резистентность

Особенности комбинации цефоперазон – сульбактам (сульперазон) • • • Эффективность против Гр- бактерий, устойчивых к ЦС -3 Активность против отдельных продуцентов БЛРС (как карбапенемы). Активность против анаэробных бактерий Активность против синегнойной палочки и ацинетобактер Сохранность фармакокинетических свойств цефоперазона. В. П. Яковлев, 2003

Карбапенемы • • Имипенем-циластатин Меропенем Эртапенем Маленькая молекула - цвиттерион Устойчивость к В-лактамазам Связывание с ПСБ - 2 Низкий уровень эндотоксинемии

Карбапенемы: что проверено временем? ! Сверхширокий спектр действия Низкая токсичность «Жизнеспасающий эффект» Компонент стандартов лечения тяжелых инфекций Возможности монотерапии Успешная история применения (в том числе в России) Дорогостоящие антибиотики

Причины эффективности карбапенемов Устойчивость к -лактамазам (включая БЛРС) Молекула - цвиттерион (мембраны) Специфичность мишени (ПСБ-2) Постантибиотический эффект Отсутствие инокулюм-эффекта Широта и мощность действия

Позиционирование антибиотиков в стационаре: Карбапенемы (имипенем, меропенем) • Наиболее надежные средства эмпирической терапии • Увеличение использования приводит к: – Элиминации резистентных штаммов Enterobacteriaceae (прежде всего, продуцентов БЛРС и Амр. С бета-лактамаз) – Селекции полирезистентных штаммов P. aeruginosa на фоне имипенема Ингибитор-защищенные бета-лактамы (пиперациллин/тазобактам, цефоперазон/сульбактам) • Допустимо использование в схемах ротации • Основное показание – абдоминальные инфекции • Не целесообразны при P. aeruginosa

Клинические различия карбапенемов Бактериологически: имипенем > грам (+), меропенем > грам ( ) * Имипенем - дети до 3 -х месяцев - преимущество в ортопедии, при панкреатите - возможности «ступенчатой терапии» - выше риск судорог (ингибитор рецепторов ГАМК, NMDA) Меропенем - преимущество при менингитах - возможность вводить болюсно - выше эффект в отношении P. aeruginosa * White К et al, Diagn Microbiol Infect Dis. 2001: 1 Страчунский Л. С. с соавт. , 2002.

«Старые» антибиотики ШСД • • Тетрациклины Чаще – урология (хламидии) Диспепсии, кандидоз, псевдомембр. колит, холестаз, кальций, фотодерматоз Основной препарат – доксициклин Хлорамфеникол Хорошее всасывание Сальмонеллезы? Инфекции ЦНС (пневмококк, менингококк, инфлюэнца) Анемии, невриты, серый синдром
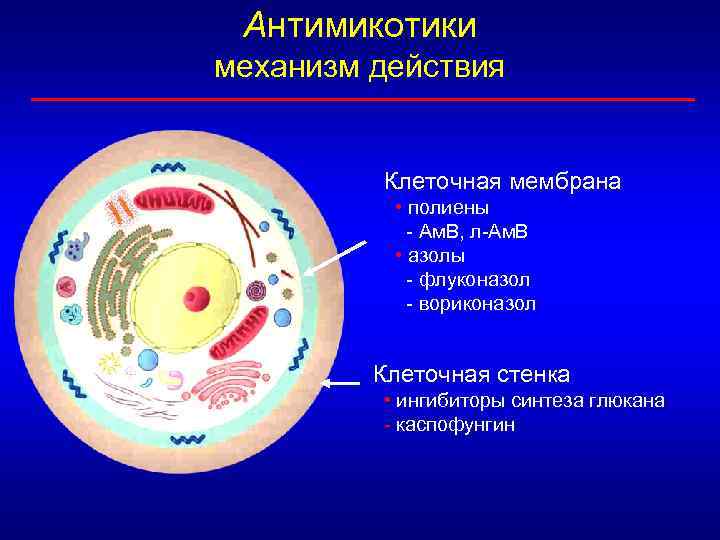
Антимикотики механизм действия Клеточная мембрана • полиены - Ам. В, л-Ам. В • азолы - флуконазол - вориконазол Клеточная стенка • ингибиторы синтеза глюкана - каспофунгин
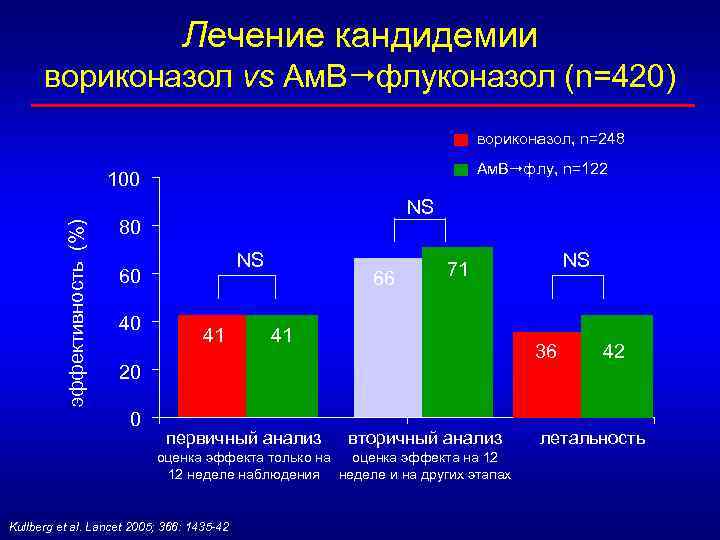
Лечение кандидемии вориконазол vs Ам. В флуконазол (n=420) вориконазол, n=248 Ам. B флу, n=122 эффективность (%) 100 NS 80 NS 60 40 41 66 41 36 20 0 первичный анализ вторичный анализ оценка эффекта только на оценка эффекта на 12 12 неделе наблюдения неделе и на других этапах Kullberg et al. Lancet 2005; 366: 1435 -42 NS 71 42 летальность

Системные антимикотики - безопасность • Амфотерицин В - нефротоксичность (снижать Na. Cl) • Кетоконазол, итраконазол - гепатотоксичность, снижение секреции стероидов • Флуконазол - токсический потенциал невысок

Новые классы/группы антибиотиков, внедренные в практику за последние 10 лет • Оксазолидиноны – Линезолид • Преодоление резистентности Грам + (GISA, VRE) – В перспективе эперезолид, AZD 2563 • Новые фторхинолоны – Левофлоксацин, моксифлоксацин, гатифлоксацин • Повышенная активность против S. pneu, S. aureus • Наиболее высокая у моксифлоксацина (+анаэробы) • По действию на Грам(-) бактерии преимуществ не имеют • Кетолиды (производные 14 -членных макролидов) – Телитромицин • Преодоление резистентности S. pneu, БГСА – По действию на Грам(-) преимуществ нет

Новые классы/группы антибиотиков, находящиеся на II-III фазе КИ (перспектива 2 -3 г) • Липопептиды – Даптомицин • Преодоление резистентности Грам(+) (преим. VRE) • Полусинтетические гликопептиды – Оритаванцин, Далбаванцин • Преодоление резистентности Грам(+), усиление бактерицидности • Глицилциклины – производные миноциклина – Тайгециклин • Широкий спектр – Грам(+) и Грам(-) • Активен против MRSA, PRSP, VRE • Слабая антипсевдомонадная активность

FDA категории риска для плода при использовании антимикробных средств А отсутствие риска и отдаленных ______ последствий для плода В С D X нет контролируемых испытаний, подтверждающих риск развития фетальных поражений Подтверждена токсичность у животных, риск для человека неопределен Существует риск для плода человека, но польза от применения превышает риск Существует риск для плода человека и нет преимуществ. Противопоказаны у беременных Бета-лактамы, цефалоспорины, эритромицин, азитромицин Хлорамфеникол, ФХ кларитромицин, ванкомицин, гентамицин, бисептол Тетрациклин, аминогликозиды ____

Антибиотики у беременных • Средняя частота назначения – 12% • Реальный риск для плода? ? – Олеандомицин – незрелость – Кларитромицин – спонтанные аборты – Триметоприм – дефекты ССС • Теоретический риск – С: фторхинолоны, ванкомицин, гентамицин, имипенем – D: тетрациклин, другие аминогликозиды – Х: нет Чилова Р. Я. И соавт, 2005


А-биот. Испр. 14.ppt