Клиническая эффективность ГА.ppt
- Количество слайдов: 88
 Клиническая эффективность глатирамера ацетата (Копаксона) Omar Khan
Клиническая эффективность глатирамера ацетата (Копаксона) Omar Khan
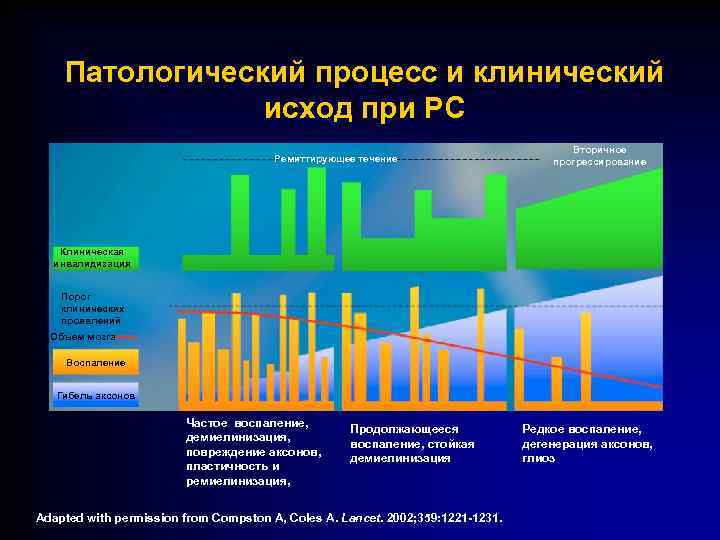 Патологический процесс и клинический исход при РС Ремиттирующее течение Вторичное прогрессирование Клиническая инвалидизация Порог клинических проявлений Объем мозга Воспаление Гибель аксонов Частое воспаление, демиелинизация, повреждение аксонов, пластичность и ремиелинизация, Продолжающееся воспаление, стойкая демиелинизация Adapted with permission from Compston A, Coles A. Lancet. 2002; 359: 1221 -1231. Редкое воспаление, дегенерация аксонов, глиоз
Патологический процесс и клинический исход при РС Ремиттирующее течение Вторичное прогрессирование Клиническая инвалидизация Порог клинических проявлений Объем мозга Воспаление Гибель аксонов Частое воспаление, демиелинизация, повреждение аксонов, пластичность и ремиелинизация, Продолжающееся воспаление, стойкая демиелинизация Adapted with permission from Compston A, Coles A. Lancet. 2002; 359: 1221 -1231. Редкое воспаление, дегенерация аксонов, глиоз
 Двойственная природа воспаления и нейродегенерации при РС Фаза воспаления Обострения Острое течение Множественные очаги Очаги накопления гадолинийсодержащего контраста Наличие ремиссий Неспецифическое повреждение аксонов Фаза дегенерации Прогрессирование Хроническое течение Диффузное поражение Отсутствие очагов накопления гадолиний-содержащего контраста Постоянное нарастание тяжести состояния Вторичная гибель аксонов С обострениями Без обострений Время
Двойственная природа воспаления и нейродегенерации при РС Фаза воспаления Обострения Острое течение Множественные очаги Очаги накопления гадолинийсодержащего контраста Наличие ремиссий Неспецифическое повреждение аксонов Фаза дегенерации Прогрессирование Хроническое течение Диффузное поражение Отсутствие очагов накопления гадолиний-содержащего контраста Постоянное нарастание тяжести состояния Вторичная гибель аксонов С обострениями Без обострений Время
 Восстановление после обострений и прогрессирование РС • Данные пациентов из групп плацебо 20 исследований и баз данных, включая: • Базовые исследования препаратов Авонекс, Бетаферон, Копаксон и Ребиф • Базы данных COSTAR и EDMUS • Исследования естественного течения РС Mellen и Scripps • Оценка влияния обострений на прогрессирование заболевания с использованием шкал: • Шкала EDSS • Неврологическая шкала Скриппс (SNRS) • Простой способ оценки неврологического дефицита, основанный на применении балльной системы оценки высших психический функций, двигательной системы и др. (в норме 0, от 1 до 4 баллов возрастание или убывание) Lublin FD et al. , Neurology 2003; 61: 1528– 1532
Восстановление после обострений и прогрессирование РС • Данные пациентов из групп плацебо 20 исследований и баз данных, включая: • Базовые исследования препаратов Авонекс, Бетаферон, Копаксон и Ребиф • Базы данных COSTAR и EDMUS • Исследования естественного течения РС Mellen и Scripps • Оценка влияния обострений на прогрессирование заболевания с использованием шкал: • Шкала EDSS • Неврологическая шкала Скриппс (SNRS) • Простой способ оценки неврологического дефицита, основанный на применении балльной системы оценки высших психический функций, двигательной системы и др. (в норме 0, от 1 до 4 баллов возрастание или убывание) Lublin FD et al. , Neurology 2003; 61: 1528– 1532
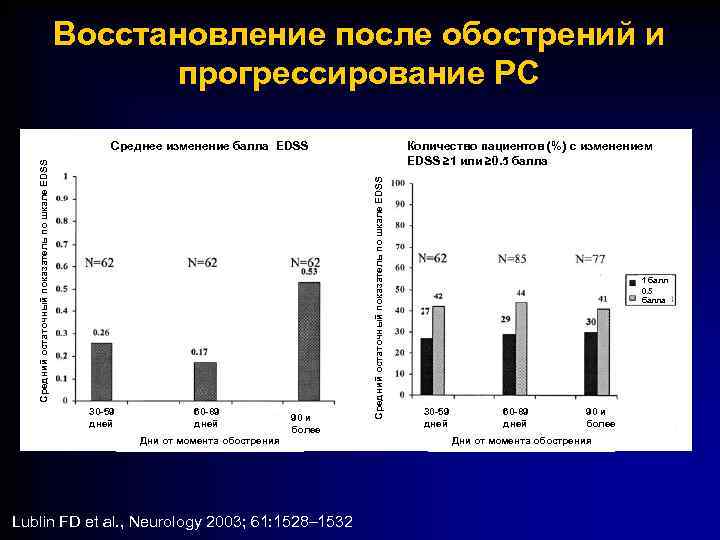 Восстановление после обострений и прогрессирование РС 30 -59 дней 60 -89 дней Дни от момента обострения 90 и более Lublin FD et al. , Neurology 2003; 61: 1528– 1532 Количество пациентов (%) с изменением EDSS ≥ 1 или ≥ 0. 5 балла Средний остаточный показатель по шкале EDSS Среднее изменение балла EDSS 1 балл 0. 5 балла 30 -59 дней 60 -89 дней 90 и более Дни от момента обострения
Восстановление после обострений и прогрессирование РС 30 -59 дней 60 -89 дней Дни от момента обострения 90 и более Lublin FD et al. , Neurology 2003; 61: 1528– 1532 Количество пациентов (%) с изменением EDSS ≥ 1 или ≥ 0. 5 балла Средний остаточный показатель по шкале EDSS Среднее изменение балла EDSS 1 балл 0. 5 балла 30 -59 дней 60 -89 дней 90 и более Дни от момента обострения
 Исследования естественного течения болезни Шведское исследование Вероятность начала прогрессирования в течение 8 - 9 лет (n=255 смешанная форма) Runmarker & Anderson 1993 Brain 116: 117 -34 Канадское исследование 57% из 118 пациентов с РРС достигли оценки 6 баллов по шкале EDSS за 15 лет Weinshenker et al. , (1989) Brain 112(Pt 1): 133 -46 Французское исследование От дебюта РРС до достижения 4 баллов по шкале EDSS проходит в среднем 8. 4 года (n=1567) Confavreux et al. , (2000) NEJM 343: 1430 -8
Исследования естественного течения болезни Шведское исследование Вероятность начала прогрессирования в течение 8 - 9 лет (n=255 смешанная форма) Runmarker & Anderson 1993 Brain 116: 117 -34 Канадское исследование 57% из 118 пациентов с РРС достигли оценки 6 баллов по шкале EDSS за 15 лет Weinshenker et al. , (1989) Brain 112(Pt 1): 133 -46 Французское исследование От дебюта РРС до достижения 4 баллов по шкале EDSS проходит в среднем 8. 4 года (n=1567) Confavreux et al. , (2000) NEJM 343: 1430 -8
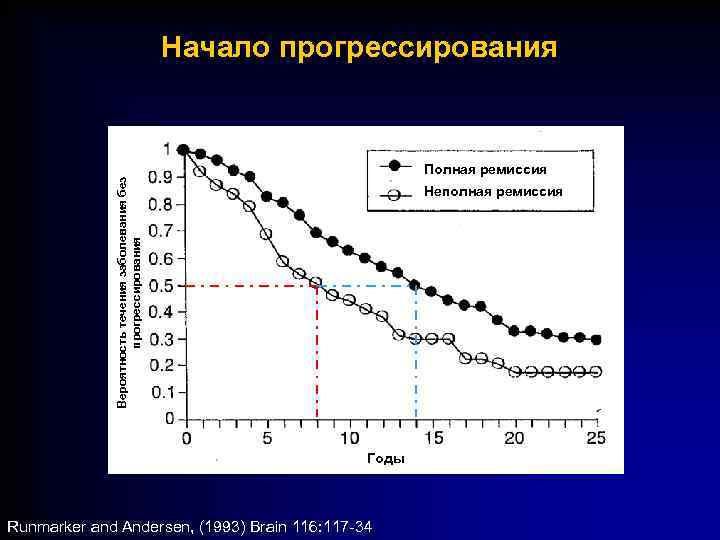 Начало прогрессирования Вероятность течения заболевания без прогрессирования Полная ремиссия Неполная ремиссия Годы Runmarker and Andersen, (1993) Brain 116: 117 -34
Начало прогрессирования Вероятность течения заболевания без прогрессирования Полная ремиссия Неполная ремиссия Годы Runmarker and Andersen, (1993) Brain 116: 117 -34
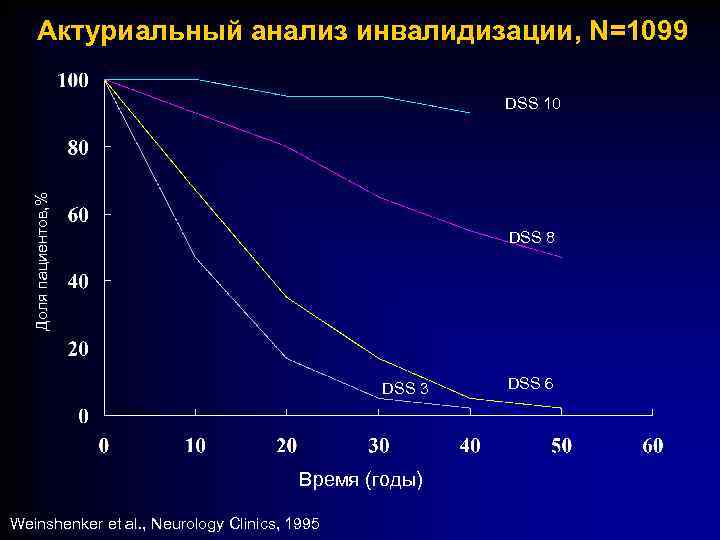 Актуриальный анализ инвалидизации, N=1099 Доля пациентов, % DSS 10 DSS 8 DSS 3 Время (годы) Weinshenker et al. , Neurology Clinics, 1995 DSS 6
Актуриальный анализ инвалидизации, N=1099 Доля пациентов, % DSS 10 DSS 8 DSS 3 Время (годы) Weinshenker et al. , Neurology Clinics, 1995 DSS 6
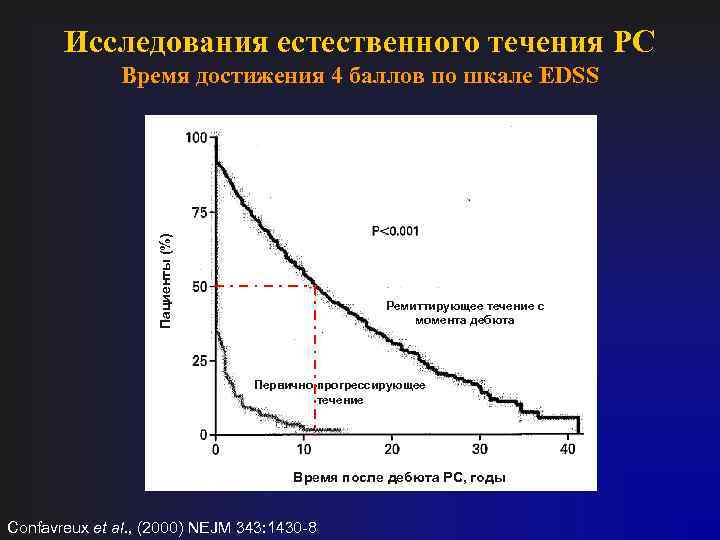 Исследования естественного течения РС Пациенты (%) Время достижения 4 баллов по шкале EDSS Ремиттирующее течение с момента дебюта Первично-прогрессирующее течение Время после дебюта РС, годы Confavreux et al. , (2000) NEJM 343: 1430 -8
Исследования естественного течения РС Пациенты (%) Время достижения 4 баллов по шкале EDSS Ремиттирующее течение с момента дебюта Первично-прогрессирующее течение Время после дебюта РС, годы Confavreux et al. , (2000) NEJM 343: 1430 -8
 Пилотное исследование эффективности ГА при ремиттирующем рассеянном склерозе M. B. Bornstein, MD; A. Miller, MD; S. Slagle, MPH; M. Weitzman, MSW; H. Crystal, MD; E. Drexler, MD; M. Keilson, MD; A. Merriam, MD; S. Wassertheil-Smoller, Ph. D; V. Spada, MSc; W. Weiss, BA; R. Arnon, Ph. D; I. Jacobsohn; D. Teitelbaum, Ph. D; and M. Sela, Ph. D. N Engl J Med. 1987 317(7): 408 -14.
Пилотное исследование эффективности ГА при ремиттирующем рассеянном склерозе M. B. Bornstein, MD; A. Miller, MD; S. Slagle, MPH; M. Weitzman, MSW; H. Crystal, MD; E. Drexler, MD; M. Keilson, MD; A. Merriam, MD; S. Wassertheil-Smoller, Ph. D; V. Spada, MSc; W. Weiss, BA; R. Arnon, Ph. D; I. Jacobsohn; D. Teitelbaum, Ph. D; and M. Sela, Ph. D. N Engl J Med. 1987 317(7): 408 -14.
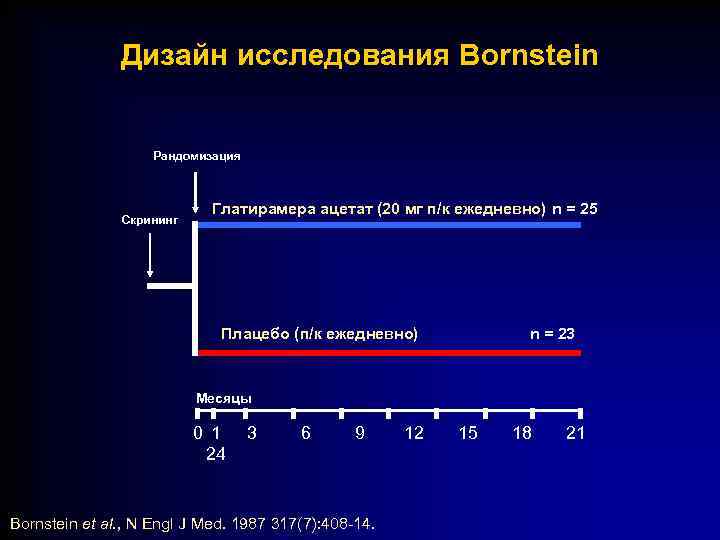 Дизайн исследования Bornstein Рандомизация Скрининг Глатирамера ацетат (20 мг п/к ежедневно) n = 25 Плацебо (п/к ежедневно) n = 23 Месяцы 0 1 24 3 6 9 Bornstein et al. , N Engl J Med. 1987 317(7): 408 -14. 12 15 18 21
Дизайн исследования Bornstein Рандомизация Скрининг Глатирамера ацетат (20 мг п/к ежедневно) n = 25 Плацебо (п/к ежедневно) n = 23 Месяцы 0 1 24 3 6 9 Bornstein et al. , N Engl J Med. 1987 317(7): 408 -14. 12 15 18 21
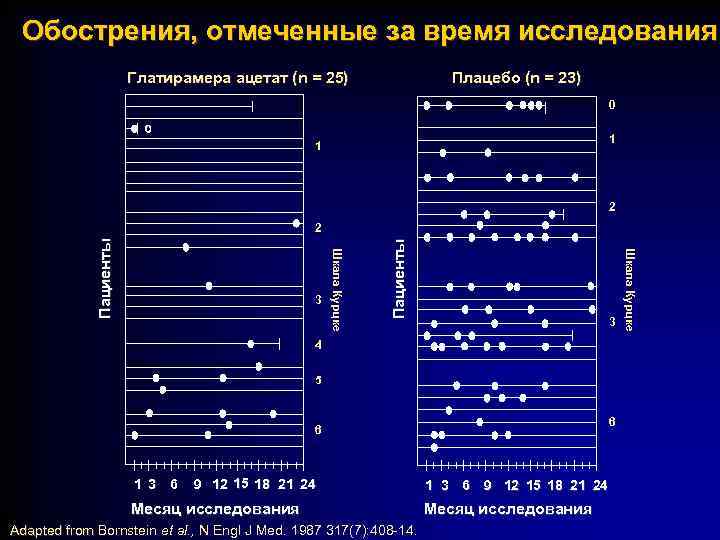 Обострения, отмеченные за время исследования Плацебо (n = 23) Глатирамера ацетат (n = 25) 0 1 1 2 Пациенты 3 4 5 6 6 1 3 6 9 12 15 18 21 24 Месяц исследования Adapted from Bornstein et al. , N Engl J Med. 1987 317(7): 408 -14. Adapted from 1 3 6 9 12 15 18 21 24 Месяц исследования Шкала Курцке 3 Шкала Курцке Пациенты 2
Обострения, отмеченные за время исследования Плацебо (n = 23) Глатирамера ацетат (n = 25) 0 1 1 2 Пациенты 3 4 5 6 6 1 3 6 9 12 15 18 21 24 Месяц исследования Adapted from Bornstein et al. , N Engl J Med. 1987 317(7): 408 -14. Adapted from 1 3 6 9 12 15 18 21 24 Месяц исследования Шкала Курцке 3 Шкала Курцке Пациенты 2
 Изменения степени инвалидизации по истечении двух лет Изменения показателя по шкале Курцке Ухудшение 4 3 2 1 Промежуточный результат Стабильность (0) улучшение – 1 – 2 – 3 Промежуточный результат Всего Все случаи Плацебо n % Глатирамера ацетат % n 1 3 2 5 4. 4 13. 0 8. 7 21. 7 0 1 1 3 4. 0 12. 0 11 9 47. 8 39. 1 5 12 20. 0 48. 0 2 0 1 8. 7 5 4. 4 0 12 52. 2 23 100. 0 Bornstein et al. , N Engl J Med. 1987 317(7): 408 -14. 20. 0 3 12. 0 20 80. 0 25 100. 0
Изменения степени инвалидизации по истечении двух лет Изменения показателя по шкале Курцке Ухудшение 4 3 2 1 Промежуточный результат Стабильность (0) улучшение – 1 – 2 – 3 Промежуточный результат Всего Все случаи Плацебо n % Глатирамера ацетат % n 1 3 2 5 4. 4 13. 0 8. 7 21. 7 0 1 1 3 4. 0 12. 0 11 9 47. 8 39. 1 5 12 20. 0 48. 0 2 0 1 8. 7 5 4. 4 0 12 52. 2 23 100. 0 Bornstein et al. , N Engl J Med. 1987 317(7): 408 -14. 20. 0 3 12. 0 20 80. 0 25 100. 0
 Вероятность не-ухудшения Время до начала прогрессирования в течение двух лет 1. 00 0. 80 Глатирамера ацетат 0. 60 Плацебо 0. 40 0. 20 0. 00 0 3 6 9 12 15 18 21 24 Месяц исследования Bornstein et al. , N Engl J Med. 1987 317(7): 408 -14.
Вероятность не-ухудшения Время до начала прогрессирования в течение двух лет 1. 00 0. 80 Глатирамера ацетат 0. 60 Плацебо 0. 40 0. 20 0. 00 0 3 6 9 12 15 18 21 24 Месяц исследования Bornstein et al. , N Engl J Med. 1987 317(7): 408 -14.
 Кополимер 1 (ГА) снижает частоту обострений и уменьшает степень инвалидизации при ремиттирующем рассеянном склерозе : Результаты мультицентрового, двойного слепого, плацебо-контролируемого исследования III фазы K. P. Johnson, MD; B. R. Brooks, MD; J. A. Cohen, MD; C. C. Ford, MD; J. Goldstein, MD; R. P. Lisak, MD; L. W. Myers, MD; H. S. Panitch, MD; J. W. Rose, MD; R. B. Schiffer, MD; T. Vollmer, MD; L. P. Weiner, MD; J. S. Wolinsky, MD; and the Copolymer 1 Multiple Sclerosis Study Group. Johnson KP et al. Neurology 1995 45: 1268 -76.
Кополимер 1 (ГА) снижает частоту обострений и уменьшает степень инвалидизации при ремиттирующем рассеянном склерозе : Результаты мультицентрового, двойного слепого, плацебо-контролируемого исследования III фазы K. P. Johnson, MD; B. R. Brooks, MD; J. A. Cohen, MD; C. C. Ford, MD; J. Goldstein, MD; R. P. Lisak, MD; L. W. Myers, MD; H. S. Panitch, MD; J. W. Rose, MD; R. B. Schiffer, MD; T. Vollmer, MD; L. P. Weiner, MD; J. S. Wolinsky, MD; and the Copolymer 1 Multiple Sclerosis Study Group. Johnson KP et al. Neurology 1995 45: 1268 -76.
 Глатирамера ацетат (Копаксон) хорошо переносится и оказывает стойкое влияние на частоту обострений рассеянного склероза и степень инвалидизации K. P. Johnson, MD; B. R. Brooks, MD; J. A. Cohen, MD; C. C. Ford, MD; J. Goldstein, MD; R. P. Lisak, MD; L. W. Myers, MD; H. S. Panitch, MD; J. W. Rose, MD; R. B. Schiffer, MD; T. Vollmer, MD; L. P. Weiner, MD; J. S. Wolinsky, MD; and the Copolymer 1 Multiple Sclerosis Study Group. Johnson KP et al. Neurology 1998 50: 701 -8.
Глатирамера ацетат (Копаксон) хорошо переносится и оказывает стойкое влияние на частоту обострений рассеянного склероза и степень инвалидизации K. P. Johnson, MD; B. R. Brooks, MD; J. A. Cohen, MD; C. C. Ford, MD; J. Goldstein, MD; R. P. Lisak, MD; L. W. Myers, MD; H. S. Panitch, MD; J. W. Rose, MD; R. B. Schiffer, MD; T. Vollmer, MD; L. P. Weiner, MD; J. S. Wolinsky, MD; and the Copolymer 1 Multiple Sclerosis Study Group. Johnson KP et al. Neurology 1998 50: 701 -8.
 Критерии включения в базовое исследование в США • Соответствие критериям достоверного РС по Позеру (Poser, 1993) • Возраст от 18 до 45 лет • Сохранная способность к самостоятельному передвижению, EDSS 0 - 5. 0 баллов • 2 и более четко зафиксированных обострения за последние два года • Дебют РС по крайней мере за 1 год до рандомизации • Неврологическая стабильность в течение 30 дней до включения • Отсутствие терапии кортикостероидами в течение 30 дней до включения • Отсутствие патогенетического лечения РС в анамнезе • Использование адекватных методов контрацепции Johnson KP et al. Neurology 1995 45: 1268 -76.
Критерии включения в базовое исследование в США • Соответствие критериям достоверного РС по Позеру (Poser, 1993) • Возраст от 18 до 45 лет • Сохранная способность к самостоятельному передвижению, EDSS 0 - 5. 0 баллов • 2 и более четко зафиксированных обострения за последние два года • Дебют РС по крайней мере за 1 год до рандомизации • Неврологическая стабильность в течение 30 дней до включения • Отсутствие терапии кортикостероидами в течение 30 дней до включения • Отсутствие патогенетического лечения РС в анамнезе • Использование адекватных методов контрацепции Johnson KP et al. Neurology 1995 45: 1268 -76.
 Дизайн исследования Глатирамера Ацетата Базовое исследование в США + продолжение е ни Johnson KP et al. Neurology 1998 50: 701 -8. же ол од Пр е ни е юч л Вк Основной 24 месячный период Открытая фаза
Дизайн исследования Глатирамера Ацетата Базовое исследование в США + продолжение е ни Johnson KP et al. Neurology 1998 50: 701 -8. же ол од Пр е ни е юч л Вк Основной 24 месячный период Открытая фаза
 Характеристики пациентов на момент включения: базовое исследование в США ГА Плацебо (n=125) (n=126) Возраст (гг; среднее ± ст. откл. ) 34. 6 ± 6. 0 34. 3 ± 6. 5 Пол Женщины Мужчины 88 (70. 4%) 37 (29. 6%) 96 (76. 2%) 30 (23. 8%) Длительность РС (гг) Среднее ± ст. откл. 7. 3 ± 4. 9 6. 6 ± 5. 1 Частота обострений в последние 2 года Среднее ± ст. откл. 2. 9 ± 1. 3 2. 9 ± 1. 1 EDSS при включении Среднее ± ст. откл. 2. 8 ± 1. 2 2. 4 ± 1. 3 Johnson KP et al. Neurology 1995 45: 1268 -76.
Характеристики пациентов на момент включения: базовое исследование в США ГА Плацебо (n=125) (n=126) Возраст (гг; среднее ± ст. откл. ) 34. 6 ± 6. 0 34. 3 ± 6. 5 Пол Женщины Мужчины 88 (70. 4%) 37 (29. 6%) 96 (76. 2%) 30 (23. 8%) Длительность РС (гг) Среднее ± ст. откл. 7. 3 ± 4. 9 6. 6 ± 5. 1 Частота обострений в последние 2 года Среднее ± ст. откл. 2. 9 ± 1. 3 2. 9 ± 1. 1 EDSS при включении Среднее ± ст. откл. 2. 8 ± 1. 2 2. 4 ± 1. 3 Johnson KP et al. Neurology 1995 45: 1268 -76.
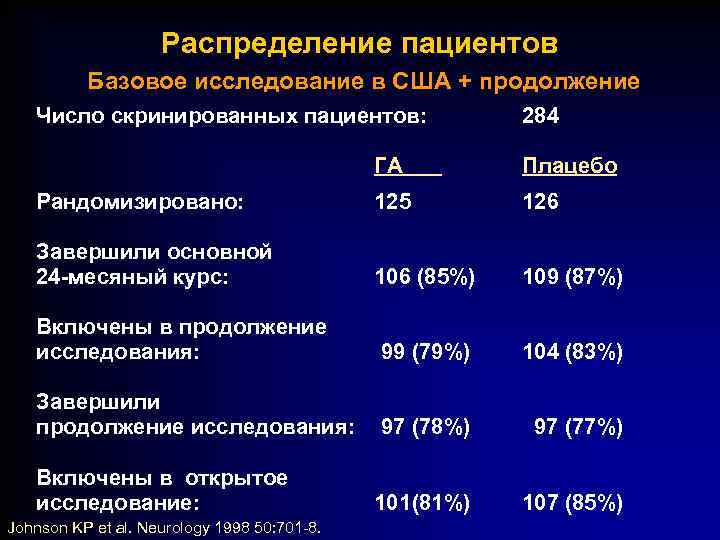 Распределение пациентов Базовое исследование в США + продолжение Число скринированных пациентов: 284 ГА Плацебо Рандомизировано: 125 126 Завершили основной 24 -месяный курс: 106 (85%) 109 (87%) Включены в продолжение исследования: 99 (79%) 104 (83%) Завершили продолжение исследования: 97 (78%) 97 (77%) Включены в открытое исследование: 101(81%) 107 (85%) Johnson KP et al. Neurology 1998 50: 701 -8.
Распределение пациентов Базовое исследование в США + продолжение Число скринированных пациентов: 284 ГА Плацебо Рандомизировано: 125 126 Завершили основной 24 -месяный курс: 106 (85%) 109 (87%) Включены в продолжение исследования: 99 (79%) 104 (83%) Завершили продолжение исследования: 97 (78%) 97 (77%) Включены в открытое исследование: 101(81%) 107 (85%) Johnson KP et al. Neurology 1998 50: 701 -8.
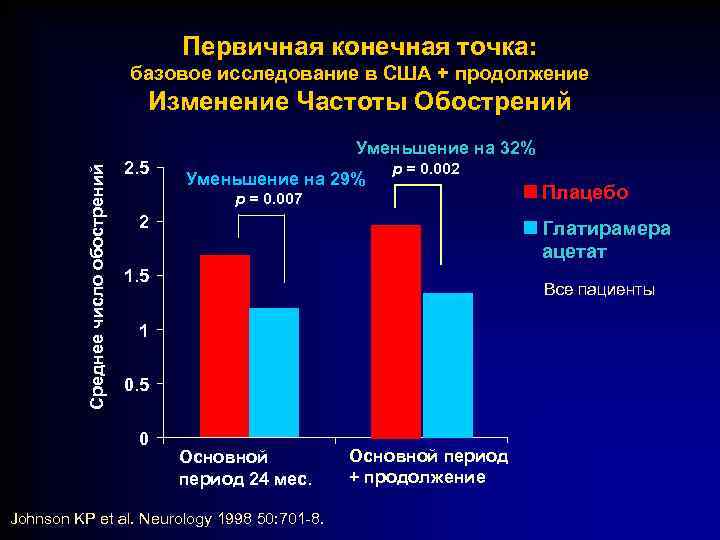 Первичная конечная точка: базовое исследование в США + продолжение Среднее число обострений Изменение Частоты Обострений 2. 5 Уменьшение на 32% Уменьшение на 29% p = 0. 002 p = 0. 007 2 Глатирамера ацетат 1. 5 Все пациенты 1 0. 5 0 Плацебо Основной период 24 мес. Johnson KP et al. Neurology 1998 50: 701 -8. Основной период + продолжение
Первичная конечная точка: базовое исследование в США + продолжение Среднее число обострений Изменение Частоты Обострений 2. 5 Уменьшение на 32% Уменьшение на 29% p = 0. 002 p = 0. 007 2 Глатирамера ацетат 1. 5 Все пациенты 1 0. 5 0 Плацебо Основной период 24 мес. Johnson KP et al. Neurology 1998 50: 701 -8. Основной период + продолжение
 Вторичная конечная точка: базовое исследование в США + продолжение Доля пациентов без обострений p = 0. 098 p = 0. 035 Плацебо Глатирамера ацетат Johnson KP et al. Neurology 1998 50: 701 -8.
Вторичная конечная точка: базовое исследование в США + продолжение Доля пациентов без обострений p = 0. 098 p = 0. 035 Плацебо Глатирамера ацетат Johnson KP et al. Neurology 1998 50: 701 -8.
 Вторичная конечная точка: базовое исследование в США + продолжение Динамика степени инвалидизации за время исследования Доля пациентов (%) Основной период (2 года) p=0. 024, BL to 24 mo. p=0. 023, RMA Изменение EDSS 1 балла Johnson et al. , Neurol. 1995; 45: 1268 -76. Продолжение (до 35 месяцев) p=0. 001, BL to Last Visit p=0. 024, RMA Изменение EDSS 1 балла Johnson et al. , Neurol. 1998; 50: 701 -8.
Вторичная конечная точка: базовое исследование в США + продолжение Динамика степени инвалидизации за время исследования Доля пациентов (%) Основной период (2 года) p=0. 024, BL to 24 mo. p=0. 023, RMA Изменение EDSS 1 балла Johnson et al. , Neurol. 1995; 45: 1268 -76. Продолжение (до 35 месяцев) p=0. 001, BL to Last Visit p=0. 024, RMA Изменение EDSS 1 балла Johnson et al. , Neurol. 1998; 50: 701 -8.
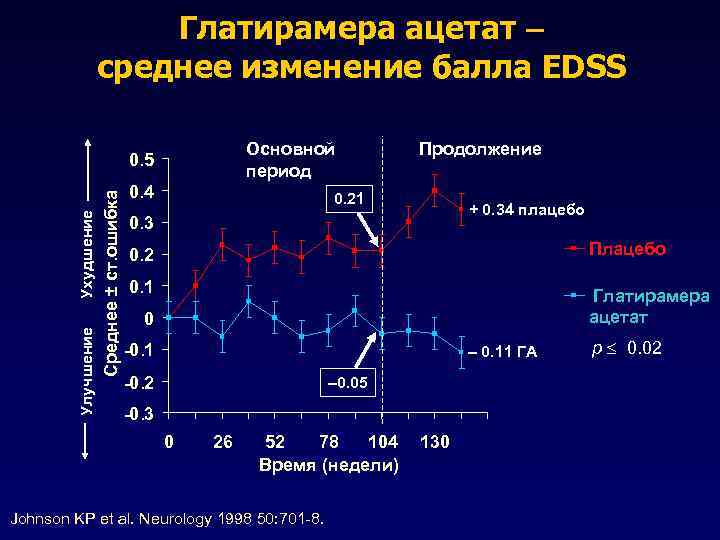 Глатирамера ацетат – среднее изменение балла EDSS Основной период Среднее ± ст. ошибка Улучшение Ухудшение 0. 5 0. 4 Продолжение 0. 21 + 0. 34 плацебо 0. 3 Плацебо 0. 2 0. 1 Глатирамера ацетат 0 -0. 1 – 0. 11 ГА -0. 2 – 0. 05 -0. 3 0 26 52 78 104 Время (недели) Johnson KP et al. Neurology 1998 50: 701 -8. 130 p 0. 02
Глатирамера ацетат – среднее изменение балла EDSS Основной период Среднее ± ст. ошибка Улучшение Ухудшение 0. 5 0. 4 Продолжение 0. 21 + 0. 34 плацебо 0. 3 Плацебо 0. 2 0. 1 Глатирамера ацетат 0 -0. 1 – 0. 11 ГА -0. 2 – 0. 05 -0. 3 0 26 52 78 104 Время (недели) Johnson KP et al. Neurology 1998 50: 701 -8. 130 p 0. 02
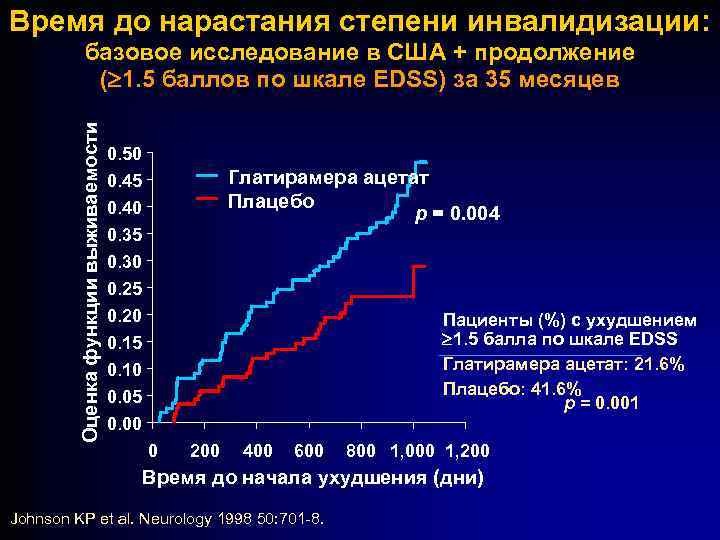 Время до нарастания степени инвалидизации: Оценка функции выживаемости базовое исследование в США + продолжение ( 1. 5 баллов по шкале EDSS) за 35 месяцев 0. 50 Глатирамера ацетат Плацебо p = 0. 004 0. 45 0. 40 0. 35 0. 30 0. 25 0. 20 Пациенты (%) с ухудшением 1. 5 балла по шкале EDSS Глатирамера ацетат: 21. 6% Плацебо: 41. 6% p = 0. 001 0. 15 0. 10 0. 05 0. 00 0 200 400 600 800 1, 000 1, 200 Время до начала ухудшения (дни) Johnson KP et al. Neurology 1998 50: 701 -8.
Время до нарастания степени инвалидизации: Оценка функции выживаемости базовое исследование в США + продолжение ( 1. 5 баллов по шкале EDSS) за 35 месяцев 0. 50 Глатирамера ацетат Плацебо p = 0. 004 0. 45 0. 40 0. 35 0. 30 0. 25 0. 20 Пациенты (%) с ухудшением 1. 5 балла по шкале EDSS Глатирамера ацетат: 21. 6% Плацебо: 41. 6% p = 0. 001 0. 15 0. 10 0. 05 0. 00 0 200 400 600 800 1, 000 1, 200 Время до начала ухудшения (дни) Johnson KP et al. Neurology 1998 50: 701 -8.
 Глатирамера ацетат: базовое исследование в США + продолжение Заключение • Клинический эффект ГА сохранялся и после продолжения исследования: – Снижение частоты обострений (29% за 24 месяца; 33% за время продолжения исследования) – Степень инвалидизации (Улучшение vs. Ухудшение) • ГА прекрасно переносится и имеет высокие показатели безопасности. • Наиболее длительное из исследований по лечению РС. когда-либо проводившихся – Планируется продолжение в течение 10 и более лет Johnson KP et al. , Neurol. 1998; 50: 701 -8.
Глатирамера ацетат: базовое исследование в США + продолжение Заключение • Клинический эффект ГА сохранялся и после продолжения исследования: – Снижение частоты обострений (29% за 24 месяца; 33% за время продолжения исследования) – Степень инвалидизации (Улучшение vs. Ухудшение) • ГА прекрасно переносится и имеет высокие показатели безопасности. • Наиболее длительное из исследований по лечению РС. когда-либо проводившихся – Планируется продолжение в течение 10 и более лет Johnson KP et al. , Neurol. 1998; 50: 701 -8.
 Европейско-Канадское МРТ исследование
Европейско-Канадское МРТ исследование
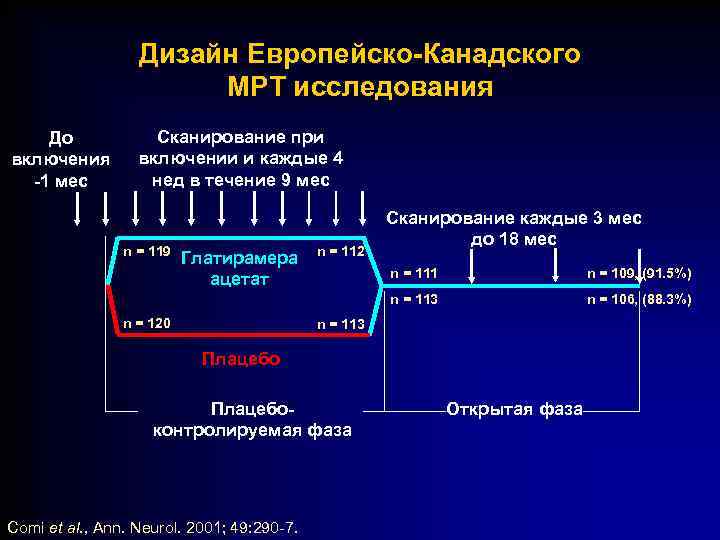 Дизайн Европейско-Канадского МРТ исследования До включения -1 мес Сканирование при включении и каждые 4 нед в течение 9 мес n = 119 Глатирамера ацетат n = 112 Сканирование каждые 3 мес до 18 мес n = 109, (91. 5%) n = 113 n = 120 n = 111 n = 106, (88. 3%) n = 113 Плацебоконтролируемая фаза Comi et al. , Ann. Neurol. 2001; 49: 290 -7. Открытая фаза
Дизайн Европейско-Канадского МРТ исследования До включения -1 мес Сканирование при включении и каждые 4 нед в течение 9 мес n = 119 Глатирамера ацетат n = 112 Сканирование каждые 3 мес до 18 мес n = 109, (91. 5%) n = 113 n = 120 n = 111 n = 106, (88. 3%) n = 113 Плацебоконтролируемая фаза Comi et al. , Ann. Neurol. 2001; 49: 290 -7. Открытая фаза
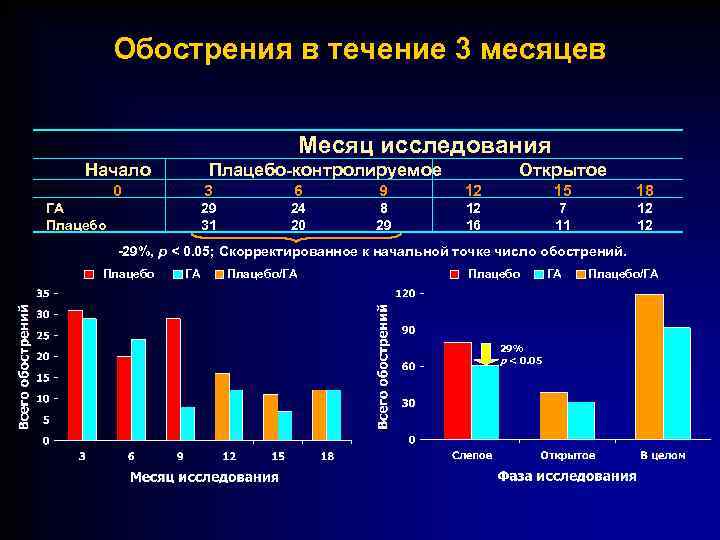 Обострения в течение 3 месяцев Месяц исследования Начало Плацебо-контролируемое 0 Открытое 3 9 12 15 18 29 31 ГА Плацебо 6 24 20 8 29 12 16 7 11 12 12 -29%, p < 0. 05; Скорректированное к начальной точке число обострений. Плацебо ГА Плацебо/ГА Плацебо 29% p < 0. 05 ГА Плацебо/ГА
Обострения в течение 3 месяцев Месяц исследования Начало Плацебо-контролируемое 0 Открытое 3 9 12 15 18 29 31 ГА Плацебо 6 24 20 8 29 12 16 7 11 12 12 -29%, p < 0. 05; Скорректированное к начальной точке число обострений. Плацебо ГА Плацебо/ГА Плацебо 29% p < 0. 05 ГА Плацебо/ГА
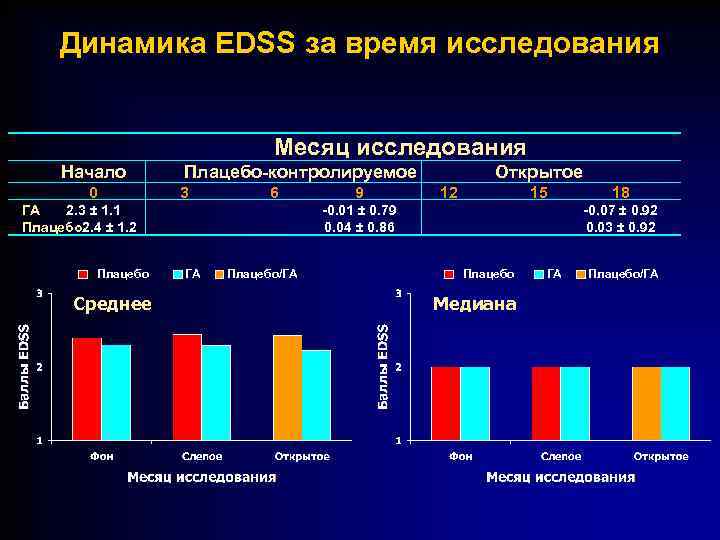 Динамика EDSS за время исследования Месяц исследования Начало 0 Плацебо-контролируемое 3 6 ГА 2. 3 ± 1. 1 Плацебо 2. 4 ± 1. 2 Плацебо Среднее 9 Открытое 12 15 -0. 01 ± 0. 79 0. 04 ± 0. 86 ГА Плацебо/ГА 18 -0. 07 ± 0. 92 0. 03 ± 0. 92 Плацебо Медиана ГА Плацебо/ГА
Динамика EDSS за время исследования Месяц исследования Начало 0 Плацебо-контролируемое 3 6 ГА 2. 3 ± 1. 1 Плацебо 2. 4 ± 1. 2 Плацебо Среднее 9 Открытое 12 15 -0. 01 ± 0. 79 0. 04 ± 0. 86 ГА Плацебо/ГА 18 -0. 07 ± 0. 92 0. 03 ± 0. 92 Плацебо Медиана ГА Плацебо/ГА
 Метаанализ данных об обострениях и степени инвалидизации трех клинических исследований Влияние глатирамера ацетата на частоту обострений и накопление неврологического дефицита при рассеянном склерозе: метаанализ трех двойных слепых, рандомизированных, плацебо-контролируемых клинических исследований Martinelli Boneschi F, Rovaris M, Johnson KP, Miller A, Wolinsky JS, Ladkani D, Shifroni G, Comi G and Filippi M Multiple Sclerosis 2003 9(4): 349 -355 Влияние глатирамера ацетата на стойкое накопление неврологического дефицита при ремиттирующем рассеянном склерозе проявилось в течение одного года: метаанализ результатов трех двойных слепых, плацебоконтролируемых клинических исследований Wolinsky JS, Johnson KP, Comi G, Miller A, Ladkani D, Shifroni G, Stark Y, Filippi M Multiple Sclerosis 2003 9(Supp 1): S 120
Метаанализ данных об обострениях и степени инвалидизации трех клинических исследований Влияние глатирамера ацетата на частоту обострений и накопление неврологического дефицита при рассеянном склерозе: метаанализ трех двойных слепых, рандомизированных, плацебо-контролируемых клинических исследований Martinelli Boneschi F, Rovaris M, Johnson KP, Miller A, Wolinsky JS, Ladkani D, Shifroni G, Comi G and Filippi M Multiple Sclerosis 2003 9(4): 349 -355 Влияние глатирамера ацетата на стойкое накопление неврологического дефицита при ремиттирующем рассеянном склерозе проявилось в течение одного года: метаанализ результатов трех двойных слепых, плацебоконтролируемых клинических исследований Wolinsky JS, Johnson KP, Comi G, Miller A, Ladkani D, Shifroni G, Stark Y, Filippi M Multiple Sclerosis 2003 9(Supp 1): S 120
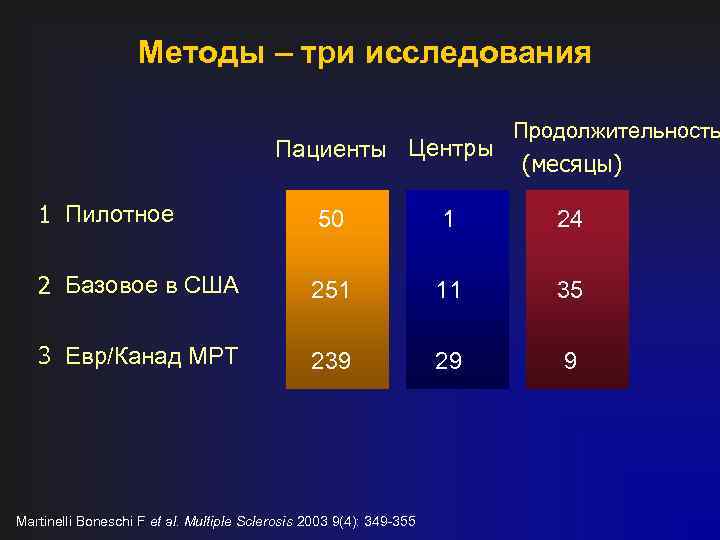 Методы – три исследования Пациенты Центры Продолжительность (месяцы) 1 Пилотное 50 1 24 2 Базовое в США 251 11 35 3 Евр/Канад МРТ 239 29 9 Martinelli Boneschi F et al. Multiple Sclerosis 2003 9(4): 349 -355
Методы – три исследования Пациенты Центры Продолжительность (месяцы) 1 Пилотное 50 1 24 2 Базовое в США 251 11 35 3 Евр/Канад МРТ 239 29 9 Martinelli Boneschi F et al. Multiple Sclerosis 2003 9(4): 349 -355
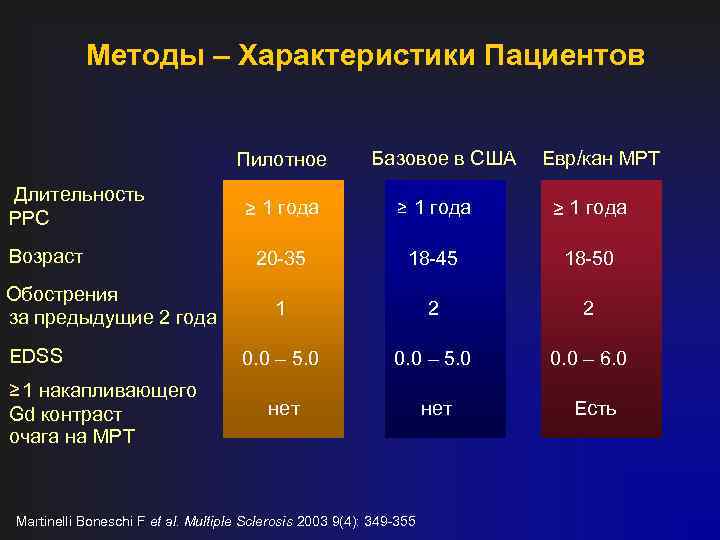 Методы – Характеристики Пациентов Пилотное Длительность РРС Возраст Обострения за предыдущие 2 года EDSS ≥ 1 накапливающего Gd контраст очага на МРТ Базовое в США Евр/кан МРТ ≥ 1 года 20 -35 18 -45 18 -50 1 2 2 0. 0 – 5. 0 0. 0 – 6. 0 нет Martinelli Boneschi F et al. Multiple Sclerosis 2003 9(4): 349 -355 Есть
Методы – Характеристики Пациентов Пилотное Длительность РРС Возраст Обострения за предыдущие 2 года EDSS ≥ 1 накапливающего Gd контраст очага на МРТ Базовое в США Евр/кан МРТ ≥ 1 года 20 -35 18 -45 18 -50 1 2 2 0. 0 – 5. 0 0. 0 – 6. 0 нет Martinelli Boneschi F et al. Multiple Sclerosis 2003 9(4): 349 -355 Есть
 Методы – Параметры оценки результата 1. Среднегодовая частота обострений (первичный результат) 2. Количество обострений 3. Время до начала первого обострения 4. Накопление неврологического дефицита (1 балл по шкале EDSS в течение 90 дней) Martinelli Boneschi F et al. Multiple Sclerosis 2003 9(4): 349 -355
Методы – Параметры оценки результата 1. Среднегодовая частота обострений (первичный результат) 2. Количество обострений 3. Время до начала первого обострения 4. Накопление неврологического дефицита (1 балл по шкале EDSS в течение 90 дней) Martinelli Boneschi F et al. Multiple Sclerosis 2003 9(4): 349 -355
 Методы – клинические параметры • Лекарственное воздействие • Обострения в течение 2 -х лет до исследования • Возраст • Категория по количеству обострений (0 -1, 2, >2) • Пол • Балл EDSS • Категория по EDSS (0 -2, 2. 5 -4, >4) • Длительность заболевания • Индекс нарастания тяжести заболевания (показатель по шкале EDSS/длительность заболевания) • Центр исследования • Тип исследования Martinelli Boneschi F et al. Multiple Sclerosis 2003 9(4): 349 -355
Методы – клинические параметры • Лекарственное воздействие • Обострения в течение 2 -х лет до исследования • Возраст • Категория по количеству обострений (0 -1, 2, >2) • Пол • Балл EDSS • Категория по EDSS (0 -2, 2. 5 -4, >4) • Длительность заболевания • Индекс нарастания тяжести заболевания (показатель по шкале EDSS/длительность заболевания) • Центр исследования • Тип исследования Martinelli Boneschi F et al. Multiple Sclerosis 2003 9(4): 349 -355
 Отношение шансов и доверительный интервал Исходя из 2 -х сценариев (n = 20 или 200) Наступление события Отсутствие события % Прогрессировавших Препарат % Не прогрессировавших Препарат A 5 (p 1) 5 (p 3) Плацебо 8 (p 2) 2 (p 4) Препарат В 50 (p 1) 50 (p 3) Плацебо 80 (p 2) 20 (p 4) ОШ = p 1 x p 4 = p 2 x p 3 ОШ = p 1 x p 4 p 2 x p 3 5 x 2 = 5 x 8 = 50 x 20 50 x 80 10 = 0. 25 40 = 1000 4000
Отношение шансов и доверительный интервал Исходя из 2 -х сценариев (n = 20 или 200) Наступление события Отсутствие события % Прогрессировавших Препарат % Не прогрессировавших Препарат A 5 (p 1) 5 (p 3) Плацебо 8 (p 2) 2 (p 4) Препарат В 50 (p 1) 50 (p 3) Плацебо 80 (p 2) 20 (p 4) ОШ = p 1 x p 4 = p 2 x p 3 ОШ = p 1 x p 4 p 2 x p 3 5 x 2 = 5 x 8 = 50 x 20 50 x 80 10 = 0. 25 40 = 1000 4000
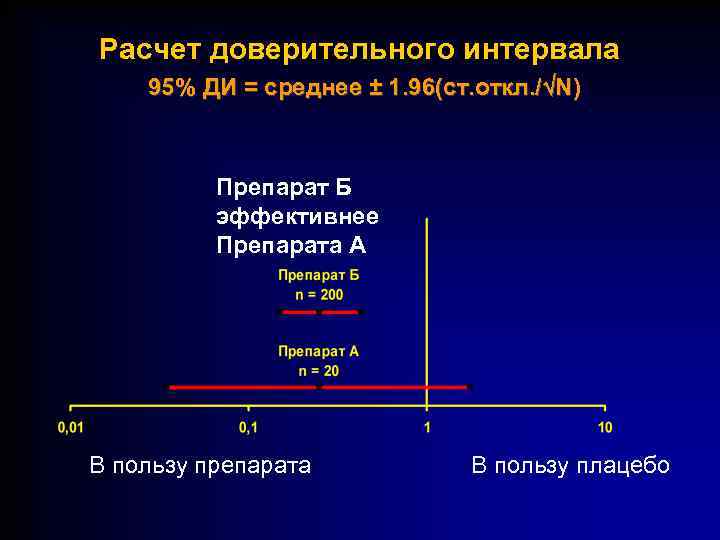 Расчет доверительного интервала Confidence Intervals 95% ДИ = среднее ± 1. 96(ст. откл. / N) Препарат Б эффективнее Препарата A В пользу препарата В пользу плацебо
Расчет доверительного интервала Confidence Intervals 95% ДИ = среднее ± 1. 96(ст. откл. / N) Препарат Б эффективнее Препарата A В пользу препарата В пользу плацебо
 Расчет доверительного интервала Confidence Intervals Влияние уровня значимости (р) Доля пациентов Без прогрессирования Плацебо Препарат Разность р А 20% 50% 30% 0. 17 Б 20% 50% 30% 0. 0001 Между двумя препаратами нет разницы ни в % соотношении, ни в ОШ, но ДИ для препарата Б значительно уже! (Соответствует значимому р)
Расчет доверительного интервала Confidence Intervals Влияние уровня значимости (р) Доля пациентов Без прогрессирования Плацебо Препарат Разность р А 20% 50% 30% 0. 17 Б 20% 50% 30% 0. 0001 Между двумя препаратами нет разницы ни в % соотношении, ни в ОШ, но ДИ для препарата Б значительно уже! (Соответствует значимому р)
 Отношение шансов Расчет: исходя из большей эффективности ГА по сравнению с плацебо (% прогрессировавших) Наступление события Отсутствие события Всего % прогрессировавших % без прогрессирования ГА 10 (p 1) 90 (p 3) 100 (p 1 + p 3) Плацебо 20 (p 2) 80 (p 4) 100 (p 2 + p 4) 30 (p 1 + p 2) 170 (p 3 + p 4) Всего ОШ = p 1 x p 4 p 2 x p 3 = 10 x 80 20 x 90 = 800 = 0. 44 1800 Точка на графике находится слева от 1 по оси Х.
Отношение шансов Расчет: исходя из большей эффективности ГА по сравнению с плацебо (% прогрессировавших) Наступление события Отсутствие события Всего % прогрессировавших % без прогрессирования ГА 10 (p 1) 90 (p 3) 100 (p 1 + p 3) Плацебо 20 (p 2) 80 (p 4) 100 (p 2 + p 4) 30 (p 1 + p 2) 170 (p 3 + p 4) Всего ОШ = p 1 x p 4 p 2 x p 3 = 10 x 80 20 x 90 = 800 = 0. 44 1800 Точка на графике находится слева от 1 по оси Х.
 Отношение шансов Примеры различных ситуаций Гипотеза: эффективность ГА не отличается от Плацебо (% прогрессировавших) ОШ = p 1 x p 4 p 2 x p 3 ОШ = 20 x 80 = 1600 = 1. 0 1600 Гипотеза: эффективность ГА ниже, чем Плацебо (% прогрессировавших) p 1 x p 4 = 20 x 90 = 1800 = 2. 25 p 2 x p 3 ОШ = = 10 x 80 800 Гипотеза: эффективность ГА выше, чем Плацебо (% прогрессировавших) p 1 x p 4 = 10 x 80 = 800 = 0. 44 p 2 x p 3 20 x 90 1800
Отношение шансов Примеры различных ситуаций Гипотеза: эффективность ГА не отличается от Плацебо (% прогрессировавших) ОШ = p 1 x p 4 p 2 x p 3 ОШ = 20 x 80 = 1600 = 1. 0 1600 Гипотеза: эффективность ГА ниже, чем Плацебо (% прогрессировавших) p 1 x p 4 = 20 x 90 = 1800 = 2. 25 p 2 x p 3 ОШ = = 10 x 80 800 Гипотеза: эффективность ГА выше, чем Плацебо (% прогрессировавших) p 1 x p 4 = 10 x 80 = 800 = 0. 44 p 2 x p 3 20 x 90 1800
 Относительный риск Расчет, исходя из большей эффективности ГА по сравнению с плацебо (% прогрессировавших) Наступление события Отсутствие события Всего % прогрессировавших % без прогрессирования ГА 10 (p 1) 90 (p 3) 100 (p 1 + p 3) Плацебо 20 (p 2) 80 (p 4) 100 (p 2 + p 4) 30 (p 1 + p 2) 170 (p 3 + p 4) всего ОР = p 1 : ( p 1+p 3) = p 2 : ( p 2+p 4) 10 : 100 20 : 100 = 1000 = 0. 50 2000 Точка на графике находится слева от 1 по оси Х. ОШ = 0. 44
Относительный риск Расчет, исходя из большей эффективности ГА по сравнению с плацебо (% прогрессировавших) Наступление события Отсутствие события Всего % прогрессировавших % без прогрессирования ГА 10 (p 1) 90 (p 3) 100 (p 1 + p 3) Плацебо 20 (p 2) 80 (p 4) 100 (p 2 + p 4) 30 (p 1 + p 2) 170 (p 3 + p 4) всего ОР = p 1 : ( p 1+p 3) = p 2 : ( p 2+p 4) 10 : 100 20 : 100 = 1000 = 0. 50 2000 Точка на графике находится слева от 1 по оси Х. ОШ = 0. 44
 Относительный риск Примеры различных возможностей Гипотеза: эффективность ГА не отличается от Плацебо (% прогрессировавших) ОР = p 1 : (p 1+p 3) = 20 x 100 = 2000 = 1. 0 ОШ=1. 0 p 2 : (p 2+p 4) 20 x 100 2000 Гипотеза: эффективность ГА ниже, чем Плацебо (% прогрессировавших) ОР = p 1 : (p 1+p 3) = p 2 : (p 2+p 4) 20 : 100 10 : 100 = 2000 = 2. 00 1000 Гипотеза: эффективность ГА выше, чем Плацебо (% прогрессировавших) ОР = p 1 : ( p 1+p 3) = 10 : 100 = 1000 = 0. 50 p 2 : ( p 2+p 4) 20 : 100 ОШ=2. 25 2000 ОШ=0. 44
Относительный риск Примеры различных возможностей Гипотеза: эффективность ГА не отличается от Плацебо (% прогрессировавших) ОР = p 1 : (p 1+p 3) = 20 x 100 = 2000 = 1. 0 ОШ=1. 0 p 2 : (p 2+p 4) 20 x 100 2000 Гипотеза: эффективность ГА ниже, чем Плацебо (% прогрессировавших) ОР = p 1 : (p 1+p 3) = p 2 : (p 2+p 4) 20 : 100 10 : 100 = 2000 = 2. 00 1000 Гипотеза: эффективность ГА выше, чем Плацебо (% прогрессировавших) ОР = p 1 : ( p 1+p 3) = 10 : 100 = 1000 = 0. 50 p 2 : ( p 2+p 4) 20 : 100 ОШ=2. 25 2000 ОШ=0. 44
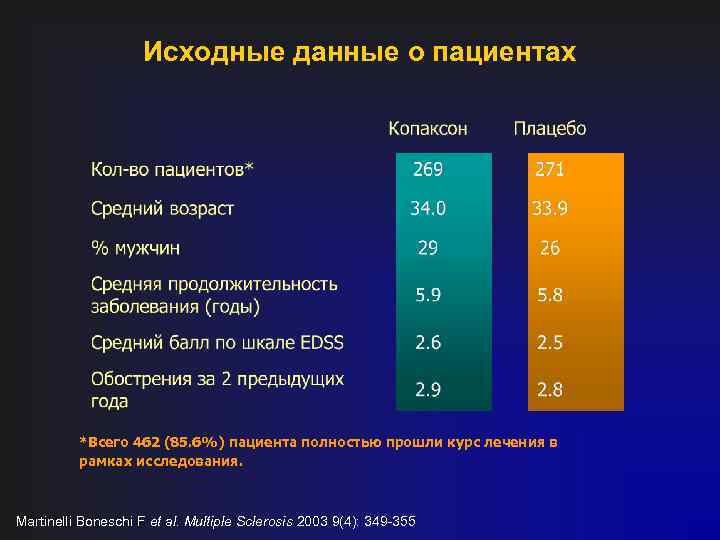 Исходные данные о пациентах *Всего 462 (85. 6%) пациента полностью прошли курс лечения в рамках исследования. Martinelli Boneschi F et al. Multiple Sclerosis 2003 9(4): 349 -355
Исходные данные о пациентах *Всего 462 (85. 6%) пациента полностью прошли курс лечения в рамках исследования. Martinelli Boneschi F et al. Multiple Sclerosis 2003 9(4): 349 -355
 Терапевтический эффект * Скорректировано по отношению к показателю по шкале EDSS на начало исследования и частоте обострений за предшествующие 2 года Martinelli Boneschi F et al. Multiple Sclerosis 2003 9(4): 349 -355
Терапевтический эффект * Скорректировано по отношению к показателю по шкале EDSS на начало исследования и частоте обострений за предшествующие 2 года Martinelli Boneschi F et al. Multiple Sclerosis 2003 9(4): 349 -355
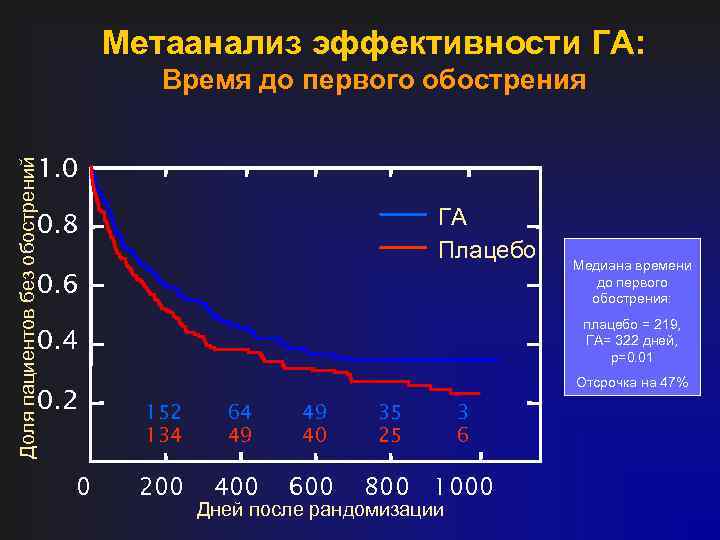 Метаанализ эффективности ГА: Время до первого обострения Доля пациентов без обострений 1. 0 ГА Плацебо 0. 8 0. 6 Медиана времени до первого обострения: 0. 4 плацебо = 219, ГА= 322 дней, p=0. 01 0. 2 Отсрочка на 47% 0 152 134 64 49 49 40 200 400 600 35 25 3 6 800 1000 Дней после рандомизации
Метаанализ эффективности ГА: Время до первого обострения Доля пациентов без обострений 1. 0 ГА Плацебо 0. 8 0. 6 Медиана времени до первого обострения: 0. 4 плацебо = 219, ГА= 322 дней, p=0. 01 0. 2 Отсрочка на 47% 0 152 134 64 49 49 40 200 400 600 35 25 3 6 800 1000 Дней после рандомизации
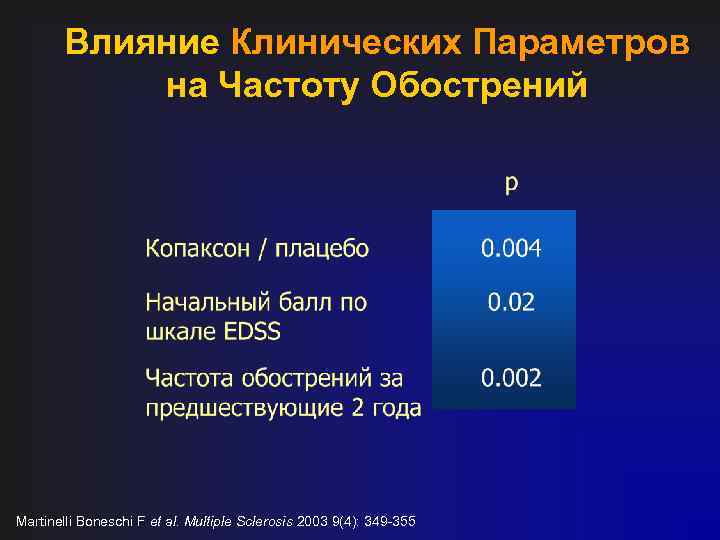 Влияние Клинических Параметров на Частоту Обострений Martinelli Boneschi F et al. Multiple Sclerosis 2003 9(4): 349 -355
Влияние Клинических Параметров на Частоту Обострений Martinelli Boneschi F et al. Multiple Sclerosis 2003 9(4): 349 -355
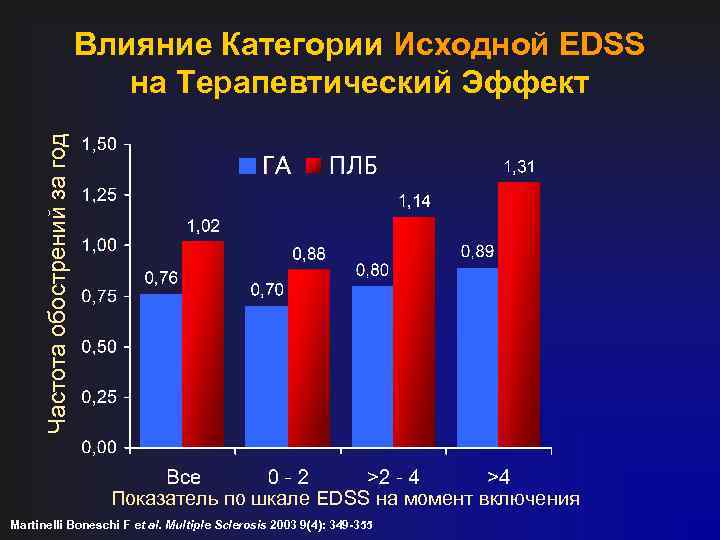 Частота обострений за год Влияние Категории Исходной EDSS на Терапевтический Эффект Показатель по шкале EDSS на момент включения Martinelli Boneschi F et al. Multiple Sclerosis 2003 9(4): 349 -355
Частота обострений за год Влияние Категории Исходной EDSS на Терапевтический Эффект Показатель по шкале EDSS на момент включения Martinelli Boneschi F et al. Multiple Sclerosis 2003 9(4): 349 -355
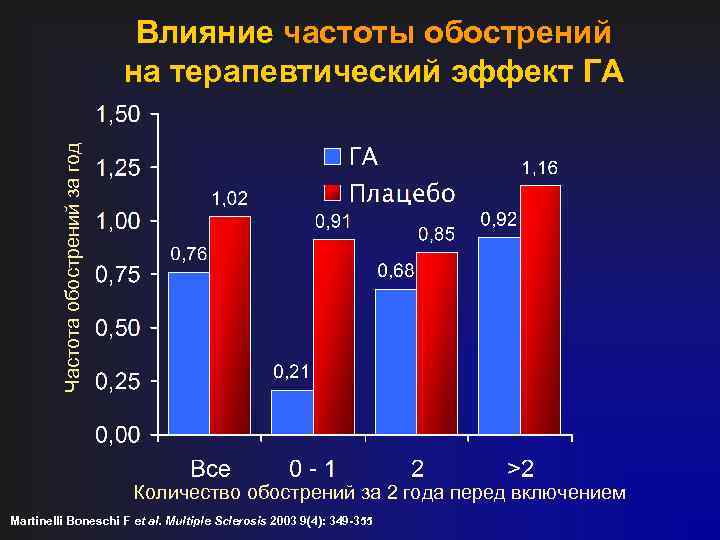 Частота обострений за год Влияние частоты обострений на терапевтический эффект ГА Количество обострений за 2 года перед включением Martinelli Boneschi F et al. Multiple Sclerosis 2003 9(4): 349 -355
Частота обострений за год Влияние частоты обострений на терапевтический эффект ГА Количество обострений за 2 года перед включением Martinelli Boneschi F et al. Multiple Sclerosis 2003 9(4): 349 -355
 Дополнительный анализ по степени инвалидизации Влияние ГА на стойкую инвалидизацию при РРС очевидно уже в течение первого года лечения: метаанализ результатов трех двойных слепых, плацебо-контролируемых клинических исследований Wolinsky JS, Johnson KP, Comi G, Miller AE, Ladkani D, Shifroni G, Stark Y and Filippi M Multiple Sclerosis 9(Supp. 1): S 120
Дополнительный анализ по степени инвалидизации Влияние ГА на стойкую инвалидизацию при РРС очевидно уже в течение первого года лечения: метаанализ результатов трех двойных слепых, плацебо-контролируемых клинических исследований Wolinsky JS, Johnson KP, Comi G, Miller AE, Ladkani D, Shifroni G, Stark Y and Filippi M Multiple Sclerosis 9(Supp. 1): S 120
 Оценка результата Первичный результат • Количество пациентов с прогрессированием ( 1 балла по шкале EDSS, сохраняющимся в течение 90 дней) в группах плацебо и ГА. Wolinsky et al. , Multiple Sclerosis 2003 9(Supp. 1): S 120. See also Neurology 2003 60; 5(Suppl. 1): A 480.
Оценка результата Первичный результат • Количество пациентов с прогрессированием ( 1 балла по шкале EDSS, сохраняющимся в течение 90 дней) в группах плацебо и ГА. Wolinsky et al. , Multiple Sclerosis 2003 9(Supp. 1): S 120. See also Neurology 2003 60; 5(Suppl. 1): A 480.
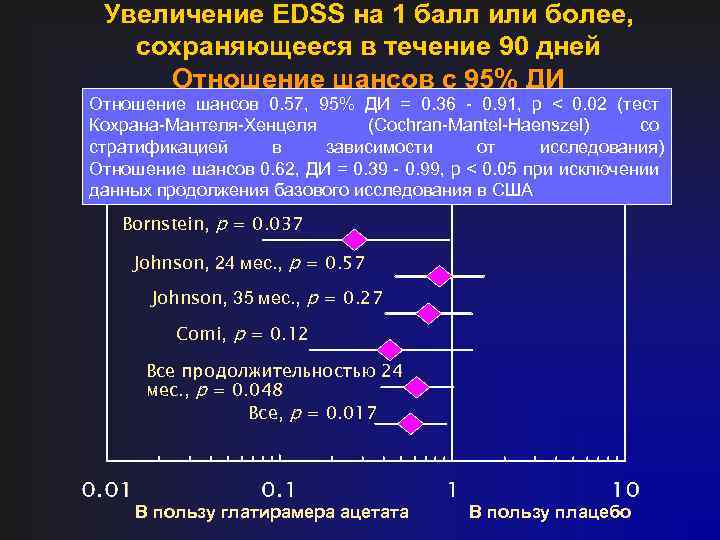 Увеличение EDSS на 1 балл или более, сохраняющееся в течение 90 дней Отношение шансов с 95% ДИ Отношение шансов 0. 57, 95% ДИ = 0. 36 - 0. 91, p < 0. 02 (тест Кохрана-Мантеля-Хенцеля (Cochran-Mantel-Haenszel) со стратификацией в зависимости от исследования) Отношение шансов 0. 62, ДИ = 0. 39 - 0. 99, p < 0. 05 при исключении данных продолжения базового исследования в США Bornstein, p = 0. 037 Johnson, 24 мес. , p = 0. 57 Johnson, 35 мес. , p = 0. 27 Comi, p = 0. 12 Все продолжительностью 24 мес. , p = 0. 048 Все, p = 0. 017 В пользу глатирамера ацетата В пользу плацебо
Увеличение EDSS на 1 балл или более, сохраняющееся в течение 90 дней Отношение шансов с 95% ДИ Отношение шансов 0. 57, 95% ДИ = 0. 36 - 0. 91, p < 0. 02 (тест Кохрана-Мантеля-Хенцеля (Cochran-Mantel-Haenszel) со стратификацией в зависимости от исследования) Отношение шансов 0. 62, ДИ = 0. 39 - 0. 99, p < 0. 05 при исключении данных продолжения базового исследования в США Bornstein, p = 0. 037 Johnson, 24 мес. , p = 0. 57 Johnson, 35 мес. , p = 0. 27 Comi, p = 0. 12 Все продолжительностью 24 мес. , p = 0. 048 Все, p = 0. 017 В пользу глатирамера ацетата В пользу плацебо
 Результат: относительные риски прогрессирования РС Относительный риск 95% ДИ p В течение одного года 0. 56 0. 34 – 0. 92 0. 02 Все данные 0. 65 0. 43 – 0. 97 0. 03 Wolinsky et al. , Multiple Sclerosis 2003 9(Supp. 1): S 120. See also Neurology 2003 60; 5(Suppl. 1): A 480.
Результат: относительные риски прогрессирования РС Относительный риск 95% ДИ p В течение одного года 0. 56 0. 34 – 0. 92 0. 02 Все данные 0. 65 0. 43 – 0. 97 0. 03 Wolinsky et al. , Multiple Sclerosis 2003 9(Supp. 1): S 120. See also Neurology 2003 60; 5(Suppl. 1): A 480.
 Доля пациентов без нарастания степени инвалидизации ( 1 балла по шкале EDSS, сохраняющейся в течение 90 дней) Доля пациентов с нарастанием EDSS ГА практически вдвое отдаляет наступление прогрессирования (оценка в Kaplan Meier estimate of the time to 25% of placebo treated subjects виде отношения 1. 88, регрессионная модель Вейбулла (Weibull accumulating sustained disability was 543 days, the GA treated subjects did regression)) not reach this milestone (p <0. 03, Log Rank test) Связь с назначением препарата (p < 0. 02) и возрастом на момент включения в исследование (p < 0. 001) являлась значимой 1. 0 ГА Плацебо 0. 8 0. 6 0. 4 234 225 0 114 108 104 95 78 70 14 22 200 400 600 800 1000 Дни после рандомизации
Доля пациентов без нарастания степени инвалидизации ( 1 балла по шкале EDSS, сохраняющейся в течение 90 дней) Доля пациентов с нарастанием EDSS ГА практически вдвое отдаляет наступление прогрессирования (оценка в Kaplan Meier estimate of the time to 25% of placebo treated subjects виде отношения 1. 88, регрессионная модель Вейбулла (Weibull accumulating sustained disability was 543 days, the GA treated subjects did regression)) not reach this milestone (p <0. 03, Log Rank test) Связь с назначением препарата (p < 0. 02) и возрастом на момент включения в исследование (p < 0. 001) являлась значимой 1. 0 ГА Плацебо 0. 8 0. 6 0. 4 234 225 0 114 108 104 95 78 70 14 22 200 400 600 800 1000 Дни после рандомизации
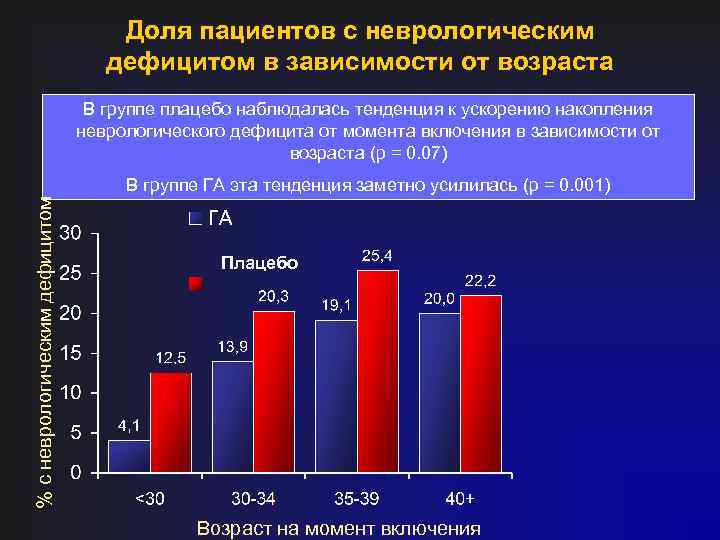 Доля пациентов с неврологическим дефицитом в зависимости от возраста % с неврологическим дефицитом В группе плацебо наблюдалась тенденция к ускорению накопления неврологического дефицита от момента включения в зависимости от Patients who relapsed were more likely to accumulate new deficits возраста (p = 0. 07) (Odds Ratio 4. 3, 95% CI = 2. 4 - 7. 6, p<0. 0001) В группе ГА эта тенденция заметно усилилась (p = 0. 001) Плацебо Возраст на момент включения
Доля пациентов с неврологическим дефицитом в зависимости от возраста % с неврологическим дефицитом В группе плацебо наблюдалась тенденция к ускорению накопления неврологического дефицита от момента включения в зависимости от Patients who relapsed were more likely to accumulate new deficits возраста (p = 0. 07) (Odds Ratio 4. 3, 95% CI = 2. 4 - 7. 6, p<0. 0001) В группе ГА эта тенденция заметно усилилась (p = 0. 001) Плацебо Возраст на момент включения
 Вопросы ранней эффективности • Сомнительная ранняя эффективность • Плохая переносимость • Нейтрализующие антитела к β-интерферонам
Вопросы ранней эффективности • Сомнительная ранняя эффективность • Плохая переносимость • Нейтрализующие антитела к β-интерферонам
 Выработка нейтрализующих АТ к различным препаратам INF • У 2 -45% пациентов, получавших INF, вырабатываются НАт. В базовых исследованиях: – у 28 -45% в ответ на Бетаферон – у 14 -24% в ответ на Ребиф – у 2 -5% в ответ на Авонекс • В датском исследовании не обнаружено различий между вероятностью появления НАт в ответ на введение Бетаферона и Ребифа (p=0. 52), однако Авонекс вызывал значительно более слабый иммунный ответ
Выработка нейтрализующих АТ к различным препаратам INF • У 2 -45% пациентов, получавших INF, вырабатываются НАт. В базовых исследованиях: – у 28 -45% в ответ на Бетаферон – у 14 -24% в ответ на Ребиф – у 2 -5% в ответ на Авонекс • В датском исследовании не обнаружено различий между вероятностью появления НАт в ответ на введение Бетаферона и Ребифа (p=0. 52), однако Авонекс вызывал значительно более слабый иммунный ответ
 Выработка Нат к β-интерферонам Ü Большая часть пациентов, у которых вырабатываются НАт, приобретают их в первые 12 -18 мес. лечения. Пациенты с высоким титром НАт остаются иммунореактивными на протяжении всего курса лечения. Выработка НАт Время (месяцы) 0 6 12 18 Влияние на клиническую эффективность Влияние на эффективность по данным МРТ
Выработка Нат к β-интерферонам Ü Большая часть пациентов, у которых вырабатываются НАт, приобретают их в первые 12 -18 мес. лечения. Пациенты с высоким титром НАт остаются иммунореактивными на протяжении всего курса лечения. Выработка НАт Время (месяцы) 0 6 12 18 Влияние на клиническую эффективность Влияние на эффективность по данным МРТ
 Влияние НАт на частоту обострений Датское исследование: • В Дании все пациенты на ИМТ регистрируются в базе данных • Клинические данные и данные о наличии НАт регистрируются через 3 и 6 месяцев, и далее каждые 6 месяцев • Данные о клинике и наличии НАт были собраны у 541 пациента, получавших INF в течение 60 месяцев – – 194 Бетаферон через день 103 Ребиф 22 еженедельно 162 Ребиф 22 три раза в неделю 82 Авонекс еженедельно • Средний балл по шкале EDSS значимо увеличился через 42 мес. у пациентов с положительной НАт-реакцией Sorensen PS et al. Lancet 2003; 362: 1184– 91
Влияние НАт на частоту обострений Датское исследование: • В Дании все пациенты на ИМТ регистрируются в базе данных • Клинические данные и данные о наличии НАт регистрируются через 3 и 6 месяцев, и далее каждые 6 месяцев • Данные о клинике и наличии НАт были собраны у 541 пациента, получавших INF в течение 60 месяцев – – 194 Бетаферон через день 103 Ребиф 22 еженедельно 162 Ребиф 22 три раза в неделю 82 Авонекс еженедельно • Средний балл по шкале EDSS значимо увеличился через 42 мес. у пациентов с положительной НАт-реакцией Sorensen PS et al. Lancet 2003; 362: 1184– 91
 Влияние НАТ на частоту обострений +49% Adapted from Sorensen PS et al. Lancet 2003; 362: 1184– 91
Влияние НАТ на частоту обострений +49% Adapted from Sorensen PS et al. Lancet 2003; 362: 1184– 91
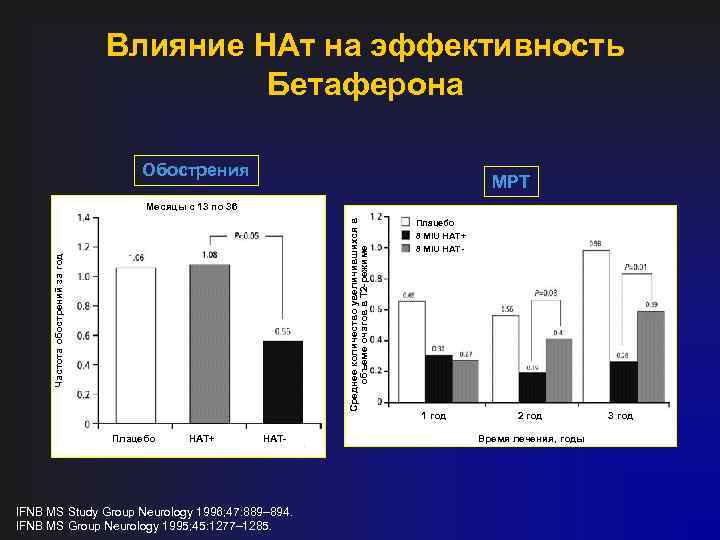 Влияние НАт на эффективность Бетаферона Обострения МРТ Частота обострений за год Среднее количество увеличившихся в объеме очагов в Т 2 -режиме Месяцы с 13 по 36 Плацебо НАТ+ НАТ- IFNB MS Study Group Neurology 1996; 47: 889– 894. IFNB MS Group Neurology 1995; 45: 1277– 1285. Плацебо 8 MIU НАТ+ 8 MIU НАТ- 1 год 2 год Время лечения, годы 3 год
Влияние НАт на эффективность Бетаферона Обострения МРТ Частота обострений за год Среднее количество увеличившихся в объеме очагов в Т 2 -режиме Месяцы с 13 по 36 Плацебо НАТ+ НАТ- IFNB MS Study Group Neurology 1996; 47: 889– 894. IFNB MS Group Neurology 1995; 45: 1277– 1285. Плацебо 8 MIU НАТ+ 8 MIU НАТ- 1 год 2 год Время лечения, годы 3 год
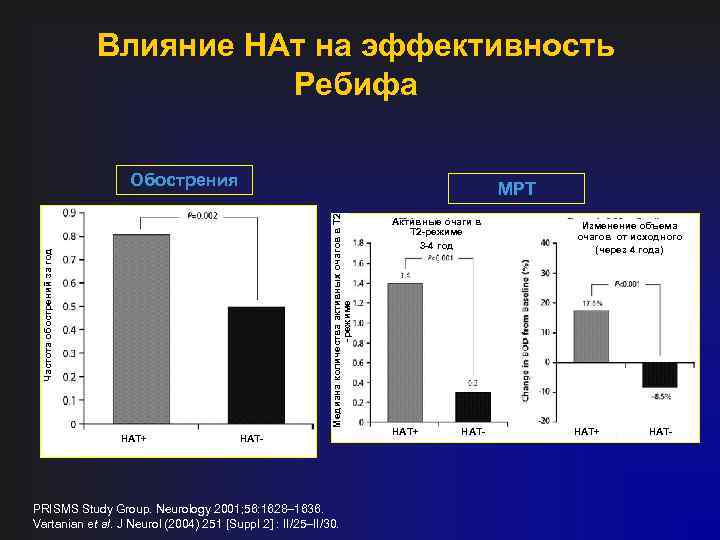 Влияние НАт на эффективность Ребифа Обострения Частота обострений за год Медиана количества активных очагов в Т 2 -режиме МРТ НАТ+ НАТ- PRISMS Study Group. Neurology 2001; 56: 1628– 1636. Vartanian et al. J Neurol (2004) 251 [Suppl 2] : II/25–II/30. Активные очаги в Т 2 -режиме 3 -4 год НАТ+ НАТ- Изменение объема очагов от исходного (через 4 года) НАТ+ НАТ-
Влияние НАт на эффективность Ребифа Обострения Частота обострений за год Медиана количества активных очагов в Т 2 -режиме МРТ НАТ+ НАТ- PRISMS Study Group. Neurology 2001; 56: 1628– 1636. Vartanian et al. J Neurol (2004) 251 [Suppl 2] : II/25–II/30. Активные очаги в Т 2 -режиме 3 -4 год НАТ+ НАТ- Изменение объема очагов от исходного (через 4 года) НАТ+ НАТ-
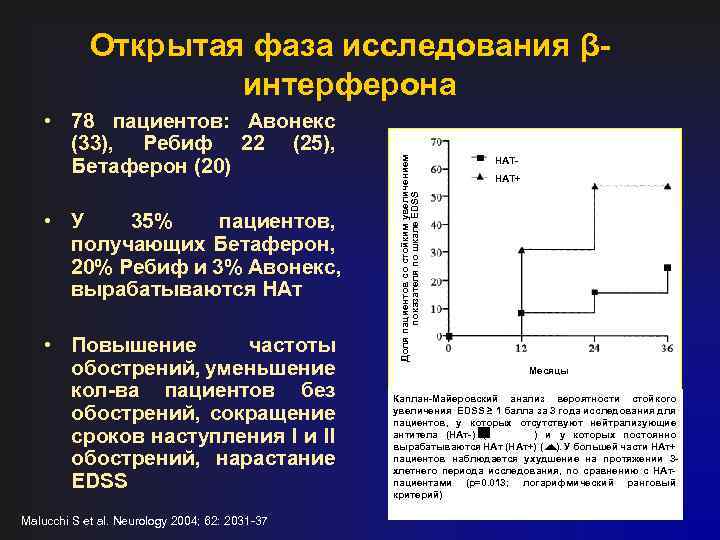 • 78 пациентов: Авонекс (33), Ребиф 22 (25), Бетаферон (20) • У 35% пациентов, получающих Бетаферон, 20% Ребиф и 3% Авонекс, вырабатываются НАт • Повышение частоты обострений, уменьшение кол-ва пациентов без обострений, сокращение сроков наступления I и II обострений, нарастание EDSS Malucchi S et al. Neurology 2004; 62: 2031 -37 Доля пациентов со стойким увеличением показателя по шкале EDSS Открытая фаза исследования βинтерферона НАТНАТ+ Месяцы Каплан-Майеровский анализ вероятности стойкого увеличения EDSS ≥ 1 балла за 3 года исследования для пациентов, у которых отсутствуют нейтрализующие антитела (НАт-) ( ) и у которых постоянно вырабатываются НАт (НАт+) ( ). У большей части НАт+ пациентов наблюдается ухудшение на протяжении 3 хлетнего периода исследования, по сравнению с НАт- пациентами (р=0. 013; логарифмический ранговый критерий)
• 78 пациентов: Авонекс (33), Ребиф 22 (25), Бетаферон (20) • У 35% пациентов, получающих Бетаферон, 20% Ребиф и 3% Авонекс, вырабатываются НАт • Повышение частоты обострений, уменьшение кол-ва пациентов без обострений, сокращение сроков наступления I и II обострений, нарастание EDSS Malucchi S et al. Neurology 2004; 62: 2031 -37 Доля пациентов со стойким увеличением показателя по шкале EDSS Открытая фаза исследования βинтерферона НАТНАТ+ Месяцы Каплан-Майеровский анализ вероятности стойкого увеличения EDSS ≥ 1 балла за 3 года исследования для пациентов, у которых отсутствуют нейтрализующие антитела (НАт-) ( ) и у которых постоянно вырабатываются НАт (НАт+) ( ). У большей части НАт+ пациентов наблюдается ухудшение на протяжении 3 хлетнего периода исследования, по сравнению с НАт- пациентами (р=0. 013; логарифмический ранговый критерий)
 Руководство по клиническому использованию результатов определения анти-IFN-β антител при рассеянном склерозе: сообщение рабочей группы EFNS по изучению антител к IFN-β при рассеянном склерозе • Обзоры, касающиеся выработки НАт и их влияния на эффективность Рекомендации: • Необходимо тестировать всех пациентов на наличие НАт на 12 -й и 24 -й месяц терапии • Допустимо прекратить тестирование тех пациентов, у которых НАТтне обнаруживаются на протяжении этого периода • • Если НАт обнаружены, тестирование необходимо периодически повторять. Если титр НАт остается высоким при повторных измерениях с 3 -6 месячным интервалом, терапию IFN-b необходимо прервать. Переход к другому IFN-препарату не дает клинических преимуществ для НАт+ пациентов
Руководство по клиническому использованию результатов определения анти-IFN-β антител при рассеянном склерозе: сообщение рабочей группы EFNS по изучению антител к IFN-β при рассеянном склерозе • Обзоры, касающиеся выработки НАт и их влияния на эффективность Рекомендации: • Необходимо тестировать всех пациентов на наличие НАт на 12 -й и 24 -й месяц терапии • Допустимо прекратить тестирование тех пациентов, у которых НАТтне обнаруживаются на протяжении этого периода • • Если НАт обнаружены, тестирование необходимо периодически повторять. Если титр НАт остается высоким при повторных измерениях с 3 -6 месячным интервалом, терапию IFN-b необходимо прервать. Переход к другому IFN-препарату не дает клинических преимуществ для НАт+ пациентов
 Глатирамера Ацетат – 10 лет доказанной эффективности CC Ford, KP Johnson, RP Lisak, HS Panitch, G Shifroni, JS Wolinsky, and the COPAXONE® Study Group. Проспективное открытое исследование глатирамера ацетата: более десяти лет непрерывного использования для лечения рассеянного склероза Multiple Sclerosis 2006; 12: 309 -320
Глатирамера Ацетат – 10 лет доказанной эффективности CC Ford, KP Johnson, RP Lisak, HS Panitch, G Shifroni, JS Wolinsky, and the COPAXONE® Study Group. Проспективное открытое исследование глатирамера ацетата: более десяти лет непрерывного использования для лечения рассеянного склероза Multiple Sclerosis 2006; 12: 309 -320
 10 лет эффективности Дизайн исследования § Оценка степени инвалидизации пациентов по шкале EDSS каждые 6 месяцев в клиническом центре § Пациенты, которые по какой-либо причине прекратили прием глатирамера ацетата (ГА), исключаются из исследования § Пациенты получают только монотерапию ГА § Длительное наблюдение (ДН) исключенных из исследования пациентов требует визитов в клинический центр для оценки неврологического статуса (EDSS) Ford et al. Mult Scler 2006; 12: 309 -20
10 лет эффективности Дизайн исследования § Оценка степени инвалидизации пациентов по шкале EDSS каждые 6 месяцев в клиническом центре § Пациенты, которые по какой-либо причине прекратили прием глатирамера ацетата (ГА), исключаются из исследования § Пациенты получают только монотерапию ГА § Длительное наблюдение (ДН) исключенных из исследования пациентов требует визитов в клинический центр для оценки неврологического статуса (EDSS) Ford et al. Mult Scler 2006; 12: 309 -20
 Дизайн длительного исследования ГА Ноябрь 2003 Оценка по шкале EDSS 3 6 9 12 15 18 21 24 27 30 33 36 Текущие оценки каждые 6 месяцев • Анализ данных пациентов, продолжающих терапию • ДН* выбывших пациентов Без перерыва (n=108) 10 лет Глатирамера ацетат m. ITT** (n=232) 6. 99 лет Плацебо 4. 26 лет Всего исключено (n=124) Двойная слепая, плацебоконтролируемая фаза 0 Дополнительная открытая фаза 35† Месяцы 60 50 возвратились для ДН 120+ *ДН – длительное наблюдение; **m. ITT – модифицированная популяция, Johnson et al. Neurology 1995; 45: 1268 -76. подлежащая лечению †В связи со сдвигом включения, длительность исследования составила Johnson et al. Neurology 1998; 50: 701 -8. Ford et al. Mult Scler 2006; 12: 309 -20. 35 мес. , чтобы добиться 2 -хлетнего периода терапии для всех пациентов. Средняя длительность терапии составила 30 месяцев.
Дизайн длительного исследования ГА Ноябрь 2003 Оценка по шкале EDSS 3 6 9 12 15 18 21 24 27 30 33 36 Текущие оценки каждые 6 месяцев • Анализ данных пациентов, продолжающих терапию • ДН* выбывших пациентов Без перерыва (n=108) 10 лет Глатирамера ацетат m. ITT** (n=232) 6. 99 лет Плацебо 4. 26 лет Всего исключено (n=124) Двойная слепая, плацебоконтролируемая фаза 0 Дополнительная открытая фаза 35† Месяцы 60 50 возвратились для ДН 120+ *ДН – длительное наблюдение; **m. ITT – модифицированная популяция, Johnson et al. Neurology 1995; 45: 1268 -76. подлежащая лечению †В связи со сдвигом включения, длительность исследования составила Johnson et al. Neurology 1998; 50: 701 -8. Ford et al. Mult Scler 2006; 12: 309 -20. 35 мес. , чтобы добиться 2 -хлетнего периода терапии для всех пациентов. Средняя длительность терапии составила 30 месяцев.
 10 лет эффективности Группы пациентов m. ITT N=232 Все пациенты, которые получили хотя бы 1 дозу ГА за время исследования. Модификация исходной рандомизированной популяции (N=251): не включены 19 пациентов, которые получали только плацебо Без перерыва N=108 Пациенты, которые не прерывали участие в исследовании (по определению, не прерывали терапию ГА) до момента окончания исследования в ноябре 2003 года: средняя длительность терапии 10. 1 лет (от 8 до 12 лет). Все выбывшие из исследования N=124 Все пациенты, которые получили по крайней мере 1 дозу ГА и выбыли из исследования до ноября 2003 года. ДН выбывших из исследования N=50 Пациенты, которые получили по крайней мере 1 дозу ГА и были исключены из исследования, но вернулись для длительного наблюдения ~ через 10 лет после начала исследования. Выбывшие без ДН N=74 Пациенты, которые были исключены из исследования и недоступны для длительного наблюдения. Ford et al. Mult Scler 2006; 12: 309 -20
10 лет эффективности Группы пациентов m. ITT N=232 Все пациенты, которые получили хотя бы 1 дозу ГА за время исследования. Модификация исходной рандомизированной популяции (N=251): не включены 19 пациентов, которые получали только плацебо Без перерыва N=108 Пациенты, которые не прерывали участие в исследовании (по определению, не прерывали терапию ГА) до момента окончания исследования в ноябре 2003 года: средняя длительность терапии 10. 1 лет (от 8 до 12 лет). Все выбывшие из исследования N=124 Все пациенты, которые получили по крайней мере 1 дозу ГА и выбыли из исследования до ноября 2003 года. ДН выбывших из исследования N=50 Пациенты, которые получили по крайней мере 1 дозу ГА и были исключены из исследования, но вернулись для длительного наблюдения ~ через 10 лет после начала исследования. Выбывшие без ДН N=74 Пациенты, которые были исключены из исследования и недоступны для длительного наблюдения. Ford et al. Mult Scler 2006; 12: 309 -20
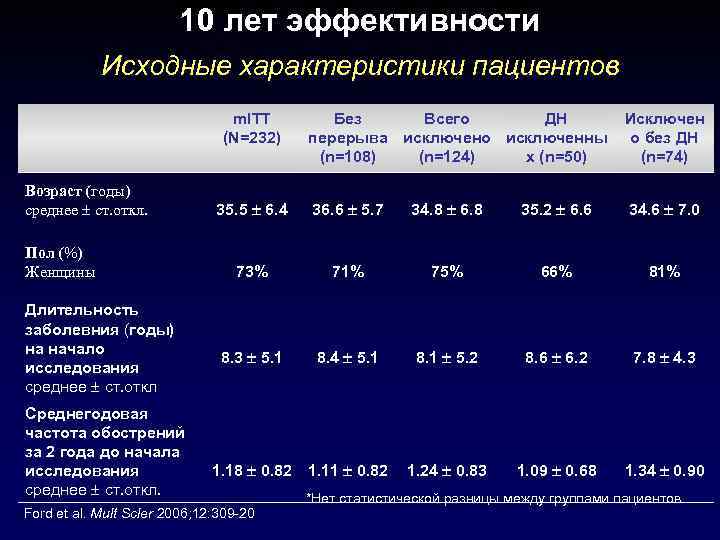 10 лет эффективности Исходные характеристики пациентов m. ITT (N=232) Возраст (годы) среднее ст. откл. Пол (%) Женщины Длительность заболевния (годы) на начало исследования среднее ст. откл Среднегодовая частота обострений за 2 года до начала исследования среднее ст. откл. Без Всего ДН перерыва исключено исключенны (n=108) (n=124) х (n=50) Исключен о без ДН (n=74) 35. 5 6. 4 36. 6 5. 7 34. 8 6. 8 35. 2 6. 6 34. 6 7. 0 73% 71% 75% 66% 81% 8. 3 5. 1 8. 4 5. 1 8. 1 5. 2 8. 6 6. 2 7. 8 4. 3 1. 18 0. 82 1. 11 0. 82 1. 24 0. 83 1. 09 0. 68 1. 34 0. 90 Ford et al. Mult Scler 2006; 12: 309 -20 *Нет статистической разницы между группами пациентов
10 лет эффективности Исходные характеристики пациентов m. ITT (N=232) Возраст (годы) среднее ст. откл. Пол (%) Женщины Длительность заболевния (годы) на начало исследования среднее ст. откл Среднегодовая частота обострений за 2 года до начала исследования среднее ст. откл. Без Всего ДН перерыва исключено исключенны (n=108) (n=124) х (n=50) Исключен о без ДН (n=74) 35. 5 6. 4 36. 6 5. 7 34. 8 6. 8 35. 2 6. 6 34. 6 7. 0 73% 71% 75% 66% 81% 8. 3 5. 1 8. 4 5. 1 8. 1 5. 2 8. 6 6. 2 7. 8 4. 3 1. 18 0. 82 1. 11 0. 82 1. 24 0. 83 1. 09 0. 68 1. 34 0. 90 Ford et al. Mult Scler 2006; 12: 309 -20 *Нет статистической разницы между группами пациентов
 10 лет эффективности Причины выбывания пациентов Причины выбывания N Решение пациента/ подкатегории* N (%) Всего 124 Всего 87 (100) Потерян контакт 14 Субъективное ухудшение состояния 27 (31) Побочные реакции 23 Желание сменить или комбинировать терапию 22 (25) Трудности, неспособность или нежелание придерживаться протокола исследования 30 (34) Решение пациента/другое 87 Беременность 8 (9) *Подкатегории определяются набором письменных комментариев, полученных при последних визитах, которые распределяются по группам на основании независимого анализа и консенсусного мнения 3 специалистов, участвующих в исследовании Ford et al. Mult Scler 2006; 12: 309 -20
10 лет эффективности Причины выбывания пациентов Причины выбывания N Решение пациента/ подкатегории* N (%) Всего 124 Всего 87 (100) Потерян контакт 14 Субъективное ухудшение состояния 27 (31) Побочные реакции 23 Желание сменить или комбинировать терапию 22 (25) Трудности, неспособность или нежелание придерживаться протокола исследования 30 (34) Решение пациента/другое 87 Беременность 8 (9) *Подкатегории определяются набором письменных комментариев, полученных при последних визитах, которые распределяются по группам на основании независимого анализа и консенсусного мнения 3 специалистов, участвующих в исследовании Ford et al. Mult Scler 2006; 12: 309 -20
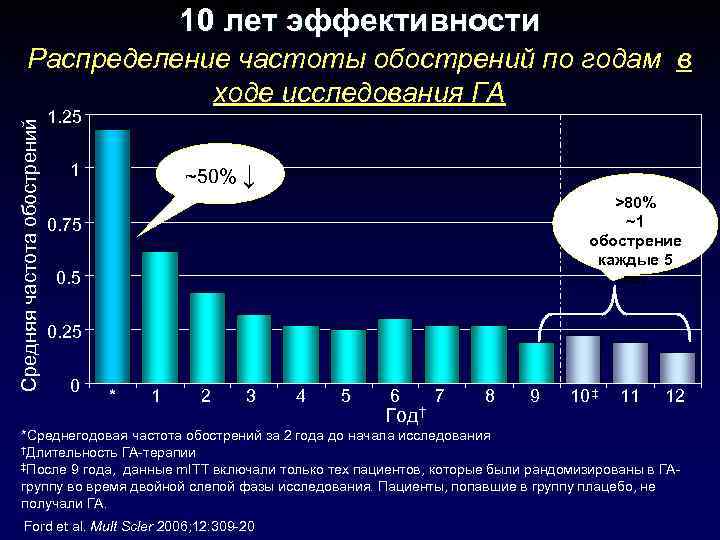 10 лет эффективности Средняя частота обострений Распределение частоты обострений по годам в ходе исследования ГА 1. 25 1 ~50% ↓ >80% ~1 обострение каждые 5 лет 0. 75 0. 25 0 ‡ * 1 2 3 4 5 6 7 8 9 10 11 12 Год† *Среднегодовая частота обострений за 2 года до начала исследования †Длительность ГА-терапии ‡После 9 года, данные m. ITТ включали только тех пациентов, которые были рандомизированы в ГАгруппу во время двойной слепой фазы исследования. Пациенты, попавшие в группу плацебо, не получали ГА. Ford et al. Mult Scler 2006; 12: 309 -20
10 лет эффективности Средняя частота обострений Распределение частоты обострений по годам в ходе исследования ГА 1. 25 1 ~50% ↓ >80% ~1 обострение каждые 5 лет 0. 75 0. 25 0 ‡ * 1 2 3 4 5 6 7 8 9 10 11 12 Год† *Среднегодовая частота обострений за 2 года до начала исследования †Длительность ГА-терапии ‡После 9 года, данные m. ITТ включали только тех пациентов, которые были рандомизированы в ГАгруппу во время двойной слепой фазы исследования. Пациенты, попавшие в группу плацебо, не получали ГА. Ford et al. Mult Scler 2006; 12: 309 -20
 10 лет эффективности Динамика EDSS в ходе исследования m. ITT (N=232) Без перерыва (n=108) Все выбывшие (n=124) 2. 79 + 1. 50 2. 50 0. 0 - 7. 0 2. 56 + 1. 35 2. 25 0. 0 - 6. 0 3. 00 1. 59 3. 00 0. 0 - 7. 0 Балл EDSS при последнем осмотре Среднее ст. откл. Медиана Разброс 3. 53 2. 08 3. 00 0. 0 – 9. 0 3. 06 1. 78 2. 50 0. 0 – 8. 0 3. 94 2. 25 3. 50 0. 0 – 9. 0 Динамика EDSS от начала ГАтерапии до момента последнего осмотра Среднее ст. откл. Медиана Разброс 0. 73 1. 66 0. 50 -3. 5 – 5. 5 0. 50 1. 65 0. 50 -3. 5 – 5. 5 0. 94 1. 65 0. 50 -3. 5 – 5. 5 В ходе исследования Исходный балл EDSS Среднее ст. откл. Медиана Разброс Ford et al. Mult Scler 2006; 12: 309 -20
10 лет эффективности Динамика EDSS в ходе исследования m. ITT (N=232) Без перерыва (n=108) Все выбывшие (n=124) 2. 79 + 1. 50 2. 50 0. 0 - 7. 0 2. 56 + 1. 35 2. 25 0. 0 - 6. 0 3. 00 1. 59 3. 00 0. 0 - 7. 0 Балл EDSS при последнем осмотре Среднее ст. откл. Медиана Разброс 3. 53 2. 08 3. 00 0. 0 – 9. 0 3. 06 1. 78 2. 50 0. 0 – 8. 0 3. 94 2. 25 3. 50 0. 0 – 9. 0 Динамика EDSS от начала ГАтерапии до момента последнего осмотра Среднее ст. откл. Медиана Разброс 0. 73 1. 66 0. 50 -3. 5 – 5. 5 0. 50 1. 65 0. 50 -3. 5 – 5. 5 0. 94 1. 65 0. 50 -3. 5 – 5. 5 В ходе исследования Исходный балл EDSS Среднее ст. откл. Медиана Разброс Ford et al. Mult Scler 2006; 12: 309 -20
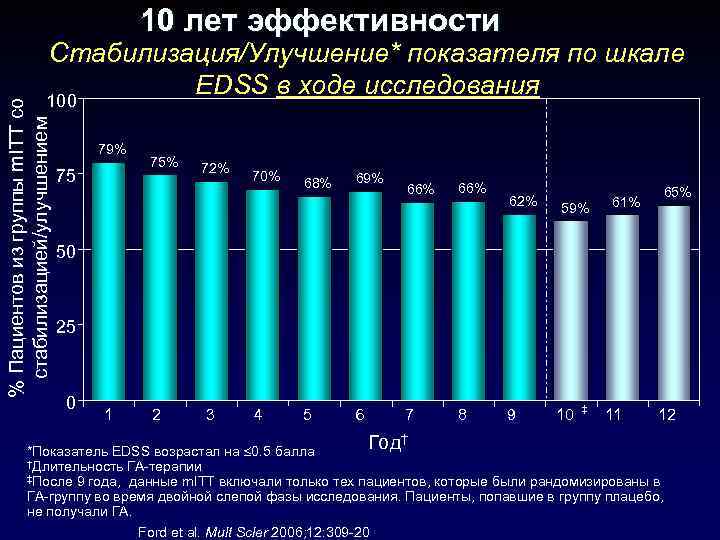 10 лет эффективности % Пациентов из группы m. ITT со стабилизацией/улучшением Стабилизация/Улучшение* показателя по шкале EDSS в ходе исследования 100 79% 75 75% 72% 70% 68% 69% 66% 62% 59% 61% 65% 50 25 0 ‡ 1 2 3 4 5 6 7 8 9 10 11 12 Год *Показатель EDSS возрастал на 0. 5 балла †Длительность ГА-терапии ‡После 9 года, данные m. ITТ включали только тех пациентов, которые были рандомизированы в ГА-группу во время двойной слепой фазы исследования. Пациенты, попавшие в группу плацебо, не получали ГА. Ford et al. Mult Scler 2006; 12: 309 -20 †
10 лет эффективности % Пациентов из группы m. ITT со стабилизацией/улучшением Стабилизация/Улучшение* показателя по шкале EDSS в ходе исследования 100 79% 75 75% 72% 70% 68% 69% 66% 62% 59% 61% 65% 50 25 0 ‡ 1 2 3 4 5 6 7 8 9 10 11 12 Год *Показатель EDSS возрастал на 0. 5 балла †Длительность ГА-терапии ‡После 9 года, данные m. ITТ включали только тех пациентов, которые были рандомизированы в ГА-группу во время двойной слепой фазы исследования. Пациенты, попавшие в группу плацебо, не получали ГА. Ford et al. Mult Scler 2006; 12: 309 -20 †
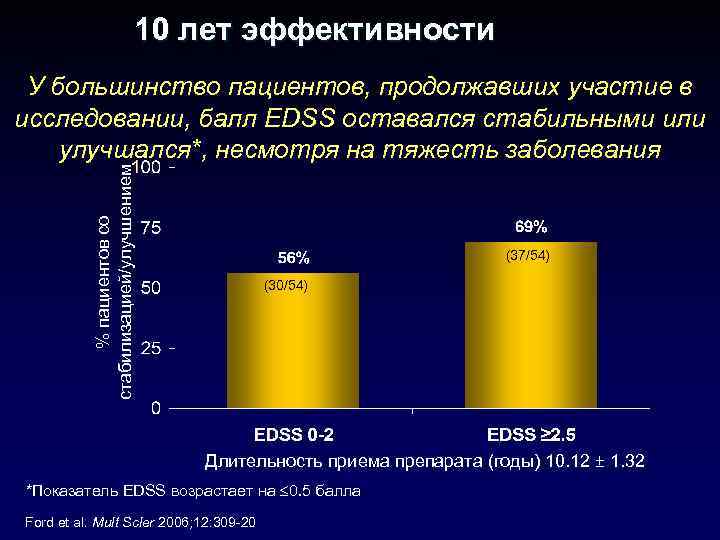 10 лет эффективности % пациентов со стабилизацией/улучшением У большинство пациентов, продолжавших участие в исследовании, балл EDSS оставался стабильными или улучшался*, несмотря на тяжесть заболевания (37/54) (30/54) Длительность приема препарата (годы) 10. 12 ± 1. 32 *Показатель EDSS возрастает на 0. 5 балла Ford et al. Mult Scler 2006; 12: 309 -20
10 лет эффективности % пациентов со стабилизацией/улучшением У большинство пациентов, продолжавших участие в исследовании, балл EDSS оставался стабильными или улучшался*, несмотря на тяжесть заболевания (37/54) (30/54) Длительность приема препарата (годы) 10. 12 ± 1. 32 *Показатель EDSS возрастает на 0. 5 балла Ford et al. Mult Scler 2006; 12: 309 -20
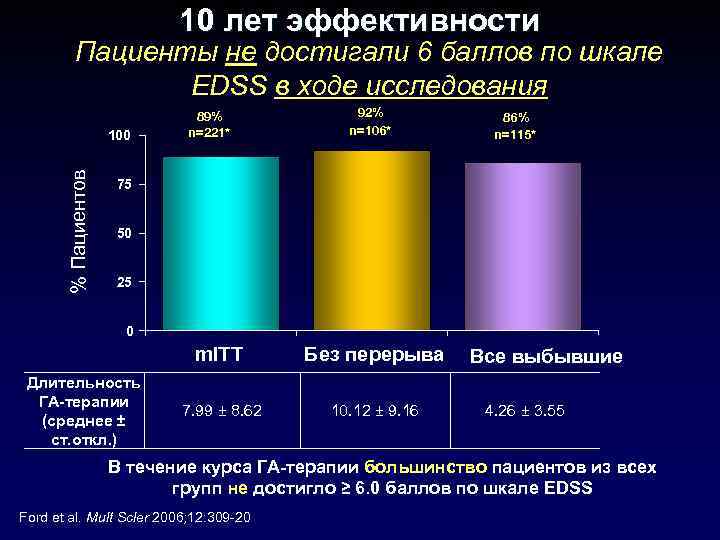 10 лет эффективности Пациенты не достигали 6 баллов по шкале EDSS в ходе исследования % Пациентов 100 89% n=221* 92% n=106* 86% n=115* 75 50 25 0 m. ITT Длительность ГА-терапии (среднее ± ст. откл. ) 7. 99 ± 8. 62 Без перерыва Все выбывшие 10. 12 ± 9. 16 4. 26 ± 3. 55 В течение курса ГА-терапии большинство пациентов из всех групп не достигло ≥ 6. 0 баллов по шкале EDSS Ford et al. Mult Scler 2006; 12: 309 -20
10 лет эффективности Пациенты не достигали 6 баллов по шкале EDSS в ходе исследования % Пациентов 100 89% n=221* 92% n=106* 86% n=115* 75 50 25 0 m. ITT Длительность ГА-терапии (среднее ± ст. откл. ) 7. 99 ± 8. 62 Без перерыва Все выбывшие 10. 12 ± 9. 16 4. 26 ± 3. 55 В течение курса ГА-терапии большинство пациентов из всех групп не достигло ≥ 6. 0 баллов по шкале EDSS Ford et al. Mult Scler 2006; 12: 309 -20
 10 лет эффективности Состояние продолжающих лечение и выбывших из исследования пациентов на отдаленном катамнестическом визите через 10 лет EDSS Балл по шкале EDSS через 10 лет при ДН Среднее ст. откл. Медиана Разброс Динамика EDSS от исходного уровня Среднее ст. откл. Медиана Разброс Без перерыва n=108 ДН исключенных n=50 р 3. 06 1. 78 2. 50 0. 0 – 8. 0 5. 22 2. 21* 6. 00 1. 0 – 9. 0 <0. 0001† 0. 50 1. 65 0. 50 -3. 5 – 5. 5 2. 24 1. 86 2. 25 3. 0 – 5. 5 <0. 0001† *Показатели по шкале EDSS не были подтверждены через 6 месяцев от начала ДН, включавшего только один визит †Ковариационный анализ (ANCOVA) балла EDSS, скорректированного к исходным значениям Ford et al. Mult Scler 2006; 12: 309 -20
10 лет эффективности Состояние продолжающих лечение и выбывших из исследования пациентов на отдаленном катамнестическом визите через 10 лет EDSS Балл по шкале EDSS через 10 лет при ДН Среднее ст. откл. Медиана Разброс Динамика EDSS от исходного уровня Среднее ст. откл. Медиана Разброс Без перерыва n=108 ДН исключенных n=50 р 3. 06 1. 78 2. 50 0. 0 – 8. 0 5. 22 2. 21* 6. 00 1. 0 – 9. 0 <0. 0001† 0. 50 1. 65 0. 50 -3. 5 – 5. 5 2. 24 1. 86 2. 25 3. 0 – 5. 5 <0. 0001† *Показатели по шкале EDSS не были подтверждены через 6 месяцев от начала ДН, включавшего только один визит †Ковариационный анализ (ANCOVA) балла EDSS, скорректированного к исходным значениям Ford et al. Mult Scler 2006; 12: 309 -20
 10 лет эффективности Состояние продолжающих лечение и выбывших из исследования пациентов на отдаленном катамнестическом визите через 10 лет EDSS Без перерыва n=108 ДН исключенных n=50 р Доля пациентов, достигших 4, 6 или 8 баллов по шкале EDSS 4 (%) 24% 68% <0. 0001† EDSS 6 (%) 8% 50% <0. 0001† EDSS 8 (%) 1% 10% <0. 0125‡ *Показатели по шкале EDSS не были подтверждены через 6 месяцев от начала ДН, включавшего только один визит † Критерий хи-квадрат ( 2) ‡ Точный критерий Фишера Ford et al. Mult Scler 2006; 12: 309 -20
10 лет эффективности Состояние продолжающих лечение и выбывших из исследования пациентов на отдаленном катамнестическом визите через 10 лет EDSS Без перерыва n=108 ДН исключенных n=50 р Доля пациентов, достигших 4, 6 или 8 баллов по шкале EDSS 4 (%) 24% 68% <0. 0001† EDSS 6 (%) 8% 50% <0. 0001† EDSS 8 (%) 1% 10% <0. 0125‡ *Показатели по шкале EDSS не были подтверждены через 6 месяцев от начала ДН, включавшего только один визит † Критерий хи-квадрат ( 2) ‡ Точный критерий Фишера Ford et al. Mult Scler 2006; 12: 309 -20
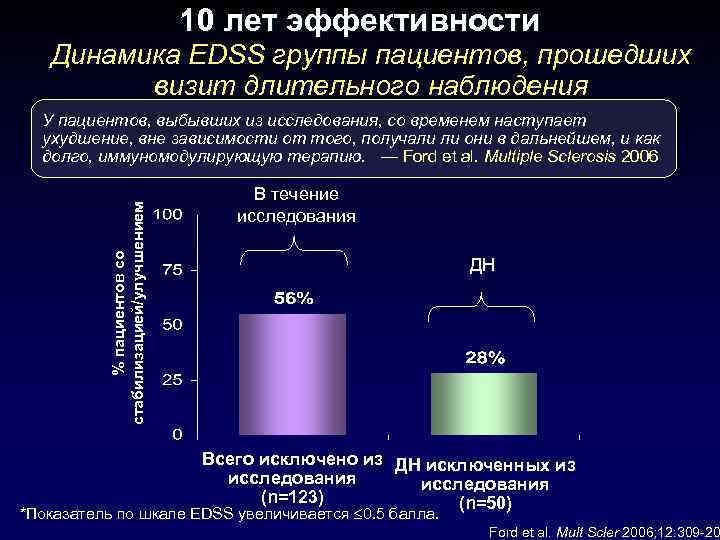 10 лет эффективности Динамика EDSS группы пациентов, прошедших визит длительного наблюдения % пациентов со стабилизацией/улучшением У пациентов, выбывших из исследования, со временем наступает ухудшение, вне зависимости от того, получали ли они в дальнейшем, и как долго, иммуномодулирующую терапию. — Ford et al. Multiple Sclerosis 2006 В течение исследования ДН Всего исключено из ДН исключенных из исследования (n=123) (n=50) *Показатель по шкале EDSS увеличивается 0. 5 балла. Ford et al. Mult Scler 2006; 12: 309 -20
10 лет эффективности Динамика EDSS группы пациентов, прошедших визит длительного наблюдения % пациентов со стабилизацией/улучшением У пациентов, выбывших из исследования, со временем наступает ухудшение, вне зависимости от того, получали ли они в дальнейшем, и как долго, иммуномодулирующую терапию. — Ford et al. Multiple Sclerosis 2006 В течение исследования ДН Всего исключено из ДН исключенных из исследования (n=123) (n=50) *Показатель по шкале EDSS увеличивается 0. 5 балла. Ford et al. Mult Scler 2006; 12: 309 -20
 10 лет эффективности Лекарственные препараты, которые получали пациенты, выбывшие из исследования После выбывания: § По имеющимся сведениям, 4 не получали никаких препаратов § Нет данных о 8 пациентах § По имеющимся данным, 38 пациентов получали следующие препараты: – 13 пациентов получали ГА – 32 пациента получал интерфероны – 14 пациентов получали иммуносупрессорные препараты (митоксантрон, метотрексат, азатиоприн, циклофосфамид) Во время длительного наблюдения § 10 пациентов получали ГА § 16 пациентов получали интерфероны § 4 пациентов получали иммуносупрессорные препараты (митоксантрон, метотрексат) Ford et al. Mult Scler 2006; 12: 309 -20
10 лет эффективности Лекарственные препараты, которые получали пациенты, выбывшие из исследования После выбывания: § По имеющимся сведениям, 4 не получали никаких препаратов § Нет данных о 8 пациентах § По имеющимся данным, 38 пациентов получали следующие препараты: – 13 пациентов получали ГА – 32 пациента получал интерфероны – 14 пациентов получали иммуносупрессорные препараты (митоксантрон, метотрексат, азатиоприн, циклофосфамид) Во время длительного наблюдения § 10 пациентов получали ГА § 16 пациентов получали интерфероны § 4 пациентов получали иммуносупрессорные препараты (митоксантрон, метотрексат) Ford et al. Mult Scler 2006; 12: 309 -20
 10 лет эффективности Обзор ключевых моментов • Проспективное исследование различных методов лечения РРС длительностью свыше 5 лет, в течение которых каждые 6 месяцев оценивался неврологический статус и безопасность • Частота обострений снижалась более чем на 80% за 10 лет, соответственно, не возрастал показатель по шкале EDSS – равносильно 1 обострению за 5 лет • Через 10 и более лет непрерывной ГА терапии 92% пациентов сохранили способность самостоятельно передвигаться • У большинства пациентов показатель по шкале EDSS оставался стабильным или улучшался (возрастал менее, чем на 0. 5 балла) в ходе ГА терапии • Глатирамера ацетат хорошо переносился в течение всего исследования Ford et al. Mult Scler 2006; 12: 309 -20
10 лет эффективности Обзор ключевых моментов • Проспективное исследование различных методов лечения РРС длительностью свыше 5 лет, в течение которых каждые 6 месяцев оценивался неврологический статус и безопасность • Частота обострений снижалась более чем на 80% за 10 лет, соответственно, не возрастал показатель по шкале EDSS – равносильно 1 обострению за 5 лет • Через 10 и более лет непрерывной ГА терапии 92% пациентов сохранили способность самостоятельно передвигаться • У большинства пациентов показатель по шкале EDSS оставался стабильным или улучшался (возрастал менее, чем на 0. 5 балла) в ходе ГА терапии • Глатирамера ацетат хорошо переносился в течение всего исследования Ford et al. Mult Scler 2006; 12: 309 -20
 Благоприятные показатели безопасности ГА терапии сохранялись при длительном применении § Наиболее часто в течение исследования встречались следующие побочные эффекты: § Локальные реакции в месте введения § Непосредственная реакция на введение (IPIR) по имеющимся сведениям, частота появления побочных реакций со временем убывала § Не было обнаружено связи между долговременным применением ГА и возникновением каких-либо иных иммунно-опосредованных расстройств, инфекционных заболеваний или злокачественных новообразований. Желание больных РРС продолжать самостоятельное ежедневное подкожное введение ГА в течение более чем десятилетия характеризует великолепную переносимость этого препарата — Ford et al. Multiple Sclerosis 2006 12: 309 -20 Ford et al. Mult Scler 2006; 12: 309 -20
Благоприятные показатели безопасности ГА терапии сохранялись при длительном применении § Наиболее часто в течение исследования встречались следующие побочные эффекты: § Локальные реакции в месте введения § Непосредственная реакция на введение (IPIR) по имеющимся сведениям, частота появления побочных реакций со временем убывала § Не было обнаружено связи между долговременным применением ГА и возникновением каких-либо иных иммунно-опосредованных расстройств, инфекционных заболеваний или злокачественных новообразований. Желание больных РРС продолжать самостоятельное ежедневное подкожное введение ГА в течение более чем десятилетия характеризует великолепную переносимость этого препарата — Ford et al. Multiple Sclerosis 2006 12: 309 -20 Ford et al. Mult Scler 2006; 12: 309 -20
 Проспективное наблюдение эффективности После базового исследования ГА ГА (Копаксон®, Teva) 12+ лет 0 1 2 3 4 5 6 7 n=251; 125 Копаксон®, 126 плацебо, 19 пациентов группы плацебо из 251 в базовом исследовании не были включены в открытую фазу исследованияf (125 Копаксон® по рандомизации/107 плацебо -активный контроль) [Ford CC, Mult Scler 2006 12: 309 -20] n=372; 125 Бетаферон® 1. 6 млн. МЕ, 124 Бетаферон® 8 млн. МЕ, 123 плацебо [IFNß Study Group, Neurology 1995 45: 1277 -85] IFN -1 a п/к (Ребиф®, Serono): 4 года n=560; 184 Ребиф® 44 мкг, 189 Ребиф® 22 мкг, 187 плацебо; на начало 3 года, 172 пациента группы плацебо рандомизировано в группы активной терапии 22 мкг (n=85) или 44 мкг (n=87); далее в каждой группе активной терапии было по 167 пациентов [PRISMS Study Group Neurology 2001; 56: 1628 -36] 57%* 2 года 1. 3%* 5 лет 77%* 4 года Натализумаб (Тисабри®, Elan): 2 года Монотерапевтическое исследование: n=942; Тисабри® 300 мг (n=627) или плацебо (n=315) [Polman CH, N Engl J Med. 2006; 354: 899 -910] *Доля пациентов, полностью прошедших исследование 9 10 11 12 13 43%* IFN -1 a в/м (Авонекс®, Biogen): 2 года n=301; 158 Авонекс®, 143 плацебо; субпопуляция (85 Авонекс®, 87 плацебо) пациентов, участвовавших в исследовании в течение 2 -х лет [Jacobs LD, Ann Neurol 1996 39: 285 -94] IFN -1 a п/к (Бетаферон®, Schering): 5 лет 8 91%* 2 года 12+ лет
Проспективное наблюдение эффективности После базового исследования ГА ГА (Копаксон®, Teva) 12+ лет 0 1 2 3 4 5 6 7 n=251; 125 Копаксон®, 126 плацебо, 19 пациентов группы плацебо из 251 в базовом исследовании не были включены в открытую фазу исследованияf (125 Копаксон® по рандомизации/107 плацебо -активный контроль) [Ford CC, Mult Scler 2006 12: 309 -20] n=372; 125 Бетаферон® 1. 6 млн. МЕ, 124 Бетаферон® 8 млн. МЕ, 123 плацебо [IFNß Study Group, Neurology 1995 45: 1277 -85] IFN -1 a п/к (Ребиф®, Serono): 4 года n=560; 184 Ребиф® 44 мкг, 189 Ребиф® 22 мкг, 187 плацебо; на начало 3 года, 172 пациента группы плацебо рандомизировано в группы активной терапии 22 мкг (n=85) или 44 мкг (n=87); далее в каждой группе активной терапии было по 167 пациентов [PRISMS Study Group Neurology 2001; 56: 1628 -36] 57%* 2 года 1. 3%* 5 лет 77%* 4 года Натализумаб (Тисабри®, Elan): 2 года Монотерапевтическое исследование: n=942; Тисабри® 300 мг (n=627) или плацебо (n=315) [Polman CH, N Engl J Med. 2006; 354: 899 -910] *Доля пациентов, полностью прошедших исследование 9 10 11 12 13 43%* IFN -1 a в/м (Авонекс®, Biogen): 2 года n=301; 158 Авонекс®, 143 плацебо; субпопуляция (85 Авонекс®, 87 плацебо) пациентов, участвовавших в исследовании в течение 2 -х лет [Jacobs LD, Ann Neurol 1996 39: 285 -94] IFN -1 a п/к (Бетаферон®, Schering): 5 лет 8 91%* 2 года 12+ лет
 Данные долговременного наблюдения при РРС Сравнение дизайнов исследований Дизайн исследования ГА 1 (Копаксон®, Teva) • Проспективное непрерывное исследование длительностью 15 лет • Клинические и лабораторные обследования каждые 6 месяцев IFN -1 a п/к 2 (Ребиф®, Serono) • Ретроспективный анализ, не-непрерывная терапия • Изучение медицинских карт и один визит за 8 лет, с получением комплексной иммуномодулирующей INF терапии IFN -1 b п/к 3 (Бетаферон®, Schering) • Ретроспективный анализ, не-непрерывная терапия • Один визит в клинический центр после в среднем 10 лет терапии Бетафероном (>80% группы) IFN -1 a в/м 4 (Авонекс®, Biogen) • Ретроспективный анализ, не-непрерывная терапия • Один визит за 8 лет, с получением комплексной иммуномодулирующей INF терапии 1. Ford CC et al. Mult Scler 2006; 12: 309 -20 2. Paty DW et al. Mult Scler 2003; 9 (Supp 1): S 138 3. Ebers G et al. Neurology 2006; 66 (Supp 2): A 32 4. Fisher et al. Neurology 2002; 59: 1412 -1420.
Данные долговременного наблюдения при РРС Сравнение дизайнов исследований Дизайн исследования ГА 1 (Копаксон®, Teva) • Проспективное непрерывное исследование длительностью 15 лет • Клинические и лабораторные обследования каждые 6 месяцев IFN -1 a п/к 2 (Ребиф®, Serono) • Ретроспективный анализ, не-непрерывная терапия • Изучение медицинских карт и один визит за 8 лет, с получением комплексной иммуномодулирующей INF терапии IFN -1 b п/к 3 (Бетаферон®, Schering) • Ретроспективный анализ, не-непрерывная терапия • Один визит в клинический центр после в среднем 10 лет терапии Бетафероном (>80% группы) IFN -1 a в/м 4 (Авонекс®, Biogen) • Ретроспективный анализ, не-непрерывная терапия • Один визит за 8 лет, с получением комплексной иммуномодулирующей INF терапии 1. Ford CC et al. Mult Scler 2006; 12: 309 -20 2. Paty DW et al. Mult Scler 2003; 9 (Supp 1): S 138 3. Ebers G et al. Neurology 2006; 66 (Supp 2): A 32 4. Fisher et al. Neurology 2002; 59: 1412 -1420.
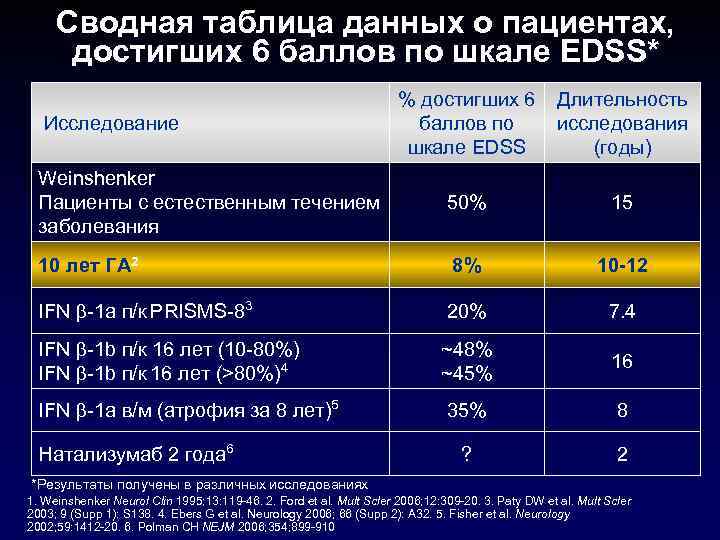 Сводная таблица данных о пациентах, достигших 6 баллов по шкале EDSS* Исследование % достигших 6 Длительность баллов по исследования шкале EDSS (годы) Weinshenker Пациенты с естественным течением заболевания 50% 15 10 лет ГА 2 8% 10 -12 IFN -1 a п/к PRISMS-83 20% 7. 4 IFN -1 b п/к 16 лет (10 -80%) IFN -1 b п/к 16 лет (>80%)4 ~48% ~45% 16 IFN -1 a в/м (атрофия за 8 лет)5 35% 8 ? 2 Натализумаб 2 года 6 *Результаты получены в различных исследованиях 1. Weinshenker Neurol Clin 1995; 13: 119 -46. 2. Ford et al. Mult Scler 2006; 12: 309 -20. 3. Paty DW et al. Mult Scler 2003; 9 (Supp 1): S 138. 4. Ebers G et al. Neurology 2006; 66 (Supp 2): A 32. 5. Fisher et al. Neurology 2002; 59: 1412 -20. 6. Polman CH NEJM 2006; 354; 899 -910
Сводная таблица данных о пациентах, достигших 6 баллов по шкале EDSS* Исследование % достигших 6 Длительность баллов по исследования шкале EDSS (годы) Weinshenker Пациенты с естественным течением заболевания 50% 15 10 лет ГА 2 8% 10 -12 IFN -1 a п/к PRISMS-83 20% 7. 4 IFN -1 b п/к 16 лет (10 -80%) IFN -1 b п/к 16 лет (>80%)4 ~48% ~45% 16 IFN -1 a в/м (атрофия за 8 лет)5 35% 8 ? 2 Натализумаб 2 года 6 *Результаты получены в различных исследованиях 1. Weinshenker Neurol Clin 1995; 13: 119 -46. 2. Ford et al. Mult Scler 2006; 12: 309 -20. 3. Paty DW et al. Mult Scler 2003; 9 (Supp 1): S 138. 4. Ebers G et al. Neurology 2006; 66 (Supp 2): A 32. 5. Fisher et al. Neurology 2002; 59: 1412 -20. 6. Polman CH NEJM 2006; 354; 899 -910
 Длительное (до 26 лет), открытое, благотворительное исследование влияния ГА на течение ремиттирующего рассеянного склероза THANKS! Miller A. et al. Mult Scler 2005 11(Supp 1): S 84
Длительное (до 26 лет), открытое, благотворительное исследование влияния ГА на течение ремиттирующего рассеянного склероза THANKS! Miller A. et al. Mult Scler 2005 11(Supp 1): S 84
 Длительное наблюдение в исследовании Miller: 26 лет • 46 больных РРС начали лечение ГА, некоторые в 1978 г. в рамках благотворительного исследования, некоторые после исследования Bornstein – 18 пациентов продолжают терапию до настоящего времени – 28 пациентов прервали участие • У оставшихся 18 пациентов – Средняя продолжительность заболевания 24 года – Средняя продолжительность лечения 17 лет • Частота обострений за год снизилась на 97%, с 3. 06 до 0. 09 обострений в год • Показатель по шкале EDSS вырос от 2. 6 балла всего лишь до 3. 1 балла Miller A. et al. Mult Scler 2005 11(Supp 1): S 84
Длительное наблюдение в исследовании Miller: 26 лет • 46 больных РРС начали лечение ГА, некоторые в 1978 г. в рамках благотворительного исследования, некоторые после исследования Bornstein – 18 пациентов продолжают терапию до настоящего времени – 28 пациентов прервали участие • У оставшихся 18 пациентов – Средняя продолжительность заболевания 24 года – Средняя продолжительность лечения 17 лет • Частота обострений за год снизилась на 97%, с 3. 06 до 0. 09 обострений в год • Показатель по шкале EDSS вырос от 2. 6 балла всего лишь до 3. 1 балла Miller A. et al. Mult Scler 2005 11(Supp 1): S 84
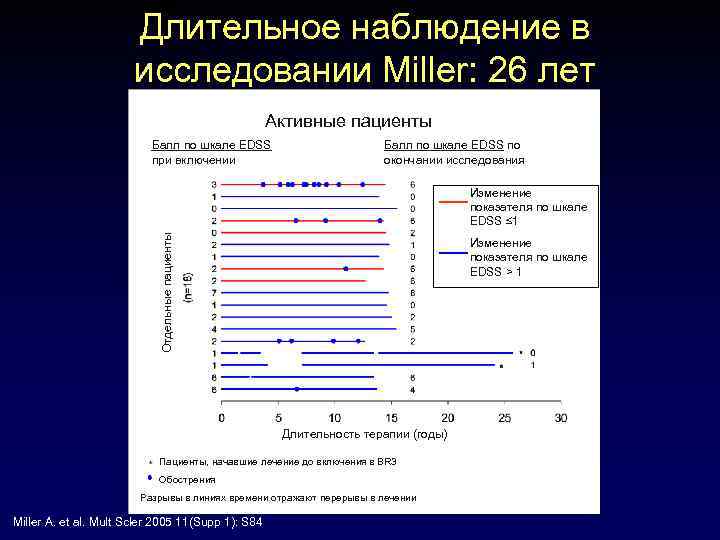 Длительное наблюдение в исследовании Miller: 26 лет Активные пациенты Балл по шкале EDSS при включении Балл по шкале EDSS по окончании исследования Отдельные пациенты Изменение показателя по шкале EDSS ≤ 1 Изменение показателя по шкале EDSS > 1 Длительность терапии (годы) Пациенты, начавшие лечение до включения в BR 3 Обострения Разрывы в линиях времени отражают перерывы в лечении Miller A. et al. Mult Scler 2005 11(Supp 1): S 84
Длительное наблюдение в исследовании Miller: 26 лет Активные пациенты Балл по шкале EDSS при включении Балл по шкале EDSS по окончании исследования Отдельные пациенты Изменение показателя по шкале EDSS ≤ 1 Изменение показателя по шкале EDSS > 1 Длительность терапии (годы) Пациенты, начавшие лечение до включения в BR 3 Обострения Разрывы в линиях времени отражают перерывы в лечении Miller A. et al. Mult Scler 2005 11(Supp 1): S 84
 Заключение • Копаксон обладает двойным механизмом действия: он вызывает мощный Th 2 -сдвиг и в то же время оказывает непосредственное нейропротективное действие в ЦНС • Эти свойства подтверждаются стойкостью благоприятных клинических эффектов применения Копаксона в течение 10 лет – наиболее долгое из всех клинических исследований РС • Будущие стратегии лечения должны уделять наибольшее внимание минимизации повреждения аксонов и процессов, ведущих к разрушению тканей ЦНС • Применение Копаксона на ранней стадии заболевания является наиболее рациональным способом минимизации длительной инвалидизации при РС
Заключение • Копаксон обладает двойным механизмом действия: он вызывает мощный Th 2 -сдвиг и в то же время оказывает непосредственное нейропротективное действие в ЦНС • Эти свойства подтверждаются стойкостью благоприятных клинических эффектов применения Копаксона в течение 10 лет – наиболее долгое из всех клинических исследований РС • Будущие стратегии лечения должны уделять наибольшее внимание минимизации повреждения аксонов и процессов, ведущих к разрушению тканей ЦНС • Применение Копаксона на ранней стадии заболевания является наиболее рациональным способом минимизации длительной инвалидизации при РС



