Лекция 10 клеточная инженерия.ppt
- Количество слайдов: 55
 Клеточная и тканевая инженерия o o o Клеточная инженерия основана на использовании принципиально нового биообъекта – изолированной культуры клеток или тканей. Клеточная инженерия позволяет выделять и культивировать ткани и клетки высших многоклеточных организмов (животных, человека и растений). Культивирование тканей и клеток происходит вне организма – in vitro
Клеточная и тканевая инженерия o o o Клеточная инженерия основана на использовании принципиально нового биообъекта – изолированной культуры клеток или тканей. Клеточная инженерия позволяет выделять и культивировать ткани и клетки высших многоклеточных организмов (животных, человека и растений). Культивирование тканей и клеток происходит вне организма – in vitro
 Культура клеток и тканей. Краткая история предмета o o Идея о возможности культивирования клеток вне организма впервые была высказана в конце прошлого столетия, но первые культуры клеток животных были получены в начале нашего века Культивирование растительных клеток на искусственных питательных средах долгое время не удавалось. Лишь в 30 -е годы были достигнуты первые успехи в этой области, которые и обеспечили бурный расцвет данного направления.
Культура клеток и тканей. Краткая история предмета o o Идея о возможности культивирования клеток вне организма впервые была высказана в конце прошлого столетия, но первые культуры клеток животных были получены в начале нашего века Культивирование растительных клеток на искусственных питательных средах долгое время не удавалось. Лишь в 30 -е годы были достигнуты первые успехи в этой области, которые и обеспечили бурный расцвет данного направления.
 Культура клеток и тканей. Краткая история предмета o 1 этап (1892 -1902 гг. ) первые попытки стимуляции роста растительных тканей и органов на фильтровальной бумаге, пропитанной сахарозой (Х. Фехтинг и К. Рехингер, Германия)
Культура клеток и тканей. Краткая история предмета o 1 этап (1892 -1902 гг. ) первые попытки стимуляции роста растительных тканей и органов на фильтровальной бумаге, пропитанной сахарозой (Х. Фехтинг и К. Рехингер, Германия)
 Культура клеток и тканей. Краткая история предмета o o 2 этап. (1902 – 1922 гг. ) создание первых питательных сред для культивирования тканей животных с использованием плазмы крови и зародышевой жидкости. Первые успешные опыты по культуре ткани осуществил в 1907 Р. Гаррисон (США), поместив в каплю лимфы кусочек зачатка нервной системы зародыша лягушки. Клетки зачатка оставались живыми несколько недель, из них вырастали нервные волокна.
Культура клеток и тканей. Краткая история предмета o o 2 этап. (1902 – 1922 гг. ) создание первых питательных сред для культивирования тканей животных с использованием плазмы крови и зародышевой жидкости. Первые успешные опыты по культуре ткани осуществил в 1907 Р. Гаррисон (США), поместив в каплю лимфы кусочек зачатка нервной системы зародыша лягушки. Клетки зачатка оставались живыми несколько недель, из них вырастали нервные волокна.
 Культура клеток и тканей. Краткая история предмета o 3 этап (1922 -1932 гг. ) начало культивирования изолированных тканей корней растений. В Роббинс, США и В. Котте, Германия показали возможность выращивания меристем кончиков корней томатов и кукурузы на синтетической питательной среде. Однако через определенное время растительные ткани бурели и погибали.
Культура клеток и тканей. Краткая история предмета o 3 этап (1922 -1932 гг. ) начало культивирования изолированных тканей корней растений. В Роббинс, США и В. Котте, Германия показали возможность выращивания меристем кончиков корней томатов и кукурузы на синтетической питательной среде. Однако через определенное время растительные ткани бурели и погибали.
 Культура клеток и тканей. Краткая история предмета o 4 этап (1932 -1940 гг. ) подлинное развитие метода культуры растительных тканей. Р. Готре, Франция и Ф. Уайт, США показали, что при периодической пересадке на свежую питательную среду кончики корней могут расти неограниченно долго. Были разработаны методы культивирования новых объектов - тканей древесных растений. Работы по культивированию тканей быстро развиваются, было успешно введено в культуру много новых объектов.
Культура клеток и тканей. Краткая история предмета o 4 этап (1932 -1940 гг. ) подлинное развитие метода культуры растительных тканей. Р. Готре, Франция и Ф. Уайт, США показали, что при периодической пересадке на свежую питательную среду кончики корней могут расти неограниченно долго. Были разработаны методы культивирования новых объектов - тканей древесных растений. Работы по культивированию тканей быстро развиваются, было успешно введено в культуру много новых объектов.
 Культура клеток и тканей. Краткая история предмета o o 5 этап (1940 -1960 гг. ) появление методов гормональной регуляции деления клеток растительной ткани. В 1959 г. был предложен метод выращивания большой массы клеточных суспензий. Существенный сдвиг также произошёл в связи с установлением возможности культивирования клеточной взвеси, получаемой из любой ткани под воздействием протеолитического фермента трипсина, растворяющего межклеточное вещество. Для клеточных культур начали использовать синтетическую жидкую питательную среду, содержащая физиологический раствор, 12 аминокислот, витамины, глюкозу и, как правило, сыворотку крови (2— 10%). Обязательно добавление к этой среде антибиотиков — пенициллина и стрептомицина.
Культура клеток и тканей. Краткая история предмета o o 5 этап (1940 -1960 гг. ) появление методов гормональной регуляции деления клеток растительной ткани. В 1959 г. был предложен метод выращивания большой массы клеточных суспензий. Существенный сдвиг также произошёл в связи с установлением возможности культивирования клеточной взвеси, получаемой из любой ткани под воздействием протеолитического фермента трипсина, растворяющего межклеточное вещество. Для клеточных культур начали использовать синтетическую жидкую питательную среду, содержащая физиологический раствор, 12 аминокислот, витамины, глюкозу и, как правило, сыворотку крови (2— 10%). Обязательно добавление к этой среде антибиотиков — пенициллина и стрептомицина.
 Культура клеток и тканей. Краткая история предмета 6 этап (1960 -1975 гг. ). Получение и культивирование и искусственное слияние протопластов (Коккинг и Пауэр, 1970 г. ). Разработка метода клонального микроразмножения растений in vitrо (Ж. Морель). Получение оздоровленного материала орхидей и картофеля. o
Культура клеток и тканей. Краткая история предмета 6 этап (1960 -1975 гг. ). Получение и культивирование и искусственное слияние протопластов (Коккинг и Пауэр, 1970 г. ). Разработка метода клонального микроразмножения растений in vitrо (Ж. Морель). Получение оздоровленного материала орхидей и картофеля. o
 Культура клеток и тканей. Краткая история предмета o o 7 этап (1975 г. – настоящее время) С помощью метода генетической инженерии разработан эффективный метод переноса генов двудольных растений.
Культура клеток и тканей. Краткая история предмета o o 7 этап (1975 г. – настоящее время) С помощью метода генетической инженерии разработан эффективный метод переноса генов двудольных растений.
 Основные направления исследований клеточной биотехнологии растений. o o o Использование изолированных клеток в селекции растений in vitro Использование культуры изолированных тканей для размножения и оздоровления посадочного материала Использование способности изолированных растительных клеток продуцировать ценные для медицины, парфюмерии и косметики вторичные метаболиты (алкалоиды, стероиды, гликозиды, гормоны, эфирные масла и др. )
Основные направления исследований клеточной биотехнологии растений. o o o Использование изолированных клеток в селекции растений in vitro Использование культуры изолированных тканей для размножения и оздоровления посадочного материала Использование способности изолированных растительных клеток продуцировать ценные для медицины, парфюмерии и косметики вторичные метаболиты (алкалоиды, стероиды, гликозиды, гормоны, эфирные масла и др. )
 В зависимости от степени приспособления к условиям существования вне организма клеточные культуры делят на 3 категории: o o o Первичные культуры, которые могут быть получены практически из любого органа, однако даже при систематической смене питательной среды (пассажей) сохраняются лишь 20— 30 дней, а затем гибнут; Штаммы, получаемые в особых условиях из эмбриональных тканей человека и животных; их характерная черта — стабильность биологических свойств, в частности постоянство диплоидного набора хромосом; клетки сохраняются без изменения в течение 10— 12 мес. (до 50 пассажей); Стабильные линии, полностью адаптированные к существованию вне организма; их получают из нормальных и раковых тканей и размножают неограниченно долгое время.
В зависимости от степени приспособления к условиям существования вне организма клеточные культуры делят на 3 категории: o o o Первичные культуры, которые могут быть получены практически из любого органа, однако даже при систематической смене питательной среды (пассажей) сохраняются лишь 20— 30 дней, а затем гибнут; Штаммы, получаемые в особых условиях из эмбриональных тканей человека и животных; их характерная черта — стабильность биологических свойств, в частности постоянство диплоидного набора хромосом; клетки сохраняются без изменения в течение 10— 12 мес. (до 50 пассажей); Стабильные линии, полностью адаптированные к существованию вне организма; их получают из нормальных и раковых тканей и размножают неограниченно долгое время.
 Техника введения и культивирования изолированных клеток и тканей Стерильность o o o Необходимым условием работы с культурой изолированных тканей является соблюдение строгой стерильности. Богатая питательная среда – прекрасный субстрат для развития микроорганизмов Изолированные фрагменты (экспланты) легко поражаются микроорганизмами. Необходимо тщательно стерилизовать как эксплант, так и питательную среду. Все манипуляции с изолированными тканями проводят в стерильными инструментами в стерильных помещениях (ламинар-боксе)
Техника введения и культивирования изолированных клеток и тканей Стерильность o o o Необходимым условием работы с культурой изолированных тканей является соблюдение строгой стерильности. Богатая питательная среда – прекрасный субстрат для развития микроорганизмов Изолированные фрагменты (экспланты) легко поражаются микроорганизмами. Необходимо тщательно стерилизовать как эксплант, так и питательную среду. Все манипуляции с изолированными тканями проводят в стерильными инструментами в стерильных помещениях (ламинар-боксе)
 Техника введения и культивирования изолированных клеток и тканей Питательные среды o o o o Питательные среды для культивирования изолированных клеток и тканей должны включать в себя все необходимые макро- и микро- элементы Макроэлементы: азот, фосфор, калий, кальций, магний, сера, железо) Микроэлементы (бор, марганец, цинк, медь, молибден) Витамины Углеводы (сахароза или глюкоза) Гормоны или их синтетические аналоги (индукторы клеточных делений) Гидролизат казеина Аминокислоты
Техника введения и культивирования изолированных клеток и тканей Питательные среды o o o o Питательные среды для культивирования изолированных клеток и тканей должны включать в себя все необходимые макро- и микро- элементы Макроэлементы: азот, фосфор, калий, кальций, магний, сера, железо) Микроэлементы (бор, марганец, цинк, медь, молибден) Витамины Углеводы (сахароза или глюкоза) Гормоны или их синтетические аналоги (индукторы клеточных делений) Гидролизат казеина Аминокислоты
 Техника введения и культивирования изолированных клеток и тканей Ламинар-боксы o o o Стерильность обеспечивается с помощью бактериальных воздушных фильтров За 10 -20 минут до начала работы ламинар-бакс облучают ультрафиолетовыми лампами. Внутреннюю поверхность ламинара и все оборудование протирают 70% этанолом
Техника введения и культивирования изолированных клеток и тканей Ламинар-боксы o o o Стерильность обеспечивается с помощью бактериальных воздушных фильтров За 10 -20 минут до начала работы ламинар-бакс облучают ультрафиолетовыми лампами. Внутреннюю поверхность ламинара и все оборудование протирают 70% этанолом
 Техника введения и культивирования изолированных клеток и тканей o o Условия культивирования Освещение. Большинство калусных тканей получают в темноте или при рассеянном свете. Морфогенез ткани проводят на свету в климатической камере с учетом фотопериодизма. Оптимальная влажность 60 -70% Оптимальная температура 22 -25 град.
Техника введения и культивирования изолированных клеток и тканей o o Условия культивирования Освещение. Большинство калусных тканей получают в темноте или при рассеянном свете. Морфогенез ткани проводят на свету в климатической камере с учетом фотопериодизма. Оптимальная влажность 60 -70% Оптимальная температура 22 -25 град.
 Каллусная ткань o o o КАЛЛУС, каллюс (от лат. callus — мозоль), растительная ткань, образующаяся на поверхности ран в результате деления пограничных к ране. Каллусная ткань способствует зарастанию ран, срастанию прививок и т. д. В биотехнологии калусная ткань образуется в стерильной культуре на эксплантах Каллус - неорганизованные или недифференцированные клетки, способные дать начало целому растению.
Каллусная ткань o o o КАЛЛУС, каллюс (от лат. callus — мозоль), растительная ткань, образующаяся на поверхности ран в результате деления пограничных к ране. Каллусная ткань способствует зарастанию ран, срастанию прививок и т. д. В биотехнологии калусная ткань образуется в стерильной культуре на эксплантах Каллус - неорганизованные или недифференцированные клетки, способные дать начало целому растению.
 Каллусная ткань o o Каллусная ткань выполняет в растениях следующие функции: Защитные (изолирование мест повреждений, заживление ран) Запасание питательных веществ и синтез вторичных метаболитов (защита от заражений микроорганизмами) Способность к регенерации утраченных органов (корни, побеги).
Каллусная ткань o o Каллусная ткань выполняет в растениях следующие функции: Защитные (изолирование мест повреждений, заживление ран) Запасание питательных веществ и синтез вторичных метаболитов (защита от заражений микроорганизмами) Способность к регенерации утраченных органов (корни, побеги).
 Способы получения каллусной ткани o o o Каллусную ткань in vitro можно получить практически из любой ткани растения – стебля, корня, листа, лепестков, тычинок и др. Каллусная ткань аморфна и не имеет конкретной анатомической структуры. Обязательным условием дедифференцировки растительной клетки и превращения ее в каллусную является присутствие в питательной среде двух групп фитогормонов: ауксинов и цитокининов. Ауксины вызывают процесс дедифференцировки клетки. Цитокинины вызывают деление (пролиферацию) дедифференцированных клеток.
Способы получения каллусной ткани o o o Каллусную ткань in vitro можно получить практически из любой ткани растения – стебля, корня, листа, лепестков, тычинок и др. Каллусная ткань аморфна и не имеет конкретной анатомической структуры. Обязательным условием дедифференцировки растительной клетки и превращения ее в каллусную является присутствие в питательной среде двух групп фитогормонов: ауксинов и цитокининов. Ауксины вызывают процесс дедифференцировки клетки. Цитокинины вызывают деление (пролиферацию) дедифференцированных клеток.
 Типы культивируемых растительных клеток o o o Основным типом культивируемых растительных клеток является каллусная ткань. Реже культивируют клетки опухолевых тканей растений. Культуры опухолевых клеток внешне и по морфологии мало отличаются от культур каллусных клеток. Главным отличием опухолевых клеток является их гормональная независимость, это обеспечивает им рост на питательных средах без добавок фитогормонов или их аналогов. Опухолевые клетки лишены способности давать начало организованным структурам, таким, как корни или побеги в процессе органогенеза. Каллусные клетки в культуре могут спонтанно приобретать гормононезависимость, природа которой может быть следствием мутации или результатом экспрессии генов, определяющих независимость клетки от гормонов.
Типы культивируемых растительных клеток o o o Основным типом культивируемых растительных клеток является каллусная ткань. Реже культивируют клетки опухолевых тканей растений. Культуры опухолевых клеток внешне и по морфологии мало отличаются от культур каллусных клеток. Главным отличием опухолевых клеток является их гормональная независимость, это обеспечивает им рост на питательных средах без добавок фитогормонов или их аналогов. Опухолевые клетки лишены способности давать начало организованным структурам, таким, как корни или побеги в процессе органогенеза. Каллусные клетки в культуре могут спонтанно приобретать гормононезависимость, природа которой может быть следствием мутации или результатом экспрессии генов, определяющих независимость клетки от гормонов.
 Способы получения каллусной ткани o o o Если в питательную среду без этих фитогормонов поместить любой растительный эксплант (кусочек стебля, листа, корня), состоящий из специализированных (дифференцировавнных) клеток, то деление клеток не произойдет и каллусная ткань не образуется. Дифференцированные клетки не способны к делению. Для приобретения дифференцированными клетками способности к делению необходима их дедифференцировка и превращение специализированной клетки в каллусную.
Способы получения каллусной ткани o o o Если в питательную среду без этих фитогормонов поместить любой растительный эксплант (кусочек стебля, листа, корня), состоящий из специализированных (дифференцировавнных) клеток, то деление клеток не произойдет и каллусная ткань не образуется. Дифференцированные клетки не способны к делению. Для приобретения дифференцированными клетками способности к делению необходима их дедифференцировка и превращение специализированной клетки в каллусную.
 Способы культивирования каллусной ткани o o Переход клетки in vitro из дифференцированного состояния к дедифференцировке и активным клеточным делениям обусловлен изменением активности генов (эпигеномная изменчивость). Изменение активности генов приводит к изменению белкового состава клеток, в каллусе появляются специфические белки и исчезают белки характерные для фотосинтезирующих клеток листа.
Способы культивирования каллусной ткани o o Переход клетки in vitro из дифференцированного состояния к дедифференцировке и активным клеточным делениям обусловлен изменением активности генов (эпигеномная изменчивость). Изменение активности генов приводит к изменению белкового состава клеток, в каллусе появляются специфические белки и исчезают белки характерные для фотосинтезирующих клеток листа.
 Способы культивирования каллусной ткани in vitro o o Каллусная клетка имеет свой цикл развития и повторяет развитие любой другой клетки (деление, растяжение и дифференцировка), затем наступает старение и отмирание клетки. Чтобы не произошло старения, утраты способности к делению и отмирания каллусных клеток, первичный каллус, возникающий на эксплантах, через 4 -6 недель переносят на свежую питательную среду (пассируют). При регулярном пассировании способность к делению можно поддерживать очень долго (десятки лет)
Способы культивирования каллусной ткани in vitro o o Каллусная клетка имеет свой цикл развития и повторяет развитие любой другой клетки (деление, растяжение и дифференцировка), затем наступает старение и отмирание клетки. Чтобы не произошло старения, утраты способности к делению и отмирания каллусных клеток, первичный каллус, возникающий на эксплантах, через 4 -6 недель переносят на свежую питательную среду (пассируют). При регулярном пассировании способность к делению можно поддерживать очень долго (десятки лет)
 Морфогенез в калусных тканях. Развитие многоклеточных организмов. o o 1. 2. 3. Вторичная дифференцировка. В культуре каллусной ткани возникают организованные структуры из неорганизованной массы клеток. Виды вторичной дифференцировки: Образование в каллусной ткани отдельных дифференцированных клеток Образование в каллусе различных тканей Образование в каллусе органов и зародышей, т. е. органогенез (развитие целого растения). Морфогенез можно получить только при условии подбора оптимальной питательной среды, физических факторов, баланса фитогормонов и присутствия сигнальных белков в клетках.
Морфогенез в калусных тканях. Развитие многоклеточных организмов. o o 1. 2. 3. Вторичная дифференцировка. В культуре каллусной ткани возникают организованные структуры из неорганизованной массы клеток. Виды вторичной дифференцировки: Образование в каллусной ткани отдельных дифференцированных клеток Образование в каллусе различных тканей Образование в каллусе органов и зародышей, т. е. органогенез (развитие целого растения). Морфогенез можно получить только при условии подбора оптимальной питательной среды, физических факторов, баланса фитогормонов и присутствия сигнальных белков в клетках.
 Растения из культуры тканей Культура тканей банана
Растения из культуры тканей Культура тканей банана
 ПЕРЕРЫВ
ПЕРЕРЫВ
 Культура клеточных суспензий o o Дедифференцированные клетки можно культивировать не только на твердых, но и на жидких питательных средах (суспензионные культуры) Суспензию клеток получают из каллусной ткани, предварительно полученной на твердой агаризованной питательной среде. Суспензию клеток помещают в жидкую питательную среду и постоянно перемешивают Клеточные суспензии в биотехнологии используют для получения вторичных метаболитов.
Культура клеточных суспензий o o Дедифференцированные клетки можно культивировать не только на твердых, но и на жидких питательных средах (суспензионные культуры) Суспензию клеток получают из каллусной ткани, предварительно полученной на твердой агаризованной питательной среде. Суспензию клеток помещают в жидкую питательную среду и постоянно перемешивают Клеточные суспензии в биотехнологии используют для получения вторичных метаболитов.
 Клеточная биотехнология и получение вторичных метаболитов o o o Каллусная ткань – источник веществ вторичного метаболизма Существующие методы культивирования изолированных клеток в условиях in vitro позволяют использовать их для синтеза вторичных метаболитов. Каллусные клетки могут синтезировать вторичные метаболиты по качественному и количественному составу схожие с интактным растением. Вещества вторичного биосинтеза получают как правило из суспензионной культуры в биореакторах или ферментерах
Клеточная биотехнология и получение вторичных метаболитов o o o Каллусная ткань – источник веществ вторичного метаболизма Существующие методы культивирования изолированных клеток в условиях in vitro позволяют использовать их для синтеза вторичных метаболитов. Каллусные клетки могут синтезировать вторичные метаболиты по качественному и количественному составу схожие с интактным растением. Вещества вторичного биосинтеза получают как правило из суспензионной культуры в биореакторах или ферментерах
 Клеточные биотехнологии и медицинские препараты o o Диосгенин из клеток диоскореи Диосгенин - растительный сапонин, имеющий структуру схожую со стероидами В организме диосгенин используется для синтеза прогестерона, и входит в состав оральных контрацептивов для женщин. Диосгенин крайне нежелательно принимать мужчинам. Диосгенин составной компонент анаболического комплекса Viraloid
Клеточные биотехнологии и медицинские препараты o o Диосгенин из клеток диоскореи Диосгенин - растительный сапонин, имеющий структуру схожую со стероидами В организме диосгенин используется для синтеза прогестерона, и входит в состав оральных контрацептивов для женщин. Диосгенин крайне нежелательно принимать мужчинам. Диосгенин составной компонент анаболического комплекса Viraloid
 Клеточные биотехнологии и медицинские препараты o o Аймалин – алкалоид индольного типа из клеток раувольфии змеиной Аймалин относится к антиаритмическим препаратам I группы и способен купировать приступы мерцательной аритмии и пароксизмальной тахикардии.
Клеточные биотехнологии и медицинские препараты o o Аймалин – алкалоид индольного типа из клеток раувольфии змеиной Аймалин относится к антиаритмическим препаратам I группы и способен купировать приступы мерцательной аритмии и пароксизмальной тахикардии.
 Клеточные биотехнологии и медицинские препараты o o Тонизирующие вещества из клеток женьшеня стимулирует ЦНС, уменьшая общую слабость, повышенную утомляемость, сонливость, повышает АД, умственную и физическую работоспособность; стимулирует половую функцию. Снижает содержание холестерина и глюкозы в крови, активирует деятельность надпочечников и стимулирует аппетит. Фармакологическая активность обусловлена содержанием сапониновых гликозидов (панаксозиды А и В, панаквилон, панаксин), эфирных и жирных масел, стеролов, пептидов, витаминов и минералов.
Клеточные биотехнологии и медицинские препараты o o Тонизирующие вещества из клеток женьшеня стимулирует ЦНС, уменьшая общую слабость, повышенную утомляемость, сонливость, повышает АД, умственную и физическую работоспособность; стимулирует половую функцию. Снижает содержание холестерина и глюкозы в крови, активирует деятельность надпочечников и стимулирует аппетит. Фармакологическая активность обусловлена содержанием сапониновых гликозидов (панаксозиды А и В, панаквилон, панаксин), эфирных и жирных масел, стеролов, пептидов, витаминов и минералов.
 Клеточные биотехнологии и медицинские препараты o Стевия препарат стевиозид Стевиозид зарегистрирован в качестве пищевой добавки E 960 как подсластитель. Медицинские исследования показали хорошие результаты использования экстракта стевии для лечения ожирения и гипертонии
Клеточные биотехнологии и медицинские препараты o Стевия препарат стевиозид Стевиозид зарегистрирован в качестве пищевой добавки E 960 как подсластитель. Медицинские исследования показали хорошие результаты использования экстракта стевии для лечения ожирения и гипертонии
 Клеточные биотехнологии и медицинские препараты o Тис ягодный – таксол противораковый препарат
Клеточные биотехнологии и медицинские препараты o Тис ягодный – таксол противораковый препарат
 Протопласты Получения изолированных протопластов растительных клеток o o o ПРОТОПЛА СТ - все содержимое клетки, за исключением клеточной оболочки. Протопласт сохраняет все свойства, присущие растительной клетке. Растительные протопласты – это ограниченные мембраной цитоплазматические образования, обладающие внутриклеточными органеллами и характеризующиеся структурной целостностью и способностью осуществлять активный метаболизм, а также реакции биосинтеза и трансформации энергии.
Протопласты Получения изолированных протопластов растительных клеток o o o ПРОТОПЛА СТ - все содержимое клетки, за исключением клеточной оболочки. Протопласт сохраняет все свойства, присущие растительной клетке. Растительные протопласты – это ограниченные мембраной цитоплазматические образования, обладающие внутриклеточными органеллами и характеризующиеся структурной целостностью и способностью осуществлять активный метаболизм, а также реакции биосинтеза и трансформации энергии.
 Методы получения протопластов (удаление клеточных стенок) o o Механический. Впервые протопласты растительных клеток были получены при изучении плазмолиза (в 1892 г. ) в клетках водного растения – телореза. Способ получения был весьма примитивным. Тонкая полоска ткани растения выдерживалась сначала в 0, 1 М растворе сахарозы до тех пор, пока протопласт не "сожмется" и не отойдет от клеточных стенок, затем бритвой делался разрез полоски и протопласты высвобождались в среду. Ферментативный. Клеточная стенка удаляется с помощью ферментов. Таким методом уже в 1919 г. были получены протопласты клеток грибов в результате обработки их клеточных стенок желудочным соком улитки. В микробиологических экспериментах протопласты получают путем разрушения клеточных стенок бактерий ферментом лизоцимом.
Методы получения протопластов (удаление клеточных стенок) o o Механический. Впервые протопласты растительных клеток были получены при изучении плазмолиза (в 1892 г. ) в клетках водного растения – телореза. Способ получения был весьма примитивным. Тонкая полоска ткани растения выдерживалась сначала в 0, 1 М растворе сахарозы до тех пор, пока протопласт не "сожмется" и не отойдет от клеточных стенок, затем бритвой делался разрез полоски и протопласты высвобождались в среду. Ферментативный. Клеточная стенка удаляется с помощью ферментов. Таким методом уже в 1919 г. были получены протопласты клеток грибов в результате обработки их клеточных стенок желудочным соком улитки. В микробиологических экспериментах протопласты получают путем разрушения клеточных стенок бактерий ферментом лизоцимом.
 Культивирование протопластов o 1. 2. Для культивирования протопластов используются два методических приема: Инкубирование в каплях жидкой среды. В этом случае суспензию протопластов в виде капель помещают на пластиковые чашки Петри. Помещение в агаровый слой. В этом случае суспензию протопластов наливают в пластиковые чашки Петри, добавляют равный объем той же среды с 1% агаром при температуре не выше 45 о. С. После остывания чашки Петри переворачивают и культивируют при 28 о. С. В данном случае протопласты фиксированы в одном положении и физически отделены друг от друга.
Культивирование протопластов o 1. 2. Для культивирования протопластов используются два методических приема: Инкубирование в каплях жидкой среды. В этом случае суспензию протопластов в виде капель помещают на пластиковые чашки Петри. Помещение в агаровый слой. В этом случае суспензию протопластов наливают в пластиковые чашки Петри, добавляют равный объем той же среды с 1% агаром при температуре не выше 45 о. С. После остывания чашки Петри переворачивают и культивируют при 28 о. С. В данном случае протопласты фиксированы в одном положении и физически отделены друг от друга.
 Биотехнология протопластов Слияние протопластов (гибридизация) o o o Полученные из обычных клеток протопласты, ещё не образовавшие клеточной стенки, могут сливаться между собой. Слияние протопластов - это своеобразный метод соматической гибридизации. В отличие от обычной, где сливаются половые клетки, в качестве родительских при соматической гибридизации используются диплоидные клетки растений.
Биотехнология протопластов Слияние протопластов (гибридизация) o o o Полученные из обычных клеток протопласты, ещё не образовавшие клеточной стенки, могут сливаться между собой. Слияние протопластов - это своеобразный метод соматической гибридизации. В отличие от обычной, где сливаются половые клетки, в качестве родительских при соматической гибридизации используются диплоидные клетки растений.
 Гибридомы o o Гибридома — это линия клеток, полученнаая в результате слияния нормальных клеток с «бессмертными» раковыми клетками. Гибридомы используется для получения моноклональных антител
Гибридомы o o Гибридома — это линия клеток, полученнаая в результате слияния нормальных клеток с «бессмертными» раковыми клетками. Гибридомы используется для получения моноклональных антител
 Гибридизация животных клеток o o 1. 2. Гибриды соматических клеток были открыты лишь в 60 -х годах прошлого века При изучении межвидовых гибридных клеток, способных к пролиферации были сделаны два очень важных наблюдения: - в гибридах могут проявиться оба генома; - в долгоживущих межвидовых гибридах элиминируются хромосомы только одного вида.
Гибридизация животных клеток o o 1. 2. Гибриды соматических клеток были открыты лишь в 60 -х годах прошлого века При изучении межвидовых гибридных клеток, способных к пролиферации были сделаны два очень важных наблюдения: - в гибридах могут проявиться оба генома; - в долгоживущих межвидовых гибридах элиминируются хромосомы только одного вида.
 Гибридизация животных клеток. Механизм слияния клеток o o o Для индукции слияния клеток используются вещества различной природы. Ионы Са 2+, полиэтиленгликоль, лизолецитин, моноолеат глицерина, вирус Сендай. Первый этап слияния - сближение мембран соседних клеток и установление между ними тесного контакта. На втором этапе гликопротеиды, расположенные на поверхности, начинают высвобождаться и притягиваются к местам прикрепления вирусных частиц. Третий этап - мицелизация обнажившихся липидов двух противолежащих мембран. Четвертый этап - слияние мембран.
Гибридизация животных клеток. Механизм слияния клеток o o o Для индукции слияния клеток используются вещества различной природы. Ионы Са 2+, полиэтиленгликоль, лизолецитин, моноолеат глицерина, вирус Сендай. Первый этап слияния - сближение мембран соседних клеток и установление между ними тесного контакта. На втором этапе гликопротеиды, расположенные на поверхности, начинают высвобождаться и притягиваются к местам прикрепления вирусных частиц. Третий этап - мицелизация обнажившихся липидов двух противолежащих мембран. Четвертый этап - слияние мембран.
 Техника гибридизации может позволить следующее: o o Скрещивание генетически отдаленных видов растений (организмов). Получение асимметричных гибридов, несущих генный набор одного из родителей наряду с несколькими хромосомами, органеллами или цитоплазмой другого. Слияние трёх и более клеток. Получение гибридов, представляющих сумму генотипов родителей.
Техника гибридизации может позволить следующее: o o Скрещивание генетически отдаленных видов растений (организмов). Получение асимметричных гибридов, несущих генный набор одного из родителей наряду с несколькими хромосомами, органеллами или цитоплазмой другого. Слияние трёх и более клеток. Получение гибридов, представляющих сумму генотипов родителей.
 Виды соматических гибридов o o o Впервые зрелый межвидовой гибрид был получен в результате гибридизации протопластов двух сортов табака в 1972 г. Каллус этого гибрида мог расти на безгормональной среде. Гибридное растение цвело. С тех пор были получены многие жизнеспособные внутривидовые, межвидовые, межродовые гибриды.
Виды соматических гибридов o o o Впервые зрелый межвидовой гибрид был получен в результате гибридизации протопластов двух сортов табака в 1972 г. Каллус этого гибрида мог расти на безгормональной среде. Гибридное растение цвело. С тех пор были получены многие жизнеспособные внутривидовые, межвидовые, межродовые гибриды.
 Соматические гибриды o o Осуществлено слияние протопластов культурного картофеля сорта с протопластами дикого картофеля. Известно, что у дикого картофеля клубни очень мелкие. Вместе с тем, растение устойчиво ко многим заболеваниям. Культурный картофель сорта образует крупные клубни, но растения этого сорта восприимчивы к болезням. Соматические гибриды по форме листьев и кустов, размеру клубней занимали промежуточное положение между культурными и дикими растениями. Вместе с тем гибрид, полученный в результате соматической гибридизации, оказался устойчивым к вирусам.
Соматические гибриды o o Осуществлено слияние протопластов культурного картофеля сорта с протопластами дикого картофеля. Известно, что у дикого картофеля клубни очень мелкие. Вместе с тем, растение устойчиво ко многим заболеваниям. Культурный картофель сорта образует крупные клубни, но растения этого сорта восприимчивы к болезням. Соматические гибриды по форме листьев и кустов, размеру клубней занимали промежуточное положение между культурными и дикими растениями. Вместе с тем гибрид, полученный в результате соматической гибридизации, оказался устойчивым к вирусам.
 Создание межродовых гибридов o o o картофель + томат (Г. Мельхерс, 1978 г. ) Ячмень + рис (Х. Кисака с соавт. , 1997) Арабидопсис + турнепс (Ю. Глеба) Красавка + табак Морковь + сныть Соя + табак (К. Као и В. Веттером в 1976 -77 гг)
Создание межродовых гибридов o o o картофель + томат (Г. Мельхерс, 1978 г. ) Ячмень + рис (Х. Кисака с соавт. , 1997) Арабидопсис + турнепс (Ю. Глеба) Красавка + табак Морковь + сныть Соя + табак (К. Као и В. Веттером в 1976 -77 гг)
 Получение межцарственных гибридов o o Изучение клеток "животное + растение" показало, что на этапе слияния видоспецифичность не проявляется, поэтому можно слить даже животную и растительную клетки. На более поздних этапах онтогенеза эти различия сказываются, что было установлено в экспериментах по слиянию протопластов арабидопсиса и табака с лимфоцитами человека. При этом происходило слияние цитоплазмы, а ядра не сливались. Эдвард Коккинг параллельно проводил изучение ультраструктуры таких гибридов, работая с клетками амфибий и протопластами моркови. После объединения клеток ядра амфибии были окружены тонким слоем собственной цитоплазмы, но уже через 48 часов отмечалось полное смешивание цитоплазмы и регенерация клеточной стенки.
Получение межцарственных гибридов o o Изучение клеток "животное + растение" показало, что на этапе слияния видоспецифичность не проявляется, поэтому можно слить даже животную и растительную клетки. На более поздних этапах онтогенеза эти различия сказываются, что было установлено в экспериментах по слиянию протопластов арабидопсиса и табака с лимфоцитами человека. При этом происходило слияние цитоплазмы, а ядра не сливались. Эдвард Коккинг параллельно проводил изучение ультраструктуры таких гибридов, работая с клетками амфибий и протопластами моркови. После объединения клеток ядра амфибии были окружены тонким слоем собственной цитоплазмы, но уже через 48 часов отмечалось полное смешивание цитоплазмы и регенерация клеточной стенки.
 Культуры животных клеток и тканей o Чтобы показать способность клеток животных расти и делиться в культуре, потребовалось разработать ряд подходов и методик: 1. Методики получения чистых клеток, свободных от экзогенных прокариотов и грибов. 2. Разработка питательных сред, в которых рост изолированных клеток не подавляется. 3. Контроль за развитием клеток. 4. Методики непрерывного культивирования культур клеток животных in vitro и поддержания их свободными от других биологических агентов.
Культуры животных клеток и тканей o Чтобы показать способность клеток животных расти и делиться в культуре, потребовалось разработать ряд подходов и методик: 1. Методики получения чистых клеток, свободных от экзогенных прокариотов и грибов. 2. Разработка питательных сред, в которых рост изолированных клеток не подавляется. 3. Контроль за развитием клеток. 4. Методики непрерывного культивирования культур клеток животных in vitro и поддержания их свободными от других биологических агентов.
 История развития культуры животных клеток и тканей o o o Впервые клоны клеток в культуре из одиночной клетки были получены Эрлом с сотрудниками в 1948 году. В 1961 г. Хейфлик и Мурхед выделили линию диплоидных клеток человека (НДС) WI-38 Первые суспензионные культуры клеток животных, как правило, основывались на клетках злокачественных тканей. Это — клетки He. La, выделенные 8 февраля 1951 года из раковой опухоли шейки матки пациентки по имени Henrietta Lacks. Эта линия используется и в настоящее время во многих лабораториях мира.
История развития культуры животных клеток и тканей o o o Впервые клоны клеток в культуре из одиночной клетки были получены Эрлом с сотрудниками в 1948 году. В 1961 г. Хейфлик и Мурхед выделили линию диплоидных клеток человека (НДС) WI-38 Первые суспензионные культуры клеток животных, как правило, основывались на клетках злокачественных тканей. Это — клетки He. La, выделенные 8 февраля 1951 года из раковой опухоли шейки матки пациентки по имени Henrietta Lacks. Эта линия используется и в настоящее время во многих лабораториях мира.
 Культивирование клеток животных и человека o o Список типов клеток, которые введены в культуру, достаточно велик. Это элементы соединительной ткани человека (фибробласты), скелетные ткани (кость и хрящи), скелетные, сердечные и гладкие мышцы, эпителиальные ткани (печень, легкие, почки и др. ), клетки нервной системы, эндокринные клетки (надпочечники, гипофиз), меланоциты и различные опухолевые клетки.
Культивирование клеток животных и человека o o Список типов клеток, которые введены в культуру, достаточно велик. Это элементы соединительной ткани человека (фибробласты), скелетные ткани (кость и хрящи), скелетные, сердечные и гладкие мышцы, эпителиальные ткани (печень, легкие, почки и др. ), клетки нервной системы, эндокринные клетки (надпочечники, гипофиз), меланоциты и различные опухолевые клетки.
 Культивирование клеток животных и человека o o Какую ткань лучше брать для введения в культуру, взрослую или эмбриональную, нормальную или опухолевую? Культуры, полученные из эмбриональных тканей, характеризуются лучшей выживаемостью и более активным ростом по сравнению с соответствующими зрелыми тканями. Причиной этого служит низкий уровень специализации клеток в в эмбрионах.
Культивирование клеток животных и человека o o Какую ткань лучше брать для введения в культуру, взрослую или эмбриональную, нормальную или опухолевую? Культуры, полученные из эмбриональных тканей, характеризуются лучшей выживаемостью и более активным ростом по сравнению с соответствующими зрелыми тканями. Причиной этого служит низкий уровень специализации клеток в в эмбрионах.
 Культивирование клеток o o o Клетки одного и того же типа в ткани взаимодействуют друг с другом и согласовывают скорость деления, чтобы поддерживать надлежащую плотность популяции. Выступы цитоплазмы при контакте с соседней мембраной ингибируют движение. Клетки в этом случае направляют свое развитие в другом направлении (феномен контактного ингибирования). Когда культура станет монослойной, активность ложноножек и движение клеток прекращается.
Культивирование клеток o o o Клетки одного и того же типа в ткани взаимодействуют друг с другом и согласовывают скорость деления, чтобы поддерживать надлежащую плотность популяции. Выступы цитоплазмы при контакте с соседней мембраной ингибируют движение. Клетки в этом случае направляют свое развитие в другом направлении (феномен контактного ингибирования). Когда культура станет монослойной, активность ложноножек и движение клеток прекращается.
 Питательные среды и условия культивирования o o o Культуры клеток животных и человека предъявляют определенные требования к жидкой (питательная среда), газообразной (концентрация газов) и твердой (поверхность субстрата) фазе. Питательная среда представляет собой раствор определенного состава, к которому добавляются компоненты невыясненного биологического происхождения (добавки плазмы, сыворотки крови, тканевые экстракты и т. д. ). Основу питательных сред составляют солевые растворы. Минеральные компоненты в этих растворах подобраны так, что раствор выполняет буферные функции, поддерживая постоянный кислотно-щелочной баланс среды в процессе культивирования. Постоянство р. Н среды является одним из главных требований условий культивирования.
Питательные среды и условия культивирования o o o Культуры клеток животных и человека предъявляют определенные требования к жидкой (питательная среда), газообразной (концентрация газов) и твердой (поверхность субстрата) фазе. Питательная среда представляет собой раствор определенного состава, к которому добавляются компоненты невыясненного биологического происхождения (добавки плазмы, сыворотки крови, тканевые экстракты и т. д. ). Основу питательных сред составляют солевые растворы. Минеральные компоненты в этих растворах подобраны так, что раствор выполняет буферные функции, поддерживая постоянный кислотно-щелочной баланс среды в процессе культивирования. Постоянство р. Н среды является одним из главных требований условий культивирования.
 Системы культивирования клеток o o Непроточные культуры - тип культур, в котором клетки вводят в фиксированный объем среды. По мере роста клеток происходит использование питательных веществ и накопление метаболитов, поэтому среда должна периодически меняться, что приводит к изменению клеточного метаболизма, называемого еще и физиологической дифференцировкой. Со временем, в результате истощения среды происходит прекращение пролиферации клеток. Проточные культуры обеспечивают истинные гомеостатические условия без изменения концентрации питательных веществ и метаболитов, а также числа клеток. Гомеостаз обусловлен постоянным вхождением среды в культуру и одновременным удалением равного объема среды с клетками. Такие системы пригодны для суспензионных культур и монослойных культур на микроносителях.
Системы культивирования клеток o o Непроточные культуры - тип культур, в котором клетки вводят в фиксированный объем среды. По мере роста клеток происходит использование питательных веществ и накопление метаболитов, поэтому среда должна периодически меняться, что приводит к изменению клеточного метаболизма, называемого еще и физиологической дифференцировкой. Со временем, в результате истощения среды происходит прекращение пролиферации клеток. Проточные культуры обеспечивают истинные гомеостатические условия без изменения концентрации питательных веществ и метаболитов, а также числа клеток. Гомеостаз обусловлен постоянным вхождением среды в культуру и одновременным удалением равного объема среды с клетками. Такие системы пригодны для суспензионных культур и монослойных культур на микроносителях.
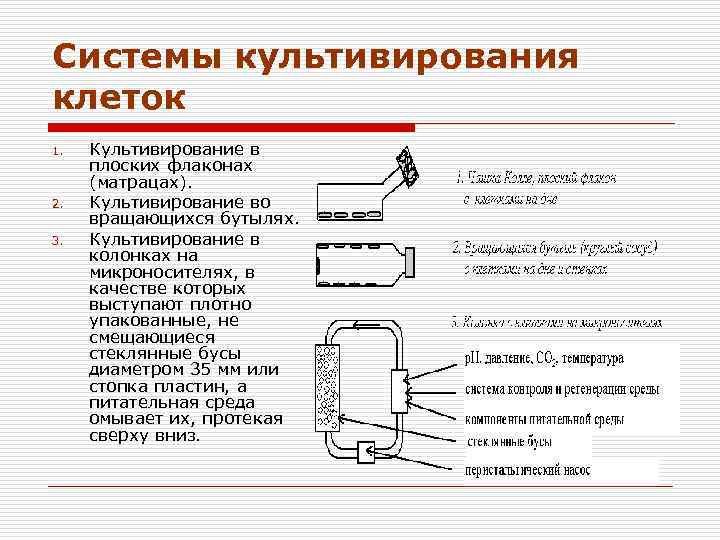 Системы культивирования клеток 1. 2. 3. Культивирование в плоских флаконах (матрацах). Культивирование во вращающихся бутылях. Культивирование в колонках на микроносителях, в качестве которых выступают плотно упакованные, не смещающиеся стеклянные бусы диаметром 35 мм или стопка пластин, а питательная среда омывает их, протекая сверху вниз.
Системы культивирования клеток 1. 2. 3. Культивирование в плоских флаконах (матрацах). Культивирование во вращающихся бутылях. Культивирование в колонках на микроносителях, в качестве которых выступают плотно упакованные, не смещающиеся стеклянные бусы диаметром 35 мм или стопка пластин, а питательная среда омывает их, протекая сверху вниз.
 Использование культуры клеток человека o o o Практически любые клетки человека могут быть введены в культуру и служить средством и объектом во многих медико-биологических исследованиях. Благодаря культивированию клеток возможности исследования и диагностики расширяются почти беспредельно. Клеточные линии применяют для тестирования и изучения механизма действия различных веществ, которые могут быть использованы в качестве лекарственных препаратов, детергентов, косметических средств, инсектицидов, консервантов
Использование культуры клеток человека o o o Практически любые клетки человека могут быть введены в культуру и служить средством и объектом во многих медико-биологических исследованиях. Благодаря культивированию клеток возможности исследования и диагностики расширяются почти беспредельно. Клеточные линии применяют для тестирования и изучения механизма действия различных веществ, которые могут быть использованы в качестве лекарственных препаратов, детергентов, косметических средств, инсектицидов, консервантов
 Использование культуры клеток человека o o 1. 2. 3. Наибольшее распространение получили культуры фибробластов (клетки соединительной ткани). Гринбергом в 1978 году была показана возможность экстраполяции данных, полученных на культивируемых фибробластах, на условия in vivo. Фибробласты in vitro сохраняют важнейшие черты, свойственные клеткам в организме, а также онтогенетические и индивидуально генотипические свойства организма-донора. Нет другого такого типа клеток, который в полной мере мог бы представлять свойства клеток организма. Изменения, которые возникают при введении фибробластов в культуру, можно легко контролировать и свести к минимуму при создании соответствующих условий.
Использование культуры клеток человека o o 1. 2. 3. Наибольшее распространение получили культуры фибробластов (клетки соединительной ткани). Гринбергом в 1978 году была показана возможность экстраполяции данных, полученных на культивируемых фибробластах, на условия in vivo. Фибробласты in vitro сохраняют важнейшие черты, свойственные клеткам в организме, а также онтогенетические и индивидуально генотипические свойства организма-донора. Нет другого такого типа клеток, который в полной мере мог бы представлять свойства клеток организма. Изменения, которые возникают при введении фибробластов в культуру, можно легко контролировать и свести к минимуму при создании соответствующих условий.
 Культивирование органов o Первые исследования в области культивирования органов и тканей относятся к концу прошлого века. Уже в 1897 году немецкий ученый Лёб (В. Loeb) опубликовал данные о культивировании фрагментов печени, почек, щитовидной железы и яичников кролика на небольших кровяных сгустках в культуральных пробирках.
Культивирование органов o Первые исследования в области культивирования органов и тканей относятся к концу прошлого века. Уже в 1897 году немецкий ученый Лёб (В. Loeb) опубликовал данные о культивировании фрагментов печени, почек, щитовидной железы и яичников кролика на небольших кровяных сгустках в культуральных пробирках.


