Клеточная цитотоксичность.ppt
- Количество слайдов: 30
 Клеточная цитотоксичность и иммунная защита
Клеточная цитотоксичность и иммунная защита
 Цитотоксичность – это механизм, с помощью которого лейкоциты способны распознавать и деструктировать другие клетки. Известно несколько типов клеток, обладающих цитотоксической активностью: F Цитотоксические Т-лимфоциты (ЦТЛ) F Естественные киллеры (NK) F Макрофаги (это нелимфоидные цтотоксические эффекторы, они действуют только опосредованно)
Цитотоксичность – это механизм, с помощью которого лейкоциты способны распознавать и деструктировать другие клетки. Известно несколько типов клеток, обладающих цитотоксической активностью: F Цитотоксические Т-лимфоциты (ЦТЛ) F Естественные киллеры (NK) F Макрофаги (это нелимфоидные цтотоксические эффекторы, они действуют только опосредованно)
 Цитотоксические Т-лимфоциты ЦТЛ распознают специфические АГ, презентированные молекулами МНС. Большинство ЦТЛ относится к CD 8+ Т-клеткам, распознающим АГ в комплексе с молекулами МНС I; CD 4+ Т-клеток меньше, однако они могут распознавать АГ в комплексе с молекулами МНС II. Основные маркеры ЦТЛ: ь CD 2 (рецептор функционального АГ лимфоцита 1 [LFA 1], адгезия) ь CD 3 (сигнальный комплекс TCR) ь CD 58, CD 44 (адгезия)
Цитотоксические Т-лимфоциты ЦТЛ распознают специфические АГ, презентированные молекулами МНС. Большинство ЦТЛ относится к CD 8+ Т-клеткам, распознающим АГ в комплексе с молекулами МНС I; CD 4+ Т-клеток меньше, однако они могут распознавать АГ в комплексе с молекулами МНС II. Основные маркеры ЦТЛ: ь CD 2 (рецептор функционального АГ лимфоцита 1 [LFA 1], адгезия) ь CD 3 (сигнальный комплекс TCR) ь CD 58, CD 44 (адгезия)
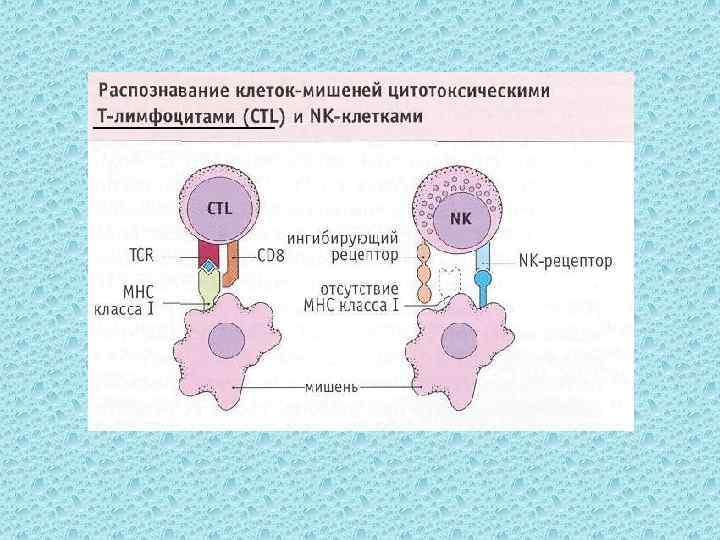
 ЦТЛ осуществляют киллинг своих мишеней несколькими механизмами: v прямой сигнал по типу клетка-к-клетке, передаваемый через поверхностные молекулы v сигнал, опосредованный цитокинами v экзоцитоз содержимого гранул Выбор механизма лизиса зависит от характеристик клетки-мишени.
ЦТЛ осуществляют киллинг своих мишеней несколькими механизмами: v прямой сигнал по типу клетка-к-клетке, передаваемый через поверхностные молекулы v сигнал, опосредованный цитокинами v экзоцитоз содержимого гранул Выбор механизма лизиса зависит от характеристик клетки-мишени.
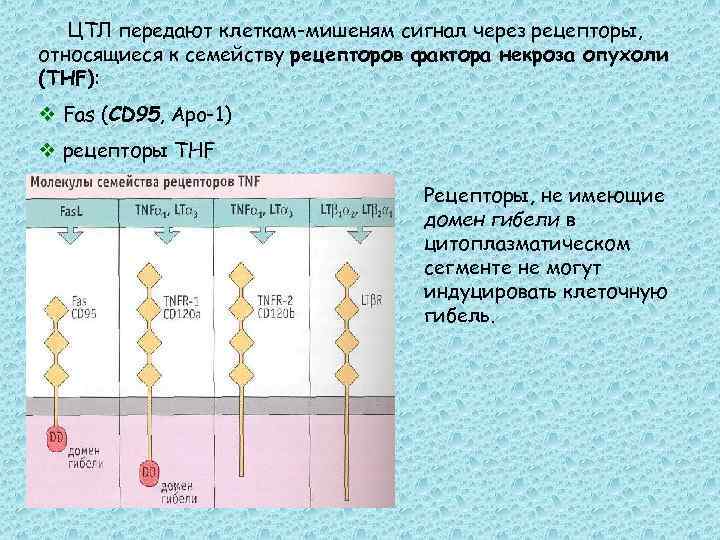 ЦТЛ передают клеткам-мишеням сигнал через рецепторы, относящиеся к семейству рецепторов фактора некроза опухоли (THF): v Fas (CD 95, Apo-1) v рецепторы THF Рецепторы, не имеющие домен гибели в цитоплазматическом сегменте не могут индуцировать клеточную гибель.
ЦТЛ передают клеткам-мишеням сигнал через рецепторы, относящиеся к семейству рецепторов фактора некроза опухоли (THF): v Fas (CD 95, Apo-1) v рецепторы THF Рецепторы, не имеющие домен гибели в цитоплазматическом сегменте не могут индуцировать клеточную гибель.
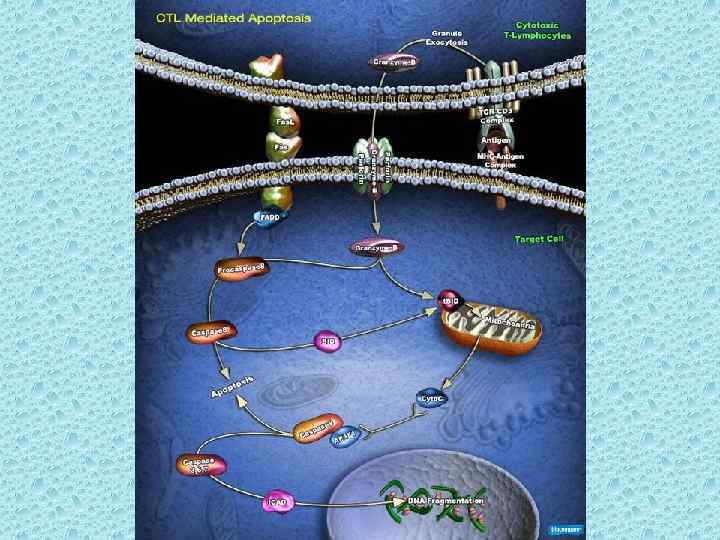
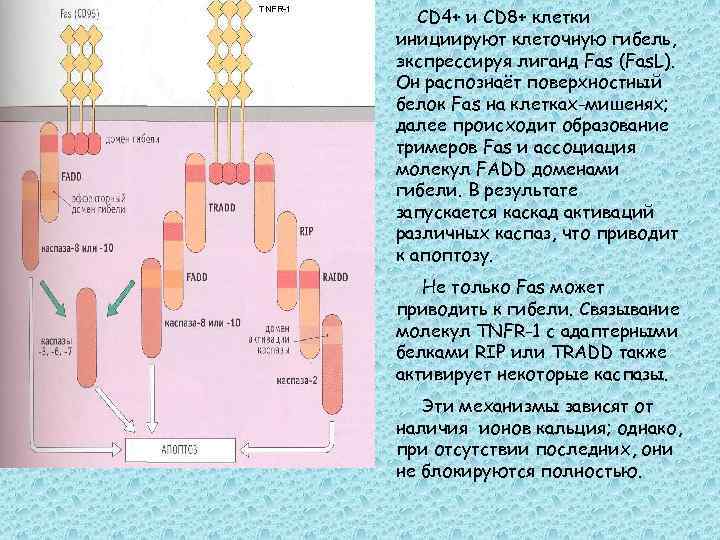 TNFR-1 CD 4+ и CD 8+ клетки инициируют клеточную гибель, экспрессируя лиганд Fas (Fas. L). Он распознаёт поверхностный белок Fas на клетках-мишенях; далее происходит образование тримеров Fas и ассоциация молекул FADD доменами гибели. В результате запускается каскад активаций различных каспаз, что приводит к апоптозу. Не только Fas может приводить к гибели. Связывание молекул TNFR-1 с адаптерными белками RIP или TRADD также активирует некоторые каспазы. Эти механизмы зависят от наличия ионов кальция; однако, при отсутствии последних, они не блокируются полностью.
TNFR-1 CD 4+ и CD 8+ клетки инициируют клеточную гибель, экспрессируя лиганд Fas (Fas. L). Он распознаёт поверхностный белок Fas на клетках-мишенях; далее происходит образование тримеров Fas и ассоциация молекул FADD доменами гибели. В результате запускается каскад активаций различных каспаз, что приводит к апоптозу. Не только Fas может приводить к гибели. Связывание молекул TNFR-1 с адаптерными белками RIP или TRADD также активирует некоторые каспазы. Эти механизмы зависят от наличия ионов кальция; однако, при отсутствии последних, они не блокируются полностью.
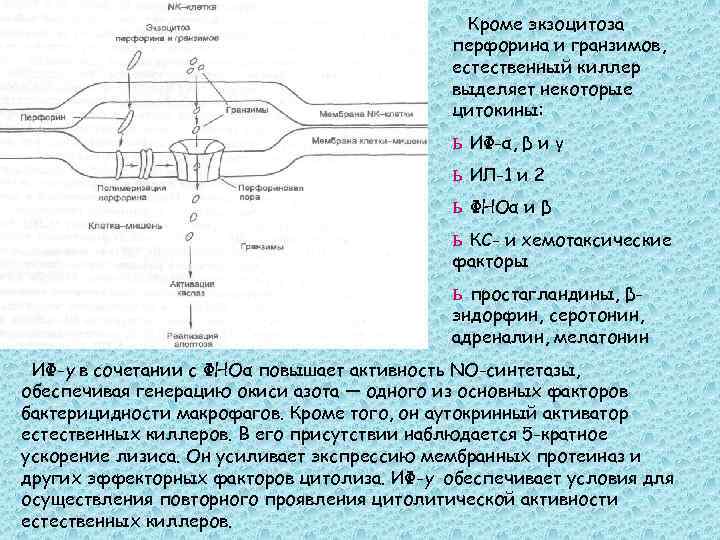
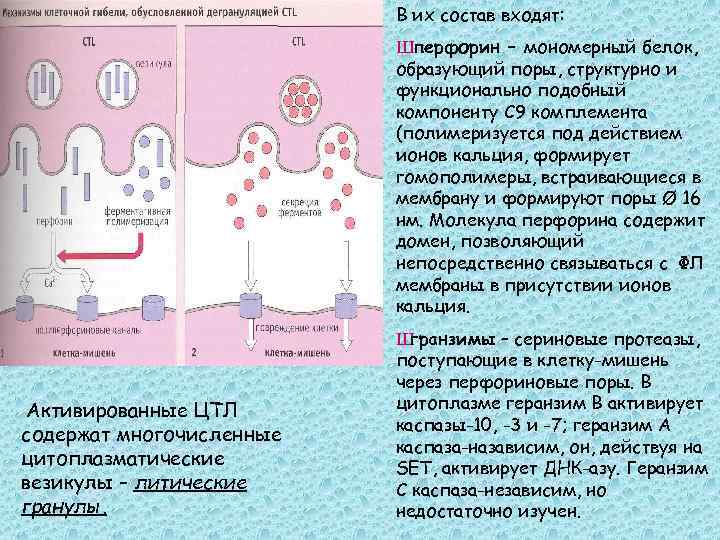 В их состав входят: Шперфорин – мономерный белок, образующий поры, структурно и функционально подобный компоненту С 9 комплемента (полимеризуется под действием ионов кальция, формирует гомополимеры, встраивающиеся в мембрану и формируют поры Ø 16 нм. Молекула перфорина содержит домен, позволяющий непосредственно связываться с ФЛ мембраны в присутствии ионов кальция. Активированные ЦТЛ содержат многочисленные цитоплазматические везикулы – литические гранулы. Ш гранзимы – сериновые протеазы, поступающие в клетку-мишень через перфориновые поры. В цитоплазме геранзим В активирует каспазы-10, -3 и -7; геранзим А каспаза-назависим, он, действуя на SET, активирует ДНК-азу. Геранзим С каспаза-независим, но недостаточно изучен.
В их состав входят: Шперфорин – мономерный белок, образующий поры, структурно и функционально подобный компоненту С 9 комплемента (полимеризуется под действием ионов кальция, формирует гомополимеры, встраивающиеся в мембрану и формируют поры Ø 16 нм. Молекула перфорина содержит домен, позволяющий непосредственно связываться с ФЛ мембраны в присутствии ионов кальция. Активированные ЦТЛ содержат многочисленные цитоплазматические везикулы – литические гранулы. Ш гранзимы – сериновые протеазы, поступающие в клетку-мишень через перфориновые поры. В цитоплазме геранзим В активирует каспазы-10, -3 и -7; геранзим А каспаза-назависим, он, действуя на SET, активирует ДНК-азу. Геранзим С каспаза-независим, но недостаточно изучен.
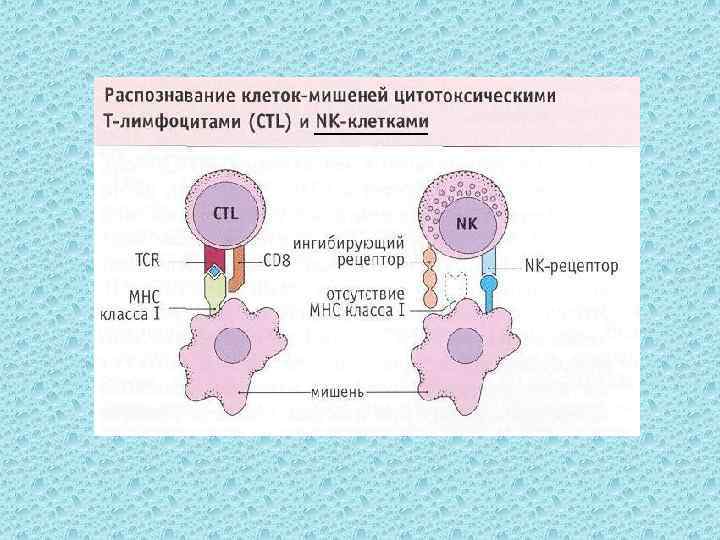
 NK - клетки Большая часть образуется из больших гранулярных лимфоцитов. Многие из NK o имеют фенотип CD 3 -, CD 16+, CD 56+, CD 94+ o не содержит продуктов реаранжировки генов TCR o реагируют только с МНС I Разделяют на две группы (ингибирующие рецепторы): o мембранные гликопротеины 2 типа, содержащие лектиновый, кальцезависимый домен o члены суперсемейства Ig (киллерный Ig-подобный рецептор, KIR)
NK - клетки Большая часть образуется из больших гранулярных лимфоцитов. Многие из NK o имеют фенотип CD 3 -, CD 16+, CD 56+, CD 94+ o не содержит продуктов реаранжировки генов TCR o реагируют только с МНС I Разделяют на две группы (ингибирующие рецепторы): o мембранные гликопротеины 2 типа, содержащие лектиновый, кальцезависимый домен o члены суперсемейства Ig (киллерный Ig-подобный рецептор, KIR)
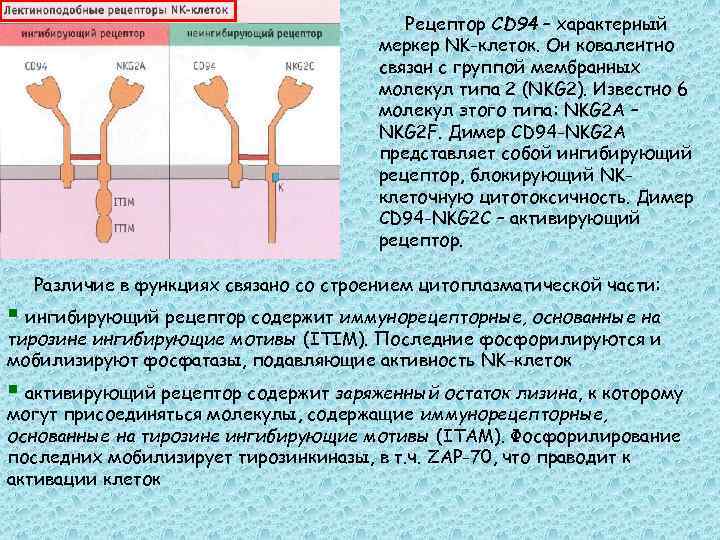 Рецептор CD 94 – характерный меркер NK-клеток. Он ковалентно связан с группой мембранных молекул типа 2 (NKG 2). Известно 6 молекул этого типа: NKG 2 A – NKG 2 F. Димер CD 94 -NKG 2 A представляет собой ингибирующий рецептор, блокирующий NKклеточную цитотоксичность. Димер CD 94 -NKG 2 С – активирующий рецептор. Различие в функциях связано со строением цитоплазматической части: § ингибирующий рецептор содержит иммунорецепторные, основанные на тирозине ингибирующие мотивы (ITIM). Последние фосфорилируются и мобилизируют фосфатазы, подавляющие активность NK-клеток § активирующий рецептор содержит заряженный остаток лизина, к которому могут присоединяться молекулы, содержащие иммунорецепторные, основанные на тирозине ингибирующие мотивы (ITАM). Фосфорилирование последних мобилизирует тирозинкиназы, в т. ч. ZAP-70, что праводит к активации клеток
Рецептор CD 94 – характерный меркер NK-клеток. Он ковалентно связан с группой мембранных молекул типа 2 (NKG 2). Известно 6 молекул этого типа: NKG 2 A – NKG 2 F. Димер CD 94 -NKG 2 A представляет собой ингибирующий рецептор, блокирующий NKклеточную цитотоксичность. Димер CD 94 -NKG 2 С – активирующий рецептор. Различие в функциях связано со строением цитоплазматической части: § ингибирующий рецептор содержит иммунорецепторные, основанные на тирозине ингибирующие мотивы (ITIM). Последние фосфорилируются и мобилизируют фосфатазы, подавляющие активность NK-клеток § активирующий рецептор содержит заряженный остаток лизина, к которому могут присоединяться молекулы, содержащие иммунорецепторные, основанные на тирозине ингибирующие мотивы (ITАM). Фосфорилирование последних мобилизирует тирозинкиназы, в т. ч. ZAP-70, что праводит к активации клеток
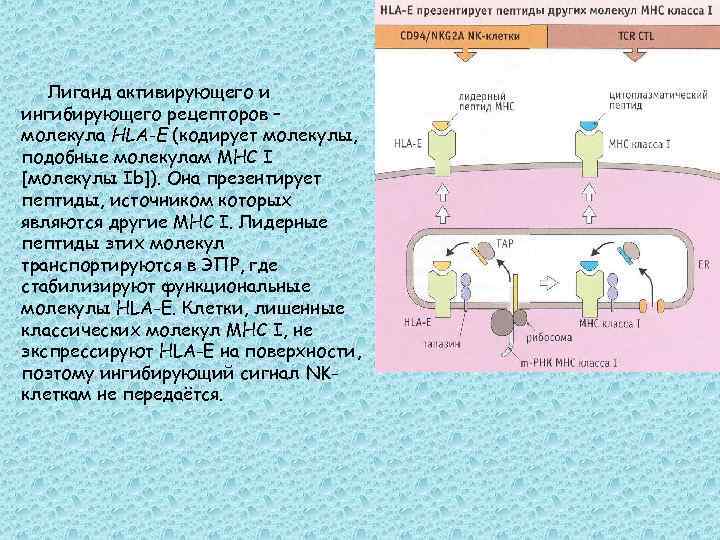 Лиганд активирующего и ингибирующего рецепторов – молекула HLA-E (кодирует молекулы, подобные молекулам МНС I [молекулы Ib]). Она презентирует пептиды, источником которых являются другие МНС I. Лидерные пептиды этих молекул транспортируются в ЭПР, где стабилизируют функциональные молекулы HLA-E. Клетки, лишенные классических молекул МНС I, не экспрессируют HLA-E на поверхности, поэтому ингибирующий сигнал NKклеткам не передаётся.
Лиганд активирующего и ингибирующего рецепторов – молекула HLA-E (кодирует молекулы, подобные молекулам МНС I [молекулы Ib]). Она презентирует пептиды, источником которых являются другие МНС I. Лидерные пептиды этих молекул транспортируются в ЭПР, где стабилизируют функциональные молекулы HLA-E. Клетки, лишенные классических молекул МНС I, не экспрессируют HLA-E на поверхности, поэтому ингибирующий сигнал NKклеткам не передаётся.
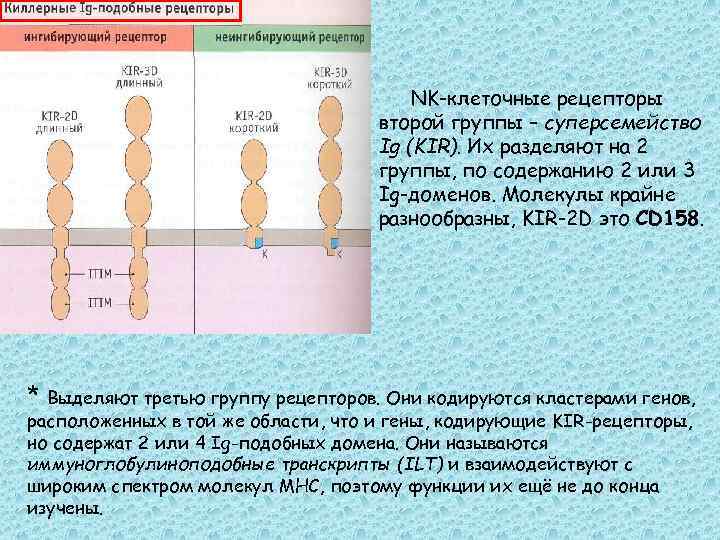 NK-клеточные рецепторы второй группы – суперсемейство Ig (KIR). Их разделяют на 2 группы, по содержанию 2 или 3 Ig-доменов. Молекулы крайне разнообразны, KIR-2 D это CD 158. * Выделяют третью группу рецепторов. Они кодируются кластерами генов, расположенных в той же области, что и гены, кодирующие KIR-рецепторы, но содержат 2 или 4 Ig-подобных домена. Они называются иммуноглобулиноподобные транскрипты (ILT) и взаимодействуют с широким спектром молекул МНС, поэтому функции их ещё не до конца изучены.
NK-клеточные рецепторы второй группы – суперсемейство Ig (KIR). Их разделяют на 2 группы, по содержанию 2 или 3 Ig-доменов. Молекулы крайне разнообразны, KIR-2 D это CD 158. * Выделяют третью группу рецепторов. Они кодируются кластерами генов, расположенных в той же области, что и гены, кодирующие KIR-рецепторы, но содержат 2 или 4 Ig-подобных домена. Они называются иммуноглобулиноподобные транскрипты (ILT) и взаимодействуют с широким спектром молекул МНС, поэтому функции их ещё не до конца изучены.
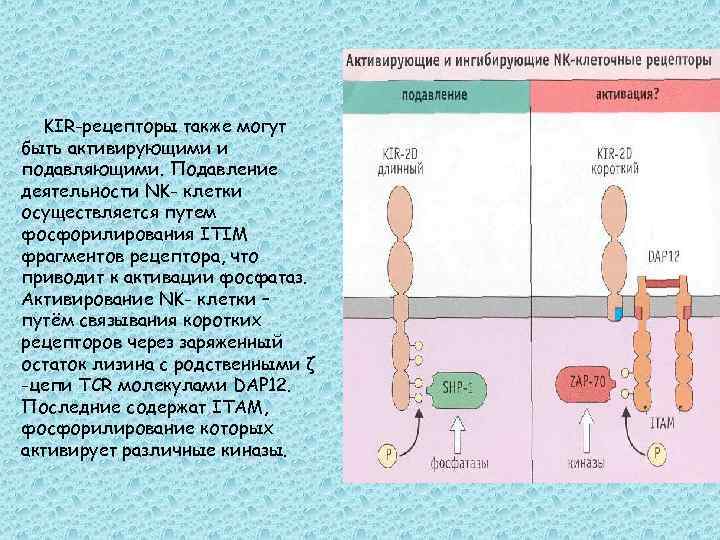 KIR-рецепторы также могут быть активирующими и подавляющими. Подавление деятельности NK- клетки осуществляется путем фосфорилирования ITIM фрагментов рецептора, что приводит к активации фосфатаз. Активирование NK- клетки – путём связывания коротких рецепторов через заряженный остаток лизина с родственными ζ -цепи TCR молекулами DAP 12. Последние содержат ITAM, фосфорилирование которых активирует различные киназы.
KIR-рецепторы также могут быть активирующими и подавляющими. Подавление деятельности NK- клетки осуществляется путем фосфорилирования ITIM фрагментов рецептора, что приводит к активации фосфатаз. Активирование NK- клетки – путём связывания коротких рецепторов через заряженный остаток лизина с родственными ζ -цепи TCR молекулами DAP 12. Последние содержат ITAM, фосфорилирование которых активирует различные киназы.
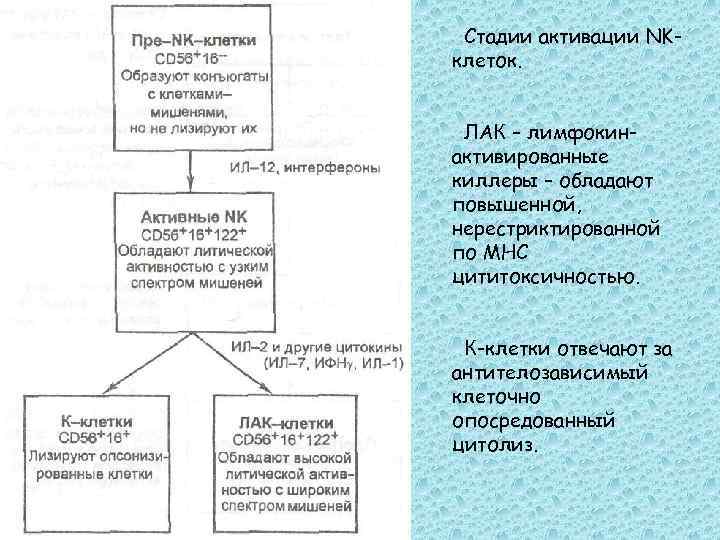 Стадии активации NKклеток. ЛАК – лимфокинактивированные киллеры – обладают повышенной, нерестриктированной по МНС цититоксичностью. К-клетки отвечают за антителозависимый клеточно опосредованный цитолиз.
Стадии активации NKклеток. ЛАК – лимфокинактивированные киллеры – обладают повышенной, нерестриктированной по МНС цититоксичностью. К-клетки отвечают за антителозависимый клеточно опосредованный цитолиз.
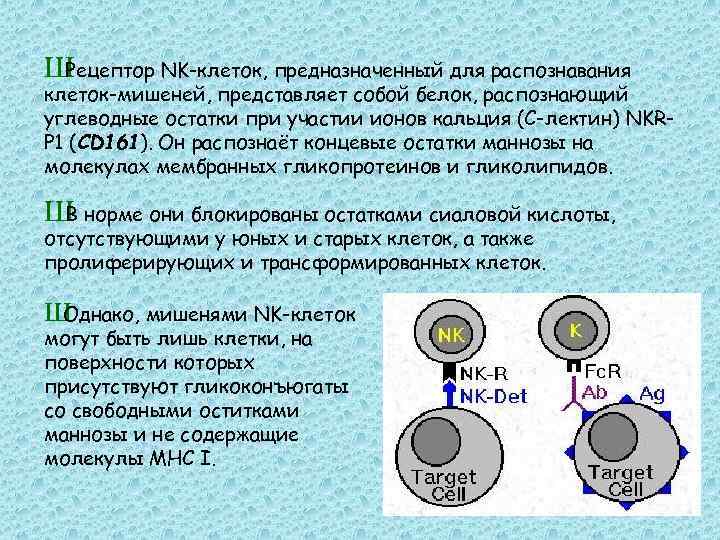 Ш Рецептор NK-клеток, предназначенный для распознавания клеток-мишеней, представляет собой белок, распознающий углеводные остатки при участии ионов кальция (С-лектин) NKRP 1 (CD 161). Он распознаёт концевые остатки маннозы на молекулах мембранных гликопротеинов и гликолипидов. Ш норме они блокированы остатками сиаловой кислоты, В отсутствующими у юных и старых клеток, а также пролиферирующих и трансформированных клеток. Ш Однако, мишенями NK-клеток могут быть лишь клетки, на поверхности которых присутствуют гликоконъюгаты со свободными оститками маннозы и не содержащие молекулы МНС I.
Ш Рецептор NK-клеток, предназначенный для распознавания клеток-мишеней, представляет собой белок, распознающий углеводные остатки при участии ионов кальция (С-лектин) NKRP 1 (CD 161). Он распознаёт концевые остатки маннозы на молекулах мембранных гликопротеинов и гликолипидов. Ш норме они блокированы остатками сиаловой кислоты, В отсутствующими у юных и старых клеток, а также пролиферирующих и трансформированных клеток. Ш Однако, мишенями NK-клеток могут быть лишь клетки, на поверхности которых присутствуют гликоконъюгаты со свободными оститками маннозы и не содержащие молекулы МНС I.
 v При соблюдении условий, определяемых узнаванием углеводных компонентов клеточной поверхности и отсутствием распознавания молекул МНС, происходит сближение NK-клеток с их мишенями. v Оно обусловлено связыванием рецептора с гликоконъюгатом и сопутствующими адгезивными взаимодействиями. В качестве участников этого взаимодействия рассматриваются различные адгезивные молекулы — CD 57, ганглиозиды, β-цепь ламинина, CD 2, различные типы интегринов, особенно β 2 -интегрин LFA-1, распознающий молекулы ICAM-1, 2 и 3. v Предполагают, что распознающие и распознаваемые молекулы при установлении контактов NK-клеток и клеток-мишеней могут меняться местами, поскольку и те и другие могут присутствовать как на киллерах, так и на их мишенях. Это должно способствовать упрочению контактов между клетками. Особое место в этом отношении занимает молекула Fcрецептора типа Fcγlll (CD 16), которая экспрессируется на значительной части NK-клеток. Поскольку эти рецепторы распознают Fc-порции иммуноглобулинов (Ig. G 3 и Ig. Gl), они обусловливают распознавание клеток, опсонизированных антителами соответствующих классов. v Конечным результатом такого распознавания является цитолиз, обозначаемый как антителозависимый клеточно опосредованный цитолиз (осуществляется К-клетками).
v При соблюдении условий, определяемых узнаванием углеводных компонентов клеточной поверхности и отсутствием распознавания молекул МНС, происходит сближение NK-клеток с их мишенями. v Оно обусловлено связыванием рецептора с гликоконъюгатом и сопутствующими адгезивными взаимодействиями. В качестве участников этого взаимодействия рассматриваются различные адгезивные молекулы — CD 57, ганглиозиды, β-цепь ламинина, CD 2, различные типы интегринов, особенно β 2 -интегрин LFA-1, распознающий молекулы ICAM-1, 2 и 3. v Предполагают, что распознающие и распознаваемые молекулы при установлении контактов NK-клеток и клеток-мишеней могут меняться местами, поскольку и те и другие могут присутствовать как на киллерах, так и на их мишенях. Это должно способствовать упрочению контактов между клетками. Особое место в этом отношении занимает молекула Fcрецептора типа Fcγlll (CD 16), которая экспрессируется на значительной части NK-клеток. Поскольку эти рецепторы распознают Fc-порции иммуноглобулинов (Ig. G 3 и Ig. Gl), они обусловливают распознавание клеток, опсонизированных антителами соответствующих классов. v Конечным результатом такого распознавания является цитолиз, обозначаемый как антителозависимый клеточно опосредованный цитолиз (осуществляется К-клетками).
 Кроме экзоцитоза перфорина и гранзимов, естественный киллер выделяет некоторые цитокины: ь ИФ-α, β и γ ь ИЛ-1 и 2 ь ФНОα и β ь КС- и хемотаксические факторы ь простагландины, β- эндорфин, серотонин, адреналин, мелатонин ИФ-γ в сочетании с ФНОα повышает активность NO-синтетазы, обеспечивая генерацию окиси азота — одного из основных факторов бактерицидности макрофагов. Кроме того, он аутокринный активатор естественных киллеров. В его присутствии наблюдается 5 -кратное ускорение лизиса. Он усиливает экспрессию мембранных протеиназ и других эффекторных факторов цитолиза. ИФ-γ обеспечивает условия для осуществления повторного проявления цитолитической активности естественных киллеров.
Кроме экзоцитоза перфорина и гранзимов, естественный киллер выделяет некоторые цитокины: ь ИФ-α, β и γ ь ИЛ-1 и 2 ь ФНОα и β ь КС- и хемотаксические факторы ь простагландины, β- эндорфин, серотонин, адреналин, мелатонин ИФ-γ в сочетании с ФНОα повышает активность NO-синтетазы, обеспечивая генерацию окиси азота — одного из основных факторов бактерицидности макрофагов. Кроме того, он аутокринный активатор естественных киллеров. В его присутствии наблюдается 5 -кратное ускорение лизиса. Он усиливает экспрессию мембранных протеиназ и других эффекторных факторов цитолиза. ИФ-γ обеспечивает условия для осуществления повторного проявления цитолитической активности естественных киллеров.
 Макрофаги o Для поддержания гомеостаза в тканях и при иммунном, воспалительном и патологическом ответах клетки погибают, включая механизмы апоптоза или некроза с выделением потенциальных продуктов повреждения. o Апоптозные клетки быстро и эффективно удаляются макрофагами.
Макрофаги o Для поддержания гомеостаза в тканях и при иммунном, воспалительном и патологическом ответах клетки погибают, включая механизмы апоптоза или некроза с выделением потенциальных продуктов повреждения. o Апоптозные клетки быстро и эффективно удаляются макрофагами.
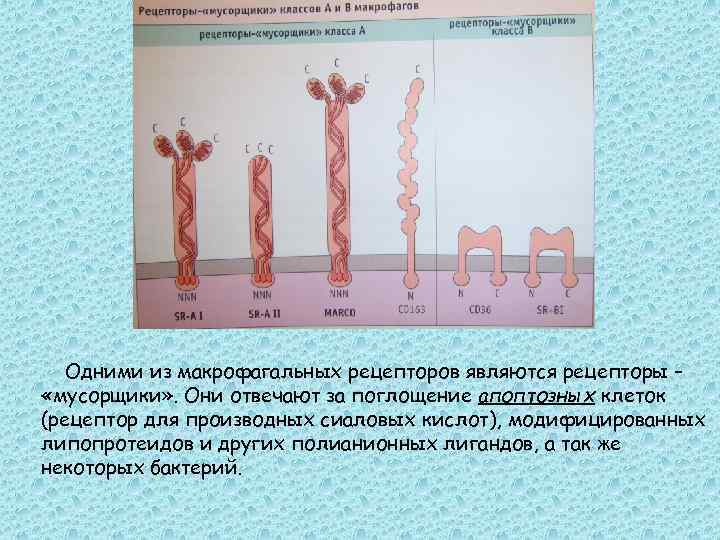 Одними из макрофагальных рецепторов являются рецепторы – «мусорщики» . Они отвечают за поглощение апоптозных клеток (рецептор для производных сиаловых кислот), модифицированных липопротеидов и других полианионных лигандов, а так же некоторых бактерий.
Одними из макрофагальных рецепторов являются рецепторы – «мусорщики» . Они отвечают за поглощение апоптозных клеток (рецептор для производных сиаловых кислот), модифицированных липопротеидов и других полианионных лигандов, а так же некоторых бактерий.
 • Наиболее изучен маннозный рецептор. Он содержит восемь лектиновых доменов С-типа и отдельный лектиновый домен в дистальном сегменте, связывающийся с сульфатированными гликиконъюгатами (этот домен богат цистеином). • Кроме того, клеточно- ассоциированные или растворимые маннозные прецепторы могут доставлять АГ В и/или Т-клеткам, модулируя их иммунный ответ. • Концевой домен маннозного рецептора также спосбствует клиренсу гормонов, содержащих сходные сульфатированные структуры. • DC-SIGN участвует о взаимодействиях между антигенпрезентирующими и Т-клетками и в микробном распознавании. • Дектин имеет внутриклеточный ITAM, отвечающий за поглощение грибов и внутриклеточную передачу сигнала.
• Наиболее изучен маннозный рецептор. Он содержит восемь лектиновых доменов С-типа и отдельный лектиновый домен в дистальном сегменте, связывающийся с сульфатированными гликиконъюгатами (этот домен богат цистеином). • Кроме того, клеточно- ассоциированные или растворимые маннозные прецепторы могут доставлять АГ В и/или Т-клеткам, модулируя их иммунный ответ. • Концевой домен маннозного рецептора также спосбствует клиренсу гормонов, содержащих сходные сульфатированные структуры. • DC-SIGN участвует о взаимодействиях между антигенпрезентирующими и Т-клетками и в микробном распознавании. • Дектин имеет внутриклеточный ITAM, отвечающий за поглощение грибов и внутриклеточную передачу сигнала.
 Предыдущие рецепторы участвовали в распознавании апоптозных клеток. Для узнавания некротизированных клеток и бактерий макрофагу необходимы: 1) Fc-рецепторы – опсонизирующие рецепторы для разных подклассов иммуноглобулинов. Содержат иммунорецепторные, основанные на тирозине ингибирующие мотивы (ITIM) и иммунорецепторные, основанные на тирозине ингибирующие мотивы (ITАM), которые взаимодействуют с другими молекулами мембраны, цитоплазматическими киназами и/или фосфатазами регулируют сложные сигнальные пути активации эффекторых ответов; 2) рецепторы комплемента - гетеродимерные рецепторы для С 3 продуктов расщепления: - CR 1 [CD 35] связывает С 3 b и С 4 b, обладает кофакторной и ускоряющей распад активностью, участвует в процессинге иммунных комплексов; - CR 3 [CD 11 b/CD 18] связывает i. C 3 b, участвует в клеточной адгезии (рецептор смешанного типа, имеет несколько лигандов, в т. ч. фибриноген; - CR 4 [CD 11 с/CD 18] связывает i. C 3 b, участвует в клеточной адгезии; 3) CD 14 – рецептор для комплекса бактериальных липополисахаридов.
Предыдущие рецепторы участвовали в распознавании апоптозных клеток. Для узнавания некротизированных клеток и бактерий макрофагу необходимы: 1) Fc-рецепторы – опсонизирующие рецепторы для разных подклассов иммуноглобулинов. Содержат иммунорецепторные, основанные на тирозине ингибирующие мотивы (ITIM) и иммунорецепторные, основанные на тирозине ингибирующие мотивы (ITАM), которые взаимодействуют с другими молекулами мембраны, цитоплазматическими киназами и/или фосфатазами регулируют сложные сигнальные пути активации эффекторых ответов; 2) рецепторы комплемента - гетеродимерные рецепторы для С 3 продуктов расщепления: - CR 1 [CD 35] связывает С 3 b и С 4 b, обладает кофакторной и ускоряющей распад активностью, участвует в процессинге иммунных комплексов; - CR 3 [CD 11 b/CD 18] связывает i. C 3 b, участвует в клеточной адгезии (рецептор смешанного типа, имеет несколько лигандов, в т. ч. фибриноген; - CR 4 [CD 11 с/CD 18] связывает i. C 3 b, участвует в клеточной адгезии; 3) CD 14 – рецептор для комплекса бактериальных липополисахаридов.
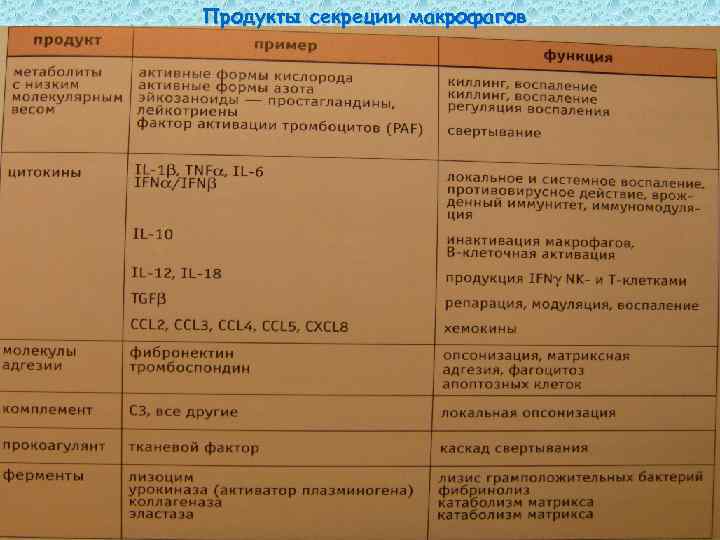 Продукты секреции макрофагов
Продукты секреции макрофагов
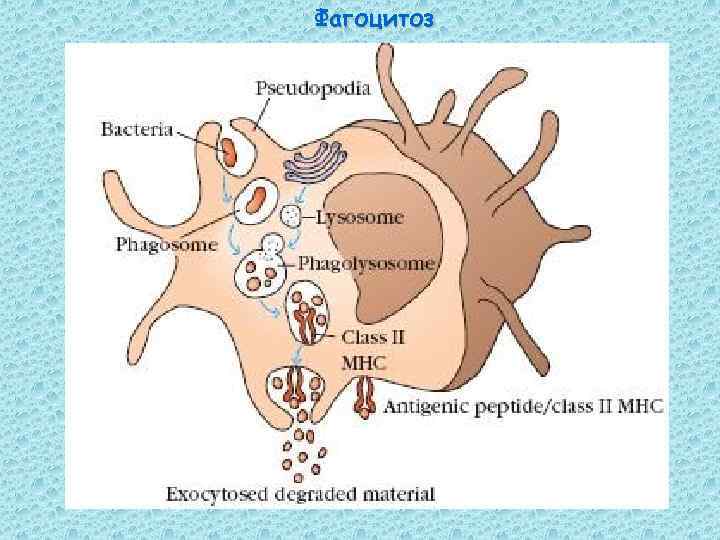 Фагоцитоз
Фагоцитоз
 Активированные различными стимулами макрофаги продуцируют более высокий уровень лизоцима и провоспалительных цитотоксинов, хемокинов, факторов роста и протеаз по сравнению с «покоящимися» макрофагами. v v Одно из главных отличий между ними – способность генерировать перекись водорода и другие кислородсодержащие метаболиты. v Кроме того, активированные макрофага могут экспрессировать высокий уровень индуцибельной синтазы оксида азота (i. NOS), катализирующей продукцию оксида азота (NO) из аргинина. v Секреция оксида азота макрофагами оказывает влияние на соседние сосуды и лейкоциты, способствует киллингу внутриклеточных патогенов.
Активированные различными стимулами макрофаги продуцируют более высокий уровень лизоцима и провоспалительных цитотоксинов, хемокинов, факторов роста и протеаз по сравнению с «покоящимися» макрофагами. v v Одно из главных отличий между ними – способность генерировать перекись водорода и другие кислородсодержащие метаболиты. v Кроме того, активированные макрофага могут экспрессировать высокий уровень индуцибельной синтазы оксида азота (i. NOS), катализирующей продукцию оксида азота (NO) из аргинина. v Секреция оксида азота макрофагами оказывает влияние на соседние сосуды и лейкоциты, способствует киллингу внутриклеточных патогенов.
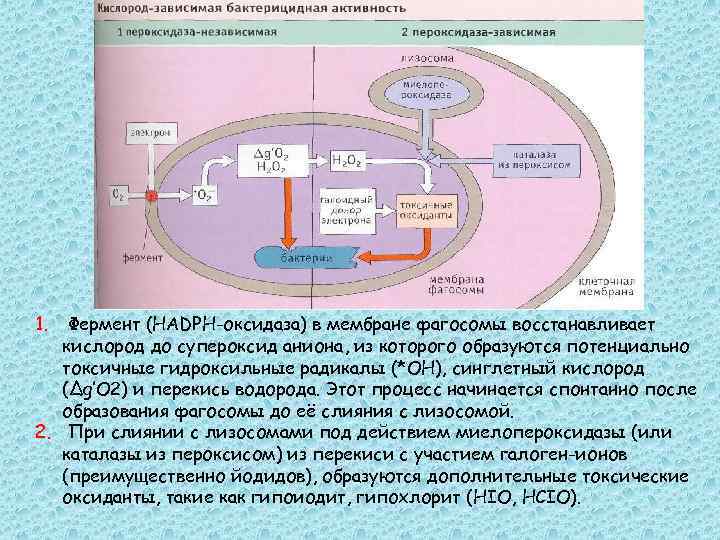 1. Фермент (HADPH-оксидаза) в мембране фагосомы восстанавливает кислород до супероксид аниона, из которого образуются потенциально токсичные гидроксильные радикалы (*ОН), синглетный кислород (Δg’O 2) и перекись водорода. Этот процесс начинается спонтанно после образования фагосомы до её слияния с лизосомой. 2. При слиянии с лизосомами под действием миелопероксидазы (или каталазы из пероксисом) из перекиси с участием галоген-ионов (преимущественно йодидов), образуются дополнительные токсические оксиданты, такие как гипоиодит, гипохлорит (HIO, HCIO).
1. Фермент (HADPH-оксидаза) в мембране фагосомы восстанавливает кислород до супероксид аниона, из которого образуются потенциально токсичные гидроксильные радикалы (*ОН), синглетный кислород (Δg’O 2) и перекись водорода. Этот процесс начинается спонтанно после образования фагосомы до её слияния с лизосомой. 2. При слиянии с лизосомами под действием миелопероксидазы (или каталазы из пероксисом) из перекиси с участием галоген-ионов (преимущественно йодидов), образуются дополнительные токсические оксиданты, такие как гипоиодит, гипохлорит (HIO, HCIO).
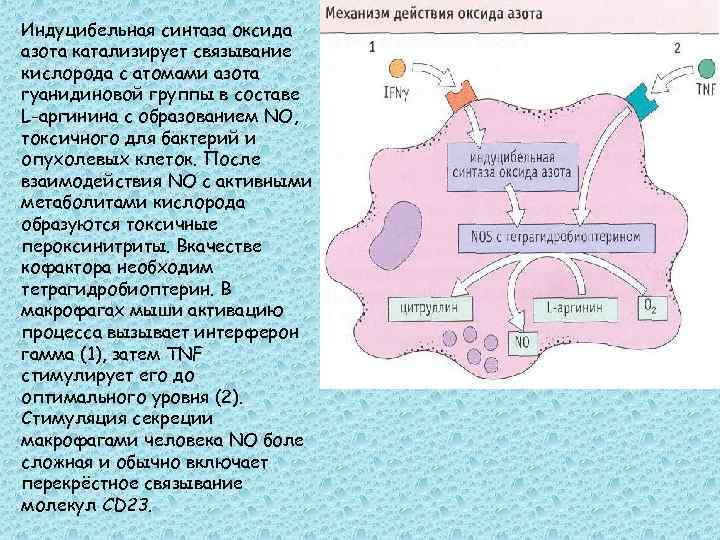 Индуцибельная синтаза оксида азота катализирует связывание кислорода с атомами азота гуанидиновой группы в составе L-аргинина с образованием NO, токсичного для бактерий и опухолевых клеток. После взаимодействия NO с активными метаболитами кислорода образуются токсичные пероксинитриты. Вкачестве кофактора необходим тетрагидробиоптерин. В макрофагах мыши активацию процесса вызывает интерферон гамма (1), затем TNF стимулирует его до оптимального уровня (2). Стимуляция секреции макрофагами человека NO боле сложная и обычно включает перекрёстное связывание молекул CD 23.
Индуцибельная синтаза оксида азота катализирует связывание кислорода с атомами азота гуанидиновой группы в составе L-аргинина с образованием NO, токсичного для бактерий и опухолевых клеток. После взаимодействия NO с активными метаболитами кислорода образуются токсичные пероксинитриты. Вкачестве кофактора необходим тетрагидробиоптерин. В макрофагах мыши активацию процесса вызывает интерферон гамма (1), затем TNF стимулирует его до оптимального уровня (2). Стимуляция секреции макрофагами человека NO боле сложная и обычно включает перекрёстное связывание молекул CD 23.



