Lecture_1.ppt
- Количество слайдов: 92
 КЛАСТЕРНЫЕ СОЕДИНЕНИЯ
КЛАСТЕРНЫЕ СОЕДИНЕНИЯ
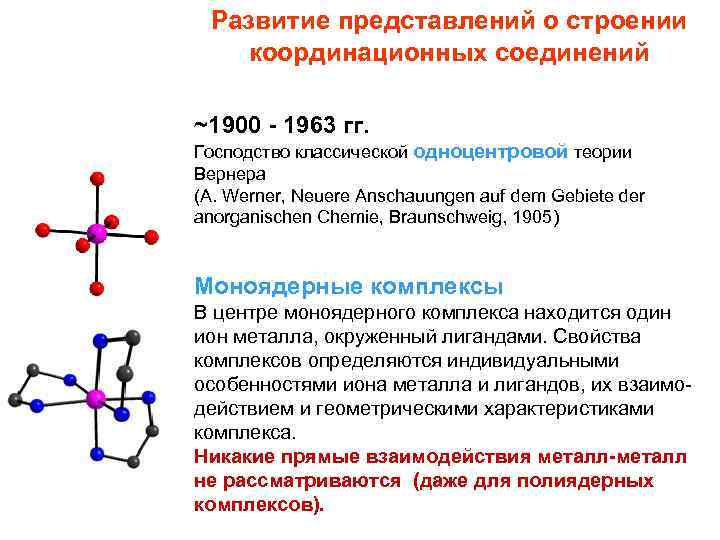 Развитие представлений о строении координационных соединений ~1900 - 1963 гг. Господство классической одноцентровой теории Вернера (A. Werner, Neuere Anschauungen auf dem Gebiete der anorganischen Chemie, Braunschweig, 1905) Моноядерные комплексы В центре моноядерного комплекса находится один ион металла, окруженный лигандами. Свойства комплексов определяются индивидуальными особенностями иона металла и лигандов, их взаимодействием и геометрическими характеристиками комплекса. Никакие прямые взаимодействия металл-металл не рассматриваются (даже для полиядерных комплексов).
Развитие представлений о строении координационных соединений ~1900 - 1963 гг. Господство классической одноцентровой теории Вернера (A. Werner, Neuere Anschauungen auf dem Gebiete der anorganischen Chemie, Braunschweig, 1905) Моноядерные комплексы В центре моноядерного комплекса находится один ион металла, окруженный лигандами. Свойства комплексов определяются индивидуальными особенностями иона металла и лигандов, их взаимодействием и геометрическими характеристиками комплекса. Никакие прямые взаимодействия металл-металл не рассматриваются (даже для полиядерных комплексов).
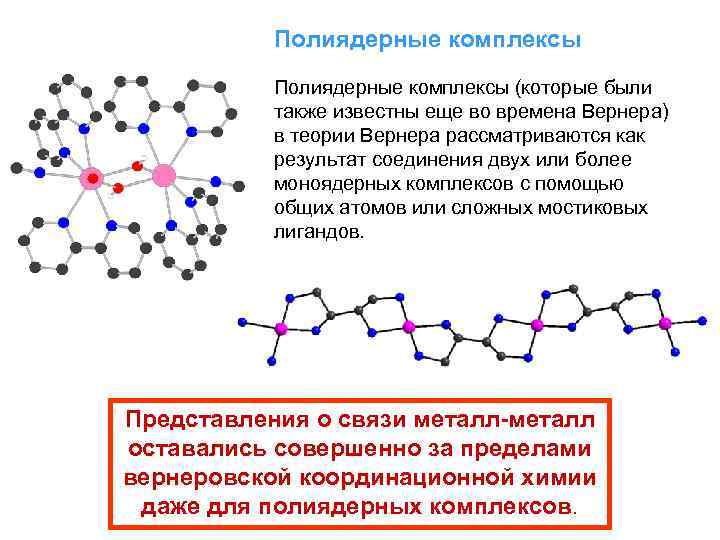 Полиядерные комплексы (которые были также известны еще во времена Вернера) в теории Вернера рассматриваются как результат соединения двух или более моноядерных комплексов с помощью общих атомов или сложных мостиковых лигандов. Представления о связи металл-металл оставались совершенно за пределами вернеровской координационной химии даже для полиядерных комплексов.
Полиядерные комплексы (которые были также известны еще во времена Вернера) в теории Вернера рассматриваются как результат соединения двух или более моноядерных комплексов с помощью общих атомов или сложных мостиковых лигандов. Представления о связи металл-металл оставались совершенно за пределами вернеровской координационной химии даже для полиядерных комплексов.
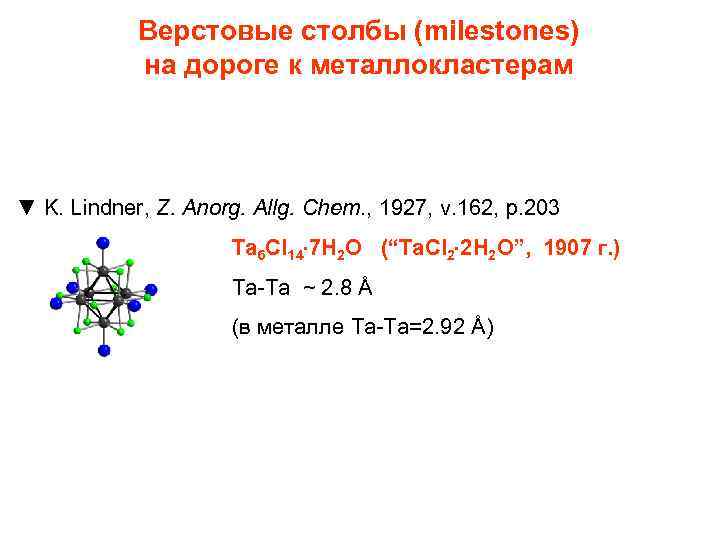 Верстовые столбы (milestones) на дороге к металлокластерам ▼ K. Lindner, Z. Anorg. Allg. Chem. , 1927, v. 162, p. 203 Ta 6 Cl 14 7 H 2 O (“Ta. Cl 2 2 H 2 O”, 1907 г. ) Ta-Ta ~ 2. 8 Å (в металле Ta-Ta=2. 92 Å)
Верстовые столбы (milestones) на дороге к металлокластерам ▼ K. Lindner, Z. Anorg. Allg. Chem. , 1927, v. 162, p. 203 Ta 6 Cl 14 7 H 2 O (“Ta. Cl 2 2 H 2 O”, 1907 г. ) Ta-Ta ~ 2. 8 Å (в металле Ta-Ta=2. 92 Å)
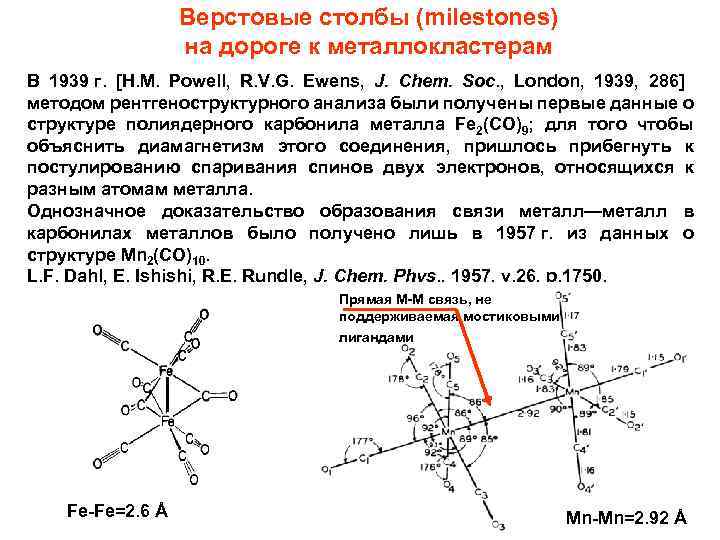 Верстовые столбы (milestones) на дороге к металлокластерам В 1939 г. [H. M. Powell, R. V. G. Ewens, J. Chem. Soc. , London, 1939, 286] методом рентгеноструктурного анализа были получены первые данные о структуре полиядерного карбонила металла Fе 2(СО)9; для того чтобы объяснить диамагнетизм этого соединения, пришлось прибегнуть к постулированию спаривания спинов двух электронов, относящихся к разным атомам металла. Однозначное доказательство образования связи металл—металл в карбонилах металлов было получено лишь в 1957 г. из данных о структуре Мn 2(СО)10. L. F. Dahl, E. Ishishi, R. E. Rundle, J. Chem. Phys. , 1957, v. 26, p. 1750. Прямая М-М связь, не поддерживаемая мостиковыми лигандами Fe-Fe=2. 6 Å Mn-Mn=2. 92 Å
Верстовые столбы (milestones) на дороге к металлокластерам В 1939 г. [H. M. Powell, R. V. G. Ewens, J. Chem. Soc. , London, 1939, 286] методом рентгеноструктурного анализа были получены первые данные о структуре полиядерного карбонила металла Fе 2(СО)9; для того чтобы объяснить диамагнетизм этого соединения, пришлось прибегнуть к постулированию спаривания спинов двух электронов, относящихся к разным атомам металла. Однозначное доказательство образования связи металл—металл в карбонилах металлов было получено лишь в 1957 г. из данных о структуре Мn 2(СО)10. L. F. Dahl, E. Ishishi, R. E. Rundle, J. Chem. Phys. , 1957, v. 26, p. 1750. Прямая М-М связь, не поддерживаемая мостиковыми лигандами Fe-Fe=2. 6 Å Mn-Mn=2. 92 Å
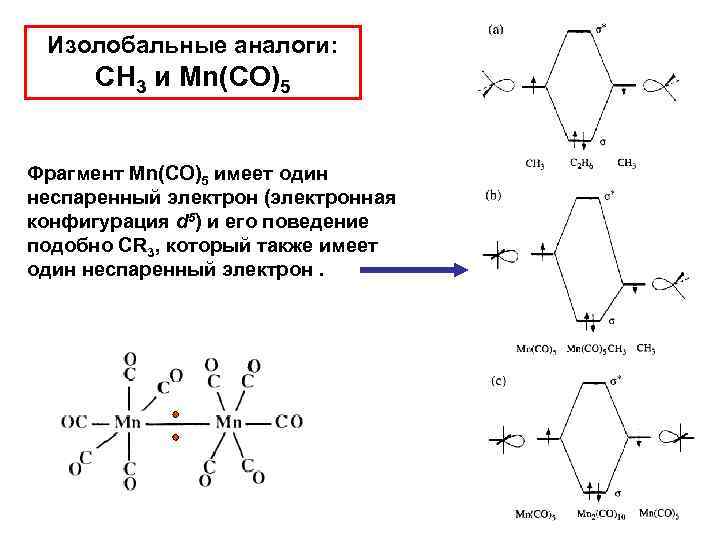 Изолобальные аналоги: CH 3 и Mn(CO)5 Фрагмент Mn(CO)5 имеет один неспаренный электрон (электронная конфигурация d 5) и его поведение подобно CR 3, который также имеет один неспаренный электрон.
Изолобальные аналоги: CH 3 и Mn(CO)5 Фрагмент Mn(CO)5 имеет один неспаренный электрон (электронная конфигурация d 5) и его поведение подобно CR 3, который также имеет один неспаренный электрон.
 Изолобальная аналогия • Определение: Два “фрагмента” называются изолобальными если их граничные орбитали: a) имеют подобную симметрию, б) имеют приблизительно одинаковую энергию и в) одинаковое число электронов. • Изолобальная аналогия позволяет связать структурные принципы органических, неорганических и металлорганических соединений и найти общее в ряду CH 3, NH 2, OH, F, Cl, Co(CO)4 , Cp. Mo(CO)3 • • Эти «фрагменты» или “строительные блоки” могут замещать друга в cложных структурах. Например, можно построить ряды: CH 3 -CH 3, NH 2 -NH 2, HO-OH, F-F, Cl-Cl, (CO)4 Co-Co(CO)4, Cp. Mo(CO)3 -Mo(CO)3 Cp CH 3 -NH 2, CH 3 -OH, CH 3 -F, CH 3 -Cl, CH 3 -Co(CO)4, CH 3 -Mo(CO)3 Cp NH 2 -OH, NH 2 -F, NH 2 -Cl, NH 2 -Co(CO)4, NH 2 -Mo(CO)3 Cp etc.
Изолобальная аналогия • Определение: Два “фрагмента” называются изолобальными если их граничные орбитали: a) имеют подобную симметрию, б) имеют приблизительно одинаковую энергию и в) одинаковое число электронов. • Изолобальная аналогия позволяет связать структурные принципы органических, неорганических и металлорганических соединений и найти общее в ряду CH 3, NH 2, OH, F, Cl, Co(CO)4 , Cp. Mo(CO)3 • • Эти «фрагменты» или “строительные блоки” могут замещать друга в cложных структурах. Например, можно построить ряды: CH 3 -CH 3, NH 2 -NH 2, HO-OH, F-F, Cl-Cl, (CO)4 Co-Co(CO)4, Cp. Mo(CO)3 -Mo(CO)3 Cp CH 3 -NH 2, CH 3 -OH, CH 3 -F, CH 3 -Cl, CH 3 -Co(CO)4, CH 3 -Mo(CO)3 Cp NH 2 -OH, NH 2 -F, NH 2 -Cl, NH 2 -Co(CO)4, NH 2 -Mo(CO)3 Cp etc.
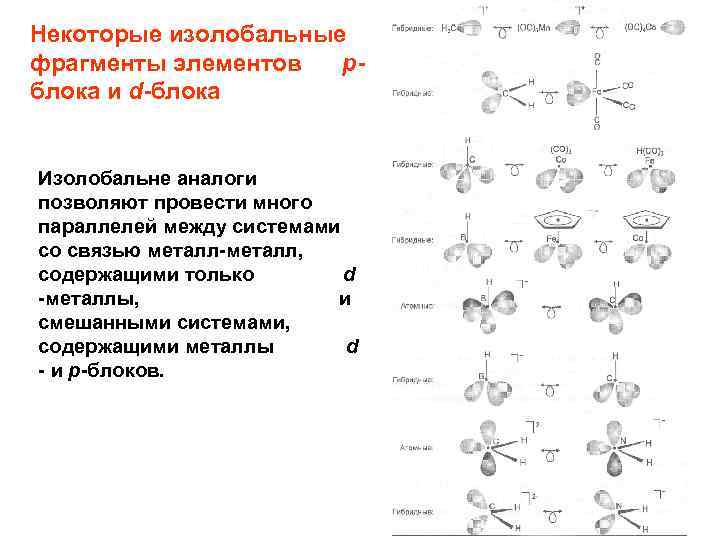 Некоторые изолобальные фрагменты элементов рблока и d-блока Изолобальне аналоги позволяют провести много параллелей между системами со связью металл-металл, содержащими только d -металлы, и смешанными системами, содержащими металлы d - и p-блоков.
Некоторые изолобальные фрагменты элементов рблока и d-блока Изолобальне аналоги позволяют провести много параллелей между системами со связью металл-металл, содержащими только d -металлы, и смешанными системами, содержащими металлы d - и p-блоков.
 Верстовые столбы (milestones) на дороге к металлокластерам В 1946 г. Броссетом было показано, что низший хлорид молибдена содержит октаэдрические группировки из атомов металла с межатомным расстоянием Мо—Мо, даже более коротким (~ 2. 6 Å), чем в металлическом молибдене (2. 725 Å). Броссет, по-видимому, был одним из первых, кто обратил внимание на оригинальность подобных соединений: он назвал эту группу соединений стафилоядерными. Staphylé (греческий) – виноградная гроздь. К сожалению, этот термин не получил распространения и был предан забвению. ▼ C. Brosset, Arkiv Kemi, Miner. Geol. , 1946, v. A 22, p. 10 Mo 6 Cl 12 Mo-Mo ~ 2. 6 Å (в металле Mo-Mo=2. 725 Å)
Верстовые столбы (milestones) на дороге к металлокластерам В 1946 г. Броссетом было показано, что низший хлорид молибдена содержит октаэдрические группировки из атомов металла с межатомным расстоянием Мо—Мо, даже более коротким (~ 2. 6 Å), чем в металлическом молибдене (2. 725 Å). Броссет, по-видимому, был одним из первых, кто обратил внимание на оригинальность подобных соединений: он назвал эту группу соединений стафилоядерными. Staphylé (греческий) – виноградная гроздь. К сожалению, этот термин не получил распространения и был предан забвению. ▼ C. Brosset, Arkiv Kemi, Miner. Geol. , 1946, v. A 22, p. 10 Mo 6 Cl 12 Mo-Mo ~ 2. 6 Å (в металле Mo-Mo=2. 725 Å)
 Верстовые столбы (milestones) на дороге к металлокластерам Принципиально важным этапом в исследовании «невернеровских» координационных соединений явились работы, выполненные в начале шестидесятых годов прошедшего столетия в России (Козьмин П. А. , Кузнецов В. Г. , Тронев В. Г. ) и в США (F. A. Cotton с сотрудниками) по синтезу и изучению структуры галогенидных комплексов рения Re(III) [d 4 электронная конфигурация] с кратными связями металл-металл.
Верстовые столбы (milestones) на дороге к металлокластерам Принципиально важным этапом в исследовании «невернеровских» координационных соединений явились работы, выполненные в начале шестидесятых годов прошедшего столетия в России (Козьмин П. А. , Кузнецов В. Г. , Тронев В. Г. ) и в США (F. A. Cotton с сотрудниками) по синтезу и изучению структуры галогенидных комплексов рения Re(III) [d 4 электронная конфигурация] с кратными связями металл-металл.
 ▼ В. Г. Кузнецов, П. А. Козьмин, Журн. структ. химии, 1963, т. 4, с. 55; Тезисы докл. IV совещания по кристаллохимии, Кишинев, 1961, с. 74 -75. [Re 2 Cl 8]2 - “(py. H)HRe. Cl 4” Re-Re ~ 2. 24 Å (4 -х кратные связи) (в металле Re-Re=2. 75 Å) ▼ J. A. Bertrand, F. A. Cotton, W. A. Dollase, JACS, 1963, v. 85, p. 1349; Inorg. Chem. , 1963, v. 2, p. 1166. Re 3 Cl 9 (K 3 Re 3 Cl 12 = “KRe. Cl 4”) Re-Re ~ 2. 47 Å (2 -х кратные связи) (в металле Re-Re=2. 75 Å)
▼ В. Г. Кузнецов, П. А. Козьмин, Журн. структ. химии, 1963, т. 4, с. 55; Тезисы докл. IV совещания по кристаллохимии, Кишинев, 1961, с. 74 -75. [Re 2 Cl 8]2 - “(py. H)HRe. Cl 4” Re-Re ~ 2. 24 Å (4 -х кратные связи) (в металле Re-Re=2. 75 Å) ▼ J. A. Bertrand, F. A. Cotton, W. A. Dollase, JACS, 1963, v. 85, p. 1349; Inorg. Chem. , 1963, v. 2, p. 1166. Re 3 Cl 9 (K 3 Re 3 Cl 12 = “KRe. Cl 4”) Re-Re ~ 2. 47 Å (2 -х кратные связи) (в металле Re-Re=2. 75 Å)
 1963 год – начало год «невернеровской» координационной химии Широкое использование рентгеноструктурного анализа как главного метода характеризации комплексов
1963 год – начало год «невернеровской» координационной химии Широкое использование рентгеноструктурного анализа как главного метода характеризации комплексов
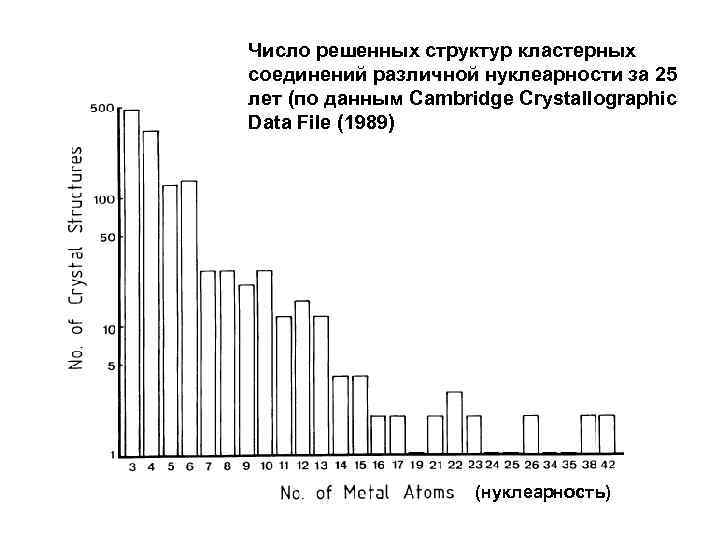 Число решенных структур кластерных соединений различной нуклеарности за 25 лет (по данным Cambridge Crystallographic Data File (1989) (нуклеарность)
Число решенных структур кластерных соединений различной нуклеарности за 25 лет (по данным Cambridge Crystallographic Data File (1989) (нуклеарность)
 В 1964 году американский химик проф. F. Albert Cotton ввел в координационную химию термин МЕТАЛЛОКЛАСТЕР: “Metal atom cluster is a finite group of metal atoms that are held together mainly, or at least to a significant extent, by bonds directly between the metal atoms, even though some nonmetal atoms may also be intimately associated with the cluster”. (Cotton F. A. , Inorg. Chem. , 1964, v. 3, 1217) МЕТАЛЛОКЛАСТЕР – это ограниченная группа атомов металла, которые удерживаются вместе главным образом (или по крайней мере в существенной степени) непосредственно связями между атомами металлов, даже если некоторые атомы неметаллов могут быть также тесно связанными с кластером. Cluster (англ. ) – гроздь, группа, рой пчел, скопление однородных предметов
В 1964 году американский химик проф. F. Albert Cotton ввел в координационную химию термин МЕТАЛЛОКЛАСТЕР: “Metal atom cluster is a finite group of metal atoms that are held together mainly, or at least to a significant extent, by bonds directly between the metal atoms, even though some nonmetal atoms may also be intimately associated with the cluster”. (Cotton F. A. , Inorg. Chem. , 1964, v. 3, 1217) МЕТАЛЛОКЛАСТЕР – это ограниченная группа атомов металла, которые удерживаются вместе главным образом (или по крайней мере в существенной степени) непосредственно связями между атомами металлов, даже если некоторые атомы неметаллов могут быть также тесно связанными с кластером. Cluster (англ. ) – гроздь, группа, рой пчел, скопление однородных предметов
 Cluster (англ. ) – гроздь, группа, рой пчел, скопление однородных предметов
Cluster (англ. ) – гроздь, группа, рой пчел, скопление однородных предметов
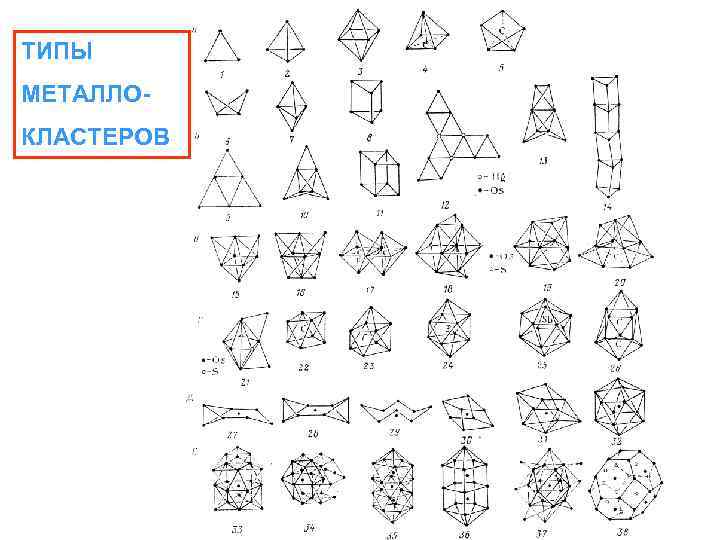 ТИПЫ МЕТАЛЛОКЛАСТЕРОВ
ТИПЫ МЕТАЛЛОКЛАСТЕРОВ
 F. Albert Cotton was born in Philadelphia, PA in 1930 and received his A. B. and Ph. D. degrees from Temple and Harvard Universities, respectively. He was on the faculty of MIT from 1955 to 1971 and has been at Texas A&M since 1972. He has been recognized by both ACS awards in inorganic chemistry, the ACS Priestley Medal, the AIC Gold Medal, the Robert A. Welch Prize, the King Faisal Prize, the Paracelsus Prize, the Wolf Prize and the National Medal of Science. His interests have been in inorganic, organometallic and structural chemistry. He discovered the existence of quadruple bonds, as well as related triple, double and single bonds in a similar structural context, and has explored their chemistry extensively. February 2007
F. Albert Cotton was born in Philadelphia, PA in 1930 and received his A. B. and Ph. D. degrees from Temple and Harvard Universities, respectively. He was on the faculty of MIT from 1955 to 1971 and has been at Texas A&M since 1972. He has been recognized by both ACS awards in inorganic chemistry, the ACS Priestley Medal, the AIC Gold Medal, the Robert A. Welch Prize, the King Faisal Prize, the Paracelsus Prize, the Wolf Prize and the National Medal of Science. His interests have been in inorganic, organometallic and structural chemistry. He discovered the existence of quadruple bonds, as well as related triple, double and single bonds in a similar structural context, and has explored their chemistry extensively. February 2007
 Prof. Arndt Simon (14. 01. 1940, Dresden) 1960 -1964 Chemistry Studies and Diploma at University Münster; 1964 -1966 Thesis with Harald Schäfer; 1967 -1971 Habilitation; 1972 (Associate) Professor in Münster; 1974 - Member of the Max-Planck Society; Director at "Max-Planck-Institut für Festkörperforschung", Stuttgart; 1975 - Honorary Professor at University Stuttgart. Topics: Alkali Metal Suboxides; Subnitrides of Alkaline Earth Metals; Metalrich Halides and Oxides of Heavy d-Metals; Condensed Clusters; Interstitial Atoms in Metal Clusters; Metalrich Binary and Ternary Halides of Lanthanides; Thorium Cluster Compounds; Intermetallic Compounds (Pauling-Simon Rule); Structures and Phase Transitions in Molecular Crystals; Structure Property Relations (Photo Cathodes, Amorphous Metals, Magnetic Order and Frustration, Spin Crossover, Spin Glasses); Superconductivity
Prof. Arndt Simon (14. 01. 1940, Dresden) 1960 -1964 Chemistry Studies and Diploma at University Münster; 1964 -1966 Thesis with Harald Schäfer; 1967 -1971 Habilitation; 1972 (Associate) Professor in Münster; 1974 - Member of the Max-Planck Society; Director at "Max-Planck-Institut für Festkörperforschung", Stuttgart; 1975 - Honorary Professor at University Stuttgart. Topics: Alkali Metal Suboxides; Subnitrides of Alkaline Earth Metals; Metalrich Halides and Oxides of Heavy d-Metals; Condensed Clusters; Interstitial Atoms in Metal Clusters; Metalrich Binary and Ternary Halides of Lanthanides; Thorium Cluster Compounds; Intermetallic Compounds (Pauling-Simon Rule); Structures and Phase Transitions in Molecular Crystals; Structure Property Relations (Photo Cathodes, Amorphous Metals, Magnetic Order and Frustration, Spin Crossover, Spin Glasses); Superconductivity

 John D. Corbett was born in Yakima, WA, in 1926. B. S. (1948), Ph. D. (1952, physical chemistry) degrees at the University of Washington. He has been associated with the Department of Chemistry and Ames Laboratory (DOE) at Iowa State University ever since, where he is presently Professor of Chemistry, Distinguished Professor in the College of Liberal Arts and Sciences, and Senior Chemist. The general longterm focus of his program has been wide-ranging exploratory synthesis along metal-salt interfaces coupled with structural and bonding characterizations. Corbett earlier received the 1986 ACS Award in Inorganic Chemistry, an Alexander von Humboldt Senior Scientist Award, and two Department of Energy Awards in Materials Chemistry. He is a member of the National Academy of Sciences.
John D. Corbett was born in Yakima, WA, in 1926. B. S. (1948), Ph. D. (1952, physical chemistry) degrees at the University of Washington. He has been associated with the Department of Chemistry and Ames Laboratory (DOE) at Iowa State University ever since, where he is presently Professor of Chemistry, Distinguished Professor in the College of Liberal Arts and Sciences, and Senior Chemist. The general longterm focus of his program has been wide-ranging exploratory synthesis along metal-salt interfaces coupled with structural and bonding characterizations. Corbett earlier received the 1986 ACS Award in Inorganic Chemistry, an Alexander von Humboldt Senior Scientist Award, and two Department of Energy Awards in Materials Chemistry. He is a member of the National Academy of Sciences.
 Как можно увидеть, Коттон по существу повторил определение Броссета (см. об этом выше), заменив греческое стафилоядерный (Staphylé – виноградная гроздь) на английское кластерный (Cluster [англ. ] – гроздь, группа, рой пчел, скопление однородных предметов). Может быть, единственно важным дополнением в формулировке Коттона является уточнение о том, что атомы металла в металлокластере должны быть связаны непосредственно, то есть, должны реализоваться прямые металл-металл связи. Любое определение несовершенно! Новосибирск – это то место, где интенсивно обсуждались формулировки и другие концептуальные определения кластерной химии в начале ее зарождения.
Как можно увидеть, Коттон по существу повторил определение Броссета (см. об этом выше), заменив греческое стафилоядерный (Staphylé – виноградная гроздь) на английское кластерный (Cluster [англ. ] – гроздь, группа, рой пчел, скопление однородных предметов). Может быть, единственно важным дополнением в формулировке Коттона является уточнение о том, что атомы металла в металлокластере должны быть связаны непосредственно, то есть, должны реализоваться прямые металл-металл связи. Любое определение несовершенно! Новосибирск – это то место, где интенсивно обсуждались формулировки и другие концептуальные определения кластерной химии в начале ее зарождения.
 Metal Cluster A metal atom cluster may be defined as a group of two or more metal atoms in which there are substantial and direct bonds between the metal atoms. F. A. Cotton, G. Wilkinson, C. A. Murillo, M. Bochmann, Advanced Inorganic Chemistry 5 th ed. (Wiley, New York, p. 1053, 1988).
Metal Cluster A metal atom cluster may be defined as a group of two or more metal atoms in which there are substantial and direct bonds between the metal atoms. F. A. Cotton, G. Wilkinson, C. A. Murillo, M. Bochmann, Advanced Inorganic Chemistry 5 th ed. (Wiley, New York, p. 1053, 1988).
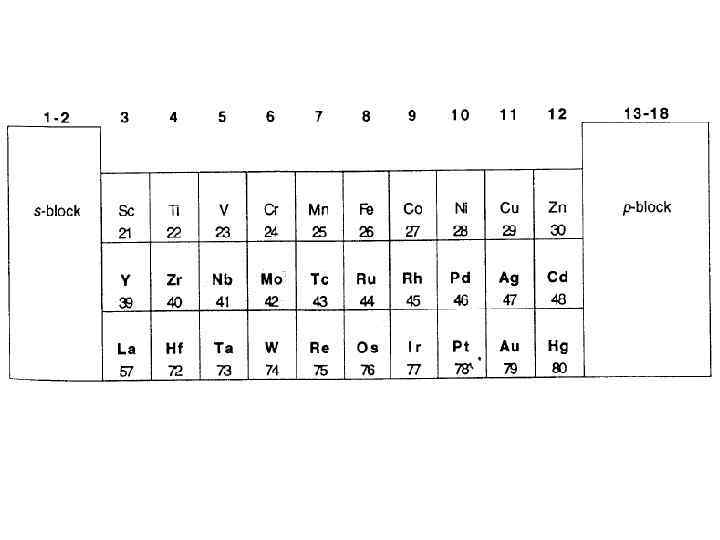
 Периодическая таблица элементов
Периодическая таблица элементов
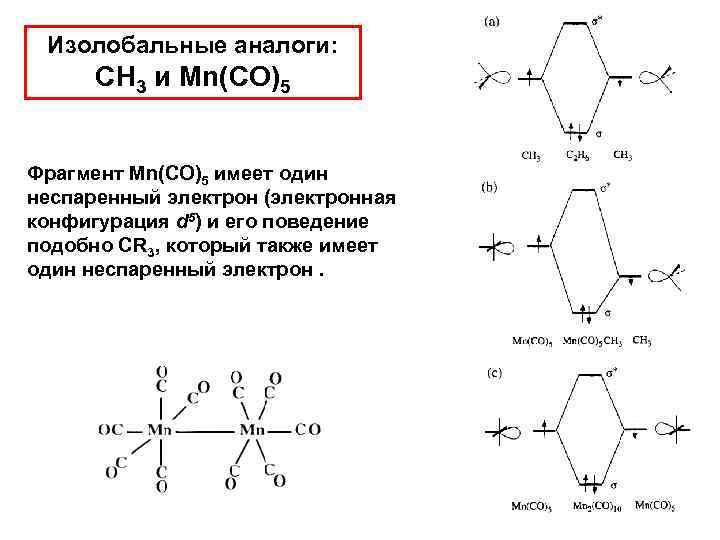 Изолобальные аналоги: CH 3 и Mn(CO)5 Фрагмент Mn(CO)5 имеет один неспаренный электрон (электронная конфигурация d 5) и его поведение подобно CR 3, который также имеет один неспаренный электрон.
Изолобальные аналоги: CH 3 и Mn(CO)5 Фрагмент Mn(CO)5 имеет один неспаренный электрон (электронная конфигурация d 5) и его поведение подобно CR 3, который также имеет один неспаренный электрон.
 Возможные взаимодействия между ионами переходных металлов с различной электронной конфигурацией dn (n - число валентных электронов у иона металла) Простейший случай: биядерные комплексы Ионы металла находятся в высшей степени окисления; электронная конфигурация d 0; образование связи металл-металл невозможно. Расстояния между атомами металла большие. d 0 • • d 1 • • Ионы металла имеют d 1 электронную конфигурацию: 1. Электроны локализованы на металлических центрах. Связь металл-металл отсутствует. Расстояния между атомами металла большие. Возможны обменные взаимодействия спинов через лиганды. 2. Электроны обоих атомов используются на образование локализованной ковалентной двухэлектронной двухцентровой (2 е 2 с) связи металл-металл с коротким расстоянием М-М. • •
Возможные взаимодействия между ионами переходных металлов с различной электронной конфигурацией dn (n - число валентных электронов у иона металла) Простейший случай: биядерные комплексы Ионы металла находятся в высшей степени окисления; электронная конфигурация d 0; образование связи металл-металл невозможно. Расстояния между атомами металла большие. d 0 • • d 1 • • Ионы металла имеют d 1 электронную конфигурацию: 1. Электроны локализованы на металлических центрах. Связь металл-металл отсутствует. Расстояния между атомами металла большие. Возможны обменные взаимодействия спинов через лиганды. 2. Электроны обоих атомов используются на образование локализованной ковалентной двухэлектронной двухцентровой (2 е 2 с) связи металл-металл с коротким расстоянием М-М. • •
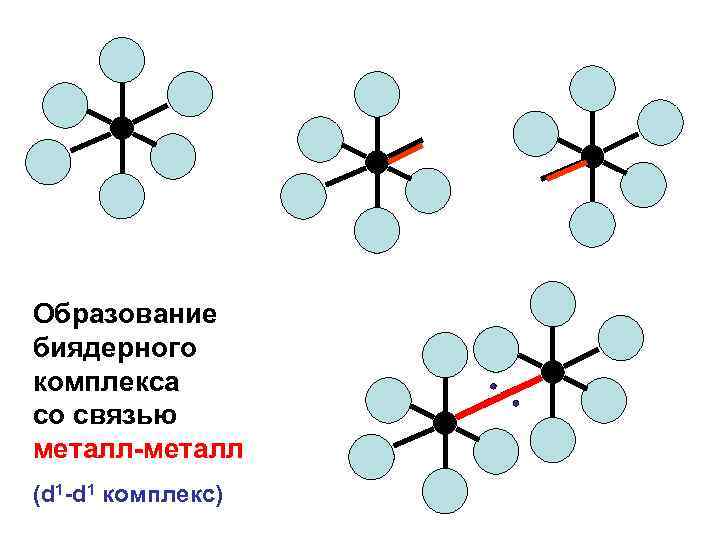 Образование биядерного комплекса со связью металл-металл (d 1 -d 1 комплекс)
Образование биядерного комплекса со связью металл-металл (d 1 -d 1 комплекс)
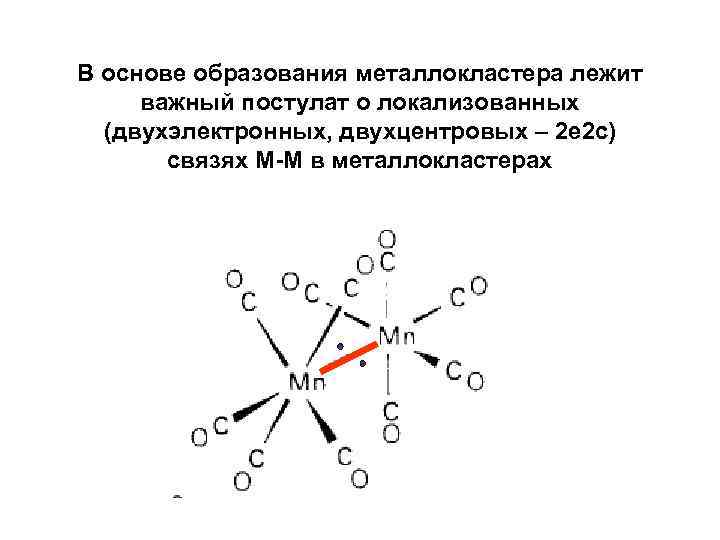 В основе образования металлокластера лежит важный постулат о локализованных (двухэлектронных, двухцентровых – 2 е 2 с) связях М-М в металлокластерах
В основе образования металлокластера лежит важный постулат о локализованных (двухэлектронных, двухцентровых – 2 е 2 с) связях М-М в металлокластерах
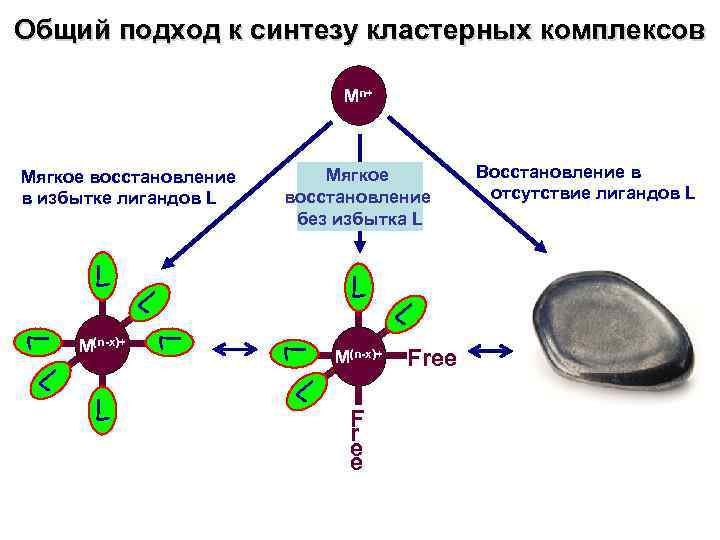 Общий подход к синтезу кластерных комплексов Mn+ Мягкое восстановление в избытке лигандов L Мягкое восстановление без избытка L L L M(n-x)+ L L L F r e e Free Восстановление в отсутствие лигандов L
Общий подход к синтезу кластерных комплексов Mn+ Мягкое восстановление в избытке лигандов L Мягкое восстановление без избытка L L L M(n-x)+ L L L F r e e Free Восстановление в отсутствие лигандов L
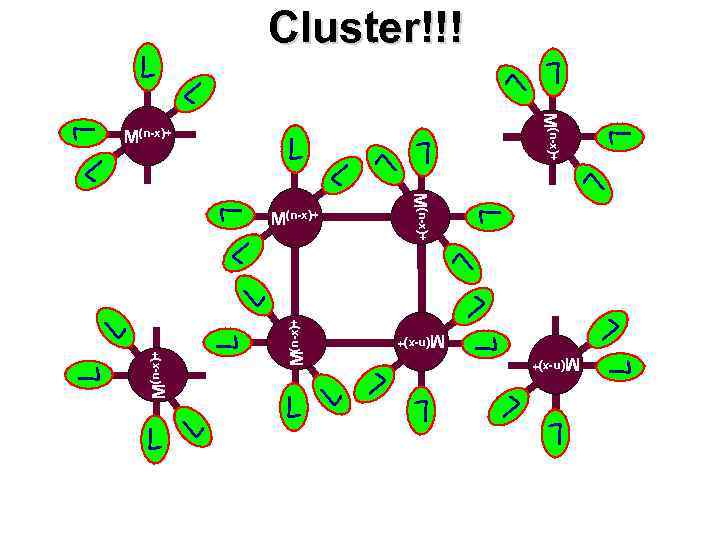 Cluster!!! L L L L L M(n-x)+ L L M(n-x)+ L L L L M(n-x)+ L L
Cluster!!! L L L L L M(n-x)+ L L M(n-x)+ L L L L M(n-x)+ L L
 B C
B C
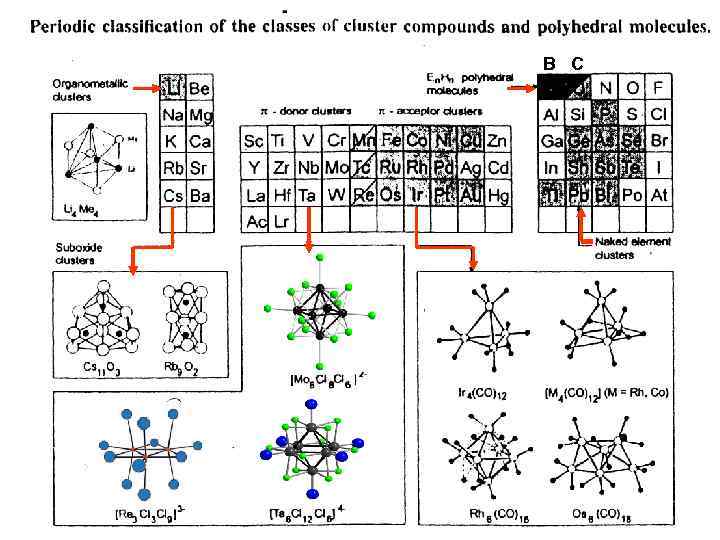
 Кластеры переходных металлов обычно стабилизируются лигандами. Кластеры пост-переходных элементов существуют без лигандов, и поэтому они получили название безлигандных кластеров (в англоязычной литературе – Naked Clusters; naked - голый, нагой; обнаженный). Кластеры переходных металлов обычно кристаллизуются в высокосимметричных структурах (платоновы или архимедовы тела). Безлигандные кластеры пост-переходных элементов, наоборот, часто имеют неправильные структуры.
Кластеры переходных металлов обычно стабилизируются лигандами. Кластеры пост-переходных элементов существуют без лигандов, и поэтому они получили название безлигандных кластеров (в англоязычной литературе – Naked Clusters; naked - голый, нагой; обнаженный). Кластеры переходных металлов обычно кристаллизуются в высокосимметричных структурах (платоновы или архимедовы тела). Безлигандные кластеры пост-переходных элементов, наоборот, часто имеют неправильные структуры.
 Под термином "нанотехнологии" Российская корпорация нанотехнологий РОСНАНО понимает совокупность технологических методов и приемов, используемых при изучении, проектировании, производстве и применении структур, устройств и систем, включающих целенаправленный контроль и модификацию формы, размера, интеграции и взаимодействия составляющих их отдельных наномасштабных элементов (с характерными размерами порядка 100 нм и меньше), наличие которых определяет ключевые характеристики и свойства получаемых продуктов. Объектами нанотехнологий могут быть как непосредственно низкоразмерные объекты - наноэлементы с характерными размерами как минимум по одному измерению (наночастицы, нанопорошки, нанотрубки, нановолокна, нанопленки), так и макроскопические объекты (объемные материалы, отдельные элементы устройств и систем), структура которых контролируемо создается с разрешением на уровне отдельных наноэлементов. При этом под устройствами или системами, изготовленными с использованием нанотехнологий, понимаются таковые, в которых как минимум один компонент является объектом нанотехнологий (т. е. существует как минимум одна стадия технологического процесса, результатом которой является объект нанотехнологий).
Под термином "нанотехнологии" Российская корпорация нанотехнологий РОСНАНО понимает совокупность технологических методов и приемов, используемых при изучении, проектировании, производстве и применении структур, устройств и систем, включающих целенаправленный контроль и модификацию формы, размера, интеграции и взаимодействия составляющих их отдельных наномасштабных элементов (с характерными размерами порядка 100 нм и меньше), наличие которых определяет ключевые характеристики и свойства получаемых продуктов. Объектами нанотехнологий могут быть как непосредственно низкоразмерные объекты - наноэлементы с характерными размерами как минимум по одному измерению (наночастицы, нанопорошки, нанотрубки, нановолокна, нанопленки), так и макроскопические объекты (объемные материалы, отдельные элементы устройств и систем), структура которых контролируемо создается с разрешением на уровне отдельных наноэлементов. При этом под устройствами или системами, изготовленными с использованием нанотехнологий, понимаются таковые, в которых как минимум один компонент является объектом нанотехнологий (т. е. существует как минимум одна стадия технологического процесса, результатом которой является объект нанотехнологий).
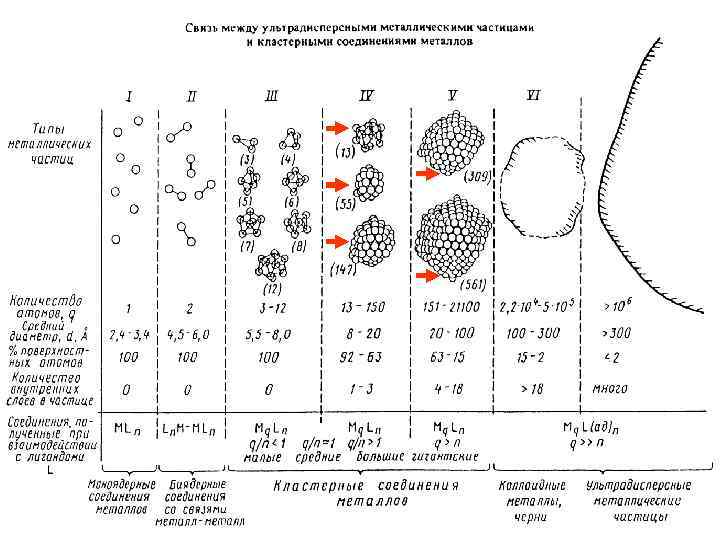
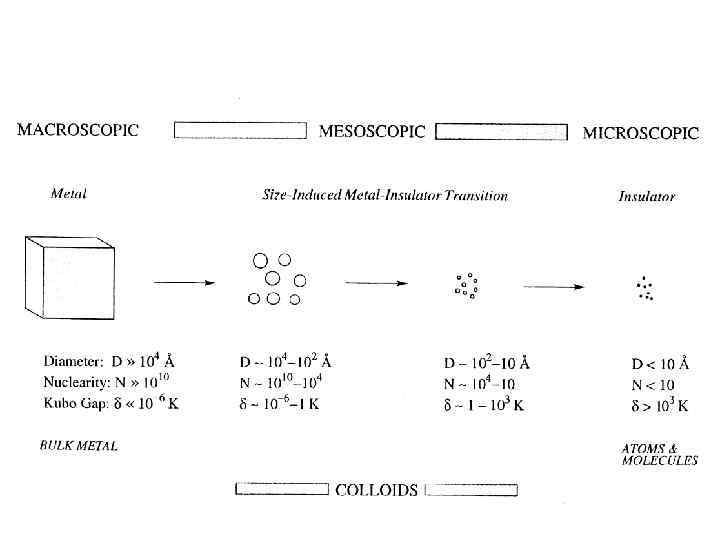
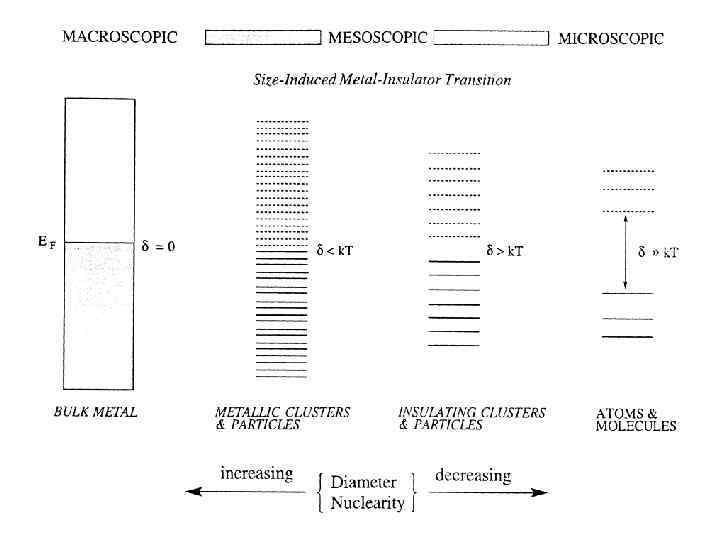
 Кластеры Mn с «магическим» числом атомов металла n, которые получаются при окружении данного атома последовательными оболочками атомов (иллюстрация предполагает кубооктаэдрическую упаковку) Структуры многих металлов представляют собой плотную упаковку одинаковых шаров (приближение жестких сфер), в которой каждый шар имеет 12 соседей (КЧ=12). Простейшим плотноупакованным металлокластером является фрагмент М 13. При такой укладке объем незанятого пространства равен 26%.
Кластеры Mn с «магическим» числом атомов металла n, которые получаются при окружении данного атома последовательными оболочками атомов (иллюстрация предполагает кубооктаэдрическую упаковку) Структуры многих металлов представляют собой плотную упаковку одинаковых шаров (приближение жестких сфер), в которой каждый шар имеет 12 соседей (КЧ=12). Простейшим плотноупакованным металлокластером является фрагмент М 13. При такой укладке объем незанятого пространства равен 26%.
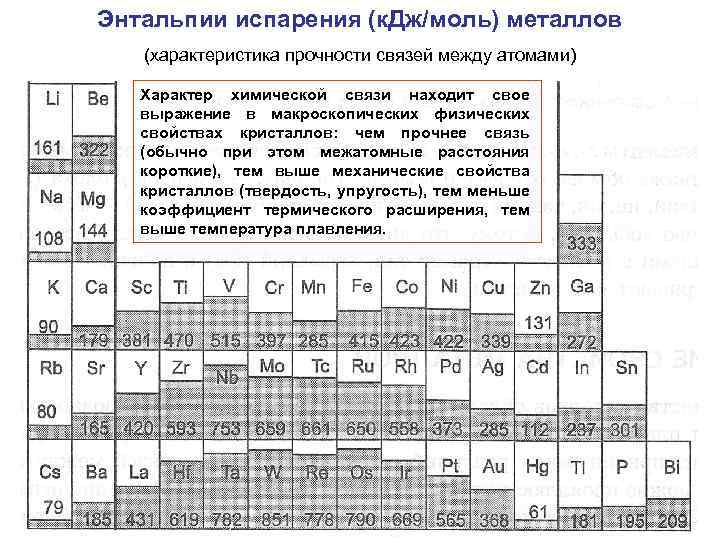 Энтальпии испарения (к. Дж/моль) металлов (характеристика прочности связей между атомами) Характер химической связи находит свое выражение в макроскопических физических свойствах кристаллов: чем прочнее связь (обычно при этом межатомные расстояния короткие), тем выше механические свойства кристаллов (твердость, упругость), тем меньше коэффициент термического расширения, тем выше температура плавления.
Энтальпии испарения (к. Дж/моль) металлов (характеристика прочности связей между атомами) Характер химической связи находит свое выражение в макроскопических физических свойствах кристаллов: чем прочнее связь (обычно при этом межатомные расстояния короткие), тем выше механические свойства кристаллов (твердость, упругость), тем меньше коэффициент термического расширения, тем выше температура плавления.
 Энергии диссоциации Do связи металл-металл в димерах M 2 (рассчитаны масс-спектрометрическим методом в паровой фазе)
Энергии диссоциации Do связи металл-металл в димерах M 2 (рассчитаны масс-спектрометрическим методом в паровой фазе)
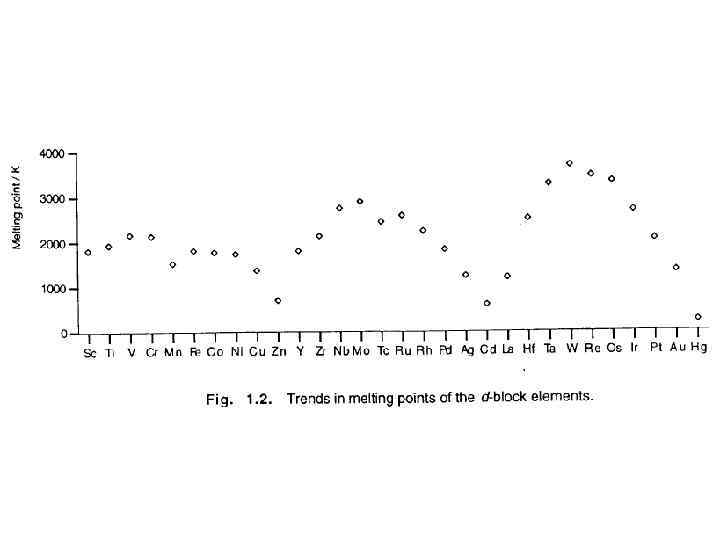
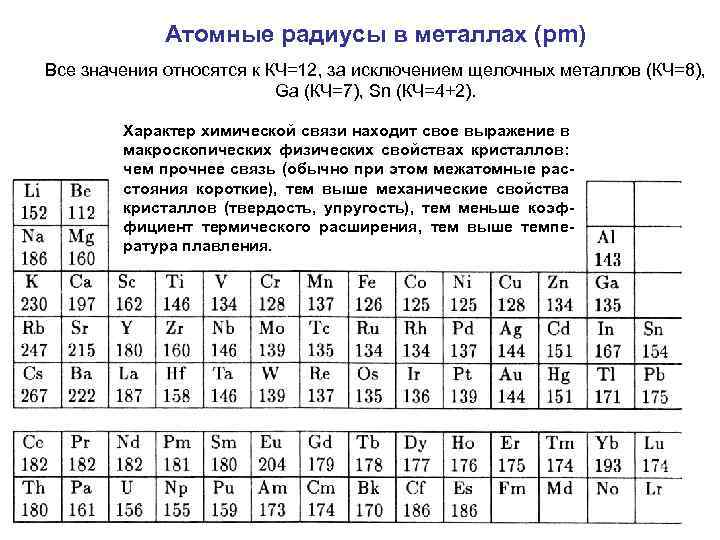 Атомные радиусы в металлах (рm) Все значения относятся к КЧ=12, за исключением щелочных металлов (КЧ=8), Ga (КЧ=7), Sn (КЧ=4+2). Характер химической связи находит свое выражение в макроскопических физических свойствах кристаллов: чем прочнее связь (обычно при этом межатомные расстояния короткие), тем выше механические свойства кристаллов (твердость, упругость), тем меньше коэффициент термического расширения, тем выше температура плавления.
Атомные радиусы в металлах (рm) Все значения относятся к КЧ=12, за исключением щелочных металлов (КЧ=8), Ga (КЧ=7), Sn (КЧ=4+2). Характер химической связи находит свое выражение в макроскопических физических свойствах кристаллов: чем прочнее связь (обычно при этом межатомные расстояния короткие), тем выше механические свойства кристаллов (твердость, упругость), тем меньше коэффициент термического расширения, тем выше температура плавления.

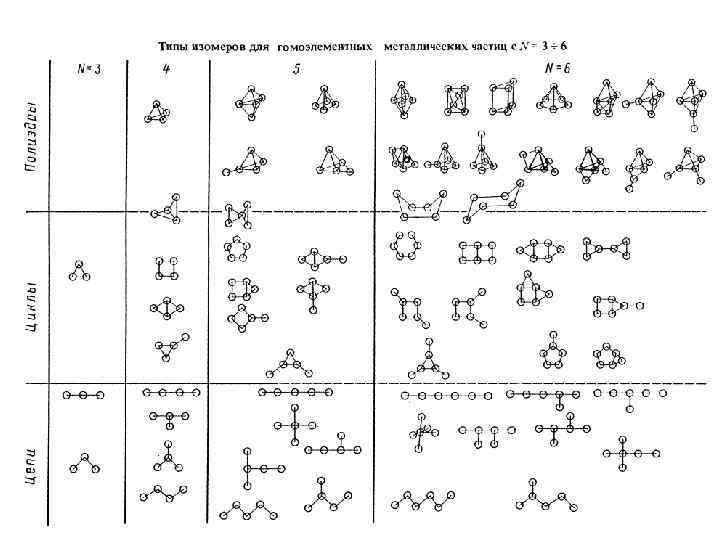
 Электронное строение металлокластерных комплексов «Магическое» число КВЭ как критерий устойчивости металлокластерного комплекса
Электронное строение металлокластерных комплексов «Магическое» число КВЭ как критерий устойчивости металлокластерного комплекса
 Нуклиды не хочу обидеть. Но нам важнее электрон: Его ни взвесить, ни увидеть, Но вездесущ, мерзавец, он. Умеет он везде вертеться! К нему полезно приглядеться… «Электроны в химии» Из иронической поэзии Владимира Федорова
Нуклиды не хочу обидеть. Но нам важнее электрон: Его ни взвесить, ни увидеть, Но вездесущ, мерзавец, он. Умеет он везде вертеться! К нему полезно приглядеться… «Электроны в химии» Из иронической поэзии Владимира Федорова
 Возможные взаимодействия между ионами переходных металлов с различной электронной конфигурацией dn (n - число валентных электронов у иона металла) Простейший случай: биядерные комплексы Ионы металла находятся в высшей степени окисления; электронная конфигурация d 0; образование связи металл-металл невозможно. Расстояния между атомами металла большие. d 0 • • d 1 • • Ионы металла имеют d 1 электронную конфигурацию: 1. Электроны локализованы на металлических центрах. Связь металл-металл отсутствует. Расстояния между атомами металла большие. Возможны обменные взаимодействия спинов через лиганды. 2. Электроны обоих атомов используются на образование локализованной ковалентной двухэлектронной двухцентровой (2 е 2 с) связи металл-металл с коротким расстоянием М-М. • •
Возможные взаимодействия между ионами переходных металлов с различной электронной конфигурацией dn (n - число валентных электронов у иона металла) Простейший случай: биядерные комплексы Ионы металла находятся в высшей степени окисления; электронная конфигурация d 0; образование связи металл-металл невозможно. Расстояния между атомами металла большие. d 0 • • d 1 • • Ионы металла имеют d 1 электронную конфигурацию: 1. Электроны локализованы на металлических центрах. Связь металл-металл отсутствует. Расстояния между атомами металла большие. Возможны обменные взаимодействия спинов через лиганды. 2. Электроны обоих атомов используются на образование локализованной ковалентной двухэлектронной двухцентровой (2 е 2 с) связи металл-металл с коротким расстоянием М-М. • •
 Кластерные «скелетные» электроны (КСЭ) – это количество электронов, непосредственно участвующих в образовании связей металл-металл. Число КСЭ для электроноточных кластеров Mn вычисляется по формуле: КСЭ= 2 b где b - число ребер полиэдра в металлокластере Mn. Кластерные валентные электроны (КВЭ). Простейший подход к вычислению числа КВЭ кластерного комплекса состоит в том, что атомы металлов и лиганды принимаются незаряженными. В этом случае число КВЭ вычисляется по схеме: КВЭ = (суммарное число электронов валентных оболочек атомов металлов, образующих металлокластер) + (число электронов, поставляемых всеми лигандами по принятым правилам); для заряженных комплексов добавляется заряд комплекса, взятый с обратным знаком. ********* В англоязычной литературе используется термин valence electron concentration (VEC).
Кластерные «скелетные» электроны (КСЭ) – это количество электронов, непосредственно участвующих в образовании связей металл-металл. Число КСЭ для электроноточных кластеров Mn вычисляется по формуле: КСЭ= 2 b где b - число ребер полиэдра в металлокластере Mn. Кластерные валентные электроны (КВЭ). Простейший подход к вычислению числа КВЭ кластерного комплекса состоит в том, что атомы металлов и лиганды принимаются незаряженными. В этом случае число КВЭ вычисляется по схеме: КВЭ = (суммарное число электронов валентных оболочек атомов металлов, образующих металлокластер) + (число электронов, поставляемых всеми лигандами по принятым правилам); для заряженных комплексов добавляется заряд комплекса, взятый с обратным знаком. ********* В англоязычной литературе используется термин valence electron concentration (VEC).
 В основе образования металлокластера лежит важный постулат о локализованных (двухэлектронных, двухцентровых – 2 е 2 с) связях М-М в металлокластерах Кластерные «скелетные» электроны (КСЭ) – это количество электронов, непосредственно участвующих в образовании связей металл-металл. Число КСЭ для электроноточных (2 e 2 c) кластеров Mn вычисляется по формуле: КСЭ= 2 b где b - число ребер полиэдра в металлокластере Mn.
В основе образования металлокластера лежит важный постулат о локализованных (двухэлектронных, двухцентровых – 2 е 2 с) связях М-М в металлокластерах Кластерные «скелетные» электроны (КСЭ) – это количество электронов, непосредственно участвующих в образовании связей металл-металл. Число КСЭ для электроноточных (2 e 2 c) кластеров Mn вычисляется по формуле: КСЭ= 2 b где b - число ребер полиэдра в металлокластере Mn.
 Структура и устойчивость металлокластеров, и их зависимость от числа кластерных валентных электронов Для металлоорганических соединений с малыми кластерами (октаэдрические M 6 и более крупные кластеры не подчиняются этой модели) между числом кластерных валентных электронов и структурой имеется взаимосвязь, которая легко объясняется на основе локальных ММ и М-L электронных пар связывания и известного полуэмпирического правила 18 валентных электронов (правило Сиджвика или эффективного атомного номера - ЭAH): атом переходного металла в устойчивой структуре стремится достичь завершенной 18 -ти электронной оболочки. • Таким образом, в основе данной модели лежит важный постулат о локализованных (двухэлектронных, двухцентровых – 2 е 2 с) связях М-М в металлокластерах. При этом в электронной структуре такого комплекса все связующие МО полностью заполнены, а разрыхляющие МО – пусты. _______ • Аналогичное правило ЭАН применимо для элементов главных групп, стремящихся к завершенной 8 электронной оболочки.
Структура и устойчивость металлокластеров, и их зависимость от числа кластерных валентных электронов Для металлоорганических соединений с малыми кластерами (октаэдрические M 6 и более крупные кластеры не подчиняются этой модели) между числом кластерных валентных электронов и структурой имеется взаимосвязь, которая легко объясняется на основе локальных ММ и М-L электронных пар связывания и известного полуэмпирического правила 18 валентных электронов (правило Сиджвика или эффективного атомного номера - ЭAH): атом переходного металла в устойчивой структуре стремится достичь завершенной 18 -ти электронной оболочки. • Таким образом, в основе данной модели лежит важный постулат о локализованных (двухэлектронных, двухцентровых – 2 е 2 с) связях М-М в металлокластерах. При этом в электронной структуре такого комплекса все связующие МО полностью заполнены, а разрыхляющие МО – пусты. _______ • Аналогичное правило ЭАН применимо для элементов главных групп, стремящихся к завершенной 8 электронной оболочки.
 Правило ЭАН, правило 18 электронов, правило инертного газа, правило Сиджвика Стехиометрия многих комплексов переходных металлов подчиняется правилу эффективного атомного номера (ЭАН). В соответствие с эти правилом число валентных электронов у металла в комплексе должно равняться числу электронов в оболочке ближайшего к данному металлу инертного газа. Правило определяет способность атома металла наиболее полно использовать при образовании связей с лигандами свои валентные nd, (n+1)s и (n+1)p орбитали, которые суммарно могут быть заполнены 18 электронами. Для подсчета ЭАН к числу электронов на внешней оболочке атома металла прибавляют число электронов, формально передаваемых атому металла лигандами. Правило ЭАН выполняется, если энергии nd, (n+1)s и (n+1)p орбиталей близки, а орбитали доступны для связывания с лигандами. Правило помогает установить формулы новых соединений.
Правило ЭАН, правило 18 электронов, правило инертного газа, правило Сиджвика Стехиометрия многих комплексов переходных металлов подчиняется правилу эффективного атомного номера (ЭАН). В соответствие с эти правилом число валентных электронов у металла в комплексе должно равняться числу электронов в оболочке ближайшего к данному металлу инертного газа. Правило определяет способность атома металла наиболее полно использовать при образовании связей с лигандами свои валентные nd, (n+1)s и (n+1)p орбитали, которые суммарно могут быть заполнены 18 электронами. Для подсчета ЭАН к числу электронов на внешней оболочке атома металла прибавляют число электронов, формально передаваемых атому металла лигандами. Правило ЭАН выполняется, если энергии nd, (n+1)s и (n+1)p орбиталей близки, а орбитали доступны для связывания с лигандами. Правило помогает установить формулы новых соединений.
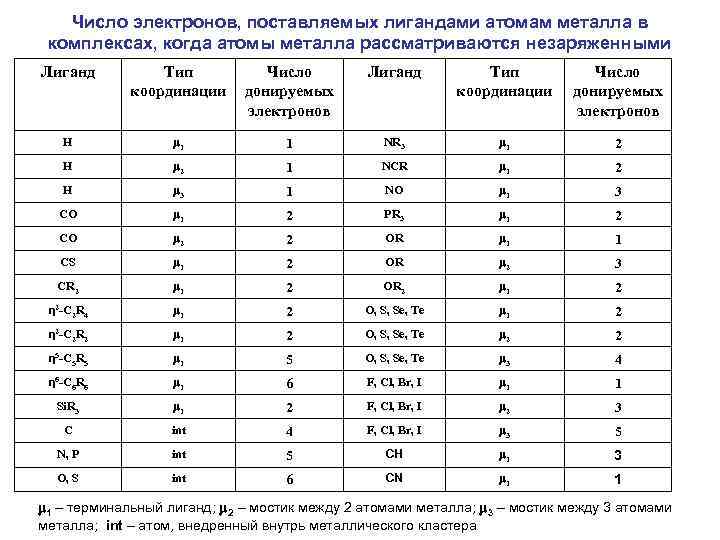 Число электронов, поставляемых лигандами атомам металла в комплексах, когда атомы металла рассматриваются незаряженными Лиганд Тип координации Число донируемых электронов H 1 1 NR 3 1 2 H 2 1 NCR 1 2 H 3 1 NO 1 3 CO 1 2 PR 3 1 2 CO 2 2 OR 1 1 CS 1 2 OR 2 3 CR 2 1 2 OR 2 1 2 η 2 -C 2 R 4 1 2 O, S, Se, Te 1 2 η 2 -C 2 R 2 1 2 O, S, Se, Te 2 2 η 5 -C 5 R 5 1 5 O, S, Se, Te 3 4 η 6 -C 6 R 6 1 6 F, Cl, Br, I 1 1 Si. R 3 1 2 F, Cl, Br, I 2 3 C int 4 F, Cl, Br, I 3 5 N, P int 5 CH 1 3 O, S int 6 CN 1 1 1 – терминальный лиганд; 2 – мостик между 2 атомами металла; 3 – мостик между 3 атомами металла; int – атом, внедренный внутрь металлического кластера
Число электронов, поставляемых лигандами атомам металла в комплексах, когда атомы металла рассматриваются незаряженными Лиганд Тип координации Число донируемых электронов H 1 1 NR 3 1 2 H 2 1 NCR 1 2 H 3 1 NO 1 3 CO 1 2 PR 3 1 2 CO 2 2 OR 1 1 CS 1 2 OR 2 3 CR 2 1 2 OR 2 1 2 η 2 -C 2 R 4 1 2 O, S, Se, Te 1 2 η 2 -C 2 R 2 1 2 O, S, Se, Te 2 2 η 5 -C 5 R 5 1 5 O, S, Se, Te 3 4 η 6 -C 6 R 6 1 6 F, Cl, Br, I 1 1 Si. R 3 1 2 F, Cl, Br, I 2 3 C int 4 F, Cl, Br, I 3 5 N, P int 5 CH 1 3 O, S int 6 CN 1 1 1 – терминальный лиганд; 2 – мостик между 2 атомами металла; 3 – мостик между 3 атомами металла; int – атом, внедренный внутрь металлического кластера
 «Mагические» числа КВЭ Используя правило ЭАН, легко вычислить «магические» числа КВЭ для ряда кластеров определенной структуры для элементов главных групп и для переходных металлов: Тип кластера Треугольник Тетраэдр Тригональная бипирамида Октаэдр Тригональная призма Куб элементы переходные главных групп металлы 18 48 20 60 22 72 24 84 30 90 40 120 У кластерного комплекса с «магическим» числом КВЭ электронная структура характеризуется тем, что все связующие МО полностью заполнены, а разрыхляющие МО – пусты.
«Mагические» числа КВЭ Используя правило ЭАН, легко вычислить «магические» числа КВЭ для ряда кластеров определенной структуры для элементов главных групп и для переходных металлов: Тип кластера Треугольник Тетраэдр Тригональная бипирамида Октаэдр Тригональная призма Куб элементы переходные главных групп металлы 18 48 20 60 22 72 24 84 30 90 40 120 У кластерного комплекса с «магическим» числом КВЭ электронная структура характеризуется тем, что все связующие МО полностью заполнены, а разрыхляющие МО – пусты.
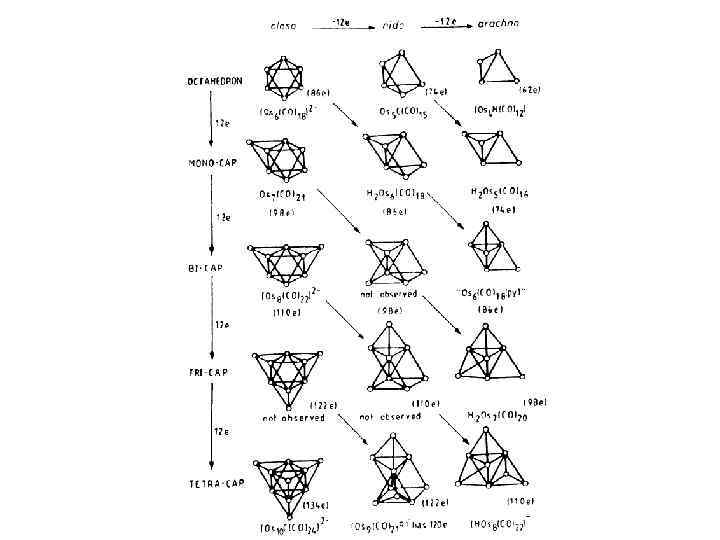
 Closo – кластеры по своим электронным свойствам подразделяются на несколько групп: 1. Электроноточные кластеры, в которых каждое ребро полиэдра Мn представляет собой двухэлектронную двухцентровую металл-металл связь (2 е 2 с). 2. Электронодефицитные кластеры, в которых реализуются двухэлектронные трехцентровые металл-металл связи типа 2 е 3 с (связь трех атомов металла в треугольных гранях полиэдров Мn). 3. Кластеры, подчиняющиеся правилу Уэйда (K. Wade, Electron deficient compounds, L. , Nelson, 1971), предложенному для полиэдрических гидридов бора и карборанов. Позднее это правило было уточнено Д. Мингосом (Mingos D. M. P. , Wales D. J. , Introduction to cluster chemistry, 1980) и Дж. Лойером (Lauher J. W. , JACS, 1978, v. 100, p. 5305) и перенесено на крупные металлокластерные соединения. 4. Другие кластеры, не входящие в выше приведенные группы.
Closo – кластеры по своим электронным свойствам подразделяются на несколько групп: 1. Электроноточные кластеры, в которых каждое ребро полиэдра Мn представляет собой двухэлектронную двухцентровую металл-металл связь (2 е 2 с). 2. Электронодефицитные кластеры, в которых реализуются двухэлектронные трехцентровые металл-металл связи типа 2 е 3 с (связь трех атомов металла в треугольных гранях полиэдров Мn). 3. Кластеры, подчиняющиеся правилу Уэйда (K. Wade, Electron deficient compounds, L. , Nelson, 1971), предложенному для полиэдрических гидридов бора и карборанов. Позднее это правило было уточнено Д. Мингосом (Mingos D. M. P. , Wales D. J. , Introduction to cluster chemistry, 1980) и Дж. Лойером (Lauher J. W. , JACS, 1978, v. 100, p. 5305) и перенесено на крупные металлокластерные соединения. 4. Другие кластеры, не входящие в выше приведенные группы.
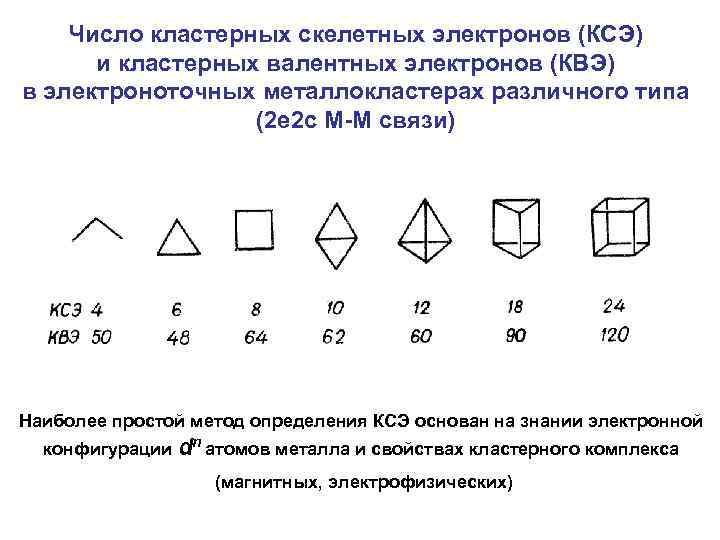 Число кластерных скелетных электронов (КСЭ) и кластерных валентных электронов (КВЭ) в электроноточных металлокластерах различного типа (2 е 2 с M-M связи) Наиболее простой метод определения КСЭ основан на знании электронной конфигурации dn атомов металла и свойствах кластерного комплекса (магнитных, электрофизических)
Число кластерных скелетных электронов (КСЭ) и кластерных валентных электронов (КВЭ) в электроноточных металлокластерах различного типа (2 е 2 с M-M связи) Наиболее простой метод определения КСЭ основан на знании электронной конфигурации dn атомов металла и свойствах кластерного комплекса (магнитных, электрофизических)
 Корреляция числа кластерных валентных электронов и структуры металлокластера
Корреляция числа кластерных валентных электронов и структуры металлокластера
 Некоторые применения величины КВЭ В электроноточных кластерах знание величины КВЭ (g) позволяет определить тип кластера, т. е. число 2 e 2 c М-М связей b (ребер полиэдра) в кластере Mn, используя простые формулы: b = ½ (8 n – g) b = ½ (18 n – g) для элементов главных групп для переходных элементов В электронодефицитных кластерах реализуются связи типа 2 е 3 с по треугольным граням кластерного дельта-полиэдра, что наблюдается в тетраэдрических, тригонально-бипирамидальных и октаэдрических кластерах. Число треугольных полиэдрических граней d, имеющих 2 е 3 с связи, определяется по формулам: d = ¼ (8 n – g) для элементов главных групп d = ¼ (18 n – g) для переходных элементов где n – число атомов в кластере. _______ Уравнения применимы только для тех случаев, когда в дельта-полиэдрических кластерах образуются металл-металл связи только типа 2 е 3 с.
Некоторые применения величины КВЭ В электроноточных кластерах знание величины КВЭ (g) позволяет определить тип кластера, т. е. число 2 e 2 c М-М связей b (ребер полиэдра) в кластере Mn, используя простые формулы: b = ½ (8 n – g) b = ½ (18 n – g) для элементов главных групп для переходных элементов В электронодефицитных кластерах реализуются связи типа 2 е 3 с по треугольным граням кластерного дельта-полиэдра, что наблюдается в тетраэдрических, тригонально-бипирамидальных и октаэдрических кластерах. Число треугольных полиэдрических граней d, имеющих 2 е 3 с связи, определяется по формулам: d = ¼ (8 n – g) для элементов главных групп d = ¼ (18 n – g) для переходных элементов где n – число атомов в кластере. _______ Уравнения применимы только для тех случаев, когда в дельта-полиэдрических кластерах образуются металл-металл связи только типа 2 е 3 с.
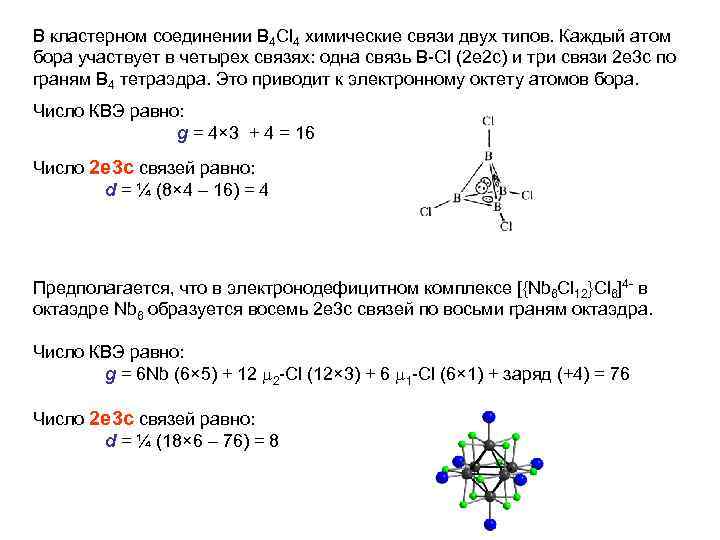 В кластерном соединении B 4 Cl 4 химические связи двух типов. Каждый атом бора участвует в четырех связях: одна связь B-Cl (2 е 2 с) и три связи 2 е 3 с по граням B 4 тетраэдра. Это приводит к электронному октету атомов бора. Число КВЭ равно: g = 4× 3 + 4 = 16 Число 2 е 3 с связей равно: d = ¼ (8× 4 – 16) = 4 Предполагается, что в электронодефицитном комплексе [{Nb 6 Cl 12}Cl 6]4 - в октаэдре Nb 6 образуется восемь 2 е 3 с связей по восьми граням октаэдра. Число КВЭ равно: g = 6 Nb (6× 5) + 12 2 -Cl (12× 3) + 6 1 -Cl (6× 1) + заряд (+4) = 76 Число 2 е 3 с связей равно: d = ¼ (18× 6 – 76) = 8
В кластерном соединении B 4 Cl 4 химические связи двух типов. Каждый атом бора участвует в четырех связях: одна связь B-Cl (2 е 2 с) и три связи 2 е 3 с по граням B 4 тетраэдра. Это приводит к электронному октету атомов бора. Число КВЭ равно: g = 4× 3 + 4 = 16 Число 2 е 3 с связей равно: d = ¼ (8× 4 – 16) = 4 Предполагается, что в электронодефицитном комплексе [{Nb 6 Cl 12}Cl 6]4 - в октаэдре Nb 6 образуется восемь 2 е 3 с связей по восьми граням октаэдра. Число КВЭ равно: g = 6 Nb (6× 5) + 12 2 -Cl (12× 3) + 6 1 -Cl (6× 1) + заряд (+4) = 76 Число 2 е 3 с связей равно: d = ¼ (18× 6 – 76) = 8
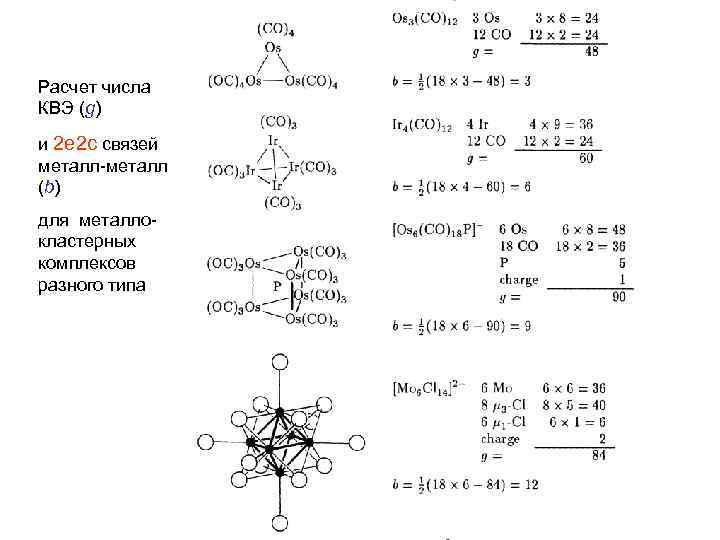 Расчет числа КВЭ (g) и 2 e 2 c связей металл-металл (b) для металлокластерных комплексов разного типа
Расчет числа КВЭ (g) и 2 e 2 c связей металл-металл (b) для металлокластерных комплексов разного типа
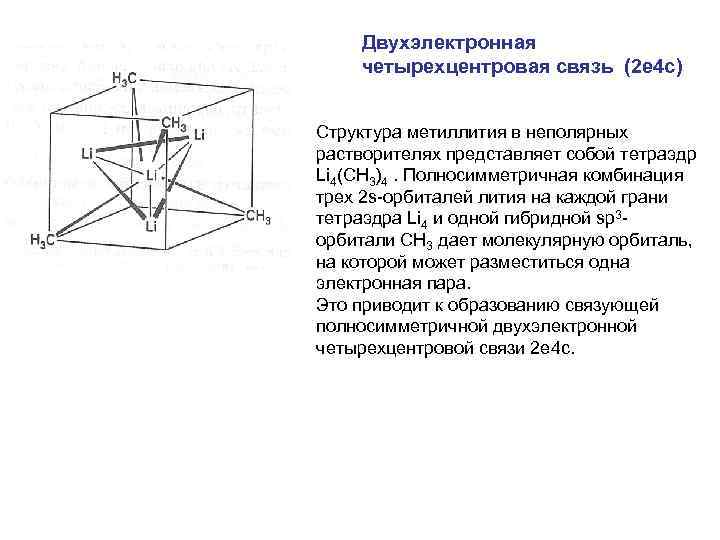 Двухэлектронная четырехцентровая связь (2 e 4 c) Структура метиллития в неполярных растворителях представляет собой тетраэдр Li 4(CH 3)4. Полносимметричная комбинация трех 2 s-орбиталей лития на каждой грани тетраэдра Li 4 и одной гибридной sp 3 орбитали СH 3 дает молекулярную орбиталь, на которой может разместиться одна электронная пара. Это приводит к образованию связующей полносимметричной двухэлектронной четырехцентровой связи 2 е 4 с.
Двухэлектронная четырехцентровая связь (2 e 4 c) Структура метиллития в неполярных растворителях представляет собой тетраэдр Li 4(CH 3)4. Полносимметричная комбинация трех 2 s-орбиталей лития на каждой грани тетраэдра Li 4 и одной гибридной sp 3 орбитали СH 3 дает молекулярную орбиталь, на которой может разместиться одна электронная пара. Это приводит к образованию связующей полносимметричной двухэлектронной четырехцентровой связи 2 е 4 с.
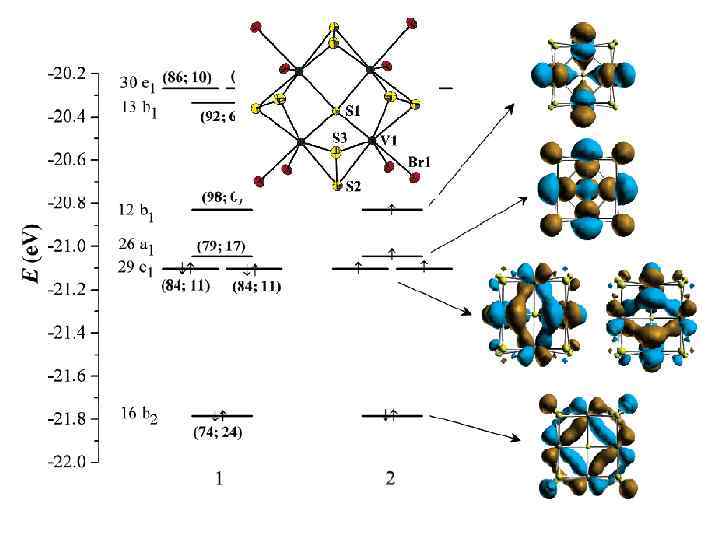
 Стабильность кластерных соединений Прочность связи М-М увеличивается при движении вниз по группе (возможно, из-за большего размера d-орбиталей более тяжелых атомов). Это, по-видимому, объясняет, почему для 4 d и 5 d элементов существует намного больше кластерных соединений, чем для 3 d металлов. Наиболее прочная связь металл-металл в простых веществах наблюдается для элементов 4 d и 5 d рядов; эта же закономерность сохраняется и для их соединений. Для р-элементов наблюдается обратная закономерность: связь элемент-элемент ослабевает при движении вниз по группе.
Стабильность кластерных соединений Прочность связи М-М увеличивается при движении вниз по группе (возможно, из-за большего размера d-орбиталей более тяжелых атомов). Это, по-видимому, объясняет, почему для 4 d и 5 d элементов существует намного больше кластерных соединений, чем для 3 d металлов. Наиболее прочная связь металл-металл в простых веществах наблюдается для элементов 4 d и 5 d рядов; эта же закономерность сохраняется и для их соединений. Для р-элементов наблюдается обратная закономерность: связь элемент-элемент ослабевает при движении вниз по группе.
 Лигандная предпочтительность Для переходных металлов IV-VI групп наиболее типичны кластерные комплексы с π - донорными лигандами (галогенид- и халькогенид- ионы). Для металлов конца переходных рядов характерны карбонильные соединения (π - акцепторые CO лиганды). Электронные причины лигандной предпочтительности: донирование электронов в электронодефицитные «высоковалентные» галогенидные (халькогенидные) металлокластеры или снятие избыточной электронной плотности с низковалентных (нульвалентных) карбонильных металлокластеров.
Лигандная предпочтительность Для переходных металлов IV-VI групп наиболее типичны кластерные комплексы с π - донорными лигандами (галогенид- и халькогенид- ионы). Для металлов конца переходных рядов характерны карбонильные соединения (π - акцепторые CO лиганды). Электронные причины лигандной предпочтительности: донирование электронов в электронодефицитные «высоковалентные» галогенидные (халькогенидные) металлокластеры или снятие избыточной электронной плотности с низковалентных (нульвалентных) карбонильных металлокластеров.
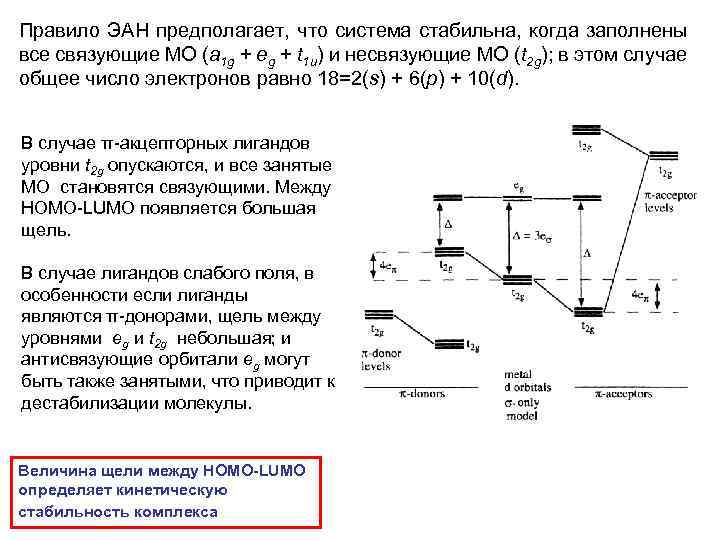 Правило ЭАН предполагает, что система стабильна, когда заполнены все связующие MO (a 1 g + eg + t 1 u) и несвязующие МО (t 2 g); в этом случае общее число электронов равно 18=2(s) + 6(p) + 10(d). В случае π-акцепторных лигандов уровни t 2 g опускаются, и все занятые МО становятся связующими. Между НОМО-LUMO появляется большая щель. В случае лигандов слабого поля, в особенности если лиганды являются π-донорами, щель между уровнями eg и t 2 g небольшая; и антисвязующие орбитали eg могут быть также занятыми, что приводит к дестабилизации молекулы. Величина щели между НОМО-LUMO определяет кинетическую стабильность комплекса
Правило ЭАН предполагает, что система стабильна, когда заполнены все связующие MO (a 1 g + eg + t 1 u) и несвязующие МО (t 2 g); в этом случае общее число электронов равно 18=2(s) + 6(p) + 10(d). В случае π-акцепторных лигандов уровни t 2 g опускаются, и все занятые МО становятся связующими. Между НОМО-LUMO появляется большая щель. В случае лигандов слабого поля, в особенности если лиганды являются π-донорами, щель между уровнями eg и t 2 g небольшая; и антисвязующие орбитали eg могут быть также занятыми, что приводит к дестабилизации молекулы. Величина щели между НОМО-LUMO определяет кинетическую стабильность комплекса
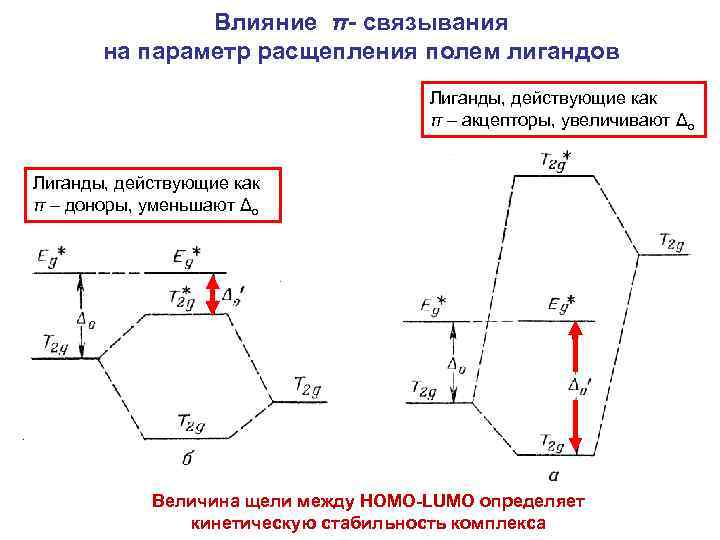 Влияние π- связывания на параметр расщепления полем лигандов Лиганды, действующие как π – акцепторы, увеличивают Δо Лиганды, действующие как π – доноры, уменьшают Δо Величина щели между НОМО-LUMO определяет кинетическую стабильность комплекса
Влияние π- связывания на параметр расщепления полем лигандов Лиганды, действующие как π – акцепторы, увеличивают Δо Лиганды, действующие как π – доноры, уменьшают Δо Величина щели между НОМО-LUMO определяет кинетическую стабильность комплекса
 Взаимодействие π-орбиталей лигандов и t 2 g – орбиталей атомов металла зависит, с одной стороны, от соотношения энергии этих орбиталей, а с другой – от того, являются ли орбитали лиганда заполненными или вакантными. π – донорные лиганды (Cl-, Br-, S 2 -, ОН-, H 2 O и др. ) еще до образования связи имеют заполненные орбитали π – симметрии относительно оси связи М - L. Энергии этих заполненных π – орбиталей достаточно близки к энергии dорбиталей металлов, но все же чуть меньше. Как правило, такие лиганды не содержат свободных π – орбиталей с низкой энергией, так что рассматривают только заполненные орбитали. Поскольку заполненные π – орбитали донорного лиганда лежат ниже по энергии, чем частично заполненные dорбитали металла, то при образовании МО с t 2 g – орбиталями металла связывающие орбитали располагаются ниже, чем орбитали лигандов, а разрыхляющие МО – выше энергии d-орбиталей свободного иона металла. Электроны свободных пар лигандов заполняют связывающие орбитали, тогда как электроны, первоначально располагающиеся на d-орбиталях центрального атома металла, занимают разрыхляющие t 2 g – орбитали. В результате прежде несвязывающие t 2 g – орбитали иона металла становятся разрыхляющими и, значит, их энергия повышается , приближаясь к энергии разрыхляющей eg- орбитали, принадлежащей в основном металлу. Следовательно, лиганды, являющиеся сильными π– донорами, уменьшают Δo.
Взаимодействие π-орбиталей лигандов и t 2 g – орбиталей атомов металла зависит, с одной стороны, от соотношения энергии этих орбиталей, а с другой – от того, являются ли орбитали лиганда заполненными или вакантными. π – донорные лиганды (Cl-, Br-, S 2 -, ОН-, H 2 O и др. ) еще до образования связи имеют заполненные орбитали π – симметрии относительно оси связи М - L. Энергии этих заполненных π – орбиталей достаточно близки к энергии dорбиталей металлов, но все же чуть меньше. Как правило, такие лиганды не содержат свободных π – орбиталей с низкой энергией, так что рассматривают только заполненные орбитали. Поскольку заполненные π – орбитали донорного лиганда лежат ниже по энергии, чем частично заполненные dорбитали металла, то при образовании МО с t 2 g – орбиталями металла связывающие орбитали располагаются ниже, чем орбитали лигандов, а разрыхляющие МО – выше энергии d-орбиталей свободного иона металла. Электроны свободных пар лигандов заполняют связывающие орбитали, тогда как электроны, первоначально располагающиеся на d-орбиталях центрального атома металла, занимают разрыхляющие t 2 g – орбитали. В результате прежде несвязывающие t 2 g – орбитали иона металла становятся разрыхляющими и, значит, их энергия повышается , приближаясь к энергии разрыхляющей eg- орбитали, принадлежащей в основном металлу. Следовательно, лиганды, являющиеся сильными π– донорами, уменьшают Δo.
 π – акцепторные лиганды (PR 3, СО) содержат заполненные π – орбитали (энергия которых обычно ниже энергии t 2 g – орбиталей), и свободные π – орбитали. π – акцепторные орбитали, как правило, представляют собой незаполненные разрыхляющие орбитали лиганда. Эти орбитали расположены выше по энергии, чем d-орбитали металла. Поэтому в молекулярных комплексах связующие МО преимущественно имеют характер d-орбиталей металла. Эти связывающие орбитали несколько ниже по энергии, чем dорбитали металла. В результате при взаимодействии с π – акцептором Δo возрастает. Порядок расположения лигандов в спектрохимическом ряду можно объяснить влиянием π – связывания: I- < Br- < Cl- < F- < H 2 O < NH 3 < CN- < PR 3
π – акцепторные лиганды (PR 3, СО) содержат заполненные π – орбитали (энергия которых обычно ниже энергии t 2 g – орбиталей), и свободные π – орбитали. π – акцепторные орбитали, как правило, представляют собой незаполненные разрыхляющие орбитали лиганда. Эти орбитали расположены выше по энергии, чем d-орбитали металла. Поэтому в молекулярных комплексах связующие МО преимущественно имеют характер d-орбиталей металла. Эти связывающие орбитали несколько ниже по энергии, чем dорбитали металла. В результате при взаимодействии с π – акцептором Δo возрастает. Порядок расположения лигандов в спектрохимическом ряду можно объяснить влиянием π – связывания: I- < Br- < Cl- < F- < H 2 O < NH 3 < CN- < PR 3
![Особенности координации лигандов в металлокластерных комплексах [Re 12( 6 -C)( 3 -S)14( 2 -S)3(CN)6]8 Особенности координации лигандов в металлокластерных комплексах [Re 12( 6 -C)( 3 -S)14( 2 -S)3(CN)6]8](https://present5.com/presentation/5652994_182162819/image-67.jpg) Особенности координации лигандов в металлокластерных комплексах [Re 12( 6 -C)( 3 -S)14( 2 -S)3(CN)6]8 - [V 4( 4 -S)( 2 -S 2)4 Br 8/2]
Особенности координации лигандов в металлокластерных комплексах [Re 12( 6 -C)( 3 -S)14( 2 -S)3(CN)6]8 - [V 4( 4 -S)( 2 -S 2)4 Br 8/2]
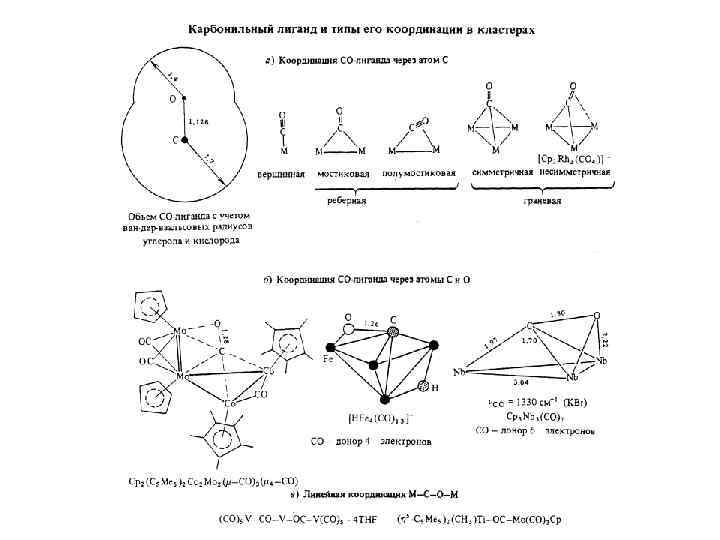
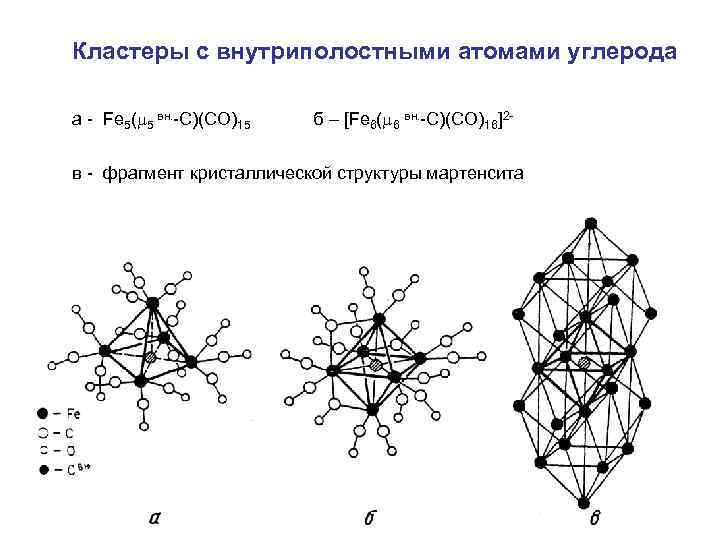 Кластеры с внутриполостными атомами углерода a - Fe 5( 5 вн. -С)(CO)15 б – [Fe 6( 6 вн. -С)(CO)16]2 - в - фрагмент кристаллической структуры мартенсита
Кластеры с внутриполостными атомами углерода a - Fe 5( 5 вн. -С)(CO)15 б – [Fe 6( 6 вн. -С)(CO)16]2 - в - фрагмент кристаллической структуры мартенсита
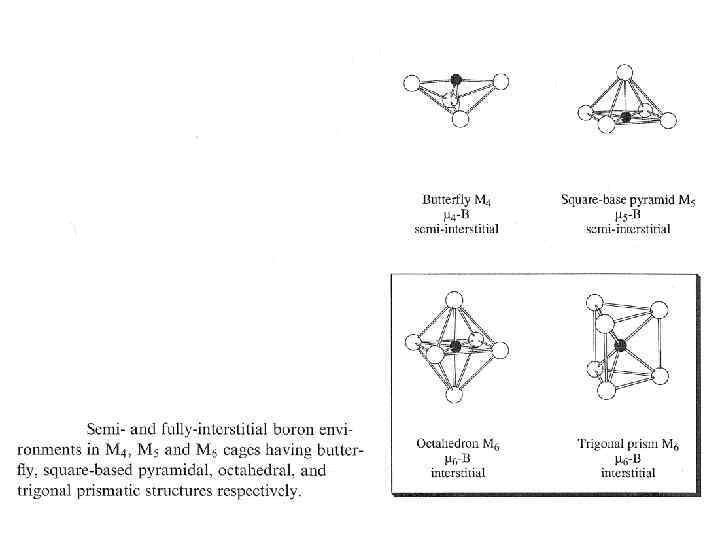
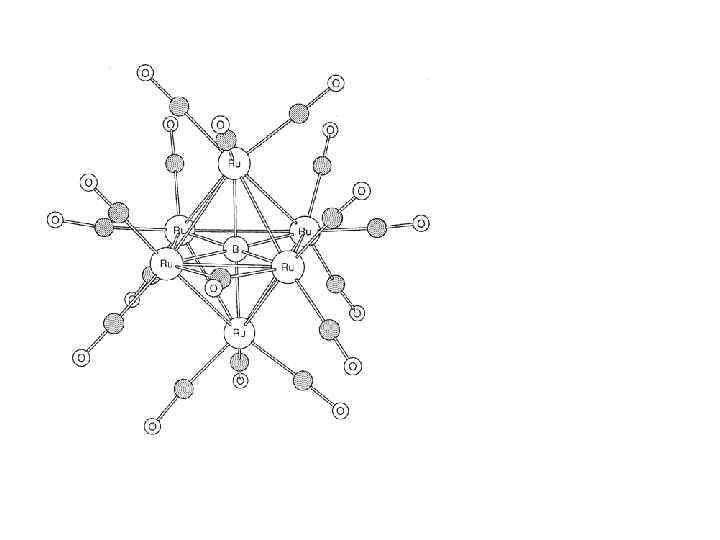
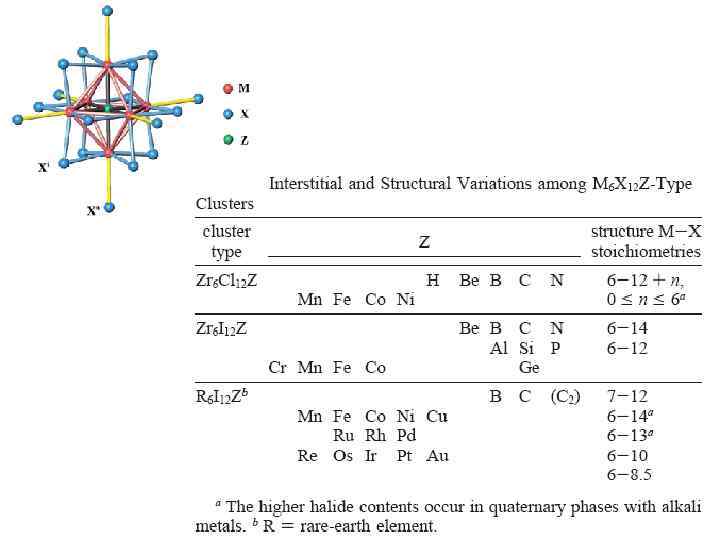
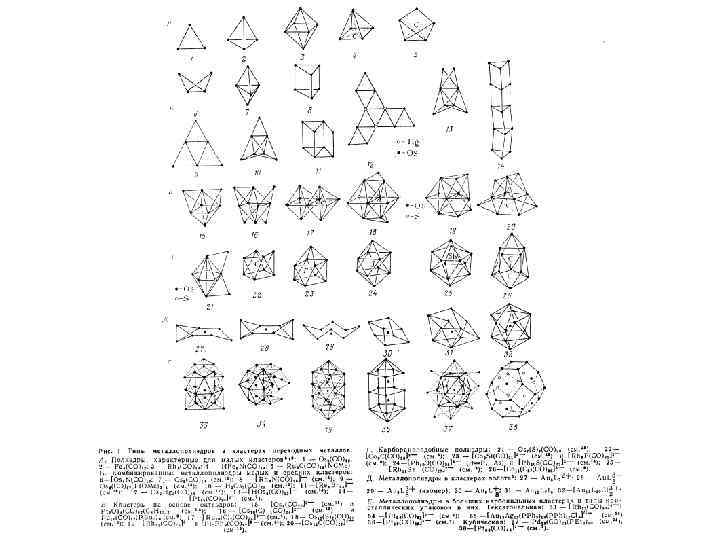
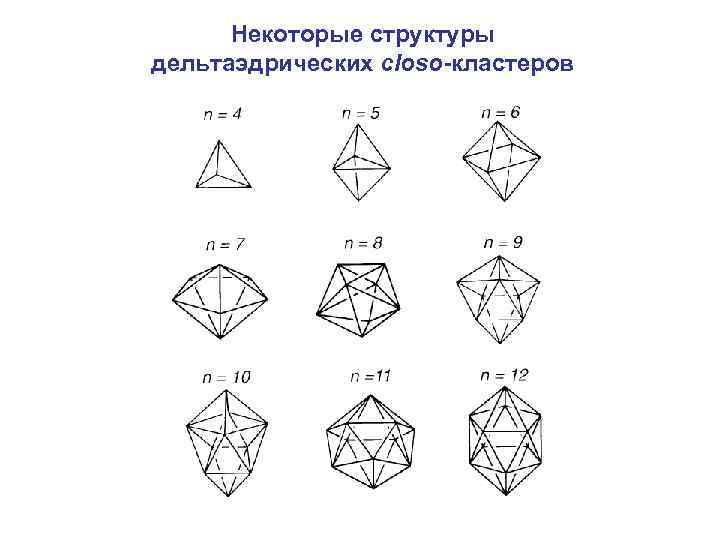 Некоторые структуры дельтаэдрических closo-кластеров
Некоторые структуры дельтаэдрических closo-кластеров
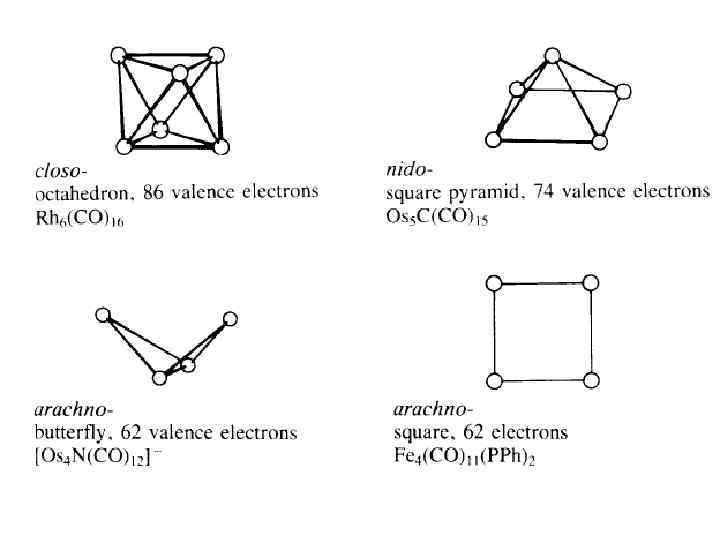
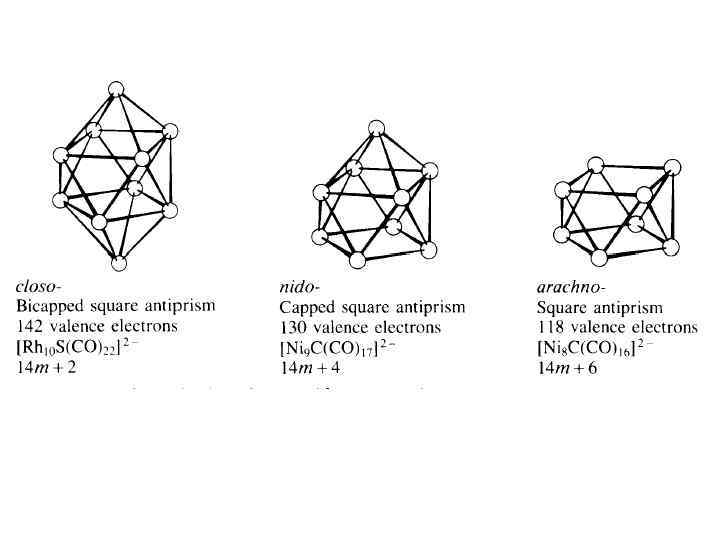
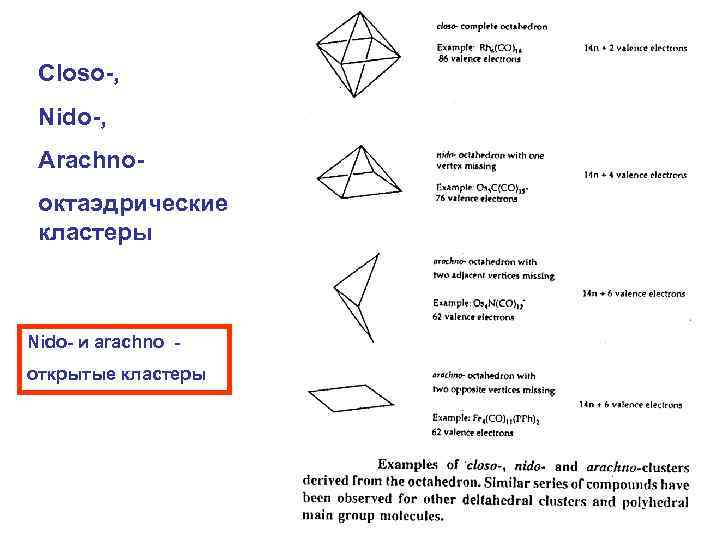 Closo-, Nido-, Arachnoоктаэдрические кластеры Nido- и arachno открытые кластеры
Closo-, Nido-, Arachnoоктаэдрические кластеры Nido- и arachno открытые кластеры
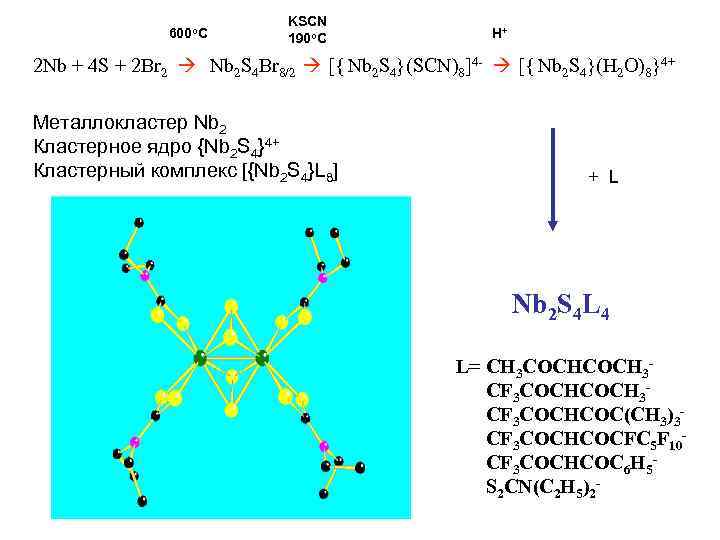 600 o. C KSCN 190 o. C H+ 2 Nb + 4 S + 2 Br 2 Nb 2 S 4 Br 8/2 [{ Nb 2 S 4}(SCN)8]4 - [{ Nb 2 S 4}(H 2 O)8}4+ Металлокластер Nb 2 Кластерное ядро {Nb 2 S 4}4+ Кластерный комплекс [{Nb 2 S 4}L 8] + L Nb 2 S 4 L 4 L= CH 3 COCHCOCH 3 CF 3 COCHCOC(CH 3)3 CF 3 COCHCOCFC 5 F 10 CF 3 COCHCOC 6 H 5 S 2 CN(C 2 H 5)2 -
600 o. C KSCN 190 o. C H+ 2 Nb + 4 S + 2 Br 2 Nb 2 S 4 Br 8/2 [{ Nb 2 S 4}(SCN)8]4 - [{ Nb 2 S 4}(H 2 O)8}4+ Металлокластер Nb 2 Кластерное ядро {Nb 2 S 4}4+ Кластерный комплекс [{Nb 2 S 4}L 8] + L Nb 2 S 4 L 4 L= CH 3 COCHCOCH 3 CF 3 COCHCOC(CH 3)3 CF 3 COCHCOCFC 5 F 10 CF 3 COCHCOC 6 H 5 S 2 CN(C 2 H 5)2 -
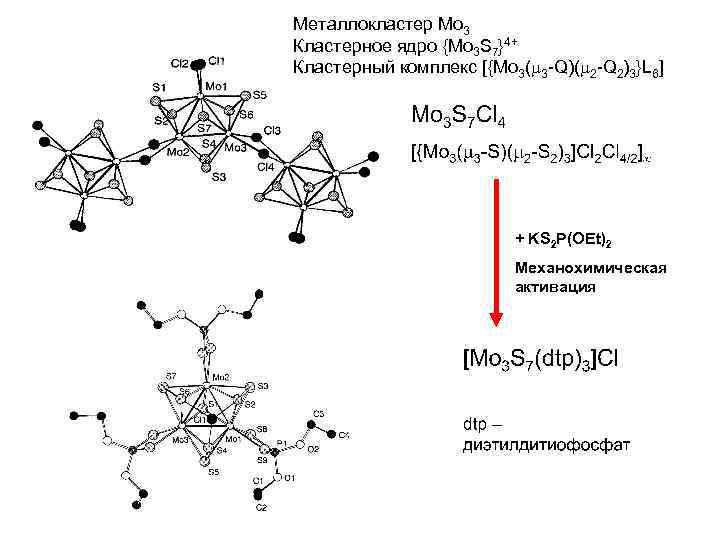 Металлокластер Mo 3 Кластерное ядро {Mo 3 S 7}4+ Кластерный комплекс [{Mo 3( 3 -Q)( 2 -Q 2)3}L 6] + KS 2 P(OEt)2 Механохимическая активация
Металлокластер Mo 3 Кластерное ядро {Mo 3 S 7}4+ Кластерный комплекс [{Mo 3( 3 -Q)( 2 -Q 2)3}L 6] + KS 2 P(OEt)2 Механохимическая активация
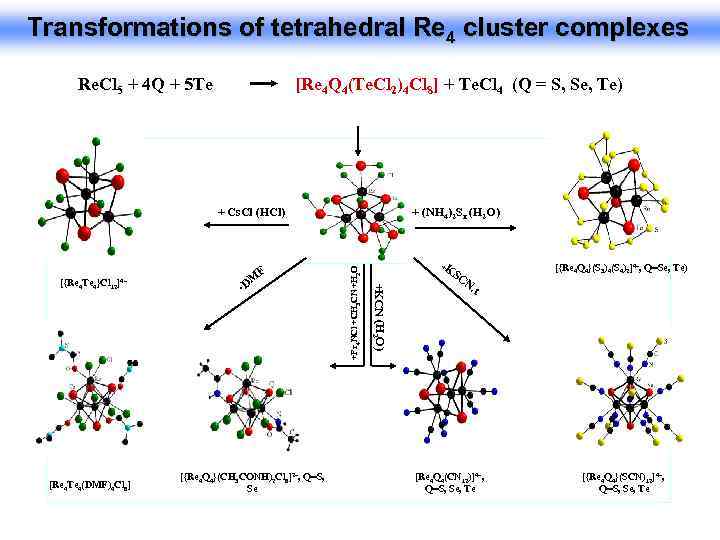 Transformations of tetrahedral Re 4 cluster complexes Re. Cl 5 + 4 Q + 5 Te [Re 4 Q 4(Te. Cl 2)4 Cl 8] + Te. Cl 4 (Q = S, Se, Te) [Re 4 Te 4(DMF)4 Cl 8] + DM [{Re 4 Q 4}(CH 3 CONH)2 Cl 8]2–, Q=S, Se + +KCN (H 2 O) [{Re 4 Te 4}Cl 12]4– F + (NH 4)2 Sx (H 2 O) +Pr 4 NCl +CH 3 CN +H 2 O + Cs. Cl (HCl) KS CN , [{Re 4 Q 4}(S 3)4(S 4)2]4–, Q=Se, Te) t [Re 4 Q 4(CN 12)]4–, Q=S, Se, Te [{Re 4 Q 4}(SCN)12]4–, Q=S, Se, Te
Transformations of tetrahedral Re 4 cluster complexes Re. Cl 5 + 4 Q + 5 Te [Re 4 Q 4(Te. Cl 2)4 Cl 8] + Te. Cl 4 (Q = S, Se, Te) [Re 4 Te 4(DMF)4 Cl 8] + DM [{Re 4 Q 4}(CH 3 CONH)2 Cl 8]2–, Q=S, Se + +KCN (H 2 O) [{Re 4 Te 4}Cl 12]4– F + (NH 4)2 Sx (H 2 O) +Pr 4 NCl +CH 3 CN +H 2 O + Cs. Cl (HCl) KS CN , [{Re 4 Q 4}(S 3)4(S 4)2]4–, Q=Se, Te) t [Re 4 Q 4(CN 12)]4–, Q=S, Se, Te [{Re 4 Q 4}(SCN)12]4–, Q=S, Se, Te
![6. 5 A Кластерный комплекс [{Re 6 S 8}(CN)6]4– Кластерное ядро {Re 6 ( 6. 5 A Кластерный комплекс [{Re 6 S 8}(CN)6]4– Кластерное ядро {Re 6 (](https://present5.com/presentation/5652994_182162819/image-83.jpg) 6. 5 A Кластерный комплекс [{Re 6 S 8}(CN)6]4– Кластерное ядро {Re 6 ( 3 -S 8)}2+ Металлический кластер – октаэдр Re 6 ~11 А
6. 5 A Кластерный комплекс [{Re 6 S 8}(CN)6]4– Кластерное ядро {Re 6 ( 3 -S 8)}2+ Металлический кластер – октаэдр Re 6 ~11 А
![Complexes [Re 6 Q 8 L 6] {Re 6 Q 8}L 6 Q=S, Se, Complexes [Re 6 Q 8 L 6] {Re 6 Q 8}L 6 Q=S, Se,](https://present5.com/presentation/5652994_182162819/image-84.jpg) Complexes [Re 6 Q 8 L 6] {Re 6 Q 8}L 6 Q=S, Se, Te, Cl, Br, O L= F, Cl, Br, I, OH, H 2 O, CN, SCN… N-, P-, O-, S- π-donor organic ligands Q [Re 6 Se 4 Br 4]6+ L [Re 5 Os. Se 8]3+ [Re 5 Mo. Se 8]+ [Re 6 Se 8]2+ VEC=24 e/Re 6 {[Re 6 Se 8](H 2 O)6}2+ {[Re 6 Se 8]Br 6}4 -
Complexes [Re 6 Q 8 L 6] {Re 6 Q 8}L 6 Q=S, Se, Te, Cl, Br, O L= F, Cl, Br, I, OH, H 2 O, CN, SCN… N-, P-, O-, S- π-donor organic ligands Q [Re 6 Se 4 Br 4]6+ L [Re 5 Os. Se 8]3+ [Re 5 Mo. Se 8]+ [Re 6 Se 8]2+ VEC=24 e/Re 6 {[Re 6 Se 8](H 2 O)6}2+ {[Re 6 Se 8]Br 6}4 -
 • Имеется глубокая аналогия между кластерными соединениями металлов и каркасными соединениями неметаллических элементов, таких, как B, P, As и др. • В настоящее время для большинства элементов (как для переходных, так и для непереходных металлов) получены соединения, содержащие остов в виде цепей, циклов, каркасов и полиэдров, образованных данным элементом, в которых имеются связи элемент-элемент. • Химию кластерных соединений образно можно определить как «органическую химию» неуглеродных элементов (С. П. Губин).
• Имеется глубокая аналогия между кластерными соединениями металлов и каркасными соединениями неметаллических элементов, таких, как B, P, As и др. • В настоящее время для большинства элементов (как для переходных, так и для непереходных металлов) получены соединения, содержащие остов в виде цепей, циклов, каркасов и полиэдров, образованных данным элементом, в которых имеются связи элемент-элемент. • Химию кластерных соединений образно можно определить как «органическую химию» неуглеродных элементов (С. П. Губин).
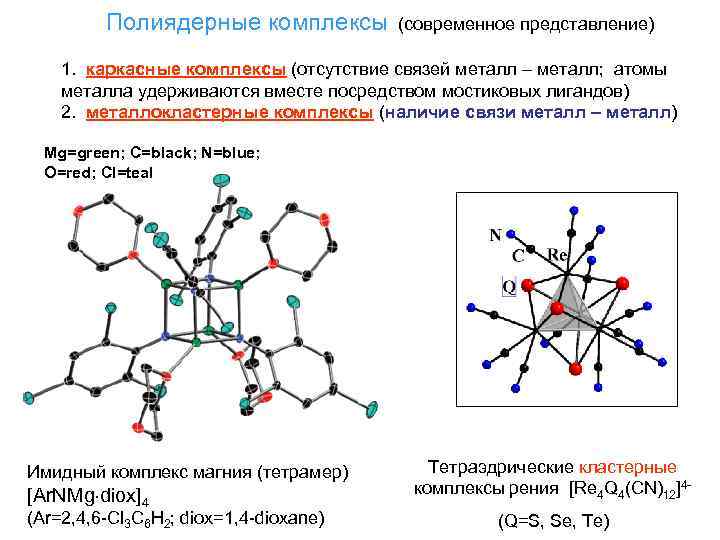 Полиядерные комплексы (современное представление) 1. каркасные комплексы (отсутствие связей металл – металл; атомы металла удерживаются вместе посредством мостиковых лигандов) 2. металлокластерные комплексы (наличие связи металл – металл) Mg=green; C=black; N=blue; O=red; Cl=teal Тетраэдрические кластерные Имидный комплекс магния (тетрамер) комплексы рения [Re 4 Q 4(CN)12]4[Ar. NMg diox]4 (Ar=2, 4, 6 -Cl 3 C 6 H 2; diox=1, 4 -dioxane) (Q=S, Se, Te)
Полиядерные комплексы (современное представление) 1. каркасные комплексы (отсутствие связей металл – металл; атомы металла удерживаются вместе посредством мостиковых лигандов) 2. металлокластерные комплексы (наличие связи металл – металл) Mg=green; C=black; N=blue; O=red; Cl=teal Тетраэдрические кластерные Имидный комплекс магния (тетрамер) комплексы рения [Re 4 Q 4(CN)12]4[Ar. NMg diox]4 (Ar=2, 4, 6 -Cl 3 C 6 H 2; diox=1, 4 -dioxane) (Q=S, Se, Te)
![[Cp. VCl 2(PMe 3] + Se(Si. Me 3)2 (THF) V 6( 6 -O)( 3 [Cp. VCl 2(PMe 3] + Se(Si. Me 3)2 (THF) V 6( 6 -O)( 3](https://present5.com/presentation/5652994_182162819/image-87.jpg) [Cp. VCl 2(PMe 3] + Se(Si. Me 3)2 (THF) V 6( 6 -O)( 3 -Se)8(PMe 3)6 Металлокластерный комплекс D. Fenske, A. Grissinger, M. Loos und J. Magull Neue oktaedrische Metallcluster des Zr und V. Die Kristallstrukturen von [Cp 6 Zr 6 S 9] und [V 6 Se 8 O(PMe 3)6]. Z. anorg. allg. Chem. 1991, 598/599, 121 -128 [(V 3+)6(O 2 -)(Se 2 -)8(PMe 3)6] V. . . V 2, 794 -2, 839 Å d 2 – электронная конфигурация Zr 4+ КВЭ=12
[Cp. VCl 2(PMe 3] + Se(Si. Me 3)2 (THF) V 6( 6 -O)( 3 -Se)8(PMe 3)6 Металлокластерный комплекс D. Fenske, A. Grissinger, M. Loos und J. Magull Neue oktaedrische Metallcluster des Zr und V. Die Kristallstrukturen von [Cp 6 Zr 6 S 9] und [V 6 Se 8 O(PMe 3)6]. Z. anorg. allg. Chem. 1991, 598/599, 121 -128 [(V 3+)6(O 2 -)(Se 2 -)8(PMe 3)6] V. . . V 2, 794 -2, 839 Å d 2 – электронная конфигурация Zr 4+ КВЭ=12
![[Cp. Zr. Cl 3] + S(Si. Me 3)2 (THF) Zr 6( 6 -S)( 3 [Cp. Zr. Cl 3] + S(Si. Me 3)2 (THF) Zr 6( 6 -S)( 3](https://present5.com/presentation/5652994_182162819/image-88.jpg) [Cp. Zr. Cl 3] + S(Si. Me 3)2 (THF) Zr 6( 6 -S)( 3 -S)8(Cp)6 Каркасный полиядерный комплекс D. Fenske, A. Grissinger, M. Loos und J. Magull Neue oktaedrische Metallcluster des Zr und V. Die Kristallstrukturen von [Cp 6 Zr 6 S 9] und [V 6 Se 8 O(PMe 3)6]. Z. anorg. allg. Chem. 1991, 598/599, 121 -128 [(Zr 4+)6(S 2 -)9(Cp 1 -)6] Zr. . . Zr 3, 634 -3, 643 Å d 0 – электронная конфигурация Zr 4+ КВЭ = 0 «ложный металлокластер»
[Cp. Zr. Cl 3] + S(Si. Me 3)2 (THF) Zr 6( 6 -S)( 3 -S)8(Cp)6 Каркасный полиядерный комплекс D. Fenske, A. Grissinger, M. Loos und J. Magull Neue oktaedrische Metallcluster des Zr und V. Die Kristallstrukturen von [Cp 6 Zr 6 S 9] und [V 6 Se 8 O(PMe 3)6]. Z. anorg. allg. Chem. 1991, 598/599, 121 -128 [(Zr 4+)6(S 2 -)9(Cp 1 -)6] Zr. . . Zr 3, 634 -3, 643 Å d 0 – электронная конфигурация Zr 4+ КВЭ = 0 «ложный металлокластер»
![Комплекс [Nb 6 Cl 18 ]4 - Металлокластерный комплекс Полиоксомолибдат-ион [Mo 6 O 19]2 Комплекс [Nb 6 Cl 18 ]4 - Металлокластерный комплекс Полиоксомолибдат-ион [Mo 6 O 19]2](https://present5.com/presentation/5652994_182162819/image-89.jpg) Комплекс [Nb 6 Cl 18 ]4 - Металлокластерный комплекс Полиоксомолибдат-ион [Mo 6 O 19]2 Каркасный полиядерный комплекс «ложный металлокластер» [(Nb 2. 33+)6(Cl-)18]4 - Nb. . . Nb 3, 634 -3, 643 Å d 2. 67 – электронная конфигурация Nb 2. 33+ КВЭ = 16 [(Mo 6+)6(O 2 -)19]2 - Mo. . . Mo 3, 634 -3, 643 Å d 0 – электронная конфигурация Mo 6+ КВЭ = 0
Комплекс [Nb 6 Cl 18 ]4 - Металлокластерный комплекс Полиоксомолибдат-ион [Mo 6 O 19]2 Каркасный полиядерный комплекс «ложный металлокластер» [(Nb 2. 33+)6(Cl-)18]4 - Nb. . . Nb 3, 634 -3, 643 Å d 2. 67 – электронная конфигурация Nb 2. 33+ КВЭ = 16 [(Mo 6+)6(O 2 -)19]2 - Mo. . . Mo 3, 634 -3, 643 Å d 0 – электронная конфигурация Mo 6+ КВЭ = 0
 По классификации С. П. Губина: Кластерные соединения, в которых связи М-М находятся в пределах дискретного молекулярного комплекса, называются молекулярными. Когда связи М-М участвуют в образовании протяженной пространственной структуры полимерного характера, такие соединения называют кластерными материалами. Стабильность кластерных соединений Прочность связи М-М увеличивается при движении вниз по группе (возможно, из-за большего размера d-орбиталей более тяжелых атомов). Это, по-видимому, объясняет, почему для 4 d и 5 d элементов существует намного больше кластерных соединений, чем для 3 d металлов. Наиболее прочная связь металл-металл в простых веществах наблюдается для элементов 4 d и 5 d рядов; эта же закономерность сохраняется и для их соединений. Для р-элементов наблюдается обратная закономерность: связь элемент-элемент ослабевает при движении вниз по группе.
По классификации С. П. Губина: Кластерные соединения, в которых связи М-М находятся в пределах дискретного молекулярного комплекса, называются молекулярными. Когда связи М-М участвуют в образовании протяженной пространственной структуры полимерного характера, такие соединения называют кластерными материалами. Стабильность кластерных соединений Прочность связи М-М увеличивается при движении вниз по группе (возможно, из-за большего размера d-орбиталей более тяжелых атомов). Это, по-видимому, объясняет, почему для 4 d и 5 d элементов существует намного больше кластерных соединений, чем для 3 d металлов. Наиболее прочная связь металл-металл в простых веществах наблюдается для элементов 4 d и 5 d рядов; эта же закономерность сохраняется и для их соединений. Для р-элементов наблюдается обратная закономерность: связь элемент-элемент ослабевает при движении вниз по группе.
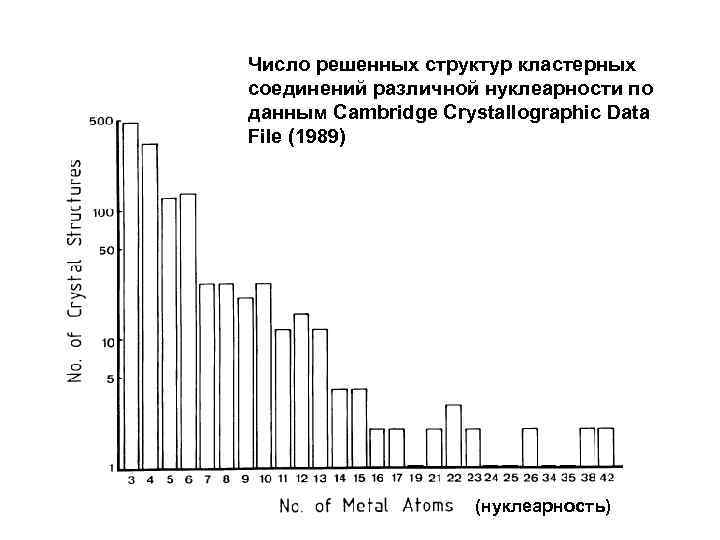 Число решенных структур кластерных соединений различной нуклеарности по данным Cambridge Crystallographic Data File (1989) (нуклеарность)
Число решенных структур кластерных соединений различной нуклеарности по данным Cambridge Crystallographic Data File (1989) (нуклеарность)



