ОВР.ppt
- Количество слайдов: 38
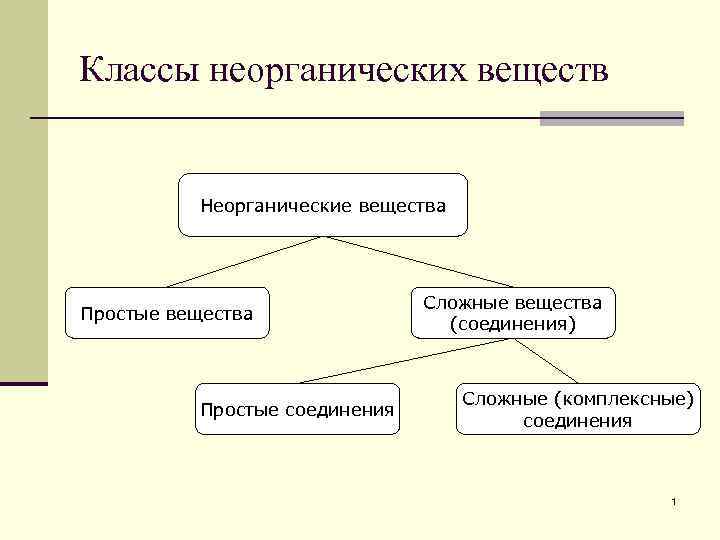 Классы неорганических веществ Неорганические вещества Простые соединения Сложные вещества (соединения) Сложные (комплексные) соединения 1
Классы неорганических веществ Неорганические вещества Простые соединения Сложные вещества (соединения) Сложные (комплексные) соединения 1
 Простые вещества n Неметаллы n 22, включая 6 благородных газов n Имеют высокие значения электроотрицательности (χ): F 4, 1; O 3, 5; N 3, 1 n Образуют анионы n Металлы n 11 типичных, остальные – "амфотерные" n Имеют низкие значения электроотрицательности (χ): K 0, 91; Li 0, 97; Ca 1, 04 n Образуют катионы 2
Простые вещества n Неметаллы n 22, включая 6 благородных газов n Имеют высокие значения электроотрицательности (χ): F 4, 1; O 3, 5; N 3, 1 n Образуют анионы n Металлы n 11 типичных, остальные – "амфотерные" n Имеют низкие значения электроотрицательности (χ): K 0, 91; Li 0, 97; Ca 1, 04 n Образуют катионы 2
 Окислительновосстановительные реакции (ОВР) Химические реакции Без изменения степени окисления (обменные) С изменением степени окисления (ОВР) 3
Окислительновосстановительные реакции (ОВР) Химические реакции Без изменения степени окисления (обменные) С изменением степени окисления (ОВР) 3
 Степень окисления n формальный (условный) заряд атома в соединении, вычисленный, исходя из предположения, что соединение состоит из ионов n Степень окисления: Cl. VII, Mo. VI, F–I (римские цифры) n Заряд иона в растворе: Ba 2+, Na+, S 2– (арабские цифры) 4
Степень окисления n формальный (условный) заряд атома в соединении, вычисленный, исходя из предположения, что соединение состоит из ионов n Степень окисления: Cl. VII, Mo. VI, F–I (римские цифры) n Заряд иона в растворе: Ba 2+, Na+, S 2– (арабские цифры) 4
 Степень окисления n не совпадает с истинным зарядом атома в соединении H+0, 17 Cl– 0, 17 n не совпадает с валентностью (числом ковалентных связей) H–O–I–H 5
Степень окисления n не совпадает с истинным зарядом атома в соединении H+0, 17 Cl– 0, 17 n не совпадает с валентностью (числом ковалентных связей) H–O–I–H 5
 Изменение степени окисления n = перераспределение электронной плотности ("передача электронов") 2 e– n HCl. O + H 2 S = HCl + S + H 2 O Окислитель (Ок) Восстановитель (Вс) Cl. I, HCl. O S–II, H 2 S Понижает степень окисления Повышает степень окисления Принимает электроны Отдает электроны Восстанавливается Окисляется Cl. I S–II + 2 e– = Cl–I – 2 e– = S 0 6
Изменение степени окисления n = перераспределение электронной плотности ("передача электронов") 2 e– n HCl. O + H 2 S = HCl + S + H 2 O Окислитель (Ок) Восстановитель (Вс) Cl. I, HCl. O S–II, H 2 S Понижает степень окисления Повышает степень окисления Принимает электроны Отдает электроны Восстанавливается Окисляется Cl. I S–II + 2 e– = Cl–I – 2 e– = S 0 6
 Подбор коэффициентов в уравнениях ОВР Метод электронного баланса n n n 1. Записывают формулы реагентов и продуктов, находят элементы, которые понижают и повышают степени окисления 2. Записывают атомы с указанием изменяющихся степеней окисления 3. Составляют уравнения полуреакций восстановления и окисления, соблюдая для каждой из них законы сохранения числа атомов и заряда 4. Находят наименьшее общее кратное (н. о. к. ) числа переданных в каждой полуреакции электронов и подбирают дополнительные множители для уравнений полуреакций так, чтобы число принятых электронов стало равным числу отданных электронов 5. Проставляют полученные коэффициенты в схему реакции 6. Уравнивают числа остальных атомов n Mn. CO 3 + KCl. O 3 Mn. O 2 + KCl +. . . n Mn. II → Mn. IV Cl. V → Cl–I n n n Mn. II – 2 e– = Mn. IV Cl. V + 6 e– = Cl–I n н. о. к. 6 Mn. II – 2 e– = Mn. IV Cl. V + 6 e– = Cl–I n 3 Mn. CO 3 + KCl. O 3 3 Mn. O 2 + KCl +. . . n 3 Mn. CO 3 + KCl. O 3 3 Mn. O 2 + KCl + 3 CO 2 n n |3 |1 7
Подбор коэффициентов в уравнениях ОВР Метод электронного баланса n n n 1. Записывают формулы реагентов и продуктов, находят элементы, которые понижают и повышают степени окисления 2. Записывают атомы с указанием изменяющихся степеней окисления 3. Составляют уравнения полуреакций восстановления и окисления, соблюдая для каждой из них законы сохранения числа атомов и заряда 4. Находят наименьшее общее кратное (н. о. к. ) числа переданных в каждой полуреакции электронов и подбирают дополнительные множители для уравнений полуреакций так, чтобы число принятых электронов стало равным числу отданных электронов 5. Проставляют полученные коэффициенты в схему реакции 6. Уравнивают числа остальных атомов n Mn. CO 3 + KCl. O 3 Mn. O 2 + KCl +. . . n Mn. II → Mn. IV Cl. V → Cl–I n n n Mn. II – 2 e– = Mn. IV Cl. V + 6 e– = Cl–I n н. о. к. 6 Mn. II – 2 e– = Mn. IV Cl. V + 6 e– = Cl–I n 3 Mn. CO 3 + KCl. O 3 3 Mn. O 2 + KCl +. . . n 3 Mn. CO 3 + KCl. O 3 3 Mn. O 2 + KCl + 3 CO 2 n n |3 |1 7
 Подбор коэффициентов в уравнениях ОВР Метод электронного баланса Fe. S 2 + O 2 Fe 2 O 3 + SO 2 n Fe. II – 1 e– = Fe. III – 11 e– n 2 S–I – 10 e– = 2 SIV n O 2 + 4 e– = 2 O–II +4 e– 4 Fe. S 2 + 11 O 2 = 2 Fe 2 O 3 + 8 SO 2 4 11 8
Подбор коэффициентов в уравнениях ОВР Метод электронного баланса Fe. S 2 + O 2 Fe 2 O 3 + SO 2 n Fe. II – 1 e– = Fe. III – 11 e– n 2 S–I – 10 e– = 2 SIV n O 2 + 4 e– = 2 O–II +4 e– 4 Fe. S 2 + 11 O 2 = 2 Fe 2 O 3 + 8 SO 2 4 11 8
 Подбор коэффициентов в уравнениях ОВР Метод электронно-ионных полуреакций n n n 1. Записывают формулы реагентов и продуктов, находят окислитель, восстановитель и среду 2. Записывают формулы окислителя и восстановителя и соответствующие продукты реакции в ионном виде 3. Составляют ионные уравнения полуреакций восстановления и окисления, соблюдая для каждой из них законы сохранения числа атомов и заряда 4. Находят наименьшее общее кратное (н. о. к. ) числа переданных в каждой полуреакции электронов и подбирают дополнительные множители для уравнений полуреакций так, чтобы число принятых электронов стало равным числу отданных электронов 5. Составляют ионное уравнение реакции 6. Уравнивают числа остальных атомов, участвующих в реакции, и получают уравнение реакции с подобранными коэффициентами n n K 2 Cr 2 O 7 + H 2 SO 4 + H 2 S S +. . . Ок Среда Вс n n n Cr 2 O 72– + H+ + H 2 S S + Cr 3+ + H 2 O Cr 2 O 72– (Оф) → Cr 3+ (Вф) H 2 S (Вф) → S (Оф) n n Cr 2 O 72– + 8 H+ + 6 e– = 2 Cr 3+ + 7 H 2 O H 2 S – 2 e– = S + 2 H+ n n n н. о. к. 6 Cr 2 O 72– + 8 H+ + 6 e– = 2 Cr 3+ + 7 H 2 O | 1 H 2 S – 2 e– = S + 2 H+ |3 n Cr 2 O 72– + 8 H+ + 3 H 2 S = 3 S + 2 Cr 3+ + 7 H 2 O n K 2 Cr 2 O 7 + 4 H 2 SO 4 + 3 H 2 S = 3 S + Cr 2(SO 4)3 + 7 H 2 O + K 2 SO 4 9
Подбор коэффициентов в уравнениях ОВР Метод электронно-ионных полуреакций n n n 1. Записывают формулы реагентов и продуктов, находят окислитель, восстановитель и среду 2. Записывают формулы окислителя и восстановителя и соответствующие продукты реакции в ионном виде 3. Составляют ионные уравнения полуреакций восстановления и окисления, соблюдая для каждой из них законы сохранения числа атомов и заряда 4. Находят наименьшее общее кратное (н. о. к. ) числа переданных в каждой полуреакции электронов и подбирают дополнительные множители для уравнений полуреакций так, чтобы число принятых электронов стало равным числу отданных электронов 5. Составляют ионное уравнение реакции 6. Уравнивают числа остальных атомов, участвующих в реакции, и получают уравнение реакции с подобранными коэффициентами n n K 2 Cr 2 O 7 + H 2 SO 4 + H 2 S S +. . . Ок Среда Вс n n n Cr 2 O 72– + H+ + H 2 S S + Cr 3+ + H 2 O Cr 2 O 72– (Оф) → Cr 3+ (Вф) H 2 S (Вф) → S (Оф) n n Cr 2 O 72– + 8 H+ + 6 e– = 2 Cr 3+ + 7 H 2 O H 2 S – 2 e– = S + 2 H+ n n n н. о. к. 6 Cr 2 O 72– + 8 H+ + 6 e– = 2 Cr 3+ + 7 H 2 O | 1 H 2 S – 2 e– = S + 2 H+ |3 n Cr 2 O 72– + 8 H+ + 3 H 2 S = 3 S + 2 Cr 3+ + 7 H 2 O n K 2 Cr 2 O 7 + 4 H 2 SO 4 + 3 H 2 S = 3 S + Cr 2(SO 4)3 + 7 H 2 O + K 2 SO 4 9
![Подбор числа атомов водорода и кислорода n Кислотная среда n [HI] = H+ n Подбор числа атомов водорода и кислорода n Кислотная среда n [HI] = H+ n](https://present5.com/presentation/3/-43958340_132785077.pdf-img/-43958340_132785077.pdf-10.jpg) Подбор числа атомов водорода и кислорода n Кислотная среда n [HI] = H+ n [O–II] + 2 H+ = H 2 O n Щелочная среда n [HI] + OH– = H 2 O n [O–II] + H 2 O = 2 OH– Пример [Cr(OH)6]3– Cr. O 42– Щелочная среда 6[HI] + 6 OH– = 6 H 2 O 2[O–II] + 2 H 2 O = 4 OH– [Cr(OH)6]3– + 2 OH– – 3 e– = Cr. O 42– + 4 H 2 O 10
Подбор числа атомов водорода и кислорода n Кислотная среда n [HI] = H+ n [O–II] + 2 H+ = H 2 O n Щелочная среда n [HI] + OH– = H 2 O n [O–II] + H 2 O = 2 OH– Пример [Cr(OH)6]3– Cr. O 42– Щелочная среда 6[HI] + 6 OH– = 6 H 2 O 2[O–II] + 2 H 2 O = 4 OH– [Cr(OH)6]3– + 2 OH– – 3 e– = Cr. O 42– + 4 H 2 O 10
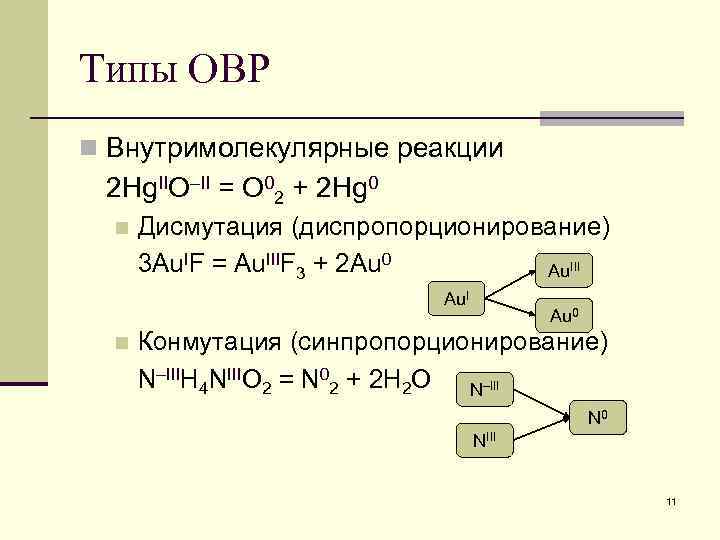 Типы ОВР n Внутримолекулярные реакции 2 Hg. IIO–II = O 02 + 2 Hg 0 n Дисмутация (диспропорционирование) 3 Au. IF = Au. IIIF 3 + 2 Au 0 Au. III Au. I n Au 0 Конмутация (синпропорционирование) N–IIIH 4 NIIIO 2 = N 02 + 2 H 2 O N–III N 0 NIII 11
Типы ОВР n Внутримолекулярные реакции 2 Hg. IIO–II = O 02 + 2 Hg 0 n Дисмутация (диспропорционирование) 3 Au. IF = Au. IIIF 3 + 2 Au 0 Au. III Au. I n Au 0 Конмутация (синпропорционирование) N–IIIH 4 NIIIO 2 = N 02 + 2 H 2 O N–III N 0 NIII 11
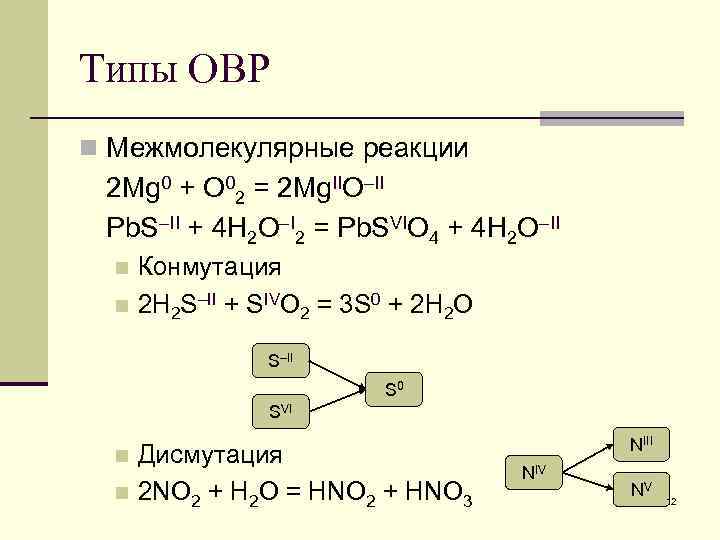 Типы ОВР n Межмолекулярные реакции 2 Mg 0 + O 02 = 2 Mg. IIO–II Pb. S–II + 4 H 2 O–I 2 = Pb. SVIO 4 + 4 H 2 O–II Конмутация n 2 H 2 S–II + SIVO 2 = 3 S 0 + 2 H 2 O n S–II S 0 SVI Дисмутация n 2 NO 2 + H 2 O = HNO 2 + HNO 3 n NIII NIV NV 12
Типы ОВР n Межмолекулярные реакции 2 Mg 0 + O 02 = 2 Mg. IIO–II Pb. S–II + 4 H 2 O–I 2 = Pb. SVIO 4 + 4 H 2 O–II Конмутация n 2 H 2 S–II + SIVO 2 = 3 S 0 + 2 H 2 O n S–II S 0 SVI Дисмутация n 2 NO 2 + H 2 O = HNO 2 + HNO 3 n NIII NIV NV 12
 Типичные окислители и восстановители n Окислители: n n Простые вещества – элементы с высокой электроотрицательностью (F 2, O 2, Cl 2 и т. д. ) Сложные вещества – содержащие элементы в высоких степенях окисления (Fe 3+, Cr. VI 2 O 72–, Mn. VIIO 4– и т. д. ) Окислительная активность возрастает в кислотной среде n Восстановители: n n Простые вещества – элементы с низкой электроотрицательностью (металлы, С, H 2 и т. д. ) Сложные вещества – содержащие элементы в низких степенях окисления (Sn 2+, S 2–, NIIIO 2– и т. д. ) Восстановительная способность возрастает в щелочной среде 13
Типичные окислители и восстановители n Окислители: n n Простые вещества – элементы с высокой электроотрицательностью (F 2, O 2, Cl 2 и т. д. ) Сложные вещества – содержащие элементы в высоких степенях окисления (Fe 3+, Cr. VI 2 O 72–, Mn. VIIO 4– и т. д. ) Окислительная активность возрастает в кислотной среде n Восстановители: n n Простые вещества – элементы с низкой электроотрицательностью (металлы, С, H 2 и т. д. ) Сложные вещества – содержащие элементы в низких степенях окисления (Sn 2+, S 2–, NIIIO 2– и т. д. ) Восстановительная способность возрастает в щелочной среде 13
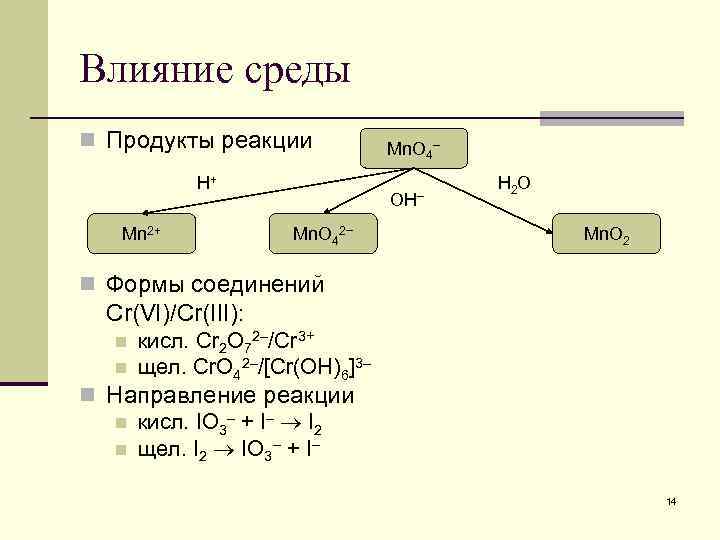 Влияние среды n Продукты реакции H+ Mn 2+ Mn. O 4– OH– Mn. O 42– H 2 O Mn. O 2 n Формы соединений Cr(VI)/Cr(III): n n кисл. Cr 2 O 72–/Cr 3+ щел. Cr. O 42–/[Cr(OH)6]3– n Направление реакции n кисл. IO 3– + I– I 2 n щел. I 2 IO 3– + I– 14
Влияние среды n Продукты реакции H+ Mn 2+ Mn. O 4– OH– Mn. O 42– H 2 O Mn. O 2 n Формы соединений Cr(VI)/Cr(III): n n кисл. Cr 2 O 72–/Cr 3+ щел. Cr. O 42–/[Cr(OH)6]3– n Направление реакции n кисл. IO 3– + I– I 2 n щел. I 2 IO 3– + I– 14
 Направление ОВР n Br– + Pb. O 2 + H+ Br 2 + Pb 2+ + H 2 O n Br– + Fe 3+ ≠ Br 2 + Fe 2+ n Br 2 + Fe 2+ Br– + Fe 3+ n Количественная мера окислительной способности Ок (и восстановительной способности Вс) – электродный потенциал φ 15
Направление ОВР n Br– + Pb. O 2 + H+ Br 2 + Pb 2+ + H 2 O n Br– + Fe 3+ ≠ Br 2 + Fe 2+ n Br 2 + Fe 2+ Br– + Fe 3+ n Количественная мера окислительной способности Ок (и восстановительной способности Вс) – электродный потенциал φ 15
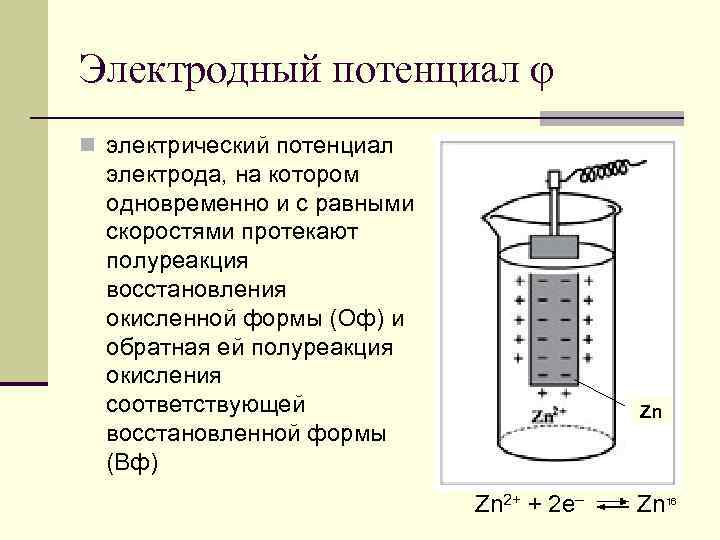 Электродный потенциал φ n электрический потенциал электрода, на котором одновременно и с равными скоростями протекают полуреакция восстановления окисленной формы (Оф) и обратная ей полуреакция окисления соответствующей восстановленной формы (Вф) Zn Zn 2+ + 2 e– Zn 16
Электродный потенциал φ n электрический потенциал электрода, на котором одновременно и с равными скоростями протекают полуреакция восстановления окисленной формы (Оф) и обратная ей полуреакция окисления соответствующей восстановленной формы (Вф) Zn Zn 2+ + 2 e– Zn 16
 Разность потенциалов Δφ n Оф(1) + Вф(2) n Оф(1) + n 1 e– n Вф(2) – n 1 e– Вф(1) + Оф(2) Вф(1) Оф(2) Δφ = φ1 – φ2 Δφ > 0 Оф(1)/Вф(1) φ1 Оф(2)/Вф(2) φ2 Δφ < 0 17
Разность потенциалов Δφ n Оф(1) + Вф(2) n Оф(1) + n 1 e– n Вф(2) – n 1 e– Вф(1) + Оф(2) Вф(1) Оф(2) Δφ = φ1 – φ2 Δφ > 0 Оф(1)/Вф(1) φ1 Оф(2)/Вф(2) φ2 Δφ < 0 17
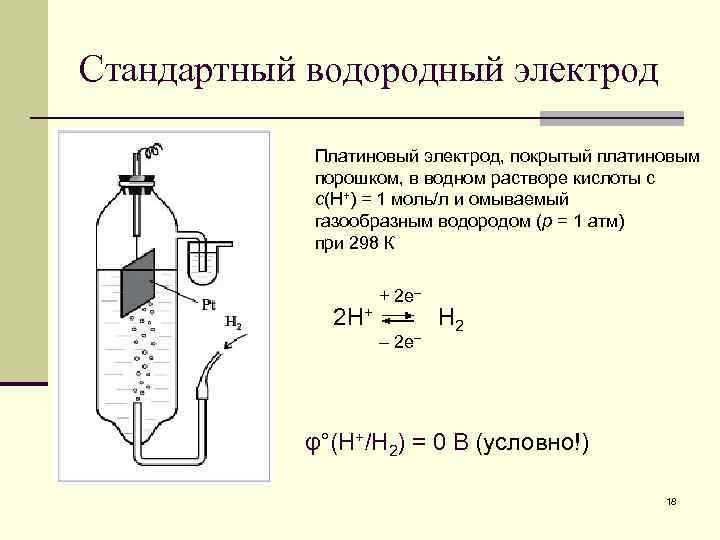 Стандартный водородный электрод Платиновый электрод, покрытый платиновым порошком, в водном растворе кислоты с с(Н+) = 1 моль/л и омываемый газообразным водородом (р = 1 атм) при 298 К 2 H+ + 2 e– – 2 e– H 2 φ°(H+/H 2) = 0 В (условно!) 18
Стандартный водородный электрод Платиновый электрод, покрытый платиновым порошком, в водном растворе кислоты с с(Н+) = 1 моль/л и омываемый газообразным водородом (р = 1 атм) при 298 К 2 H+ + 2 e– – 2 e– H 2 φ°(H+/H 2) = 0 В (условно!) 18
 Стандартный потенциал полуреакции восстановления φ° n n Оф + Н 2 Вф + 2 Н+ Δφ° = φ°(Оф/Вф) – φ°(Н+/Н 2) = φ°(Оф/Вф) Данные приведены в справочниках Стандартные условия: ci = 1 моль/л (для каждого участника реакции в растворе) n pi = 1 атм (для каждого газообразного участника реакции) n Т = 298 К (обычно) ст. у. ≠ н. у. (0°С, 1 атм) n 19
Стандартный потенциал полуреакции восстановления φ° n n Оф + Н 2 Вф + 2 Н+ Δφ° = φ°(Оф/Вф) – φ°(Н+/Н 2) = φ°(Оф/Вф) Данные приведены в справочниках Стандартные условия: ci = 1 моль/л (для каждого участника реакции в растворе) n pi = 1 атм (для каждого газообразного участника реакции) n Т = 298 К (обычно) ст. у. ≠ н. у. (0°С, 1 атм) n 19
 Сравнение φ° Li n ЭХРН φ°, В Zn Pb – 3, 1 – 0, 8 – 0, 1 H 0 Cu Au +0, 3 +1, 4 (Mn+/M) n Сила Ок и Вс φ°, В Pb. O 2 Pb 2+ 1, 5 Br 2 Br– 1, 1 Сила Вс Вф Сила Ок Оф 20
Сравнение φ° Li n ЭХРН φ°, В Zn Pb – 3, 1 – 0, 8 – 0, 1 H 0 Cu Au +0, 3 +1, 4 (Mn+/M) n Сила Ок и Вс φ°, В Pb. O 2 Pb 2+ 1, 5 Br 2 Br– 1, 1 Сила Вс Вф Сила Ок Оф 20
 Критерий протекания ОВР в стандартных условиях n ОВР протекает в прямом направлении в стандартных условиях, если Δφ° = φ°(Ок) – φ°(Вс) > 0 В n ОВР протекает в обратном направлении в стандартных условиях, если Δφ° = φ°(Ок) – φ°(Вс) < 0 В 21
Критерий протекания ОВР в стандартных условиях n ОВР протекает в прямом направлении в стандартных условиях, если Δφ° = φ°(Ок) – φ°(Вс) > 0 В n ОВР протекает в обратном направлении в стандартных условиях, если Δφ° = φ°(Ок) – φ°(Вс) < 0 В 21
 Уравнение Нернста n На практике стандартные условия не используются n Оф + ne– = Вф n Mn. O 4– + 8 H+ + 5 e– = Mn 2+ + 4 H 2 O n Во время протекания реакции φ измерить нельзя, но можно вычислить n По мере протекания реакции φ(Ок) , а φ(Вс) n Когда φ(Ок) = φ(Вс), реакция прекращается 22
Уравнение Нернста n На практике стандартные условия не используются n Оф + ne– = Вф n Mn. O 4– + 8 H+ + 5 e– = Mn 2+ + 4 H 2 O n Во время протекания реакции φ измерить нельзя, но можно вычислить n По мере протекания реакции φ(Ок) , а φ(Вс) n Когда φ(Ок) = φ(Вс), реакция прекращается 22
 Критерий полноты протекания ОВР n ОВР протекает в прямом направлении до конца при любых начальных условиях, если Δφ° > 0, 4 В n ОВР протекает в обратном направлении до конца при любых начальных условиях, если Δφ° < – 0, 4 В n Можно изменить направление ОВР, меняя условия, если 0 < Δφ° < 0, 4 В (в ст. у. ) или – 0, 4 < Δφ° < 0 В (в ст. у. ) 23
Критерий полноты протекания ОВР n ОВР протекает в прямом направлении до конца при любых начальных условиях, если Δφ° > 0, 4 В n ОВР протекает в обратном направлении до конца при любых начальных условиях, если Δφ° < – 0, 4 В n Можно изменить направление ОВР, меняя условия, если 0 < Δφ° < 0, 4 В (в ст. у. ) или – 0, 4 < Δφ° < 0 В (в ст. у. ) 23
 Пример n Cu(т) + 2 H 2 SO 4 = Cu. SO 4 + SO 2(г) + 2 H 2 O n Δφ° = – 0, 179 В n В стандартных условиях n Cu. SO 4 + SO 2(г) + 2 H 2 O = Cu(т) + 2 H 2 SO 4 n При повышении c(H 2 SO 4), удалении SO 2 n Температура почти не влияет на φ°, влияет на скорость реакции, удаление газообразных веществ 24
Пример n Cu(т) + 2 H 2 SO 4 = Cu. SO 4 + SO 2(г) + 2 H 2 O n Δφ° = – 0, 179 В n В стандартных условиях n Cu. SO 4 + SO 2(г) + 2 H 2 O = Cu(т) + 2 H 2 SO 4 n При повышении c(H 2 SO 4), удалении SO 2 n Температура почти не влияет на φ°, влияет на скорость реакции, удаление газообразных веществ 24
 Кинетические затруднения n Обычно ОВР идут быстро, но не всегда n Fe 3+ + NH 4+ ≠ N 2 + Fe 2+ + H+ n Δφ° = 0, 499 В n 2 катиона n I– + NO 3– + H+ ≠ I 2 + NO + H 2 O n Δφ° = 0, 420 В n 2 аниона n + Zn: n NO 3– + Zn + 3 H+ = HNO 2 + H 2 O + Zn 2+ n 2 I– + 2 HNO 2 + 2 H+ = I 2 + 2 NO + H 2 O n анион + молекула 25
Кинетические затруднения n Обычно ОВР идут быстро, но не всегда n Fe 3+ + NH 4+ ≠ N 2 + Fe 2+ + H+ n Δφ° = 0, 499 В n 2 катиона n I– + NO 3– + H+ ≠ I 2 + NO + H 2 O n Δφ° = 0, 420 В n 2 аниона n + Zn: n NO 3– + Zn + 3 H+ = HNO 2 + H 2 O + Zn 2+ n 2 I– + 2 HNO 2 + 2 H+ = I 2 + 2 NO + H 2 O n анион + молекула 25
 Пример n Какие галогениды могут быть окислены катионом Fe 3+ в стандартных условиях? n 2 Г– + 2 Fe 3+ = Г 2 + 2 Fe 2+ n Оф/Вф φ°, В Δφ°, В ст. у. n Fe 3+/Fe 2+ 0, 77 n F 2/F– 2, 86 – 2, 09 n Cl 2/Cl– 1, 36 – 0, 59 n Br 2/Br– 1, 07 – 0, 30 n I 2/I– 0, 54 +0, 23 26
Пример n Какие галогениды могут быть окислены катионом Fe 3+ в стандартных условиях? n 2 Г– + 2 Fe 3+ = Г 2 + 2 Fe 2+ n Оф/Вф φ°, В Δφ°, В ст. у. n Fe 3+/Fe 2+ 0, 77 n F 2/F– 2, 86 – 2, 09 n Cl 2/Cl– 1, 36 – 0, 59 n Br 2/Br– 1, 07 – 0, 30 n I 2/I– 0, 54 +0, 23 26
 Диаграмма Латимера 0, 77 Fe 3+ 1 e– – 0, 44 Fe 2+ 2 e– Fe 27
Диаграмма Латимера 0, 77 Fe 3+ 1 e– – 0, 44 Fe 2+ 2 e– Fe 27
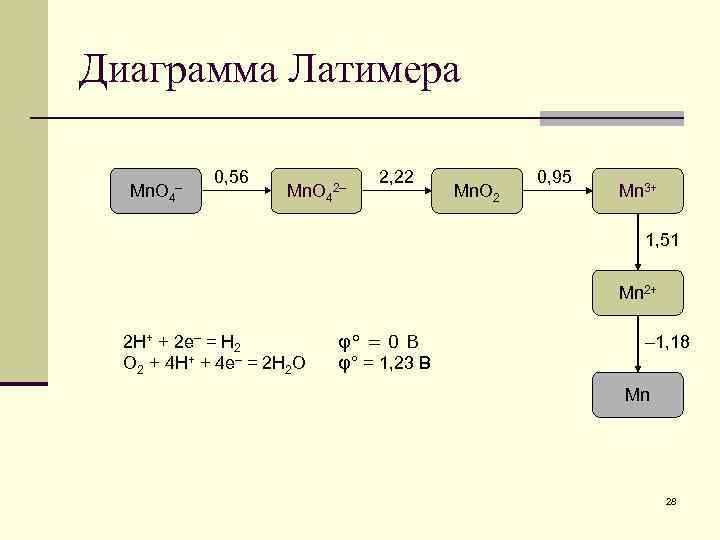 Диаграмма Латимера Mn. O 4 – 0, 56 Mn. O 4 2– 2, 22 Mn. O 2 0, 95 Mn 3+ 1, 51 Mn 2+ 2 H+ + 2 e– = H 2 O 2 + 4 H+ + 4 e– = 2 H 2 O φ° = 0 В φ° = 1, 23 В – 1, 18 Mn 28
Диаграмма Латимера Mn. O 4 – 0, 56 Mn. O 4 2– 2, 22 Mn. O 2 0, 95 Mn 3+ 1, 51 Mn 2+ 2 H+ + 2 e– = H 2 O 2 + 4 H+ + 4 e– = 2 H 2 O φ° = 0 В φ° = 1, 23 В – 1, 18 Mn 28
 Зависимость φ° от среды n Оф + h. H+ + ne– = Вф + H 2 O n IO 3– + I– I 2 ? n φ°(I 2/I–) = 0, 54 В n 2 IO 3– + 12 H+ + 10 e– = I 2 + 6 H 2 O n φ°щел. (IO 3–/I 2) = 0, 196 В n φ°кисл. (IO 3–/I 2) = 0, 196 + 0, 828(12/10) = 1, 190 В Среда Δφ° = φ°(IO 3–/I 2) – φ°(I 2/I–) Направление реакции Кисл. 1, 190 – 0, 54 > 0 Щел. 0, 196 – 0, 54 > 0 29
Зависимость φ° от среды n Оф + h. H+ + ne– = Вф + H 2 O n IO 3– + I– I 2 ? n φ°(I 2/I–) = 0, 54 В n 2 IO 3– + 12 H+ + 10 e– = I 2 + 6 H 2 O n φ°щел. (IO 3–/I 2) = 0, 196 В n φ°кисл. (IO 3–/I 2) = 0, 196 + 0, 828(12/10) = 1, 190 В Среда Δφ° = φ°(IO 3–/I 2) – φ°(I 2/I–) Направление реакции Кисл. 1, 190 – 0, 54 > 0 Щел. 0, 196 – 0, 54 > 0 29
 Зависимость φ° от среды I 2 I- + IO 3 - I 2
Зависимость φ° от среды I 2 I- + IO 3 - I 2
 Стехиометрические расчеты по уравнению реакции n n n, моль M, г/моль VM, л/моль с, моль/л (М) n n = m/M n = V/VM n=c. V Для реакции a. A + b. B +. . . = d. D + e. E +. . . n(A)/a = n(B)/b = n(D)/d = n(E)/e =. . . 31
Стехиометрические расчеты по уравнению реакции n n n, моль M, г/моль VM, л/моль с, моль/л (М) n n = m/M n = V/VM n=c. V Для реакции a. A + b. B +. . . = d. D + e. E +. . . n(A)/a = n(B)/b = n(D)/d = n(E)/e =. . . 31
 Стехиометрические расчеты по уравнению реакции 32
Стехиометрические расчеты по уравнению реакции 32
 Задача n Смешали 0, 2 л 0, 25 М водного раствора KMn. O 4 и 0, 2 л 0, 25 М водного раствора KI. Определить массу осадка. m(ос. ) = ? V(р. KMn. O 4) = 0, 2 л c(KMn. O 4) = 0, 25 моль/л V(р. KI) = 0, 2 л c(KI) = 0, 25 моль/л Решение 2 KMn. O 4 + 4 H 2 O + 6 KI= 2 Mn. O 2 + 8 KOH + 3 I 2 M(Mn. O 2) = 87 г/моль, M(I 2) = 254 г/моль 33
Задача n Смешали 0, 2 л 0, 25 М водного раствора KMn. O 4 и 0, 2 л 0, 25 М водного раствора KI. Определить массу осадка. m(ос. ) = ? V(р. KMn. O 4) = 0, 2 л c(KMn. O 4) = 0, 25 моль/л V(р. KI) = 0, 2 л c(KI) = 0, 25 моль/л Решение 2 KMn. O 4 + 4 H 2 O + 6 KI= 2 Mn. O 2 + 8 KOH + 3 I 2 M(Mn. O 2) = 87 г/моль, M(I 2) = 254 г/моль 33
 Задача n(KMn. O 4) = c(KMn. O 4)V(p. KMn. O 4) n(KMn. O 4) = 0, 25. 0, 2 = 0, 05 (моль) n(KI) = c(KI)V(p. KI) neq(KI) = 0, 25. 0, 2 = 0, 05 (моль) По уравнению реакции n(KMn. O 4)/2 = n(KI)/6 = n(Mn. O 2)/2 = n(I 2)/3 KMn. O 4 в избытке, расчет по KI n(Mn. O 2) = m(Mn. O 2) / M(Mn. O 2) m(Mn. O 2) = n(KI)M(Mn. O 2) / 3 m(I 2) = n (KI)M(I 2) / 2 34
Задача n(KMn. O 4) = c(KMn. O 4)V(p. KMn. O 4) n(KMn. O 4) = 0, 25. 0, 2 = 0, 05 (моль) n(KI) = c(KI)V(p. KI) neq(KI) = 0, 25. 0, 2 = 0, 05 (моль) По уравнению реакции n(KMn. O 4)/2 = n(KI)/6 = n(Mn. O 2)/2 = n(I 2)/3 KMn. O 4 в избытке, расчет по KI n(Mn. O 2) = m(Mn. O 2) / M(Mn. O 2) m(Mn. O 2) = n(KI)M(Mn. O 2) / 3 m(I 2) = n (KI)M(I 2) / 2 34
 Стехиометрические расчеты по закону эквивалентов n Эквивалент – условная (реально не существующая) частица, в z раз меньшая, чем формульная единица n z – эквивалентное число (≥ 1) n Для ОВР (в уравнении полуреакции) n K 2 Cr 2 O 7 + 4 H 2 SO 4 + 6 HCl = 3 Cl 2 + Cr 2(SO 4)3 + 7 H 2 O + K 2 SO 4 n n Cr 2 O 72– + 14 H+ + 6 e– = 2 Cr 3+ + 7 H 2 O 2 Cl– – 2 e– = Cl 2 n z(Cr 2 O 72–) = 6, z(Cr 3+) = 3, z(Cl–) = 1, z(Cl 2) = 2
Стехиометрические расчеты по закону эквивалентов n Эквивалент – условная (реально не существующая) частица, в z раз меньшая, чем формульная единица n z – эквивалентное число (≥ 1) n Для ОВР (в уравнении полуреакции) n K 2 Cr 2 O 7 + 4 H 2 SO 4 + 6 HCl = 3 Cl 2 + Cr 2(SO 4)3 + 7 H 2 O + K 2 SO 4 n n Cr 2 O 72– + 14 H+ + 6 e– = 2 Cr 3+ + 7 H 2 O 2 Cl– – 2 e– = Cl 2 n z(Cr 2 O 72–) = 6, z(Cr 3+) = 3, z(Cl–) = 1, z(Cl 2) = 2
 Основные соотношения n Формульная единица n n, моль n M, г/моль n VM, л/моль n с, моль/л (М) n Эквивалент n neq = z n, моль n Meq = M / z, г/моль n Veq = VM /z, л/моль n ceq = z c, моль/л (н. , N) Закон эквивалентов Для реакции a. A + b. B +. . . = d. D + e. E +. . . neq(A) = neq(B) = neq(D) = neq(E) =. . .
Основные соотношения n Формульная единица n n, моль n M, г/моль n VM, л/моль n с, моль/л (М) n Эквивалент n neq = z n, моль n Meq = M / z, г/моль n Veq = VM /z, л/моль n ceq = z c, моль/л (н. , N) Закон эквивалентов Для реакции a. A + b. B +. . . = d. D + e. E +. . . neq(A) = neq(B) = neq(D) = neq(E) =. . .
 Задача (решение по закону эквивалентов) n Смешали 0, 2 л 0, 25 М водного раствора KMn. O 4 и 0, 2 л 0, 25 М водного раствора KI. Определить массу осадка. m(ос. ) = ? V(р. KMn. O 4) = 0, 2 л c(KMn. O 4) = 0, 25 моль/л V(р. KI) = 0, 2 л c(KI) = 0, 25 моль/л Решение Mn. O 4– + 2 H 2 O + 3 e– = Mn. O 2 + 4 OH– 2 I– – 2 e– = I 2 M(Mn. O 2) = 87 г/моль, M(I 2) = 254 г/моль z(KMn. O 4) = 3, z(KI) = 1, z(Mn. O 2) = 3, z(I 2) = 2
Задача (решение по закону эквивалентов) n Смешали 0, 2 л 0, 25 М водного раствора KMn. O 4 и 0, 2 л 0, 25 М водного раствора KI. Определить массу осадка. m(ос. ) = ? V(р. KMn. O 4) = 0, 2 л c(KMn. O 4) = 0, 25 моль/л V(р. KI) = 0, 2 л c(KI) = 0, 25 моль/л Решение Mn. O 4– + 2 H 2 O + 3 e– = Mn. O 2 + 4 OH– 2 I– – 2 e– = I 2 M(Mn. O 2) = 87 г/моль, M(I 2) = 254 г/моль z(KMn. O 4) = 3, z(KI) = 1, z(Mn. O 2) = 3, z(I 2) = 2
 Задача (решение по закону эквивалентов) neq(KMn. O 4) = z(KMn. O 4)c(KMn. O 4)V(p. KMn. O 4) neq(KMn. O 4) = 3. 0, 25. 0, 2 = 0, 15 (моль) neq(KI) = z(KI)c(KI)V(p. KI) neq(KI) = 1. 0, 25. 0, 2 = 0, 05 (моль) KMn. O 4 в избытке, расчет по KI neq(Mn. O 2) = z(Mn. O 2)m(Mn. O 2) / M(Mn. O 2) = neq(KI) m(Mn. O 2) = neq(Mn. O 2)M(Mn. O 2) / z(Mn. O 2) = neq(KI)M(Mn. O 2) / z(Mn. O 2) m(I 2) = neq(KI)M(I 2) / z(I 2)
Задача (решение по закону эквивалентов) neq(KMn. O 4) = z(KMn. O 4)c(KMn. O 4)V(p. KMn. O 4) neq(KMn. O 4) = 3. 0, 25. 0, 2 = 0, 15 (моль) neq(KI) = z(KI)c(KI)V(p. KI) neq(KI) = 1. 0, 25. 0, 2 = 0, 05 (моль) KMn. O 4 в избытке, расчет по KI neq(Mn. O 2) = z(Mn. O 2)m(Mn. O 2) / M(Mn. O 2) = neq(KI) m(Mn. O 2) = neq(Mn. O 2)M(Mn. O 2) / z(Mn. O 2) = neq(KI)M(Mn. O 2) / z(Mn. O 2) m(I 2) = neq(KI)M(I 2) / z(I 2)


