Лекция 6 Поли- и гетеро.ppt
- Количество слайдов: 50
 Классификация, номенклатура органических соединений. Поли- и гетерофункциональные соединения. Кафедра медицинской и биологической химии ХМГМА Лекция 6
Классификация, номенклатура органических соединений. Поли- и гетерофункциональные соединения. Кафедра медицинской и биологической химии ХМГМА Лекция 6
 План лекции n n n Классификация органических соединений. Полифункциональные соединения. Гетерофункциональные соединения. Особенности химического поведения полии гетерофункциональных соединений: кислотно-основные свойства (амфолиты), циклизация и хелатообразование. Взаимное влияние функциональных групп. Влияние различных факторов на процесс образования циклов (стерический, энтропийный). Лактоны. Лактамы. Кетоенольная таутомерия. Полии гетерофункциональность как один из характерных признаков органических соединений, участвующих в процессах жизнедеятельности и используемых в качестве лекарственных веществ.
План лекции n n n Классификация органических соединений. Полифункциональные соединения. Гетерофункциональные соединения. Особенности химического поведения полии гетерофункциональных соединений: кислотно-основные свойства (амфолиты), циклизация и хелатообразование. Взаимное влияние функциональных групп. Влияние различных факторов на процесс образования циклов (стерический, энтропийный). Лактоны. Лактамы. Кетоенольная таутомерия. Полии гетерофункциональность как один из характерных признаков органических соединений, участвующих в процессах жизнедеятельности и используемых в качестве лекарственных веществ.
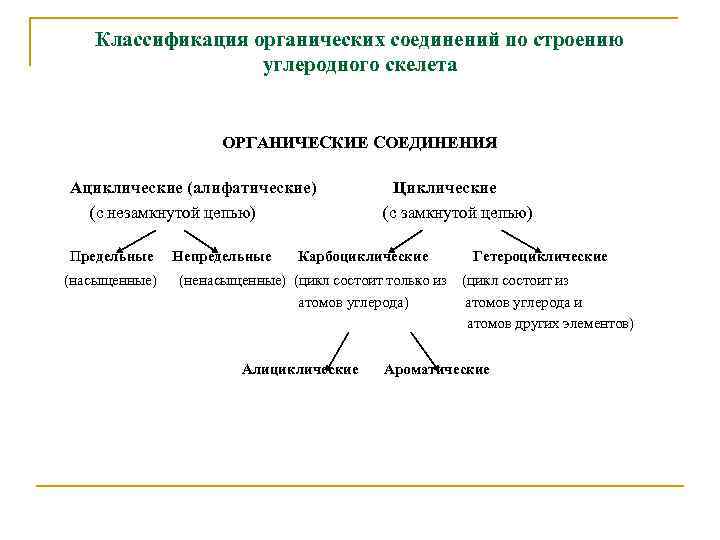 Классификация органических соединений по строению углеродного скелета ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ Ациклические (алифатические) (с незамкнутой цепью) Предельные (насыщенные) Непредельные Циклические (с замкнутой цепью) Карбоциклические (ненасыщенные) (цикл состоит только из атомов углерода) Алициклические Гетероциклические (цикл состоит из атомов углерода и атомов других элементов) Ароматические
Классификация органических соединений по строению углеродного скелета ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ Ациклические (алифатические) (с незамкнутой цепью) Предельные (насыщенные) Непредельные Циклические (с замкнутой цепью) Карбоциклические (ненасыщенные) (цикл состоит только из атомов углерода) Алициклические Гетероциклические (цикл состоит из атомов углерода и атомов других элементов) Ароматические
 Основные классы органических соединений
Основные классы органических соединений
 Основные понятия Вещество, вступающее в химическую реакцию и предоставляющее реакционные центры – называют субстратом. Реакционный центр - определенный фрагмент молекулы, непосредственно участвующий в той или иной реакции. В определенных реакциях могут участвовать определенные реакционные центры. Реагент – соединение, действующее на субстрат, и образующее активную частицу. Из реагента могут образоваться следующие активные частицы: Радикалы (R) – частицы с одним не спаренным электроном, образующиеся при гомолитическом разрыве ковалентной связи. При этом каждый атом остается с одним не спаренным электроном. Радикалы неустойчивы. При гетеролитическом разрыве ковалентной связи образуются: Нуклеофилы (Nu) – частицы, имеющие электронную пару на внешнем энергетическом уровне и несущие отрицательный заряд. Электрофилы (Е) – частицы, имеющие свободную орбиталь и несущие положительный заряд.
Основные понятия Вещество, вступающее в химическую реакцию и предоставляющее реакционные центры – называют субстратом. Реакционный центр - определенный фрагмент молекулы, непосредственно участвующий в той или иной реакции. В определенных реакциях могут участвовать определенные реакционные центры. Реагент – соединение, действующее на субстрат, и образующее активную частицу. Из реагента могут образоваться следующие активные частицы: Радикалы (R) – частицы с одним не спаренным электроном, образующиеся при гомолитическом разрыве ковалентной связи. При этом каждый атом остается с одним не спаренным электроном. Радикалы неустойчивы. При гетеролитическом разрыве ковалентной связи образуются: Нуклеофилы (Nu) – частицы, имеющие электронную пару на внешнем энергетическом уровне и несущие отрицательный заряд. Электрофилы (Е) – частицы, имеющие свободную орбиталь и несущие положительный заряд.
 Классификация органических реакций n n По молекулярности – количеству молекул, участвующих в реакции. Различают моно-, ди-, тримолекулярные реакции. По типу химической реакции: кислотно-основные – КОР, окислительно-восстановительные – ОВР, лигандообменные (комплексообразование), осаждения… По признаку изменения числа и состава исходных веществ и продуктов реакции: присоединения, замещения, отщепления. По механизму: радикальное замещение – SR, электрофильное замещение – SE, электрофильное присоединение – АЕ, нуклеофильное замещение – SN, нуклеофильное присоединение – AN, элиминирование – Е, ионные реакции, перегруппировки.
Классификация органических реакций n n По молекулярности – количеству молекул, участвующих в реакции. Различают моно-, ди-, тримолекулярные реакции. По типу химической реакции: кислотно-основные – КОР, окислительно-восстановительные – ОВР, лигандообменные (комплексообразование), осаждения… По признаку изменения числа и состава исходных веществ и продуктов реакции: присоединения, замещения, отщепления. По механизму: радикальное замещение – SR, электрофильное замещение – SE, электрофильное присоединение – АЕ, нуклеофильное замещение – SN, нуклеофильное присоединение – AN, элиминирование – Е, ионные реакции, перегруппировки.
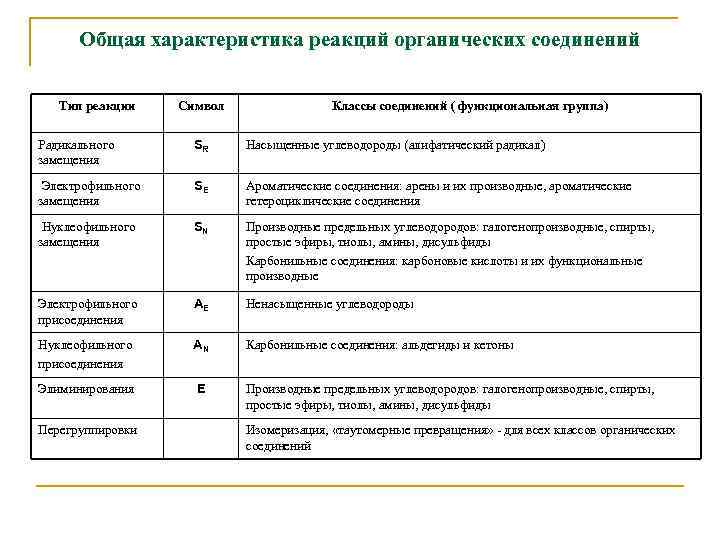 Общая характеристика реакций органических соединений Тип реакции Символ Классы соединений ( функциональная группа) Радикального замещения SR Насыщенные углеводороды (алифатический радикал) Электрофильного замещения SE Ароматические соединения: арены и их производные, ароматические гетероциклические соединения Нуклеофильного замещения SN Производные предельных углеводородов: галогенопроизводные, спирты, простые эфиры, тиолы, амины, дисульфиды Карбонильные соединения: карбоновые кислоты и их функциональные производные Электрофильного присоединения AE Ненасыщенные углеводороды Нуклеофильного присоединения AN Карбонильные соединения: альдегиды и кетоны Элиминирования E Производные предельных углеводородов: галогенопроизводные, спирты, простые эфиры, тиолы, амины, дисульфиды Перегруппировки Изомеризация, «таутомерные превращения» - для всех классов органических соединений
Общая характеристика реакций органических соединений Тип реакции Символ Классы соединений ( функциональная группа) Радикального замещения SR Насыщенные углеводороды (алифатический радикал) Электрофильного замещения SE Ароматические соединения: арены и их производные, ароматические гетероциклические соединения Нуклеофильного замещения SN Производные предельных углеводородов: галогенопроизводные, спирты, простые эфиры, тиолы, амины, дисульфиды Карбонильные соединения: карбоновые кислоты и их функциональные производные Электрофильного присоединения AE Ненасыщенные углеводороды Нуклеофильного присоединения AN Карбонильные соединения: альдегиды и кетоны Элиминирования E Производные предельных углеводородов: галогенопроизводные, спирты, простые эфиры, тиолы, амины, дисульфиды Перегруппировки Изомеризация, «таутомерные превращения» - для всех классов органических соединений
 Полифункциональными называют соединения, в молекулах которых присутствуют две и более одинаковые функциональные группы. Гетерофункциональными называют соединения, в молекулах которых имеются различные функциональные группы.
Полифункциональными называют соединения, в молекулах которых присутствуют две и более одинаковые функциональные группы. Гетерофункциональными называют соединения, в молекулах которых имеются различные функциональные группы.
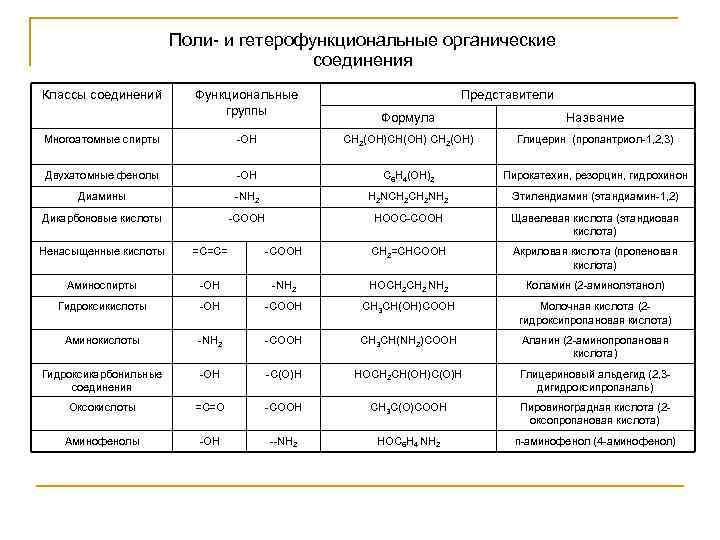 Поли- и гетерофункциональные органические соединения Классы соединений Функциональные группы Представители Формула Название Многоатомные спирты -ОН СН 2(ОН)СН(ОН) СН 2(ОН) Глицерин (пропантриол-1, 2, 3) Двухатомные фенолы -ОН С 6 Н 4(ОН)2 Пирокатехин, резорцин, гидрохинон Диамины -NH 2 H 2 NCH 2 NH 2 Этилендиамин (этандиамин-1, 2) Дикарбоновые кислоты -СООН НООС-СООН Щавелевая кислота (этандиовая кислота) Ненасыщенные кислоты =С=С= -СООН СН 2=СНСООН Акриловая кислота (пропеновая кислота) Аминоспирты -ОН -NH 2 НОСН 2 NH 2 Коламин (2 -аминолэтанол) Гидроксикислоты -ОН -СООН СН 3 СН(ОН)СООН Молочная кислота (2 гидроксипропановая кислота) Аминокислоты -NH 2 -СООН СН 3 СН(NH 2)СООН Аланин (2 -аминопропановая кислота) Гидроксикарбонильные соединения -ОН -С(О)Н НОСН 2 СН(ОН)С(О)Н Глицериновый альдегид (2, 3 дигидроксипропаналь) Оксокислоты =С=О -СООН СН 3 С(О)СООН Пировиноградная кислота (2 оксопропановая кислота) Аминофенолы -ОН --NH 2 НОС 6 Н 4 NH 2 n-аминофенол (4 -аминофенол)
Поли- и гетерофункциональные органические соединения Классы соединений Функциональные группы Представители Формула Название Многоатомные спирты -ОН СН 2(ОН)СН(ОН) СН 2(ОН) Глицерин (пропантриол-1, 2, 3) Двухатомные фенолы -ОН С 6 Н 4(ОН)2 Пирокатехин, резорцин, гидрохинон Диамины -NH 2 H 2 NCH 2 NH 2 Этилендиамин (этандиамин-1, 2) Дикарбоновые кислоты -СООН НООС-СООН Щавелевая кислота (этандиовая кислота) Ненасыщенные кислоты =С=С= -СООН СН 2=СНСООН Акриловая кислота (пропеновая кислота) Аминоспирты -ОН -NH 2 НОСН 2 NH 2 Коламин (2 -аминолэтанол) Гидроксикислоты -ОН -СООН СН 3 СН(ОН)СООН Молочная кислота (2 гидроксипропановая кислота) Аминокислоты -NH 2 -СООН СН 3 СН(NH 2)СООН Аланин (2 -аминопропановая кислота) Гидроксикарбонильные соединения -ОН -С(О)Н НОСН 2 СН(ОН)С(О)Н Глицериновый альдегид (2, 3 дигидроксипропаналь) Оксокислоты =С=О -СООН СН 3 С(О)СООН Пировиноградная кислота (2 оксопропановая кислота) Аминофенолы -ОН --NH 2 НОС 6 Н 4 NH 2 n-аминофенол (4 -аминофенол)
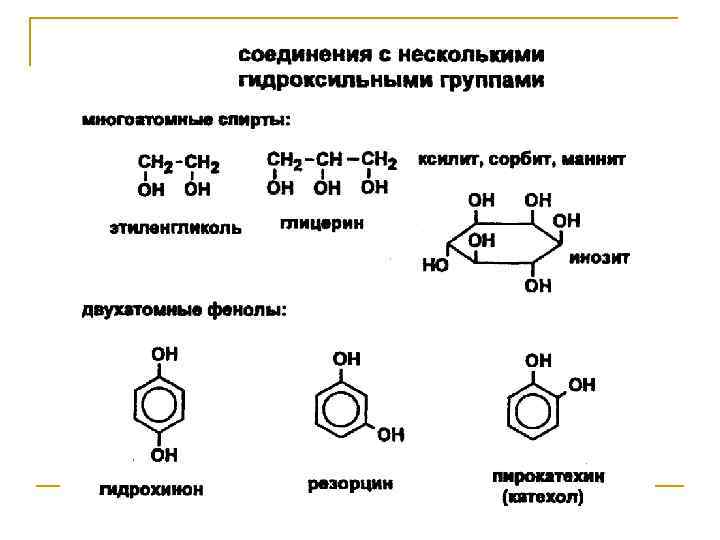

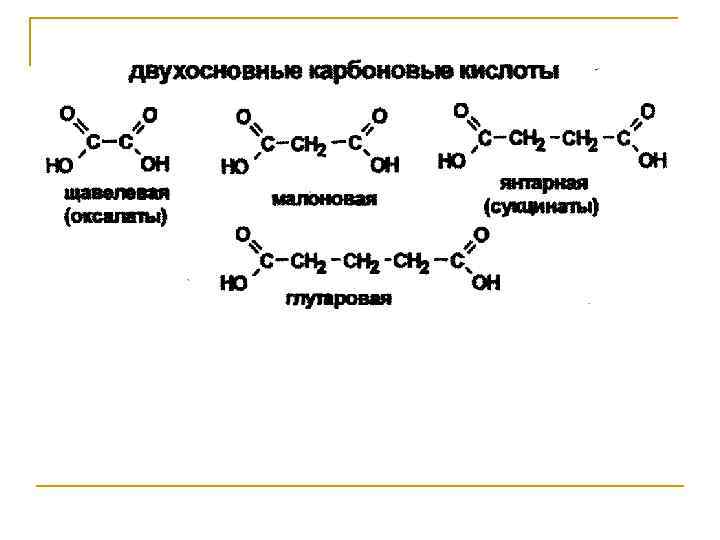
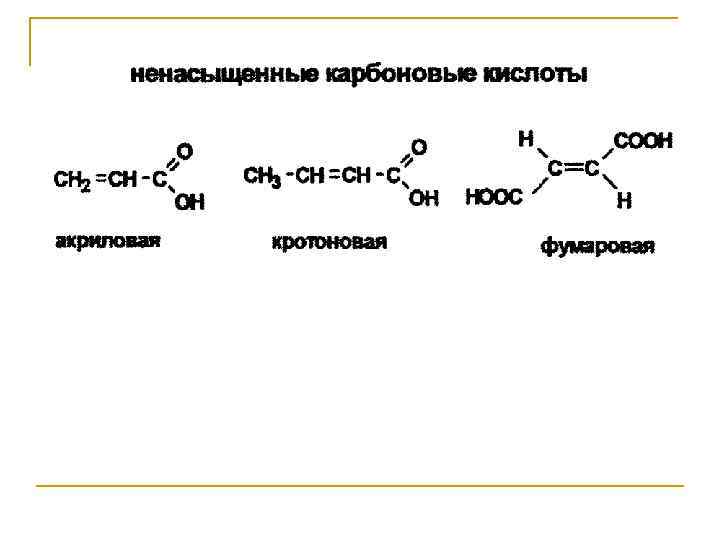
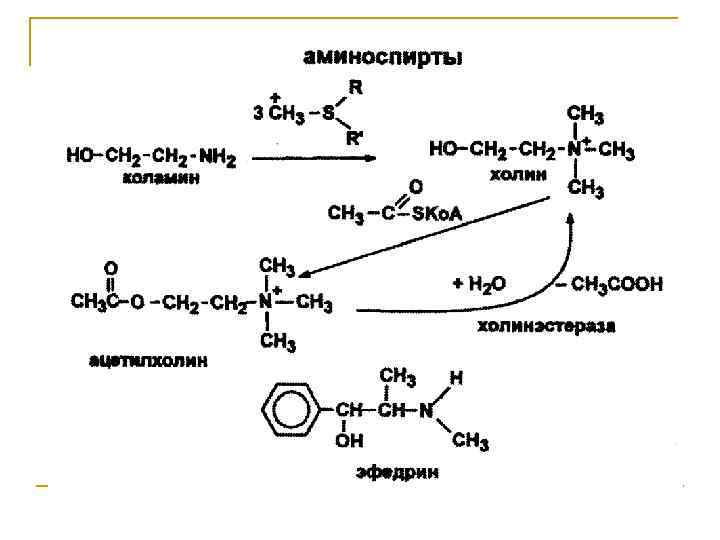
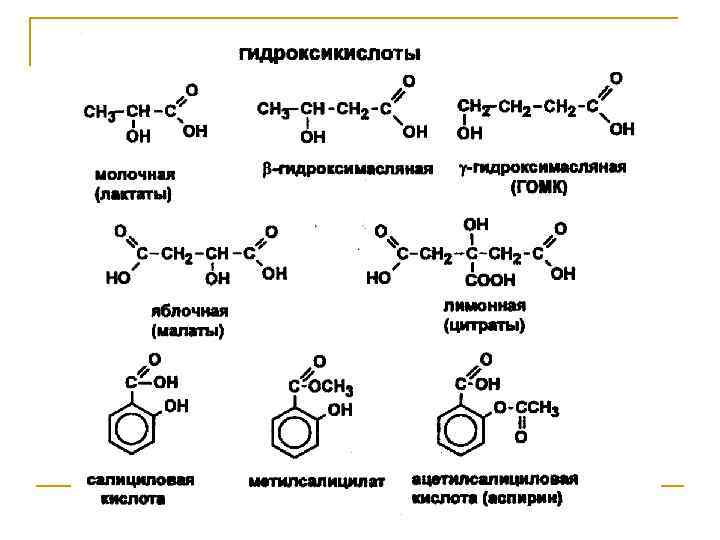
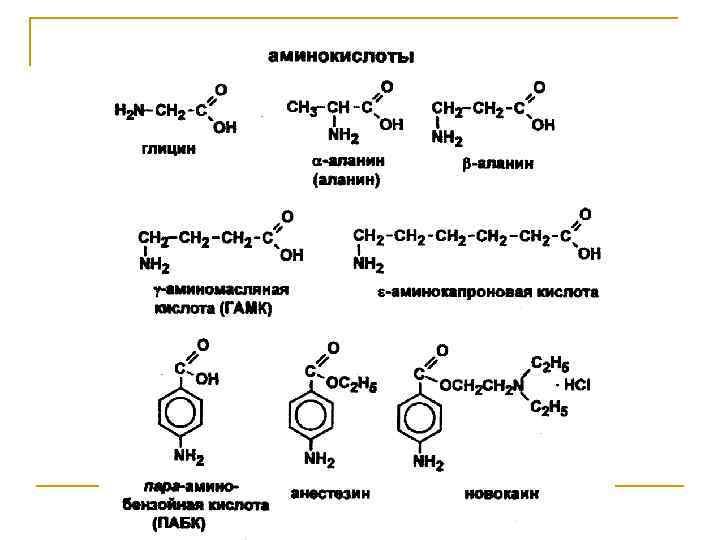
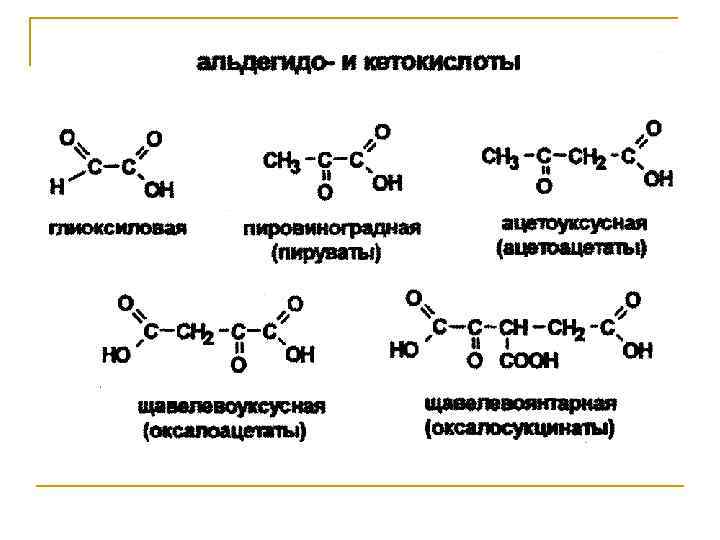
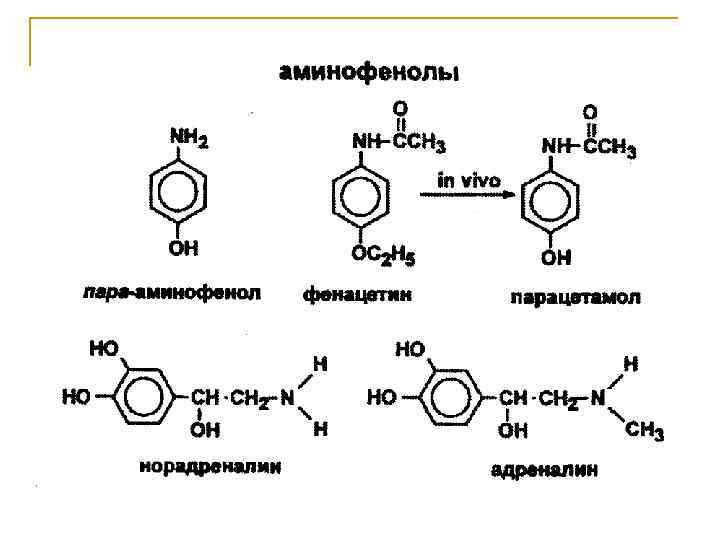
 Особенности химических свойств поли- и гетерофункциональных соединений Большее разнообразие химических превращений, связанное с наличием нескольких функциональных групп; Усиление или ослабление реакционной способности, определяемое взаимным влиянием функциональных групп; Специфические свойства, не характерные для монофункциональных соединений.
Особенности химических свойств поли- и гетерофункциональных соединений Большее разнообразие химических превращений, связанное с наличием нескольких функциональных групп; Усиление или ослабление реакционной способности, определяемое взаимным влиянием функциональных групп; Специфические свойства, не характерные для монофункциональных соединений.
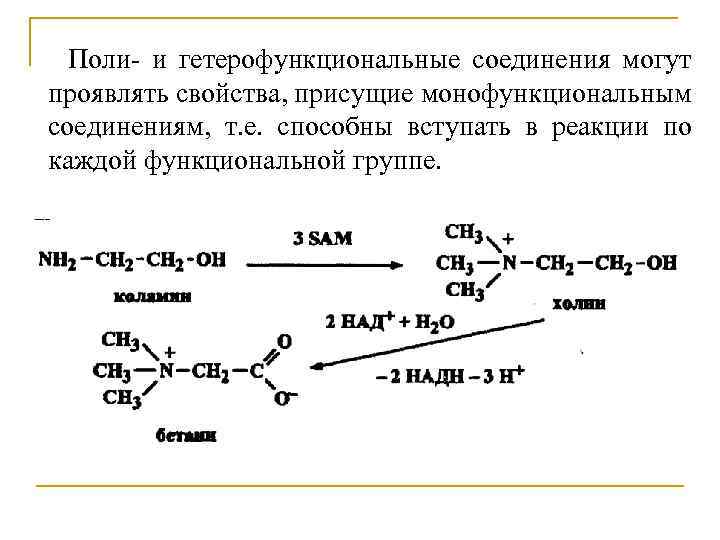 Поли- и гетерофункциональные соединения могут проявлять свойства, присущие монофункциональным соединениям, т. е. способны вступать в реакции по каждой функциональной группе.
Поли- и гетерофункциональные соединения могут проявлять свойства, присущие монофункциональным соединениям, т. е. способны вступать в реакции по каждой функциональной группе.
 Одновременное наличие нескольких функциональных групп в молекуле ведет к появлению определенных различий в свойствах моно-, полии гетерофункциональных соединений. В поли- и гетерофункциональных соединениях может наблюдаться усиление или, наоборот, ослабление некоторых свойств, характерных для монофункциональных соединений; могут появляться специфические химические свойства, которые наиболее важны для обеспечения биологических функций, выполняемых этими веществами.
Одновременное наличие нескольких функциональных групп в молекуле ведет к появлению определенных различий в свойствах моно-, полии гетерофункциональных соединений. В поли- и гетерофункциональных соединениях может наблюдаться усиление или, наоборот, ослабление некоторых свойств, характерных для монофункциональных соединений; могут появляться специфические химические свойства, которые наиболее важны для обеспечения биологических функций, выполняемых этими веществами.
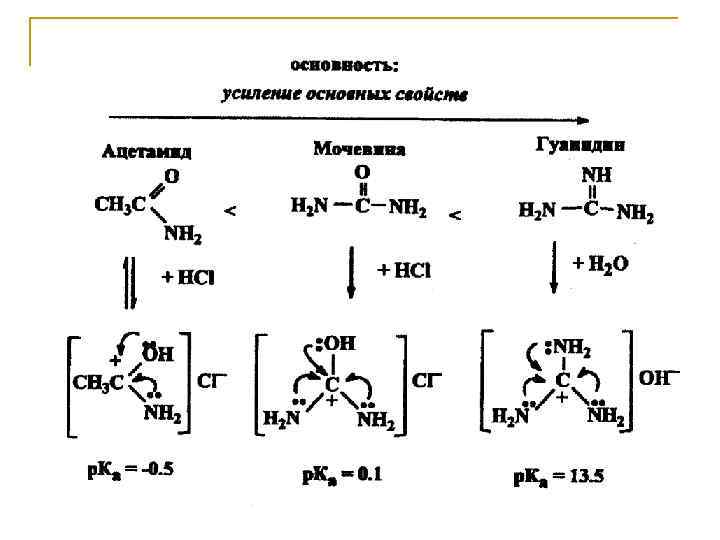
 Кислотность. Наличие дополнительного электроноакцепторного заместителя, например, в алифатических спиртах и кислотах, повышает их кислотность. Основность. С накоплением аминогрупп в молекуле, как правило, основность повышается. Так, ацетамид проявляет нейтральный характер и не реагирует с разбавленными минеральными кислотами, мочевина образует с ними достаточно устойчивые соли, а гуанидин в водном растворе ионизирован практически полностью.
Кислотность. Наличие дополнительного электроноакцепторного заместителя, например, в алифатических спиртах и кислотах, повышает их кислотность. Основность. С накоплением аминогрупп в молекуле, как правило, основность повышается. Так, ацетамид проявляет нейтральный характер и не реагирует с разбавленными минеральными кислотами, мочевина образует с ними достаточно устойчивые соли, а гуанидин в водном растворе ионизирован практически полностью.
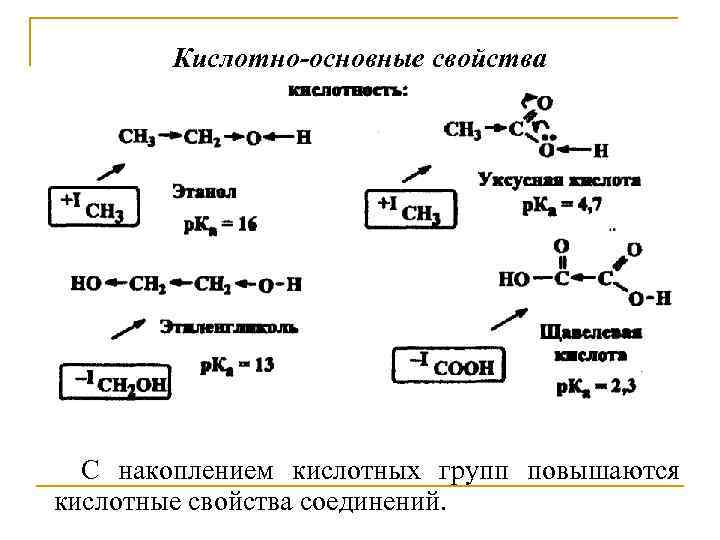 Кислотно-основные свойства С накоплением кислотных групп повышаются кислотные свойства соединений.
Кислотно-основные свойства С накоплением кислотных групп повышаются кислотные свойства соединений.
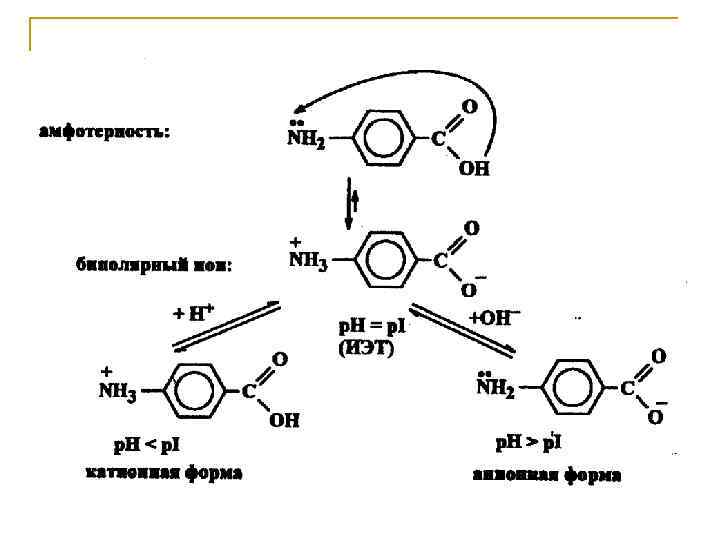
 Амфотерность. Гетерофункциональные соединения, содержащие одновременно кислотные и основные функциональные группы, например аминокислоты, проявляют амфотерные свойства – способность взаимодействовать как с кислотами, так и с основаниями. В нейтральных водных растворах или кристаллическом состоянии аминокислоты существуют преимущественно в форме внутренних солей (диполярных ионов), что повышает их растворимость в воде; в кислых растворах – в катионной форме, в щелочных – в анионной форме.
Амфотерность. Гетерофункциональные соединения, содержащие одновременно кислотные и основные функциональные группы, например аминокислоты, проявляют амфотерные свойства – способность взаимодействовать как с кислотами, так и с основаниями. В нейтральных водных растворах или кристаллическом состоянии аминокислоты существуют преимущественно в форме внутренних солей (диполярных ионов), что повышает их растворимость в воде; в кислых растворах – в катионной форме, в щелочных – в анионной форме.
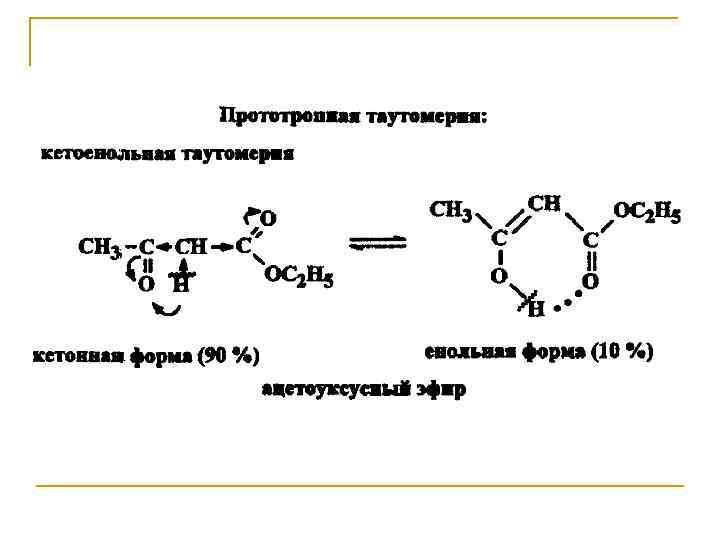
 Кето-енольная таутомерия. Протонная подвижность атома водорода у α-углерода в монокарбонильных соединениях (слабого СНкислотного центра) проявляется в их способности к реакциям конденсации. Карбонильное соединение в кетонной форме может существовать в равновесии с изомером – енольной формой. Такой вид изомерии называют таутомерией, а изомеры, находящиеся в состоянии подвижного равновесия, таутомерами.
Кето-енольная таутомерия. Протонная подвижность атома водорода у α-углерода в монокарбонильных соединениях (слабого СНкислотного центра) проявляется в их способности к реакциям конденсации. Карбонильное соединение в кетонной форме может существовать в равновесии с изомером – енольной формой. Такой вид изомерии называют таутомерией, а изомеры, находящиеся в состоянии подвижного равновесия, таутомерами.
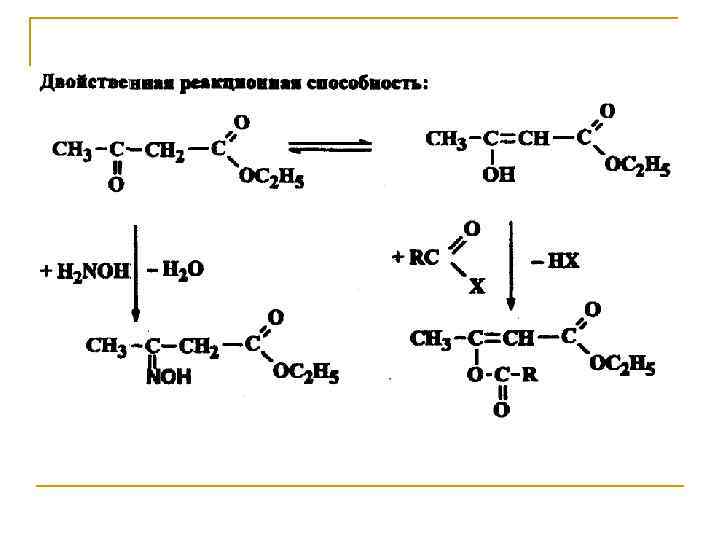
 В рассматриваемом случае между кетонной и енольной формами осуществляется перенос протона, поэтому такое равновенсие называется прототропной таутомерией, в частности, кетоенольной таутомерией. В монокарбонильных соединениях (альдегидах, кетонах, сложных эфирах) равновесие практически полностью смещено в сторону кетонной формы. При наличии второй электроноакцепторной группы у α-углерода (например, нитрогруппы –NO 2, карбонильной группы >С=О) содержание енольной формы резко возрастает.
В рассматриваемом случае между кетонной и енольной формами осуществляется перенос протона, поэтому такое равновенсие называется прототропной таутомерией, в частности, кетоенольной таутомерией. В монокарбонильных соединениях (альдегидах, кетонах, сложных эфирах) равновесие практически полностью смещено в сторону кетонной формы. При наличии второй электроноакцепторной группы у α-углерода (например, нитрогруппы –NO 2, карбонильной группы >С=О) содержание енольной формы резко возрастает.
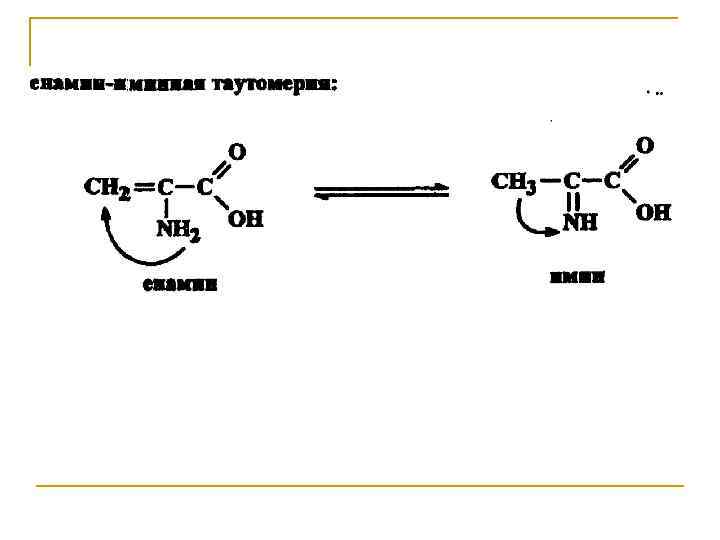
 Влияние гетерофункционального заместителя на реакционный центр Нуклеофильное замещение. Наличие дополнительной функциональной группы способствует поляризации связи углерод– гетероатом, увеличивая ее реакционную способность. Например, α-галогенокарбоновые кислоты обладают повышенной реакционной способностью в реакциях нуклеофильного замещения по сравнению с обычными алкилгалогенидами, из-за влияния электроноакцепторной карбоксильной группы – СООН, увеличивающей на α-углероде положительный заряд.
Влияние гетерофункционального заместителя на реакционный центр Нуклеофильное замещение. Наличие дополнительной функциональной группы способствует поляризации связи углерод– гетероатом, увеличивая ее реакционную способность. Например, α-галогенокарбоновые кислоты обладают повышенной реакционной способностью в реакциях нуклеофильного замещения по сравнению с обычными алкилгалогенидами, из-за влияния электроноакцепторной карбоксильной группы – СООН, увеличивающей на α-углероде положительный заряд.
 Алкилирование. Соединения с β-хлорэтилтио (Cl. CH 2 S–) и β-хлорэтиламиногруппой (Cl. CH 2 N<) в реакциях нуклеофильного замещения претерпевают «внутреннее» нуклеофильное замещение, образуя трехчленные циклы, которые далее расщепляются под действием внешних нуклеофилов. Эта способность делает их сильными алкилирующими агентами с важными биологическими свойствами. Соединения типа иприта высокотоксичны оказывают кожно-нарывное действие. Cl. CH 2–S–CH 2 Cl и
Алкилирование. Соединения с β-хлорэтилтио (Cl. CH 2 S–) и β-хлорэтиламиногруппой (Cl. CH 2 N<) в реакциях нуклеофильного замещения претерпевают «внутреннее» нуклеофильное замещение, образуя трехчленные циклы, которые далее расщепляются под действием внешних нуклеофилов. Эта способность делает их сильными алкилирующими агентами с важными биологическими свойствами. Соединения типа иприта высокотоксичны оказывают кожно-нарывное действие. Cl. CH 2–S–CH 2 Cl и
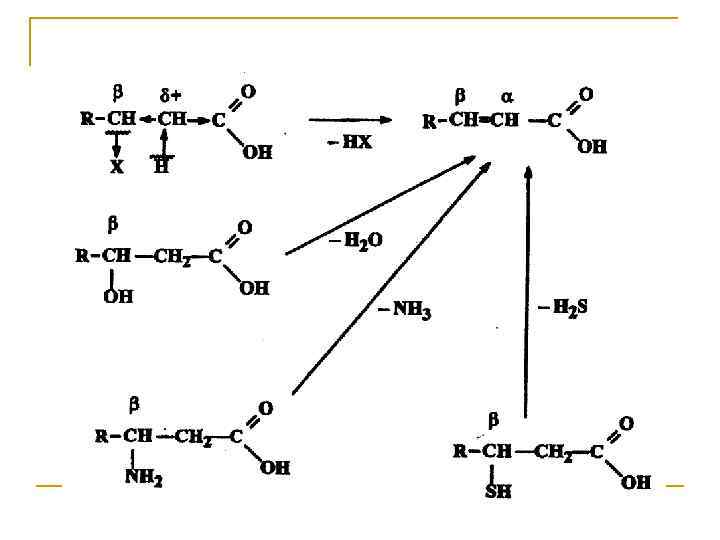
 Элиминирование. Реакции элиминирования в полифункциональных соединениях осуществляются в мягких условиях, что объясняется высокой протонной подвижностью αводорода, обусловленной электронным влиянием двух электроноакцепторных групп (X и СООН).
Элиминирование. Реакции элиминирования в полифункциональных соединениях осуществляются в мягких условиях, что объясняется высокой протонной подвижностью αводорода, обусловленной электронным влиянием двух электроноакцепторных групп (X и СООН).
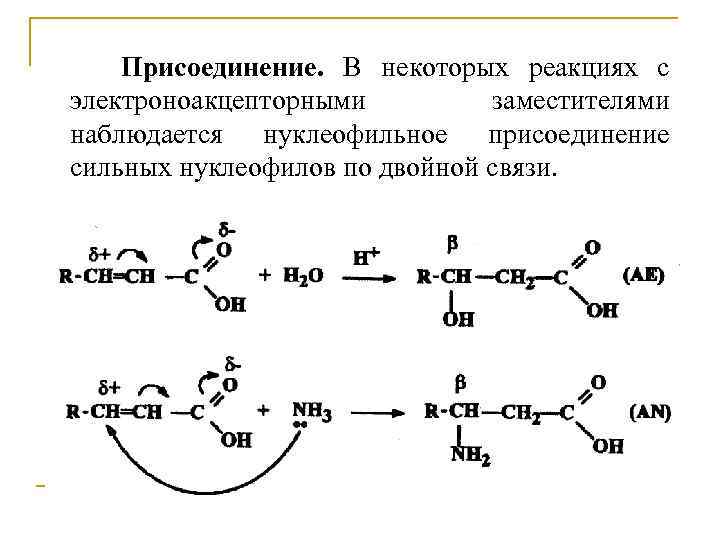 Присоединение. В некоторых реакциях с электроноакцепторными заместителями наблюдается нуклеофильное присоединение сильных нуклеофилов по двойной связи.
Присоединение. В некоторых реакциях с электроноакцепторными заместителями наблюдается нуклеофильное присоединение сильных нуклеофилов по двойной связи.
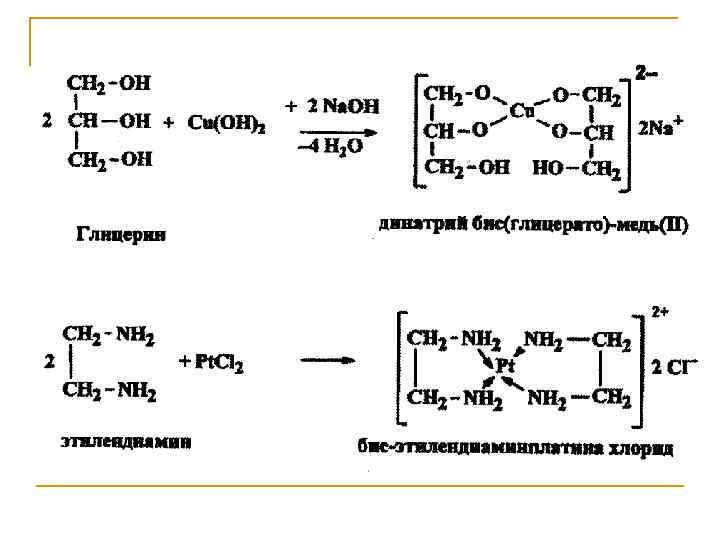
 Хелатообразование. Полии гетерофункциональные соединения, содержащие одновалентные функциональные группы, такие, как ОН- или NH 2 -группы, у соседних атомов углерода, при взаимодействии с гидроксидами тяжелых металлов образуют внутрикомплексные, так называемые хелатные, соединения, которые хорошо растворимы в воде и интенсивно окрашены.
Хелатообразование. Полии гетерофункциональные соединения, содержащие одновалентные функциональные группы, такие, как ОН- или NH 2 -группы, у соседних атомов углерода, при взаимодействии с гидроксидами тяжелых металлов образуют внутрикомплексные, так называемые хелатные, соединения, которые хорошо растворимы в воде и интенсивно окрашены.
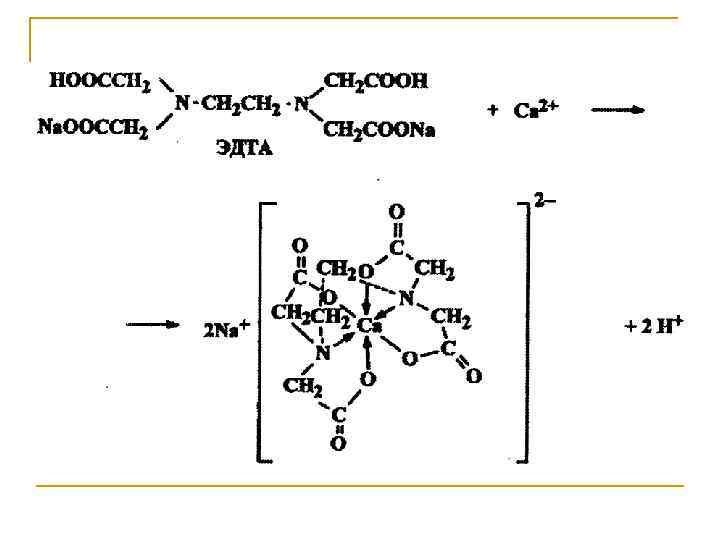
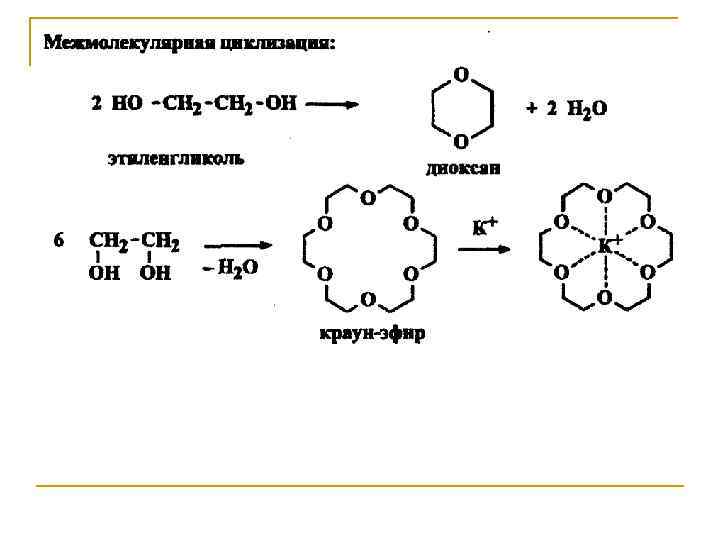
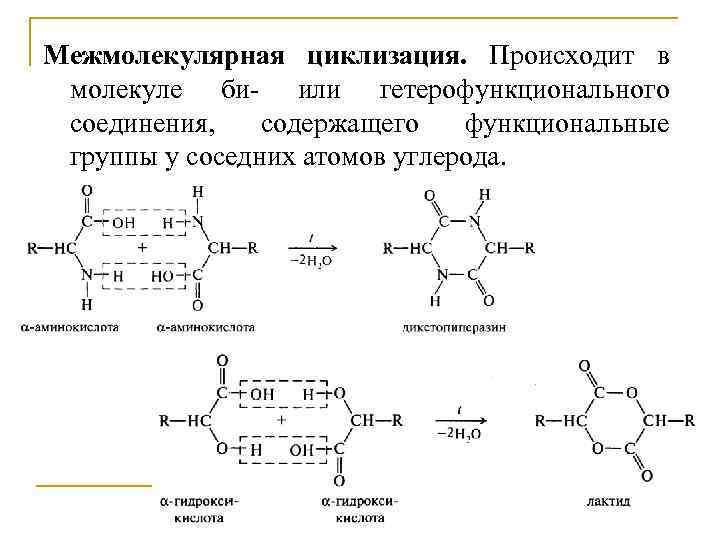 Межмолекулярная циклизация. Происходит в молекуле би- или гетерофункционального соединения, содержащего функциональные группы у соседних атомов углерода.
Межмолекулярная циклизация. Происходит в молекуле би- или гетерофункционального соединения, содержащего функциональные группы у соседних атомов углерода.
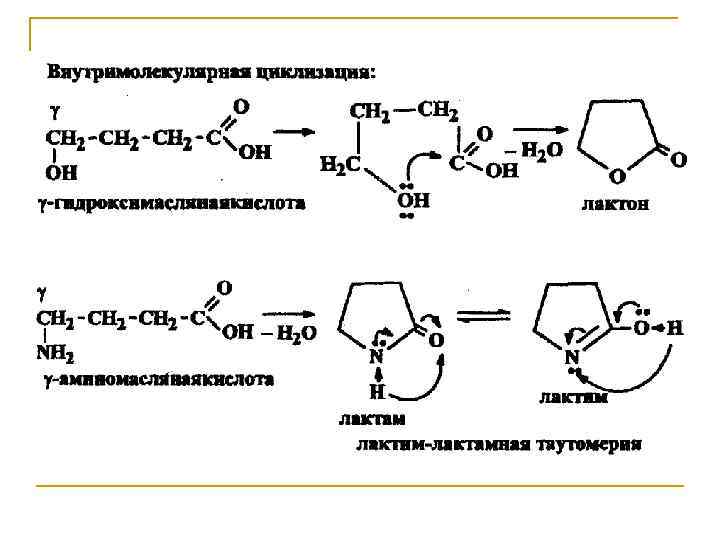
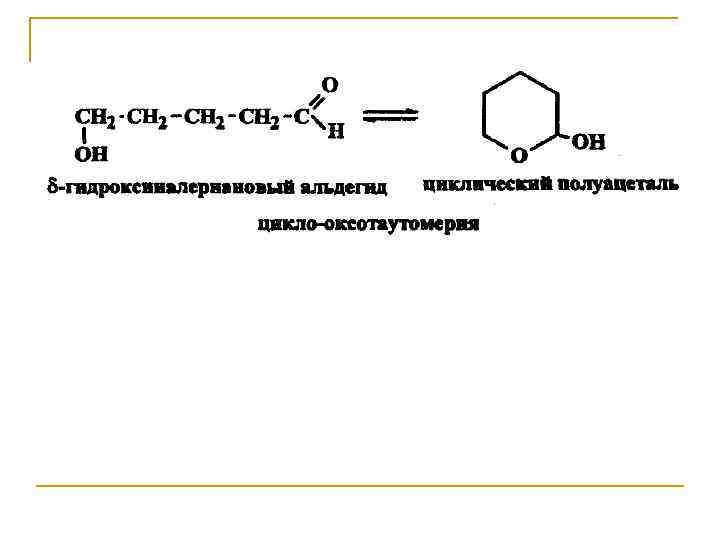
 Внутримолекулярная циклизация. Молекулы многих поли- или гетерофункциональных соединений могут принимать в пространстве клешневидные конформации, в которых различные функциональные группы оказываются сближенными. Вследствие этого между ними может осуществляться взаимодействие с образованием циклических продуктов. Особенно легко внутримолекулярная циклизация протекает в тех случаях, когда она приводит к образованию термодинамически устойчивых пяти-, шестичленных циклов.
Внутримолекулярная циклизация. Молекулы многих поли- или гетерофункциональных соединений могут принимать в пространстве клешневидные конформации, в которых различные функциональные группы оказываются сближенными. Вследствие этого между ними может осуществляться взаимодействие с образованием циклических продуктов. Особенно легко внутримолекулярная циклизация протекает в тех случаях, когда она приводит к образованию термодинамически устойчивых пяти-, шестичленных циклов.
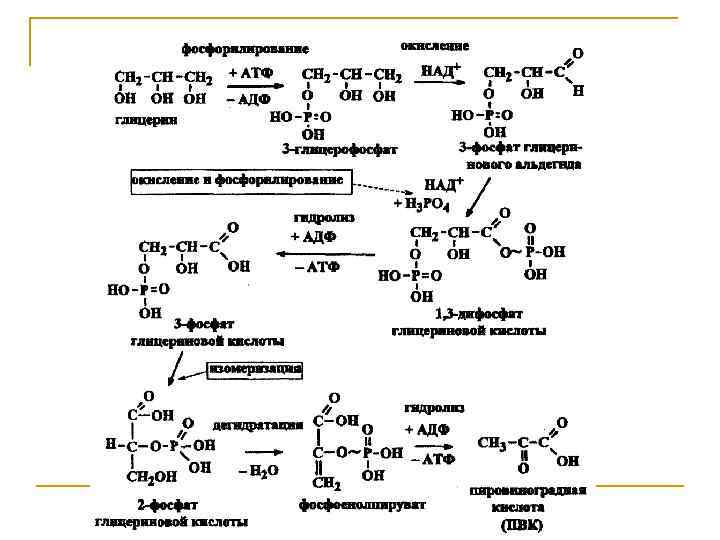
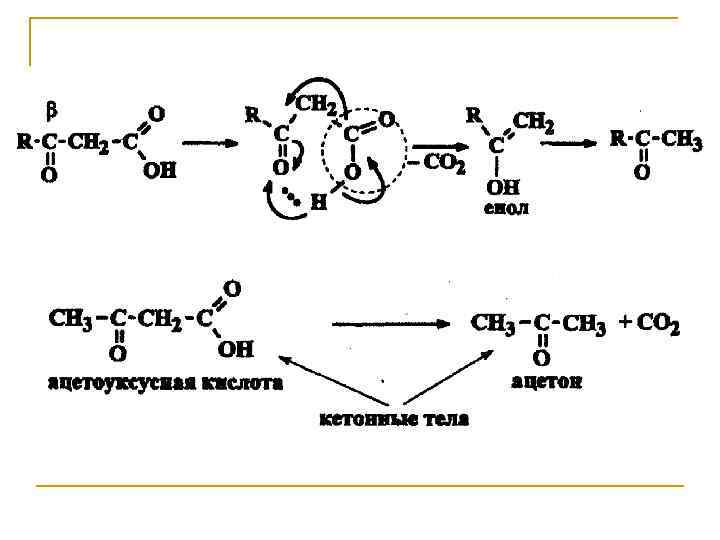
 Декарбоксилирование. Это одна из наиболее важных реакций карбоновых кислот. Незамещенные монокарбоновые кислоты декарбоксилируются чрезвычайно трудно. Реакция протекает легче при наличии у α-углерода электроноакцепторной группы, поляризующей связь С-СООН этого атома с карбоксильной группой. Большое значение имеет ферментативное декарбоксилирование α- и β-оксокислот, а также αаминокислот в организме.
Декарбоксилирование. Это одна из наиболее важных реакций карбоновых кислот. Незамещенные монокарбоновые кислоты декарбоксилируются чрезвычайно трудно. Реакция протекает легче при наличии у α-углерода электроноакцепторной группы, поляризующей связь С-СООН этого атома с карбоксильной группой. Большое значение имеет ферментативное декарбоксилирование α- и β-оксокислот, а также αаминокислот в организме.
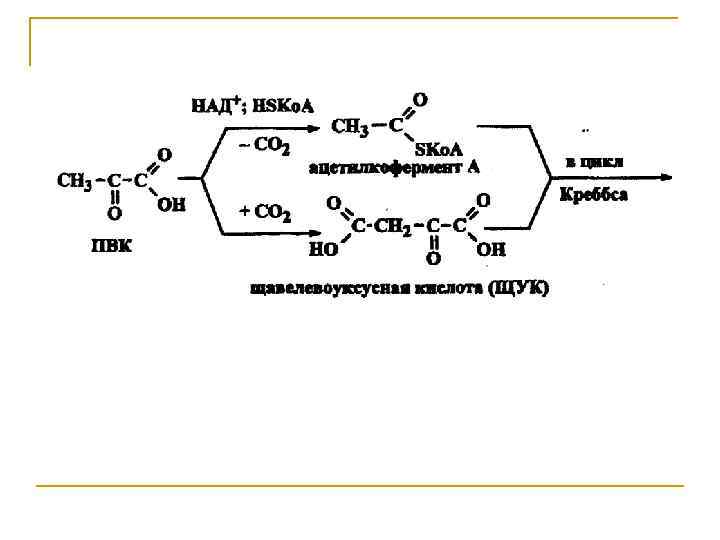
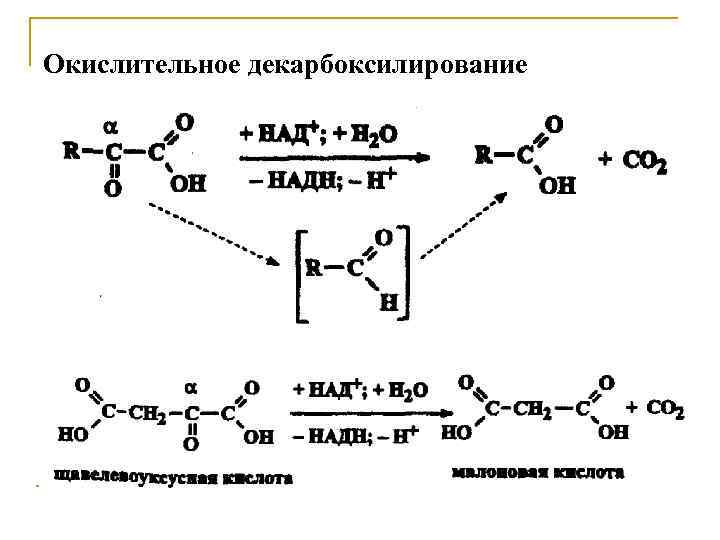 Окислительное декарбоксилирование
Окислительное декарбоксилирование