оксиды 11 класс.ppt
- Количество слайдов: 16
 Классификация неорганических веществ. Оксиды. 11 класс
Классификация неорганических веществ. Оксиды. 11 класс
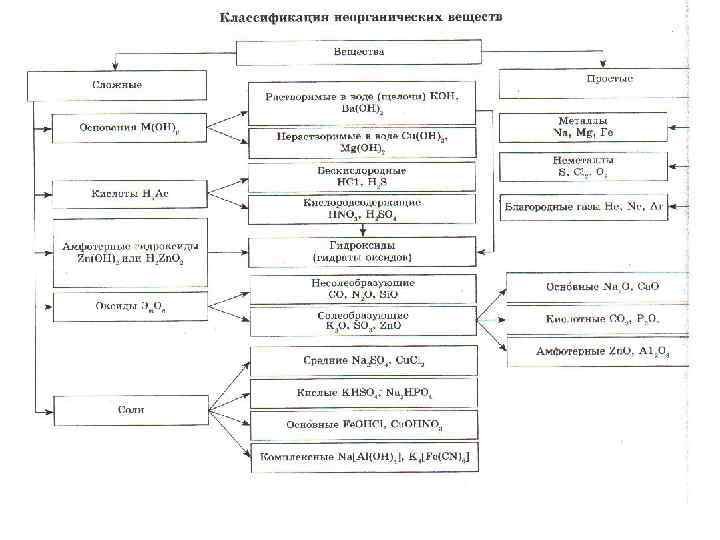
 ОКСИДЫ • Оксиды- бинарные соединения с кислородом в степени окисления (-2). • Общая формула оксидов: Эm. On где m число атомов элемента Э, а n – число атомов кислорода.
ОКСИДЫ • Оксиды- бинарные соединения с кислородом в степени окисления (-2). • Общая формула оксидов: Эm. On где m число атомов элемента Э, а n – число атомов кислорода.
 Классификация оксидов
Классификация оксидов
 Несолеобразующие оксиды • Несолеебразующими называются такие оксиды, которые не взаимодействуют ни со щелочами, ни с кислотами и не образуют солей. Их немного, в их состав входят неметаллы.
Несолеобразующие оксиды • Несолеебразующими называются такие оксиды, которые не взаимодействуют ни со щелочами, ни с кислотами и не образуют солей. Их немного, в их состав входят неметаллы.
 Солеобразующие • Солеобразующими называются такие оксиды, которые взаимодействуют с кислотами или основаниями и образуют при этом соль и воду. • Среди солеобразующих оксидов различают оксиды: основные, кислотные, амфотерные.
Солеобразующие • Солеобразующими называются такие оксиды, которые взаимодействуют с кислотами или основаниями и образуют при этом соль и воду. • Среди солеобразующих оксидов различают оксиды: основные, кислотные, амфотерные.
 Основные оксиды • Основные оксиды - это такие оксиды, которым соответствуют основания. Например: Са. О - Са(ОН)2 Na 2 O - Na. OH
Основные оксиды • Основные оксиды - это такие оксиды, которым соответствуют основания. Например: Са. О - Са(ОН)2 Na 2 O - Na. OH
 Кислотные оксиды • Кислотные оксиды - это такие оксиды, которым соответствуют кислоты. • Это оксиды неметаллов: N 2 O 5 соответствует Н NO 3 , SO 3 – H 2 SO 4 А так же оксиды металлов с большим значением степеней окисления: Сr 2 O 3 - H 2 Сr O 4 Mn 2 O 7 - H Mn. O 4
Кислотные оксиды • Кислотные оксиды - это такие оксиды, которым соответствуют кислоты. • Это оксиды неметаллов: N 2 O 5 соответствует Н NO 3 , SO 3 – H 2 SO 4 А так же оксиды металлов с большим значением степеней окисления: Сr 2 O 3 - H 2 Сr O 4 Mn 2 O 7 - H Mn. O 4
 Амфотерные оксиды • Амфотерными называются оксиды, которые в зависимости от условий проявляют основные или кислотные свойства. • Это Zn. O, Al 2 O 3, Cr 2 O 3, V 2 O 3 • Амфотерные оксиды с водой непосредственно не соединяются.
Амфотерные оксиды • Амфотерными называются оксиды, которые в зависимости от условий проявляют основные или кислотные свойства. • Это Zn. O, Al 2 O 3, Cr 2 O 3, V 2 O 3 • Амфотерные оксиды с водой непосредственно не соединяются.
 Получение оксидов 1) окисление металлов: 2 Cu + O 2 = 2 Cu. O 2) окисление неметаллов: C + O 2 = CO 2 3) разложение кислот: Н 2 SО 4 = SО 2 + Н 2 О 4) разложение солей: Ca. CО 3 = Ca. О + CО 2 5) разложение оснований: Fe(ОН)2 = Fe. О + Н 2 О 6) горение сложных веществ: C 2 H 5 OH + 3 О 2 → 2 CО 2 + 3 Н 2 О
Получение оксидов 1) окисление металлов: 2 Cu + O 2 = 2 Cu. O 2) окисление неметаллов: C + O 2 = CO 2 3) разложение кислот: Н 2 SО 4 = SО 2 + Н 2 О 4) разложение солей: Ca. CО 3 = Ca. О + CО 2 5) разложение оснований: Fe(ОН)2 = Fe. О + Н 2 О 6) горение сложных веществ: C 2 H 5 OH + 3 О 2 → 2 CО 2 + 3 Н 2 О
 Химические свойства оксидов. 1. Основные оксиды а) взаимодействие с кислотами: Ba. O + 2 HCl = Ba. Cl 2 + H 2 O б) взаимодействие с водой: Mg. O + H 2 O = Mg(OH)2 в) взаимодействие с кислотным оксидом: Ca. O + CO 2 = Ca. CO 3 г) взаимодействие с амфотерным оксидом: Na 2 O + Zn. O = Na 2 Zn. O 2 цинкат натрия
Химические свойства оксидов. 1. Основные оксиды а) взаимодействие с кислотами: Ba. O + 2 HCl = Ba. Cl 2 + H 2 O б) взаимодействие с водой: Mg. O + H 2 O = Mg(OH)2 в) взаимодействие с кислотным оксидом: Ca. O + CO 2 = Ca. CO 3 г) взаимодействие с амфотерным оксидом: Na 2 O + Zn. O = Na 2 Zn. O 2 цинкат натрия
 2. Кислотные оксиды. а) взаимодействие с водой: SO 3 + H 2 O = H 2 SO 4 оксид серы (VI) б) взаимодействие с основанием: Ca(OH)2 + CO 2 = Ca. CO 3 + H 2 O гидроксид кальция в) взаимодействие с основным оксидом: CO 2 + Ca. O = Ca. CO 3 карбонат кальция
2. Кислотные оксиды. а) взаимодействие с водой: SO 3 + H 2 O = H 2 SO 4 оксид серы (VI) б) взаимодействие с основанием: Ca(OH)2 + CO 2 = Ca. CO 3 + H 2 O гидроксид кальция в) взаимодействие с основным оксидом: CO 2 + Ca. O = Ca. CO 3 карбонат кальция
 3. Амфотерные оксиды. а) взаимодействие с кислотами: Zn. O + 2 HCl = Zn. Cl 2 + H 2 O хлорид цинка б) взаимодействие с основаниями: Zn. O + 2 Na. OH = Na 2 Zn. O 2 + H 2 O гидроксид натрия
3. Амфотерные оксиды. а) взаимодействие с кислотами: Zn. O + 2 HCl = Zn. Cl 2 + H 2 O хлорид цинка б) взаимодействие с основаниями: Zn. O + 2 Na. OH = Na 2 Zn. O 2 + H 2 O гидроксид натрия
 Применение оксидов: Fe 2 O 3 – оксид железа (III) – темно-красного цвета – гематит или красный железняк – для изготовления красок. Fe 3 O 4 – оксид железа (II, III) – минерал магнетит или магнитный железняк, хороший проводник электричества – для получения и изготовления электродов. Ca. O – оксид кальция (II) – порошок белого цвета – «негашеная» известь, используют в строительстве. Al 2 O 3 – оксид алюминия (III) – минерал твердый корунд – как полирующее средство. SO 2 – оксид серы (IV) или сернистый газ – бесцветный газ, имеющий удушливый запах, убивает микроорганизмы, плесневые грибки – окуривают подвалы, погреба, при перевозке и хранении фруктов и ягод.
Применение оксидов: Fe 2 O 3 – оксид железа (III) – темно-красного цвета – гематит или красный железняк – для изготовления красок. Fe 3 O 4 – оксид железа (II, III) – минерал магнетит или магнитный железняк, хороший проводник электричества – для получения и изготовления электродов. Ca. O – оксид кальция (II) – порошок белого цвета – «негашеная» известь, используют в строительстве. Al 2 O 3 – оксид алюминия (III) – минерал твердый корунд – как полирующее средство. SO 2 – оксид серы (IV) или сернистый газ – бесцветный газ, имеющий удушливый запах, убивает микроорганизмы, плесневые грибки – окуривают подвалы, погреба, при перевозке и хранении фруктов и ягод.
 Применение оксидов: CO 2 – оксид углерода (IV), углекислый газ. Твердый оксид углерода – сухой лед. Для изготовления соды, сахара, газированных напитков, в жидком виде в огнетушителях. Si. O 2 – оксид кремния (IV) – твердое, тугоплавкое вещество в природе в двух видах: 1) кристаллический кремнезем – в виде минерала кварца и его разновидностей: горный хрусталь, халцедон, агат, яшма, кремень – используют в силикатной промышленности, строительстве. 2) аморфный кремнезем Si. O 2 ∙ n. H 2 O – минерал опал. Применяют соединения оксида кремния в ювелирном деле, изготовлении химической посуды, кварцевых ламп. Для создания цветных стекол используют следующие оксиды: Cо 2 O 3 – синий цвет , Cr 2 O 3 – зеленый цвет, Mn. O 2 – розовый цвет.
Применение оксидов: CO 2 – оксид углерода (IV), углекислый газ. Твердый оксид углерода – сухой лед. Для изготовления соды, сахара, газированных напитков, в жидком виде в огнетушителях. Si. O 2 – оксид кремния (IV) – твердое, тугоплавкое вещество в природе в двух видах: 1) кристаллический кремнезем – в виде минерала кварца и его разновидностей: горный хрусталь, халцедон, агат, яшма, кремень – используют в силикатной промышленности, строительстве. 2) аморфный кремнезем Si. O 2 ∙ n. H 2 O – минерал опал. Применяют соединения оксида кремния в ювелирном деле, изготовлении химической посуды, кварцевых ламп. Для создания цветных стекол используют следующие оксиды: Cо 2 O 3 – синий цвет , Cr 2 O 3 – зеленый цвет, Mn. O 2 – розовый цвет.
 Закре пление Закончите уравнения химических реакций, дайте название веществам: а) P + O 2 → б) Al + O 2 → в) H 2 SO 4 + Fe 2 O 3 → г) Ba. O + HCl → д) C 2 H 4 + O 2 →
Закре пление Закончите уравнения химических реакций, дайте название веществам: а) P + O 2 → б) Al + O 2 → в) H 2 SO 4 + Fe 2 O 3 → г) Ba. O + HCl → д) C 2 H 4 + O 2 →


