11_klass_-_klassifikatsiya_neorganicheskih_veshchestv.ppt
- Количество слайдов: 13

Классификация неорганических веществ
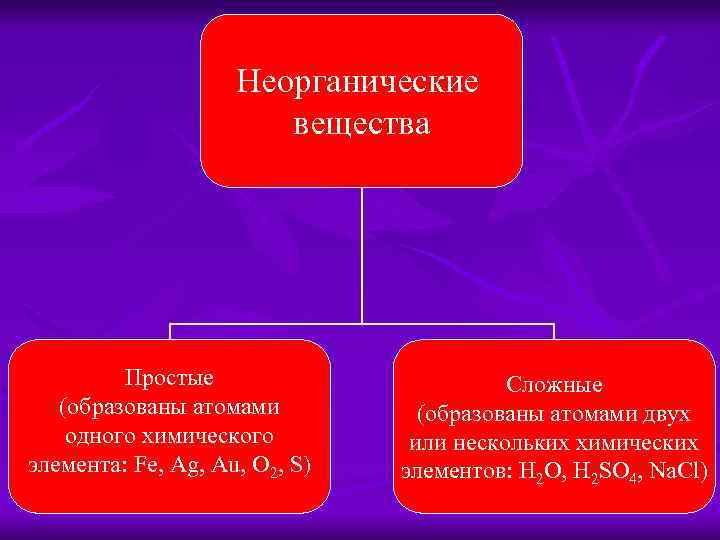
Неорганические вещества Простые (образованы атомами одного химического элемента: Fe, Ag, Au, O 2, S) Сложные (образованы атомами двух или нескольких химических элементов: H 2 O, H 2 SO 4, Na. Cl)
Простые вещества Металлы (Fe, Ag, Au) Неметаллы (H 2, O 2, S)
Сложные вещества Оксиды Основания Кислоты Соли

Оксиды Их молекулы образованы атомами двух химических элементов, один из которых – кислород: H 2 O, Ca. O, SO 3, Mn 2 O 7. Все оксиды делятся на солеобразующие и несолеобразующие (безразличные). Солеобразующие, в свою очередь, делятся на основные, кислотные, амфотерные. Основные – оксиды, которым соответствуют основания: Na 2 O, Ca. O. Кислотные – оксиды, которым соответствуют кислоты: SO 2, P 4 O 10, Cr. O 3, Mn 2 O 7. Амфотерные – оксиды, сочетающие в себе свойства основных и кислотных оксидов: Be. O, Zn. O, Cr 2 O 3, Al 2 O 3. Несолеобразующие – некоторые оксиды неметаллов, не имеющие соответствующих им кислот и солей: N 2 O, NO, CO.

Основания Их молекулы образованы атомом металла и одной или несколькими гидроксогруппами –OH, число которых в молекуле основания определяется валентностью металла. Основания делятся на: - растворимые в воде (щёлочи): Na. OH, Ca(OH)2, и нерастворимые: Cu(OH)2, Mg(OH)2; - однокислотные: Na. OH, Cu. OH, Li. OH, KOHдвухкислотные: Ca(OH)2, Mg(OH)2, Fe(OH)2, многокислотные: Fe(OH)3, Ti(OH)4.

Кислоты Их молекулы образованы атомами водорода, способными при химических реакциях замещаться на атомы металлов, и кислотным остатком, валентность которого определяется числом атомов водорода. Кислоты делятся на: - бескислородные: HCl, HBr, H 2 S - и кислородосодержащие: HNO 3, H 2 SO 4; - одноосновные: HCl, HBr, HNO 3, - двухосновные: H 2 SO 4, H 2 Si. O 3, -многоосновные: H 3 PO 4, H 4 Si. O 4.

Соли Различают соли средние (нормальные), кислые, основные, двойные, смешанные, комплексные. 1. Средние (нормальные) соли образованы атомами металла и кислотными остатками: хлориды (Na. Cl), нитраты (Al(NO 3)3), сульфаты (Mg. SO 4) и т. д. 2. Кислые соли образованы атомами металла, атомами водорода и кислотными остатками: KHSO 4 – гидросульфат калия, Ca(H 2 PO 4)2 – дигидрортофосфат кальция. Хлорид аммония NH 4 Cl относится к средним солям!

3. Основные соли образованы атомами металла, гидроксогруппами –OH и кислотными остатками: Cu(OH)Cl – гидроксохлорид меди (II), Cr(OH)2 NO 3 – дигидроксонитрат хрома (III). 4. Двойные соли образованы атомами двух металлов и кислотными остатками: KNa 2 PO 4 – ортофосфат калиядинатрия, KAl(SO 4)2 – сульфат калия-алюминия. 5. Смешанные соли образованы атомами металла и кислотными остатками двух разных кислот: Ca. Cl(OCl) – смешанный хлорид-гипохлорит кальция (хлорная или белильная известь). 6. Комплексные соли содержат в своём составе комплексные ионы: [Cu(NH 3)4]SO 4 – сульфат тетраамминмеди (II), K 3[Fe(CN)6] – гексациано-феррат (III) калия. Не являются комплексными солями H[Au. Cl 4] – тетрахлораурат водорода, [Ag(NH 3)2]OH – гидроксид диамминсеребра.

Упражнение 1 Установите соответствие между формулами веществ и классами неорганических соединений, к которым они относятся: 1. 2. 3. 4. 5. Формулы веществ: SO 2 Mg(OH)NO 2 Al 2 O 3 Cr(OH)3 H 4 Si. O 4 Классы веществ: А. Кислородосодержащая кислота. Б. Щёлочь. В. Кислотный оксид. Г. Амфотерный оксид. Д. Средняя соль. Е. Амфотерный гидроксид. Ж. Основная соль.

Ответы 1–В 2–Ж 3–Г 4–Е 5–А

Упражнение 2 Установите соответствие между формулами веществ и классами неорганических соединений, к которым они относятся: 1. 2. 3. 4. 5. Формулы веществ: NH 4 Cl NH 4 HSO 4 Mg(OH)Cl. O 4 Mg. Li. PO 4 Cr(NO 3)(NO 2) Классы веществ: А. Двойная соль. Б. Смешанная соль. В. Средняя соль. Г. Комплексная соль. Д. Основная соль. Е. Кислая соль.

Ответы 1–В 2–Е 3–Д 4–А 5–Б
11_klass_-_klassifikatsiya_neorganicheskih_veshchestv.ppt