диагн преп.ppt
- Количество слайдов: 44
 Классификация, изготовление и контроль диагностических препаратов
Классификация, изготовление и контроль диагностических препаратов
 Предварительный диагноз любой болезни ставят на основе клинических признаков и сборе анамнеза. Что бы подтвердить или уточнить то или иное заболевание необходимо дополнительное лабораторное исследование на данное заболевание. Диагностические препараты облегчают и упрощают пути диагностики. При проведении диагностического исследования необходимы диагностические наборы, антигены, т сыворотки, вакцины.
Предварительный диагноз любой болезни ставят на основе клинических признаков и сборе анамнеза. Что бы подтвердить или уточнить то или иное заболевание необходимо дополнительное лабораторное исследование на данное заболевание. Диагностические препараты облегчают и упрощают пути диагностики. При проведении диагностического исследования необходимы диагностические наборы, антигены, т сыворотки, вакцины.
 Классификация диагностических препаратов u Диагностические сыворотки u Диагностические антигены u Аллергены u Бактериофаги u Диагностические препараты высоких технологий- микрочипы (генные, клеточные, белковые, биосенсоры, наночастицы и др. )
Классификация диагностических препаратов u Диагностические сыворотки u Диагностические антигены u Аллергены u Бактериофаги u Диагностические препараты высоких технологий- микрочипы (генные, клеточные, белковые, биосенсоры, наночастицы и др. )
 ВАКЦИНЫ Инактивирова нные вакцины Живые вакцин ы ВАКЦИНЫ- предназначены для создания искусственного иммунитета. Генноинженерные вакцины
ВАКЦИНЫ Инактивирова нные вакцины Живые вакцин ы ВАКЦИНЫ- предназначены для создания искусственного иммунитета. Генноинженерные вакцины
 Инактивированные вакцины. Адъюванты (помогающий)- это вещества антигенной и неантигенной природы, различные по химическому составу, которые при совместном с антигеном введении в организм вызывают неспецифическое стимулирование иммуногенеза. Из адъювантов неорганической природы используют гидроксид алюминия- минеральный гель, алюмокалиевые квасцы. Приготовление адъювантных вакцин состоит в добавлении у готовому микробному антигену соответствующего адъюванта в оптимальных пропорциях. К числу наиболее эффективных адъювантов относят легкие минеральные масла со стабилизатором- безводным ланолином. Водную суспензию антигена и минеральное масло эмульгируют до получения стабильно-масляной эмульсии. Вакцины с такими адъювантами называют эмульгированными.
Инактивированные вакцины. Адъюванты (помогающий)- это вещества антигенной и неантигенной природы, различные по химическому составу, которые при совместном с антигеном введении в организм вызывают неспецифическое стимулирование иммуногенеза. Из адъювантов неорганической природы используют гидроксид алюминия- минеральный гель, алюмокалиевые квасцы. Приготовление адъювантных вакцин состоит в добавлении у готовому микробному антигену соответствующего адъюванта в оптимальных пропорциях. К числу наиболее эффективных адъювантов относят легкие минеральные масла со стабилизатором- безводным ланолином. Водную суспензию антигена и минеральное масло эмульгируют до получения стабильно-масляной эмульсии. Вакцины с такими адъювантами называют эмульгированными.
 Вакцины инактивированные корпускулярные. Содержат цельные инактивированные микробные клетки. При конструировании вакцин в их состав включают штаммы одного или нескольких сероваров, в зависимости от антигенной гетерогенности конкретного возбудителя. Используют штаммы бактерий без признаков диссоциации. Бактериальную массу чаще получают путем выращивания вакцинных штаммов в жидких питательных средах ферментах. На следующем этапе бактреиальные клетки инактивируют физическими (прогревание при 55 -60°С, УЗ, УФО, ИО) или химическими методами (формалин, глутаровый альдегид, β- пропиолактон, кристаллвиолет, метиленовый синий и т. д. ). К любому методу инактивации микроорганизмов предъявляют 2 основных требования: полное инактивация клеток возбудителя, отсутствие существенных нарушений в антигенных и имунногенных свойствах возбудителя. После инактивации устанавливают необходимую концентрацию микробных клеток в одном миллилитре суспензии, добавляют тот или иной адъювант препарат расфасовывают и контролируют.
Вакцины инактивированные корпускулярные. Содержат цельные инактивированные микробные клетки. При конструировании вакцин в их состав включают штаммы одного или нескольких сероваров, в зависимости от антигенной гетерогенности конкретного возбудителя. Используют штаммы бактерий без признаков диссоциации. Бактериальную массу чаще получают путем выращивания вакцинных штаммов в жидких питательных средах ферментах. На следующем этапе бактреиальные клетки инактивируют физическими (прогревание при 55 -60°С, УЗ, УФО, ИО) или химическими методами (формалин, глутаровый альдегид, β- пропиолактон, кристаллвиолет, метиленовый синий и т. д. ). К любому методу инактивации микроорганизмов предъявляют 2 основных требования: полное инактивация клеток возбудителя, отсутствие существенных нарушений в антигенных и имунногенных свойствах возбудителя. После инактивации устанавливают необходимую концентрацию микробных клеток в одном миллилитре суспензии, добавляют тот или иной адъювант препарат расфасовывают и контролируют.
 Химические вакцины. в качестве иммуногенного начала содержат извлеченные тем или иным способом из микробной клетки различные соединения. К преимуществу химических вакцин относят возможность отделить иммунногеной компонент от балластных веществ клетки, что позволяет снизить риактогенность препарата. В принципе к химическим вакцинам можно отнести и анатоксин вакцин. Анатоксинвакцины. Содержат в качестве иммунногеного начала инактивированный формалином экзотоксин бактерий (анатоксин). Для получения анатоксинвакцин токсинообразующий штамм возбудителя культивируют в жидкой питательной среде в условиях, обеспечивающих максимальное накопление в культуральной жидкости. Затем культуральную жидкость отделяют от бактериальной массы и экзотоксин переводят в состоянии анатоксина воздействием формалина в тепле. Анавакцины. При производстве некоторых вакцин микробную массу и токсин не разделяют, готовый препарат содержит инактивированные микробные клетки и анатоксин (анавакцина).
Химические вакцины. в качестве иммуногенного начала содержат извлеченные тем или иным способом из микробной клетки различные соединения. К преимуществу химических вакцин относят возможность отделить иммунногеной компонент от балластных веществ клетки, что позволяет снизить риактогенность препарата. В принципе к химическим вакцинам можно отнести и анатоксин вакцин. Анатоксинвакцины. Содержат в качестве иммунногеного начала инактивированный формалином экзотоксин бактерий (анатоксин). Для получения анатоксинвакцин токсинообразующий штамм возбудителя культивируют в жидкой питательной среде в условиях, обеспечивающих максимальное накопление в культуральной жидкости. Затем культуральную жидкость отделяют от бактериальной массы и экзотоксин переводят в состоянии анатоксина воздействием формалина в тепле. Анавакцины. При производстве некоторых вакцин микробную массу и токсин не разделяют, готовый препарат содержит инактивированные микробные клетки и анатоксин (анавакцина).
 Живые вакцины. Это искусственно ослабленные или природные авирулентные (слабовирулентные) штаммы возбудителя, которые утратили способность вызывать у естественно-восприимчивых животных болезнь, но могут в течение определенного промежутка времени размножаться в организме вакциннированнго животного, вызывая иммунный ответ. Основные требования к вакцинным штаммам: отсутствие склонности к реверсии (возвращение в исходное вирулентное состояние); неконтагиозность (возбудитель вакцинного штамма не должен передаваться от вакцинированного животного к невакцинированному). Желательно, что бы вакцинный штамм нес стабильный маркер, отличающий его от эпизоотических штаммов возбудителя.
Живые вакцины. Это искусственно ослабленные или природные авирулентные (слабовирулентные) штаммы возбудителя, которые утратили способность вызывать у естественно-восприимчивых животных болезнь, но могут в течение определенного промежутка времени размножаться в организме вакциннированнго животного, вызывая иммунный ответ. Основные требования к вакцинным штаммам: отсутствие склонности к реверсии (возвращение в исходное вирулентное состояние); неконтагиозность (возбудитель вакцинного штамма не должен передаваться от вакцинированного животного к невакцинированному). Желательно, что бы вакцинный штамм нес стабильный маркер, отличающий его от эпизоотических штаммов возбудителя.
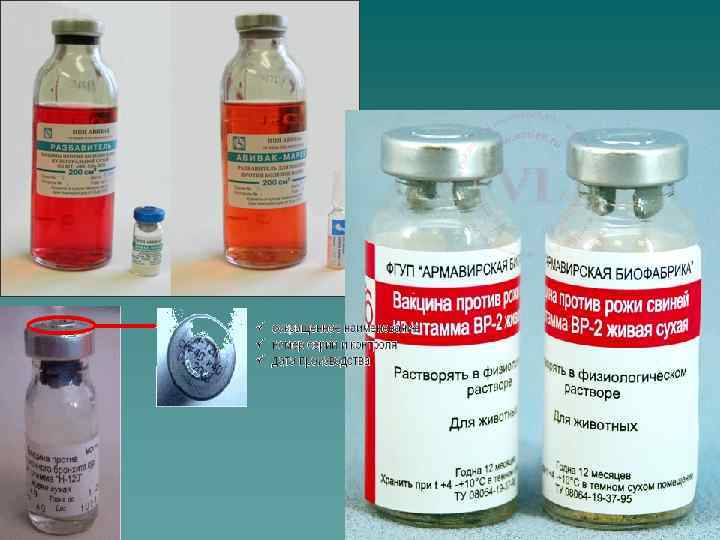
 Нобивак DHP (Nobivac DHP) Комбинированная живая вакцина против чумы плотоядных, инфекционного гепатита и парвовирусной инфекции собак. СОСТАВ Каждый флакон (1 доза) содержит: вируса чумы плотоядных (штамм Onderslepoort) не менее 10 тыс. ТЦД/50; парвовируса собак (штамм 154) не менее 10 млн. ТЦД/50; аденовируса (штамм Manhattan LPV 3 серотипа 2) 10 тыс. БОЕ. ЛЕКАРСТВЕННАЯ ФОРМА Лиофилизированная вакцина белого цвета. В качестве растворителя используется фосфатный буферный раствор для инъекций или одна из жидких вакцин (Нобивак RL или Rabies, Lерто). ПОКАЗАНИЯ Для защиты собак от чумы плотоядных, инфекционного гепатита и парвовирусного энтерита. ПРОГРАММА ВАКЦИНАЦИИ Прививают только клинически здоровых собак в возрасте 8 -9 недель с последующей вакцинацией в 12 недель. Рекомендуется проводить ежегодную ревакцинацию животных одной дозой вакцины. Использование Нобивак DHP является частью комплексной программы эффективной вакцинации собак. БИОЛОГИЧЕСКИЕ СВОЙСТВА Индуцирует у привитых животных высокий титр специфических антител к вирусам чумы плотоядных, гепатита (аденовируса собак серотипа 2) и парвовируса собак.
Нобивак DHP (Nobivac DHP) Комбинированная живая вакцина против чумы плотоядных, инфекционного гепатита и парвовирусной инфекции собак. СОСТАВ Каждый флакон (1 доза) содержит: вируса чумы плотоядных (штамм Onderslepoort) не менее 10 тыс. ТЦД/50; парвовируса собак (штамм 154) не менее 10 млн. ТЦД/50; аденовируса (штамм Manhattan LPV 3 серотипа 2) 10 тыс. БОЕ. ЛЕКАРСТВЕННАЯ ФОРМА Лиофилизированная вакцина белого цвета. В качестве растворителя используется фосфатный буферный раствор для инъекций или одна из жидких вакцин (Нобивак RL или Rabies, Lерто). ПОКАЗАНИЯ Для защиты собак от чумы плотоядных, инфекционного гепатита и парвовирусного энтерита. ПРОГРАММА ВАКЦИНАЦИИ Прививают только клинически здоровых собак в возрасте 8 -9 недель с последующей вакцинацией в 12 недель. Рекомендуется проводить ежегодную ревакцинацию животных одной дозой вакцины. Использование Нобивак DHP является частью комплексной программы эффективной вакцинации собак. БИОЛОГИЧЕСКИЕ СВОЙСТВА Индуцирует у привитых животных высокий титр специфических антител к вирусам чумы плотоядных, гепатита (аденовируса собак серотипа 2) и парвовируса собак.
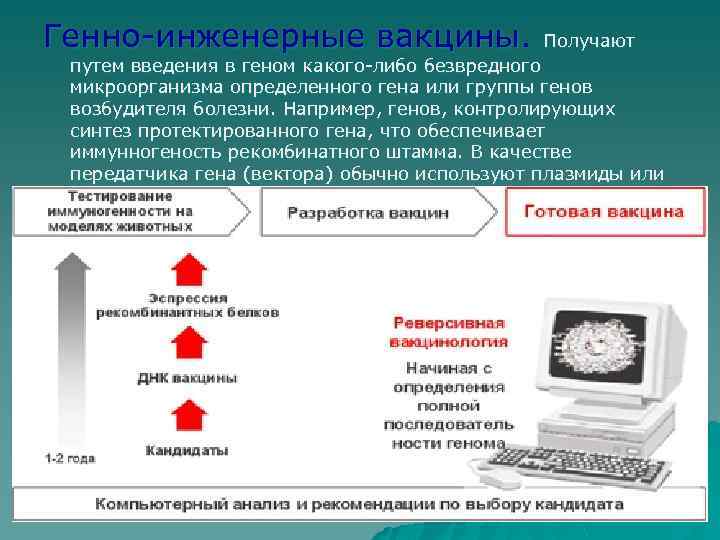 Генно-инженерные вакцины. Получают путем введения в геном какого-либо безвредного микроорганизма определенного гена или группы генов возбудителя болезни. Например, генов, контролирующих синтез протектированного гена, что обеспечивает иммунногеность рекомбинатного штамма. В качестве передатчика гена (вектора) обычно используют плазмиды или фаги.
Генно-инженерные вакцины. Получают путем введения в геном какого-либо безвредного микроорганизма определенного гена или группы генов возбудителя болезни. Например, генов, контролирующих синтез протектированного гена, что обеспечивает иммунногеность рекомбинатного штамма. В качестве передатчика гена (вектора) обычно используют плазмиды или фаги.
 Контроль вакцин Проводят по трем основным параметрам. Стерильность (инактивированные) или частоту роста (живые) контролируют посевом на питательные среды. Безвредность введением вакцины тем или иным лабораторным животным. Вакцина не должна вызывать заболевание и гибель животных. Специфическую активность (иммуногенность) контролируют следующим образом: вакцину вводят группе лабораторных животных и через промежуток времени, достаточной для выработки активного иммунитета 15 -20 суток, животных этой группы вместе с контрольными непривитыми заражают заведомо летальной дозой возбудителя. Контрольные животные должны погибнуть, 80% и более должны выжить. В некоторых случаях об иммуноегнности препарата судят по косвенным показателям: количеству агглютининов привитых животных (лептоспирозная вакцина), антитоксинов в рн (вакцина против ботулизма).
Контроль вакцин Проводят по трем основным параметрам. Стерильность (инактивированные) или частоту роста (живые) контролируют посевом на питательные среды. Безвредность введением вакцины тем или иным лабораторным животным. Вакцина не должна вызывать заболевание и гибель животных. Специфическую активность (иммуногенность) контролируют следующим образом: вакцину вводят группе лабораторных животных и через промежуток времени, достаточной для выработки активного иммунитета 15 -20 суток, животных этой группы вместе с контрольными непривитыми заражают заведомо летальной дозой возбудителя. Контрольные животные должны погибнуть, 80% и более должны выжить. В некоторых случаях об иммуноегнности препарата судят по косвенным показателям: количеству агглютининов привитых животных (лептоспирозная вакцина), антитоксинов в рн (вакцина против ботулизма).

 С целью контроля вакцины на безвредность и активность 20 -ти белым мышам массой 17 -18 г вводят п/к 0, 2 мл препарата. Вакцину считают безвредной, если погибает не более 5 -ти мышей. Через 14 дней всех оставшихся живых вакцинированных и 5 контрольных мышей заражают вирулентного штамма возбудителя рожей свиней в заведомо летальной дозе. Вакцину признают активной если погибают в течение 3 -4 суток контрольные и выживают не менее 75% вакцинированных мышей.
С целью контроля вакцины на безвредность и активность 20 -ти белым мышам массой 17 -18 г вводят п/к 0, 2 мл препарата. Вакцину считают безвредной, если погибает не более 5 -ти мышей. Через 14 дней всех оставшихся живых вакцинированных и 5 контрольных мышей заражают вирулентного штамма возбудителя рожей свиней в заведомо летальной дозе. Вакцину признают активной если погибают в течение 3 -4 суток контрольные и выживают не менее 75% вакцинированных мышей.

 Лечебно-профилактические иммунные сыворотки и иммуноглобулины Данные биопрепараты применяют для создания искусственного пассивного иммунитета. Пассивный иммунитет возникает через 20 -24 часа после инъекции препарата и длится максимум 2 -3 недели. Иммунные сыворотки получают путем многократного введения антигена животным-продуцентам (волам, лошадям). При достижении необходмимого уровня антител у животного берут кровь, сепарируют ее для получения сыворотки, котрую стерелизую фильтрованием и консервируют 0, 25 - 0, 5% фенола, 0, 01 -0, 3% тиомерсала и другими веществами По направленности действия иммуные сывортки подразделяют на антибактреиальные, антитоксические, антивирусные.
Лечебно-профилактические иммунные сыворотки и иммуноглобулины Данные биопрепараты применяют для создания искусственного пассивного иммунитета. Пассивный иммунитет возникает через 20 -24 часа после инъекции препарата и длится максимум 2 -3 недели. Иммунные сыворотки получают путем многократного введения антигена животным-продуцентам (волам, лошадям). При достижении необходмимого уровня антител у животного берут кровь, сепарируют ее для получения сыворотки, котрую стерелизую фильтрованием и консервируют 0, 25 - 0, 5% фенола, 0, 01 -0, 3% тиомерсала и другими веществами По направленности действия иммуные сывортки подразделяют на антибактреиальные, антитоксические, антивирусные.
 Антитоксические сыворотки (противодифтерийная, противостолбнячная, противоботулиническая, противогангренозная) получают иммунизацией лошадей возрастающими дозами анатоксинов, а затем и соответствующими токсинами. Сыворотки подвергают очистке и концентрации методом «Диаферм-3» , контролю на безвредность, апирогенность, затем титруют, т. е. 'определяют содержание антитоксинов в 1 мл препарата. Специфическая активность сывороток, или количество антител, измеряется с помощью методов, основанных на способности сывороток in vitro и in vivo нейтрализовать соответствующие токсины, и выражается в Международных антитоксических единицах (ME), принятых ВОЗ. За 1 ME принимается то минимальное количество сыворотки, которое способно нейтрализовать определенную дозу токсина, выражающуюся в стандартных единицах, обозначаемых как смертельные, некротические или реактивные дозы в зависимости от вида токсина и способа титрования. Титрование антитоксических сывороток может производиться тремя методами: по Району, Эрлиху и Ремеру.
Антитоксические сыворотки (противодифтерийная, противостолбнячная, противоботулиническая, противогангренозная) получают иммунизацией лошадей возрастающими дозами анатоксинов, а затем и соответствующими токсинами. Сыворотки подвергают очистке и концентрации методом «Диаферм-3» , контролю на безвредность, апирогенность, затем титруют, т. е. 'определяют содержание антитоксинов в 1 мл препарата. Специфическая активность сывороток, или количество антител, измеряется с помощью методов, основанных на способности сывороток in vitro и in vivo нейтрализовать соответствующие токсины, и выражается в Международных антитоксических единицах (ME), принятых ВОЗ. За 1 ME принимается то минимальное количество сыворотки, которое способно нейтрализовать определенную дозу токсина, выражающуюся в стандартных единицах, обозначаемых как смертельные, некротические или реактивные дозы в зависимости от вида токсина и способа титрования. Титрование антитоксических сывороток может производиться тремя методами: по Району, Эрлиху и Ремеру.
 Антибактериальные сыворотки получают гипериммунизацией лошадей соответствующими убитыми бактериями; они содержат антитела с агглютинирующими, литическими и опсонизирующими свойствами. Антибактериальные сыворотки относятся к нетитруемым препаратам, так как общепринятой единицы измерения их лечебного действия не существует. Эффективность таких сывороток мала, поэтому широкого применения они не нашли. Для очистки и концентрации антибактериальных сывороток и некоторых антивирусных используют метод, основанный на разделении белковых фракций нативных сывороток и выделении активных иммуноглобулинов этиловым спиртом при низкой температуре (метод водно -спиртового осаждения на холоду).
Антибактериальные сыворотки получают гипериммунизацией лошадей соответствующими убитыми бактериями; они содержат антитела с агглютинирующими, литическими и опсонизирующими свойствами. Антибактериальные сыворотки относятся к нетитруемым препаратам, так как общепринятой единицы измерения их лечебного действия не существует. Эффективность таких сывороток мала, поэтому широкого применения они не нашли. Для очистки и концентрации антибактериальных сывороток и некоторых антивирусных используют метод, основанный на разделении белковых фракций нативных сывороток и выделении активных иммуноглобулинов этиловым спиртом при низкой температуре (метод водно -спиртового осаждения на холоду).
 Антивирусные сыворотки также получают из сыворотки крови животных, иммунизированных вакцинными штаммами вирусов или соответствующими вирусами. Выпускают антивирусные сыворотки, очищенные методом водно-спиртового осаждения. Иммуноглобулины (гомологичные), получаемые из крови человека, готовят двух видов — противокоревой (или нормальной) и иммуноглобулины направленного действия. Преимущество этих иммуноглобулинов перед гетерогенными в том, что они практически нереактогенны и циркулируют в организме более продолжительное время. Противокоревой (или нормальный) иммуноглобулин получают из донорской, плацентарной или абортной крови, которая содержит антитела против вируса кори, а также против вирусов гриппа, гепатита, полиомиелита, возбудителей коклюша и некоторых других вирусных и бактериальных инфекций.
Антивирусные сыворотки также получают из сыворотки крови животных, иммунизированных вакцинными штаммами вирусов или соответствующими вирусами. Выпускают антивирусные сыворотки, очищенные методом водно-спиртового осаждения. Иммуноглобулины (гомологичные), получаемые из крови человека, готовят двух видов — противокоревой (или нормальной) и иммуноглобулины направленного действия. Преимущество этих иммуноглобулинов перед гетерогенными в том, что они практически нереактогенны и циркулируют в организме более продолжительное время. Противокоревой (или нормальный) иммуноглобулин получают из донорской, плацентарной или абортной крови, которая содержит антитела против вируса кори, а также против вирусов гриппа, гепатита, полиомиелита, возбудителей коклюша и некоторых других вирусных и бактериальных инфекций.
 Сывороточные препараты получают путем специальной обработки крови искусственно иммунизированных животных, а также крови людей, перенесших определенное инфекционное заболевание или иммунизированных соответствующим вакцинным препаратом. Иммунные сыворотки и иммуноглобулины используют для экстренной профилактики заболеваний с коротким инкубационным периодом, а также для лечения уже развившихся болезней После внутривенного введения сывороток иммунитет вырабатывается практически сразу после инъекции. После внутримышечного и подкожного их введения состояние невосприимчивости наступает медленнее, по мере всасывания сыворотки из места инъекции. Концентрация антител в крови достигает максимума через 12 -24 ч после инъекции. Иммуноглобулины направленного действия изготавливают из крови людей, специально иммунизированных против той или иной инфекции. Эти препараты содержат определенные антитела в повышенной концентрации и применяются в качестве специфических препаратов для экстренной профилактики и лечения ряда заболеваний (гриппа, столбняка, бешенства, клещевого энцефалита, стафилококковых инфекций).
Сывороточные препараты получают путем специальной обработки крови искусственно иммунизированных животных, а также крови людей, перенесших определенное инфекционное заболевание или иммунизированных соответствующим вакцинным препаратом. Иммунные сыворотки и иммуноглобулины используют для экстренной профилактики заболеваний с коротким инкубационным периодом, а также для лечения уже развившихся болезней После внутривенного введения сывороток иммунитет вырабатывается практически сразу после инъекции. После внутримышечного и подкожного их введения состояние невосприимчивости наступает медленнее, по мере всасывания сыворотки из места инъекции. Концентрация антител в крови достигает максимума через 12 -24 ч после инъекции. Иммуноглобулины направленного действия изготавливают из крови людей, специально иммунизированных против той или иной инфекции. Эти препараты содержат определенные антитела в повышенной концентрации и применяются в качестве специфических препаратов для экстренной профилактики и лечения ряда заболеваний (гриппа, столбняка, бешенства, клещевого энцефалита, стафилококковых инфекций).
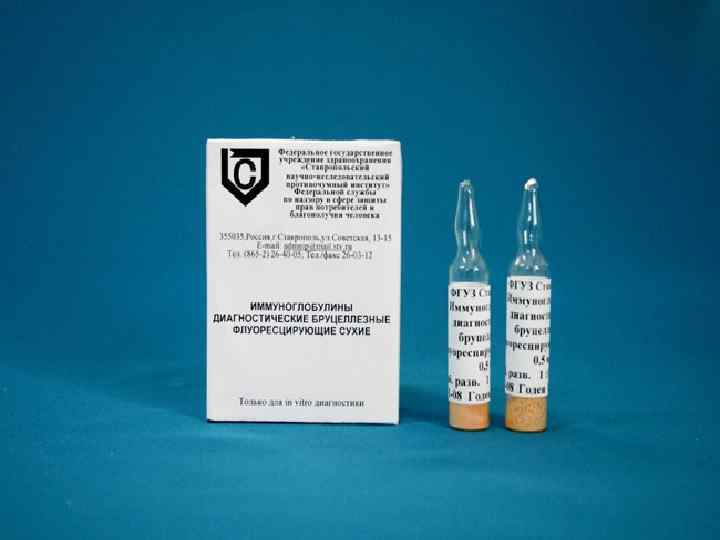
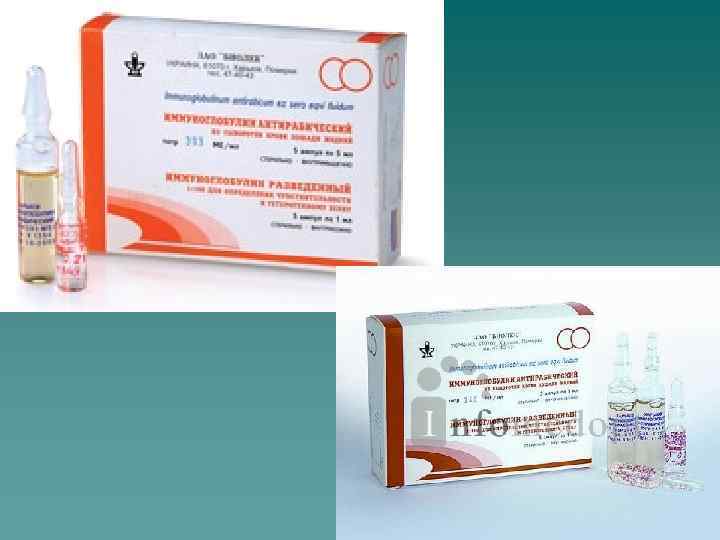
 Контроль сывороточных препаратов Включает в себя проверку на стерильность, безвредность и специфическую активность. Стерильность препаратов проверяют посевом на питательные среды (МПА, МПБ, МППБ, агар Сабуро или Чепека). Безвредность каждой серии контролируют введением сывортки контрольным животным. Определение превентивных (защитных) свойств сыворотки на естественно-восприимчивых или лабораторных животных заключается в том, что животным вводят сыворотку (п/к, в/м или в/б), а через 20 -24 часа иммунизированных и контрольных животных заражают летальной дозой гомологичного вирулентного микроорганизма. Иммунизированные животные должны остаться здоровыми при гибели или характерном переболевании контрольных. Активность антитоксических и ряда противовирусных сывороток определяют в реакциях нейтрализации. Количество антител в сывортках устанавливают при помощи различных серологических реакциях (РСК, РА, РНГА, РДП ит. д. )
Контроль сывороточных препаратов Включает в себя проверку на стерильность, безвредность и специфическую активность. Стерильность препаратов проверяют посевом на питательные среды (МПА, МПБ, МППБ, агар Сабуро или Чепека). Безвредность каждой серии контролируют введением сывортки контрольным животным. Определение превентивных (защитных) свойств сыворотки на естественно-восприимчивых или лабораторных животных заключается в том, что животным вводят сыворотку (п/к, в/м или в/б), а через 20 -24 часа иммунизированных и контрольных животных заражают летальной дозой гомологичного вирулентного микроорганизма. Иммунизированные животные должны остаться здоровыми при гибели или характерном переболевании контрольных. Активность антитоксических и ряда противовирусных сывороток определяют в реакциях нейтрализации. Количество антител в сывортках устанавливают при помощи различных серологических реакциях (РСК, РА, РНГА, РДП ит. д. )
 Животных заражают п/к, в/м или в/б
Животных заражают п/к, в/м или в/б
 Пример контроля иммунной лечебно-профилактической сыворотки (против рожи свиней) Контроль стерильности: сыворотку высевают на МПА, МПБ, МППБ, агар Сабуро. Посевы выдерживают при 37°и 20°С (агар Сабуро) 10 дней. ; среды должны остаться стерильными. Контроль безвредности: 5 -ти белым мышам массой 17 -29 г вводят п/к по 0, 5 мл сыворотки, 2 -м морским свинкам массой 250 -300 г- по 10 мл. Все привитые животные должны остаться живыми в течение 10 -ти дней. Контроль активности: 15 -ти белым мышам массой 17 -20 г вводят в/б по 0, 01, 0, 02 и 0, 03 мл (по 5 мышей на дозу) сыворотки. Через 2 часа всем привитым и 5 -ти непривитыми мышам вводят п/к 0, 1 -0, 2 мл суточной культуры вирулентного штамма возбудителя рожи свиней, разведенной 1: 200. сыворотку считают активной если в течение 10 дней все привитые животные остаются живыми, а контрольные погибают. Для концентрирования антител и удаления серологические неактивных белков (альбуминов) применяют методы, с помощью которых выделяют глобулиновую фракцию белков иммунной сыворотки. Готовые препараты иммунноглобулинов контролируют как иммунной сыворотки на стерильность, безвредность и специфическую активность.
Пример контроля иммунной лечебно-профилактической сыворотки (против рожи свиней) Контроль стерильности: сыворотку высевают на МПА, МПБ, МППБ, агар Сабуро. Посевы выдерживают при 37°и 20°С (агар Сабуро) 10 дней. ; среды должны остаться стерильными. Контроль безвредности: 5 -ти белым мышам массой 17 -29 г вводят п/к по 0, 5 мл сыворотки, 2 -м морским свинкам массой 250 -300 г- по 10 мл. Все привитые животные должны остаться живыми в течение 10 -ти дней. Контроль активности: 15 -ти белым мышам массой 17 -20 г вводят в/б по 0, 01, 0, 02 и 0, 03 мл (по 5 мышей на дозу) сыворотки. Через 2 часа всем привитым и 5 -ти непривитыми мышам вводят п/к 0, 1 -0, 2 мл суточной культуры вирулентного штамма возбудителя рожи свиней, разведенной 1: 200. сыворотку считают активной если в течение 10 дней все привитые животные остаются живыми, а контрольные погибают. Для концентрирования антител и удаления серологические неактивных белков (альбуминов) применяют методы, с помощью которых выделяют глобулиновую фракцию белков иммунной сыворотки. Готовые препараты иммунноглобулинов контролируют как иммунной сыворотки на стерильность, безвредность и специфическую активность.

 Диагностические иммунные сыворотки и глобулины Принцип получения диагн 6 остических иммунных сывороток так же, как и лечебно-профилактичеких, но диагностические сыворотки должны характеризоваться не только активностью серологических реакций, но и высокой специфичностью. С помощью диагностических сывороток обнаруживают микробные антигены тканевых материалов и идентифицируют выделенные микроорганизмы. Различают видовые сывортки (предназначены для идентификации микроорганизмов на уровне вида), групповые (идентификация на уровне серологической группы), серовариантные (на уровне серовара). Иммунные сыворотки используют в различных серологических реакциях (РА, РП, РСК, РНГА, РН, ИФА). При получении антител меченых флюорохромом и ферментами из иммунных сывороток предварительно выделяют и очищают иммунноглобулиновую фракцию. Диагностические сыворотки контролируют на стерильность, активность и специфичность.
Диагностические иммунные сыворотки и глобулины Принцип получения диагн 6 остических иммунных сывороток так же, как и лечебно-профилактичеких, но диагностические сыворотки должны характеризоваться не только активностью серологических реакций, но и высокой специфичностью. С помощью диагностических сывороток обнаруживают микробные антигены тканевых материалов и идентифицируют выделенные микроорганизмы. Различают видовые сывортки (предназначены для идентификации микроорганизмов на уровне вида), групповые (идентификация на уровне серологической группы), серовариантные (на уровне серовара). Иммунные сыворотки используют в различных серологических реакциях (РА, РП, РСК, РНГА, РН, ИФА). При получении антител меченых флюорохромом и ферментами из иммунных сывороток предварительно выделяют и очищают иммунноглобулиновую фракцию. Диагностические сыворотки контролируют на стерильность, активность и специфичность.
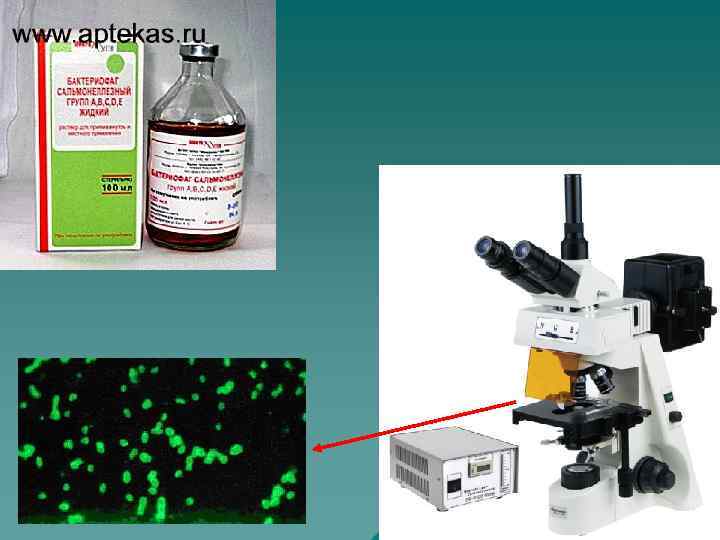
 Контроль активности диагностической сывортки на примере люминесцирующей сальмонеллезной. Из 24 часовых агаровых культур сальмонелл готовят мазки (не густые) фиксируют их, затем на каждый мазок наносят различные разведения гомологичной флуюресцирующей сыворотки. В дальнейшем препараты обрабатывает по всем предыдущим параметрам. Мазки просматривают под люминесцентным микроскопом. Максимальное разведение сыворотки, обеспечивающая свечения гомологичных микробных клеток на 3 -4 креста, считают ее красящим титром. Рабочий титр сывортки, т. е. используемой в работе равен половине красящего титра. Контроль специфической люминесцирующей сыворотки: на предметных стеклах готовят мазки из гетерологичных сальмонелл и эшерихий (по несколько культур) и обрабатывают флуоресцирующей сывороткой в рабочем титре. При микроскопии свечение гетерологичных микробов не должно быть.
Контроль активности диагностической сывортки на примере люминесцирующей сальмонеллезной. Из 24 часовых агаровых культур сальмонелл готовят мазки (не густые) фиксируют их, затем на каждый мазок наносят различные разведения гомологичной флуюресцирующей сыворотки. В дальнейшем препараты обрабатывает по всем предыдущим параметрам. Мазки просматривают под люминесцентным микроскопом. Максимальное разведение сыворотки, обеспечивающая свечения гомологичных микробных клеток на 3 -4 креста, считают ее красящим титром. Рабочий титр сывортки, т. е. используемой в работе равен половине красящего титра. Контроль специфической люминесцирующей сыворотки: на предметных стеклах готовят мазки из гетерологичных сальмонелл и эшерихий (по несколько культур) и обрабатывают флуоресцирующей сывороткой в рабочем титре. При микроскопии свечение гетерологичных микробов не должно быть.
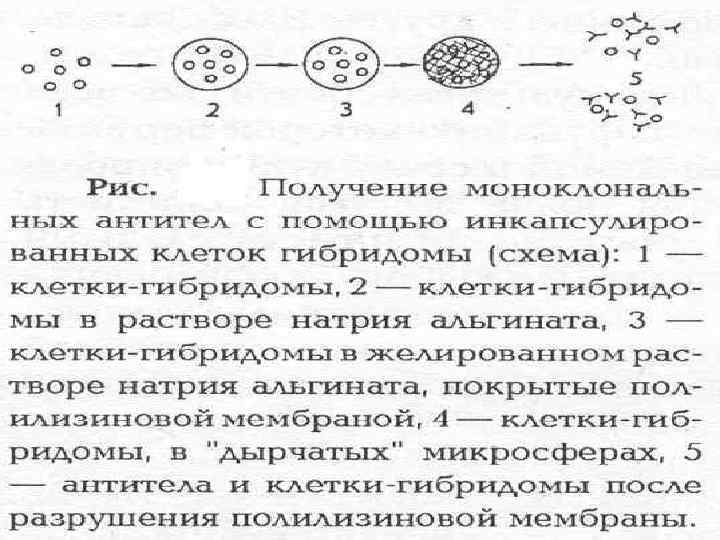
 Моноклональные антитела Обычные иммунные диагностические сыворотки (поликноланые) представляют собой смесь антител против различных антигенных детерминант возбудителя. Использование таких сыворотка для идентификации возбудителя сопряжено с получением перекрестных реакции между сероварами одного вида и даже между различными видами микроорганизмов за счет общих антигенных детерминант. Избежать таких перекрестных реакций можно различными способами. Один из методов заключается в использовании моноклональных антител. Моноклональные антитела представляют собой иммуннголобулины, продуцируемые одним клоном плазматических клеток и реагирующие с определенным антигеном эпитопом микроорганизма. Что бы получить моноклональные антитела, изолируют и поддерживают линию лимфоцитов, синтезирующих антитела определенной специфической направленности. Клетки-продуценты антител не способны расти in vitro. Злокачественная опухоль (миелома) синтезирует в больших количествах аномальные иммунноглобулины и способных неограниченному росту in vitro. Разработана методика слияния клеток миеломы с лимфоцитами, при этом гибридная клетка как и опухолевая. Способна к неограниченному росту и одновременно синтезирует антитела, как лимфоидная.
Моноклональные антитела Обычные иммунные диагностические сыворотки (поликноланые) представляют собой смесь антител против различных антигенных детерминант возбудителя. Использование таких сыворотка для идентификации возбудителя сопряжено с получением перекрестных реакции между сероварами одного вида и даже между различными видами микроорганизмов за счет общих антигенных детерминант. Избежать таких перекрестных реакций можно различными способами. Один из методов заключается в использовании моноклональных антител. Моноклональные антитела представляют собой иммуннголобулины, продуцируемые одним клоном плазматических клеток и реагирующие с определенным антигеном эпитопом микроорганизма. Что бы получить моноклональные антитела, изолируют и поддерживают линию лимфоцитов, синтезирующих антитела определенной специфической направленности. Клетки-продуценты антител не способны расти in vitro. Злокачественная опухоль (миелома) синтезирует в больших количествах аномальные иммунноглобулины и способных неограниченному росту in vitro. Разработана методика слияния клеток миеломы с лимфоцитами, при этом гибридная клетка как и опухолевая. Способна к неограниченному росту и одновременно синтезирует антитела, как лимфоидная.
 Моноклональные тела, связавшие молекулы антигена
Моноклональные тела, связавшие молекулы антигена
 Получение моноклональных антител включает в себя несколько этапов: 1. Известным антигеном иммунизируют животных. Затем из селенки выделяют В-лимфоциты. 2. Проводят слияние (гибридизация) В-лимфоцитов и миеломных клеток. Получают смесь лимфоцитов гибридных и миеломных клеток. 3. Смесь клеток культивируют в среде, содержащей ГАТ (гипосксантинаминоптерин-тимидин), что приводит к гибели лимфоцитов и миеломных клеток, т. к. на указанной среде могут расти только гибридомы. 4. Гибридомные клетки рассевают (клонируют) таким образом, что бы в лунке панели для микрокультивирования оказалась одна клетка, дающая начало клону. После размножения клеток оценивают их способность синтезировать нужные антитела (проводят скрининг). Клонирование повторяют. В конечном итоге выбирают стабильный клон, продуцирующий антитела заданной специфичности. Моноклониальные антитела выделяют либо из культуральной жидкости (клетки гибридомы выращивают in vitro), либо из асцитической (выращивание in vivo). Моноклональные антитела используют для диагностики инфенкционных болезней в иммуноферментном, радиоиммунном и иммуннофлуоресцентном анализе.
Получение моноклональных антител включает в себя несколько этапов: 1. Известным антигеном иммунизируют животных. Затем из селенки выделяют В-лимфоциты. 2. Проводят слияние (гибридизация) В-лимфоцитов и миеломных клеток. Получают смесь лимфоцитов гибридных и миеломных клеток. 3. Смесь клеток культивируют в среде, содержащей ГАТ (гипосксантинаминоптерин-тимидин), что приводит к гибели лимфоцитов и миеломных клеток, т. к. на указанной среде могут расти только гибридомы. 4. Гибридомные клетки рассевают (клонируют) таким образом, что бы в лунке панели для микрокультивирования оказалась одна клетка, дающая начало клону. После размножения клеток оценивают их способность синтезировать нужные антитела (проводят скрининг). Клонирование повторяют. В конечном итоге выбирают стабильный клон, продуцирующий антитела заданной специфичности. Моноклониальные антитела выделяют либо из культуральной жидкости (клетки гибридомы выращивают in vitro), либо из асцитической (выращивание in vivo). Моноклональные антитела используют для диагностики инфенкционных болезней в иммуноферментном, радиоиммунном и иммуннофлуоресцентном анализе.
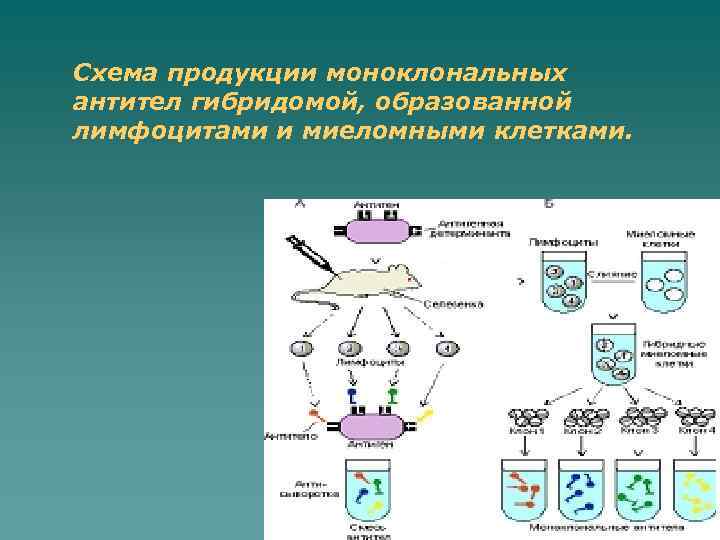 Схема продукции моноклональных антител гибридомой, образованной лимфоцитами и миеломными клетками.
Схема продукции моноклональных антител гибридомой, образованной лимфоцитами и миеломными клетками.
 Моноклональные антитела возле клетки Моноклон альные антитела Клетка
Моноклональные антитела возле клетки Моноклон альные антитела Клетка
 Диагностические антигены Предназначены для серодиагностики инфекционных болезней животных. В зависимости от типа серологической реакции антигены могут быть корпускулярными (РА, РСК), на носителях (эритроцитарные антигенные диагностикумы для РНГА, антигены на частицах латекса и т. д), растворимые (РП, РДП). Технология приготовления антигенов разнообразна, но основа для антигенов любого типа служат исходные селикционированные, без признаков диссоциации штаммов микроорганизмов.
Диагностические антигены Предназначены для серодиагностики инфекционных болезней животных. В зависимости от типа серологической реакции антигены могут быть корпускулярными (РА, РСК), на носителях (эритроцитарные антигенные диагностикумы для РНГА, антигены на частицах латекса и т. д), растворимые (РП, РДП). Технология приготовления антигенов разнообразна, но основа для антигенов любого типа служат исходные селикционированные, без признаков диссоциации штаммов микроорганизмов.
 Контроль диагностических антигенов проводят по следующим показателям. Контроль стерильности. Антиген для серологических реакций должен находиться в определенной оптимальной концентрации, выраженной, например, количеством микробных клеток в 1 мл. Активность антигена определяют в той или иной серологической реакции с заведомо положительной сывороткой. специфичность антигена испытывают в серологической реакции с заведомо отрицательной сывороткой. Корпускулярные антигены для серологических реакции осадочного типа контролируют на спонтанную агглютинацию- выпадение в осадок в отсутствие антител.
Контроль диагностических антигенов проводят по следующим показателям. Контроль стерильности. Антиген для серологических реакций должен находиться в определенной оптимальной концентрации, выраженной, например, количеством микробных клеток в 1 мл. Активность антигена определяют в той или иной серологической реакции с заведомо положительной сывороткой. специфичность антигена испытывают в серологической реакции с заведомо отрицательной сывороткой. Корпускулярные антигены для серологических реакции осадочного типа контролируют на спонтанную агглютинацию- выпадение в осадок в отсутствие антител.
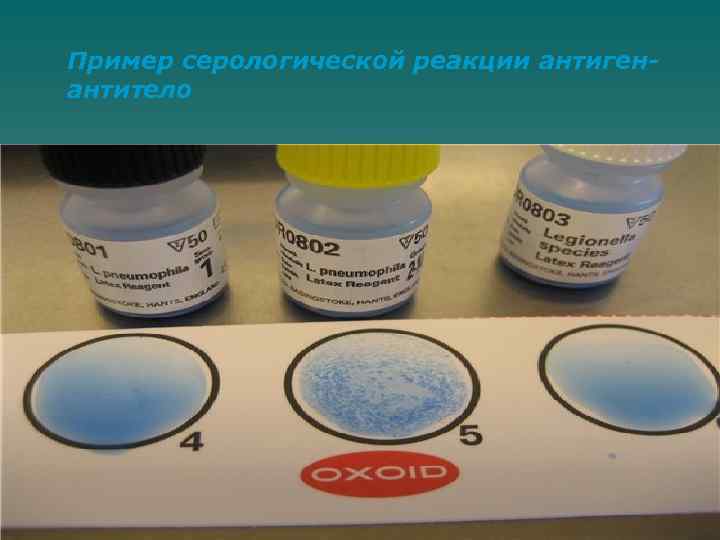 Пример серологической реакции антигенантитело
Пример серологической реакции антигенантитело
 Диагностические аллергены Данные биопрепараты (бруцеллин, туберкуллин, маллеин) представляют собой экстракты из клеток возбудтителя. В основе аллергических диагностических тестов лежит специфическая реакция иммунного воспаления на месте инъекции (аппликации) аллергена. Контроль диагностических аллергенов проводят по: -контролю стерильности -контролю безвредности -контроль специфичности
Диагностические аллергены Данные биопрепараты (бруцеллин, туберкуллин, маллеин) представляют собой экстракты из клеток возбудтителя. В основе аллергических диагностических тестов лежит специфическая реакция иммунного воспаления на месте инъекции (аппликации) аллергена. Контроль диагностических аллергенов проводят по: -контролю стерильности -контролю безвредности -контроль специфичности