СЛОЖНЫЕ БЕЛКИ.pptx
- Количество слайдов: 113

Классификация и структура сложных белков 1. Свойства белков 2. Структура белков, типы связей 3. Классификация сложных белков 4. Нуклеопротеиды, хромопротеиды. Структура и функции. 5. Гемоглобин К свойствам белков относят амфотерность, растворимость, способность к денатурации, коллоидные свойства.
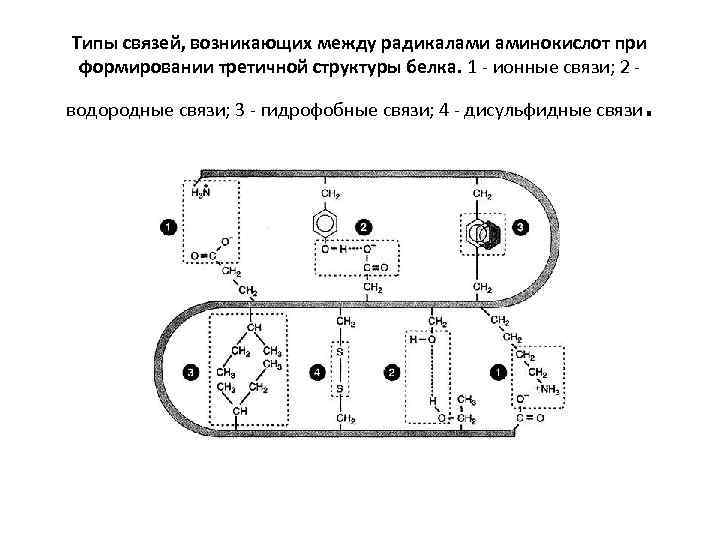
Типы связей, возникающих между радикалами аминокислот при формировании третичной структуры белка. 1 - ионные связи; 2 водородные связи; 3 - гидрофобные связи; 4 - дисульфидные связи .
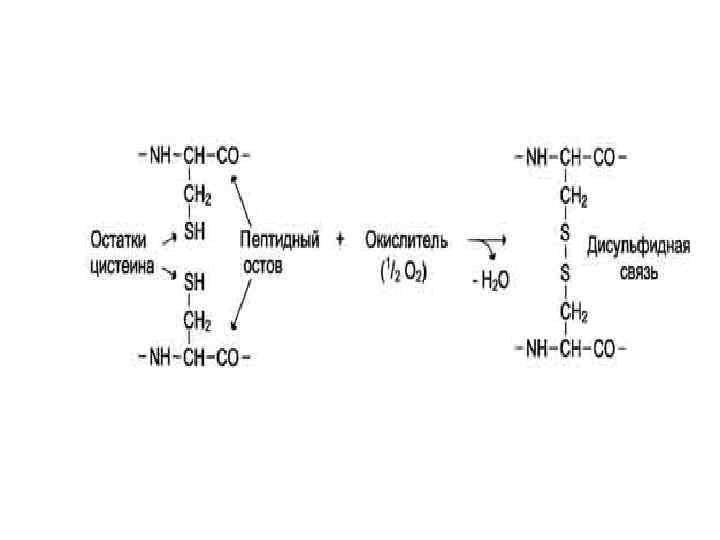

Супервторичная структура белков • Пространственная структура каждого белка определяется его первичной структурой. Однако сравнение конформаций разных по структуре и функциям белков выявило наличие у них похожих сочетаний элементов вторичной структуры. Такой специфический порядок формирования вторичных структур называют супервторичной структурой белков, формируется за счёт межрадикальных взаимодействий. • Они имеют специфические названия: "альфа-спиральповорот-альфа-спираль" (многие ДНК-связывающие белки), "структура альфа/бета-бочонка" (некоторые ферменты: триозофосфатизомераза), "лейциновая застёжка-молния" (гистоны), "цинковый палец" ( ДНКсвязывающие белки ) и др.

Формирование трёхмерной структуры белков • Процесс сворачивания полипептидной цепи в правильную пространственную структуру получил название "фолдинг белков". • Однако в клетке концентрация белков настолько высока, что существует большая вероятность взаимодействия белков с несформированной конформацией. На их поверхности располагаются гидрофобные радикалы, склонные к объединению. Поэтому для многих белков, имеющих высокую молекулярную массу и сложную пространственную структуру, фолдинг протекает при участии специальной группы белков, которые называют "шапероны" (от франц. shaperon - няня).

Классификации шаперонов (Ш) • • • В соответствии с молекулярной массой все шапероны можно разделить на 6 основных групп: высокомолекулярные, с молекулярной массой от 100 до 110 к. Д; Ш-90 - с молекулярной массой от 83 до 90 к. Д; Ш-70 - с молекулярной массой от 66 до 78 к. Д; Ш-60; Ш-40; низкомолекулярные шапероны с молекулярной массой от 15 до 30 к. Д.

Конститутивные белки (синтез которых не зависит от стрессовых воздействий на клетки организма), Индуцибельные ("белкам теплового шока"), синтез при стрессовых воздействиях на клетку резко увеличивается.
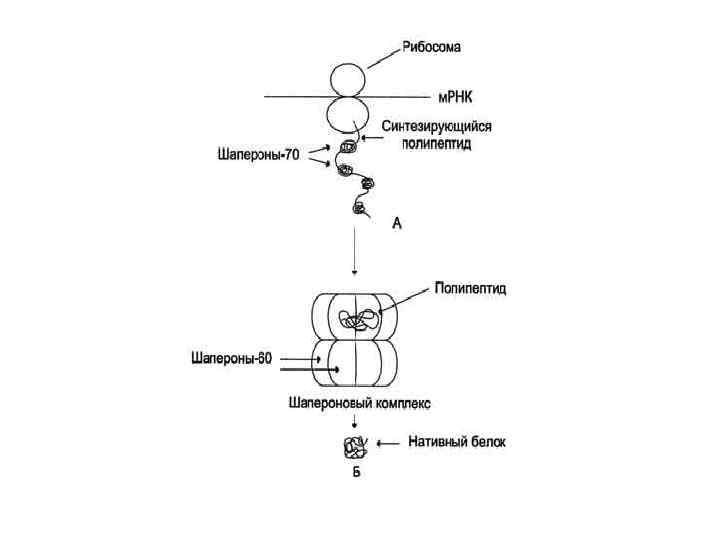

Ш-70 - высококонсервативный класс белков, присутствует во всех отделах клетки: цитоплазме, ядре, ЭР, митохондриях. В области карбоксильного конца единственной полипептидной цепи шаперонов есть участок, образованный радикалами аминокислот в форме бороздки. Он способен взаимодействовать с участками белковых молекул и развёрнутых полипептидных цепей длиной в 7 -9 аминокислот, обогащённых гидрофобными радикалами. В синтезирующейся полипептидной цепи такие участки встречают примерно через каждые 16 аминокислот.

Фолдинг многих высокомолекулярных белков, имеющих сложную конформацию (например, доменное строение), осуществляется в специальном пространстве, сформированном Ш-60 функционируют в виде олигомернoго комплекса, состоящего из 14 субъединиц. В специфической среде, в изоляции от других молекул клетки происходит перебор возможных конформаций белка, пока не будет найдена единственная, энергетически наиболее выгодная конформация .

Болезни, связанные с нарушением фолдинга белков • Некоторые растворимые в воде белки при изменении условий могут приобретать конформацию плохо растворимых, способных к агрегации молекул, образующих в клетках фибриллярные отложения - амилоид (от лат. amylum крахмал). • В результате нарушаются структура и функция клеток, наблюдают их дегенеративные изменения. Развиваются болезни, называемые амилоидозами. Для каждого вида амилоидоза характерен определённый тип амилоида. В настоящее время описано более 15 таких болезней.

Болезнь Альцгеймера - наиболее часто отмечаемый бета-амилоидоз нервной системы, как правило, в преклонном возрасте. Характеризуюется прогрессирующим расстройством памяти и полной деградацией личности. В ткани мозга откладывается бета-амилоид - белок, образующий нерастворимые фибриллы, нарушающие структуру и функции нервных клеток, бета-амилоид - продукт изменения конформаций нормального белка организма человека.

Прионы (proteinaceous infectious particle - белковая инфекционная частица) - особый класс белков, обладающих инфекционными свойствами. Попадая в организм человека или спонтанно возникая в нём, они способны вызывать тяжёлые неизлечимые заболевания ЦНС, называемые прионовыми болезнями.

Прионовый белок: - кодируется тем же геном, что и его нормальный аналог, т. е. имеет идентичную первичную структуру, но обладает другой конформацией: характеризуется высоким содержанием бета-слоёв, в то время как нормальный белок имеет много альфаспиральных участков - обладает устойчивостью к действию протеаз и, попадая в ткань мозга или образуясь там спонтанно, способствует превращению нормального белка в прионовый в результате межбелковых взаимодействий.

Куру - прионовая болезнь аборигенов Новой Гвинеи, эпидемический характер которой связан с традиционным каннибализмом в этих племенах и передачей инфекционного белка от одной особи к другой. Заражением людей прионами может происходить при употреблении мясопродуктов, полученных от животных, являющихся носителями прионов, вызывающих "бешенство коров" (болезнь Кройтцфельдта-Якоба).

Конформационная лабильность белков - склонностью к небольшим изменениям конформации за счёт разрыва одних и образования других слабых связей. Белки состоят из огромного числа атомов, находящихся в постоянном (броуновском) движении, что приводит к небольшим перемещениям отдельных участков полипептидной цепи, которые обычно не нарушают общую структуру белка и его функции. Конформация белка может меняться при изменении химических и физических свойств среды, а также при взаимодействии белка с другими молекулами. При этом происходит изменение пространственной структуры не только участка, контактирующего с другой молекулой, но и конформации белка в целом.

денатурация Все белки с одинаковой первичной структурой, находящиеся в одинаковых условиях, приобретают одинаковую, характерную для данного индивидуального белка конформацию, определяющую его специфическую функцию. Функционально активную конформацию белка называют "нативная структура". • Потеря нативной конформации сопровождается утратой специфической функции белков. Этот процесс носит название денатурации белков.

Факторы, вызывающие денатурацию белков: - высокая t 0 (более 50 0 С), - интенсивное встряхивание раствора, - органические вещества (С 2 Н 5 ОН …), - кислоты и щелочи, - соли тяжелых металлов, - детергенты (различные мыла).

Доменная структура белков Если полипептидная цепь белка содержит более 200 аминокислот, как правило, её пространственная структура сформирована в виде двух или более доменов. Домен - участок полипептидной цепи, который в процессе формирования пространственной структуры приобрёл независимо от других участков той же цепи конформацию глобулярного белка (лёгкая цепь иммуноглобулина G состоит из двух доменов).

Четвертичная структура белка. Комплементарность протомеров. Количество и взаиморасположение полипептидных цепей в пространстве называют "четвертичная структура белков". Отдельные полипептидные цепи в таком белке носят название протомеров, или субъединиц. Белок, содержащий в своём составе несколько протомеров, называют олигомерным (гексокиназа – 2 протомера, лактатдегидрогеназа – 4 протомера). Присоединение отдельных протомеров олигомерного белка происходят благодаря формированию на их поверхности контактных участков. Специфичность связывания контактных участков определяется их комплементарностью. Комплементарность - пространственное и химическое соответствие взаимодействующих поверхностей.

Функционирование белков. У сложных белков, кроме белковой цепи, имеется дополнительная небелковая группа. Она называется лиганд (лат. ligo - связываю), то есть молекула, связанная с белком. В случае если лиганд несет структурную и/или функциональную нагрузку, он называется простетической группой

В роли лиганда могут выступать любые молекулы: • молекулы, выполняющие в белке структурную функцию – липиды, углеводы, нуклеиновые кислоты, минеральные элементы, какие-либо другие органические соединения: гем в гемоглобине, углеводы в гликопротеинах, ДНК и РНК в нуклеопротеинах, медь в церулоплазмине, • переносимые белками молекулы: железо в трансферрине • субстраты для ферментов – любые молекулы и даже другие белки.

Узнавание лиганда обеспечивается: • комплементарностью структуры центра связывания белка структуре лиганда, они подходят друг к другу как ключ к замку: соответствие фермента и субстрата, • иногда узнавание может зависеть от реакционной способности атома, к которому присоединяется лиганд: связывание кислорода железом гемоглобина, или жирной кислоты с альбумином.

Функции лиганда в составе сложного белка разнообразны: • изменяет свойства белков (заряд, растворимость, термолабильность): фосфорная кислота в фосфопротеинах или остатки моносахаридов в гликопротеинах, • защищает белок от протеолиза вне и внутри клетки: углеводная часть в гликопротеинах, • в виде лиганда обеспечивается транспорт нерастворимых в воде соединений: перенос жиров липопротеинами, • придает биологическую активность и определяет функцию белка: нуклеиновая кислота в нуклеопротеинах, гем в гемоглобине, углевод в рецепторных белках, • влияет на проникновение через мембраны, внутриклеточную миграцию, сортировку и секрецию белков. Это выполняет, как правило, углеводный остаток.

Активный центр белков - определённый участок белковой молекулы, как правило, находящийся в её углублении ("кармане"), сформированный радикалами аминокислот, собранных на определённом пространственном участке при формировании третичной структуры и способный комплементарно связываться с лигандом. В линейной последовательности полипептидной цепи радикалы, формирующие активный центр, могут находиться на значительном расстоянии друг от друга.

Между функциональными группами лиганда и радикалами аминокислот, образующих активный центр, должны возникать связи, удерживающие лиганд в активном центре. Связи между лигандом и активным центром белка могут быть как нековалентными (ионными, водородными, гидрофобными), так и ковалентными.

Скорость взаимодействия белка с лигандом определяется концентрациями белка и лиганда в растворе, а также степенью комплементарности белка и лиганда. Константа диссоциации - характеристика сродства активного центра лиганду

Так как взаимодействие белка с лигандом обратимый процесс, то его можно описать следующим уравнением: где Р - белок, L - лиганд, PL - комплекс белка с лигандом, К 1 - константа скорости связывания белка с лигандом, К-1 константа скорости распада комплекса PL.

Когда скорости образования и распада комплекса равны, говорят о том, что система находится в состоянии равновесия: [P] [L] K 1 = [PL] K-1. Отсюда: Kдисс = K -1 / K 1 = [P][L] / [PL]
![Соотношение констант распада [PL] комплекса и его образования называется константой диссоциации (Кдисс) комплекса [PL]. Соотношение констант распада [PL] комплекса и его образования называется константой диссоциации (Кдисс) комплекса [PL].](https://present5.com/presentation/6343375_65879675/image-30.jpg)
Соотношение констант распада [PL] комплекса и его образования называется константой диссоциации (Кдисс) комплекса [PL]. Чем меньше Кдисс, тем больше молекул лиганда связано с белком, тем больше комплементарность между Р и L и тем больше сродство лиганда к белку. То есть между Кдисс и сродством лиганда к белку имеется обратно пропорциональная связь. Иногда при описании процесса связывания белка с лигандом используют величину, обратную Кдисс, называемую константой связывания (Ксв) или ассоциации. Kсв = 1 / Kдисс = [PL] / [P][L] Между Ксв и сродством лиганда к белку существует прямо пропорциональная зависимость.

Сложный белок, состоящий из белковой части (апопротеин) и небелковой (простетической группы), называют «холопротеин» .

В зависимости от характера простетической группы все сложные белки подразделяются на 6 классов: • Гликопротеины (углевод + белок) • Липопротеины (липиды + белок) • Металлопротеины (металл+ белок) • Фосфопротеины (фосфор+ белок) • Нуклеопротеины (нуклеиновая кислота+ белок) • Хромопротеины (окрашенный компонент + белок)

Гликопротеины (гликоконъюгаты) – это белки, содержащие углеводный компонент, ковалентно присоединенный к полипептидной основе. Содержание углеводов в них варьирует от 1 до 85% по массе. Выделяют два подкласса белков, содержащих углеводы: протеогликаны и гликопротеины: Гликопротеины Протеогликаны доля углеводов 15 -20%, не содержат уроновых кислот, доля углеводов 80 -85%, углеводные цепи содержат не более 15 звеньев, имеются уроновые кислоты, углеводные цепи крайне велики, углевод имеет регулярное строение. углевод строение. имеет нерегулярное
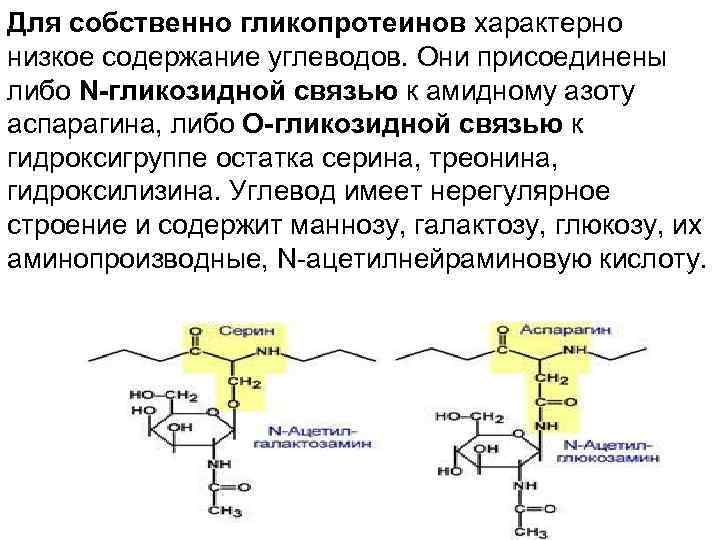
Для собственно гликопротеинов характерно низкое содержание углеводов. Они присоединены либо N-гликозидной связью к амидному азоту аспарагина, либо О-гликозидной связью к гидроксигруппе остатка серина, треонина, гидроксилизина. Углевод имеет нерегулярное строение и содержит маннозу, галактозу, глюкозу, их аминопроизводные, N-ацетилнейраминовую кислоту.

Функцией гликопротеинов являются: 1. Структурная – клеточная стенка бактерий, костный матрикс, например, коллаген, эластин. 2. Защитная – например, антитела, интерферон, факторы свертывания крови (протромбин, фибриноген) 3. Рецепторная – присоединение эффектора приводит к изменению конформации белка-рецептора, что вызывает внутриклеточный ответ. 4. Гормональная – гонадотропный, адренокортикотропный и тиреотропный гормоны. 5. Ферментативная – холинэстераза, нуклеаза. 6. Транспортная – перенос веществ в крови и через мембраны, например, трансферрин, транскортин, альбумин, Na+, К+-АТФаза
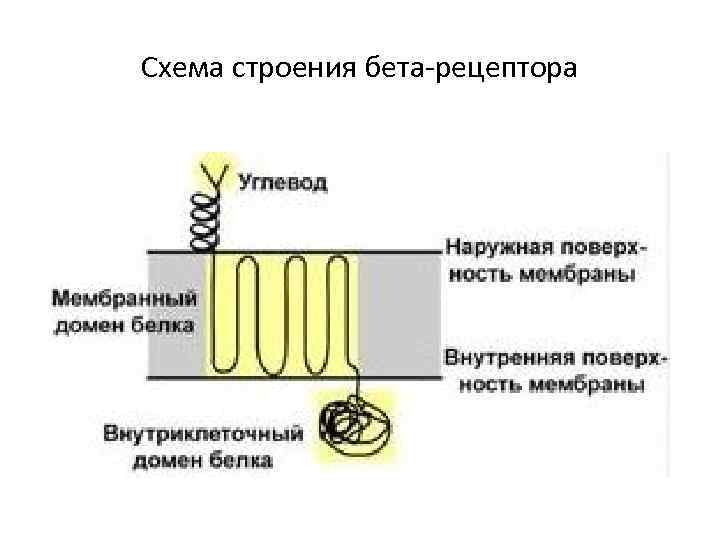
Схема строения бета-рецептора

• ЗАЩИТНЫЕ БЕЛКИ. А. Интерфероны – ингибиторы размножения вирусов. Небольшие сложные белки с массой от 25 тысяч до 40 тысяч. Они образуются в клетке в ответ на вирусную инфекцию. Б. Иммуноглобулины, или антитела, - специфические белки, вырабатываемые Влимфоцитами в ответ на попадание в организм чужеродных структур, называемых антигенами. В организме человека вырабатывается около 107 клонов В-лимфоцитов, каждый из которых специализирован на выработке одного из 107 видов иммуноглобулинов.

Выделяют 5 классов иммуноглобулинов: Ig G, Ig M, Ig A, Ig D, Ig E Различаются по молекулярной массе, концентрации в крови, характеризуются общим планом строения. Лучше изучена группа Ig G.
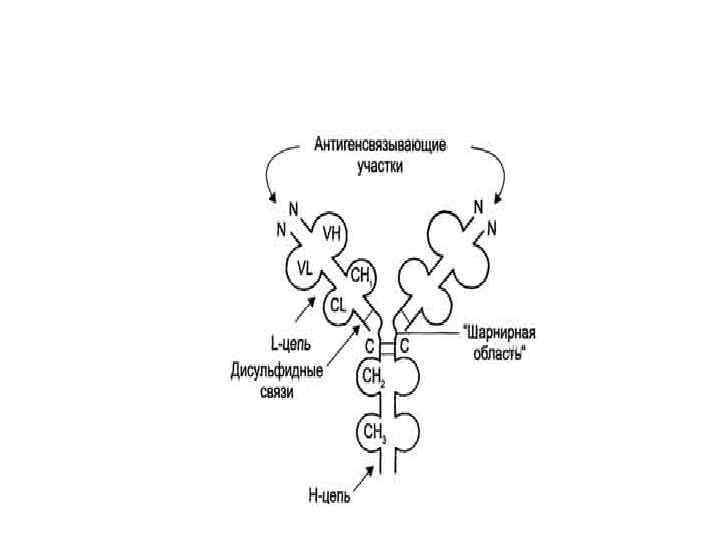

Молекула Ig. G состоит из четырёх полипептидных цепей: двух идентичных лёгких (L - от англ, light), содержащих около 220 аминокислотных остатков, и двух тяжёлых (Н - от англ. heavy), состоящих из 440 аминокислот каждая. Все 4 цепи соединены друг с другом множеством нековалентных и четырьмя дисульфидными связями. Поэтому молекулу Ig. G относят к мономерам. В шарнирной области располагается пролин.

В количественном отношении Ig. G доминируют в крови и составляют около 75% от общего количества этих белков; секретируется активированными Влимфоцитами в больших количествах при вторичном иммунном ответе, когда антиген повторно попадает в организм. Ig. G - единственный класс антител, способный проникать через плацентарный барьер и обеспечивать внутриутробную защиту плода от инфекций.

Когда В-лимфоциты впервые встречаются в жидкостях организма с неизвестным ранее антигеном, они синтезируют и секретируют в кровь Ig. M. Если антиген расположен на поверхности микроорганизма, то как следствие, происходит нарушение целостности клеточной мембраны и гибель бактериальной клетки. Ig. A - основной класс антител, присутствующий в секретах желёз организма (слюны, молока, пищеварительного сока, секретов дыхательных путей). В сыворотке крови его содержание не превышает 10 -15% от общего количества иммуноглобулинов. Образующийся при взаимодействии Ig. A с антигеном препятствует прикреплению антигенов к поверхности эпителиальных клеток и проникновению их в организм. Ig. Е - содержание этого класса иммуноглобулинов в крови крайне мало, связываются с соответствующими рецепторами на поверхности тучных клеток и базофилов. В результате они становятся рецепторами антигенов на поверхности данных клеток. После присоединения антигена клетка получает сигнал к секреции биологически активных веществ (серотонина, гистамина), хранящихся в секреторных пузырьках. Выброс этих веществ в значительной мере ответственен за развитие воспалительной реакции, а также таких аллергических реакций, как бронхиальная астма, крапивница, сенная лихорадка. Увеличение количества Ig. E может предшествовать развитию аллергических реакций. Ig. D обнаружены в крови в очень малых количествах. Мономерные белки играют роль рецепторов В-лимфоцитов; других функций у Ig. D пока не выявлено.

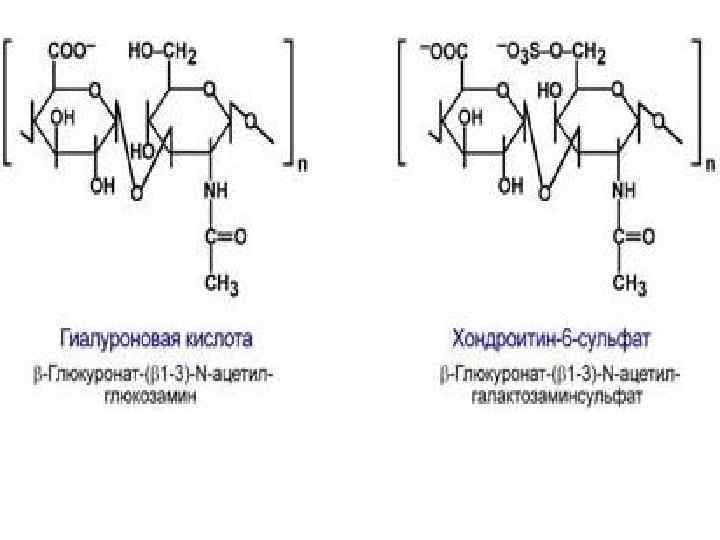
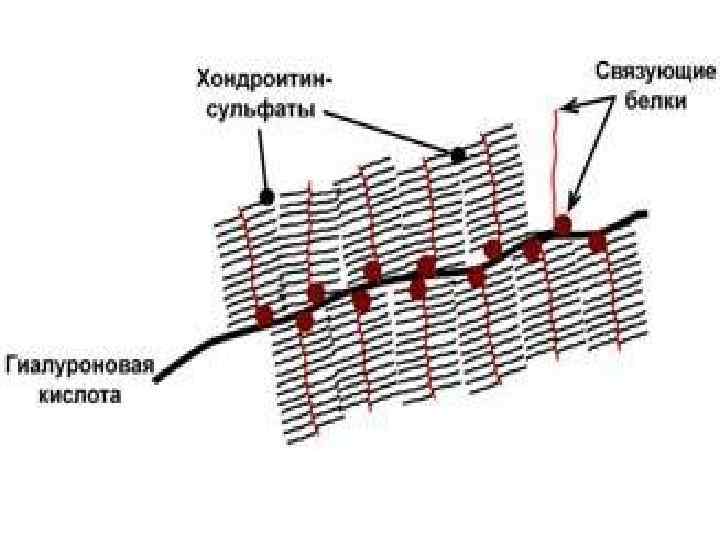
Протеогликаны – характеризуется наличием крупных полисахаридов, состоящих из повторяющихся дисахаридных остатков. Дисахариды включают в себя какую-либо уроновую кислоту и аминосахар. Дисахариды образуют олиго- и полисахаридные цепи – гликаны. Для углеводной части встречаются другие названия – кислые гетерополисахариды(т. к. имеют много кислотных групп), гликозаминогликаны (содержат аминогруппы). Основными представителями гликозаминогликанов являются гиалуроновая кислота, хондроитинсульфаты, кератансульфаты и дерматансульфаты, гепарин. Эти молекулы входят в состав протеогликанов, функцией которых является заполнение межклеточного пространства и удержание здесь воды, также они выступают как смазочный и структурный компонент суставов и других тканевых структур.

ЛИПОПРОТЕИНЫ. Небелковой частью этих белков является жир или жирные кислоты, фосфолипиды, холестерин. Широко распространены: входят в клеточные мембраны, в нервную ткань, палочки и колбочки сетчатки. Их много в сыворотке крови. Т. к. жиры не растворяются в водных растворах, они транспортируются по крови в виде липопротеиновых комплексов, в которых снаружи белковая оболочка, а внутри – жировое содержимое. Такая частица из-за белка снаружи, становится растворимой и может транспортироваться по крови. Липопротеины синтезируются в печени и имеют разное соотношение белка и липида.

Чем больше белка, тем выше плотность липопротеина. Различают липопротеины высокой плотности (ЛПВП) – 40% белка и 60% липида. ЛПОНП (липопротеины очень низкой плотности 2% белка и 98%липида). Липопротеины имеют огромное клиническое значение К липопротеинам, строго говоря, принадлежат только белки, содержащие ковалентно связанные липиды. Однако традиционно к липопротеинам относят и надмолекулярные образования, переносящие липиды в плазме крови, и состоящие из белков и молекул всех классов липидов.

Структуру транспортных липопротеинов можно сравнить с орехом, у которых имеется скорлупа и ядро. "Скорлупа" липопротеина является гидрофильной, ядро – гидрофобное. Ядро формируют неполярные эфиры холестерола (ХС) и триацилглицеролы (ТАГ). В поверхностном слое ("скорлупе") находятся фосфолипиды, холестерол, белки. Белки в липопротеинах называются апобелками, их выделяют несколько видов: А, В, С, D. В каждом типе липопротеинов преобладают соответствующие ему апобелки.
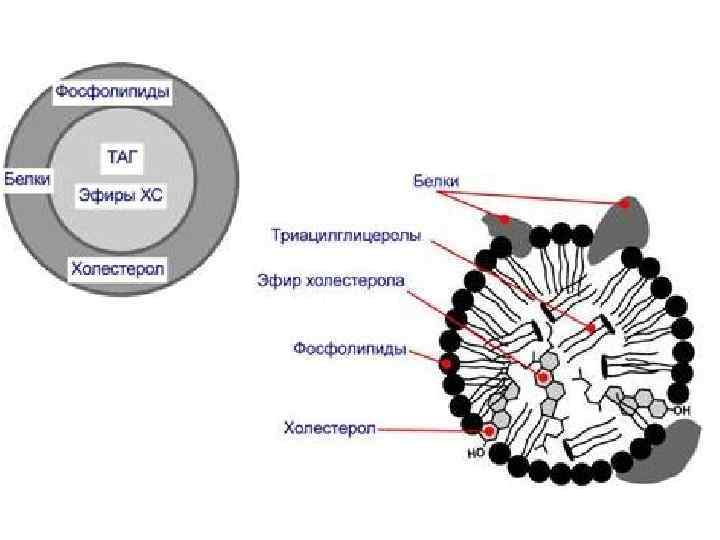

Выделяют четыре основных класса липопротеинов: • липопротеины высокой плотности (ЛПВП, αлипопротеины, α-ЛП), • липопротеины низкой плотности (ЛПНП, βлипопротеины, β-ЛП), • липопротеины очень низкой плотности (ЛПОНП, пре-βлипопротеины, пре-β-ЛП), • хиломикроны (ХМ). Концентрация и соотношение в крови тех или иных липопротеинов играют ведущую роль в возникновении такой распространенной сосудистой патологии как атеросклероз. Свойства и функции липопротеинов разных классов зависят от состава, т. е. от соотношения триацилглицеролов, холестерола и его эфиров, фосфолипидов, белков:

Функцией липопротеинов является перенос в крови триацилглицеролов и холестерола и его эфиров. По составу и количеству липопротеинов крови осуществляют диагностику. Типы липопротеинов Хиломикроны (до 90% липидов) ЛПОНП ЛПВП (до 80% белков) По направлению сверху вниз происходят изменения состава Увеличение количества белка Увеличение количества фосфолипидов Уменьшение количества

У сложных белков, кроме белковой цепи, имеется дополнительная небелковая группа. Она называется лиганд (лат. ligo - связываю), то есть молекула, связанная с белком. В случае если лиганд несет структурную и/или функциональную нагрузку, он называется простетической группой. В роли лиганда могут выступать любые молекулы: • молекулы, выполняющие в белке структурную функцию – липиды, углеводы, нуклеиновые кислоты, минеральные элементы, какие-либо другие органические соединения: гем в гемоглобине, углеводы в гликопротеинах, ДНК и РНК в нуклеопротеинах, медь в церулоплазмине, • переносимые белками молекулы: железо в трансферрине, гемоглобин в гаптоглобине, гем в гемопексине, • субстраты для ферментов – любые молекулы и даже другие белки. Узнавание лиганда обеспечивается: • комплементарностью структуры центра связывания белка структуре лиганда, иначе говоря, пространственным и химическим соответствием белка и лиганда. Они подходят друг к другу как ключ к замку, например, соответствие фермента и субстрата, • иногда узнавание может зависеть от реакционной способности атома, к которому присоединяется лиганд. Например, связывание кислорода железом гемоглобина, или жирной кислоты с альбумином. Функции лиганда в составе сложного белка разнообразны: • изменяет свойства белков (заряд, растворимость, термолабильность), например, фосфорная кислота в фосфопротеинах или остатки моносахаридов в гликопротеинах, • защищает белок от протеолиза вне и внутри клетки, например углеводная часть в гликопротеинах, • в виде лиганда обеспечивается транспорт нерастворимых в воде соединений, например, перенос жиров липопротеинами, • придает биологическую активность и определяет функцию белка, например, нуклеиновая кислота в нуклеопротеинах, гем в гемоглобине, углевод в рецепторных белках, • влияет на проникновение через мембраны, внутриклеточную миграцию, сортировку и секрецию белков. Это выполняет, как правило, углеводный остаток.

МЕТАЛЛОПРОТЕИНЫ. Если в белке содержатся ионы одного или нескольких металлов, то такие белки называются металлопротеины. Ионы металлов соединены координационными связями с функциональными группами белка. А) белки, содержащие негемовое железо, Б) белки-ферменты, содержащие металл.

А. Ферритин – водорастворимый, глобулярный белок, 24 субъединицы, внутриклеточное депо Fe ( растворимость Fe – 10 -18 М, ферритина – 10 -4 М, что в 100 триллионов выше!). Обнаруживается во всех тканях и жидкостях организма

2. Трансферрины. Водорастворимый. Белки плазмы крови, прочно, но обратимо связывают Fe (около 0, 1% ~ 4 мг, молекулярная масса ~ 80 к. Да, состоит из 679 АК). Основной источник – печень. Функция – транспорт Fe из центров поглощения в двенадцатиперстной кишке и разрушения эритроцитов (печень, селезенка, костный мозг). 3. Гемосидерин. Водонерастворимый комплекс белка с железом. Содержит много (около 30%) Fe. Постоянно обнаруживается в клетках селезенки, печени, костного мозга и лимфатических узлах; в межклеточном веществе подвергается фагоцитозу. Темно-желтый пигмент, образуется при распаде гема, аккумуляция гемосидерина в тканях и органах тела происходит при различных заболеваниях.

Б. Ко второй группе металлоферментов относятся белки + металлы. Металлы или входят в активный центр ферментов и участвуют в каталитическом акте, или являются связывающим агентом между разными группами в белке. К ферментативным металлопротеинам относятся белки, содержащие например: • медь – цитохромоксидаза, в комплексе с другими ферментами дыхательной цепи митохондрий участвует в синтезе АТФ, • цинк – алкогольдегидрогеназа, обеспечивающая метаболизм этанола и других спиртов, лактатдегидрогеназа, участвующая в метаболизме молочной кислоты, карбоангидраза, образующая угольную кислоту из CO 2 и H 2 O, щелочная фосфатаза, гидролизующая фосфорные эфиры различных соединений, α 2 -макроглобулин, антипротеазный белок крови. • селен – тиреопероксидаза, участвующая в синтезе гормонов щитовидной железы, антиоксидантный фермент глутатионпероксидаза, • кальций – α-амилаза слюны и панкреатического сока, гидролизующая крахмал.
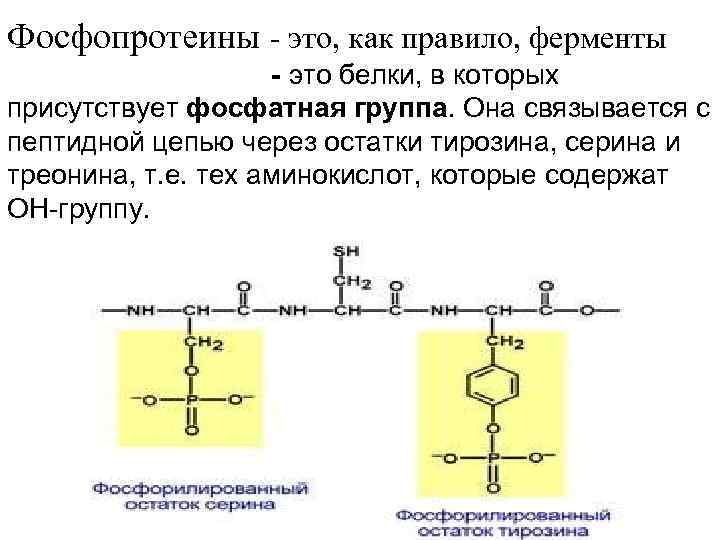
Фосфопротеины - это, как правило, ферменты - это белки, в которых присутствует фосфатная группа. Она связывается с пептидной цепью через остатки тирозина, серина и треонина, т. е. тех аминокислот, которые содержат ОН-группу.

Фосфорная кислота может выполнять: Структурную роль, придавая заряд, растворимость и изменяя свойства белка. Например, в казеине молока (содержание фосфорной кислоты около 1%), вителлин желтка куриного яйца, овальбумин белка куриного яйца, ихтулин икры рыб. . Функциональную роль. В клетке присутствует много белков, которые связаны с фосфатом не постоянно, а в зависимости от активности метаболизма. Белок может многократно переходить в фосфорилированную или в дефосфорилированную форму, что играет регулирующую роль в его работе. Особенность фосфорилированных белков в том, что молекула фосфора активирует весь белок и включает его в обмен веществ.
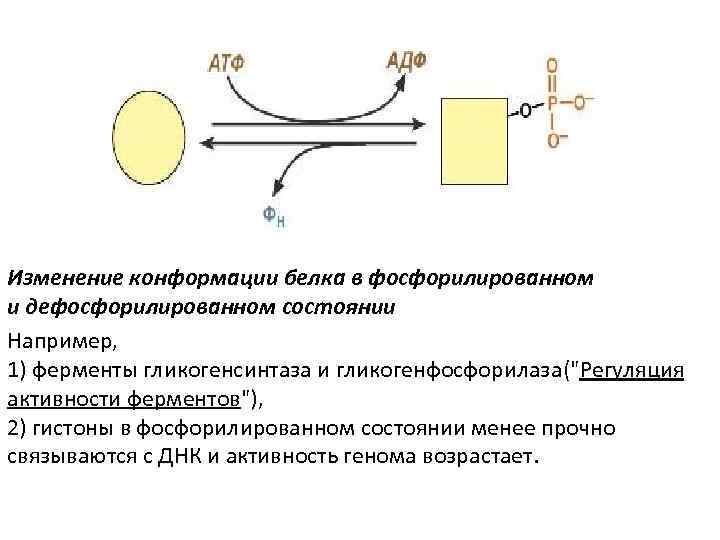
Изменение конформации белка в фосфорилированном и дефосфорилированном состоянии Например, 1) ферменты гликогенсинтаза и гликогенфосфорилаза("Регуляция активности ферментов"), 2) гистоны в фосфорилированном состоянии менее прочно связываются с ДНК и активность генома возрастает.

НУКЛЕОПРОТЕИНЫ: белок + нуклеиновая кислота Составляют существенную часть рибосом, хроматина, вирусов. В хроматине нуклеиновая кислота представлена дезоксирибонуклеиновой кислотой (ДНК) и связана с гистонами. В рибосомах рибонуклеиновая кислота (РНК) связывается со специфическими рибосомальными белками. Вирусы являются практически чистыми рибо- и дезоксирибонуклеопротеинами. Соотношение между белком и нуклеиновой кислотой колеблется от 40% до 60%. Но у некоторых нуклеопротеинов нуклеиновой кислоты всего 2%, например, нуклеопротеин вирусов (2% нуклеиновой кислоты и 98% белка).

Нуклеиновые кислоты являются полимерными молекулами и состоят из мономеров, называемых нуклеотидами. Нуклеотид состоит из 3 частей: • Азотистое основание пуринового или пиримидинового ряда, одно из четырех: • ДНК – аденин, РНК – аденин, цитозин цитозин, гуанин, тимин. урацил. • Сахар – пентоза (рибоза – РНК, дезоксирибоза – ДНК). • Остаток фосфорной кислоты – H 3 PO 4.
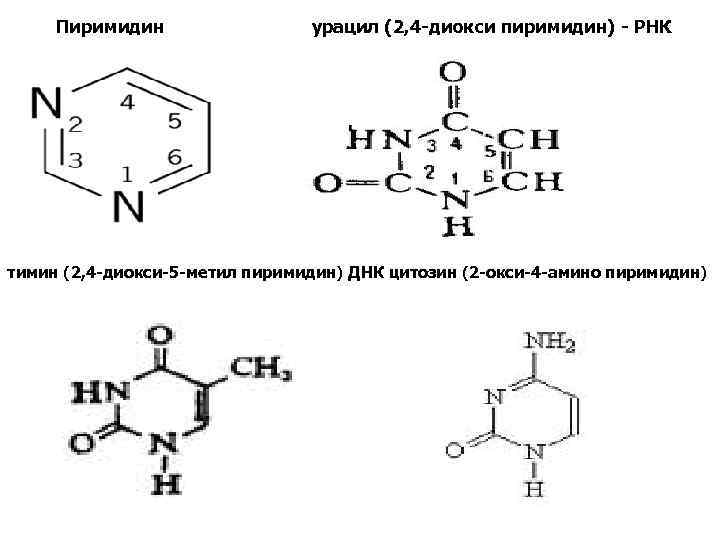
Пиримидин урацил (2, 4 -диокси пиримидин) - РНК тимин (2, 4 -диокси-5 -метил пиримидин) ДНК цитозин (2 -окси-4 -амино пиримидин)
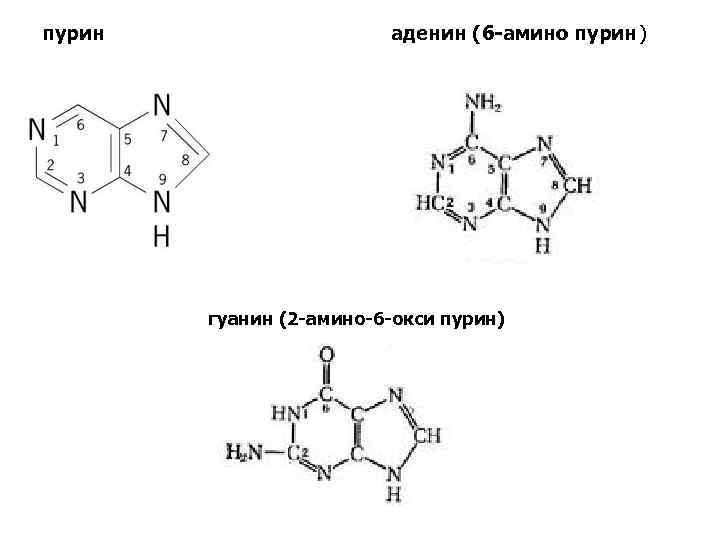
пурин аденин (6 -амино пурин) гуанин (2 -амино-6 -окси пурин)
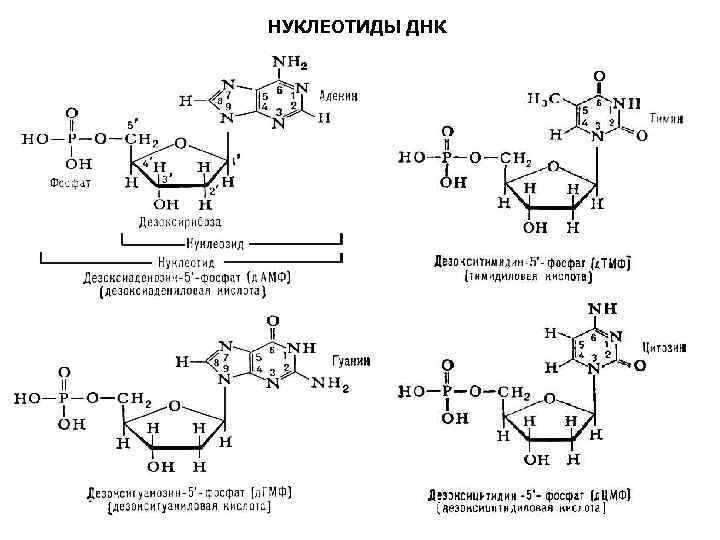
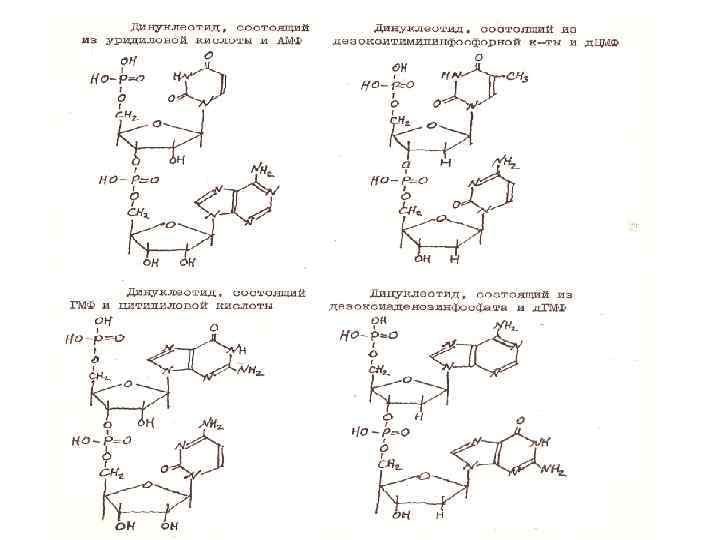
НУКЛЕОТИДЫ ДНК
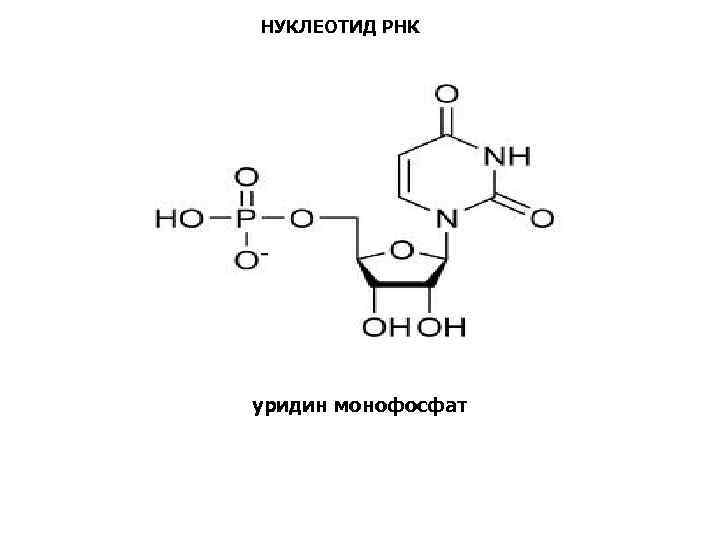
НУКЛЕОТИД РНК уридин монофосфат
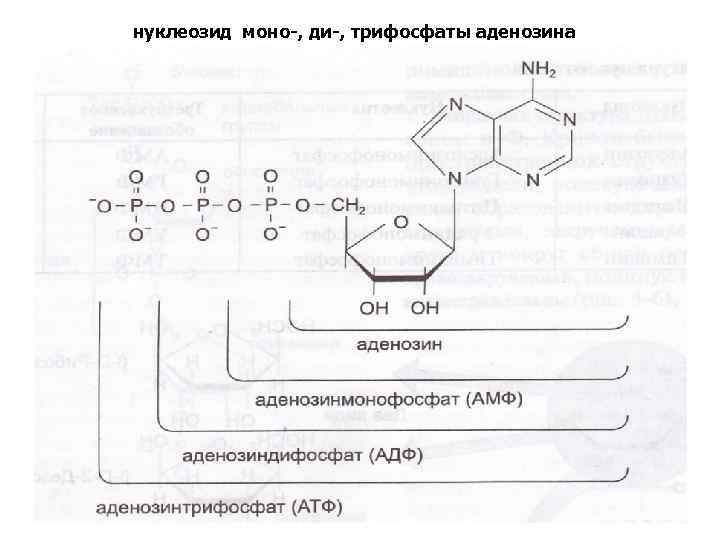
нуклеозид моно-, ди-, трифосфаты аденозина
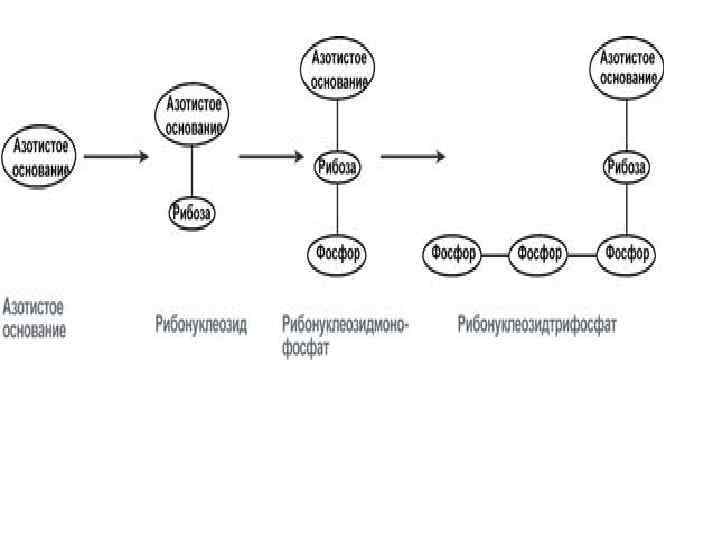

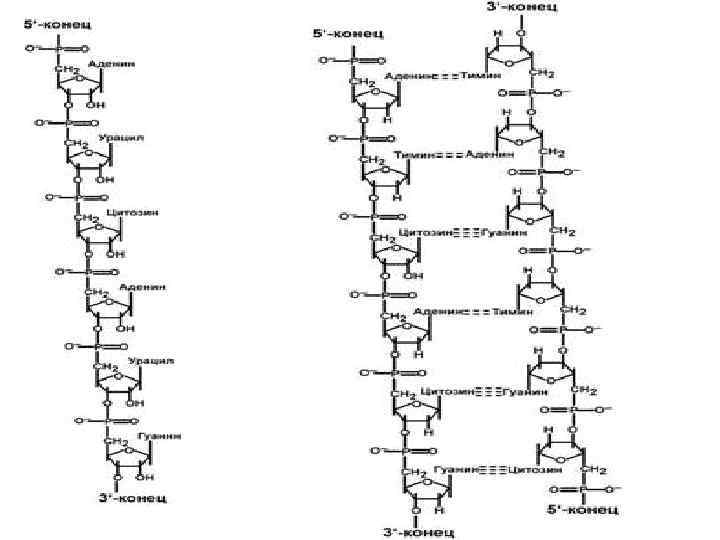
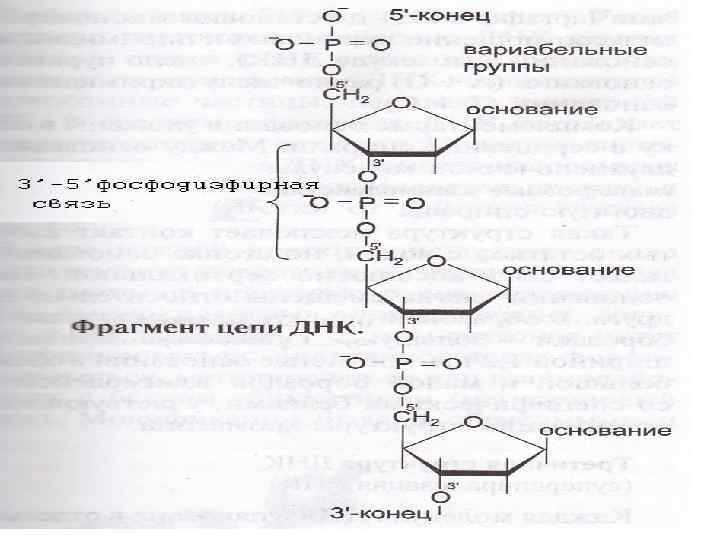
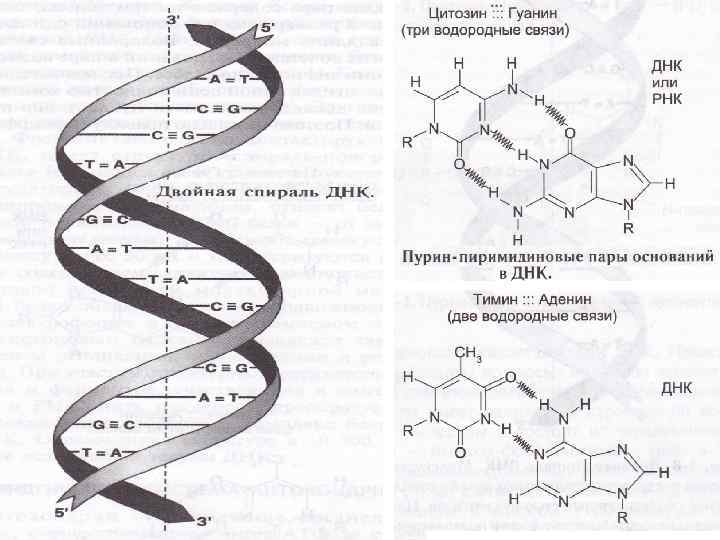
Строение и функции РНК и ДНК Выделяют два вида нуклеиновых кислот в зависимости от пентозы, входящей в их. Сахарофосфатный остов в ДНК и РНК заряжен отрицательно благодаря заряду фосфатных групп. В то же время пуриновые и пиримидиновые основания гидрофобны. Цепи ДНК и РНК обладают направленностью, т. е. имеют 3'конец и 5'-конец. В ДНК цепи антипараллельны, т. е. направлены в разные стороны. Имеется комплементарность азотистых оснований, соответствие аденин комплементарен тимину (А=Т), гуанин комплементарен цитозину (Г=Ц). Синтез цепей ДНК и РНК идет от 5' к 3' концу. На 5’ конце находится фосфатная группа, на 3’ конце – свободный гидроксил.

Отличия между РНК и ДНК: • количество цепей: в РНК одна цепь, в ДНК две цепи, • размеры: ДНК намного крупнее, • локализация в клетке: ДНК находится в ядре, почти все РНК – вне ядра, • вид моносахарида: в ДНК – дезоксирибоза, в РНК – рибоза, • азотистые основания: в ДНК имеется тимин, в РНК – урацил. функция: ДНК отвечает за хранение наследственной информации (а также воспроизведение и мутирование), РНК – за ее реализацию

ХРОМОПРОТЕИНЫ. Белок + небелковый компонент окрашенный. Хромопротеины: • Гемопротеины: - гемоглобин - миоглобин - цитохромы 2. Магнийпорфирины: хлорофилл 3. Флавопротеины: ферменты, содержащие ФАД, ФМН. и др.

• Гемопротеины • Строение гема • Подразделяются на неферментативные (гемоглобин, миоглобин) и ферменты (цитохромы, каталаза, пероксидаза). • Небелковой частью их является гем – структура, включающая в себя порфириновое кольцо (состоящее из 4 пиррольных колец) и иона Fe 2+. Железо связывается с порфириновым кольцом двумя координационными и двумя ковалентными связями.
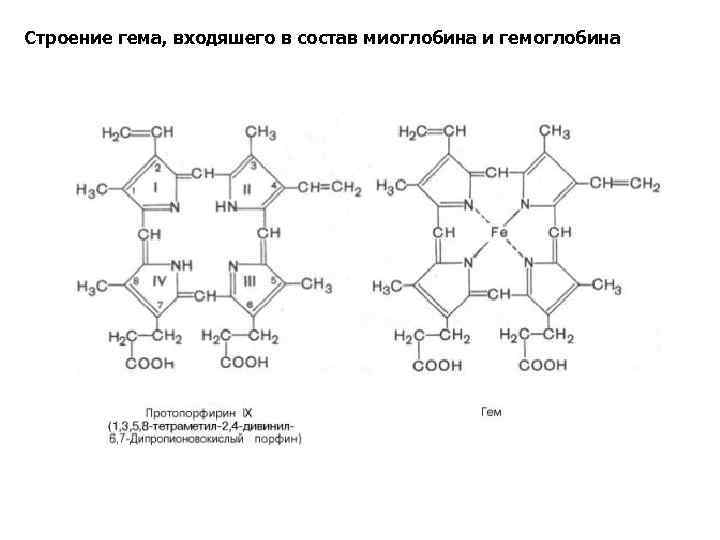
Строение гема, входяшего в состав миоглобина и гемоглобина

Цитохромы отличаются аминокислотным составом пептидных цепей и числом цепей и разделяются на типы а, b, с, d. Все они неспособны связывать кислород, кроме цитохрома а 3, который содержит ионы меди. Цитохромы находятся в составе дыхательной цепи и цепи микросомального окисления. Флавопротеины Являются ферментами окислительновосстановительных реакций, содержат производные витамина В 2 флавинмононуклеотид (ФМН) и флавинадениндинуклеотид (ФАД).

Миоглобин - глобулярный белок, - имеет только одну полипептидную цепь из 153 аминокислот, - содержит небелковую часть (гем) и белковую часть (апомиоглобин - 8 альфа-спиралей от А до Н, начиная с N-конца полипептидной цепи, и содержат от 7 до 23 аминокислот). Миоглобин содержится в красных мышцах и участвует в запасании кислорода. В условиях интенсивной мышечной работы, когда парциальное давление кислорода в ткани падает, О 2 освобождается из комплекса с миоглобином и используется в митохондриях клеток для получения необходимой для работы мышц энергии.

Внутренняя часть молекулы почти целиком состоит из гидрофобных радикалов, за исключением двух остатков Гис (Гис64 и Гис93 или Гис Е 7 и Гис F 8), располагающихся в активном центре. Они расположены по разные стороны от плоскости тема и входят в состав спиралей F и Е, между которыми располагается гем. Fe 2+ может образовывать 6 координационных связей, 4 из которых удерживают Fe 2+ в центре протопорфирина IX (соединяя его с атомами азота пиррольных колец), а 5 -я связь возникает между Fe 2+ и атомом азота имидазольного кольца Гис F 8. Гис Е 7 хотя и не связан с гемом, но необходим для правильной ориентации и присоединения другого лиганда - О 2 к миоглобину.
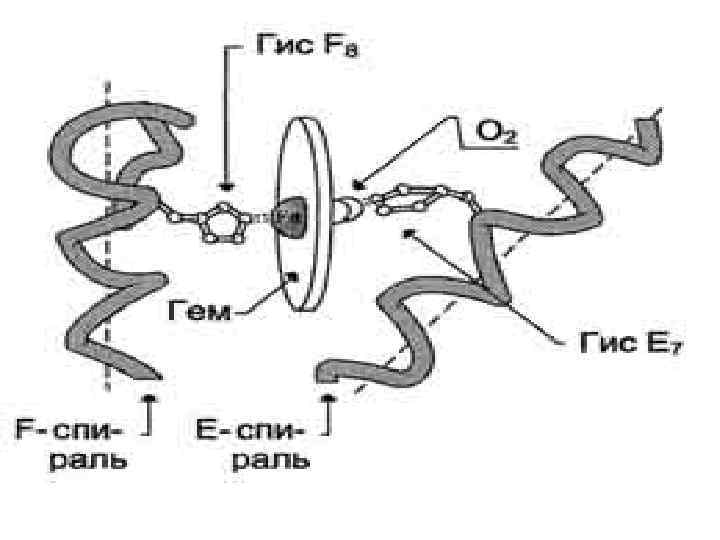

Аминокислотное окружение гема создаёт условия для довольно прочного, но обратимого связывания О 2 с Fe 2+ миоглобина. Гидрофобные остатки аминокислот, окружающие гем, препятствуют проникновению в центр связывания миоглобина воды и окислению Fe 2+ в Fe 3+. Трёхвалентное железо в составе тема не способно присоединять О 2.

Гемоглобин Молекула гемоглобина состоит из 4 полипептидных цепей (субъединиц), в каждой субъединице – гем; внутри каждого гема – один атом Fe. В одном эритроците содержится около 340 млн молекул гемоглобина. Функция – транспорт газов. Кровь ежедневно должна переносить из лёгких в ткани около 600 л, О 2. Так как О 2 плохо растворим в воде, то практически весь кислород в крови связан с гемоглобином эритроцитов.

От способности гемоглобина насыщаться О 2 в лёгких и относительно легко отдавать его в капиллярах тканей зависят количество получаемого тканями О 2 и интенсивность метаболизма. С другой стороны, О 2 - сильный окислитель, избыток поступления О 2 в ткани может привести к повреждению молекул и нарушению структуры и функций клеток. Поэтому важнейшая характеристика гемоглобина - его способность регулировать сродство к О 2 в зависимости от тканевых условий.
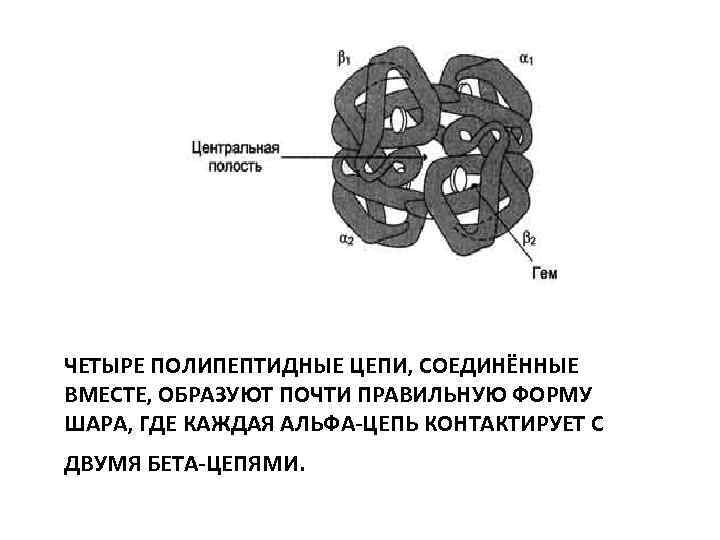
ЧЕТЫРЕ ПОЛИПЕПТИДНЫЕ ЦЕПИ, СОЕДИНЁННЫЕ ВМЕСТЕ, ОБРАЗУЮТ ПОЧТИ ПРАВИЛЬНУЮ ФОРМУ ШАРА, ГДЕ КАЖДАЯ АЛЬФА-ЦЕПЬ КОНТАКТИРУЕТ С ДВУМЯ БЕТА-ЦЕПЯМИ.

Так как в области контакта между альфа 1 - и бета 1 -, а также между альфа 2 - и бета 2 -цепями находится много гидрофобных радикалов, то между этими полипептидными цепями формируется сильное соединение за счёт возникновения в первую очередь гидрофобных, а также ионных и водородных связей. В результате образуются димеры альфа 1 бета 1, и альфа 2 бета 2. Между этими димерами в тетрамерной молекуле гемоглобина возникают в основном полярные (ионные и водородные) связи, поэтому при изменении р. Н среды в кислую или щелочную сторону в первую очередь разрушаются связи между димерами. Кроме того, димеры способны легко перемещаться относительно друга.
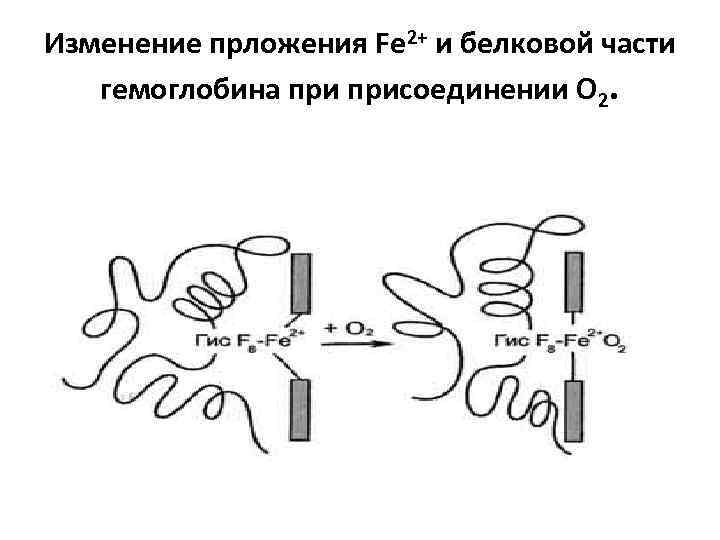
Изменение прложения Fe 2+ и белковой части гемоглобина присоединении О 2.
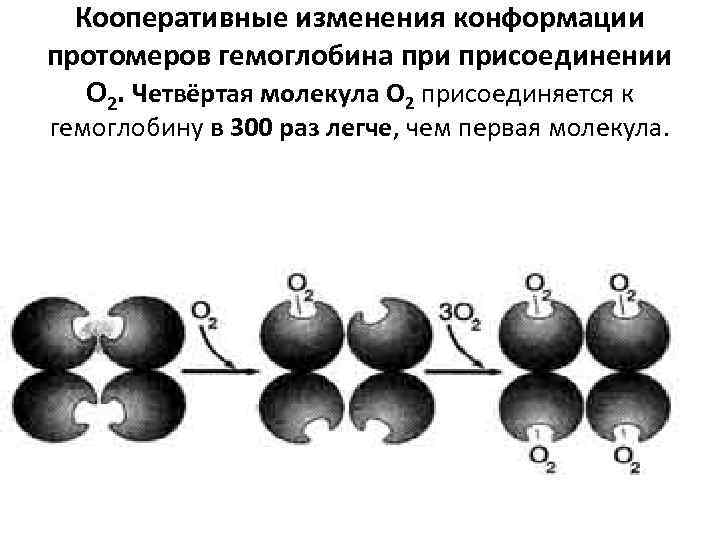
Кооперативные изменения конформации протомеров гемоглобина присоединении О 2. Четвёртая молекула О 2 присоединяется к гемоглобину в 300 раз легче, чем первая молекула.

Изменение конформации (следовательно, и функциональных свойств) всех протомеров олигомерного белка присоединении лиганда только к одному из них носит название кооперативных изменений конформации протомеров. Аналогичным образом в тканях диссоциация каждой молекулы О 2 изменяет конформацию всех протомеров и облегчает отщепление последующих молекул О 2.

Кооперативность в работе протомеров гемоглобина можно наблюдать и на кривых диссоциации О 2 для миоглобина и гемоглобина. Отношение занятых О 2 участков связывания белка к общему числу таких участков, способных к связыванию, называется степенью насыщения этих белков кислородом. Кривые диссоциации показывают, насколько насыщены данные белки О 2 при различных значениях парциального давления кислорода.
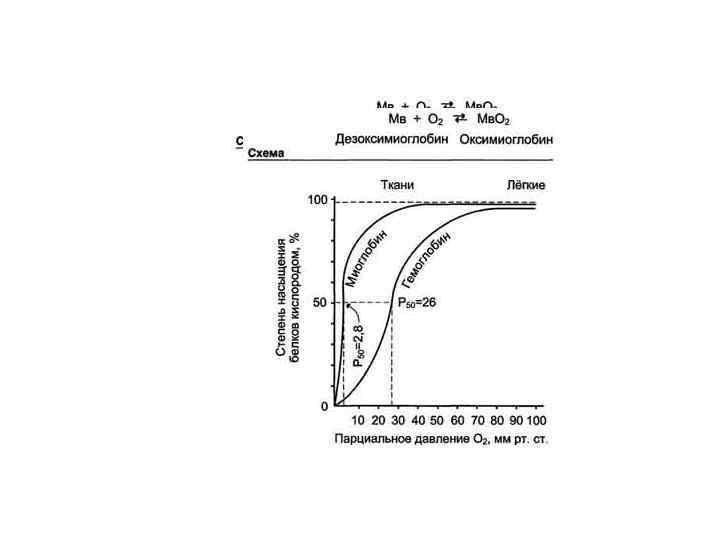

Кривая диссоциации для гемоглобина имеет сигмоидную форму (S-образную). Это указывает на то, что протомеры гемоглобина работают кооперативно: чем больше О 2 отдают протомеры, тем легче идёт отщепление последующих молекул О 2. Кривая диссоциации О 2 для миоглобина имеет вид простой гиперболы. Это указывает на то, что миоглобин обратимо связывается с лигандом, и на это не оказывают влияние никакие посторонние факторы.

Следовательно, благодаря уникальной структуре каждый из рассмотренных белков приспособлен выполнять свою функцию: миоглобин - присоединять О 2, высвобождаемый гемоглобином, накапливать в клетке и отдавать в случае крайней необходимости; гемоглобин - присоединять О 2 в лёгких, где его насыщение доходит до 100%, и отдавать О 2 в капиллярах тканей в зависимости от изменения в них давления О 2.

Окисление органических веществ с целью получения энергии происходит в митохондриях клеток с использованием О 2, доставляемого гемоглобином из лёгких. В результате окисления веществ образуются конечные продукты распада - СО 2 и Н 2 О, количество которых пропорционально интенсивности процессов окисления. СО 2, образовавшийся в тканях, транспортируется в эритроциты. В эритроцитах под действием фермента карбангидразы: СО 2 + Н 2 О ------ H 2 CO 3 ------ H+ + HCO 3 -. Равновесие реакции в эритроцитах, находящихся в капиллярах тканей, смещается вправо, так как образующиеся в результате диссоциации угольной кислоты протоны могут присоединяться к специфическим участкам молекулы гемоглобина: к радикалам Гис146 двух бета-цепей, радикалам Гис122 и концевым альфааминогруппам двух альфа-цепей.

Все эти 6 участков при переходе гемоглобина от окси- к дезоксиформе Hb (O 2 )4 ---- Hb H+ приобретают большее сродство к Н+ в результате локального изменения аминокислотного окружения вокруг этих участков (приближения к ним отрицательно заряженных карбоксильных групп аминокислот). Увеличение освобождения О 2 гемоглобином в зависимости от концентрации Н+ называют эффектом Бора.
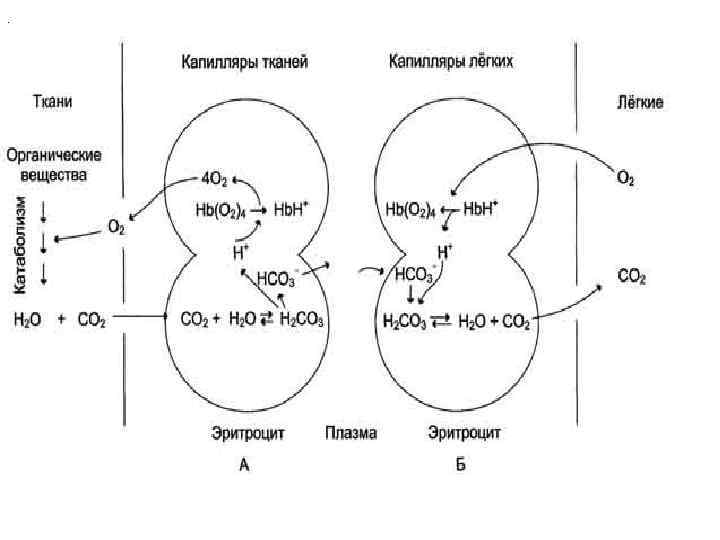
.
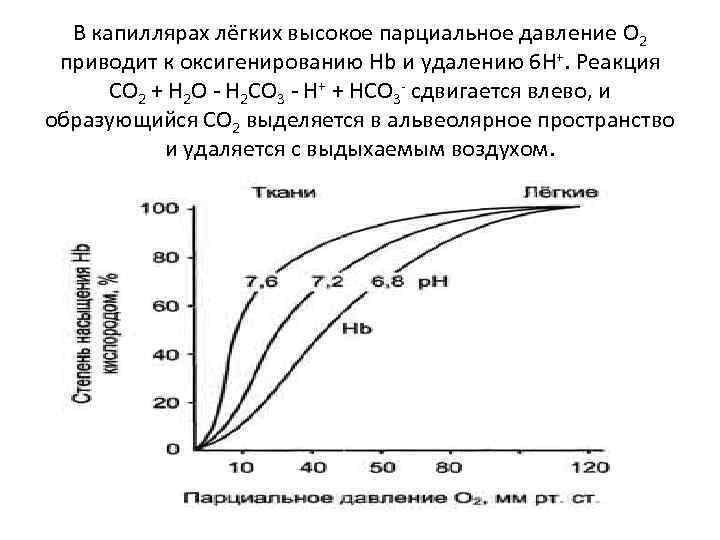
В капиллярах лёгких высокое парциальное давление О 2 приводит к оксигенированию Hb и удалению 6 H+. Реакция СО 2 + Н 2 О - Н 2 СО 3 - Н+ + НСО 3 - сдвигается влево, и образующийся СО 2 выделяется в альвеолярное пространство и удаляется с выдыхаемым воздухом.

Следовательно, молекула гемоглобина в ходе эволюции приобрела способность воспринимать и реагировать на информацию, получаемую из окружающей среды. Увеличение концентрации протонов в среде снижает сродство О 2 к гемоглобину и усиливает его транспорт в ткани.

Большая часть СО 2 транспортируется кровью в виде бикарбоната НСО 3 -. Небольшое количество СО 2 (около 15 -20%) может переноситься в лёгкие, обратимо присоединяясь к неионизированным концевым альфа-аминогруппам R-NH 2+ СО 2 = R-NH-COO + Н+, в результате образуется карбогемоглобин, где R - полипептидная цепь гемоглобина. Присоединение СО 2 к гемоглобину также снижает его сродство к О 2.
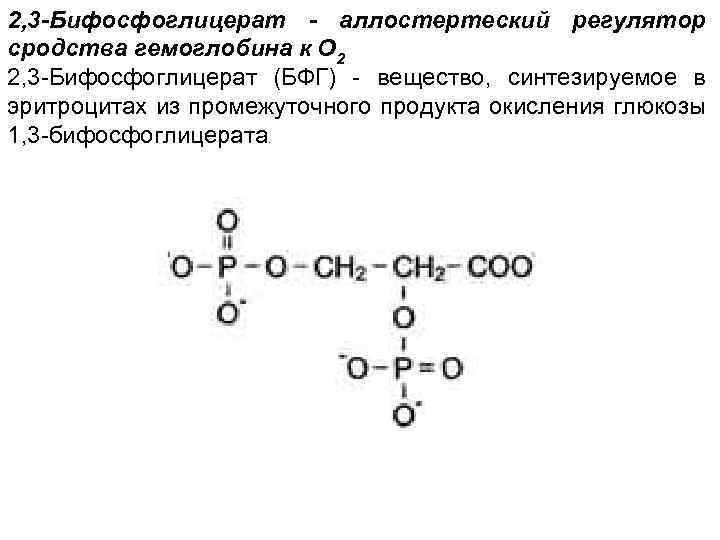
2, 3 -Бифосфоглицерат - аллостертеский регулятор сродства гемоглобина к О 2 2, 3 -Бифосфоглицерат (БФГ) - вещество, синтезируемое в эритроцитах из промежуточного продукта окисления глюкозы 1, 3 -бифосфоглицерата.

БФГ имеет сильный отрицательный заряд, присоединяется с помощью ионных связей, образующихся с положительно заряженными функциональными группами двух бета-цепей гемоглобина (Лиз 82, Гис143 бета-цепей и положительно заряженные альфа-аминогруппы N-концевого валина бета -цепей). Присоединение БФГ ещё сильнее стабилизирует жёсткую структуру дезоксигемоглобина и снижает сродство белка к О 2. В нормальньж условиях 2, 3 -БФГ присутствует в эритроцитах примерно в той же концентрации, что и гемоглобин. Центральная полость - место присоединения БФГ.

Присоединение БФГ к дезоксигемоглобину происходит в участке, где не происходит связывание О 2. Такой лиганд называется "аллостерический", а центр, где связывается аллостерический лиганд, - "аллостерический центр" (от греч. "аллос" - другой, иной, "стерос" - пространственный).

В лёгких высокое парциальное давление О 2 приводит к оксигенированию Hb. Разрыв ионных связей между димерами приводит к "расслаблению" белковой молекулы, уменьшению центральной полости и вытеснению БФГ. Такую же адаптацию наблюдают у больных с заболеваниями лёгких, при которых развивается общая гипоксия тканей.

Таким образом, олигомерный белок гемоглобин, в отличие от мономерного родственного белка миоглобина, способен присоединять к специфическим участкам 4 различных лиган-да: О 2, Н+, СО 2 и БФГ. Все эти лиганды присоединяются к пространственно разобщённым участкам, но конформационные изменения белка в месте присоединения одного лиганда передаются на весь олигомерный белок и изменяют сродство к нему других лигандов. Следовательно, благодаря воздействию регуляторных лигандов олигомерные белки способны приспосабливать свою конформацию и фунцию к изменениям, происходящим в окружающей среде

Гемоглобины человека В эритроцитах взрослого человека гемоглобин составляет 90% от всех белков данной клетки. • Гемоглобин А - основной гемоглобин взрослого организма, составляет около 98% от общего количества гемоглобина, тетрамер, 2 альфа и 2 бета. • Гемоглобин A 2 находится в организме взрослого человека в меньшей концентрации, на его долю приходится около 2% общего гемоглобина. Он состоит из 2 альфа и 2 дельта-цепей. • Гемоглобин А 1 с - гемоглобин А, модифицированный ковалентным присоединением к нему глюкозы (так называемый гликозилированный гемоглобин).

Гены, кодирующие альфа-цепи и сходные с ними дзэта-цепи, располагаются на 16 -й хромосоме, а гены, кодирующие бета-цепи и сходные с ними гамма-, дельта- и эпсилон-цепи, - на 11 -й хромосоме. В норме гемоглобины содержат две цепи из первой группы (альфа или дзэта) и две - из второй (бета, дельта, эпсилон или гамма). Последовательная экспрессия различных генов глобина во время онтогенеза приводит к смене преобладающего типа гемоглобина.

• Эмбриональный гемоглобин синтезируется в эмбриональном желточном мешке через 2 недели после оплодотворения. Представляет собой тетрамер: 2 дзета, 2 эпсилон. Через 6 нед. , после формирования печени в ней начинает синтезироваться Hb F, который постепенно замещает эмбриональный гемоглобин. • Фетальный гемоглобин (Hb F) , синтезируется в печени и костном мозге плода до периода его рождения ( с 8 нед. ). Имеет тетрамерную структуру, состоящую из 2 альфа- и 2 гамма-цепей. После рождения ребёнка постепенно замещается на Hb А, который начинает синтезироваться в клетках костного мозга уже на 8 -м месяце развития плода.

В физиологических условиях Hb. F имеет более высокое сродство к О 2, чем Нb. А, что создаёт оптимальные условия для транспорта О 2 из крови матери в кровь плода. Это свойство Hb. F обусловлено тем, что он слабее, чем НЬА связывается с 2, 3 -БФГ. Связывание 2, 3 -БФГ с НЬА происходит при участии положительно заряженных радикалов аминокислот двух бета-цепей, некоторые из которых отсутствуют в первичной структуре гамма-цепей. В среде, лишённой 2, 3 -БФГ, Нb. А и Hb. F проявляют одинаковое высокое сродство к О 2.

наследственные гемоглобинопатии В аномальных гемоглобинах изменения могут затрагивать аминокислоты: • находящиеся на поверхности белка; • участвующие в формировании активного центра; • замена которых нарушает общую трёхмерную конформацию молекулы; • изменяющие четвертичную структуру белка и его регуляторные свойства.

• Замена аминокислоты на поверхности гемоглобина А Почти все встречающиеся замены аминокислот на поверхности молекулы гемоглобина безвредны. Гемоглобин S - редкое исключение. 1904 г. чикагский врач Джеймс Херрик описал "серповидно-клеточной анемию", 1949 г. Лайнус Полинг и его сотрудники доказали, что оно вызвано изменением первичной структуры НЬА. В молекуле гемоглобина S (так назван аномальный гемоглобин) мутантными оказались 2 бета-цепи, в которых глутамат, высокополярная отрицательно заряженная аминокислота в положении 6 была заменена валином, содержащим гидрофобный радикал. 1 2 3 4 5 6 7 8 Нв. А бета- Валцепь Гис- Лей- Тре- Про- Глу - Лиз- He. S цепь Гис- Лей- Тре- Про- Вал- Глу - Лиз- бета- Вал-

2. Изменения аминокислотного состава в области активного центра гемоглобина Между гемом и белковой частью гемоглобина существует около 60 межатомных контактов. Большинство мутаций, нарушающих в той или иной мере эти контакты, приводят к развитию гемоглобинопатии и анемии. • Гемоглобин М - вариант гемоглобина А, где в результате мутации в гене альфа- или бета-цепи происходит замена гистидина в Е 7 или F 8 тирозином. В результате Fe 2+ окисляется в Fe 3+, и вместо О 2 присоединяется Н 2 О. Гемоглобин, содержащий в геме Fe 3+, называют метгемоглобином. Обычно изменения затрагивают либо альфа-, либо бета-цепи, в результате гемоглобин может переносить не более двух молекул О 2. У гетерозиготных людей отмечают цианоз, связанный с нарушением транспорта О 2, а гомозиготность по этому гену приводит к летальному исходу. • Гемоглобин Хаммерсмита ( замена Phe на Ser в D 1 )

3. Изменения аминокислотного деформирующие третичную гемоглобина состава, структуру Во всех нормальных гемоглобинах и в миоглобине в месте пересечения двух альфа-спиралей В и Е находится глицин. Так как глицин вместо радикала содержит атом водорода, в этом месте две спирали плотно прилегают друг к другу. В гемоглобине Ривердейла-Бронкса (вариант гемоглобина А) вместо Gly в положении В 6 находится Arg, имеющая объёмный радикал. В результате он не умещается в столь узком пространстве, молекула меняет конформацию и становится нестабильной.

4. Замены аминокислот в области контактов димеров, нарушающие аллостерические регуляторные функции гемоглобина Почти все варианты Hb А, где происходит замена аминокислот в области контакта димеров, проявляют пониженную кооперативность и нарушенное сродство гемоглобина к О 2. Гемоглобин Кемпси - вариант гемоглобина А, где в положении G 1 бета-цепи заменена Asp на Asn. В норме аспарагиновая кислота участвует в образовании водородной связи, стабилизирующей дезокси-гемоглобин. В результате замены эта связь не образуется, что нарушает стабильность конформации дезокси-гемоглобина, и сродство гемоглобина к О 2 повышается. У больных развивается анемия с выраженным цианозом.

Таким образом, первичная структура белка определяет особенности его конформации, строения активного центра и функций. Изменение одной аминокислоты только в одном белке может быть причиной нарушений функций данного белка и развития наследственной патологии.
СЛОЖНЫЕ БЕЛКИ.pptx