 Классификация и номенклатура неорганических веществ Лекция 5 по курсу «Общая химия»
Классификация и номенклатура неорганических веществ Лекция 5 по курсу «Общая химия»
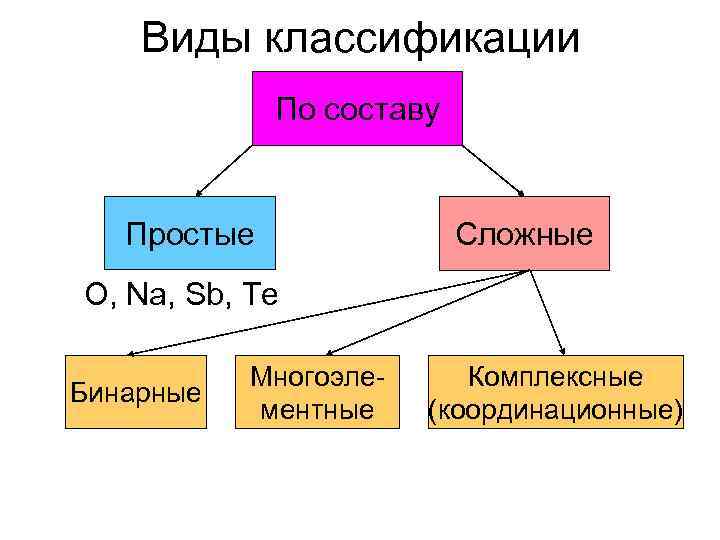 Виды классификации По составу Простые Сложные O, Na, Sb, Te Бинарные Многоэлементные Комплексные (координационные)
Виды классификации По составу Простые Сложные O, Na, Sb, Te Бинарные Многоэлементные Комплексные (координационные)
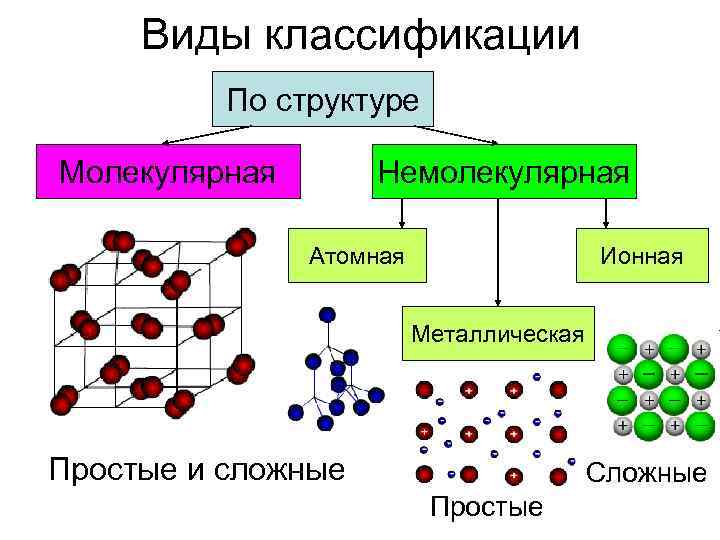 Виды классификации По структуре Молекулярная Немолекулярная Атомная Ионная Металлическая Простые и сложные Сложные Простые
Виды классификации По структуре Молекулярная Немолекулярная Атомная Ионная Металлическая Простые и сложные Сложные Простые
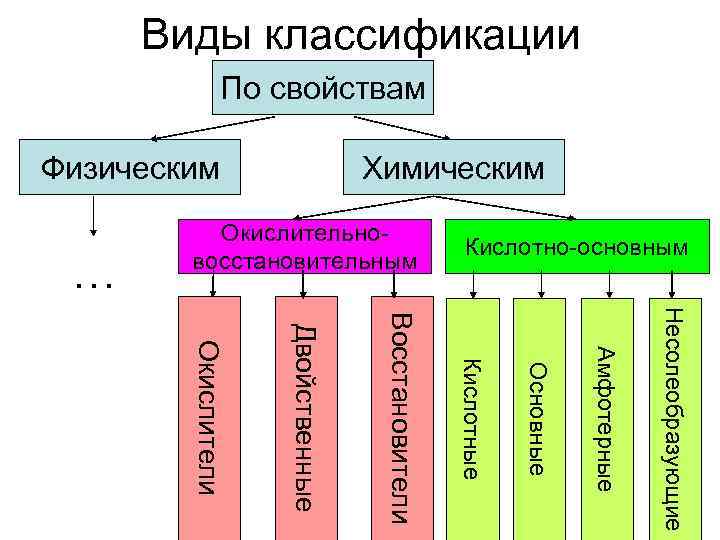 Виды классификации По свойствам Физическим … Химическим Окислительновосстановительным Кислотно-основным Несолеобразующие Амфотерные Основные Кислотные Восстановители Двойственные Окислители
Виды классификации По свойствам Физическим … Химическим Окислительновосстановительным Кислотно-основным Несолеобразующие Амфотерные Основные Кислотные Восстановители Двойственные Окислители
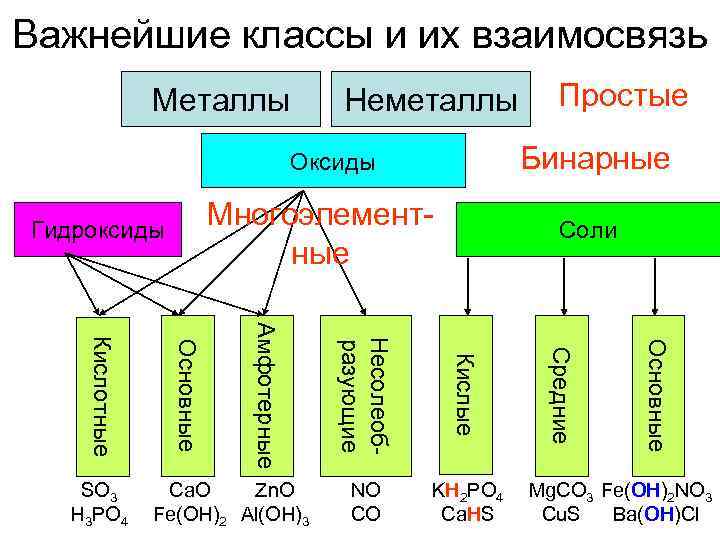 Важнейшие классы и их взаимосвязь Металлы Неметаллы Бинарные Оксиды Многоэлементные Гидроксиды KH 2 PO 4 Ca. HS Основные NO CO Средние Кислые Ca. O Zn. O Fe(OH)2 Al(OH)3 Соли Несолеобразующие Амфотерные Основные Кислотные SO 3 H 3 PO 4 Простые Mg. CO 3 Fe(OH)2 NO 3 Cu. S Ba(OH)Cl
Важнейшие классы и их взаимосвязь Металлы Неметаллы Бинарные Оксиды Многоэлементные Гидроксиды KH 2 PO 4 Ca. HS Основные NO CO Средние Кислые Ca. O Zn. O Fe(OH)2 Al(OH)3 Соли Несолеобразующие Амфотерные Основные Кислотные SO 3 H 3 PO 4 Простые Mg. CO 3 Fe(OH)2 NO 3 Cu. S Ba(OH)Cl
 Оксиды • Неметаллы: несолеобразующие (CO, N 2 O, NO, Ge. O…) или кислотные (все остальные); • Металлы: основные (+1 – +2), амфотерные (+2 – +4), кислотные (+4 – +7); • Для s-металлов – основные (кроме Be); • Для p-металлов – главным образом амфотерные; • Для d-металлов – основные (Cr. O), амфотерные (Cr 2 O 3), кислотные (Cr. O 3);
Оксиды • Неметаллы: несолеобразующие (CO, N 2 O, NO, Ge. O…) или кислотные (все остальные); • Металлы: основные (+1 – +2), амфотерные (+2 – +4), кислотные (+4 – +7); • Для s-металлов – основные (кроме Be); • Для p-металлов – главным образом амфотерные; • Для d-металлов – основные (Cr. O), амфотерные (Cr 2 O 3), кислотные (Cr. O 3);
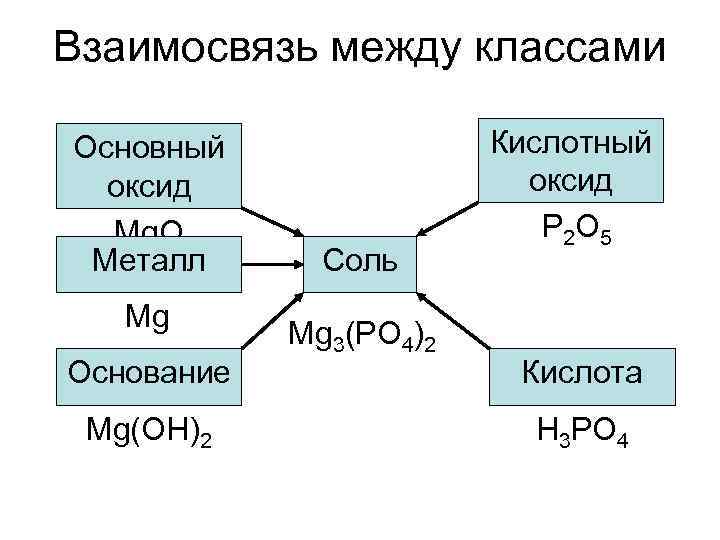 Взаимосвязь между классами Основный оксид Mg. O Металл Mg Основание Mg(OH)2 Соль Mg 3(PO 4)2 Кислотный оксид P 2 O 5 Кислота H 3 PO 4
Взаимосвязь между классами Основный оксид Mg. O Металл Mg Основание Mg(OH)2 Соль Mg 3(PO 4)2 Кислотный оксид P 2 O 5 Кислота H 3 PO 4
 Что такое кислотность и основность? Реакции в водном растворе: HCl + Ba(OH)2 = Ba. Cl 2 + HOH Na. H 2 PO 4 + 2 Na. OH = Na 3 PO 4 + 2 HOH H+ от кислоты, OH– от основания Реакции при сплавлении Zn. O + SO 3 = Zn 2+ SO 42– Zn. O + Ca(OH)2 = Ca 2+ Zn. O 22– + H 2 O Анион от кислоты, катион от основания
Что такое кислотность и основность? Реакции в водном растворе: HCl + Ba(OH)2 = Ba. Cl 2 + HOH Na. H 2 PO 4 + 2 Na. OH = Na 3 PO 4 + 2 HOH H+ от кислоты, OH– от основания Реакции при сплавлении Zn. O + SO 3 = Zn 2+ SO 42– Zn. O + Ca(OH)2 = Ca 2+ Zn. O 22– + H 2 O Анион от кислоты, катион от основания
 Амфотерные оксиды и гидроксиды: в растворе и при сплавлении Раствор Na. OH + Al(OH)3 = Na[Al(OH)4] Или: 3 Na. OH + Al(OH)3 = Na 3[Al(OH)6] (зависит от соотношения) K 2 O + Zn. O + H 2 O = K 2[Zn(OH)4] Расплав Na. OH + Al(OH)3 = Na. Al. O 2 + 2 H 2 O Или: 3 Na. OH + Al(OH)3 = Na 3 Al. O 3 + 3 H 2 O (зависит от соотношения) 2 KOH + Zn(OH)2 = K 2 Zn. O 2 + 2 H 2 O
Амфотерные оксиды и гидроксиды: в растворе и при сплавлении Раствор Na. OH + Al(OH)3 = Na[Al(OH)4] Или: 3 Na. OH + Al(OH)3 = Na 3[Al(OH)6] (зависит от соотношения) K 2 O + Zn. O + H 2 O = K 2[Zn(OH)4] Расплав Na. OH + Al(OH)3 = Na. Al. O 2 + 2 H 2 O Или: 3 Na. OH + Al(OH)3 = Na 3 Al. O 3 + 3 H 2 O (зависит от соотношения) 2 KOH + Zn(OH)2 = K 2 Zn. O 2 + 2 H 2 O
 Как составлять формулы солей a) Безводные формы Na 2 O + Sb 2 O 5 = ? 1. Найти основный (Na 2 O) и кислотный (Sb 2 O 5) 2. Записать по возрастающей ЭО: Na Sb O 3. Степени окисления: Na+1 Sb+5 O– 2 4. У элементов III-V периодов формула кислоты обычно Hx. ЭО 4: Na+1 Sb+5 O– 24 5. 1 x + 5 – 2· 4 = 0 x = 3 6. Na 3 Sb. O 4 7. 3 Na 2 O + Sb 2 O 5 = 2 Na 3 Sb. O 4
Как составлять формулы солей a) Безводные формы Na 2 O + Sb 2 O 5 = ? 1. Найти основный (Na 2 O) и кислотный (Sb 2 O 5) 2. Записать по возрастающей ЭО: Na Sb O 3. Степени окисления: Na+1 Sb+5 O– 2 4. У элементов III-V периодов формула кислоты обычно Hx. ЭО 4: Na+1 Sb+5 O– 24 5. 1 x + 5 – 2· 4 = 0 x = 3 6. Na 3 Sb. O 4 7. 3 Na 2 O + Sb 2 O 5 = 2 Na 3 Sb. O 4
 Как составлять формулы солей б) Гидроксокомплексы Na. OH + Cr(OH)3 = ? 1. Найти основание (Na. OН) и кислоту (Cr(OH)3) 2. Записать по убывающей ЭО: Na Cr OH 3. Заряды ионов: Na 1+ Cr 3+ OH– 4. Заряд +2 к. ч. = 4; Заряд +3 к. ч. = 4 или 6; 5. 1 x + 3 – 1· 4 = 0 x = 1 (Na[Cr(OH)4]) или: 1 x + 3 – 1· 6 = 0 x = 3 (Na 3[Cr(OH)6]) 6. Na. OH + Cr(OH)3 = Na[Cr(OH)4] или: 3 Na. OH + Cr(OH)3 = Na 3[Cr(OH)6]
Как составлять формулы солей б) Гидроксокомплексы Na. OH + Cr(OH)3 = ? 1. Найти основание (Na. OН) и кислоту (Cr(OH)3) 2. Записать по убывающей ЭО: Na Cr OH 3. Заряды ионов: Na 1+ Cr 3+ OH– 4. Заряд +2 к. ч. = 4; Заряд +3 к. ч. = 4 или 6; 5. 1 x + 3 – 1· 4 = 0 x = 1 (Na[Cr(OH)4]) или: 1 x + 3 – 1· 6 = 0 x = 3 (Na 3[Cr(OH)6]) 6. Na. OH + Cr(OH)3 = Na[Cr(OH)4] или: 3 Na. OH + Cr(OH)3 = Na 3[Cr(OH)6]
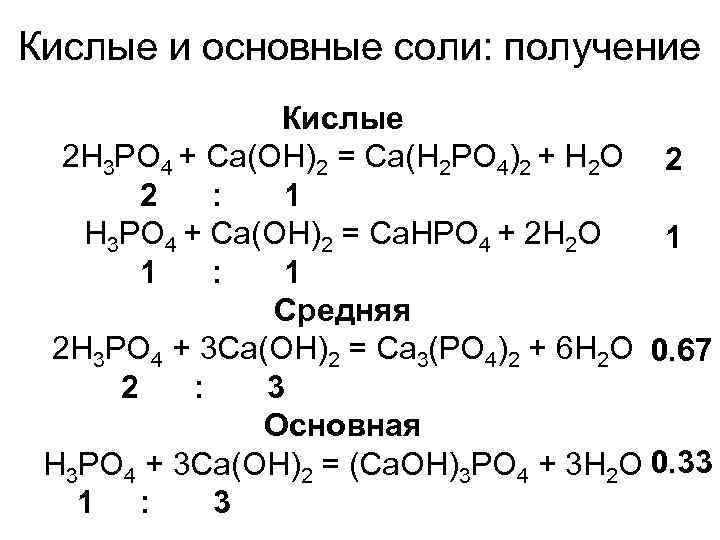 Кислые и основные соли: получение Кислые 2 H 3 PO 4 + Ca(OH)2 = Ca(H 2 PO 4)2 + H 2 O 2 2 : 1 H 3 PO 4 + Ca(OH)2 = Ca. HPO 4 + 2 H 2 O 1 1 : 1 Средняя 2 H 3 PO 4 + 3 Ca(OH)2 = Ca 3(PO 4)2 + 6 H 2 O 0. 67 2 : 3 Основная H 3 PO 4 + 3 Ca(OH)2 = (Ca. OH)3 PO 4 + 3 H 2 O 0. 33 1 : 3
Кислые и основные соли: получение Кислые 2 H 3 PO 4 + Ca(OH)2 = Ca(H 2 PO 4)2 + H 2 O 2 2 : 1 H 3 PO 4 + Ca(OH)2 = Ca. HPO 4 + 2 H 2 O 1 1 : 1 Средняя 2 H 3 PO 4 + 3 Ca(OH)2 = Ca 3(PO 4)2 + 6 H 2 O 0. 67 2 : 3 Основная H 3 PO 4 + 3 Ca(OH)2 = (Ca. OH)3 PO 4 + 3 H 2 O 0. 33 1 : 3