Галоген.ppt
- Количество слайдов: 23
 Классификация галогеноуглеводородов I. По строению углеводородного радикала: а) насыщенный - галогеналканы и циклогалогеналканы б) ненасыщенный - галогеналкены и галогеналкины в) ароматический - галогенарены II. По количеству атомов галогена: моно-, ди-, три-. . . III. По типу гибридизации углеродного атома, с которым связан галоген: а) sp 3 -гибридизованный углеродный атом:
Классификация галогеноуглеводородов I. По строению углеводородного радикала: а) насыщенный - галогеналканы и циклогалогеналканы б) ненасыщенный - галогеналкены и галогеналкины в) ароматический - галогенарены II. По количеству атомов галогена: моно-, ди-, три-. . . III. По типу гибридизации углеродного атома, с которым связан галоген: а) sp 3 -гибридизованный углеродный атом:
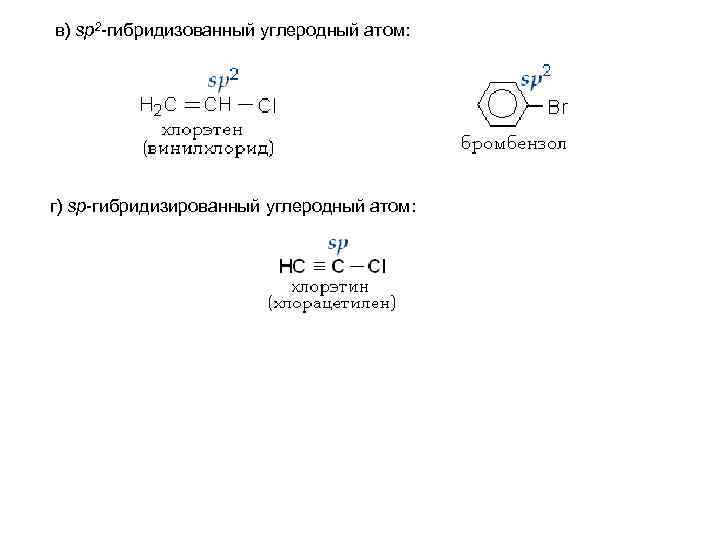 в) sp 2 -гибридизованный углеродный атом: г) sp-гибридизированный углеродный атом:
в) sp 2 -гибридизованный углеродный атом: г) sp-гибридизированный углеродный атом:
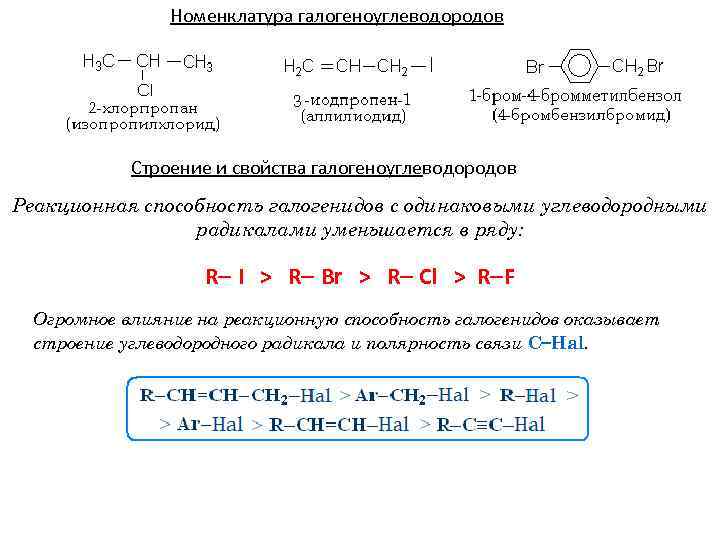 Номенклатура галогеноуглеводородов Строение и свойства галогеноуглеводородов Реакционная способность галогенидов с одинаковыми углеводородными радикалами уменьшается в ряду: R I > R Br > R Cl > R F Огромное влияние на реакционную способность галогенидов оказывает строение углеводородного радикала и полярность связи С Hal.
Номенклатура галогеноуглеводородов Строение и свойства галогеноуглеводородов Реакционная способность галогенидов с одинаковыми углеводородными радикалами уменьшается в ряду: R I > R Br > R Cl > R F Огромное влияние на реакционную способность галогенидов оказывает строение углеводородного радикала и полярность связи С Hal.
 В молекулах галогеналканов связь Сsp 3 Hal полярна, поэтому способна к разрыву по ионному механизму - реакции замещения (S) и элиминирования (отщепления) - E Если атом галогена связан с sp 2 -гибридизованным атомом (винилгалогениды и галогенарены), то кроме I-эффекта атома галогена наблюдается сопряжение неподеленной электронной пары галогена с электронами двойной связи, либо с -электронами ароматического ядра (+М-эффект).
В молекулах галогеналканов связь Сsp 3 Hal полярна, поэтому способна к разрыву по ионному механизму - реакции замещения (S) и элиминирования (отщепления) - E Если атом галогена связан с sp 2 -гибридизованным атомом (винилгалогениды и галогенарены), то кроме I-эффекта атома галогена наблюдается сопряжение неподеленной электронной пары галогена с электронами двойной связи, либо с -электронами ароматического ядра (+М-эффект).
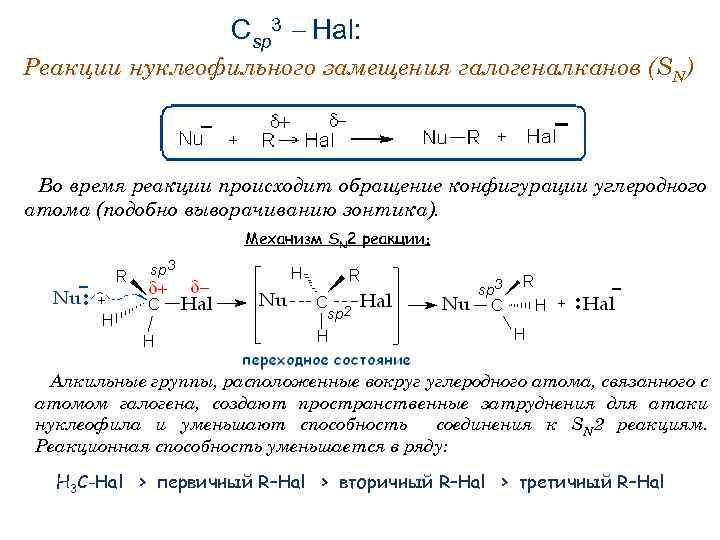 Сsp 3 Hal: Реакции нуклеофильного замещения галогеналканов (SN) Во время реакции происходит обращение конфигурации углеродного атома (подобно выворачиванию зонтика). Механизм SN 2 реакции: Алкильные группы, расположенные вокруг углеродного атома, связанного с атомом галогена, создают пространственные затруднения для атаки нуклеофила и уменьшают способность соединения к SN 2 реакциям. Реакционная способность уменьшается в ряду: Н 3 С-Hal > первичный R–Нal > вторичный R–Hal > третичный R–Hal
Сsp 3 Hal: Реакции нуклеофильного замещения галогеналканов (SN) Во время реакции происходит обращение конфигурации углеродного атома (подобно выворачиванию зонтика). Механизм SN 2 реакции: Алкильные группы, расположенные вокруг углеродного атома, связанного с атомом галогена, создают пространственные затруднения для атаки нуклеофила и уменьшают способность соединения к SN 2 реакциям. Реакционная способность уменьшается в ряду: Н 3 С-Hal > первичный R–Нal > вторичный R–Hal > третичный R–Hal
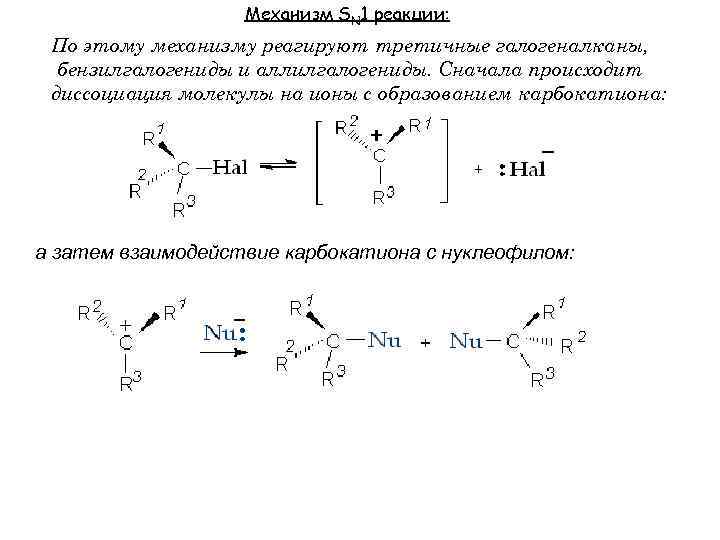 Механизм SN 1 реакции: По этому механизму реагируют третичные галогеналканы, бензилгалогениды и аллилгалогениды. Сначала происходит диссоциация молекулы на ионы с образованием карбокатиона: а затем взаимодействие карбокатиона с нуклеофилом:
Механизм SN 1 реакции: По этому механизму реагируют третичные галогеналканы, бензилгалогениды и аллилгалогениды. Сначала происходит диссоциация молекулы на ионы с образованием карбокатиона: а затем взаимодействие карбокатиона с нуклеофилом:
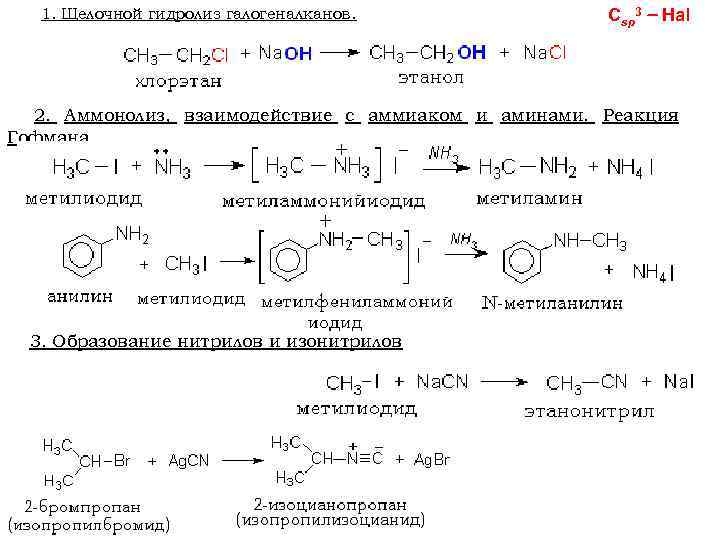 1. Щелочной гидролиз галогеналканов. Сsp 3 Hal 2. Аммонолиз, взаимодействие с аммиаком и аминами. Реакция Гофмана. 3. Образование нитрилов и изонитрилов
1. Щелочной гидролиз галогеналканов. Сsp 3 Hal 2. Аммонолиз, взаимодействие с аммиаком и аминами. Реакция Гофмана. 3. Образование нитрилов и изонитрилов
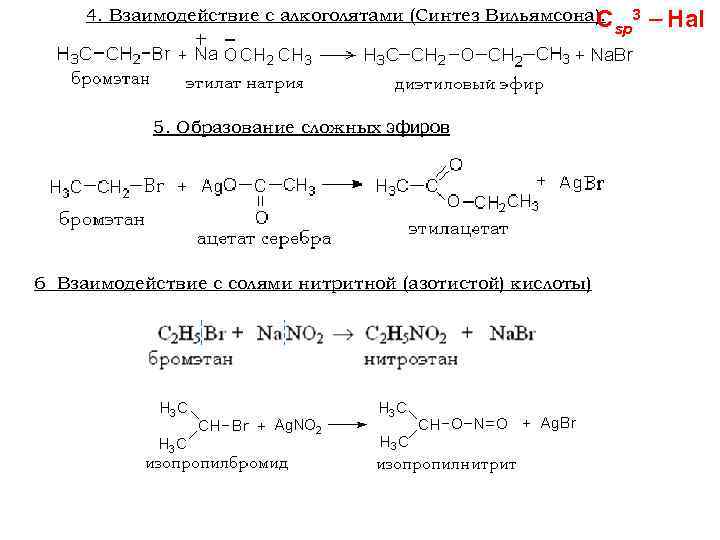 4. Взаимодействие с алкоголятами (Синтез Вильямсона). С 5. Образование сложных эфиров 6 Взаимодействие с солями нитритной (азотистой) кислоты) sp 3 Hal
4. Взаимодействие с алкоголятами (Синтез Вильямсона). С 5. Образование сложных эфиров 6 Взаимодействие с солями нитритной (азотистой) кислоты) sp 3 Hal
 Сsp 3 Hal 7. Замещение хлора и брома на йод (реакция Финкельштейна) 8. Взаимодействие с гидросульфидами и сульфидами щелочных металлов
Сsp 3 Hal 7. Замещение хлора и брома на йод (реакция Финкельштейна) 8. Взаимодействие с гидросульфидами и сульфидами щелочных металлов
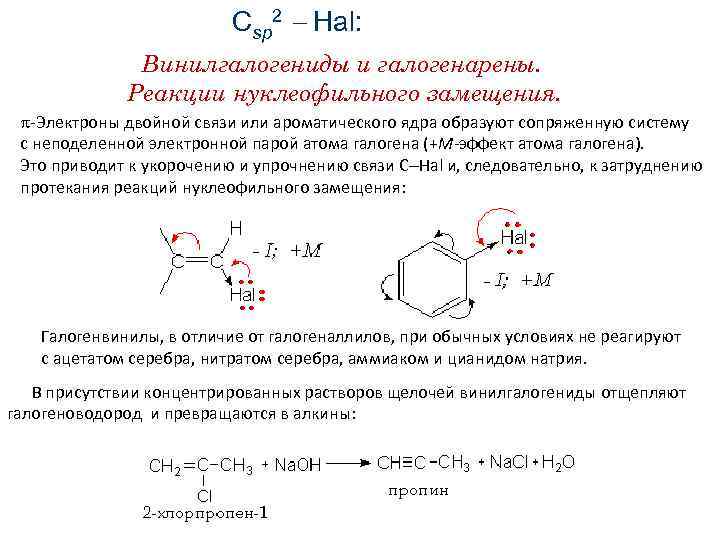 Сsp 2 Hal: Винилгалогениды и галогенарены. Реакции нуклеофильного замещения. -Электроны двойной связи или ароматического ядра образуют сопряженную систему с неподеленной электронной парой атома галогена (+М-эффект атома галогена). Это приводит к укорочению и упрочнению связи C Hal и, следовательно, к затруднению протекания реакций нуклеофильного замещения: Галогенвинилы, в отличие от галогеналлилов, при обычных условиях не реагируют с ацетатом серебра, нитратом серебра, аммиаком и цианидом натрия. В присутствии концентрированных растворов щелочей винилгалогениды отщепляют галогеноводород и превращаются в алкины:
Сsp 2 Hal: Винилгалогениды и галогенарены. Реакции нуклеофильного замещения. -Электроны двойной связи или ароматического ядра образуют сопряженную систему с неподеленной электронной парой атома галогена (+М-эффект атома галогена). Это приводит к укорочению и упрочнению связи C Hal и, следовательно, к затруднению протекания реакций нуклеофильного замещения: Галогенвинилы, в отличие от галогеналлилов, при обычных условиях не реагируют с ацетатом серебра, нитратом серебра, аммиаком и цианидом натрия. В присутствии концентрированных растворов щелочей винилгалогениды отщепляют галогеноводород и превращаются в алкины:
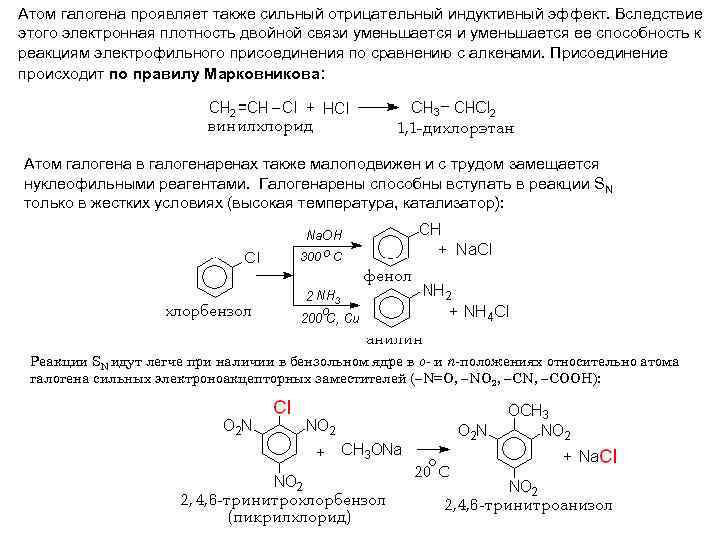 Атом галогена проявляет также сильный отрицательный индуктивный эффект. Вследствие этого электронная плотность двойной связи уменьшается ее способность к реакциям электрофильного присоединения по сравнению с алкенами. Присоединение происходит по правилу Марковникова: Атом галогена в галогенаренах также малоподвижен и с трудом замещается нуклеофильными реагентами. Галогенарены способны вступать в реакции SN только в жестких условиях (высокая температура, катализатор): Реакции SN идут легче при наличии в бензольном ядре в о- и п-положениях относительно атома галогена сильных электроноакцепторных заместителей ( N=O, NO 2, CN, COOH):
Атом галогена проявляет также сильный отрицательный индуктивный эффект. Вследствие этого электронная плотность двойной связи уменьшается ее способность к реакциям электрофильного присоединения по сравнению с алкенами. Присоединение происходит по правилу Марковникова: Атом галогена в галогенаренах также малоподвижен и с трудом замещается нуклеофильными реагентами. Галогенарены способны вступать в реакции SN только в жестких условиях (высокая температура, катализатор): Реакции SN идут легче при наличии в бензольном ядре в о- и п-положениях относительно атома галогена сильных электроноакцепторных заместителей ( N=O, NO 2, CN, COOH):
 Реакции элиминирования (отщепления) - Е. Дегидрогалогенирование и дегалогенирование В молекуле галогеналкана под влиянием –І-эффекта атома галогена водородные атомы -углеродного атома становятся более подвижными: Поэтому наряду с реакцией нуклеофильного замещения атома галогена для галогеналканов характерны реакции -элиминирования (Е). При действии спиртовых растворов щелочей от двух соседних (вицинальных) атомов углерода отщепляется молекула галогеноводорода. Отщепление происходит по правилу Зайцева: водород отщепляется от наименее гидрогенизированного углеродного атома.
Реакции элиминирования (отщепления) - Е. Дегидрогалогенирование и дегалогенирование В молекуле галогеналкана под влиянием –І-эффекта атома галогена водородные атомы -углеродного атома становятся более подвижными: Поэтому наряду с реакцией нуклеофильного замещения атома галогена для галогеналканов характерны реакции -элиминирования (Е). При действии спиртовых растворов щелочей от двух соседних (вицинальных) атомов углерода отщепляется молекула галогеноводорода. Отщепление происходит по правилу Зайцева: водород отщепляется от наименее гидрогенизированного углеродного атома.
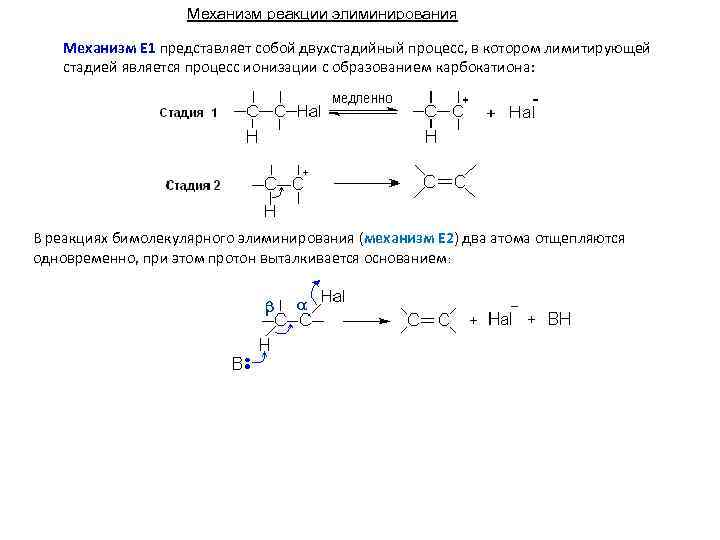 Механизм реакции элиминирования Механизм Е 1 представляет собой двухстадийный процесс, в котором лимитирующей стадией является процесс ионизации с образованием карбокатиона: В реакциях бимолекулярного элиминирования (механизм Е 2) два атома отщепляются одновременно, при этом протон выталкивается основанием:
Механизм реакции элиминирования Механизм Е 1 представляет собой двухстадийный процесс, в котором лимитирующей стадией является процесс ионизации с образованием карбокатиона: В реакциях бимолекулярного элиминирования (механизм Е 2) два атома отщепляются одновременно, при этом протон выталкивается основанием:
 В случае вицинальных дигалогеналканов (атомы галогена у соседних С-атомов) элиминирование осуществляют сильным основанием (например, амид натрия), а восстановительное элиминирование - цинком: Реакции элиминирования и нуклеофильного замещения конкурируют между собой, поэтому для проведения реакции в нужном направлении следует подбирать соответствующие условия. Например, при действии водного раствора щелочи на галогеналкан реакция будет происходить по механизму SN с образованием спирта, а при действии спиртового раствора щелочи – происходит элиминирование с образованием алкена:
В случае вицинальных дигалогеналканов (атомы галогена у соседних С-атомов) элиминирование осуществляют сильным основанием (например, амид натрия), а восстановительное элиминирование - цинком: Реакции элиминирования и нуклеофильного замещения конкурируют между собой, поэтому для проведения реакции в нужном направлении следует подбирать соответствующие условия. Например, при действии водного раствора щелочи на галогеналкан реакция будет происходить по механизму SN с образованием спирта, а при действии спиртового раствора щелочи – происходит элиминирование с образованием алкена:
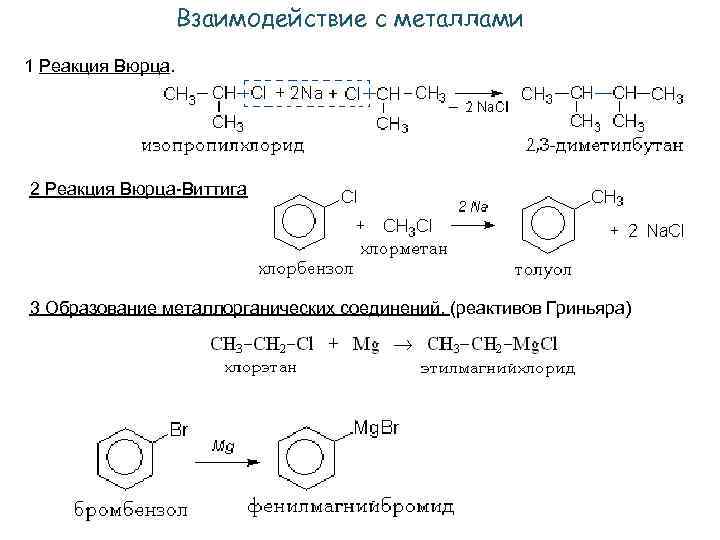 Взаимодействие с металлами 1 Реакция Вюрца. 2 Реакция Вюрца-Виттига. 3 Образование металлорганических соединений. (реактивов Гриньяра)
Взаимодействие с металлами 1 Реакция Вюрца. 2 Реакция Вюрца-Виттига. 3 Образование металлорганических соединений. (реактивов Гриньяра)
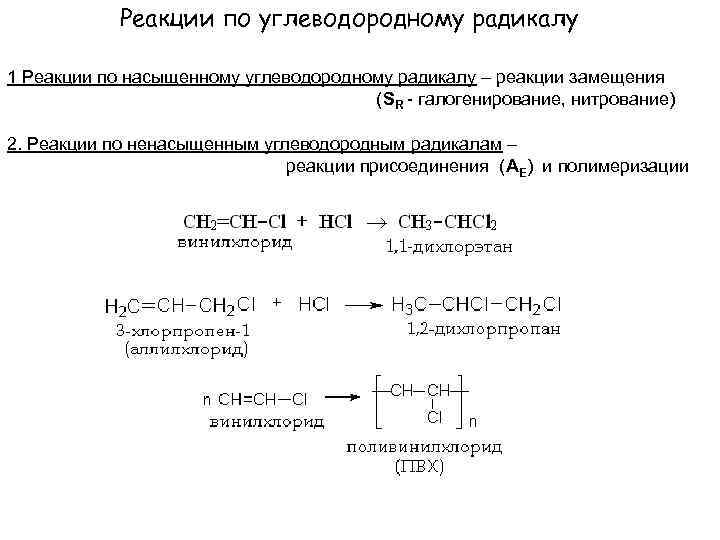 Реакции по углеводородному радикалу 1 Реакции по насыщенному углеводородному радикалу – реакции замещения (SR - галогенирование, нитрование) 2. Реакции по ненасыщенным углеводородным радикалам – реакции присоединения (AE) и полимеризации
Реакции по углеводородному радикалу 1 Реакции по насыщенному углеводородному радикалу – реакции замещения (SR - галогенирование, нитрование) 2. Реакции по ненасыщенным углеводородным радикалам – реакции присоединения (AE) и полимеризации
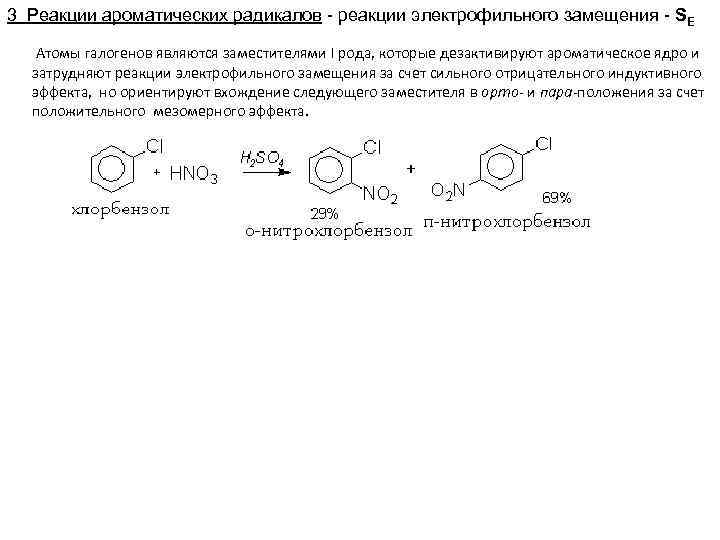 3 Реакции ароматических радикалов - реакции электрофильного замещения - SE Атомы галогенов являются заместителями I рода, которые дезактивируют ароматическое ядро и затрудняют реакции электрофильного замещения за счет сильного отрицательного индуктивного эффекта, но ориентируют вхождение следующего заместителя в орто- и пара-положения за счет положительного мезомерного эффекта.
3 Реакции ароматических радикалов - реакции электрофильного замещения - SE Атомы галогенов являются заместителями I рода, которые дезактивируют ароматическое ядро и затрудняют реакции электрофильного замещения за счет сильного отрицательного индуктивного эффекта, но ориентируют вхождение следующего заместителя в орто- и пара-положения за счет положительного мезомерного эффекта.
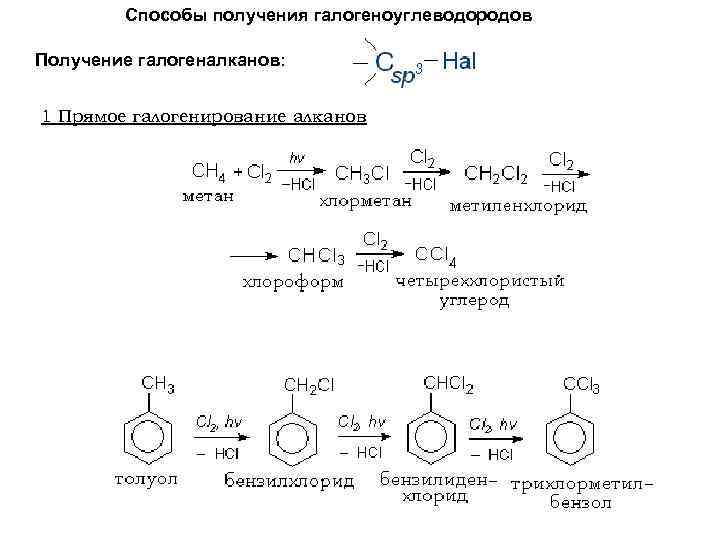 Способы получения галогеноуглеводородов Получение галогеналканов: 1 Прямое галогенирование алканов
Способы получения галогеноуглеводородов Получение галогеналканов: 1 Прямое галогенирование алканов
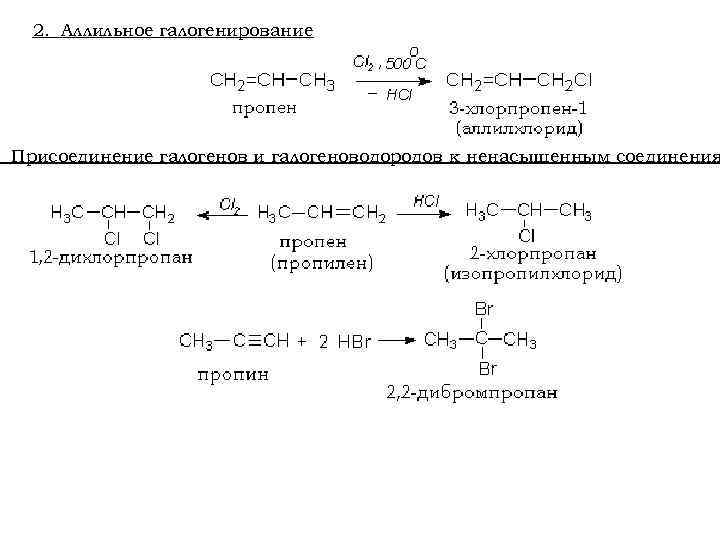 2. Аллильное галогенирование Присоединение галогенов и галогеноводородов к ненасыщенным соединения
2. Аллильное галогенирование Присоединение галогенов и галогеноводородов к ненасыщенным соединения
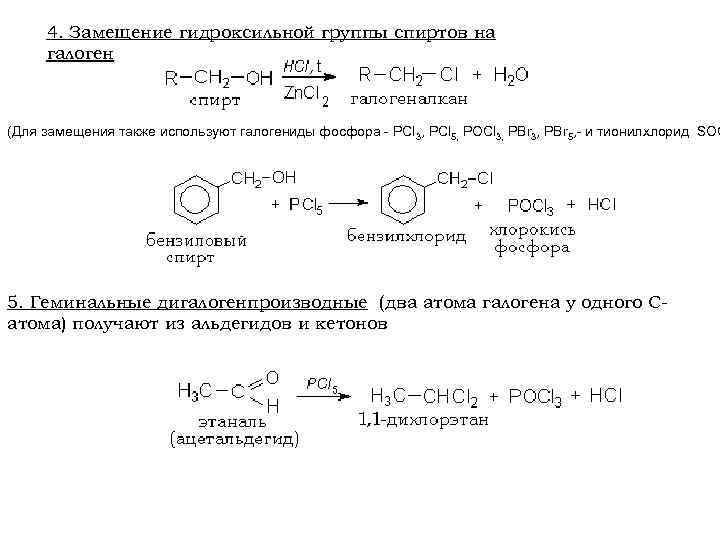 4. Замещение гидроксильной группы спиртов на галоген (Для замещения также используют галогениды фосфора - PCl 3, PCl 5, POCl 3, PBr 5, - и тионилхлорид SOC 5. Геминальные дигалогенпроизводные (два атома галогена у одного Сатома) получают из альдегидов и кетонов
4. Замещение гидроксильной группы спиртов на галоген (Для замещения также используют галогениды фосфора - PCl 3, PCl 5, POCl 3, PBr 5, - и тионилхлорид SOC 5. Геминальные дигалогенпроизводные (два атома галогена у одного Сатома) получают из альдегидов и кетонов
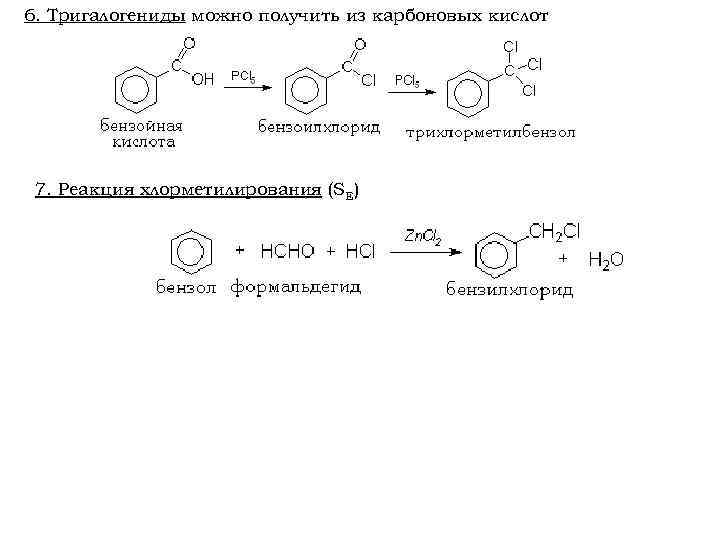 6. Тригалогениды можно получить из карбоновых кислот 7. Реакция хлорметилирования (SE)
6. Тригалогениды можно получить из карбоновых кислот 7. Реакция хлорметилирования (SE)
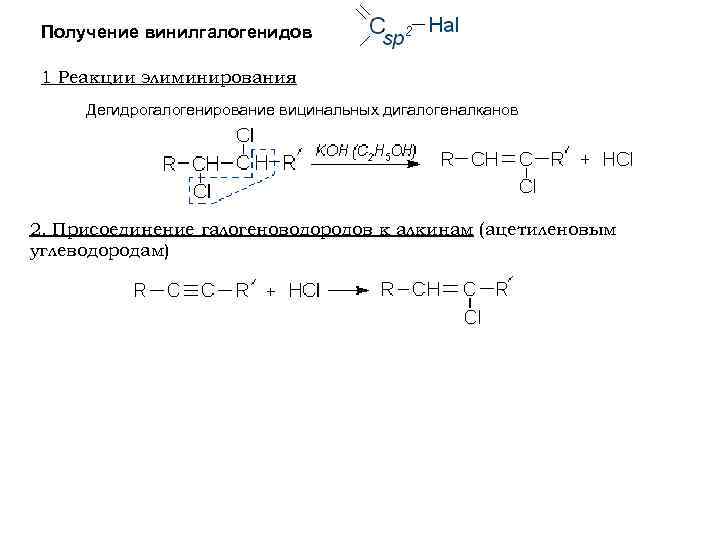 Получение винилгалогенидов 1 Реакции элиминирования Дегидрогалогенирование вицинальных дигалогеналканов 2. Присоединение галогеноводородов к алкинам (ацетиленовым углеводородам)
Получение винилгалогенидов 1 Реакции элиминирования Дегидрогалогенирование вицинальных дигалогеналканов 2. Присоединение галогеноводородов к алкинам (ацетиленовым углеводородам)
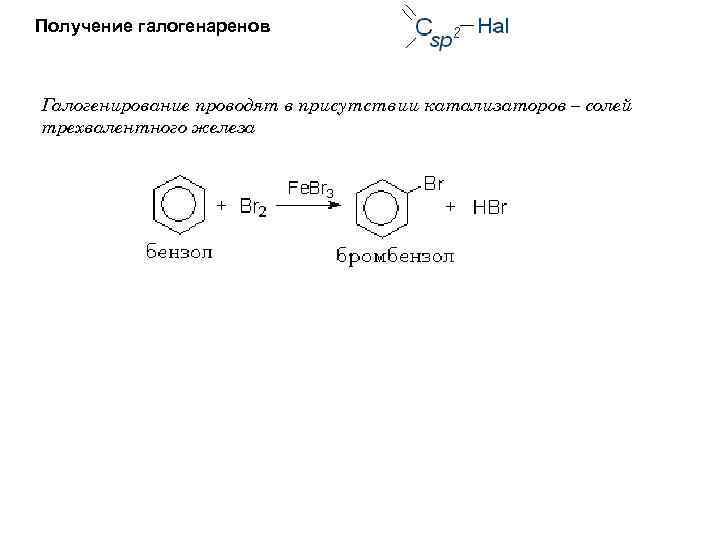 Получение галогенаренов Галогенирование проводят в присутствии катализаторов – солей трехвалентного железа
Получение галогенаренов Галогенирование проводят в присутствии катализаторов – солей трехвалентного железа


