лекция 1.2013.ppt
- Количество слайдов: 49
 Классификации, номенклатура, строение и свойства органических соединений
Классификации, номенклатура, строение и свойства органических соединений
 Функциональная группа -F, -Cl, -Br, -I (Hal) Название класса Общая формула класса R-Hal галогены Галогенопроизводные - OH гидроксильная Спирты, фенолы R-OH, Ar-OH - OR алкоксильная Простые эфиры R-O-R - SH тиольная Тиолы (тиоспирты, меркаптаны) - SR алкилтиольная Тиоэфиры (сульфиды) сульфоновая Сульфоновые кислоты (сульфокислоты) амино Амины первичные - NH 2 R-SH R-S-R R-SO 3 H R-NH 2 вторичные R-NH-R третичные -NH - R 3 N - NO 2 нитросоединения R-NO 2 - C≡N циано Нитрилы R-C≡N карбонильная Альдегиды Кетоны карбоксильная Карбоновые кислоты алкоксикарбо-нильная Сложные эфиры карбоксамидная амиды
Функциональная группа -F, -Cl, -Br, -I (Hal) Название класса Общая формула класса R-Hal галогены Галогенопроизводные - OH гидроксильная Спирты, фенолы R-OH, Ar-OH - OR алкоксильная Простые эфиры R-O-R - SH тиольная Тиолы (тиоспирты, меркаптаны) - SR алкилтиольная Тиоэфиры (сульфиды) сульфоновая Сульфоновые кислоты (сульфокислоты) амино Амины первичные - NH 2 R-SH R-S-R R-SO 3 H R-NH 2 вторичные R-NH-R третичные -NH - R 3 N - NO 2 нитросоединения R-NO 2 - C≡N циано Нитрилы R-C≡N карбонильная Альдегиды Кетоны карбоксильная Карбоновые кислоты алкоксикарбо-нильная Сложные эфиры карбоксамидная амиды
 R-OH
R-OH

 Заместительная систематическая номенклатура органических соединений (IUPAC)
Заместительная систематическая номенклатура органических соединений (IUPAC)
 Приставка (префикс) Корень Суффикс Окончание (суффикс 2)
Приставка (префикс) Корень Суффикс Окончание (суффикс 2)
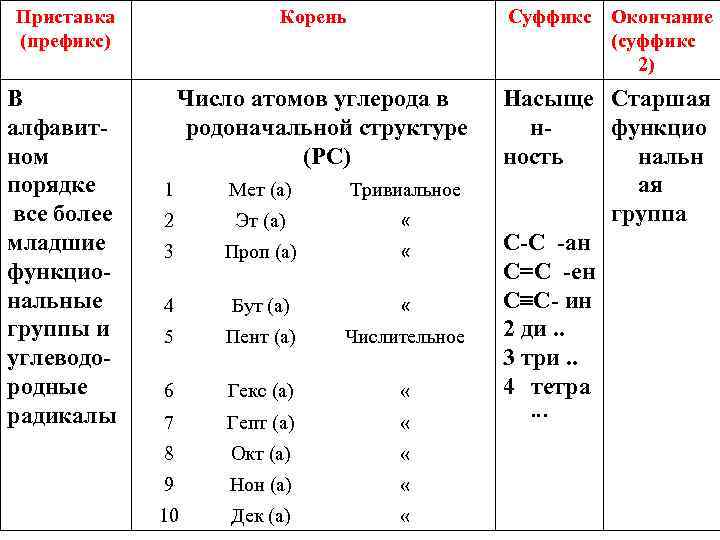 Приставка (префикс) В алфавитном порядке все более младшие функциональные группы и углеводородные радикалы Корень Суффикс Окончание (суффикс 2) Число атомов углерода в родоначальной структуре (РС) 1 Мет (а) Тривиальное 2 Эт (а) « 3 Проп (а) « 4 Бут (а) « 5 Пент (а) Числительное 6 Гекс (а) « 7 Гепт (а) « 8 Окт (а) « 9 Нон (а) « 10 Дек (а) « Насыще Старшая нфункцио ность нальн ая группа С-С -ан С=С -ен С С- ин 2 ди. . 3 три. . 4 тетра …
Приставка (префикс) В алфавитном порядке все более младшие функциональные группы и углеводородные радикалы Корень Суффикс Окончание (суффикс 2) Число атомов углерода в родоначальной структуре (РС) 1 Мет (а) Тривиальное 2 Эт (а) « 3 Проп (а) « 4 Бут (а) « 5 Пент (а) Числительное 6 Гекс (а) « 7 Гепт (а) « 8 Окт (а) « 9 Нон (а) « 10 Дек (а) « Насыще Старшая нфункцио ность нальн ая группа С-С -ан С=С -ен С С- ин 2 ди. . 3 три. . 4 тетра …
 Химическое строение органических сединений 1. Типы гибридизации атомов
Химическое строение органических сединений 1. Типы гибридизации атомов
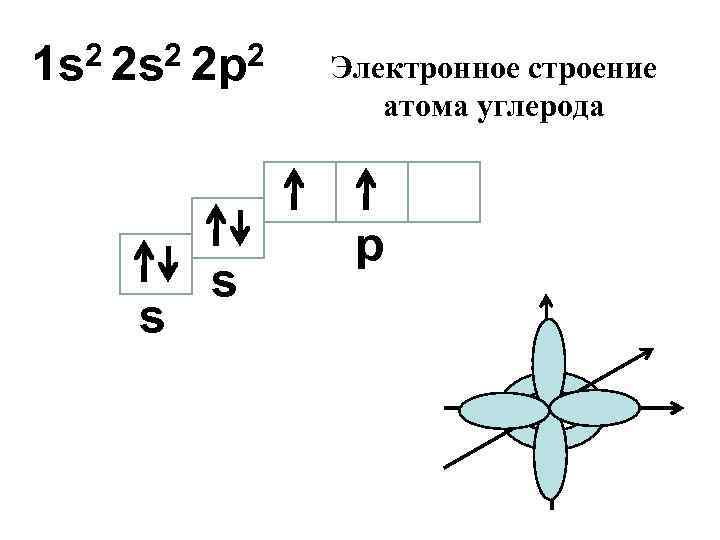 2 2 s 2 2 p 2 1 s s s Электронное строение атома углерода p
2 2 s 2 2 p 2 1 s s s Электронное строение атома углерода p
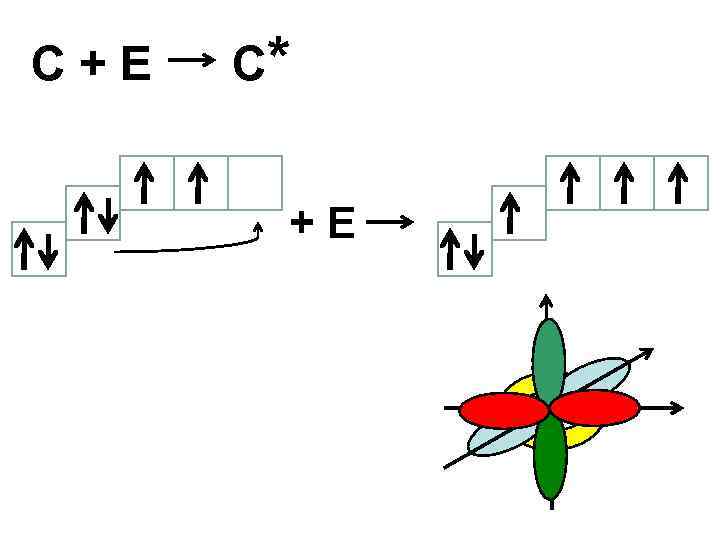 C+E C* +E
C+E C* +E
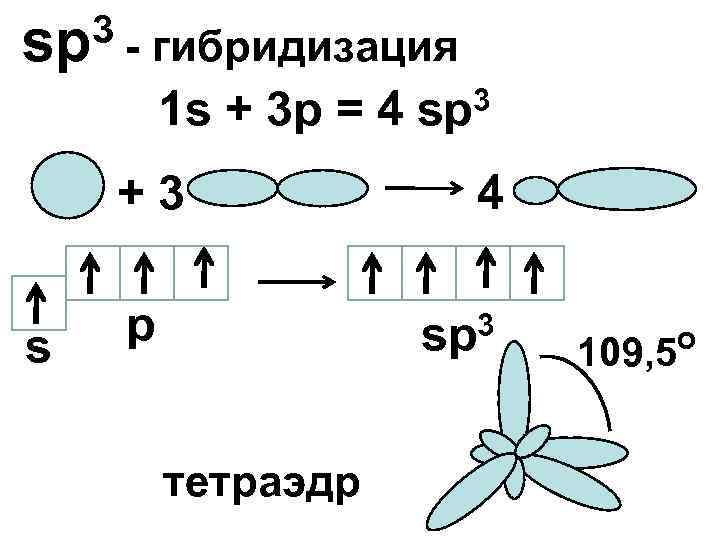 3 - гибридизация sp 1 s + 3 p = 4 +3 s p 3 sp 4 3 sp тетраэдр 109, 5 o
3 - гибридизация sp 1 s + 3 p = 4 +3 s p 3 sp 4 3 sp тетраэдр 109, 5 o
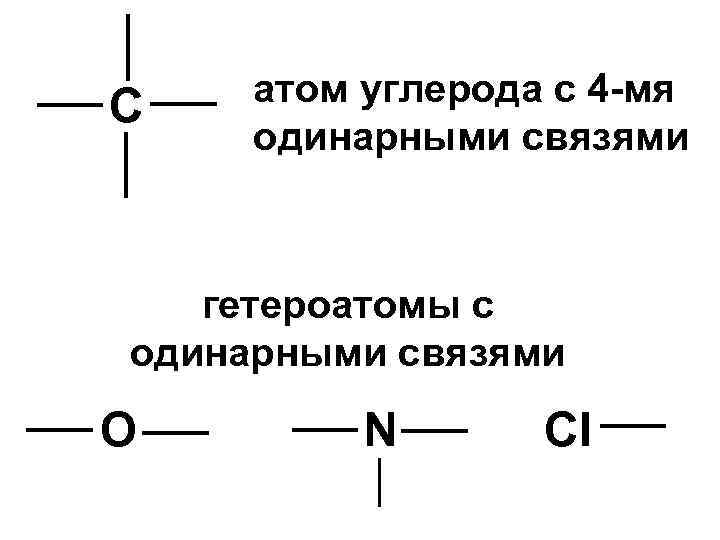 С атом углерода с 4 -мя одинарными связями гетероатомы с одинарными связями О N Cl
С атом углерода с 4 -мя одинарными связями гетероатомы с одинарными связями О N Cl
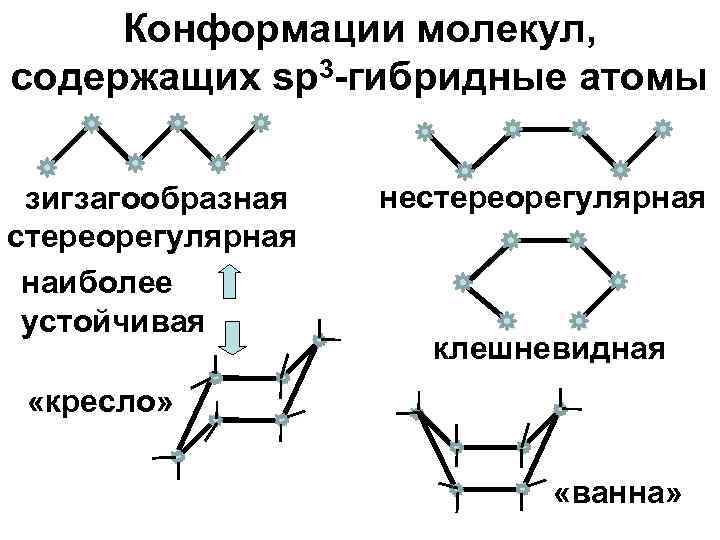 Конформации молекул, содержащих sp 3 -гибридные атомы зигзагообразная стереорегулярная наиболее устойчивая нестереорегулярная клешневидная «кресло» «ванна»
Конформации молекул, содержащих sp 3 -гибридные атомы зигзагообразная стереорегулярная наиболее устойчивая нестереорегулярная клешневидная «кресло» «ванна»
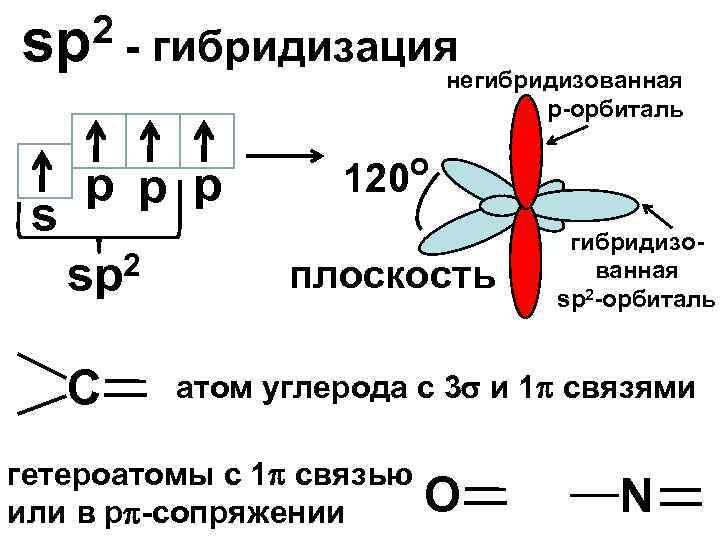 2 - гибридизация sp негибридизованная р-орбиталь s p p p 2 sp С 120 o плоскость гибридизованная sp 2 -орбиталь атом углерода с 3 и 1 связями гетероатомы с 1 связью или в р -сопряжении О N
2 - гибридизация sp негибридизованная р-орбиталь s p p p 2 sp С 120 o плоскость гибридизованная sp 2 -орбиталь атом углерода с 3 и 1 связями гетероатомы с 1 связью или в р -сопряжении О N
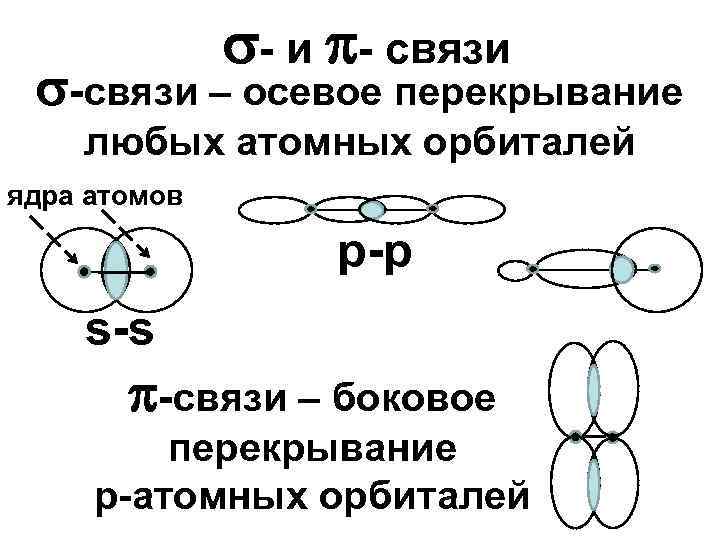 - и - связи -связи – осевое перекрывание любых атомных орбиталей ядра атомов р-р s-s -связи – боковое перекрывание р-атомных орбиталей
- и - связи -связи – осевое перекрывание любых атомных орбиталей ядра атомов р-р s-s -связи – боковое перекрывание р-атомных орбиталей
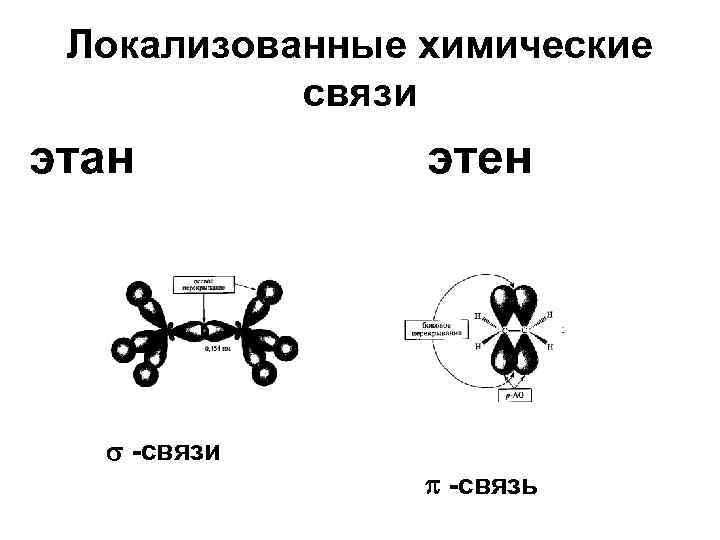 Локализованные химические связи этан -связи этен -связь
Локализованные химические связи этан -связи этен -связь
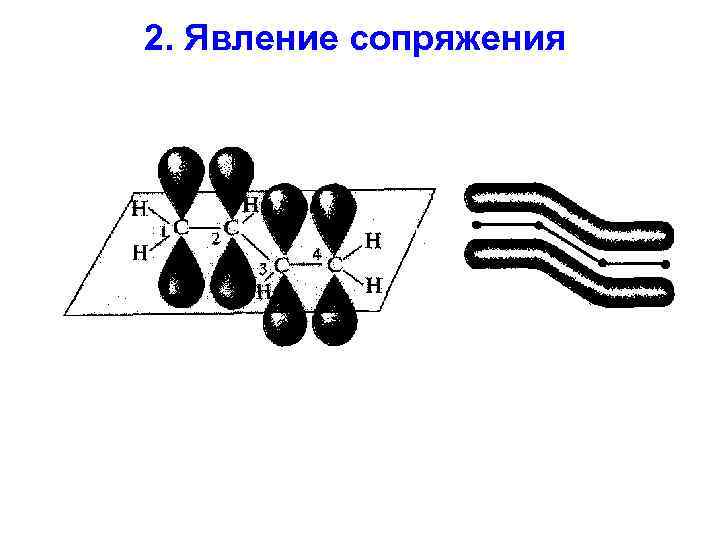 2. Явление сопряжения
2. Явление сопряжения
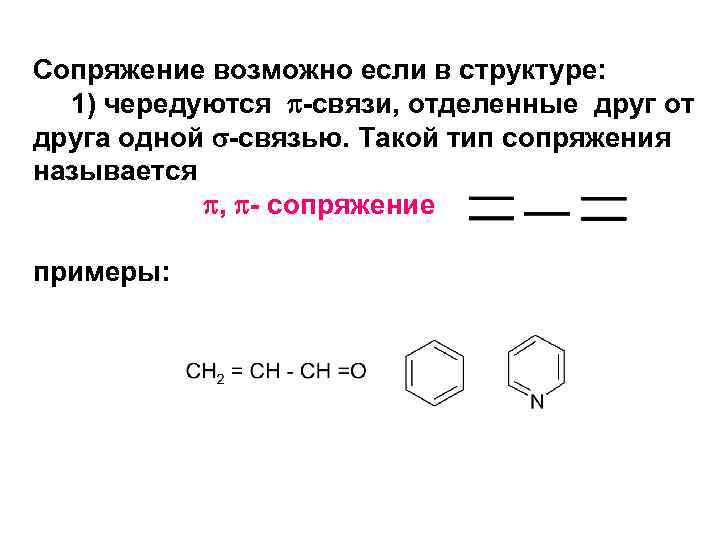 Сопряжение возможно если в структуре: 1) чередуются -связи, отделенные друг от друга одной -связью. Такой тип сопряжения называется , - сопряжение примеры:
Сопряжение возможно если в структуре: 1) чередуются -связи, отделенные друг от друга одной -связью. Такой тип сопряжения называется , - сопряжение примеры:
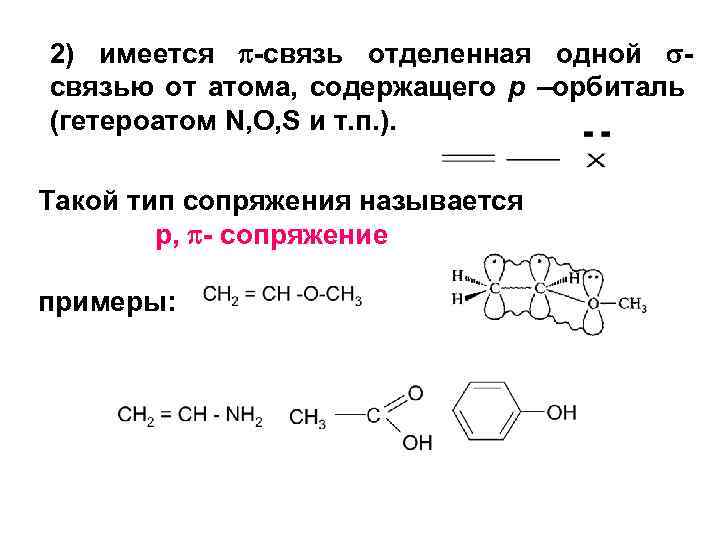 2) имеется -связь отделенная одной связью от атома, содержащего р –орбиталь (гетероатом N, O, S и т. п. ). Такой тип сопряжения называется р, - сопряжение примеры:
2) имеется -связь отделенная одной связью от атома, содержащего р –орбиталь (гетероатом N, O, S и т. п. ). Такой тип сопряжения называется р, - сопряжение примеры:
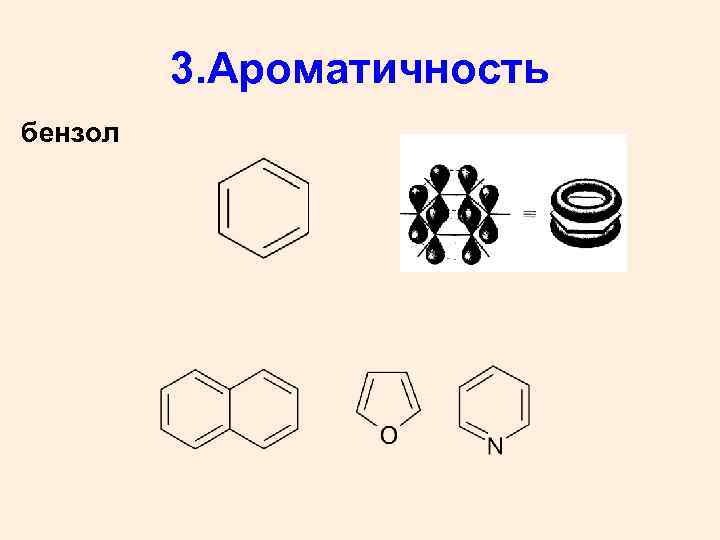 3. Ароматичность бензол
3. Ароматичность бензол
 Структурные признаки ароматичности • • • плоскостное строение циклического углеродного скелета (все атомы в sp 2 – гибридном состоянии); замкнутая -сопряженная система всех атомов цикла; сумма сопряженных электронов соответствует формуле Хюккеля 4 n+ 2 = ē в сопряжении, где n – целое число
Структурные признаки ароматичности • • • плоскостное строение циклического углеродного скелета (все атомы в sp 2 – гибридном состоянии); замкнутая -сопряженная система всех атомов цикла; сумма сопряженных электронов соответствует формуле Хюккеля 4 n+ 2 = ē в сопряжении, где n – целое число
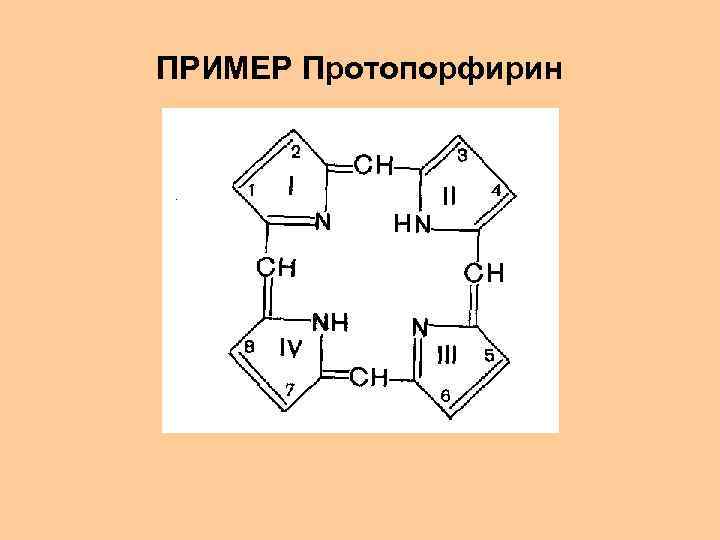 ПРИМЕР Протопорфирин
ПРИМЕР Протопорфирин
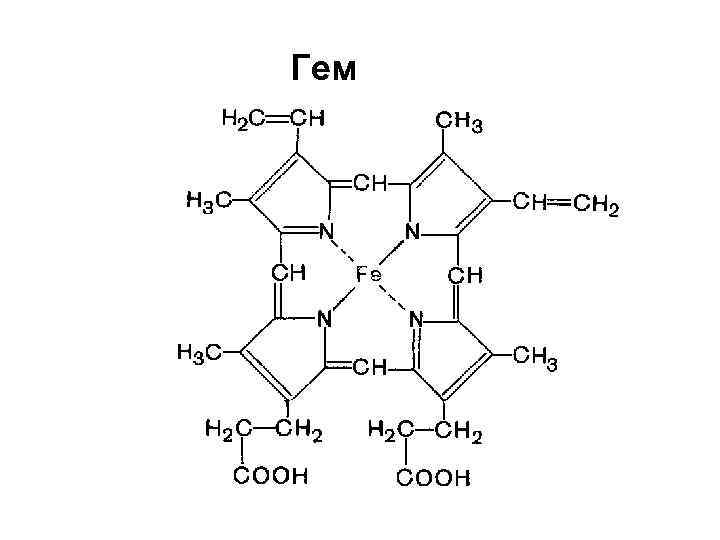 Гем
Гем
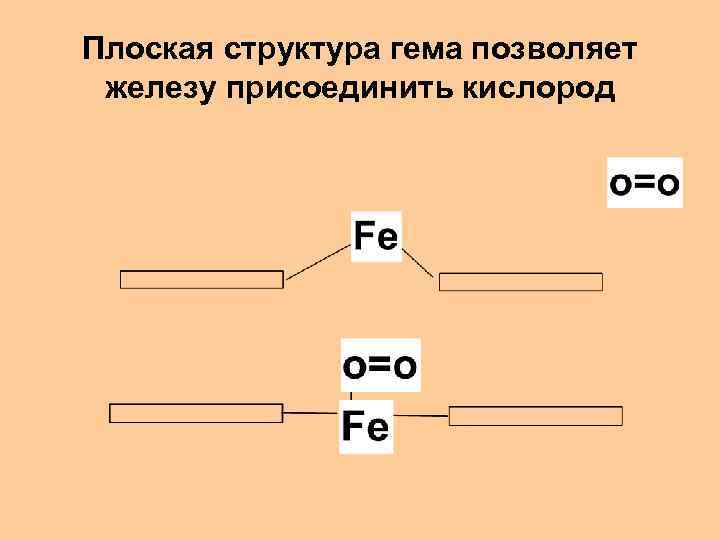 Плоская структура гема позволяет железу присоединить кислород
Плоская структура гема позволяет железу присоединить кислород
 Взаимное влияние атомов в органических молекулах
Взаимное влияние атомов в органических молекулах
 Индуктивный электронный эффект ( I) Сравнительная электроотрицательность F O N Csp 2 Csp 3 уменьшение -I +I
Индуктивный электронный эффект ( I) Сравнительная электроотрицательность F O N Csp 2 Csp 3 уменьшение -I +I
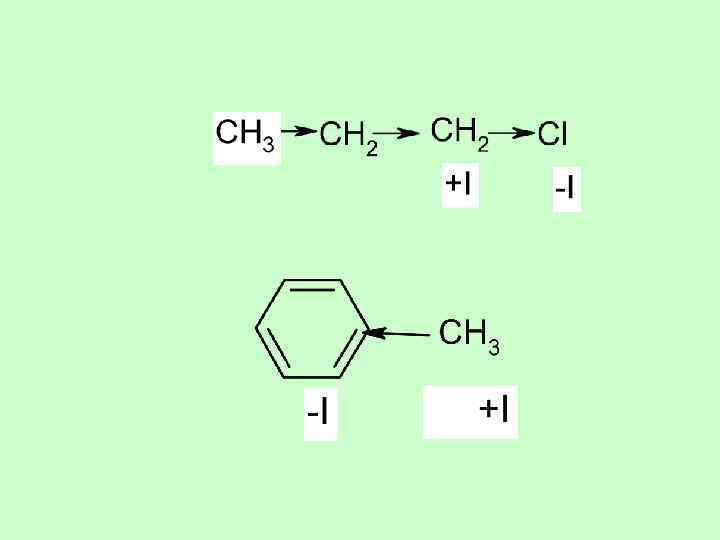
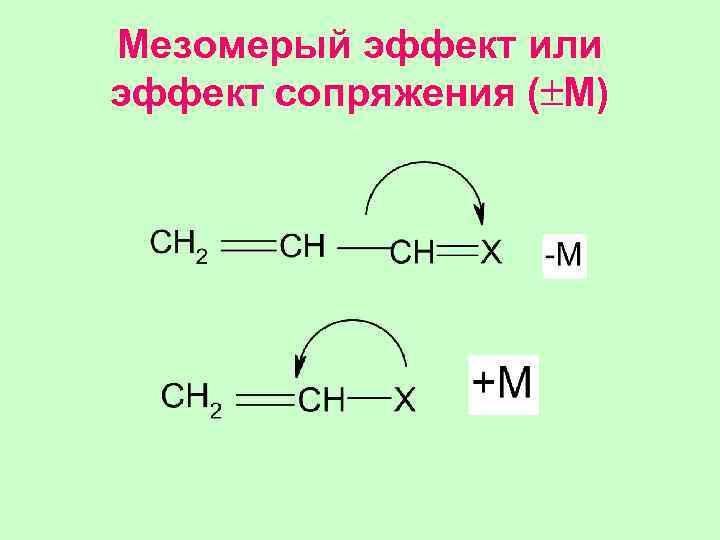 Мезомерый эффект или эффект сопряжения ( M)
Мезомерый эффект или эффект сопряжения ( M)
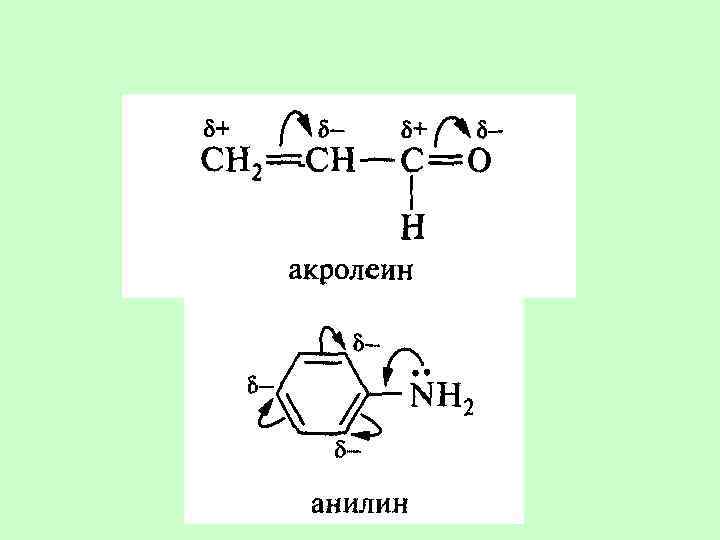
 Электронный эффекты заместителей
Электронный эффекты заместителей
 Реакционная способность органических соединений
Реакционная способность органических соединений
 Виды химических реакций I. Кислотно-основные II. Окислительно-восстановительные реакции III. Характерные реакции органических соединений IV. Качественные реакции
Виды химических реакций I. Кислотно-основные II. Окислительно-восстановительные реакции III. Характерные реакции органических соединений IV. Качественные реакции
 I. Кислотно-основные свойства органических соединений Кислота R-XH Кислотный центр -ХН -SH, -OH, -NH, -CH Основание H-X Основный центр –Х n-основания: Гетероатом с неподеленной электронной парой -Основания : -Связь между атомами углерода
I. Кислотно-основные свойства органических соединений Кислота R-XH Кислотный центр -ХН -SH, -OH, -NH, -CH Основание H-X Основный центр –Х n-основания: Гетероатом с неподеленной электронной парой -Основания : -Связь между атомами углерода
 Сравнительная сила кислот R – XH = кислота R-X- + H+ сопряженное основание (анион) Усиливают кислотность: сопряжение с кислотным центром большой радиус атома в кислотном центре высокая электроотрицательность атома в кислотном центре электроноакцепторные заместители в молекуле кислоты
Сравнительная сила кислот R – XH = кислота R-X- + H+ сопряженное основание (анион) Усиливают кислотность: сопряжение с кислотным центром большой радиус атома в кислотном центре высокая электроотрицательность атома в кислотном центре электроноакцепторные заместители в молекуле кислоты
 карбоновые кислоты фенолы тиолы многоатомные спирты одноатомные спирты амины
карбоновые кислоты фенолы тиолы многоатомные спирты одноатомные спирты амины
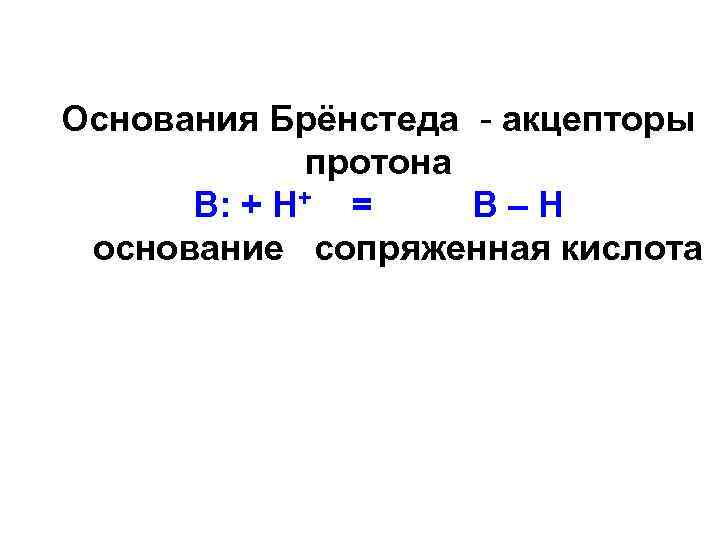 Основания Брёнстеда - акцепторы протона В: + Н+ = В–Н основание сопряженная кислота
Основания Брёнстеда - акцепторы протона В: + Н+ = В–Н основание сопряженная кислота
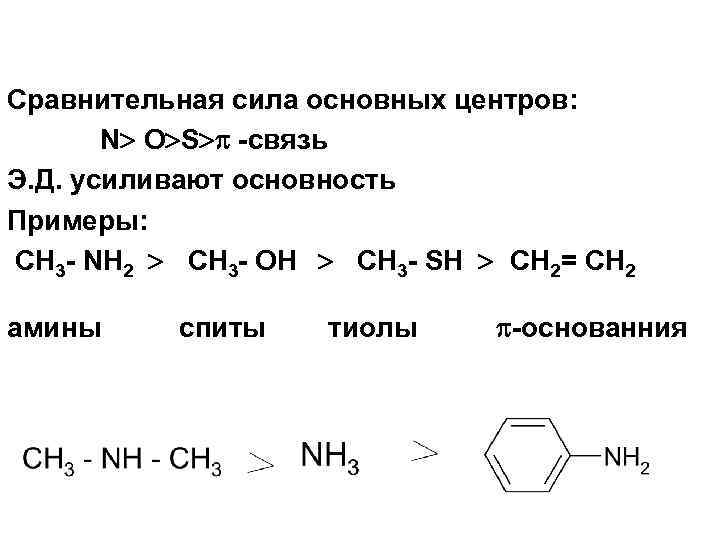 Сравнительная сила основных центров: N O S -связь Э. Д. усиливают основность Примеры: CH 3 - NH 2 CH 3 - OH CH 3 - SH CH 2= CH 2 амины спиты тиолы -основанния
Сравнительная сила основных центров: N O S -связь Э. Д. усиливают основность Примеры: CH 3 - NH 2 CH 3 - OH CH 3 - SH CH 2= CH 2 амины спиты тиолы -основанния
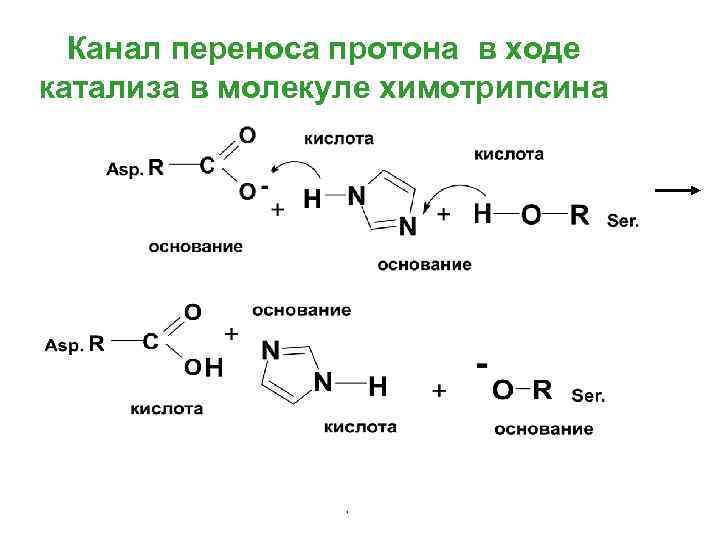 Канал переноса протона в ходе катализа в молекуле химотрипсина
Канал переноса протона в ходе катализа в молекуле химотрипсина
 Характерные реакции органических соединений
Характерные реакции органических соединений
 Основные понятия • Субстрат – вещество, у которого происходит разрыв связи у атома углерода. Определяет тип реакции • Реагент – вещество (частица), атакующая субстрат (радикал, электрофил, нуклеофил). Определяет механизм реакции.
Основные понятия • Субстрат – вещество, у которого происходит разрыв связи у атома углерода. Определяет тип реакции • Реагент – вещество (частица), атакующая субстрат (радикал, электрофил, нуклеофил). Определяет механизм реакции.
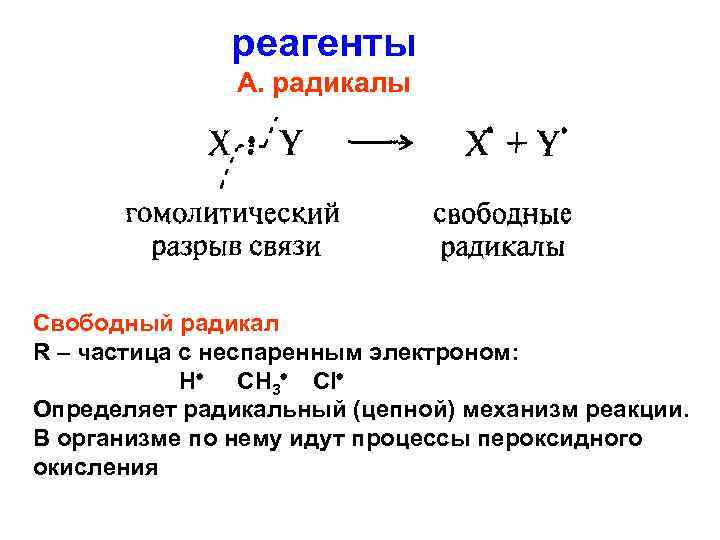 реагенты А. радикалы Свободный радикал R – частица с неспаренным электроном: Н СН 3 Сl Определяет радикальный (цепной) механизм реакции. В организме по нему идут процессы пероксидного окисления
реагенты А. радикалы Свободный радикал R – частица с неспаренным электроном: Н СН 3 Сl Определяет радикальный (цепной) механизм реакции. В организме по нему идут процессы пероксидного окисления
 Б. нуклеофилы и электрофилы • Нуклеофил –реагент с целым или частичным отрицательным зарядом (анион или молекула), содержит неподеленную электронную пару: ОН- , NH 3 , H 2 O , CH 3 OH , Электрофил - реагент с целым или частичным положительным зарядом (катион или молекула): Н+ , SO 3
Б. нуклеофилы и электрофилы • Нуклеофил –реагент с целым или частичным отрицательным зарядом (анион или молекула), содержит неподеленную электронную пару: ОН- , NH 3 , H 2 O , CH 3 OH , Электрофил - реагент с целым или частичным положительным зарядом (катион или молекула): Н+ , SO 3
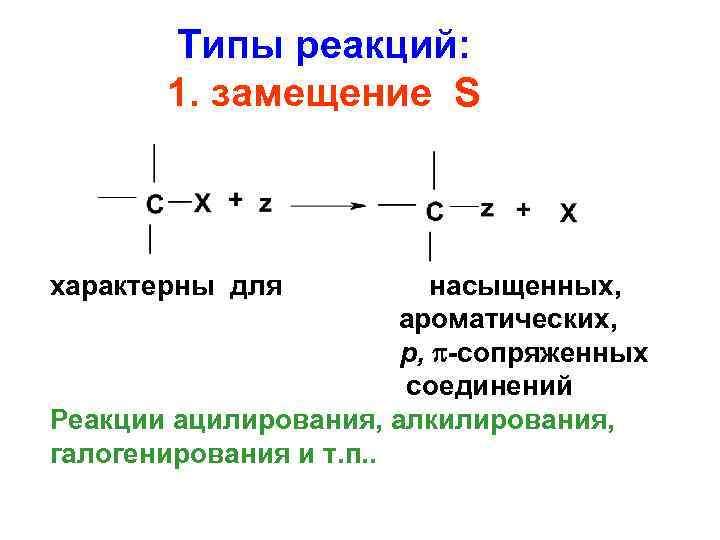 Типы реакций: 1. замещение S характерны для насыщенных, ароматических, р, -сопряженных соединений Реакции ацилирования, алкилирования, галогенирования и т. п. .
Типы реакций: 1. замещение S характерны для насыщенных, ароматических, р, -сопряженных соединений Реакции ацилирования, алкилирования, галогенирования и т. п. .
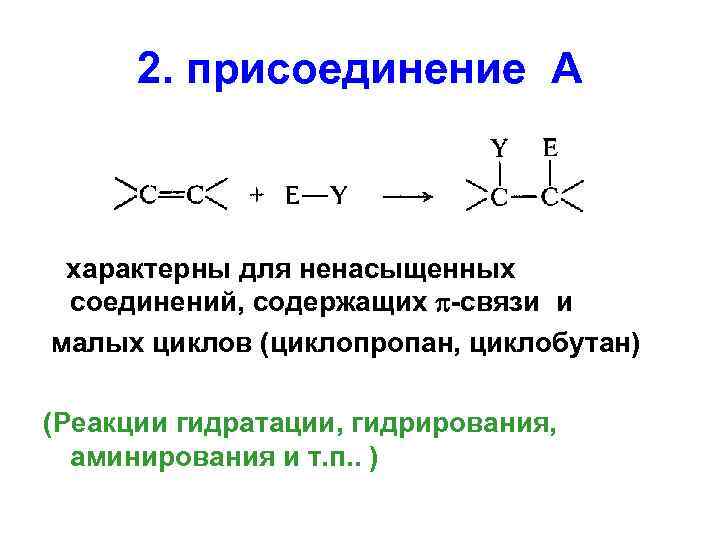 2. присоединение А характерны для ненасыщенных соединений, содержащих -связи и малых циклов (циклопропан, циклобутан) (Реакции гидратации, гидрирования, аминирования и т. п. . )
2. присоединение А характерны для ненасыщенных соединений, содержащих -связи и малых циклов (циклопропан, циклобутан) (Реакции гидратации, гидрирования, аминирования и т. п. . )
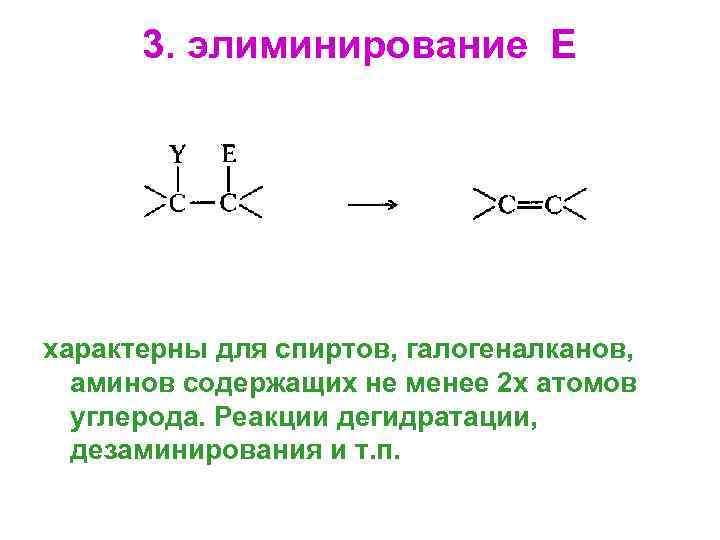 3. элиминирование Е характерны для спиртов, галогеналканов, аминов содержащих не менее 2 х атомов углерода. Реакции дегидратации, дезаминирования и т. п.
3. элиминирование Е характерны для спиртов, галогеналканов, аминов содержащих не менее 2 х атомов углерода. Реакции дегидратации, дезаминирования и т. п.
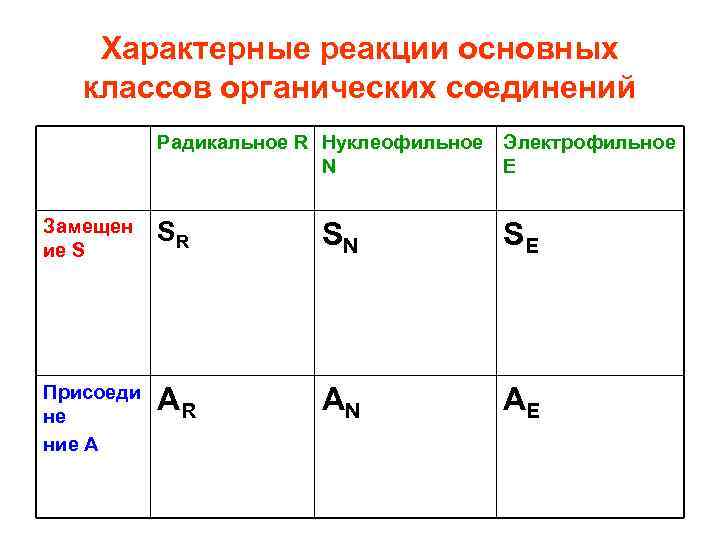 Характерные реакции основных классов органических соединений Радикальное R Нуклеофильное Электрофильное N Е Замещен ие S SR SN SE Присоеди не ние А AR AN AE
Характерные реакции основных классов органических соединений Радикальное R Нуклеофильное Электрофильное N Е Замещен ие S SR SN SE Присоеди не ние А AR AN AE
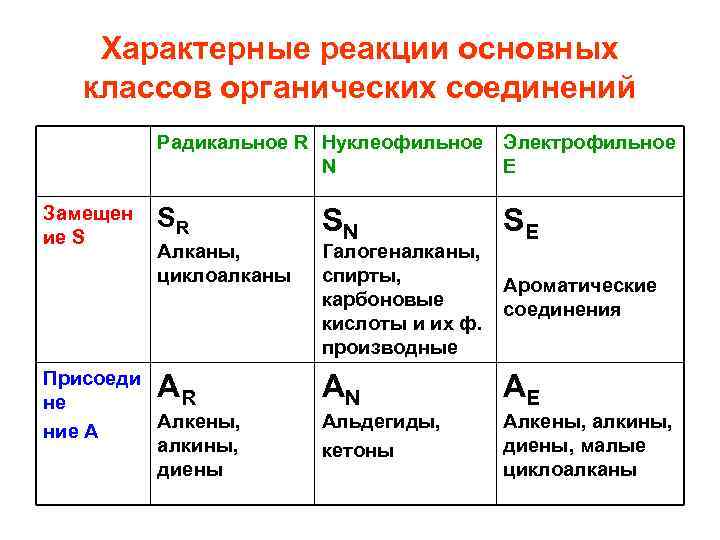 Характерные реакции основных классов органических соединений Радикальное R Нуклеофильное Электрофильное N Е Замещен ие S SR Алканы, циклоалканы Присоеди R не Алкены, ние А алкины, диены A SN Галогеналканы, спирты, карбоновые кислоты и их ф. производные SE Ароматические соединения AN AE Альдегиды, кетоны Алкены, алкины, диены, малые циклоалканы
Характерные реакции основных классов органических соединений Радикальное R Нуклеофильное Электрофильное N Е Замещен ие S SR Алканы, циклоалканы Присоеди R не Алкены, ние А алкины, диены A SN Галогеналканы, спирты, карбоновые кислоты и их ф. производные SE Ароматические соединения AN AE Альдегиды, кетоны Алкены, алкины, диены, малые циклоалканы
 Электронодоноры активизируют субстрат в реакциях электрофильного замещения SE или присоединения AE Электроноакцепторы активизируют субстрат в реакциях нуклеофильного SN замещения или присоединения AN.
Электронодоноры активизируют субстрат в реакциях электрофильного замещения SE или присоединения AE Электроноакцепторы активизируют субстрат в реакциях нуклеофильного SN замещения или присоединения AN.



