Кислоты и основания Лекция 16 по курсу














16_Кислоты и основания.ppt
- Количество слайдов: 23
 Кислоты и основания Лекция 16 по курсу «Общая химия»
Кислоты и основания Лекция 16 по курсу «Общая химия»
 Инь и Ян химии Основание Кислота
Инь и Ян химии Основание Кислота
 Теория электролитической диссоциации: недостатки • Применимо только к водным растворам, исключая: а) реакции в газовой и твердой фазе б) неводные растворы • Не все вещества, ведущие себя как кислоты, подходят под описание с точки зрения ТЭД.
Теория электролитической диссоциации: недостатки • Применимо только к водным растворам, исключая: а) реакции в газовой и твердой фазе б) неводные растворы • Не все вещества, ведущие себя как кислоты, подходят под описание с точки зрения ТЭД.
 Протолитическая теория (1923) Й. Н. Брёнстед Т. М. Лоури • Кислота – донор протона, основание – акцептор протона. • У каждой кислоты есть сопряженное ей основание (кислота минус протон): HF => F– • Чем > доля переданных (принятых) протонов, тем сильнее кислота (основание). • Равновесие смещено в сторону более слабых кислот и оснований
Протолитическая теория (1923) Й. Н. Брёнстед Т. М. Лоури • Кислота – донор протона, основание – акцептор протона. • У каждой кислоты есть сопряженное ей основание (кислота минус протон): HF => F– • Чем > доля переданных (принятых) протонов, тем сильнее кислота (основание). • Равновесие смещено в сторону более слабых кислот и оснований
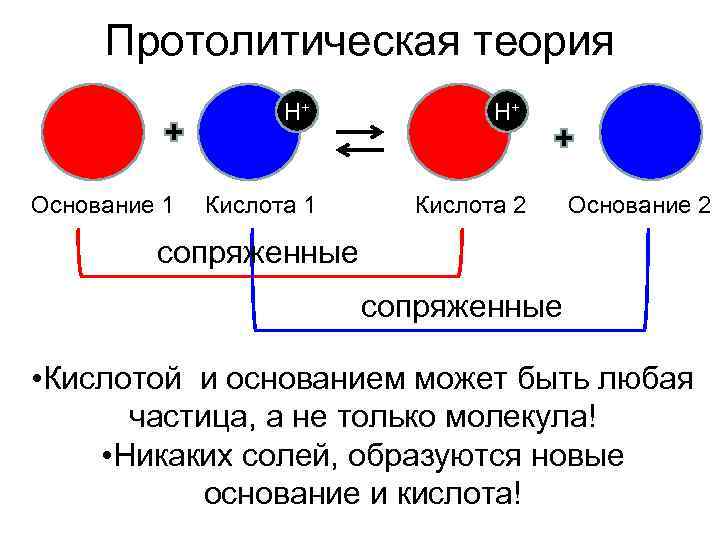
 Протолитическая теория H+ Основание 1 Кислота 1 Кислота 2 Основание 2 сопряженные сопряженные • Кислотой и основанием может быть любая частица, а не только молекула! • Никаких солей, образуются новые основание и кислота!
Протолитическая теория H+ Основание 1 Кислота 1 Кислота 2 Основание 2 сопряженные сопряженные • Кислотой и основанием может быть любая частица, а не только молекула! • Никаких солей, образуются новые основание и кислота!
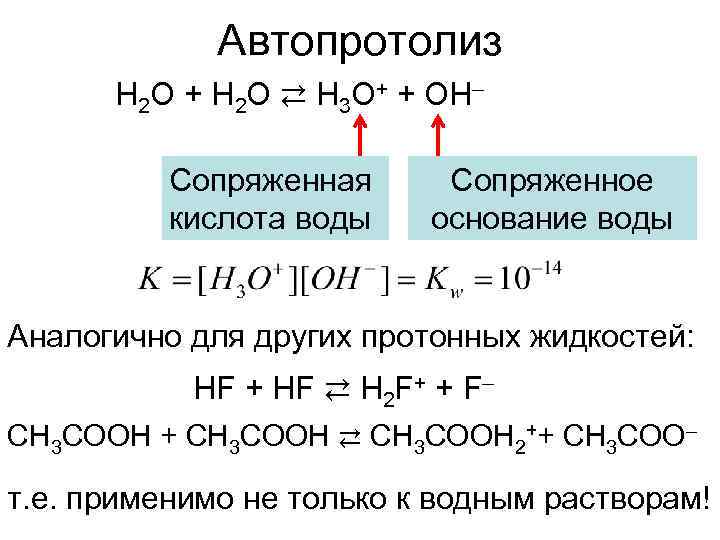
 Автопротолиз H 2 O + H 2 O ⇄ H 3 O+ + OH– Сопряженная Сопряженное кислота воды основание воды Аналогично для других протонных жидкостей: HF + HF ⇄ H 2 F+ + F– CH 3 COOH + CH 3 COOH ⇄ CH 3 COOH 2++ CH 3 COO– т. е. применимо не только к водным растворам!
Автопротолиз H 2 O + H 2 O ⇄ H 3 O+ + OH– Сопряженная Сопряженное кислота воды основание воды Аналогично для других протонных жидкостей: HF + HF ⇄ H 2 F+ + F– CH 3 COOH + CH 3 COOH ⇄ CH 3 COOH 2++ CH 3 COO– т. е. применимо не только к водным растворам!
 Константы ионизации для сопряженных кислот и оснований HF + H 2 O ⇄ H 3 O+ + F– + H 2 O ⇄ HF + OH– Аналогично для других растворителей!
Константы ионизации для сопряженных кислот и оснований HF + H 2 O ⇄ H 3 O+ + F– + H 2 O ⇄ HF + OH– Аналогично для других растворителей!
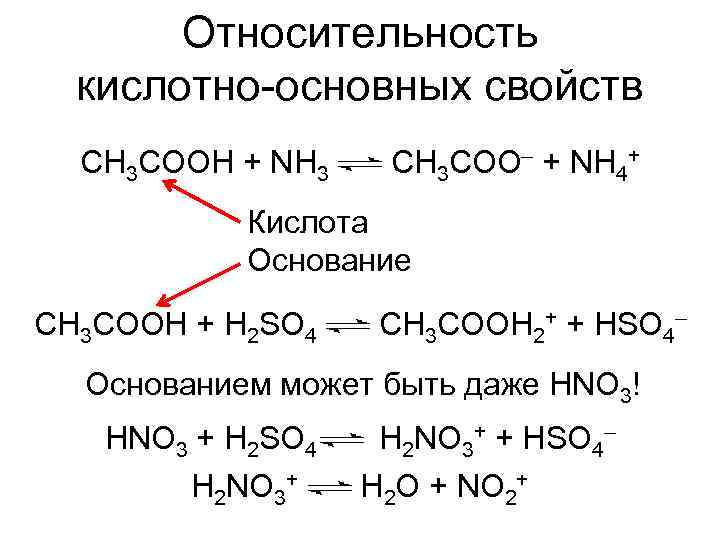
 Относительность кислотно-основных свойств CH 3 COOH + NH 3 CH 3 COO– + NH 4+ Кислота Основание CH 3 COOH + H 2 SO 4 CH 3 COOH 2+ + HSO 4– Основанием может быть даже HNO 3! HNO 3 + H 2 SO 4 H 2 NO 3+ + HSO 4– H 2 NO 3+ H 2 O + NO 2+
Относительность кислотно-основных свойств CH 3 COOH + NH 3 CH 3 COO– + NH 4+ Кислота Основание CH 3 COOH + H 2 SO 4 CH 3 COOH 2+ + HSO 4– Основанием может быть даже HNO 3! HNO 3 + H 2 SO 4 H 2 NO 3+ + HSO 4– H 2 NO 3+ H 2 O + NO 2+
 Суперкислоты (1968) Соединения, исключительно склонные отдавать протон HF + Sb. F 5 = H+[Sb. F 6]– HSO 3 F + Sb. F 5 = HSO 3+[Sb. F 6]– «Магическая кислота» Дж. А. Ола В суперкислотах протонируются даже алканы! CH 4 + H+ → CH 5+ → CH 3+ + H 2 ? ? ? CH 3+ + 3 CH 4 → (CH 3)3 C+ + 3 H 2
Суперкислоты (1968) Соединения, исключительно склонные отдавать протон HF + Sb. F 5 = H+[Sb. F 6]– HSO 3 F + Sb. F 5 = HSO 3+[Sb. F 6]– «Магическая кислота» Дж. А. Ола В суперкислотах протонируются даже алканы! CH 4 + H+ → CH 5+ → CH 3+ + H 2 ? ? ? CH 3+ + 3 CH 4 → (CH 3)3 C+ + 3 H 2
 Ограничения протолитической теории • Неприменима к реакциям без растворителя; • Неприменима к полностью апротонным (не содержащим катионов водорода и их источников) средам • Не объясняет некоторых наблюдаемых фактов (см. следующий слайд)
Ограничения протолитической теории • Неприменима к реакциям без растворителя; • Неприменима к полностью апротонным (не содержащим катионов водорода и их источников) средам • Не объясняет некоторых наблюдаемых фактов (см. следующий слайд)
 Что за вещество? • Тяжелая жидкость с едким, раздражающим запахом; • «Дымит» на воздухе; • Бурно реагирует со щелочами и NH 3; • Дает солеобразные кристаллические 4!!! Sn. Cl соединения с органическими основаниями • Растворяется в воде с сильным выделением тепла; • Раствор имеет p. H << 7;
Что за вещество? • Тяжелая жидкость с едким, раздражающим запахом; • «Дымит» на воздухе; • Бурно реагирует со щелочами и NH 3; • Дает солеобразные кристаллические 4!!! Sn. Cl соединения с органическими основаниями • Растворяется в воде с сильным выделением тепла; • Раствор имеет p. H << 7;
 Электронная теория (1923) Кислоты – акцепторы пары электронов (имеют вакантные орбитали) BF 3, Al. Cl 3, NO 2+, H+, катионы металлов… Основания – доноры пары электронов (имеют неподеленные пары) Г. Н. Льюис OH–, Cl–, F –, NH 3, H 2 O, CH 3 COO– и т. д.
Электронная теория (1923) Кислоты – акцепторы пары электронов (имеют вакантные орбитали) BF 3, Al. Cl 3, NO 2+, H+, катионы металлов… Основания – доноры пары электронов (имеют неподеленные пары) Г. Н. Льюис OH–, Cl–, F –, NH 3, H 2 O, CH 3 COO– и т. д.
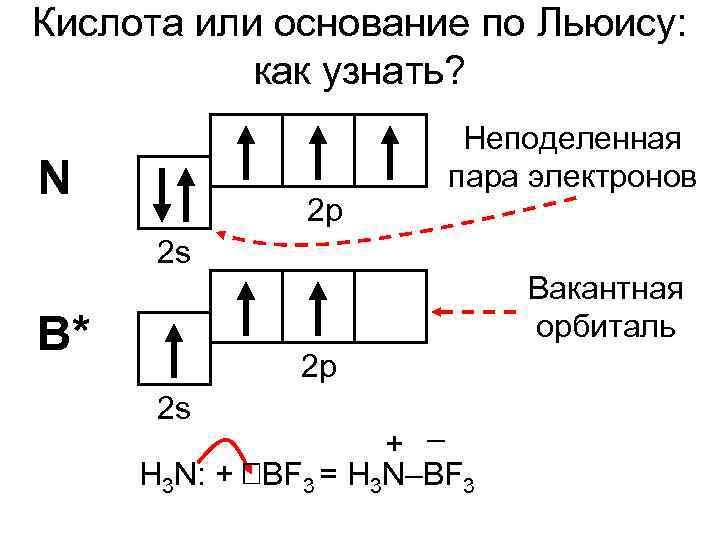
 Кислота или основание по Льюису: как узнать? Неподеленная N пара электронов 2 p 2 s Вакантная B* орбиталь 2 p 2 s + – H 3 N: + BF 3 = H 3 N–BF 3
Кислота или основание по Льюису: как узнать? Неподеленная N пара электронов 2 p 2 s Вакантная B* орбиталь 2 p 2 s + – H 3 N: + BF 3 = H 3 N–BF 3
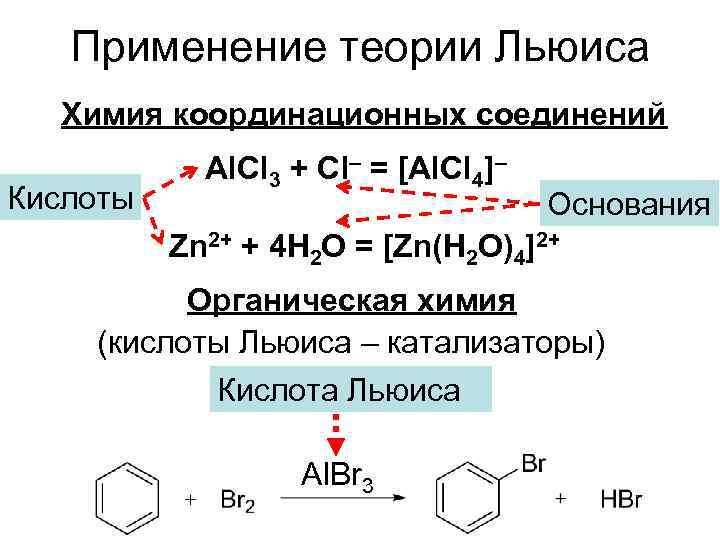
 Применение теории Льюиса Химия координационных соединений Al. Cl 3 + Cl– = [Al. Cl 4]– Кислоты Основания Zn 2+ + 4 H 2 O = [Zn(H 2 O)4]2+ Органическая химия (кислоты Льюиса – катализаторы) Кислота Льюиса Al. Br 3
Применение теории Льюиса Химия координационных соединений Al. Cl 3 + Cl– = [Al. Cl 4]– Кислоты Основания Zn 2+ + 4 H 2 O = [Zn(H 2 O)4]2+ Органическая химия (кислоты Льюиса – катализаторы) Кислота Льюиса Al. Br 3
 Ограничения теории Льюиса • Не работает для некоторых протонных кислот: HF + NH 3 = NH 4 F – но у HF нет вакантных орбиталей! • Не всегда может объяснить амфотерность (H 2 O амфотерна, но у нее только неподеленные пары!) • Не учитывает взаимного влияния атомов и групп: Неподеленная пара ? ? ? Кислота Льюиса
Ограничения теории Льюиса • Не работает для некоторых протонных кислот: HF + NH 3 = NH 4 F – но у HF нет вакантных орбиталей! • Не всегда может объяснить амфотерность (H 2 O амфотерна, но у нее только неподеленные пары!) • Не учитывает взаимного влияния атомов и групп: Неподеленная пара ? ? ? Кислота Льюиса
 Теория реакций в расплаве Лукса – Флуда • Применяется для реакций между кислородсодержащими соединениями • Хорошо описывает взаимодействия в расплаве • Кислота – акцептор аниона O 2–, основание – донор аниона O 2–. Si. O 2 + Ca. O = Ca. Si. O 3 Кислота Основание
Теория реакций в расплаве Лукса – Флуда • Применяется для реакций между кислородсодержащими соединениями • Хорошо описывает взаимодействия в расплаве • Кислота – акцептор аниона O 2–, основание – донор аниона O 2–. Si. O 2 + Ca. O = Ca. Si. O 3 Кислота Основание
 Теория «ониевых солей» Ганча • Главный признак кислотно- основной реакции – солеобразование; • То, что превращается в анион – кислота, то, что в катион – основание: Теория пригодна как для водных, А. Р. Ганч так и для неводных сред (C 2 H 5)2 O + HCl. O 4 = (C 2 H 5)2 OH+ Cl. O 4– Основание Кислота
Теория «ониевых солей» Ганча • Главный признак кислотно- основной реакции – солеобразование; • То, что превращается в анион – кислота, то, что в катион – основание: Теория пригодна как для водных, А. Р. Ганч так и для неводных сред (C 2 H 5)2 O + HCl. O 4 = (C 2 H 5)2 OH+ Cl. O 4– Основание Кислота
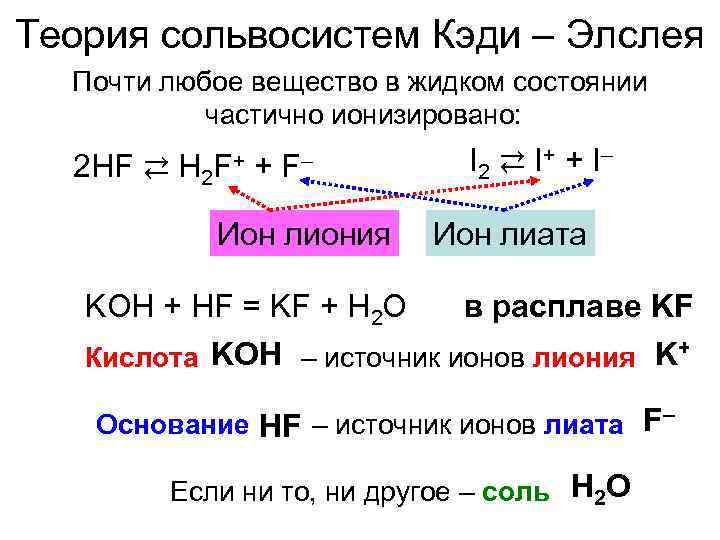
 Теория сольвосистем Кэди – Элслея Почти любое вещество в жидком состоянии частично ионизировано: 2 HF ⇄ H 2 F+ + F– I 2 ⇄ I + + I – Ион лиония Ион лиата KOH + HF = KF + H 2 O в расплаве KF Кислота KOH – источник ионов лиония K+ Основание HF – источник ионов лиата F– Если ни то, ни другое – соль H 2 O
Теория сольвосистем Кэди – Элслея Почти любое вещество в жидком состоянии частично ионизировано: 2 HF ⇄ H 2 F+ + F– I 2 ⇄ I + + I – Ион лиония Ион лиата KOH + HF = KF + H 2 O в расплаве KF Кислота KOH – источник ионов лиония K+ Основание HF – источник ионов лиата F– Если ни то, ни другое – соль H 2 O
 Обобщенная теория кислот и оснований Усановича (1938 г. ) • Кислота – донор катиона О сладкий плод твоих исканий - или акцептор аниона Закон суровый и простой: • Основание – донор аниона Нет ни кислот, ни оснований! или акцептор катиона И кислоту без оснований Всегда считали кислотой. ē: Анион – в том числе А. А. Гухман 2 Fe 3+ + 2 I– = 2 Fe 2+ + I 2 Окислитель Восстановитель Акцептор ē Донор ē М. И. Усанович Кислота Основание (1896– 1981) «Кислоты и основания – это не классы соединений; кислотность и основность – это функции вещества. Будет ли вещество кислотой или основанием, зависит от партнера» .
Обобщенная теория кислот и оснований Усановича (1938 г. ) • Кислота – донор катиона О сладкий плод твоих исканий - или акцептор аниона Закон суровый и простой: • Основание – донор аниона Нет ни кислот, ни оснований! или акцептор катиона И кислоту без оснований Всегда считали кислотой. ē: Анион – в том числе А. А. Гухман 2 Fe 3+ + 2 I– = 2 Fe 2+ + I 2 Окислитель Восстановитель Акцептор ē Донор ē М. И. Усанович Кислота Основание (1896– 1981) «Кислоты и основания – это не классы соединений; кислотность и основность – это функции вещества. Будет ли вещество кислотой или основанием, зависит от партнера» .
 Теория ЖМКО: жестких и мягких кислот и оснований Пирсона (1963) Жесткие частицы: • Маленький радиус (объем) • Высокая степень окисления • Высокая электроотрицательность Мягкие частицы: • Большой радиус (объем) • Низкая степень окисления • Низкая Р. Г. Пирсон электроотрицательность Жесткое с жестким, мягкое с мягким!
Теория ЖМКО: жестких и мягких кислот и оснований Пирсона (1963) Жесткие частицы: • Маленький радиус (объем) • Высокая степень окисления • Высокая электроотрицательность Мягкие частицы: • Большой радиус (объем) • Низкая степень окисления • Низкая Р. Г. Пирсон электроотрицательность Жесткое с жестким, мягкое с мягким!
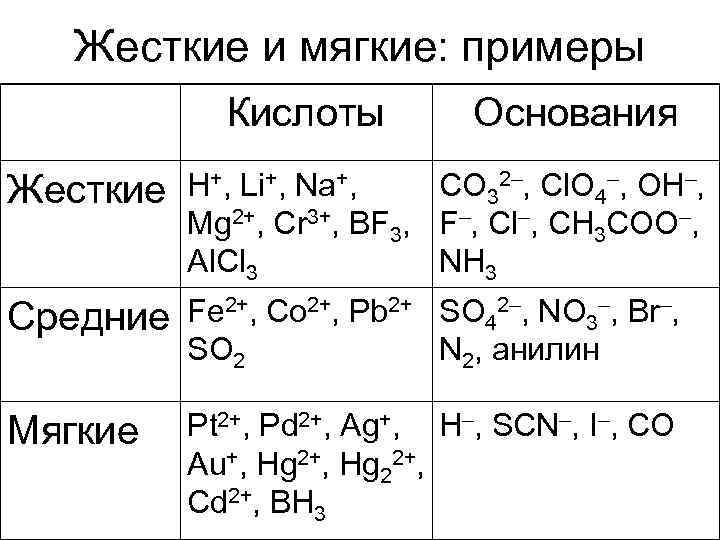
 Жесткие и мягкие: примеры Кислоты Основания Жесткие H+, Li+, Na+, CO 32–, Cl. O 4–, OH–, Mg 2+, Cr 3+, BF 3, F–, Cl–, CH 3 COO–, Al. Cl 3 NH 3 Средние Fe 2+, Co 2+, Pb 2+ SO 42–, NO 3–, Br–, SO 2 N 2, анилин Мягкие Pt 2+, Pd 2+, Ag+, H–, SCN–, I–, CO Au+, Hg 22+, Cd 2+, BH 3
Жесткие и мягкие: примеры Кислоты Основания Жесткие H+, Li+, Na+, CO 32–, Cl. O 4–, OH–, Mg 2+, Cr 3+, BF 3, F–, Cl–, CH 3 COO–, Al. Cl 3 NH 3 Средние Fe 2+, Co 2+, Pb 2+ SO 42–, NO 3–, Br–, SO 2 N 2, анилин Мягкие Pt 2+, Pd 2+, Ag+, H–, SCN–, I–, CO Au+, Hg 22+, Cd 2+, BH 3
 Теории кислотно-основного взаимодействия Теория Кислота Основание Электроли- Образует при тической диссоциации только Н+ только ОН– Протолити- Донор Н+ Акцептор Н+ ческая (Брёнстед, Лоури) Электронная Акцептор Донор (Льюис) электронной пары
Теории кислотно-основного взаимодействия Теория Кислота Основание Электроли- Образует при тической диссоциации только Н+ только ОН– Протолити- Донор Н+ Акцептор Н+ ческая (Брёнстед, Лоури) Электронная Акцептор Донор (Льюис) электронной пары
 Теории кислотно-основного взаимодействия (окончание) Теория Кислота Основание Реакций в рас- Акцептор O 2– Донор O 2– плаве (Лукс, Флуд) Ониевых солей Превращается в анион в Превращается в катион (Ганч) составе продукта в составе продукта Сольвосистем Образует тот же катион, Образует тот же анион, (Кэди, Элслей) что и растворитель Обобщенная Донор катиона/акцептор Донор аниона/акцептор (Усановича) аниона катиона ЖМКО Акцептор электронной Донор электронной (Пирсона) плотности
Теории кислотно-основного взаимодействия (окончание) Теория Кислота Основание Реакций в рас- Акцептор O 2– Донор O 2– плаве (Лукс, Флуд) Ониевых солей Превращается в анион в Превращается в катион (Ганч) составе продукта в составе продукта Сольвосистем Образует тот же катион, Образует тот же анион, (Кэди, Элслей) что и растворитель Обобщенная Донор катиона/акцептор Донор аниона/акцептор (Усановича) аниона катиона ЖМКО Акцептор электронной Донор электронной (Пирсона) плотности

