кислоты.ppt
- Количество слайдов: 27

Кислоты Электронное пособие для 8 -го класса (по учебнику Рудзитис)

Определение Кислоты – это сложные вещества, в состав которых входят атомы водорода и кислотный остаток. Общая формула: Нn(КО)m

КОН, Cu. О, Н 2 СО 3, Nа 3 РО 4 , SО 2 Н 2 СО 3 Прослушайте аудиозапись определения кислот еще раз. Ø Ответьте на вопросы: 1. В данном ряду найдите формулу кислоты. Поясните. Ø 2. Как называется вторая часть формулы? Кислотный остаток 3

КЛАССИФИКАЦИЯ КИСЛОТ. 1. По содержанию кислорода. КИСЛОТЫ бескислородные кислородсодержащие HF HCl HBr HNO 3 H 2 SO 4 HI H 2 S H 2 CO 3 H 3 PO 4
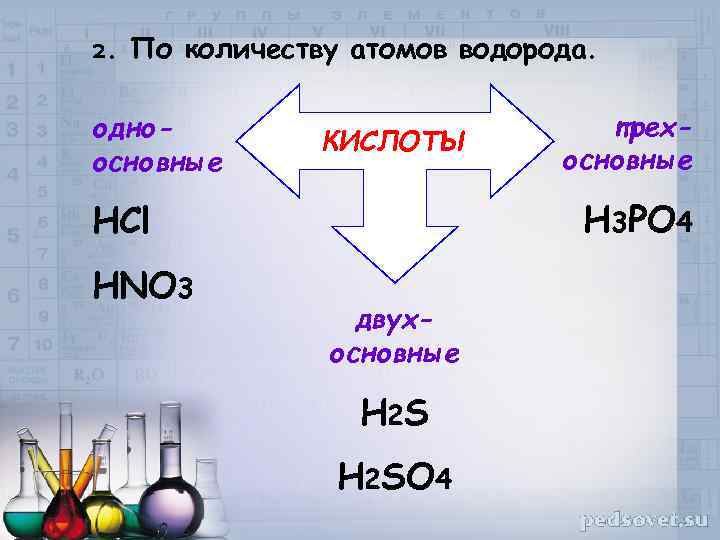
2. По количеству атомов водорода. одноосновные КИСЛОТЫ H 3 PO 4 HCl HNO 3 трехосновные двухосновные H 2 S H 2 SO 4

Порядок названий кислот: Каждой кислоте соответствует свой кислотный оксид. При этом валентность центрального атома в оксиде и в кислоте совпадают. Например в оксиде серы: IV II I IV II SO 2 в соответствующей кислоте Н 2 SO 3 V II I V II Р 2 О 5 и Н 3 РО 4 Валентность кислотного остатка определяется по количеству атомов водорода в кислоте!

Названия кислот и соответствующим им солям Кислот. Формула ный оксид кислоты Название кислоты SO 2 H 2 SO 3 H 2 SO 4 СО 2 H 2 СO 3 Si. O 2 H 2 Si. O 3 Кислотный остаток Валентность кислотног о остатка Название соли сернис- -SO 3 тая серная -SO 4 II сульфит II уголь- -СO 3 ная кремне -Si. O 3 вая II сульфат карбонат силикат II
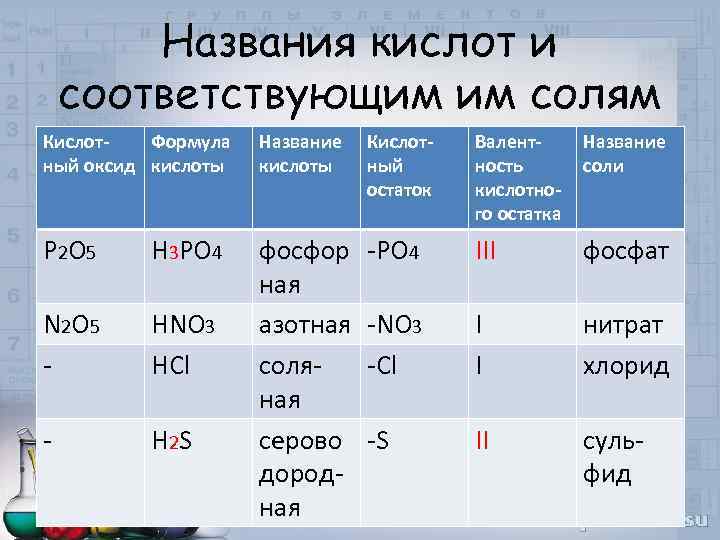
Названия кислот и соответствующим им солям Кислот. Формула ный оксид кислоты Название кислоты Кислотный остаток Валентность кислотного остатка Название соли Р 2 О 5 Н 3 РО 4 -РО 4 III фосфат N 2 O 5 - HNO 3 HCl -NO 3 -Cl I I нитрат хлорид - H 2 S фосфор ная азотная соляная серово дородная -S II сульфид

Физические свойства кислот • При обычных условиях кислоты могут быть твердыми и жидкими. • Кислоты –едкие жидкости (кроме кремневой), с кислым вкусом, без запаха, разъедают многие вещества. • Слабые кислоты угольная и сернистая при обычных условиях тут же разлагаются на кислотный оксид и воду: Н 2 SO 3 = SO 2 ↑ + H 2 O H 2 CO 3 = CO 2 ↑+ H 2 O

Получение: Бескислородные кислоты получают: - Взаимодействием неметалла с водородом: Н 2 + Сl 2 = 2 HCl - Действием на соль более сильной, или менее летучей кислотой: Fe. S + 2 HCl = Fe. Cl 2 + H 2 S↑ Полученные газообразные вещества растворяют в воде.

Получение: Кислородсодержащие кислоты можно получить: - Взаимодействием кислотных оксидов с водой (кроме оксида кремния (IV)): Р 2 О 5 + 3 Н 2 О = 2 Н 3 РО 4 - Действием на соль более сильной кислотой: Na 2 Si. O 3 +2 HCl =2 Na. Cl + H 2 Si. O 3↓

Химические свойства кислот 1. Универсальный индикатор - розовый ор индикат лакмус вода (нейтральная среда) й фиолетовы кислота (НСl, H 3 PO 4 , НNO 3, H 2 SO 4 ) (кислая среда) й красны
Действие индикаторов на кислоты

Химические свойства кислот: 2. Взаимодействие с металлами: Правило: Металлы, стоящие в ряду активности металлов до Н, вытесняют его из кислоты (исключение составляют концентрированная серная и любая азотная). 2 НСl + Zn = Zn. Cl 2 + H 2↑ Кислота + Ме = Соль + Н 2

Химические свойства кислот 3. Взаимодействие с основными оксидами: Правило: При взаимодействии основных оксидов с кислотами, образуется соль и вода. Сu. O + H 2 SO 4 = Cu. SO 4 + H 2 O (реакция идет при нагревании).

Химические свойства кислот

Химические свойства кислот 4. Взаимодействие кислот с основаниями: Правило: При взаимодействии растворимых и нерастворимых оснований с кислотами, образуется соль и вода. Реакция между кислотой и основанием называется реакцией нейтрализации. Н 2 СО 3 + 2 Na. OH = Na 2 CO 3 + 2 H 2 O

Химические свойства кислот

Химические свойства кислот 5. Взаимодействие с солями Правило: Более сильная кислота, вытесняет менее сильную из ее соли. Ряд активности кислот: HCl H 2 SO 4→HNO 3→H 3 PO 4→H 2 SO 3→H 2 CO 3→ H 2 S→H 2 Si. O 3 Примечание: кислоты в ряду расположены по мере ослабления своей силы.

Химические свойства кислот Для того, чтоб кислота прореагировала с солью, нужно чтоб она была сильнее той, которой образована соль. Пример: Са. СО 3 + 2 НСl = Ca. Cl 2 + H 2 CO 3→CO 2 ↓ H 2 O Не забываем, что H 2 CO 3 и H 2 SO 3 распадаются на кислотный оксид и воду, а H 2 Si. O 3 выпадает в осадок.

Химические свойства кислот

1. Формулы, каких веществ «лишние» и почему? 1)HCI 2)CO 2 3)Na. OH 4) H 2 SO 4 5) Na. CI 6) H 3 PO 4 7) HNO 3 9) Са. О 10) H 2 CO 3 11)Н 2 О 12)Н 2 Si. O 3 8) H 2 S

Соотнесите формулы и названия кислот Формулы Названия H 2 СО 3 СОЛЯНАЯ HСl УГОЛЬНАЯ H 2 SO 4 ФОСФОРНАЯ HNO 3 СЕРНАЯ H 3 PO 4 АЗОТНАЯ 23

Найдите кислотные остатки кислот и определите их валентность. II H 2 SO 4 III H 3 PO 4 I HСl I HNO 3 II H 2 СО 3 24

Закрепление: Составьте формулы солей: - Нитрата свинца (II) - Сульфата натрия - Карбоната кальция - Фосфата калия - Сульфита алюминия - Хлорида магния - Бромида серебра (I) - Сульфида натрия

Закрепление: С какими из перечисленных веществ будет взаимодействовать соляная кислота: оксид углерода (IV), сульфид калия, оксид магния, гидроксид алюминия, ртуть, сульфит лития, железо? Напишите соответствующие уравнения реакций.

Закрепление: Осуществите цепочки превращений: S→SO 2→H 2 SO 3→Li 2 SO 3→SO 2→Mg. SO 3→Mg. SO 4 P→P 2 O→K 3 PO 4→H 3 PO 4→Ca 3(PO 4)2→Ca. SO 4 C→CO 2→Ca. CO 3→Ca. O→Ca(OH)2→Ca(NO 3)2
кислоты.ppt