 Кислоты. 1. Названия 2. Получение 3. Свойства 4. Применение
Кислоты. 1. Названия 2. Получение 3. Свойства 4. Применение
 Кислоты l это сложные вещества, имеющие в своем составе водород, способный замещаться на металл, и кислотный остаток. Н Cl
Кислоты l это сложные вещества, имеющие в своем составе водород, способный замещаться на металл, и кислотный остаток. Н Cl
 Узнай загадочную кислоту “Из всех кислот она конечно, прима! Присутствует везде и зримо и не зримо. В животных и в растеньях есть она. С ней техника и медицина навсегда! Ее потомство “ацетаты” - очень нужные ребята, всем известный “аспирин” - он как добрый господин, жар больного понижает и здоровье возвращает!” Уксусная кислота
Узнай загадочную кислоту “Из всех кислот она конечно, прима! Присутствует везде и зримо и не зримо. В животных и в растеньях есть она. С ней техника и медицина навсегда! Ее потомство “ацетаты” - очень нужные ребята, всем известный “аспирин” - он как добрый господин, жар больного понижает и здоровье возвращает!” Уксусная кислота
 Самая важная кислота l l Для взрывчатых веществ нужна она, для красителей, лаков, лекарств идет самая важная из кислот. Фотопленка, целлулоид, полимеры, удобренья – вот ее примененье. Азотная кислота
Самая важная кислота l l Для взрывчатых веществ нужна она, для красителей, лаков, лекарств идет самая важная из кислот. Фотопленка, целлулоид, полимеры, удобренья – вот ее примененье. Азотная кислота
 Узнай загадочную кислоту Алхимикам удалось получить эту кислоту еще в X веке при прокаливании некоторых сульфатов (купоросов). Отсюда произошло ее историческое название – купоросное масло. Серная кислота
Узнай загадочную кислоту Алхимикам удалось получить эту кислоту еще в X веке при прокаливании некоторых сульфатов (купоросов). Отсюда произошло ее историческое название – купоросное масло. Серная кислота
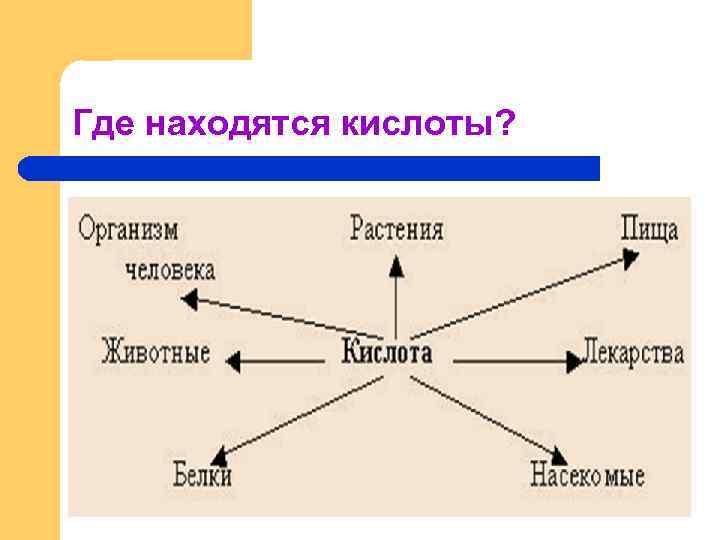 Где находятся кислоты?
Где находятся кислоты?
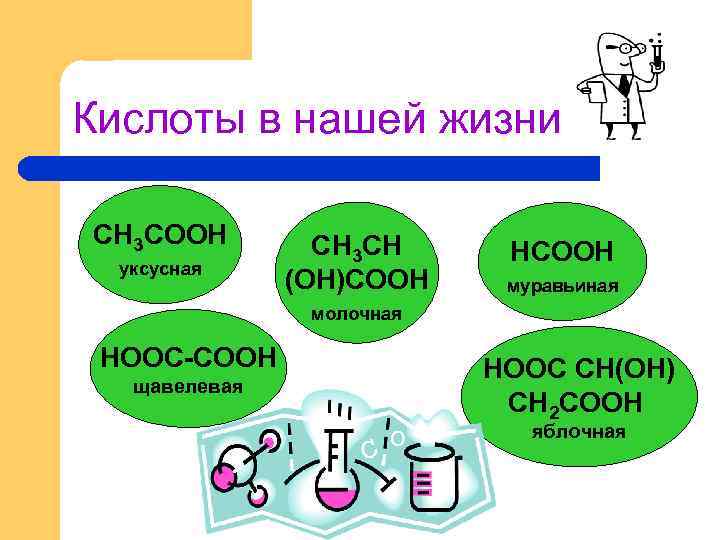 Кислоты в нашей жизни СH 3 COОH уксусная СH 3 CH (OH)COОH HCOОH муравьиная молочная НOОС-COОH щавелевая НOОС СН(ОН) СН 2 COОH яблочная
Кислоты в нашей жизни СH 3 COОH уксусная СH 3 CH (OH)COОH HCOОH муравьиная молочная НOОС-COОH щавелевая НOОС СН(ОН) СН 2 COОH яблочная
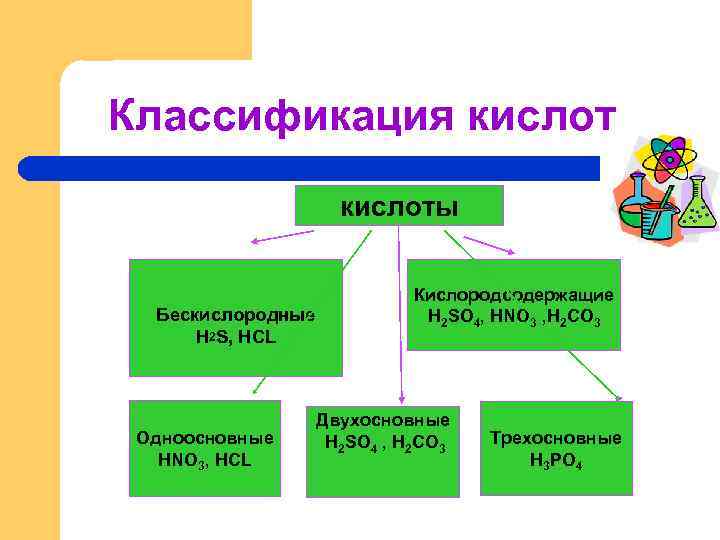 Классификация кислоты Бескислородные H 2 S, HCL Одноосновные HNO 3, HCL Кислородсодержащие H 2 SO 4, HNO 3 , H 2 CO 3 Двухосновные H 2 SO 4 , H 2 CO 3 Трехосновные H 3 PO 4
Классификация кислоты Бескислородные H 2 S, HCL Одноосновные HNO 3, HCL Кислородсодержащие H 2 SO 4, HNO 3 , H 2 CO 3 Двухосновные H 2 SO 4 , H 2 CO 3 Трехосновные H 3 PO 4
 Получение кислот
Получение кислот
 Получение кислот Кислотный оксид +Н 2 О = Кислота SO 3 + Н 2 О = Н 2 SO 4 l Простое вещ-во + Простое вещ-во = Кислота Н 2 + Cl 2 = 2 НCl l Соль + Кислота = Нерастворимая кислота Na 2 Si. O 3 + 2 НCl = Н 2 Si. O 3 + 2 Na. Cl l
Получение кислот Кислотный оксид +Н 2 О = Кислота SO 3 + Н 2 О = Н 2 SO 4 l Простое вещ-во + Простое вещ-во = Кислота Н 2 + Cl 2 = 2 НCl l Соль + Кислота = Нерастворимая кислота Na 2 Si. O 3 + 2 НCl = Н 2 Si. O 3 + 2 Na. Cl l
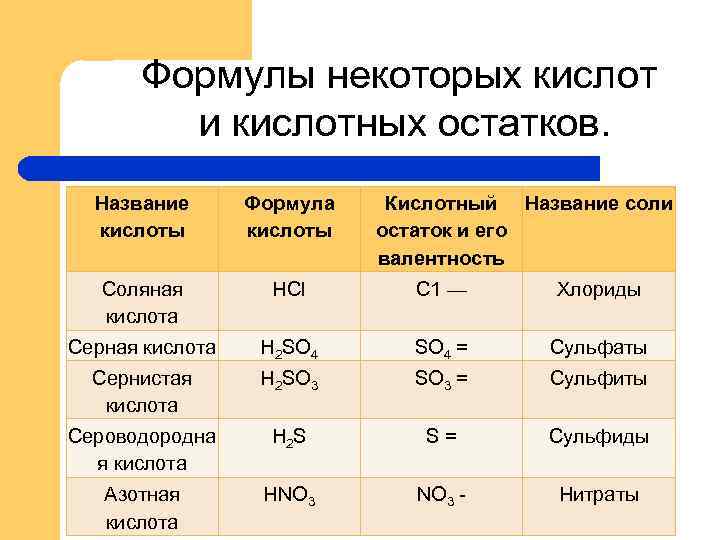 Формулы некоторых кислот и кислотных остатков. Название кислоты Формула кислоты Кислотный Название соли остаток и его валентность Соляная кислота НСl С 1 — Хлориды Серная кислота H 2 SO 4 = Сульфаты Сернистая кислота Н 2 SО 3 SO 3 = Сульфиты Сероводородна я кислота H 2 S S= Сульфиды Азотная кислота НNО 3 NO 3 - Нитраты
Формулы некоторых кислот и кислотных остатков. Название кислоты Формула кислоты Кислотный Название соли остаток и его валентность Соляная кислота НСl С 1 — Хлориды Серная кислота H 2 SO 4 = Сульфаты Сернистая кислота Н 2 SО 3 SO 3 = Сульфиты Сероводородна я кислота H 2 S S= Сульфиды Азотная кислота НNО 3 NO 3 - Нитраты
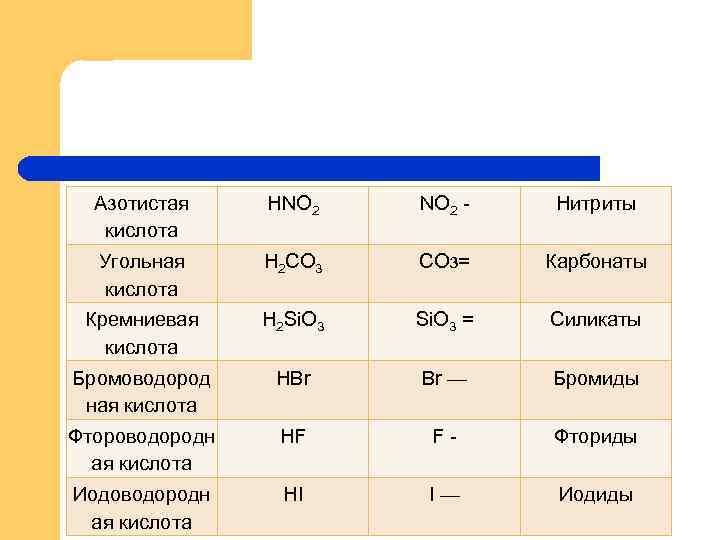 Азотистая кислота НNО 2 NO 2 - Нитриты Угольная кислота Н 2 СО 3 СOз= Карбонаты Кремниевая кислота Н 2 Si. O 3 = Силикаты Бромоводород ная кислота НВr Br — Бромиды Фтороводородн ая кислота HF F- Фториды Иодоводородн ая кислота HI I— Иодиды
Азотистая кислота НNО 2 NO 2 - Нитриты Угольная кислота Н 2 СО 3 СOз= Карбонаты Кремниевая кислота Н 2 Si. O 3 = Силикаты Бромоводород ная кислота НВr Br — Бромиды Фтороводородн ая кислота HF F- Фториды Иодоводородн ая кислота HI I— Иодиды
 Свойства кислот
Свойства кислот
 Физические свойства кислот а) жидкости (кроме кремниевой кислоты), б) без цвета, в) без запаха, г) кислые на вкус.
Физические свойства кислот а) жидкости (кроме кремниевой кислоты), б) без цвета, в) без запаха, г) кислые на вкус.
 Практическое определение химических свойств кислот Формула и название Индикаторы кислот лакмус Минеральные кислоты Органические красный метилор фенолфт анжевый алеин красный ______
Практическое определение химических свойств кислот Формула и название Индикаторы кислот лакмус Минеральные кислоты Органические красный метилор фенолфт анжевый алеин красный ______
 Химические свойства кислот 1. 2. 3. 4. 5. Действие индикатора. Взаимодействие с металлами. Взаимодействие с основными оксидами. Взаимодействие с гидроксидами. Взаимодействие с солями
Химические свойства кислот 1. 2. 3. 4. 5. Действие индикатора. Взаимодействие с металлами. Взаимодействие с основными оксидами. Взаимодействие с гидроксидами. Взаимодействие с солями
 Домашнее задание § 20, стр 76 таблица l Кому было легко – упражнение 4, 2, 5; l Кто затруднялся - упражнение 1; l Кому было трудно- конспект урока. l Для желающих – составить компьютерную презентацию по данной теме. l
Домашнее задание § 20, стр 76 таблица l Кому было легко – упражнение 4, 2, 5; l Кто затруднялся - упражнение 1; l Кому было трудно- конспект урока. l Для желающих – составить компьютерную презентацию по данной теме. l
 МОЛОДЦЫ!
МОЛОДЦЫ!