Кислотность и основность и СПИРТЫ.ppt
- Количество слайдов: 37

Кислотность и основность органических соединений

Теория Бренстеда • Кислоты – нейтральные молекулы или ионы, способные отдавать протон Н+ (доноры Н+) • Основания – нейтральные молекулы или ионы, способные присоединять Н+ (акцепторы Н+)
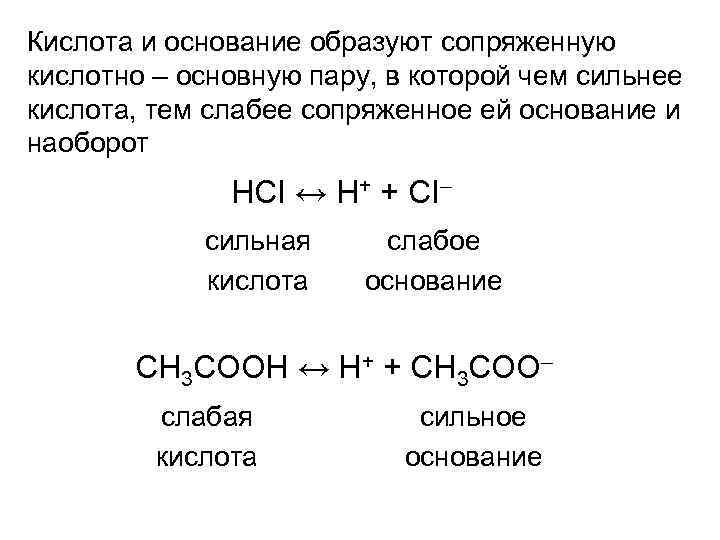
Кислота и основание образуют сопряженную кислотно – основную пару, в которой чем сильнее кислота, тем слабее сопряженное ей основание и наоборот НCI ↔ Н+ + СI– сильная кислота слабое основание СН 3 СООН ↔ Н+ + СН 3 СОО– слабая кислота сильное основание
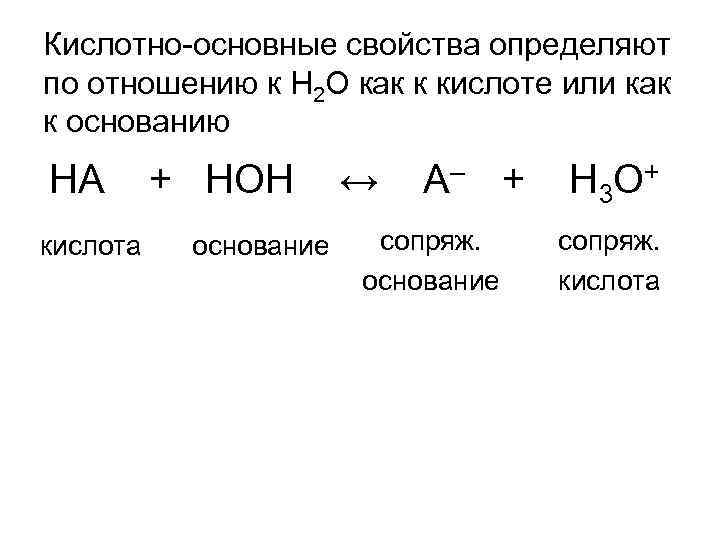
Кислотно-основные свойства определяют по отношению к Н 2 О как к кислоте или как к основанию НА кислота + НОН основание ↔ А– + сопряж. основание Н 3 О + сопряж. кислота
![Сила слабых электролитов определяется величиной константы равновесия реакции Kp = [A-]. [H 3 O+] Сила слабых электролитов определяется величиной константы равновесия реакции Kp = [A-]. [H 3 O+]](https://present5.com/presentation/3/32412685_133190904.pdf-img/32412685_133190904.pdf-5.jpg)
Сила слабых электролитов определяется величиной константы равновесия реакции Kp = [A-]. [H 3 O+] [HA]. [H 2 O] Kp. [H 2 O] = Ka = постоянные [A-]. [H 3 O+] [HA]

Чем Ка, тем сильнее кислота Для удобства вводят р. Ка = – lg. Ка К 1 = 10– 5 К 2 = 10– 10 p. К 1 = 5 p. К 1 = 10 Чем р. Ка, тем сильнее кислота

Кислоты Бренстеда Кислотный центр – элемент и связанный с ним атом водорода. В зависимости от природы элемента кислоты подразделяются: • ОН кислоты (карбоновые кислоты, спирты, фенолы) • SH кислоты (тиолы) • NH кислоты (амины, амиды, имиды) • CH кислоты (у/в и их производные)

Оценка кислотности Чем стабильнее сопряженное основание (анион), тем сильнее сопряженная кислота.

Стабильность аниона определяется степенью делокализации (–) заряда на нем и зависит от факторов: 1. Природа атома в кислотном центре 2. Стабилизация аниона за счет сопряжения 3. Характер радикала, связанного с кислотным центром 4. Влияние растворителя

1. Природа атома в кислотном центре При одинаковом радикале, чем Э. О. атома, тем устойчивость аниона, тем кислотность соединения. 2, 5 3, 0 3, 5 CH < NH < OH Для неметаллов в группах сверху вниз поляризуемость преобладает над Э. О. CH < NH < OH < SH
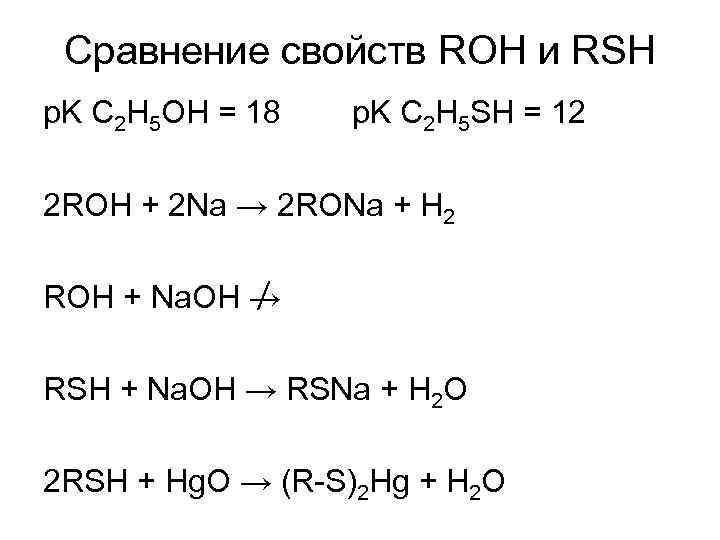
Сравнение свойств ROH и RSH p. K C 2 H 5 OH = 18 p. K C 2 H 5 SH = 12 2 ROH + 2 Na → 2 RONa + H 2 ROH + Na. OH → RSNa + H 2 O 2 RSH + Hg. O → (R-S)2 Hg + H 2 O
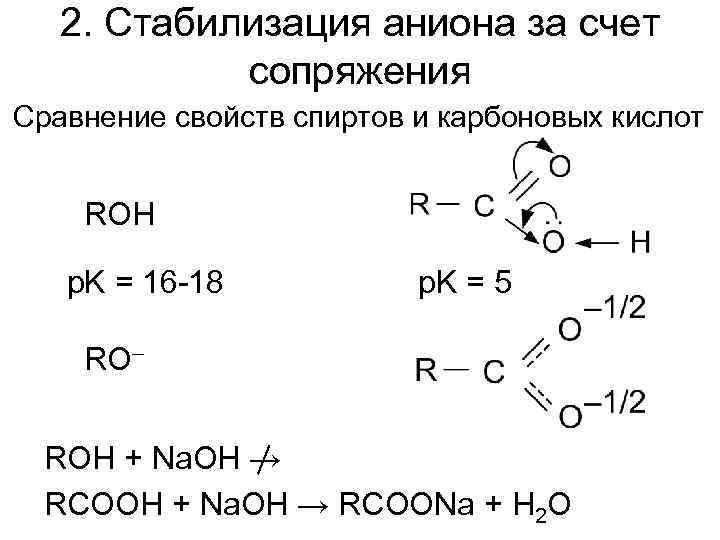
2. Стабилизация аниона за счет сопряжения Сравнение свойств спиртов и карбоновых кислот ROH p. K = 16 -18 p. K = 5 RO– ROH + Na. OH → RCOONa + H 2 O
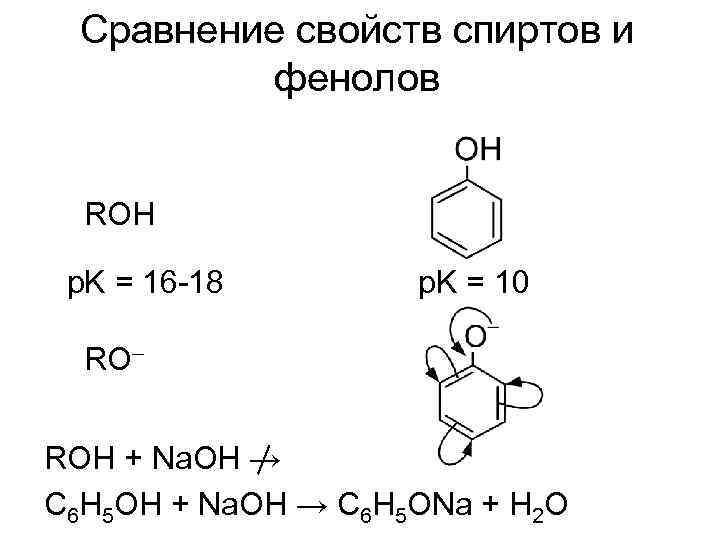
Сравнение свойств спиртов и фенолов ROH p. K = 16 -18 p. K = 10 RO– ROH + Na. OH → С 6 H 5 ONa + H 2 O
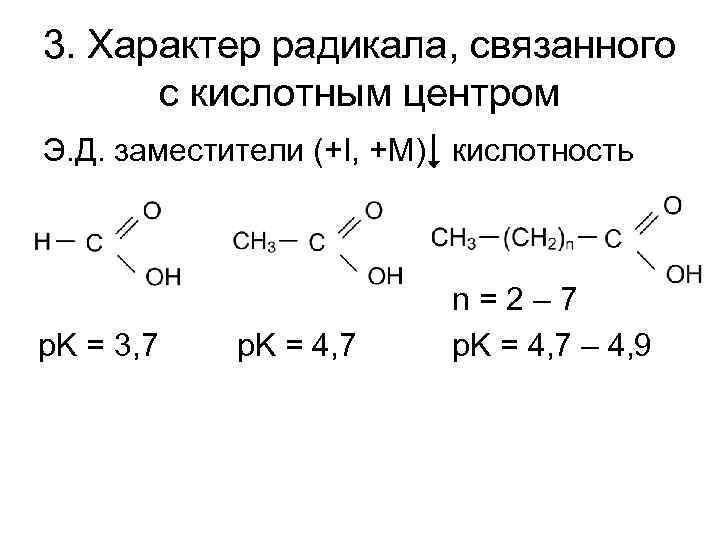
3. Характер радикала, связанного с кислотным центром Э. Д. заместители (+I, +M) кислотность p. K = 3, 7 p. K = 4, 7 n=2– 7 p. K = 4, 7 – 4, 9
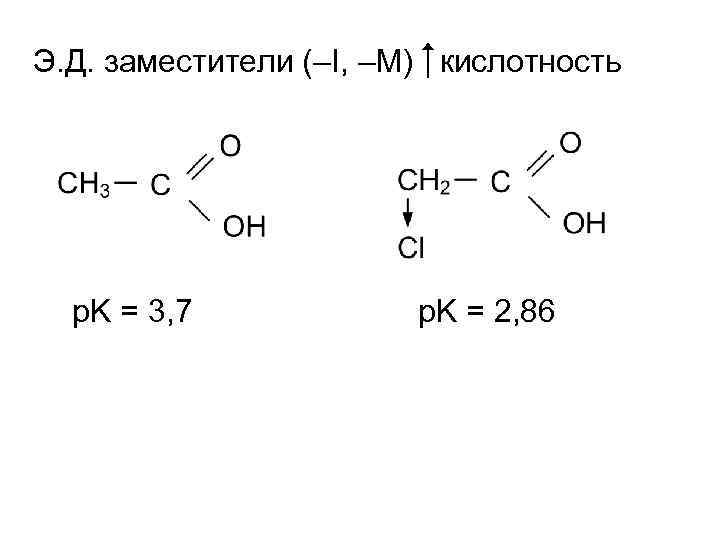
Э. Д. заместители (–I, –M) кислотность p. K = 3, 7 p. K = 2, 86

4. Влияние растворителя Чем больше гидратирован анион, тем он стабильнее, тем выше кислотность. Степень гидратации больше у маленьких ионов с большим зарядом.

ОСНОВАНИЯ БРЕНСТЕДА (акцепторы протонов Н+) • n - основания (- ониевые) • π - основания
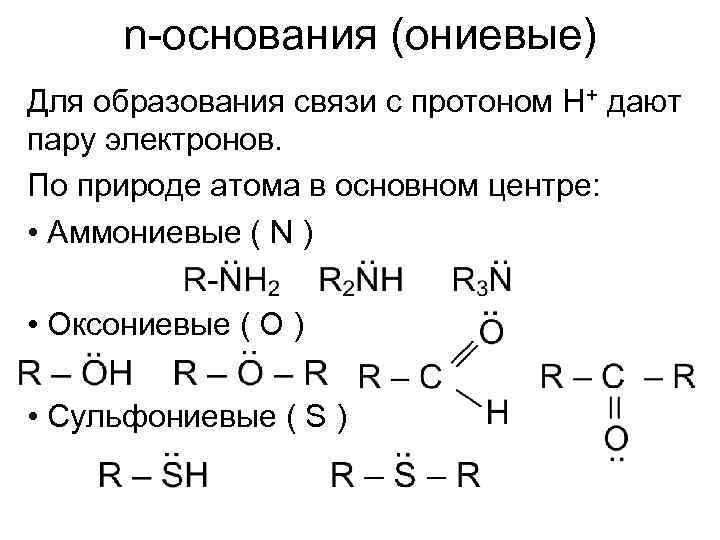
n-основания (ониевые) Для образования связи с протоном Н+ дают пару электронов. По природе атома в основном центре: • Аммониевые ( N ) • Оксониевые ( O ) • Cульфониевые ( S )
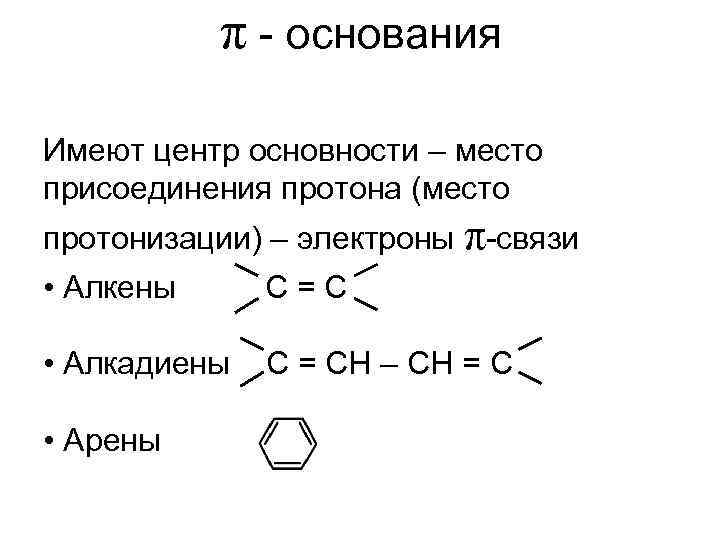
π - основания Имеют центр основности – место присоединения протона (место протонизации) – электроны π-связи • Алкены С=С • Алкадиены С = СН – СН = C • Арены
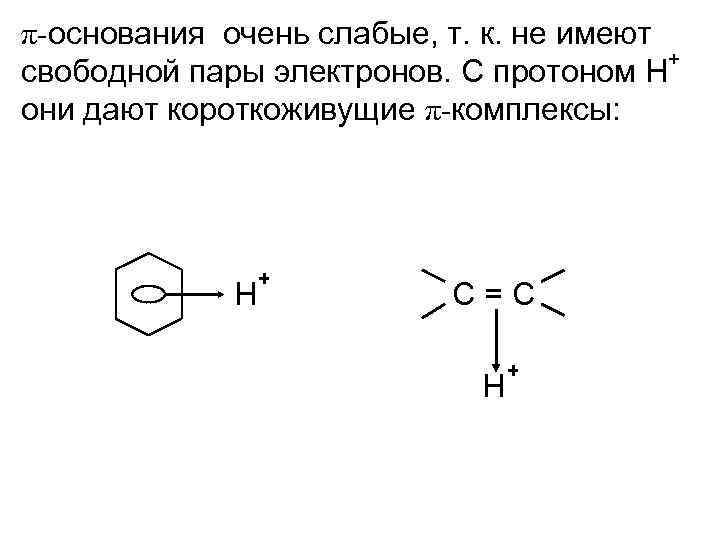
π-основания очень слабые, т. к. не имеют + свободной пары электронов. С протоном H они дают короткоживущие π-комплексы: Н + С=С Н +
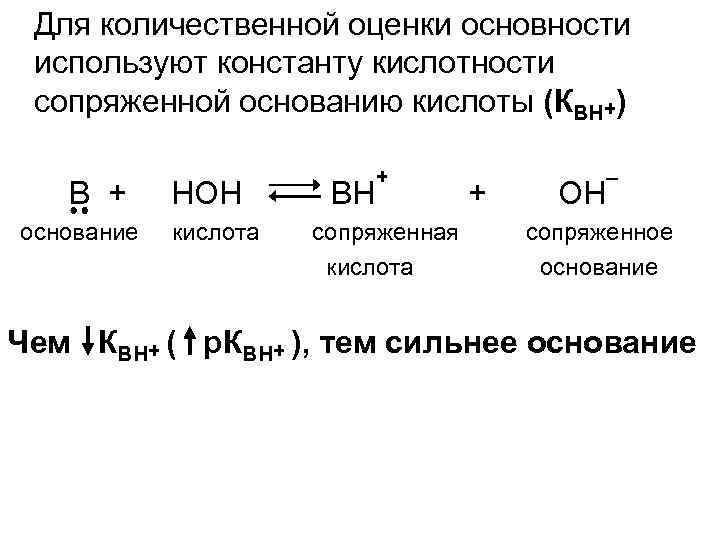
Для количественной оценки основности используют константу кислотности сопряженной основанию кислоты (КВН+) В + основание НОН кислота ВН + сопряженная кислота + ОН – сопряженное основание Чем КВН+ ( р. КВН+ ), тем сильнее основание

Факторы, влияющие на основность • Э. О. и поляризуемость: Чем э. о. и поляризуемость атома в основном центре, тем слабее основание N > O > S 3, 0 3, 5 2, 5
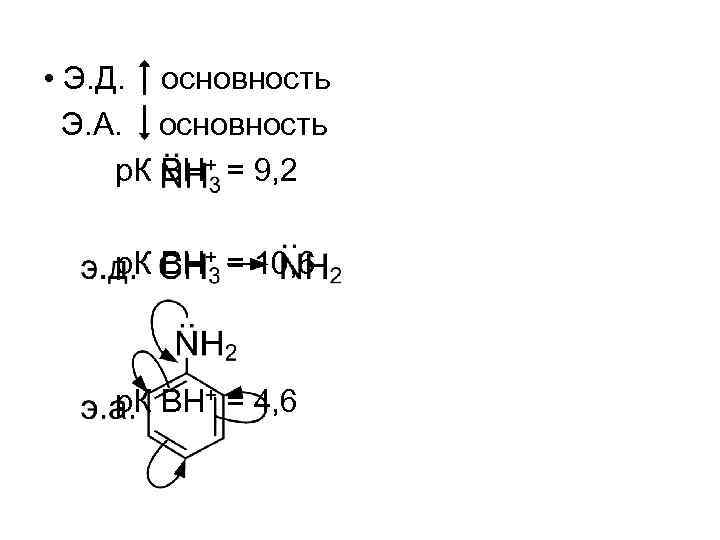
• Э. Д. основность Э. А. основность р. К ВН+ = 9, 2 р. К ВН+ = 10, 6 р. К ВН+ = 4, 6

Некоторые органические соединения проявляют амфотерность и за счет водородных и донорно – акцепторных связей между к. ц. и о. ц. образуют внутримолекулярные и межмолекулярные ассоциаты.
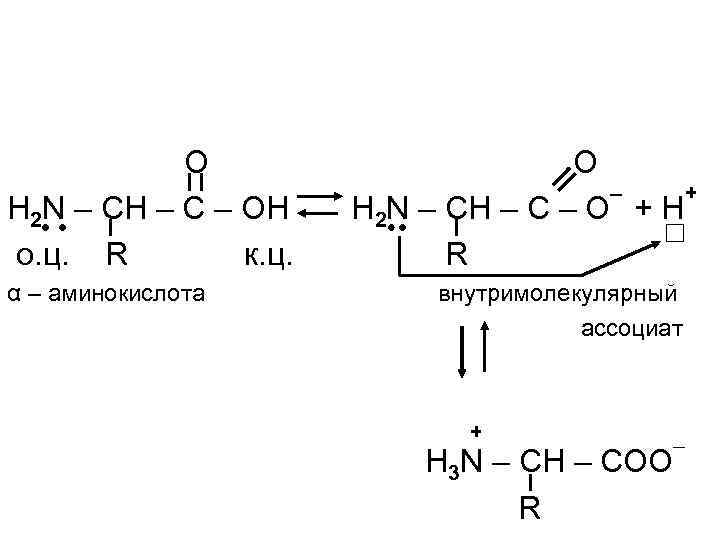
O H 2 N – CH – C – OH о. ц. R к. ц. α – аминокислота O – + H 2 N – CH – C – O + H R внутримолекулярный ассоциат + H 3 N – CH – COO R –
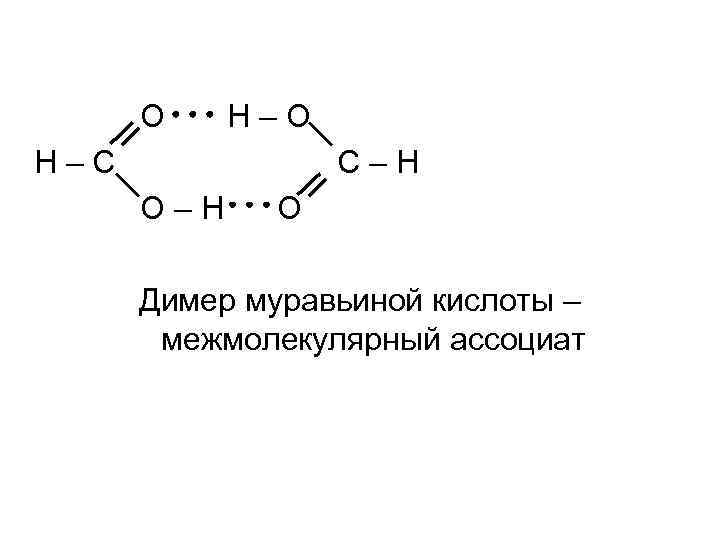
O H–C C–H O Димер муравьиной кислоты – межмолекулярный ассоциат
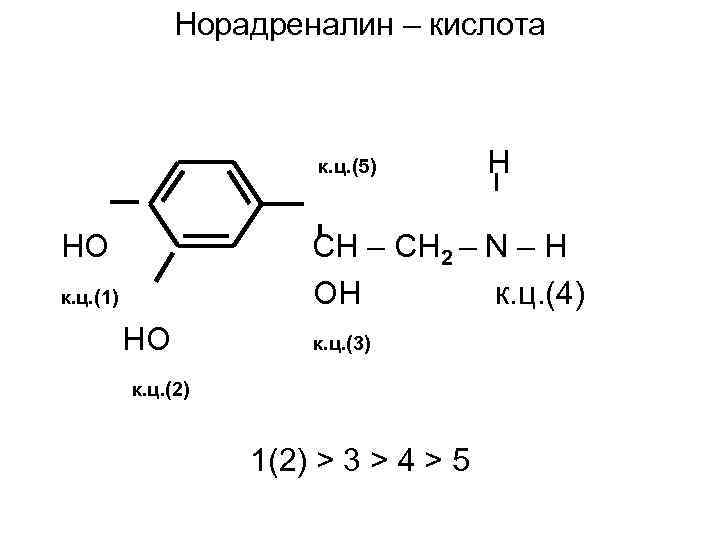
Норадреналин – кислота к. ц. (5) HO H CH – CH 2 – N – H OH к. ц. (4) к. ц. (1) HO к. ц. (3) к. ц. (2) 1(2) > 3 > 4 > 5
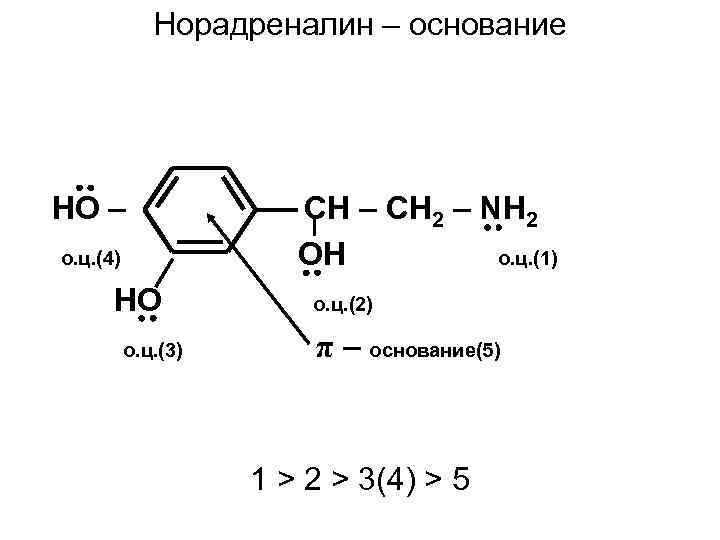
Норадреналин – основание HO – о. ц. (4) HO о. ц. (3) CH – CH 2 – NH 2 OH о. ц. (1) о. ц. (2) π – основание(5) 1 > 2 > 3(4) > 5

Гидроксисоединения (спирты)

Спирты – соединения алифатического ряда, содержащие одну или несколько гидроксильных групп. Общая формула спиртов R – OH. В зависимости от числа гидроксильных групп спирты бывают одно- и многоатомные.

Одноатомные спирты Отдельные представители: CH 3 OH – Метанол (метиловый) C 2 H 5 OH – Этанол (этиловый) C 3 H 7 OH – Пропанол (пропиловый) C 4 H 9 OH – Бутанол (бутиловый) C 5 H 11 OH – Пентанол (амиловый)
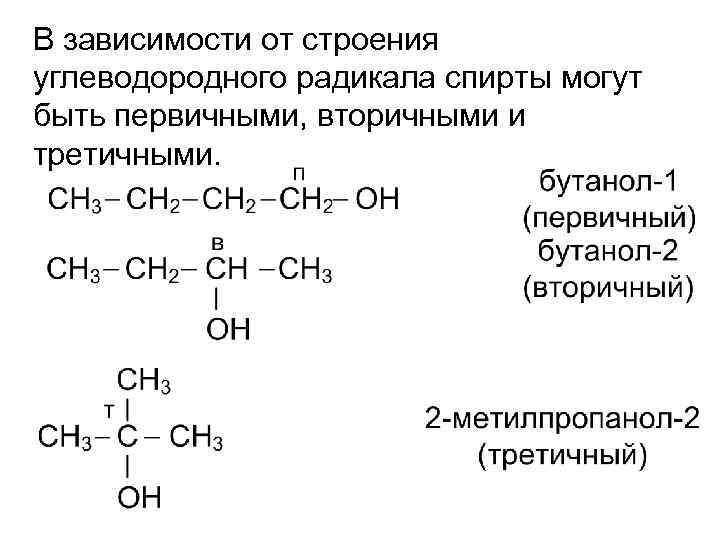
В зависимости от строения углеводородного радикала спирты могут быть первичными, вторичными и третичными.

Свойства одноатомных спиртов Физические: 1. Высокие T°КИП, так как молекулы ассоциированы за счет межмолекулярных водородных связей 2. Хорошо растворимы в воде, так как образуют водородные связи с молекулами воды

Свойства одноатомных спиртов Химические: 1. Кислые свойства. Образование алкоголятов (с металлами): 2. Образование простых эфиров (со спиртами) при нагревании в присутствии катализатора:
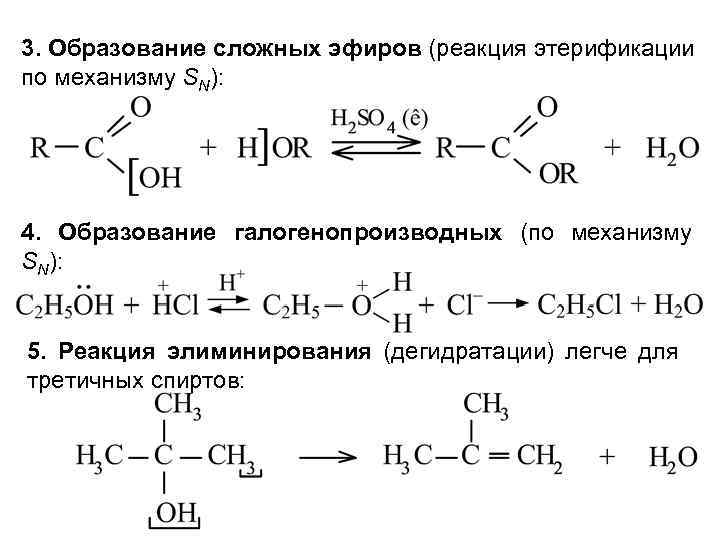
3. Образование сложных эфиров (реакция этерификации по механизму SN): 4. Образование галогенопроизводных (по механизму SN): 5. Реакция элиминирования (дегидратации) легче для третичных спиртов:
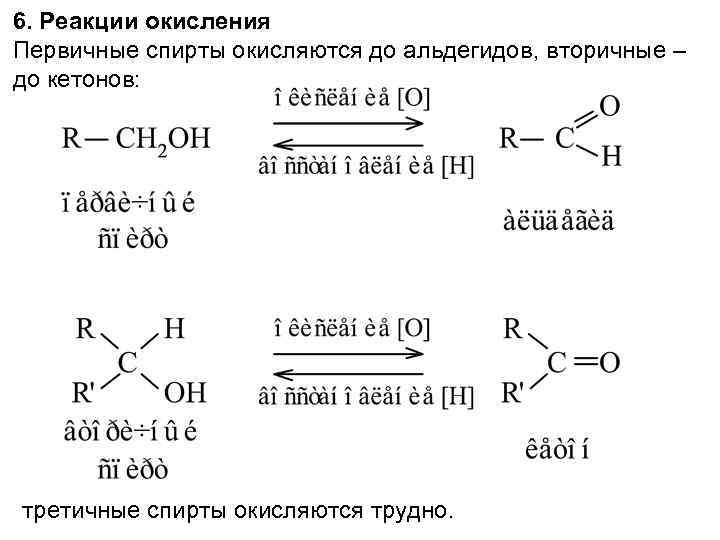
6. Реакции окисления Первичные спирты окисляются до альдегидов, вторичные – до кетонов: третичные спирты окисляются трудно.
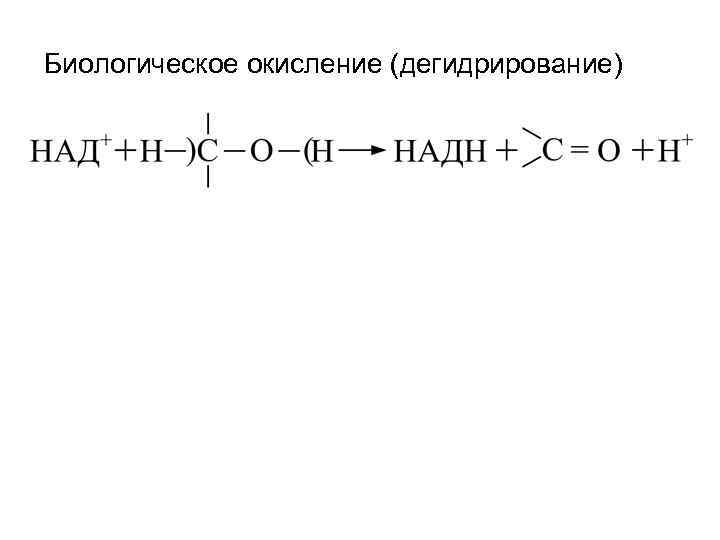
Биологическое окисление (дегидрирование)
Кислотность и основность и СПИРТЫ.ppt