кислотность и основность.ppt
- Количество слайдов: 34

КИСЛОТНОСТЬ И ОСНОВНОСТЬ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ ПО БРЕНСТЕДУ

Для оценки кислотности и основности органических соединений используют протолитическую теорию Бренстеда. По Бренстеду кислоты – доноры протонов, а основания - акцепторы протонов.

КИСЛОТЫ БРЕНСТЕДА – ДОНОРЫ H+ Любое соединение, где есть связь с водородом, можно считать кислотой Бренстеда. Атом водорода и связанный с ним гетероатом называют кислотным центром (К. Ц. ) По К. Ц. различают CH, NH-, OH- и SH- кислоты
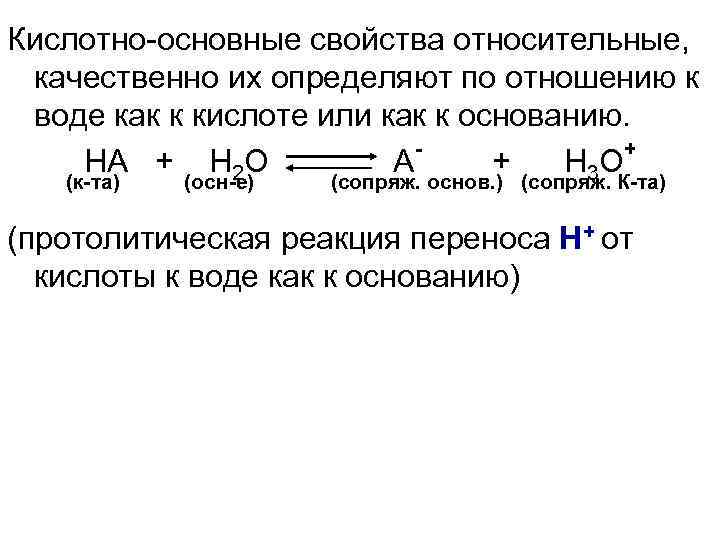
Кислотно-основные свойства относительные, качественно их определяют по отношению к воде как к кислоте или как к основанию. + HA + H 2 O A + H 3 O (к-та) (осн-е) (сопряж. основ. ) (сопряж. К-та) (протолитическая реакция переноса H+ от кислоты к воде как к основанию)

Кислота и сопряженное ей основание образуют кислотно – основную пару, в которой чем сильнее кислота, тем слабее сопряженное ей основание и наоборот. CH 3 COOH слабее HCl, и соответственно ацетат – ион CH 3 COO сильнее как основание хлорид – иона Сl

Количественно кислотность оценивают константой кислотности (Ка), которую находят через константу равновесия (Кр) + протолитической реакции переноса H от кислоты к воде.
![Kp = [A-]. [H 3 O+] [HA]. [H 2 O] Kp. [H 2 O] Kp = [A-]. [H 3 O+] [HA]. [H 2 O] Kp. [H 2 O]](https://present5.com/presentation/3/32412685_133190908.pdf-img/32412685_133190908.pdf-7.jpg)
Kp = [A-]. [H 3 O+] [HA]. [H 2 O] Kp. [H 2 O] = Ka = постоянные [A-]. [H 3 O+] [HA]

Для удобства используется показатель Ка (р. Ка = -lg. Ka) -4 • Ka (HCOOH) ~10 ; p. Ka = 3, 8 -5 • Ka (CH COOH) ~ 10 ; p. Ka = 4, 75 Чем Ка ( р. Ка), тем сильнее кислота, тем больше равновесие протолитической реакции сдвинуто вправо, тем устойчивее образующийся анион ( из II начала ТД). Значит по устойчивости аниона можно судить о силе кислоты.

Стабильность аниона зависит от степени делокализации в нем заряда: чем выше делокализация, тем устойчивее анион.

Степень делокализации заряда в анионе определяется: • природой атома в к. ц. • характером радикала, связанного с к. ц. • возможной делокализацией заряда аниона за счет сопряжения • природой растворителя

Природа атома в К. Ц. При одинаковых радикалах устойчивость аниона зависит от ЭО и поляризуемости гетероатома в к. ц. Чем выше ЭО, тем больше способность у атома нести отрицательный заряд, тем стабильнее анион. Отсюда OH- > NH- > CH- кислот ЭО: 3, 5 3, 0 2, 5

Для SH – кислот над ЭО преобладает высокая поляризуемость серы. Атом серы больше размером, чем атом кислорода и отрицательный заряд меркаптид – иона R – S распределяется легче, чем в алкоксид – ионе R – O. В результате тиоспирты проявляют более кислые свойства, чем их кислородные аналоги. (р. Ка(С 2 H 5 SH) = 12, а р. Ка(С 2 H 5 OH) = 18)

Характер радикала. При одинаковом гетероатоме в к. ц. на кислотность влияет характер радикала. ЭА повышает кислотность, т. к. способствует делокализации заряда аниона, а ЭД препятствуют делокализации заряда и потому понижает кислотность. Влияние заместителя тем сильнее, чем он ближе к к. ц.
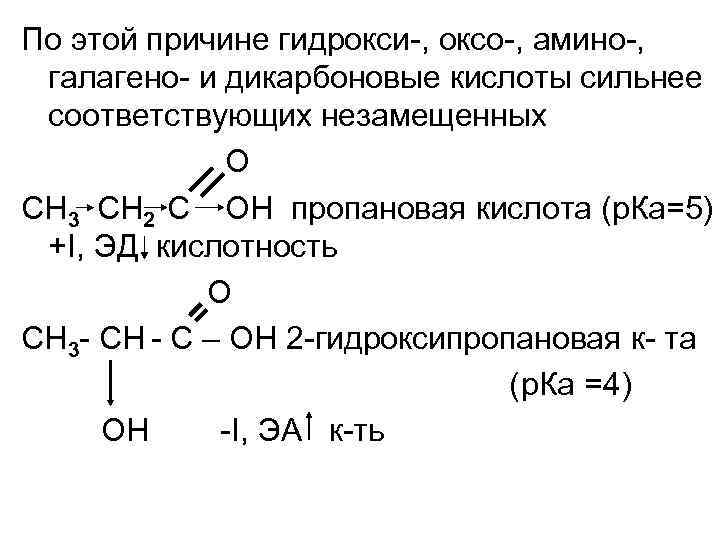
По этой причине гидрокси-, оксо-, амино-, галагено- и дикарбоновые кислоты сильнее соответствующих незамещенных O CH 3 CH 2 C OH пропановая кислота (р. Ка=5) +I, ЭД кислотность O CH 3 - CH - C – OH 2 -гидроксипропановая к- та (р. Ка =4) OH -I, ЭА к-ть

По той же причине многоатомные спирты сильнее одноатомных CH 3 CH 2 OH этанол (р. Ка=18) +I, ЭД кислотность HO CH 2 – CH 2 OH этандиол -1, 2 (р. Ка =15) -I, ЭА к-ть к. ц.
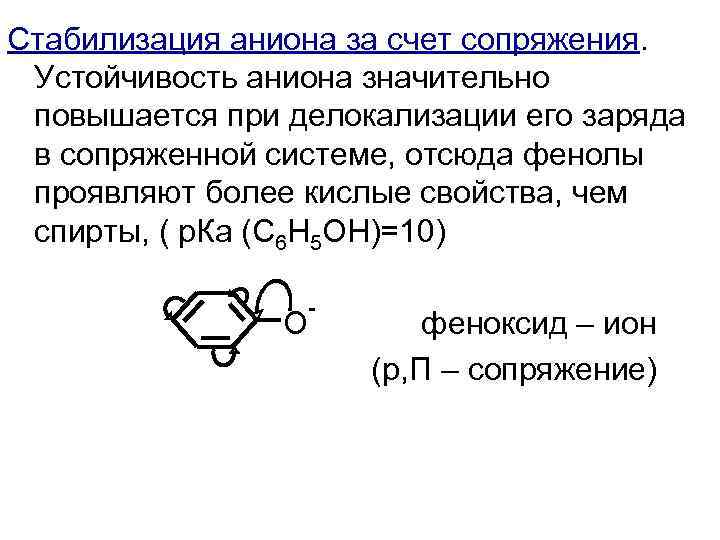
Стабилизация аниона за счет сопряжения. Устойчивость аниона значительно повышается при делокализации его заряда в сопряженной системе, отсюда фенолы проявляют более кислые свойства, чем спирты, ( р. Ка (C 6 H 5 OH)=10) О - феноксид – ион (р, П – сопряжение)
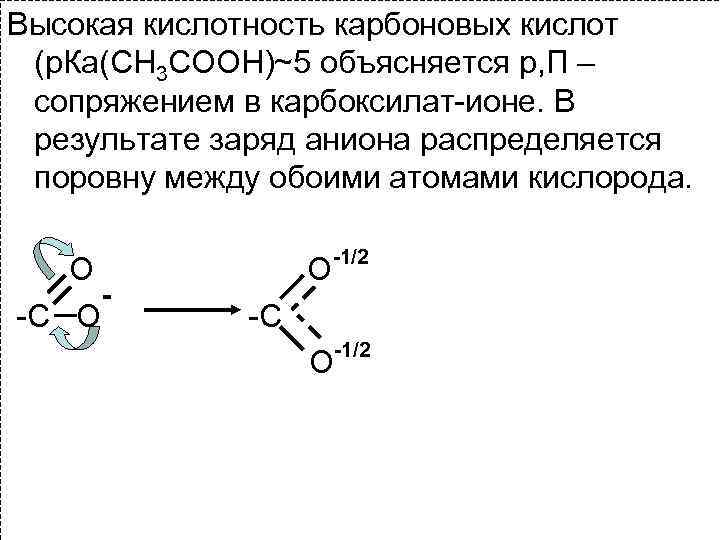
Высокая кислотность карбоновых кислот (р. Ка(CH 3 COOH)~5 объясняется р, П – сопряжением в карбоксилат-ионе. В результате заряд аниона распределяется поровну между обоими атомами кислорода. О -С О О -1/2 -С О -1/2

Всё выше сказанное легко подтверждается химическими реакциями: этанол образует соль только с металлическим натрием, фенол и этантиол реагируют уже с Na. OH, а уксусная кислота даже с солями активных металлов. 2 C 2 H 5 OH + 2 Na +I, ЭД К. Ц. Этанол (р. Ка = 18) 2 С 2 Н 5 – ONa + H 2 этилат натрия
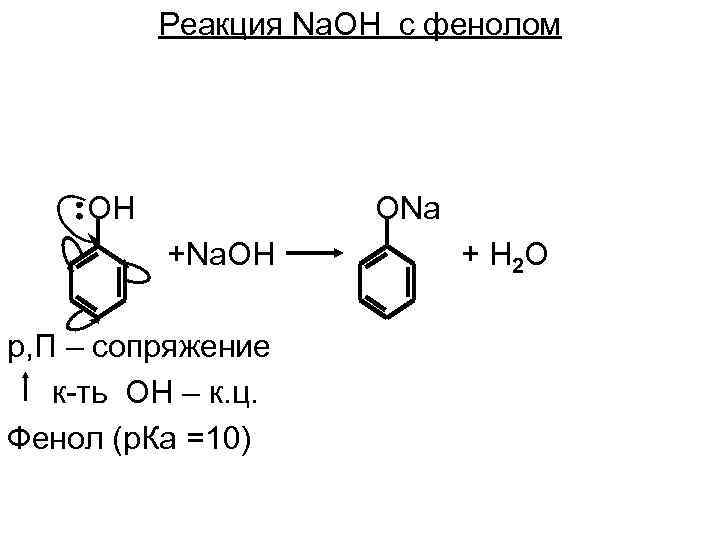
Реакция Na. OH с фенолом OH ONa +Na. OH p, П – сопряжение к-ть ОН – к. ц. Фенол (p. Ка =10) + H 2 O
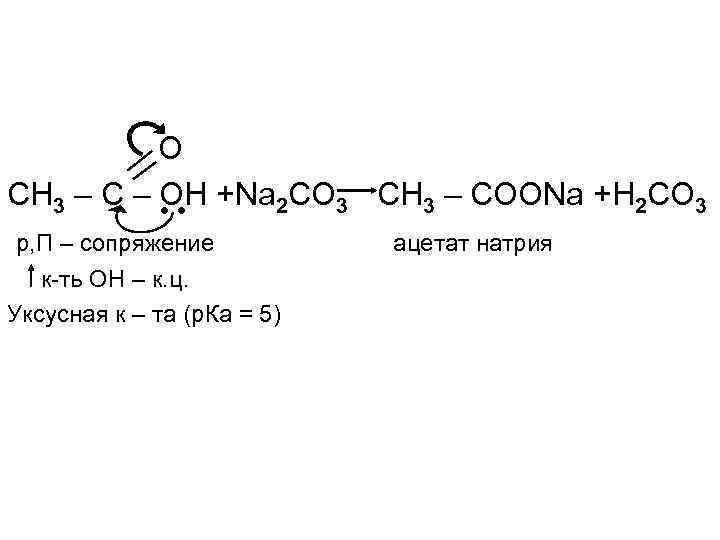
О СН 3 – С – ОН +Na 2 CO 3 CH 3 – COONa +H 2 CO 3 р, П – сопряжение к-ть ОН – к. ц. Уксусная к – та (р. Ка = 5) ацетат натрия
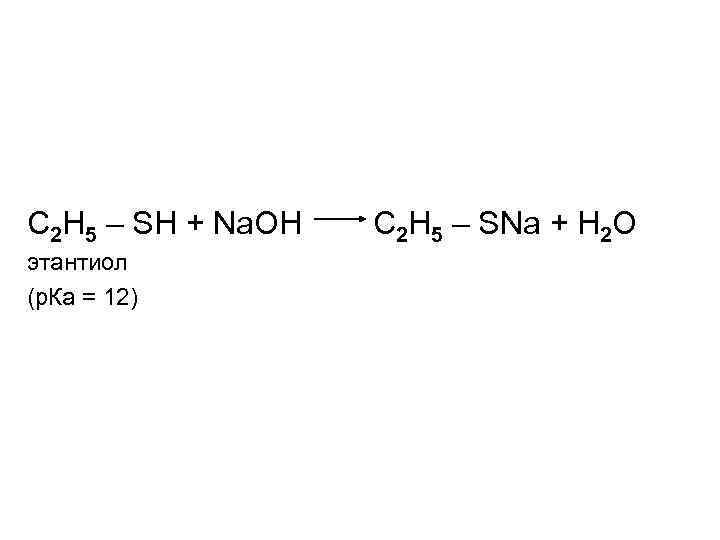
С 2 Н 5 – SH + Na. OH этантиол (р. Ка = 12) C 2 H 5 – SNa + H 2 O

Влияние растворителя. Чем больше гидротирован анион, тем он стабильнее, тем выше кислотность. Степень гидротации больше у маленьких ионов с большим зарядом.

Основания Бренстеда – + акцепторы H + Для образования ковалентной связи с H (1 s ) основаниям необходимо иметь • либо свободную пару электронов (ониевые основания или n – основания): N. , О , . S. . • либо электроны π– связи (π-основания): алкны, алкины, арены.
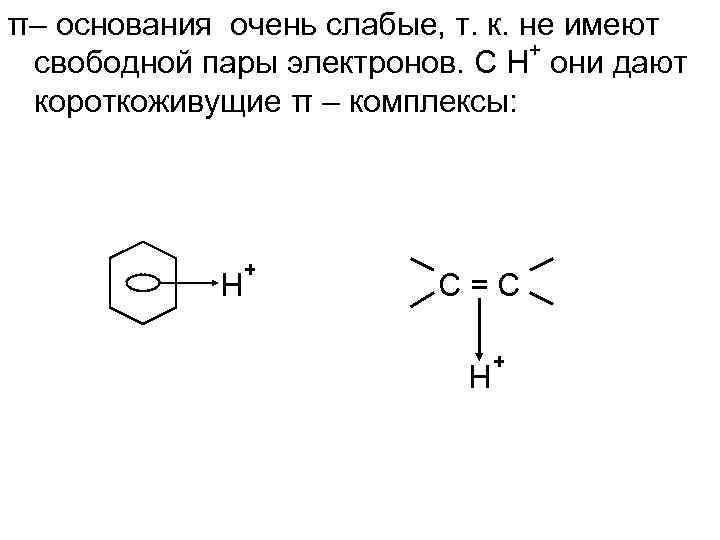
π– основания очень слабые, т. к. не имеют + свободной пары электронов. С H они дают короткоживущие π – комплексы: Н + С=С Н +
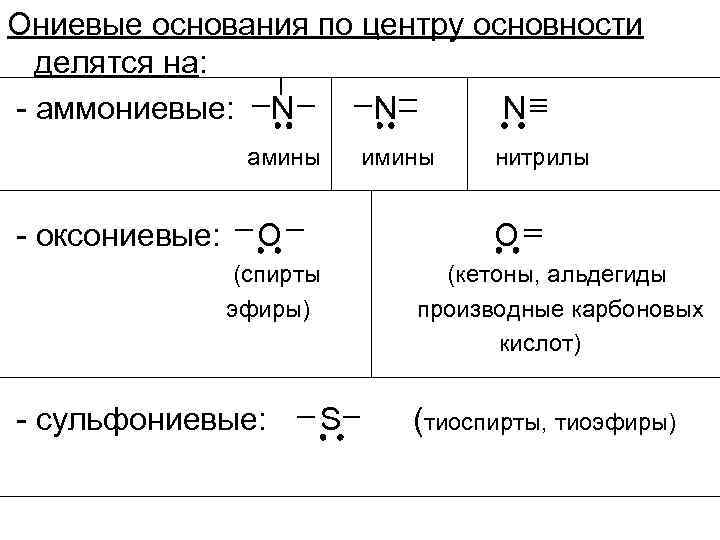
Ониевые основания по центру основности делятся на: - аммониевые: N N N амины - оксониевые: О нитрилы О (спирты эфиры) - сульфониевые: имины S (кетоны, альдегиды производные карбоновых кислот) (тиоспирты, тиоэфиры)
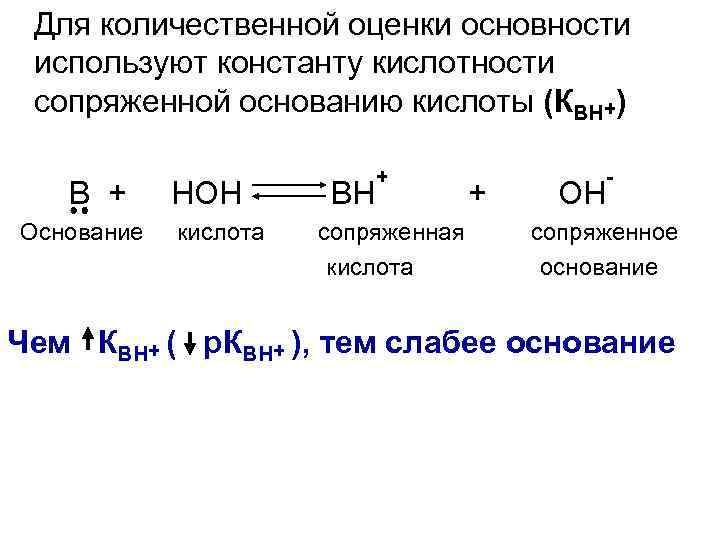
Для количественной оценки основности используют константу кислотности сопряженной основанию кислоты (КВН+) В + Основание НОН кислота ВН + сопряженная кислота + ОН - сопряженное основание Чем КВН+ ( р. КВН+ ), тем слабее основание

Факторы, влияющие на основность те же, что и на кислотность, но их влияние противоположно. • Чем ЭО атома в основном центре (о. ц. ), тем крепче он держит свободные пары электронов и тем слабее его основность (оксониевые слабее аммониевых)

• Чем выше поляризуемость, тем больше делокализована электронная плотность на атоме и тем меньше основность ( сульфониевые слабее оксониевых)
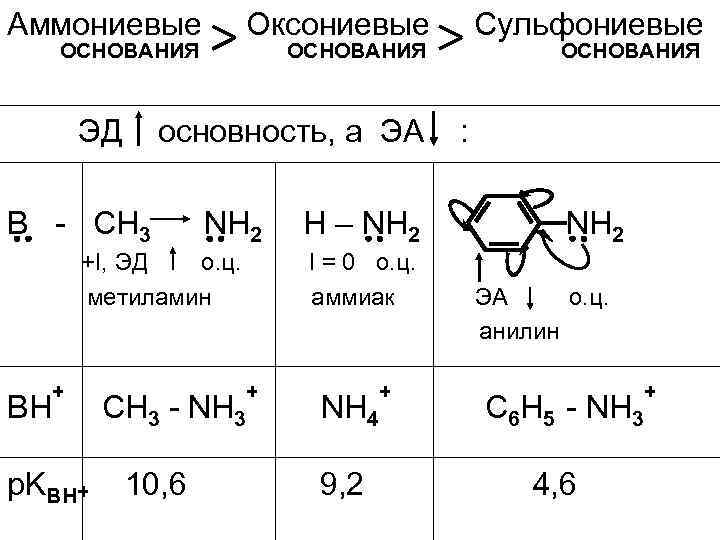
Аммониевые Оксониевые ОСНОВАНИЯ ЭД ОСНОВАНИЯ основность, а ЭА В - CH 3 NH 2 +I, ЭД о. ц. метиламин ВН + p. KВН+ СН 3 - NH 3 10, 6 Сульфониевые H – NH 2 I = 0 о. ц. аммиак + NH 4 9, 2 + ОСНОВАНИЯ : NH 2 ЭА о. ц. анилин C 6 H 5 - NH 3 4, 6 +

Некоторые органические соединения проявляют амфотерность и за счет водородных и донорно – акцепторных связей между к. ц. и о. ц. образуют внутримолекулярные и межмолекулярные ассоциаты.
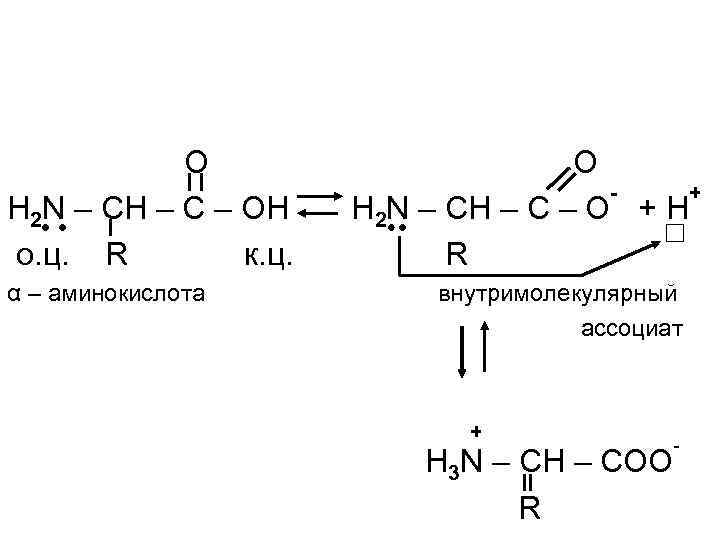
O H 2 N – CH – C – OH о. ц. R к. ц. α – аминокислота O + H 2 N – CH – C – O + H R внутримолекулярный ассоциат + H 3 N – CH – COO R -
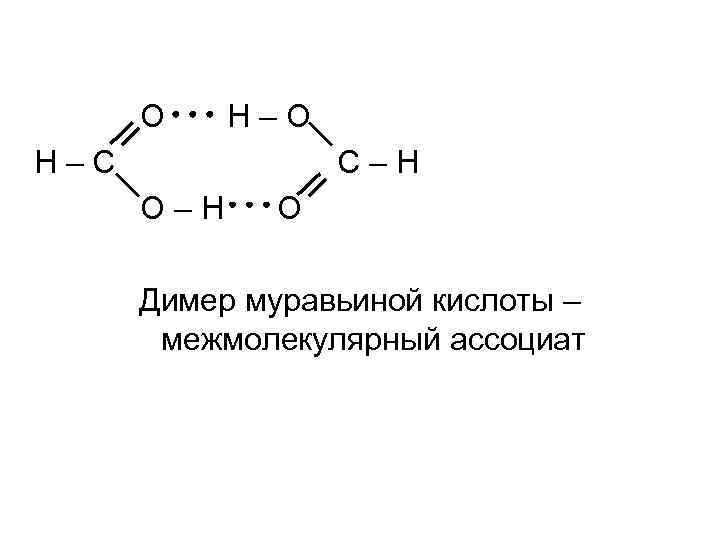
O H–C C–H O Димер муравьиной кислоты – межмолекулярный ассоциат
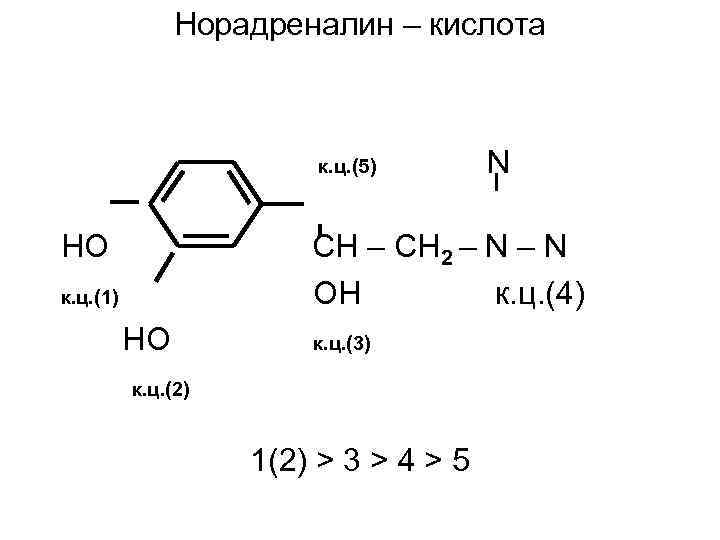
Норадреналин – кислота к. ц. (5) HO N CH – CH 2 – N OH к. ц. (4) к. ц. (1) HO к. ц. (3) к. ц. (2) 1(2) > 3 > 4 > 5
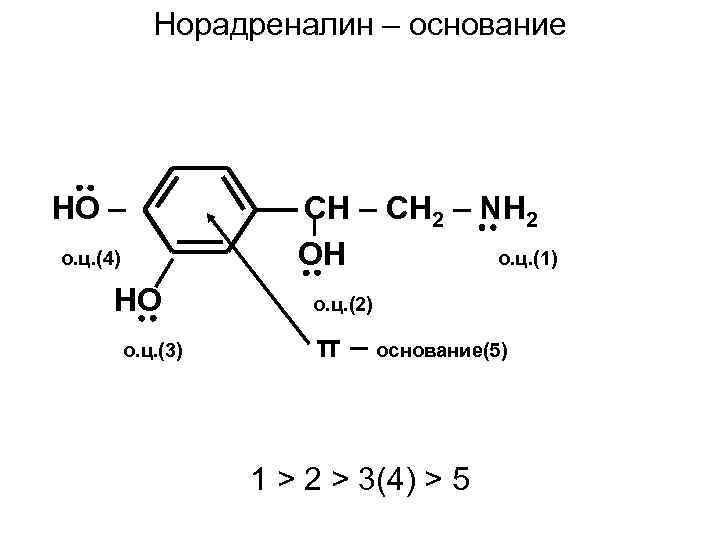
Норадреналин – основание HO – о. ц. (4) HO о. ц. (3) CH – CH 2 – NH 2 OH о. ц. (1) о. ц. (2) π – основание(5) 1 > 2 > 3(4) > 5
кислотность и основность.ppt