3.Кислотность и основность.ppt
- Количество слайдов: 21

Кислотность и оснόвность органических соединений

Теория Бренстеда-Лоури • Кислоты Бренстеда-нейтральные молекулы или ионы, оттающие Н+ (доноры Н+) • Основания Бренстеда-нейтральные мол-лы или ионы, принимающие Н+ (акцепторы Н+) • Реакция между кислотами и основаниями:
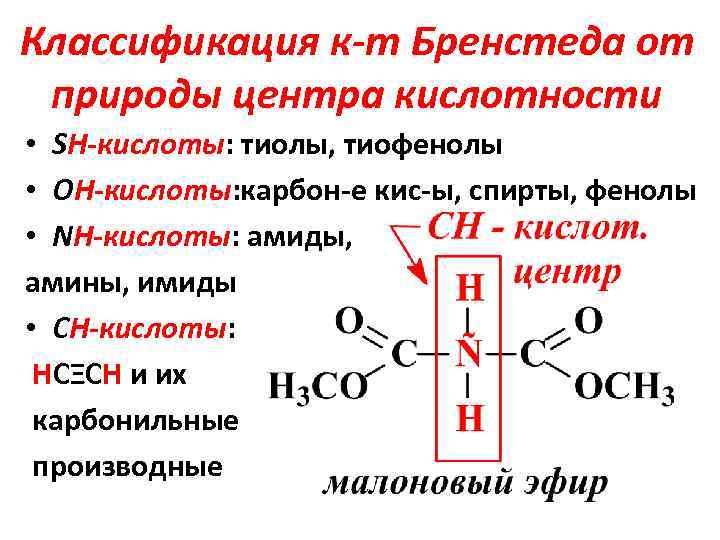
Классификация к-т Бренстеда от природы центра кислотности • SН-кислоты: тиолы, тиофенолы • ОН-кислоты: карбон-е кис-ы, спирты, фенолы • NН-кислоты: амиды, амины, имиды • СН-кислоты: НСΞСН и их карбонильные производные
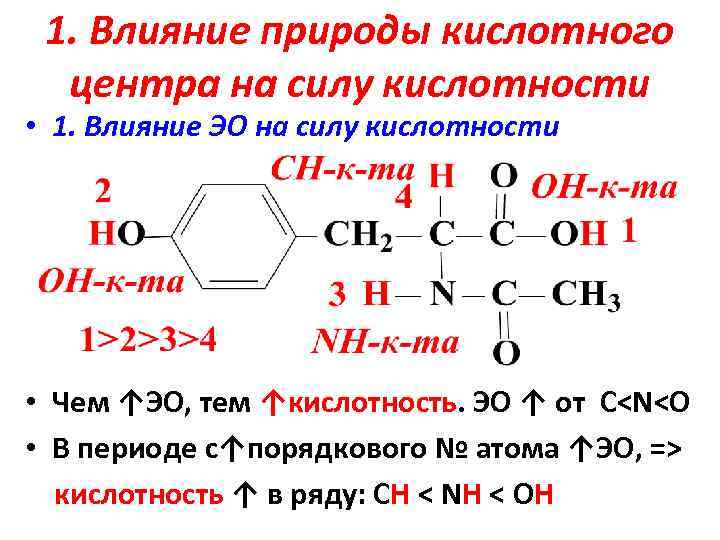
1. Влияние природы кислотного центра на силу кислотности • 1. Влияние ЭО на силу кислотности • Чем ↑ЭО, тем ↑кислотность. ЭО ↑ от C<N<O • В периоде с↑порядкового № атома ↑ЭО, => кислотность ↑ в ряду: СН < NH < OH

1. Влияние природы кислотного центра на силу кислотности • 2. Влияние поляризуемости на силу кислот • Поляризуемость - способность внешнего электронного облака смещаться под действием внешнего электрического поля. • В группах периодической системы, с ↑порядкового № атома, ЭО↓, но ↑поляризуемость. • Чем > ℓ⁻в атоме и чем дальше расположены они от ядра, тем > его поляризуемость. • Радиус S > радиуса О, => поляризуемость S>O, => кислотность SH-кислот > OH-кислот
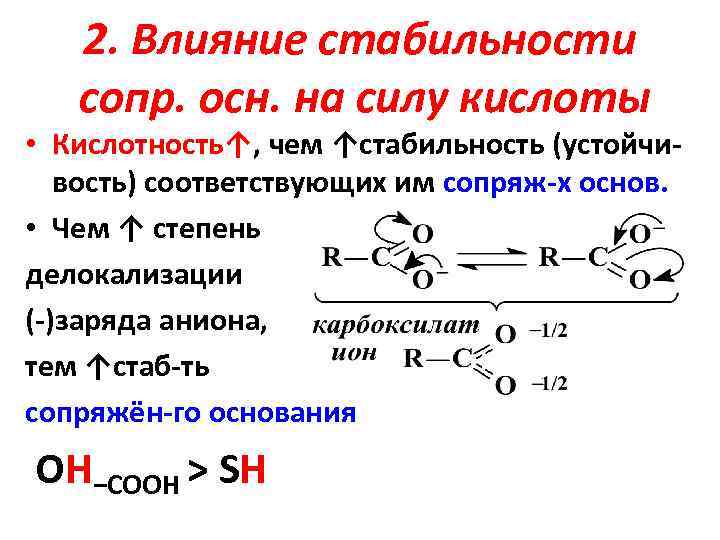
2. Влияние стабильности сопр. осн. на силу кислоты • Кислотность↑, чем ↑стабильность (устойчивость) соответствующих им сопряж-х основ. • Чем ↑ степень делокализации (-)заряда аниона, тем ↑стаб-ть cопряжён-го основания ОН−СООН > SH
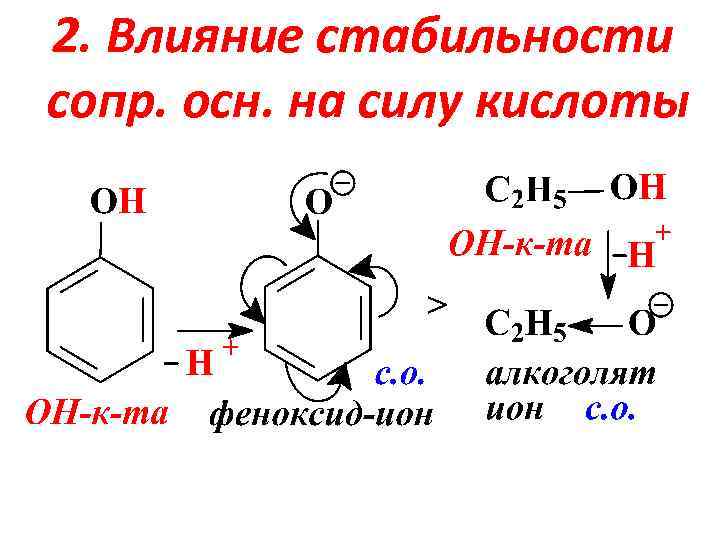
2. Влияние стабильности сопр. осн. на силу кислоты

3. Влияние заместителей на силу кислотности • 1. Эл/донорные зам-ли↓кислотность • 2. Эл/акцепторные зам-ли ↑кислотность,

4. Влияние сольватации на силу кислотности • 1. В газовой фазе (собст-ая кисл-ть) • Чем разветвлённее «С» цепь, тем лучше делокализация «-» заряда, тем↑стабильность Аn⁻, тем↑кислотность. третичные > вторичные > первичные спирты

4. Влияние сольватации на силу кислотности (продолж. ) • 2. В воде – с учётом сольватации • Чем ↑сольватация сопр. осн. , тем↑кислота • Сольватация ↑, чем ↓разветвл-е «С» цепи В воде↑кислотность: перв. >втор. >трет. спирты
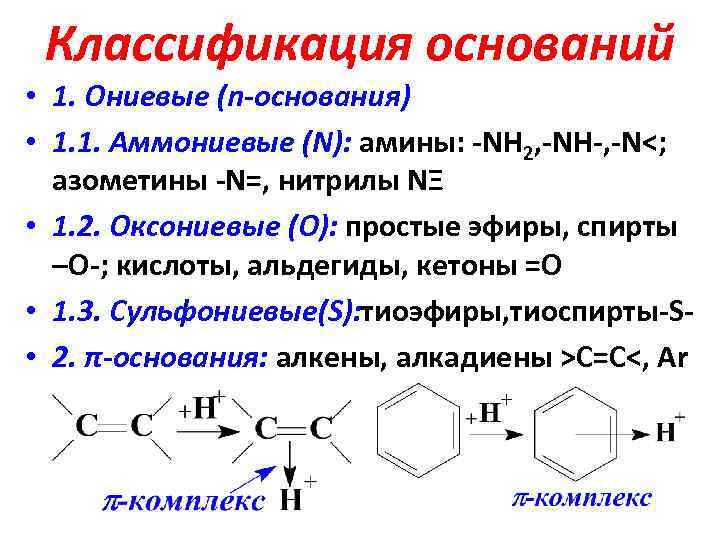
Классификация оснований • 1. Ониевые (n-основания) • 1. 1. Аммониевые (N): амины: -NH 2, -NH-, -N<; азометины -N=, нитрилы NΞ • 1. 2. Оксониевые (О): простые эфиры, спирты –О-; кислоты, альдегиды, кетоны =О • 1. 3. Сульфониевые(S): тиоэфиры, тиоспирты-S • 2. π-основания: алкены, алкадиены >C=С<, Аr
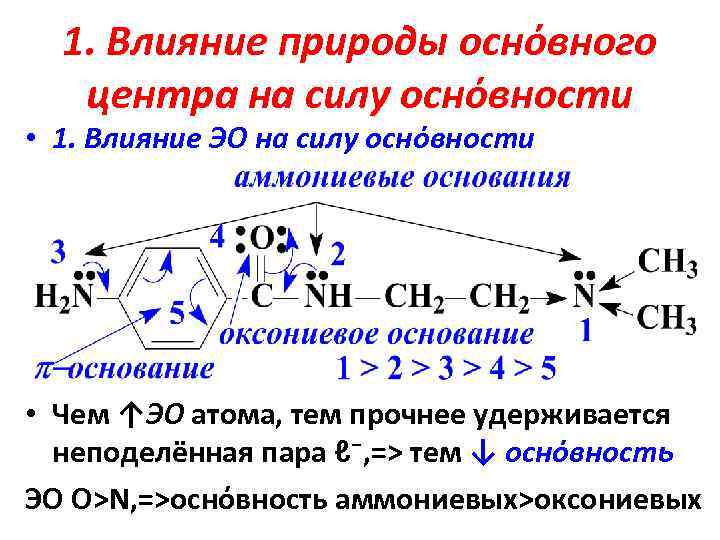
1. Влияние природы оснόвного центра на силу оснόвности • 1. Влияние ЭО на силу оснόвности • Чем ↑ЭО атома, тем прочнее удерживается неподелённая пара ℓ⁻, => тем ↓ оснόвность ЭО О>N, =>оснόвность аммониевых>оксониевых

1. Влияние природы оснόвного центра на силу оснόвности • 2. Влияние поляризуемости на силу оснόвности • Чем ↑поляризуемость, тем ↓оснόвность; у S пара ℓ⁻ рассредоточена в бόльшем объёме, чем у О и N, т. е. они слабее притягивают Н+, => оснόвность возрастает в ряду: сульфониевые < оксониевые < аммониевые основания
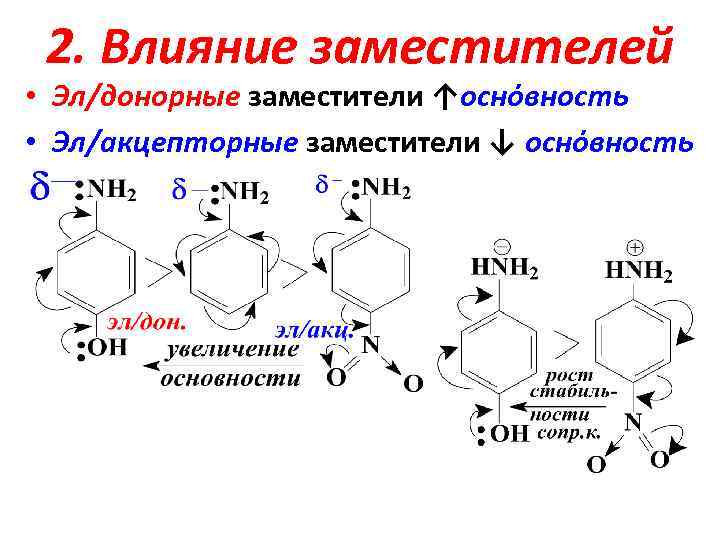
2. Влияние заместителей • Эл/донорные заместители ↑оснόвность • Эл/акцепторные заместители ↓ оснόвность
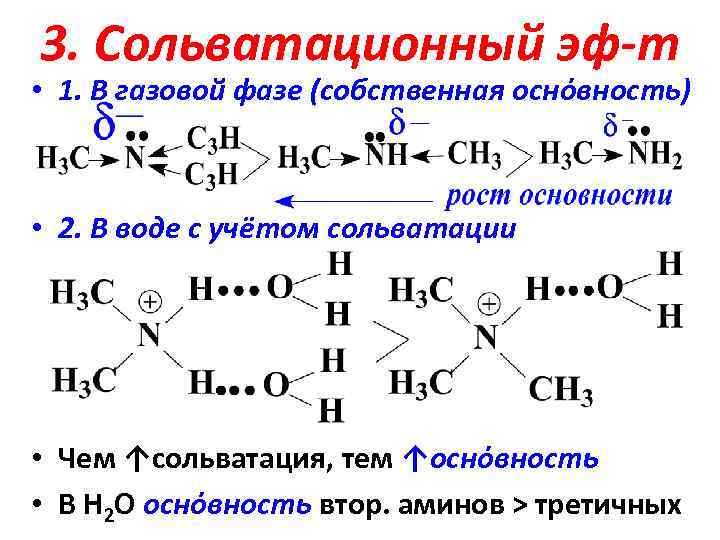
3. Сольватационный эф-т • 1. В газовой фазе (собственная оснόвность) • 2. В воде с учётом сольватации • Чем ↑сольватация, тем ↑оснόвность • В Н 2 О оснόвность втор. аминов > третичных

Теория Льюиса • Теория основана на способности в-в отдавать или принимать ℓ⁻пару с образованием связи • Кислоты Льюиса - атом, молекула или Каt+, обладающие валентной орбиталью и способные принимать пару ℓ⁻ с обр-ем ковал-ой св. • КЛ-акцепторы ℓ⁻пары: Al. Cl 3, Fe. Br 3, Zn. Cl 2, SO 3 • Основания Льюиса - атом, молекула или Аn-, обладающие парой ℓ⁻, которую способны предоставить акцептору для обр-я ковал-ой связи • ОЛ-доноры ℓ⁻пары:

Принцип Пирсона • Кислоты и основания Льюиса делятся на жёсткие и мягкие • Жёсткие основания (ЖО) – доноры ℓ⁻, с↑ЭО, ↓поляризуемостью, трудно [O]. • Прочно удерживают ℓ⁻пару: О, N, F, Cl • Мягкие основания (МО) – доноры ℓ⁻, с↓ЭО, ↑поляризуемостью, легко [O]. • Слабо удерживают ℓ⁻пару: С, S, I

Принцип Пирсона (продолж. ) • Жесткие кислоты (ЖК)– кислоты Льюиса, в которых акцепторные атомы малы по размеру, обладают большим «+» зарядом, ↑ЭО, ↓поляризуемостью: Н+, Na+, Мg 2+, Аl. Cl 3 • Мягкие кислоты (МК) - кислоты Льюиса, в которых акцепторные атомы большого размера, обладают малым «+» зарядом, ↓ЭО, ↑поляризуемостью: Ag+, Cu+, Нg 2+
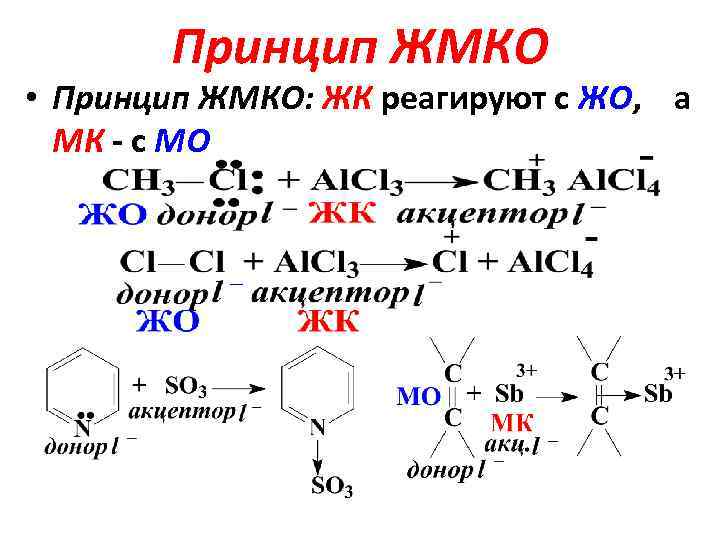
Принцип ЖМКО • Принцип ЖМКО: ЖК реагируют с ЖО, а МК - с МО

Принцип ЖМКО (продолж. ) • Принцип ЖМКО объясняет образование водородных связей в воде и отсутствие их в сероводороде • Н 2 О, ОН-, О – ЖО ; Н+ - ЖК • ЖО взаимодействует с ЖК • Н+ - ЖК ; S – МО • ЖК невзаимодействует с МО

Спасибо за внимание!
3.Кислотность и основность.ppt