Кислотно-щелочной баланс.ppt
- Количество слайдов: 35

Кислотно-щелочной баланс • Основные показатели КЩС • Буферные системы крови • Физиологические системы регуляции КЩС • Формы нарушений КЩС

р. Н • венозной крови • артериальной крови 7, 38 7, 4 • Постоянство р. Н обеспечивается кислотнощелочным равновесием • КЩС – соотношение концентрации водородных и гидроксильных ионов в биологических средах характеризуется концентрацией водородных ионов (нмоль/л) или водородным показателем (power hydrogen) – «сила водорода» • В норме: при р. Н 7, 4 концентрация Н+ составляет 40 нмоль/л при р. Н 7, 0 – 100 нмоль/л при р. Н 8, 0 – 10 нмоль/л

Регуляция КЩС • • осуществляется буферными системами (бикарбонатная и гемоглобиновая) физиологическими механизмами регуляции дыхания экскреции кислот и бикарбоната почками
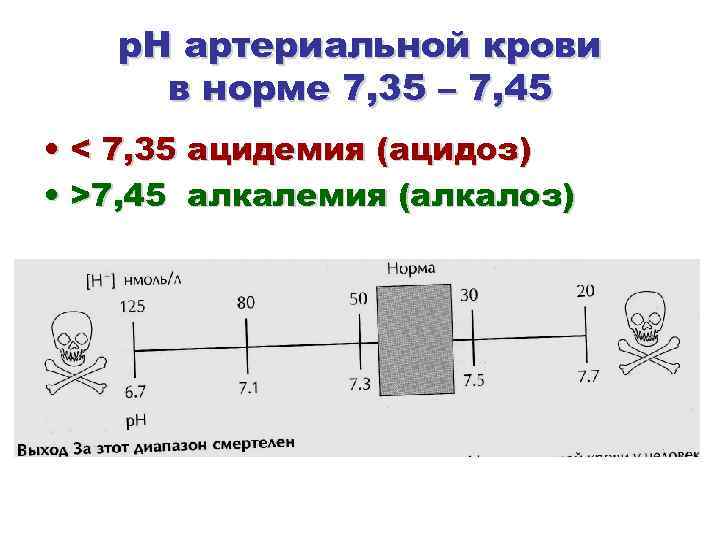
р. Н артериальной крови в норме 7, 35 – 7, 45 • < 7, 35 ацидемия (ацидоз) • >7, 45 алкалемия (алкалоз)

р. СО 2 парциальное давление углекислого газа • Определение р. СО 2 клинически используется как индекс, отражающий дыхательный компонент КОС • В плазме крови СО 2 присутствует в составе Н 2 СО 3, НСО 3 - , карбаминогемоглобина ра. СО 2 – в артериальной крови

• Основное количество СО 2 попадает в эритроциты по градиенту концентрации • В эритроцитах СО 2 превращается в угольную кислоту СО 2 + 2 Н+→ Н 2 СО 3 за счет карбонатдегидратазы • После диссоциации Н 2 СО 3 ионы Н+ связываются гемоглобиновым буфером • Hb в востановленном состоянии (без кислорода) – более мощный буфер, поэтому процесс связывания Н+ усиливается при прохождении крови через капилляры и отдачи кислорода тканям • Когда парциальное давление р. СО 2 высокое (в эритроцитах), то связывается Н+ , когда низкое (в легких), то
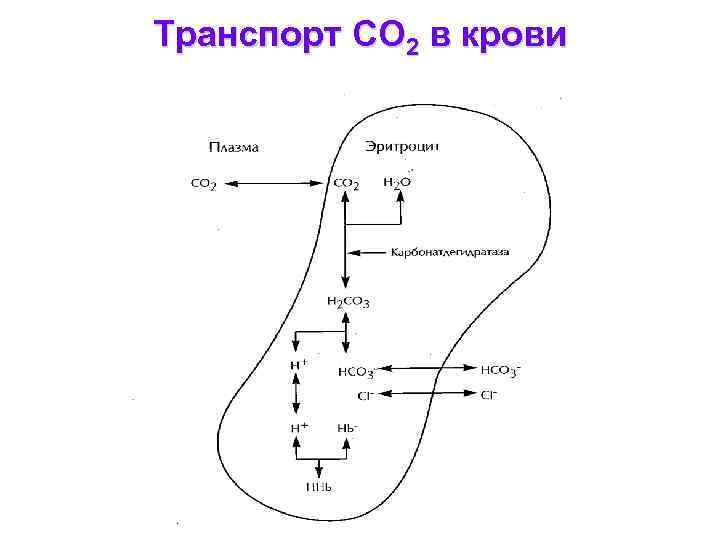
Транспорт СО 2 в крови

НСО 3 - бикарбонат метаболический компонент КОС р. Н = НСО 3 ------- Н 2 СО 3

НСО 3 - act истинный бикарбонат непосредственно измеренные значения • НСО 3 -st стандартный бикарбонат концентрация всех форм бикарбоната в плазме, уравновешенная при р. СО 2 40 мм рт. ст. при насыщении О 2 – 100%

ВВ –Buffer Bases • Состоит из бикарбонатного и небикарбонатного буферных компонентов

ВЕ –Bases Excess

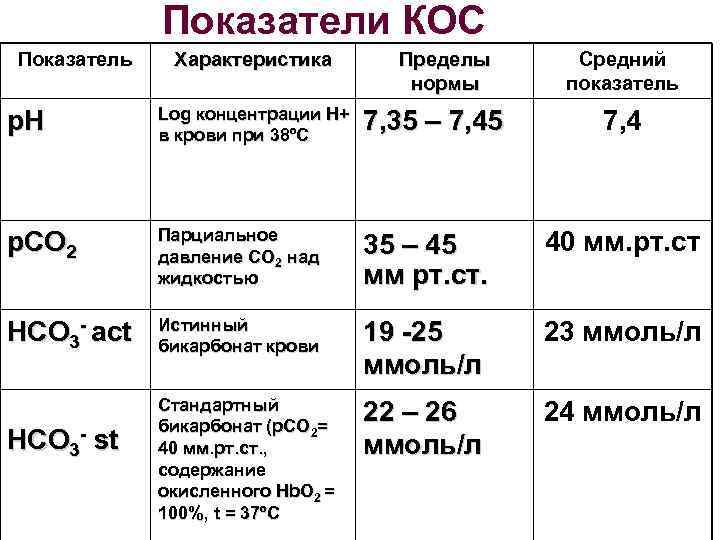
Показатели КОС Показатель Характеристика Пределы нормы Средний показатель р. Н Log концентрации Н+ в крови при 38ºС 7, 35 – 7, 45 7, 4 р. СО 2 Парциальное давление СО 2 над жидкостью 35 – 45 мм рт. ст. 40 мм. рт. ст НСО 3 - асt Истинный бикарбонат крови 19 -25 ммоль/л 23 ммоль/л Стандартный бикарбонат (р. СО 2= 40 мм. рт. ст. , содержание окисленного Hb. O 2 = 100%, t = 37ºC 22 – 26 ммоль/л 24 ммоль/л НСО 3 - st
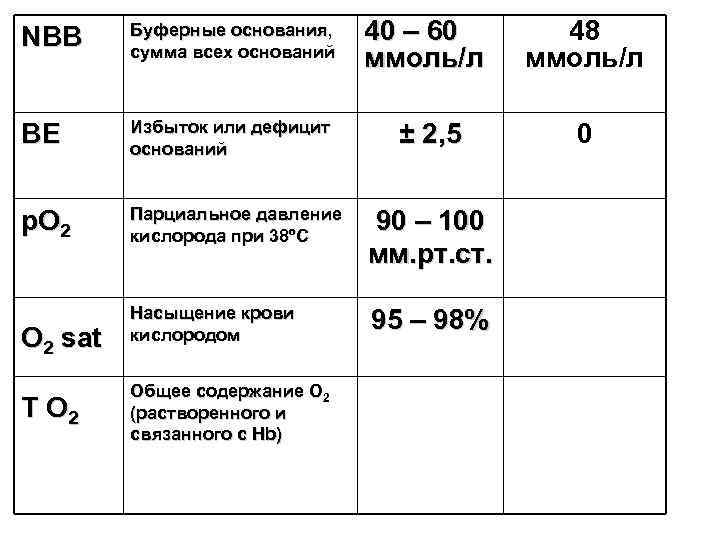
40 – 60 ммоль/л 48 ммоль/л ± 2, 5 0 NВВ Буферные основания, сумма всех оснований BE Избыток или дефицит оснований р. О 2 Парциальное давление кислорода при 38ºС 90 – 100 мм. рт. ст. Насыщение крови кислородом 95 – 98% О 2 sat Т О 2 Общее содержание О 2 (растворенного и связанного с Hb)

КЩС отражает: клеточный метаболизм, газотранспортную функцию крови, внешнее дыхание водно-солевой обмен

Буферные системы крови • Буферными называют растворы, связывающие кислоты или щелочи и тем самым препятствующие изменению р. Н • В клетках большое значение имеют буферные свойства Hb, на втором месте – бикарбонат • В плазме бикарбонат – на первом месте, белки – на втором

Бикарбонатная буферная система • Защищая организм от нарушения концентрации водородных ионов, система срабатывает практически мгновенно –за 30 с. • На долю бикарбонатного буфера приходится около 10% всей буферной емкости крови Na. HCO 3+H 2 CO 3 • При поступлении в кровь кислых продуктов водородные ионы Н+ кислот соединяются с анионами бикарбоната HCO 3 - , что приводит к образованию слабо диссоциирующей угольной кислоты H 2 CO 3, избыток её разлагается на воду и углекислый газ, который выводится из легких при дыхании • бикарбонатный буфер называют летучим

• Угольная кислота в плазме крови и межклеточной жидкости присутствует в 4 формах: СО 2 Н 2 СО 3 НСО 3 - СО 32 - • больше всего бикарбоната; растворенного СО 2 в 20 раз меньше • Ион бикарбоната НСО 3 - может выступать в виде кислоты (отдавать Н+) или щелочи (принимать Н+ ) НСО 3 -↔ Н+ + СО 32 - или НСО 3 - + Н+ ↔ Н 2 СО 3 • Если в крови увеличивается количество Н+, то ион бикарбоната выступает как акцептор, образуется угольная кислота, диссоциирующая на воду и СО 2

Основными параметрами, определяющими вклад бикарбонатной системы регуляции КОС, являются: р. СО 2 и концентрация бикарбоната (НСО 3 - )в крови

Фосфатная буферная система • Na 2 HPO 4 + Na. H 2 PO 4 соль 1 кислота 4 • Емкость этой буферной системы составляет лишь 1% общей буферной емкости крови • Буферное действие основано на связывании Н+ с НРО 42 -, с образованием Н 2 РО 4 • Н+ + НРО 42 -→ Н 2 РО 4 • Взаимодействие ионов гидроксила (ОН) осуществляется с ионами Н 2 РО 4 - • ОН- +Н 2 РО 4 - → НРО 42 - + Н 2 О

Белковая буферная система • Содержит достаточное количество кислых и основных радикалов, действует в зависимости от среды, в которой происходит диссоциация белков • При сдвиге р. Н в кислую сторону диссоциация основных групп угнетается и белок ведет себя как кислота. Связывая основание, эта кислота дает соль. С увеличением р. Н возрастает количество белков в форме соли, а при уменьшении р. Н возрастает количество белков в форме кислоты • Протеин- - Na+ ↔ протеин- - Н+

Гемоглобиновая буферная система • Составляет до 75% всей буферной емкости крови • Участие Hb в регуляции р. Н крови обусловлено его ролью в транспорте О 2 и СО 2 • При насыщении Hb кислородом в капиллярах легких Hb становится более сильной кислотой и отдает в раствор Н+. Отдавая О 2, Hb становится более слабой кислотой, он вновь способен связывать ионы Н+ • Hb эритроцитов отдает О 2 и связывает СО 2. В капиллярах легких происходит разгрузка буферных систем за счет выделения СО 2

Физиологические системы • • Легкие почки Печень жкт

Легкие • Поддерживают нормальную концентрацию СО 2 • В норме р. СО 2 = 35 – 45 мм. рт. ст • При заболеваниях дыхательной системы, приводящих к гиповентиляции (отек легких, пневмония) СО 2 не удаляется в достаточной степени легкими. В крови образуется большое количество Н 2 СО 3 и развивается респираторный ацидоз. Компенсация дыхательного ацидоза осуществляется почками путем форсированного выведения ионов Н+ и хлоридов, а также задержки (повышения реабсорбции) ионов НСО 3 • При раздражении дыхательного центра (травма черепа, кровоизлияние в мозг, печеночная кома, интоксикация салицилатами) наблюдается гипервентиляция, приводящая к усиленному выделению СО 2, связыванию ионов Н+ и сдвигу р. Н в щелочную сторону. Возникает состояние респираторного алкалоза

Почки • Сдвигают р. Н медленнее, чем легкие, им необходимо 10 – 20 часов • Почки управляют процессом выделения ионов Н+ и сохранения оснований • При ацидемии ионы Н+ экскретируются в мочу, благодаря реакции с фосфатным буфером; при этом из мочи в обмен на выделенные ионы Н+ поступают ионы Na+, которые в клетках канальцев соединяются с ионами НСО 3 и в виде бикарбоната натрия реабсорбируются • При алкалемии поступающий к клеткам почечных канальцев ион Н+ задерживается, а ион НСО 3 -, не реабсорбируясь, выделяется почками

Формы нарушений КОС • При компенсированной форме ацидоза или алкалоза отношение буферных систем нарушается и р. Н сдвигается в ту или другую сторону, но в пределах не выходящих за рамки физиологических норм • Если кислотные или щелочные сдвиги превышают способность буферных систем, те же расстройства имеют характер декомпенсированных

• Метаболический (обменный) ацидоз • Респираторный (дыхательный) ацидоз • Метаболический алкалоз • Респираторный алкалоз

Метаболический ацидоз • Накопление недоокисленных продуктов распада и органических кислот • Кетоацидозы – при диабете, голодании • Лактатацидозы – при шоке, гипоксии, сахарном диабете, заболеваниях печени, легочной и сердечной недостаточности, под действием алкоголя • Расстройства микроциркуляции и метаболизма (гипоксия) • Снижение р. Н плазмы крови, уменьшение бикарбоната, дефицит оснований • Терапия направлена на восстановление сниженного резерва бикарбонатов и борьбу с гиперкалиемией

Респираторный ацидоз • Пониженное выведение СО 2 легкими при снижении минутного объема дыхания (бронхит, пневмония, бронхиальная астма) • Эти заболевания приводят к гиповентиляции и гиперкапнии (РСО 2 более 50 мм рт. ст. ). Выше 100200 мм рт. ст. может развиться гиперкапническая кома • Снижается р. Н крови, содержание бикарбоната в острой фазе не меняется, позже – компенсаторно повышается. Повышается содержание абс. бикарбоната, избыток оснований ВЕ+ • Основная компенсация осуществляется почками, путем форсированного выведения Н+ и хлоридов, повышения реабсорбции НСО 3 - • НСО 3 st < HCO 3 act • Лечение – улучшение альвеолярной вентиляции

Метаболический алкалоз • Потеря кислых или накопление щелочных метаболитов при неукротимой рвоте, накоплении щелочных эквивалентов при тетании • р. Н выше 7, 45, ст. бикарбонат выше 27 ммоль/л, ВЕ+ превышает 2, 5 • Обычно сочетается с гипокалиемией • При тяжелом алкалозе развивается дегидратация и гипонатриемия • Профилактика и лечение: достаточное введение ионов калия, своевременное восполнение кровопотери, нормализация периферического кровообращения

Респираторный алкалоз • Резкое увеличение дыхательной функции легких при испуге, боли, ИВЛ, травмах ЦНС, сепсисе, острой почечной недостаточности • Сопровождается понижением содержания Н 2 СО 3 в крови и повышением р. Н выше 7, 5 - 7, 75 • Компенсация за счет усиления экскреции бикарбоната почками и задержания Н+ • Обычно сочетается со снижением Са 2+ , развитием тетании • Снижение К+ приводит к нарушениям сердечного ритма • При снижении РСО 2 до 20 мм. ртст. развивается вазоконстрикция, снижается мозговой кровоток • Профилактика и лечение направлены на нормализацию внешнего дыхания • НСО 3 st > HCO 3 act
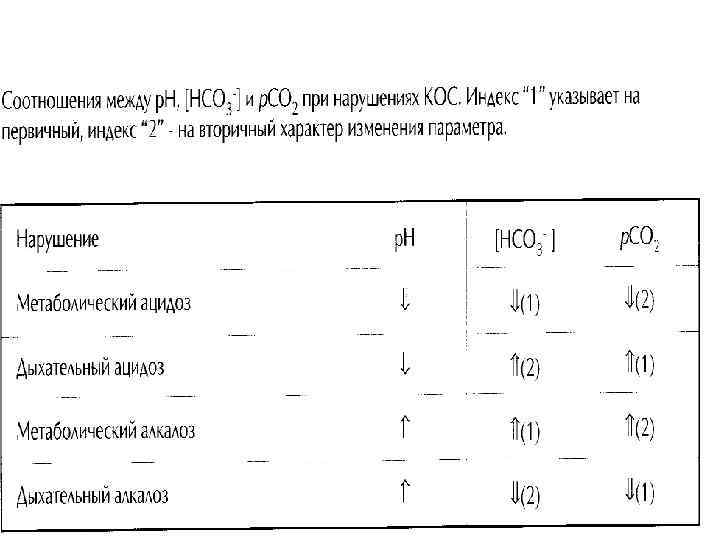

2 р. Н р. СО 2 р. О 2 HCO 3 a HCO 3 s BE O 2 sat 7, 623 ↑ ↓ 21, 0 mm. Hg ↑ 149, 4 mm. Hg 21, 9 mmol/l 28, 5 mmol/l 4, 4 mmol/l 99, 3% Electrolytes 37º C Na ↑ 151, 0 mmol/l K ↑ 6, 94 mmol/l Ca ↓ 0, 70 mmol/l

Заключение ? • 1. Метаболический ацидоз в стадии компенсации? Гиповентиляция, дефицит оснований, гипо - К и гипо-Са (сахарный диабет на фоне лечения инсулином, шок, гипоксия)? ? • 2. Респираторный алкалоз, компенсация • гипер - Na, гипо – Са • (сердечная, почечная недостаточность)? ?
Кислотно-щелочной баланс.ppt