10_Кислотно-основные взаимодействия.ppt
- Количество слайдов: 22
 Кислотно-основные взаимодействия. Принцип ЖМКО Пирсона
Кислотно-основные взаимодействия. Принцип ЖМКО Пирсона
 Электролитическая теория • первая научная ионная теория кислот и оснований (Оствальд, Аррениус, 1890 год). Согласно этой теории, кислоты - это водородсодержащие соединения, способные при электролитической диссоциации выступать в роли источника протонов (ионов Н+), а основания рассматривались как источник ионов гидроксила (ОН-).
Электролитическая теория • первая научная ионная теория кислот и оснований (Оствальд, Аррениус, 1890 год). Согласно этой теории, кислоты - это водородсодержащие соединения, способные при электролитической диссоциации выступать в роли источника протонов (ионов Н+), а основания рассматривались как источник ионов гидроксила (ОН-).
 Амфотерность • А. Ганч в 1917 -1927 годах ввел понятие об амфотерности - способности некоторых соединений проявлять как кислотные, так и основные свойства в зависимости от условий и природы реагентов, участвующих в кислотноосновном взаимодействии. • Как оказалось позже, соединений, проявляющих амфотерность, подавляющее большинство. В зависимости от природы партнера по взаимодействию кислота может выступать в роли основания, и наоборот.
Амфотерность • А. Ганч в 1917 -1927 годах ввел понятие об амфотерности - способности некоторых соединений проявлять как кислотные, так и основные свойства в зависимости от условий и природы реагентов, участвующих в кислотноосновном взаимодействии. • Как оказалось позже, соединений, проявляющих амфотерность, подавляющее большинство. В зависимости от природы партнера по взаимодействию кислота может выступать в роли основания, и наоборот.
 Теории кислот и оснований • протолитическая (И. Бренстед и Т. Лоури) и электронная (Г. Льюис) теории кислот и оснований были предложены одновременно в 1923 году. • По Бренстеду-Лоури, кислоты представляют собой вещества, способные отдавать протон, а основания - вещества, присоединяющие протон. Кислота – понятие относительное. CH 3 COOH + H 2 O = H 3 O+ + CH 3 COOH 2 SO 4 + CH 3 COOH = CH 3 C(OH)2+ + HSO 4 -
Теории кислот и оснований • протолитическая (И. Бренстед и Т. Лоури) и электронная (Г. Льюис) теории кислот и оснований были предложены одновременно в 1923 году. • По Бренстеду-Лоури, кислоты представляют собой вещества, способные отдавать протон, а основания - вещества, присоединяющие протон. Кислота – понятие относительное. CH 3 COOH + H 2 O = H 3 O+ + CH 3 COOH 2 SO 4 + CH 3 COOH = CH 3 C(OH)2+ + HSO 4 -
 В протолитической теории • Вода принята за своеобразный стандарт для оценки кислотно-основных свойств веществ - стандарт нейтральной среды. • Если в аналогичных условиях рассматриваемое вещество способно отдавать протон легче, чем вода, то его относят к группе кислот. Если вещество по способности присоединять (связывать) протон превосходит воду - это основание (основность выше, чем у воды).
В протолитической теории • Вода принята за своеобразный стандарт для оценки кислотно-основных свойств веществ - стандарт нейтральной среды. • Если в аналогичных условиях рассматриваемое вещество способно отдавать протон легче, чем вода, то его относят к группе кислот. Если вещество по способности присоединять (связывать) протон превосходит воду - это основание (основность выше, чем у воды).
 Почему вода? • Вода - одно из самых распространенных на Земле соединений. • Ее кислотно-основные свойства определяют естественный фон (атмосфера, почва, моря и океаны). • Вода хорошо растворяет многие полярные и диссоциирующие на ионы вещества. • По физическим характеристикам вода хорошо сольватирует как недиссоциированные молекулы, так и свободные ионы. • Кроме того, молекулы воды способны к автопротолизу - передаче протона между молекулами одного и того же вещества: H 2 O + H 2 O = H 3 O+ + OH-
Почему вода? • Вода - одно из самых распространенных на Земле соединений. • Ее кислотно-основные свойства определяют естественный фон (атмосфера, почва, моря и океаны). • Вода хорошо растворяет многие полярные и диссоциирующие на ионы вещества. • По физическим характеристикам вода хорошо сольватирует как недиссоциированные молекулы, так и свободные ионы. • Кроме того, молекулы воды способны к автопротолизу - передаче протона между молекулами одного и того же вещества: H 2 O + H 2 O = H 3 O+ + OH-
 Количественная мера кислотности и основности • Кислотность соединений количественно оценивается долей ионизированной формы вещества в растворе (воде) или константой равновесия (К) реакции переноса протона от кислоты к воде как основанию.
Количественная мера кислотности и основности • Кислотность соединений количественно оценивается долей ионизированной формы вещества в растворе (воде) или константой равновесия (К) реакции переноса протона от кислоты к воде как основанию.
 Принцип ЖМКО Пирсона (1963) Кислоты и основания Льюиса делятся на жёсткие и мягкие, причём мягкие кислоты преимущественно реагируют с мягкими основаниями, а жёсткие кислоты — с жёсткими основаниями. Жёсткость кислоты или основания означает его склонность образовывать связи преимущественно ионного характера, а мягкость кислоты или основания — склонность к образованию связей ковалентного характера
Принцип ЖМКО Пирсона (1963) Кислоты и основания Льюиса делятся на жёсткие и мягкие, причём мягкие кислоты преимущественно реагируют с мягкими основаниями, а жёсткие кислоты — с жёсткими основаниями. Жёсткость кислоты или основания означает его склонность образовывать связи преимущественно ионного характера, а мягкость кислоты или основания — склонность к образованию связей ковалентного характера
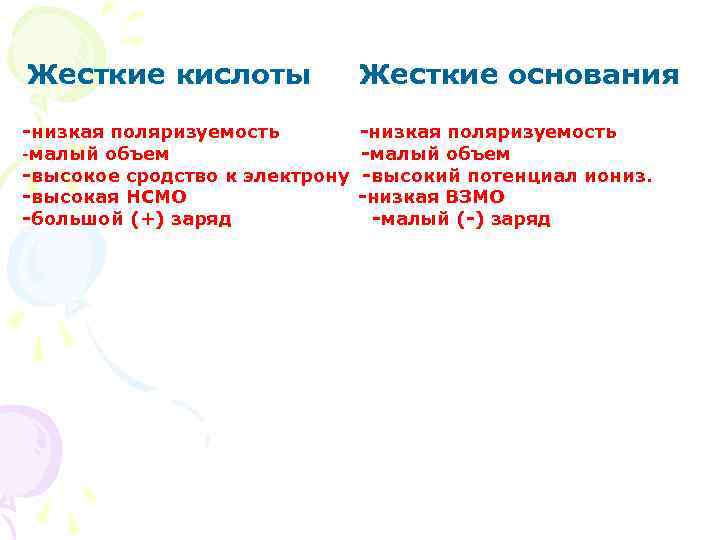 Жесткие кислоты Жесткие основания -низкая поляризуемость -малый объем -высокое сродство к электрону -высокая НСМО -большой (+) заряд -низкая поляризуемость -малый объем -высокий потенциал иониз. -низкая ВЗМО -малый (-) заряд
Жесткие кислоты Жесткие основания -низкая поляризуемость -малый объем -высокое сродство к электрону -высокая НСМО -большой (+) заряд -низкая поляризуемость -малый объем -высокий потенциал иониз. -низкая ВЗМО -малый (-) заряд
 Мягкие кислоты Мягкие основания -высокая поляризуемость -большой объем -низкая НСМО -высокая ВЗМО -малое сродство к электрону -малый потенциал иониз. -малый (+) заряд -большой (-)заряд Поляризуемость мягких кислот и оснований: в большом атоме (или ионе с малым эффективным зарядом ядра) относительно легко «искажается» электронное облако (частица поляризуется)
Мягкие кислоты Мягкие основания -высокая поляризуемость -большой объем -низкая НСМО -высокая ВЗМО -малое сродство к электрону -малый потенциал иониз. -малый (+) заряд -большой (-)заряд Поляризуемость мягких кислот и оснований: в большом атоме (или ионе с малым эффективным зарядом ядра) относительно легко «искажается» электронное облако (частица поляризуется)
 Классификация кислот и оснований в рамках принципа ЖМКО Жёсткие кислоты Промежуточные кислоты Мягкие кислоты H+, Li+, Na+, K+, Mg 2+, Ca 2+, Cu 2+, Fe 2+, Zn 2+, SO 2, R 3 C+, Al 3+, Cr 3+, Fe 3+, BF 3, B(OR)3, C 6 H 5+, NO+ Al. R 3, Al. Cl 3, SO 3, RCO+, CO 2, RSO 2+ Ag+, Cu+, Hg 2+, RS+, I+, Br+, Pb 2+, карбены Жёсткие основания Мягкие основания Промежуточные основания OH-, RO-, F-, Cl-, RCOO-, NO 3 Br-, C 6 H 5 NH 2, NO 2 -, C 5 H 5 N -, NH , RNH , H O, ROH, 3 2 2 2 -, CO 2 -, R O, NR -, NH SO 4 3 2 2 2 RS-, RSH, I-, H-, R 3 C-, алкены, C 6 H 6, R 3 P, (RO)3 P
Классификация кислот и оснований в рамках принципа ЖМКО Жёсткие кислоты Промежуточные кислоты Мягкие кислоты H+, Li+, Na+, K+, Mg 2+, Ca 2+, Cu 2+, Fe 2+, Zn 2+, SO 2, R 3 C+, Al 3+, Cr 3+, Fe 3+, BF 3, B(OR)3, C 6 H 5+, NO+ Al. R 3, Al. Cl 3, SO 3, RCO+, CO 2, RSO 2+ Ag+, Cu+, Hg 2+, RS+, I+, Br+, Pb 2+, карбены Жёсткие основания Мягкие основания Промежуточные основания OH-, RO-, F-, Cl-, RCOO-, NO 3 Br-, C 6 H 5 NH 2, NO 2 -, C 5 H 5 N -, NH , RNH , H O, ROH, 3 2 2 2 -, CO 2 -, R O, NR -, NH SO 4 3 2 2 2 RS-, RSH, I-, H-, R 3 C-, алкены, C 6 H 6, R 3 P, (RO)3 P
 • Помимо условного деления на три типа, можно также проследить зависимость жёсткости или мягкости в рядах отдельных кислот и оснований Льюиса. Например, при движении по группе периодической системы сверху вниз жёсткость оснований уменьшается: F- > Cl- > Br- > I • При движении по группе сверху вниз жёсткость кислот тоже уменьшается : Li+ > Na+ > K+; Zn 2+ > Cd 2+ > Hg 2+ • Для изоэлектронных соединений жёсткость возрастает при движении по группе слева направо: СH 3 - < NH 2 - < OH- < F-
• Помимо условного деления на три типа, можно также проследить зависимость жёсткости или мягкости в рядах отдельных кислот и оснований Льюиса. Например, при движении по группе периодической системы сверху вниз жёсткость оснований уменьшается: F- > Cl- > Br- > I • При движении по группе сверху вниз жёсткость кислот тоже уменьшается : Li+ > Na+ > K+; Zn 2+ > Cd 2+ > Hg 2+ • Для изоэлектронных соединений жёсткость возрастает при движении по группе слева направо: СH 3 - < NH 2 - < OH- < F-
 Ж. кис. + Ж. осн. = Зарядовый контроль Высоколежащая НСМО к-ты + низколежащая ВЗМО осн-я. Определяющая роль – возмущение II порядка, зарядовое взаимодействие, определяемое кулоновскими силами (~ q 1 q 2/r 2) М. кис. + М. осн. = Орбитальный контроль Низколежащая НСМО к-ты + высоколежащая ВЗМО основания. Определяющая роль – возмущение I порядка, орбитальное взаимодействие
Ж. кис. + Ж. осн. = Зарядовый контроль Высоколежащая НСМО к-ты + низколежащая ВЗМО осн-я. Определяющая роль – возмущение II порядка, зарядовое взаимодействие, определяемое кулоновскими силами (~ q 1 q 2/r 2) М. кис. + М. осн. = Орбитальный контроль Низколежащая НСМО к-ты + высоколежащая ВЗМО основания. Определяющая роль – возмущение I порядка, орбитальное взаимодействие
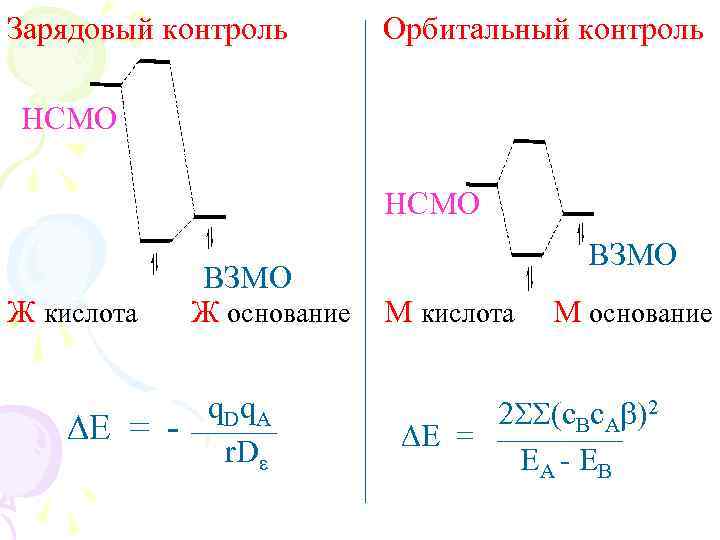 Зарядовый контроль Орбитальный контроль НСМО Ж кислота ВЗМО Ж основание q. Dq. A DE = r. De ВЗМО М кислота М основание 2 SS(c. Bc. Ab)2 DE = EA - EB
Зарядовый контроль Орбитальный контроль НСМО Ж кислота ВЗМО Ж основание q. Dq. A DE = r. De ВЗМО М кислота М основание 2 SS(c. Bc. Ab)2 DE = EA - EB
 Применение в органической химии В органической химии принцип ЖМКО широко применяется для предсказания или объяснения протекания химических реакций. Например, реакцию между тиоэфиром CH 3 COSR и алкоголят-ионом RO– можно представить как переход ацильного катиона CH 3 CO+ (жёсткой кислоты Льюиса) от мягкого основания Льюиса RS– к жёсткому основанию Льюиса RO–. Согласно принципу ЖМКО, аддукт жёсткой кислоты и жёсткого основания более устойчив, поэтому равновесие в реакции сдвинуто вправо.
Применение в органической химии В органической химии принцип ЖМКО широко применяется для предсказания или объяснения протекания химических реакций. Например, реакцию между тиоэфиром CH 3 COSR и алкоголят-ионом RO– можно представить как переход ацильного катиона CH 3 CO+ (жёсткой кислоты Льюиса) от мягкого основания Льюиса RS– к жёсткому основанию Льюиса RO–. Согласно принципу ЖМКО, аддукт жёсткой кислоты и жёсткого основания более устойчив, поэтому равновесие в реакции сдвинуто вправо.
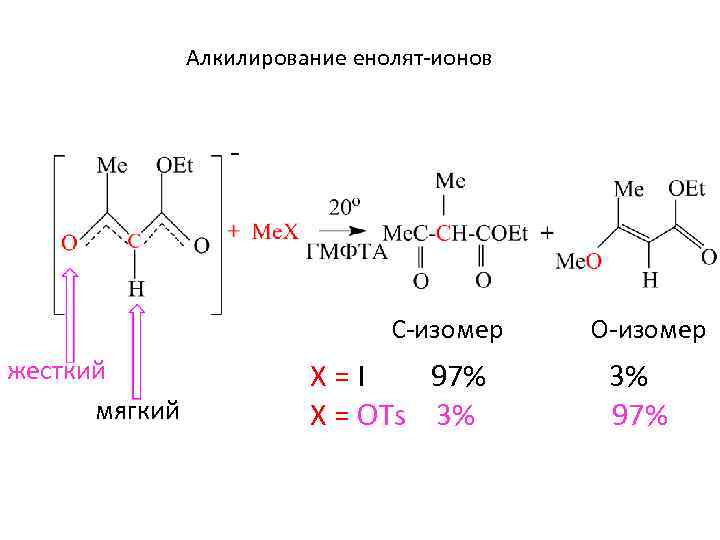
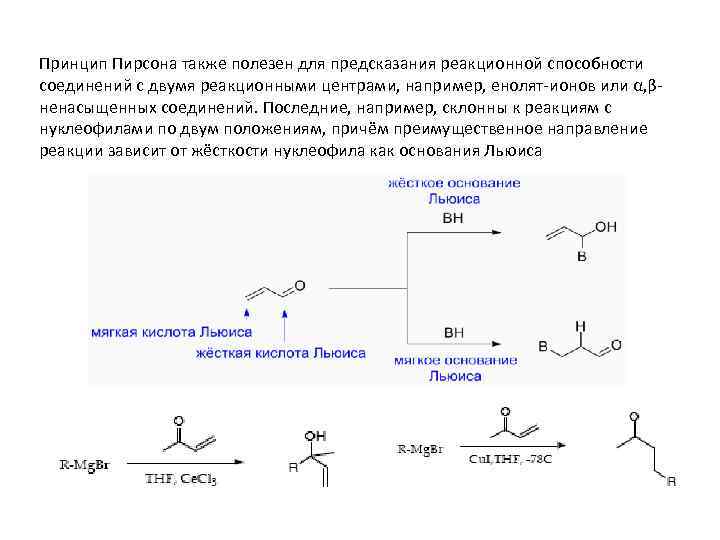 Принцип Пирсона также полезен для предсказания реакционной способности соединений с двумя реакционными центрами, например, енолят-ионов или α, βненасыщенных соединений. Последние, например, склонны к реакциям с нуклеофилами по двум положениям, причём преимущественное направление реакции зависит от жёсткости нуклеофила как основания Льюиса
Принцип Пирсона также полезен для предсказания реакционной способности соединений с двумя реакционными центрами, например, енолят-ионов или α, βненасыщенных соединений. Последние, например, склонны к реакциям с нуклеофилами по двум положениям, причём преимущественное направление реакции зависит от жёсткости нуклеофила как основания Льюиса
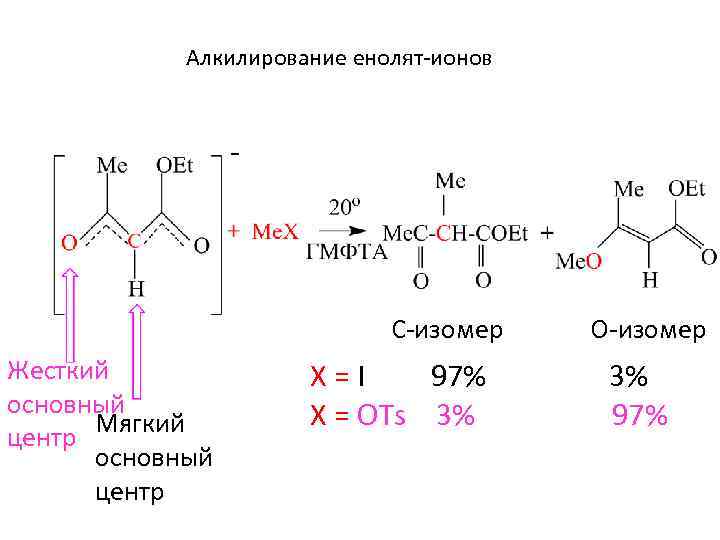 Алкилирование енолят-ионов С-изомер О-изомер Жесткий основный Мягкий центр основный центр Х = I 97% 3% X = OTs 3% 97%
Алкилирование енолят-ионов С-изомер О-изомер Жесткий основный Мягкий центр основный центр Х = I 97% 3% X = OTs 3% 97%
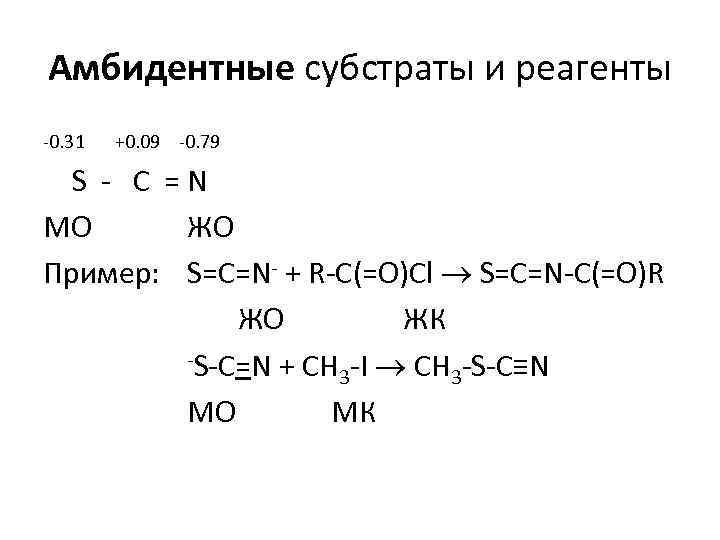 Амбидентные субстраты и реагенты -0. 31 +0. 09 -0. 79 S - C = N MО ЖО Пример: S=C=N- + R-C(=O)Cl S=C=N-C(=O)R ЖО ЖК -S-C=N + СH -I CH -S-C≡N 3 3 МО МК
Амбидентные субстраты и реагенты -0. 31 +0. 09 -0. 79 S - C = N MО ЖО Пример: S=C=N- + R-C(=O)Cl S=C=N-C(=O)R ЖО ЖК -S-C=N + СH -I CH -S-C≡N 3 3 МО МК
 Амбидентность нитрит – иона O- – N = O ЖО МО С 8 H 17 Br + Ag. NO 2 C 8 H 17 O-N=O + Ag. Br Мягкая кислота Ag+ координируется с мягким основанием N и освобождает O С 8 H 17 Br + Na. NO 2 C 8 H 17 NO 2 + Na. Br Жесткая кислота Na+ координируется с жестким основанием О и освобождает N
Амбидентность нитрит – иона O- – N = O ЖО МО С 8 H 17 Br + Ag. NO 2 C 8 H 17 O-N=O + Ag. Br Мягкая кислота Ag+ координируется с мягким основанием N и освобождает O С 8 H 17 Br + Na. NO 2 C 8 H 17 NO 2 + Na. Br Жесткая кислота Na+ координируется с жестким основанием О и освобождает N
 Амбидентность енолят-аниона • (С 2 H 5)3 OF (фторид триэтилоксония) – очень жесткий реагент – алкилирует енолят – анион по атому О (жесткому основному центру) • С 2 Н 5 I – очень мягкий реагент – алкилирует енолят-анион по атому С (мягкому основному центру)
Амбидентность енолят-аниона • (С 2 H 5)3 OF (фторид триэтилоксония) – очень жесткий реагент – алкилирует енолят – анион по атому О (жесткому основному центру) • С 2 Н 5 I – очень мягкий реагент – алкилирует енолят-анион по атому С (мягкому основному центру)
 Алкилирование енолят-ионов С-изомер О-изомер жесткий мягкий Х = I 97% 3% X = OTs 3% 97%
Алкилирование енолят-ионов С-изомер О-изомер жесткий мягкий Х = I 97% 3% X = OTs 3% 97%
![В газовой фазе: Me-OH + H-I М-Ж Ж-М Kp = [H 2 O] [Me. В газовой фазе: Me-OH + H-I М-Ж Ж-М Kp = [H 2 O] [Me.](https://present5.com/presentation/6743881_439550567/image-22.jpg) В газовой фазе: Me-OH + H-I М-Ж Ж-М Kp = [H 2 O] [Me. I] [HI] [Me. OH] Me. I + H-OH М-М Ж-Ж Kp > 109 Симбиоз лигандов во внутренней сфере комплекса [Co(NH 3)5 F]2+ более стабилен, чем [Co(NH 3)5 I]2+ [Co(CN)5 I]2+ более стабилен, чем [Co(CN)5 F]2+
В газовой фазе: Me-OH + H-I М-Ж Ж-М Kp = [H 2 O] [Me. I] [HI] [Me. OH] Me. I + H-OH М-М Ж-Ж Kp > 109 Симбиоз лигандов во внутренней сфере комплекса [Co(NH 3)5 F]2+ более стабилен, чем [Co(NH 3)5 I]2+ [Co(CN)5 I]2+ более стабилен, чем [Co(CN)5 F]2+


