кисл.-осн.равн. - копия.ppt
- Количество слайдов: 41
 КИСЛОТНО ОСНОВНЫЕ РАВНОВЕСИЯ В АНАЛИТИЧЕСКОЙ ХИМИИ.
КИСЛОТНО ОСНОВНЫЕ РАВНОВЕСИЯ В АНАЛИТИЧЕСКОЙ ХИМИИ.
 ПЛАН 1. Понятия кислоты и основания с точки зрения теорий Аррениуса, Льюиса, Пирсона и Усановича. 2. Протолитическая теории кислот и оснований. 3. Протолитические равновесия в воде. Автопротолиз. 4. Характеристика силы слабых кислот и основания. Константы кислотности и основности. 5. Классификация и свойства растворителей.
ПЛАН 1. Понятия кислоты и основания с точки зрения теорий Аррениуса, Льюиса, Пирсона и Усановича. 2. Протолитическая теории кислот и оснований. 3. Протолитические равновесия в воде. Автопротолиз. 4. Характеристика силы слабых кислот и основания. Константы кислотности и основности. 5. Классификация и свойства растворителей.
 1. ПОНЯТИЯ КИСЛОТЫ И ОСНОВАНИЯ С ТОЧКИ ЗРЕНИЯ ТЕОРИЙ АРРЕНИУСА, ЛЬЮИСА, ПИРСОНА И УСАНОВИЧА. Существует несколько теоретических концепций кислотно-основных превращений. Первой теоретической концепцией кислот и оснований была теория Аррениуса, в основе которой лежит электролитическая диссоциация веществ в растворах. По теории Аррениуса-Оствальда кислотой называлось электронейтральное вещество, которое при растворении в воде диссоциировало с образованием иона Н+, а основанием – вещество, которое диссоциировало с образованием ОН-. Однако представления теории кислот и оснований Аррениуса -Оствальда оказались неприменимыми ко многим водным и неводным растворам.
1. ПОНЯТИЯ КИСЛОТЫ И ОСНОВАНИЯ С ТОЧКИ ЗРЕНИЯ ТЕОРИЙ АРРЕНИУСА, ЛЬЮИСА, ПИРСОНА И УСАНОВИЧА. Существует несколько теоретических концепций кислотно-основных превращений. Первой теоретической концепцией кислот и оснований была теория Аррениуса, в основе которой лежит электролитическая диссоциация веществ в растворах. По теории Аррениуса-Оствальда кислотой называлось электронейтральное вещество, которое при растворении в воде диссоциировало с образованием иона Н+, а основанием – вещество, которое диссоциировало с образованием ОН-. Однако представления теории кислот и оснований Аррениуса -Оствальда оказались неприменимыми ко многим водным и неводным растворам.
 ТЕОРИЯ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ АРРЕНИУСА-ОСТВАЛЬДА. Кислоты - это вещества, образующие в водном растворе гидратированные катионы водорода Н+ (ионы HCl → H+ + Cl гидроксония) и анионы кислотного остатка. НNО 3 → H+ + NO 3 Н 2 SO 4 → H+ + HSO 4 ↔ H+ + SO 42 Основание - это вещество, образующие в водном растворе гuдрокcид-ион (гидроксильный ион) OН-. Na. OH → Na + + ОН + KOH → K + OH Са(ОН)2 → Са(ОН)+ + ОН Са(ОН)+ ↔ Са 2+ + ОН NН 3·Н 2 О ↔ NН 4 ОH ↔ NН 4+ + ОН и т. д.
ТЕОРИЯ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ АРРЕНИУСА-ОСТВАЛЬДА. Кислоты - это вещества, образующие в водном растворе гидратированные катионы водорода Н+ (ионы HCl → H+ + Cl гидроксония) и анионы кислотного остатка. НNО 3 → H+ + NO 3 Н 2 SO 4 → H+ + HSO 4 ↔ H+ + SO 42 Основание - это вещество, образующие в водном растворе гuдрокcид-ион (гидроксильный ион) OН-. Na. OH → Na + + ОН + KOH → K + OH Са(ОН)2 → Са(ОН)+ + ОН Са(ОН)+ ↔ Са 2+ + ОН NН 3·Н 2 О ↔ NН 4 ОH ↔ NН 4+ + ОН и т. д.
 ЭЛЕКТРОННАЯ ТЕОРИЯ ЛЬЮИСА Еще более общей является теория кислот и оснований американско го ученого Г. Н. Льюиса, предложенная им в 1926 г. Согласно этой тео рии, кислота соединение, способное при нять электронную пару с образованием ковалентной связи, а основание соединение, способное предоставить электронную пару для образования ковалентной связи. Типичный пример аммиак NН 3 и протон Н+, дающие катион аммония NН 4+: Н + ·· Н ׃ N + ׃ H+ = H ׃ N ׃ H ·· H основание по Льюису кислота по Льюису
ЭЛЕКТРОННАЯ ТЕОРИЯ ЛЬЮИСА Еще более общей является теория кислот и оснований американско го ученого Г. Н. Льюиса, предложенная им в 1926 г. Согласно этой тео рии, кислота соединение, способное при нять электронную пару с образованием ковалентной связи, а основание соединение, способное предоставить электронную пару для образования ковалентной связи. Типичный пример аммиак NН 3 и протон Н+, дающие катион аммония NН 4+: Н + ·· Н ׃ N + ׃ H+ = H ׃ N ׃ H ·· H основание по Льюису кислота по Льюису
 ТЕОРИИ ПИРСОНА И УСАНОВИЧА • Развитием теории Льюиса стала концепция жестких и мягких кислот Пирсона, по которой при взаимодействии кислоты – акцептора пары электронов с основанием – донором пары электронов не обязательно получается ковалентная связь, и могут возникать ионная и координационная связи. В круг кислотно основных реакций включается, таким образом, комплексообразование. • Наиболее обшей теорией кислот и оснований является теория Усановича, по которой кислотами считаются вещества, отдающие катионы или принимающие анионы (или электроны), основаниями – вещества, отдающие анионы (или электроны) и принимающие катионы. • В дальнейшем будем пользовался преимущественно протолитиче ской теорией кислот и оснований Бренстеда Лоури.
ТЕОРИИ ПИРСОНА И УСАНОВИЧА • Развитием теории Льюиса стала концепция жестких и мягких кислот Пирсона, по которой при взаимодействии кислоты – акцептора пары электронов с основанием – донором пары электронов не обязательно получается ковалентная связь, и могут возникать ионная и координационная связи. В круг кислотно основных реакций включается, таким образом, комплексообразование. • Наиболее обшей теорией кислот и оснований является теория Усановича, по которой кислотами считаются вещества, отдающие катионы или принимающие анионы (или электроны), основаниями – вещества, отдающие анионы (или электроны) и принимающие катионы. • В дальнейшем будем пользовался преимущественно протолитиче ской теорией кислот и оснований Бренстеда Лоури.
 2. ПРОТОЛИТИЧЕСКАЯ ТЕОРИЯ БРЕНСТЕДА И ЛОУРИ. • Протолитическая теория (1923 г). Теория основана на особенностях иона водорода. Протон лишен электронной оболочки, он на пять порядков меньше других ионов и очень подвижен. • В протолитической теории кислотами называются вещества, способные отдавать протон другому веществу, а основаниями – вещества, способные принимать протон. • Вещества, способные как присоединять, так и отдавать протоны, на зываются мфолитами (или амфотерными веществами). Примерами а амфолитов могут служить вода, гидрокарбонат ион HCO 3 , гидросульфид ион HS и др. Так, гидрокарбонат ион может отдавать протоны: • HCO 3 = Н+ + CO 32 • или принимать их: • HCO 3 + Н+ = Н 2 СОз = Н 2 О+СО 2↑ • Аналогично в случае гидросульфид иона: • HS = Н+ +S 2 • HS + Н+ = H 2 S
2. ПРОТОЛИТИЧЕСКАЯ ТЕОРИЯ БРЕНСТЕДА И ЛОУРИ. • Протолитическая теория (1923 г). Теория основана на особенностях иона водорода. Протон лишен электронной оболочки, он на пять порядков меньше других ионов и очень подвижен. • В протолитической теории кислотами называются вещества, способные отдавать протон другому веществу, а основаниями – вещества, способные принимать протон. • Вещества, способные как присоединять, так и отдавать протоны, на зываются мфолитами (или амфотерными веществами). Примерами а амфолитов могут служить вода, гидрокарбонат ион HCO 3 , гидросульфид ион HS и др. Так, гидрокарбонат ион может отдавать протоны: • HCO 3 = Н+ + CO 32 • или принимать их: • HCO 3 + Н+ = Н 2 СОз = Н 2 О+СО 2↑ • Аналогично в случае гидросульфид иона: • HS = Н+ +S 2 • HS + Н+ = H 2 S
 Амфолитом также является вода, поскольку она может и принимать протон и отдавать его, а также многие продукты ступенчатой диссоциации многоосновных кислот, как, например, НРО 42 , которые могут и присоединять, и отдавать протон. Кислотами, основаниями и амфолитами могут быть незаряженные и заряженные соединения. кислоты основания амфолиты HCl ↔ Н+ + Cl │ CН 3 СОО + Н+ ↔ CН 3 СОО │ H 2 O ↔ Н+ + ОН NH 4+ ↔ Н+ + NH 3 │ NH 3 + Н+ ↔ NH 4+ │ H 2 O + Н+ ↔ H 3 O+ Таким образом, протолитическая теория определяет кислоты и основания по их отношению к протону: кислоты – доноры протона, основания – акцепторы протона. Это позволяет объединить кислоты и основания общим словом протолиты, реакции между протолитами – протолитическими. Обратимые реакции с переносом протона р от кислоты НА к основанию В называют кислотно основными полуреакциями: НА ↔ р + А В + р ↔ ВН+
Амфолитом также является вода, поскольку она может и принимать протон и отдавать его, а также многие продукты ступенчатой диссоциации многоосновных кислот, как, например, НРО 42 , которые могут и присоединять, и отдавать протон. Кислотами, основаниями и амфолитами могут быть незаряженные и заряженные соединения. кислоты основания амфолиты HCl ↔ Н+ + Cl │ CН 3 СОО + Н+ ↔ CН 3 СОО │ H 2 O ↔ Н+ + ОН NH 4+ ↔ Н+ + NH 3 │ NH 3 + Н+ ↔ NH 4+ │ H 2 O + Н+ ↔ H 3 O+ Таким образом, протолитическая теория определяет кислоты и основания по их отношению к протону: кислоты – доноры протона, основания – акцепторы протона. Это позволяет объединить кислоты и основания общим словом протолиты, реакции между протолитами – протолитическими. Обратимые реакции с переносом протона р от кислоты НА к основанию В называют кислотно основными полуреакциями: НА ↔ р + А В + р ↔ ВН+
 • Кислота и получившееся при отдаче протона основание составляют сопряженную пару. В данных уравнениях это НА и А , ВН+ и В. Очевидно, что данные реакции в растворах неосуществимы: кислота может отдать протон только в присутствии акцептора протона. То есть по Бренстеду, кислота проявляет свои свойства и в отсутствие растворителя. Вещество может отдавать протон не только в водной среде, но и в неводных растворителях, в газообразном или твердом состоянии. Реакция между кислотой и основанием согласно протолитической теории, есть «борьба» за протон между двумя основаниями. Для того чтобы кислота могла отдать свой протон, необходимо наличие основания, способного принять его. При этом анион кислоты как частица, присоединяющая протон, также выступает в качестве основания. Все вещества лишь потенциально могут быть кислотами или основаниями, проявить свои кислотные или основные свойства они могут лишь в протолитической реакции, объединяющие полуреакции: НА + В ↔ ВН+ + А • к та 1 осн е 2 к та 2 осн е 1
• Кислота и получившееся при отдаче протона основание составляют сопряженную пару. В данных уравнениях это НА и А , ВН+ и В. Очевидно, что данные реакции в растворах неосуществимы: кислота может отдать протон только в присутствии акцептора протона. То есть по Бренстеду, кислота проявляет свои свойства и в отсутствие растворителя. Вещество может отдавать протон не только в водной среде, но и в неводных растворителях, в газообразном или твердом состоянии. Реакция между кислотой и основанием согласно протолитической теории, есть «борьба» за протон между двумя основаниями. Для того чтобы кислота могла отдать свой протон, необходимо наличие основания, способного принять его. При этом анион кислоты как частица, присоединяющая протон, также выступает в качестве основания. Все вещества лишь потенциально могут быть кислотами или основаниями, проявить свои кислотные или основные свойства они могут лишь в протолитической реакции, объединяющие полуреакции: НА + В ↔ ВН+ + А • к та 1 осн е 2 к та 2 осн е 1
 Вещества переносчики протонов называют протолитами. Рассмотрим, следуя протолитической теории Бренстеда Лоури, процесс обратимого перехода одноосновной кислоты в однокислотное основание в растворе: НВ ↔ Н+ + В (1) кислота основание Здесь НВ и В являются соответственно кислотой и основанием, причем они называются сопряженными кислотой и основанием: НВ кислота, сопряженная с основанием В , В основание, сопряженное с кислотой НВ. для водных растворов уравнение (1) можно представить в виде: НВ + H 2 О ↔ Н 3 О+ + В (2) кислота 1 основание 2 кислота 2 основание 1 В данном случае сопряженными являются: НВ (кислота 1) и В (основание 1), Н 3 О+ (кислота 2) и H 2 О(основание 2). Например: СН 3 СООН ↔ Н+ + СН 3 СОО кислота (уксусная) основание (ацетат ион)
Вещества переносчики протонов называют протолитами. Рассмотрим, следуя протолитической теории Бренстеда Лоури, процесс обратимого перехода одноосновной кислоты в однокислотное основание в растворе: НВ ↔ Н+ + В (1) кислота основание Здесь НВ и В являются соответственно кислотой и основанием, причем они называются сопряженными кислотой и основанием: НВ кислота, сопряженная с основанием В , В основание, сопряженное с кислотой НВ. для водных растворов уравнение (1) можно представить в виде: НВ + H 2 О ↔ Н 3 О+ + В (2) кислота 1 основание 2 кислота 2 основание 1 В данном случае сопряженными являются: НВ (кислота 1) и В (основание 1), Н 3 О+ (кислота 2) и H 2 О(основание 2). Например: СН 3 СООН ↔ Н+ + СН 3 СОО кислота (уксусная) основание (ацетат ион)
 NН 3 + Н+ ↔ NН 4+ основание (аммиак) кислота (ион аммония) HS + Н+ ↔ Н 2 S основание (гидросульфид ион) кислота (сероводородная) Согласно теории Бренстеда Лоури кислоты и основания находятся в протолическом равновесии. Протолитическое равновесие в широком смысле слова равнове сие, в котором участвует протон ион водорода Н+. В узком смысле слова протолитическuми (в отличие от прототропных) называют реак ции, в которых участвуют молекулы воды, отдающие или принимающие протоны: Н 2 О=Н+ +ОН Н 2 О+Н+ = НЗО+ В самой жидкой воде устанавливается протолитическое равновесие: Н 2 О+Н 2 О= НЗО+ +ОН ,
NН 3 + Н+ ↔ NН 4+ основание (аммиак) кислота (ион аммония) HS + Н+ ↔ Н 2 S основание (гидросульфид ион) кислота (сероводородная) Согласно теории Бренстеда Лоури кислоты и основания находятся в протолическом равновесии. Протолитическое равновесие в широком смысле слова равнове сие, в котором участвует протон ион водорода Н+. В узком смысле слова протолитическuми (в отличие от прототропных) называют реак ции, в которых участвуют молекулы воды, отдающие или принимающие протоны: Н 2 О=Н+ +ОН Н 2 О+Н+ = НЗО+ В самой жидкой воде устанавливается протолитическое равновесие: Н 2 О+Н 2 О= НЗО+ +ОН ,
 Прототропными называют такие реакции, в которых переносчиками протонов служат не молекулы воды, а частицы других веществ. Так, например, в реакции между молекулами пиридина и хлороводорода C 5 H 5 N + HCl = C 5 H 5 NН+ + Cl ион водорода переносится от молекулы хлороводорода к молекуле пиридина без участия молекул воды. Под протолитическими реакциями и равновесuями понимают любые реакции и равновесия с участием протонов. • Реакциями протолuза будем называть реакции кислот или основа ний с растворителем с участием протонов.
Прототропными называют такие реакции, в которых переносчиками протонов служат не молекулы воды, а частицы других веществ. Так, например, в реакции между молекулами пиридина и хлороводорода C 5 H 5 N + HCl = C 5 H 5 NН+ + Cl ион водорода переносится от молекулы хлороводорода к молекуле пиридина без участия молекул воды. Под протолитическими реакциями и равновесuями понимают любые реакции и равновесия с участием протонов. • Реакциями протолuза будем называть реакции кислот или основа ний с растворителем с участием протонов.
 3. ПРОТОЛИТИЧЕСКИЕ РАВНОВЕСИЯ В ВОДЕ При взаимодействии кислоты и основания образуются новые кислота и основание – «нейтрализации» в смысле исчезновения кислоты и основания нет. Одним из компонентов протолитической реакции может быть растворитель НS, способный принимать или отдавать протон: HА + HS ↔ SH 2+ + А Здесь SH – растворитель, проявляющий свойства основания (акцептор протонов). Реакция диссоциации основания имеет вид: В + HS ↔ S + ВН+ Здесь растворитель проявляет свойства донора протонов, т. е. кислоты. Данные реакции есть не что иное, как реакции диссоциации кислот и оснований в теории Аррениуса. Вещества НА и В могут быть заряженными и незаряженными. Например, в воде: HNO 2 + H 2 O ↔ H 3 O+ + NO 2 NH 4+ + H 2 O ↔ H 3 O+ + NH 3 + H 2 O ↔ ОН + NH 4+ СН 3 СОО + H 2 O ↔ ОН + СН 3 СООН
3. ПРОТОЛИТИЧЕСКИЕ РАВНОВЕСИЯ В ВОДЕ При взаимодействии кислоты и основания образуются новые кислота и основание – «нейтрализации» в смысле исчезновения кислоты и основания нет. Одним из компонентов протолитической реакции может быть растворитель НS, способный принимать или отдавать протон: HА + HS ↔ SH 2+ + А Здесь SH – растворитель, проявляющий свойства основания (акцептор протонов). Реакция диссоциации основания имеет вид: В + HS ↔ S + ВН+ Здесь растворитель проявляет свойства донора протонов, т. е. кислоты. Данные реакции есть не что иное, как реакции диссоциации кислот и оснований в теории Аррениуса. Вещества НА и В могут быть заряженными и незаряженными. Например, в воде: HNO 2 + H 2 O ↔ H 3 O+ + NO 2 NH 4+ + H 2 O ↔ H 3 O+ + NH 3 + H 2 O ↔ ОН + NH 4+ СН 3 СОО + H 2 O ↔ ОН + СН 3 СООН
 С позиций теории Аррениуса взаимодействие заряженных частиц (NH 4+ и СН 3 СОО ) с водой есть не что иное, как гидролиз солей. Способность кислоты отдавать протон, а основания принимать его можно охарактеризовать константами равновесия, которые называют соответственно константой кислотности Ка и константой основности Кb . Принимая во внимание постоянство активности растворителя, получаем константу взаимодействия кислоты НА с растворителем HS: a. SH 2+ a. А К а. НА, SH = , a. HА которую называют константой диссоциации кислоты НА или константой кислотности. Константу равновесия реакции взаимодействия основания В с растворителем HS: a. ВH+ a. S К b. В, SH = , a. В называют константой диссоциации основания или константой основности. Очевидно, что К а. НА, SH и К b. В, SH являются произведением двух гипотетических констант – «собственной» константы диссоциации кислоты НА или основания В и константы диссоциации растворителя HS по основному или кислотному типу соответственно: К а. НА, SH = К а. НА К b SH К b. В, SH = К b. В К а SH
С позиций теории Аррениуса взаимодействие заряженных частиц (NH 4+ и СН 3 СОО ) с водой есть не что иное, как гидролиз солей. Способность кислоты отдавать протон, а основания принимать его можно охарактеризовать константами равновесия, которые называют соответственно константой кислотности Ка и константой основности Кb . Принимая во внимание постоянство активности растворителя, получаем константу взаимодействия кислоты НА с растворителем HS: a. SH 2+ a. А К а. НА, SH = , a. HА которую называют константой диссоциации кислоты НА или константой кислотности. Константу равновесия реакции взаимодействия основания В с растворителем HS: a. ВH+ a. S К b. В, SH = , a. В называют константой диссоциации основания или константой основности. Очевидно, что К а. НА, SH и К b. В, SH являются произведением двух гипотетических констант – «собственной» константы диссоциации кислоты НА или основания В и константы диссоциации растворителя HS по основному или кислотному типу соответственно: К а. НА, SH = К а. НА К b SH К b. В, SH = К b. В К а SH
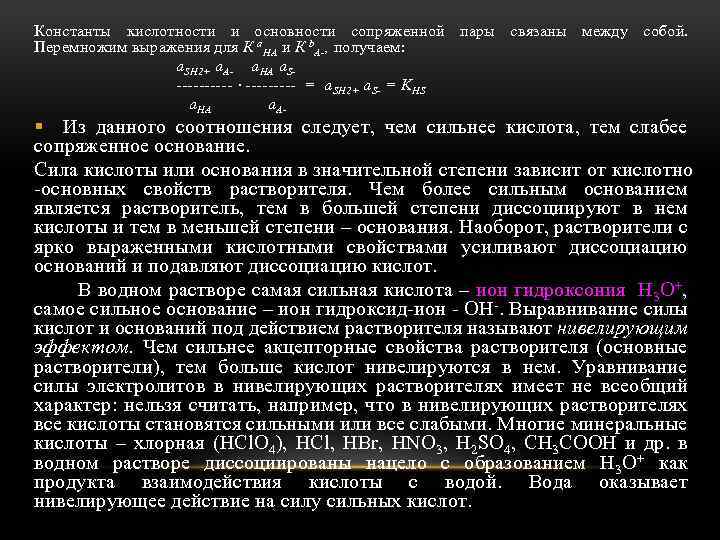 Константы кислотности и основности сопряженной пары связаны между собой. Перемножим выражения для К а. НА и К b. А , получаем: a. SH 2+ a. А a. HА a. S · = a. SH 2+ a. S = KНS a. HА a. А § Из данного соотношения следует, чем сильнее кислота, тем слабее сопряженное основание. Сила кислоты или основания в значительной степени зависит от кислотно основных свойств растворителя. Чем более сильным основанием является растворитель, тем в большей степени диссоциируют в нем кислоты и тем в меньшей степени – основания. Наоборот, растворители с ярко выраженными кислотными свойствами усиливают диссоциацию оснований и подавляют диссоциацию кислот. В водном растворе самая сильная кислота – ион гидроксония H 3 O+, самое сильное основание – ион гидроксид ион ОН. Выравнивание силы кислот и оснований под действием растворителя называют нивелирующим эффектом. Чем сильнее акцепторные свойства растворителя (основные растворители), тем больше кислот нивелируются в нем. Уравнивание силы электролитов в нивелирующих растворителях имеет не всеобщий характер: нельзя считать, например, что в нивелирующих растворителях все кислоты становятся сильными или все слабыми. Многие минеральные кислоты – хлорная (HCl. O 4), HCl, HBr, HNO 3, H 2 SO 4, CH 3 COOH и др. в водном растворе диссоциированы нацело с образованием H 3 O+ как продукта взаимодействия кислоты с водой. Вода оказывает нивелирующее действие на силу сильных кислот.
Константы кислотности и основности сопряженной пары связаны между собой. Перемножим выражения для К а. НА и К b. А , получаем: a. SH 2+ a. А a. HА a. S · = a. SH 2+ a. S = KНS a. HА a. А § Из данного соотношения следует, чем сильнее кислота, тем слабее сопряженное основание. Сила кислоты или основания в значительной степени зависит от кислотно основных свойств растворителя. Чем более сильным основанием является растворитель, тем в большей степени диссоциируют в нем кислоты и тем в меньшей степени – основания. Наоборот, растворители с ярко выраженными кислотными свойствами усиливают диссоциацию оснований и подавляют диссоциацию кислот. В водном растворе самая сильная кислота – ион гидроксония H 3 O+, самое сильное основание – ион гидроксид ион ОН. Выравнивание силы кислот и оснований под действием растворителя называют нивелирующим эффектом. Чем сильнее акцепторные свойства растворителя (основные растворители), тем больше кислот нивелируются в нем. Уравнивание силы электролитов в нивелирующих растворителях имеет не всеобщий характер: нельзя считать, например, что в нивелирующих растворителях все кислоты становятся сильными или все слабыми. Многие минеральные кислоты – хлорная (HCl. O 4), HCl, HBr, HNO 3, H 2 SO 4, CH 3 COOH и др. в водном растворе диссоциированы нацело с образованием H 3 O+ как продукта взаимодействия кислоты с водой. Вода оказывает нивелирующее действие на силу сильных кислот.
 Согласно современным представлениям в жидкой воде осуществля ется протолитическое равновесие автопротолиз воды: H 2 O + H 2 O = H 3 O+ + ОН (3) или упрощенно для краткости записи H 2 O = H+ + ОН По некоторым данным в равновесии с ионами гидpоксония Нз. О+ в жидкой воде могут находиться также ионы Нз. О+ · Н 2 О, Нз. О+ · 2 Н 2 О, однако их равновесная концентрация, по видимому, невелика. Вода слабый электролит, поэтому за константу химического рав новесия (3) можно приближенно принять концентрационную константу химического равновесия Кс выраженную через равновесные концентра ции участников реакции: [Н 3 О+][ОН ] Кс = [Н 2 О]2 и далее: Кс[Н 2 О]2 = [Н 3 О+][ОН ]
Согласно современным представлениям в жидкой воде осуществля ется протолитическое равновесие автопротолиз воды: H 2 O + H 2 O = H 3 O+ + ОН (3) или упрощенно для краткости записи H 2 O = H+ + ОН По некоторым данным в равновесии с ионами гидpоксония Нз. О+ в жидкой воде могут находиться также ионы Нз. О+ · Н 2 О, Нз. О+ · 2 Н 2 О, однако их равновесная концентрация, по видимому, невелика. Вода слабый электролит, поэтому за константу химического рав новесия (3) можно приближенно принять концентрационную константу химического равновесия Кс выраженную через равновесные концентра ции участников реакции: [Н 3 О+][ОН ] Кс = [Н 2 О]2 и далее: Кс[Н 2 О]2 = [Н 3 О+][ОН ]
 При постоянной температуре Т = const константа химического равнове сия постоянна: Кс = const. Концентрация воды в чистой воде также посто янна равнa и 55, 55 моль/л, т. е. [Н 2 О]2 = 55, 552 = const. Произведение Кс[Н 2 О] двух постоянных величин также постоянная величина, кото рую обозначим символом w: K Кс[Н 2 О]2 = const = Kw. Тогда для автопротолиза воды имеем: Kw = [Н 3 О+][ОН ] (4) или упрощенно: Kw = [Н+][ОН ] Величина Kw, называется константа автопротолиза воды или ион ноепроизведение воды. Она постоянна при постоянной температуре. При комнатной температуре (25 ос = 298, 15 К) числовое значение Kw равно Kw = 1, 008· 10 14 ≈ 10 14. Так как числовые значения Kw очень маленькие, то вместо них при нято использовать отрицательный десятичный логарифм ( «силовой пока затель» ) величины Kw. При комнатной температуре p. Kw = lg. Кw = lg. I 0 14 = 14 (5)
При постоянной температуре Т = const константа химического равнове сия постоянна: Кс = const. Концентрация воды в чистой воде также посто янна равнa и 55, 55 моль/л, т. е. [Н 2 О]2 = 55, 552 = const. Произведение Кс[Н 2 О] двух постоянных величин также постоянная величина, кото рую обозначим символом w: K Кс[Н 2 О]2 = const = Kw. Тогда для автопротолиза воды имеем: Kw = [Н 3 О+][ОН ] (4) или упрощенно: Kw = [Н+][ОН ] Величина Kw, называется константа автопротолиза воды или ион ноепроизведение воды. Она постоянна при постоянной температуре. При комнатной температуре (25 ос = 298, 15 К) числовое значение Kw равно Kw = 1, 008· 10 14 ≈ 10 14. Так как числовые значения Kw очень маленькие, то вместо них при нято использовать отрицательный десятичный логарифм ( «силовой пока затель» ) величины Kw. При комнатной температуре p. Kw = lg. Кw = lg. I 0 14 = 14 (5)
 Поскольку в соответствии с формулой (3) в чистой жидкой воде кон центрации ионов водорода и ионов гидроксила одинаковы [Н 3 О+] = [ОН ], то при комнатной температуре, учитывая (4), (5) и то, что Kw = 10 14, имеем для чистой жидкой воды: [Нз. О+] = [ОН ] = 10 7, p. H= lg[Н+]= lg. I 0 7 =7, (6) р. ОН = lg [ОН ] = lg. I 0 7 = 7, p. Kw = р. Н + р. ОН = 14. Таким образом, при комнатной температуре: в кислых водных растворах р. Н < 7, в нейтральных водных растворах р. Н = 7, в щелочных водных растворах р. Н > 7. В соотношениях (4), (5), (6) фигурируют равновесные концен трации ионов водорода и гидроксильных групп. Более строгими являются соотношения, выраженные через равновесные активности ионов: р. Н = lgа(Н 3 О+), р. ОН= lgа(ОН ), Kw = а(Н 3 О+ )а(ОН ) или упрощенно Kw = a(H+)a(OH ) (7) Для сильно разбавленных кислых и щелочных растворов результаты расчетов по формулам (4), (5), (6), с одной стороны, и по формулам (7), с другой стороны,
Поскольку в соответствии с формулой (3) в чистой жидкой воде кон центрации ионов водорода и ионов гидроксила одинаковы [Н 3 О+] = [ОН ], то при комнатной температуре, учитывая (4), (5) и то, что Kw = 10 14, имеем для чистой жидкой воды: [Нз. О+] = [ОН ] = 10 7, p. H= lg[Н+]= lg. I 0 7 =7, (6) р. ОН = lg [ОН ] = lg. I 0 7 = 7, p. Kw = р. Н + р. ОН = 14. Таким образом, при комнатной температуре: в кислых водных растворах р. Н < 7, в нейтральных водных растворах р. Н = 7, в щелочных водных растворах р. Н > 7. В соотношениях (4), (5), (6) фигурируют равновесные концен трации ионов водорода и гидроксильных групп. Более строгими являются соотношения, выраженные через равновесные активности ионов: р. Н = lgа(Н 3 О+), р. ОН= lgа(ОН ), Kw = а(Н 3 О+ )а(ОН ) или упрощенно Kw = a(H+)a(OH ) (7) Для сильно разбавленных кислых и щелочных растворов результаты расчетов по формулам (4), (5), (6), с одной стороны, и по формулам (7), с другой стороны,
 КОНСТАНТЫ КИСЛОТНОСТИ, ОСНОВНОСТИ И ИХ ПОКАЗАТЕЛИ Слабые кислоты и основания, будучи слабыми электролитами, в водных растворах распадаются на ионы лишь в незначительной меpe (степень диссоциации на ионы а « 1). В их растворах устанавливается равновесие между ионами и непродиссоциированными молекулами. Рассмотрим, например, равновесие в водном растворе слабого элек тролита уксусной кислоты СН 3 СООН: СН 3 СООН +Н 2 О = НЗО+ + СН 3 СОО Запишем выражение для константы К этого химического равновесия: а(Н 3 О+)а(СН 3 СОО ) К = а(СН 3 СООН)а(Н 2 О) гдe все активности равновесные. Преобразуем это выражение, учиты вая, что активность воды а(Н 2 О) = const: а(Н 3 О+)а(СН 3 СОО ) Ка(Н 2 О) = = Ка = const при Т = const а(СН 3 СООН) где Ка истинная термодинамическая константа химического равнове сия, выраженная через равновесные активности участников реакции.
КОНСТАНТЫ КИСЛОТНОСТИ, ОСНОВНОСТИ И ИХ ПОКАЗАТЕЛИ Слабые кислоты и основания, будучи слабыми электролитами, в водных растворах распадаются на ионы лишь в незначительной меpe (степень диссоциации на ионы а « 1). В их растворах устанавливается равновесие между ионами и непродиссоциированными молекулами. Рассмотрим, например, равновесие в водном растворе слабого элек тролита уксусной кислоты СН 3 СООН: СН 3 СООН +Н 2 О = НЗО+ + СН 3 СОО Запишем выражение для константы К этого химического равновесия: а(Н 3 О+)а(СН 3 СОО ) К = а(СН 3 СООН)а(Н 2 О) гдe все активности равновесные. Преобразуем это выражение, учиты вая, что активность воды а(Н 2 О) = const: а(Н 3 О+)а(СН 3 СОО ) Ка(Н 2 О) = = Ка = const при Т = const а(СН 3 СООН) где Ка истинная термодинамическая константа химического равнове сия, выраженная через равновесные активности участников реакции.
 Поскольку для слабых электролитов степень диссоциации на ионы а « 1, то коэффициенты активности близки к единице и поэтому [Н 3 О+][СН 3 СОО ] Ка ≈ Кс = [СН 3 СООН] где все концентрации равновесны. Таким образом, равновесие, устанавливающееся при диссоциации уксусной кислоты в воде, характеризуется константой равновесия Кс, которую можно назвать константой диссоциации (ионизации) уксусной кислоты или константой кислотности уксусной кислоты.
Поскольку для слабых электролитов степень диссоциации на ионы а « 1, то коэффициенты активности близки к единице и поэтому [Н 3 О+][СН 3 СОО ] Ка ≈ Кс = [СН 3 СООН] где все концентрации равновесны. Таким образом, равновесие, устанавливающееся при диссоциации уксусной кислоты в воде, характеризуется константой равновесия Кс, которую можно назвать константой диссоциации (ионизации) уксусной кислоты или константой кислотности уксусной кислоты.
 5. КЛАССИФИКАЦИЯ И СВОЙСТВА РАСТВОРИТЕЛЕЙ. Из всего многообразия свойств жидкостей с точки зрения аналитика наибольшее значение имеют донорно–акцепторная способность по отношению к протону и диэлектрическая проницаемость. По этому признаку растворители делятся на апротонные и протолитические. Молекулы апротонных растворителей неспособны к отщеплению протонов или к их присоединению, они не ионизированы. Растворенные в апротонных растворителях кислоты и основания также неспособны к диссоциации. Примером апротонных растворителей служит бензол или CCl 4 и т. п. Молекулы протолитических растворителей могут присоединять или отщеплять протоны. Они в свою очередь делятся на группы: протофильные (основные) растворители, склонные к присоединению протона (пиридин и другие амины); протогенные (кислые) растворители, молекулы которых мало склонны к присоединению протонов, но легко их отщепляют (например, HF, безводные H 2 SO 4, СН 3 СООН); амфипротные, способные присоединять и отдавать протон (вода, жидкий аммиак, спирты, карбоновые кислоты и др. ).
5. КЛАССИФИКАЦИЯ И СВОЙСТВА РАСТВОРИТЕЛЕЙ. Из всего многообразия свойств жидкостей с точки зрения аналитика наибольшее значение имеют донорно–акцепторная способность по отношению к протону и диэлектрическая проницаемость. По этому признаку растворители делятся на апротонные и протолитические. Молекулы апротонных растворителей неспособны к отщеплению протонов или к их присоединению, они не ионизированы. Растворенные в апротонных растворителях кислоты и основания также неспособны к диссоциации. Примером апротонных растворителей служит бензол или CCl 4 и т. п. Молекулы протолитических растворителей могут присоединять или отщеплять протоны. Они в свою очередь делятся на группы: протофильные (основные) растворители, склонные к присоединению протона (пиридин и другие амины); протогенные (кислые) растворители, молекулы которых мало склонны к присоединению протонов, но легко их отщепляют (например, HF, безводные H 2 SO 4, СН 3 СООН); амфипротные, способные присоединять и отдавать протон (вода, жидкий аммиак, спирты, карбоновые кислоты и др. ).
 Амфипротные растворители способны к переносу протона от одной молекулы растворителя к другой. Если обозначить протоносодержащий растворитель HS, то реакцию автопротолиза можно записать: HS + HS ↔ SH 2+ + S В результате получаются ионы лиония SH 2+ и лиата S. C 2 Н 5 ОН + C 2 Н 5 ОН ↔ C 2 Н 5 ОН 2+ + C 2 Н 5 О этилоний этилат CН 3 ОН + CН 3 ОН ↔ CН 3 ОН 2+ + CН 3 О метилоний метилат Константы этих и подобных равновесий называются константами автопротолиза KSН = a SH 2+ a S Так же как и константы диссоциации, они зависят от температуры и ионной силы. Для аналитической химии важна классификация растворителей по их способности дифференцировать или нивелировать силу кислот и оснований. По этому критерию все растворители делят на две группы.
Амфипротные растворители способны к переносу протона от одной молекулы растворителя к другой. Если обозначить протоносодержащий растворитель HS, то реакцию автопротолиза можно записать: HS + HS ↔ SH 2+ + S В результате получаются ионы лиония SH 2+ и лиата S. C 2 Н 5 ОН + C 2 Н 5 ОН ↔ C 2 Н 5 ОН 2+ + C 2 Н 5 О этилоний этилат CН 3 ОН + CН 3 ОН ↔ CН 3 ОН 2+ + CН 3 О метилоний метилат Константы этих и подобных равновесий называются константами автопротолиза KSН = a SH 2+ a S Так же как и константы диссоциации, они зависят от температуры и ионной силы. Для аналитической химии важна классификация растворителей по их способности дифференцировать или нивелировать силу кислот и оснований. По этому критерию все растворители делят на две группы.
 • Нивелирующие растворители – это растворители, в которых сохраняется соотношение в силе кислот или оснований, характерное для водных растворов этих электролитов. К нивелирующим растворителям относят в первую очередь химические соединения, содержащие гидроксильные группы, например спирты, фенолы и др. • Чем сильнее донорные свойства растворителя (кислотные растворители), тем больше оснований нивелируются в нем, так многие основания – Na. OH, NH 3, Na. C 2 H 5 O в водном растворе диссоциируют до ОН. В амфипротных (амфотерных) растворителях нивелируются и кислоты и основания. В протофильных растворителях основания нивелироваться не могут. В инертных апротонных растворителях нивелирования вообще не наблюдается. В результате нивелирования константа равновесия теряет смысл, поскольку нет молекул исходной кислоты или основания. • Дифференцирующие растворители – это растворители, в которых проявляется значительное различие в силе кислот и оснований.
• Нивелирующие растворители – это растворители, в которых сохраняется соотношение в силе кислот или оснований, характерное для водных растворов этих электролитов. К нивелирующим растворителям относят в первую очередь химические соединения, содержащие гидроксильные группы, например спирты, фенолы и др. • Чем сильнее донорные свойства растворителя (кислотные растворители), тем больше оснований нивелируются в нем, так многие основания – Na. OH, NH 3, Na. C 2 H 5 O в водном растворе диссоциируют до ОН. В амфипротных (амфотерных) растворителях нивелируются и кислоты и основания. В протофильных растворителях основания нивелироваться не могут. В инертных апротонных растворителях нивелирования вообще не наблюдается. В результате нивелирования константа равновесия теряет смысл, поскольку нет молекул исходной кислоты или основания. • Дифференцирующие растворители – это растворители, в которых проявляется значительное различие в силе кислот и оснований.
 • Сильные кислоты в более кислотных растворителях труднее отдают протон и могут проявлять свою собственную природу, как и основания в более основных растворителях. Такой эффект называется дифференцирующим. В дифференцирующих растворителях проявляются значительные различия в силе кислот, оснований и других электролитов. Многие кислоты и основания, полностью диссоциированные в водном растворе, существенно различаются по силе в дифференцирующих растворителях. Например, дифференцирующим эффектом по отношению к сильным кислотам обладает безводная уксусная кислота (слабый акцептор протона). • Благодаря дифференцирующему эффекту удалось определить константы диссоциации сильных кислот в других растворителях. Это позволило расположить кислоты по донорной способности в ряд: • HCl. O 4 > НI > HBr > HCl > H 2 SO 4 > HNO 3 > H 3 O+
• Сильные кислоты в более кислотных растворителях труднее отдают протон и могут проявлять свою собственную природу, как и основания в более основных растворителях. Такой эффект называется дифференцирующим. В дифференцирующих растворителях проявляются значительные различия в силе кислот, оснований и других электролитов. Многие кислоты и основания, полностью диссоциированные в водном растворе, существенно различаются по силе в дифференцирующих растворителях. Например, дифференцирующим эффектом по отношению к сильным кислотам обладает безводная уксусная кислота (слабый акцептор протона). • Благодаря дифференцирующему эффекту удалось определить константы диссоциации сильных кислот в других растворителях. Это позволило расположить кислоты по донорной способности в ряд: • HCl. O 4 > НI > HBr > HCl > H 2 SO 4 > HNO 3 > H 3 O+
 • Нивелирование кислот и оснований обуславливает ограниченность интервала кислотности в каждом растворителе, поскольку в растворе не может быть кислоты сильнее, чем лионий, и основания сильнее, чем лиат. Если выразить кислотность в единицах р. Н, то интервал кислотности должен быть равен р. КSН автопротолиза растворителя. Показатель константы автопротолиза р. КSН = lg. КSН непосредственно показывает протяженность шкалы кислотности в данном растворителе. Для водных растворов этот интервал составляет 14 единиц р. Н, для этанольных растворов 19 единиц р. Н, для уксусных растворов – 12, 22 единицы р. Н, для растворов в жидком аммиаке – 33 единицы р. Н и т. д.
• Нивелирование кислот и оснований обуславливает ограниченность интервала кислотности в каждом растворителе, поскольку в растворе не может быть кислоты сильнее, чем лионий, и основания сильнее, чем лиат. Если выразить кислотность в единицах р. Н, то интервал кислотности должен быть равен р. КSН автопротолиза растворителя. Показатель константы автопротолиза р. КSН = lg. КSН непосредственно показывает протяженность шкалы кислотности в данном растворителе. Для водных растворов этот интервал составляет 14 единиц р. Н, для этанольных растворов 19 единиц р. Н, для уксусных растворов – 12, 22 единицы р. Н, для растворов в жидком аммиаке – 33 единицы р. Н и т. д.
 ХАРАКТЕРИСТИКА СИЛЫ СЛАБЫХ КИСЛОТ И ОСНОВАНИЯ. Для кислот характерны следующие общие свойства: а) способность взаимодействовать с основаниями с образованием солей; б) способность взаимодействовать с некоторыми металлами с выделением водорода; в) способность изменять цвет индикаторов, в частности, вызывать красную окраску лакмуса; г) кислый вкус. Водные растворы оснований обладают следующими общими свойствами: а) способностью взаимодействовать с кислотами с образованием солей; б) способностью изменять цвет индикаторов иначе, чем для кислот (например, они вызывают синюю окраску лакмуса); в) своеобразным мыльным вкусом. Основные свойства гидроксидов одного и того же элемента усиливаются с уменьшением валентности элемента. Так, основные свойства дигидроксида железа Fe(OH)2 выражены сильнее, чем у тригидроксида Fe(OH)3. Это утверждение равносильно тому, что кислотные свойства Fe(OH)3 проявляются сильнее, чем у Fe(OH)2.
ХАРАКТЕРИСТИКА СИЛЫ СЛАБЫХ КИСЛОТ И ОСНОВАНИЯ. Для кислот характерны следующие общие свойства: а) способность взаимодействовать с основаниями с образованием солей; б) способность взаимодействовать с некоторыми металлами с выделением водорода; в) способность изменять цвет индикаторов, в частности, вызывать красную окраску лакмуса; г) кислый вкус. Водные растворы оснований обладают следующими общими свойствами: а) способностью взаимодействовать с кислотами с образованием солей; б) способностью изменять цвет индикаторов иначе, чем для кислот (например, они вызывают синюю окраску лакмуса); в) своеобразным мыльным вкусом. Основные свойства гидроксидов одного и того же элемента усиливаются с уменьшением валентности элемента. Так, основные свойства дигидроксида железа Fe(OH)2 выражены сильнее, чем у тригидроксида Fe(OH)3. Это утверждение равносильно тому, что кислотные свойства Fe(OH)3 проявляются сильнее, чем у Fe(OH)2.
 НАСКОЛЬКО ЛЕГКО КИСЛОТА ОТДАЕТ ПРОТОНЫ МОЛЕКУЛАМ ДАННОГО РАСТВОРИТЕЛЯ. 1. Действие растворов кислот на индикаторы. Практически все кислоты (кроме кремниевой) хорошо растворимы в воде. Растворы кислот в воде изменяют окраску специальных веществ - индикаторов. По окраске индикаторов определяют присутствие кислоты. Индикатор лакмус окрашивается растворами кислот в красный цвет, индикатор метиловый оранжевый - тоже в красный цвет. 2. Взаимодействие кислот с основаниями. Эта реакция, как вы уже знаете, называется реакцией нейтрализации. Кислота реагируют с основанием с образованием соли, в которой всегда в неизменном виде обнаруживается кислотный остаток. Вторым продуктом реакции нейтрализации обязательно является вода. Например: H 2 SO 4 + Ca(OH)2 = Ca. SO 4 + 2 H 2 O Для реакций нейтрализации достаточно, чтобы хотя бы одно из реагирующих веществ было растворимо в воде. Поскольку практически все кислоты растворимы в воде, они вступают в реакции нейтрализации не только с растворимыми, но и с нерастворимыми основаниями. Исключением является кремниевая кислота, которая плохо растворима в воде и поэтому может реагировать только с растворимыми основаниями - такими как Na. OH и KOH: H 2 Si. O 3 + 2 Na. OH = Na 2 Si. O 3 + 2 H 2 O 3. Взаимодействие кислот с основными оксидами. Поскольку основные оксиды - ближайшие родственники оснований - с ними кислоты также вступают в реакции нейтрализации: 2 HCl + Ca. O = Ca. Cl 2 + H 2 O Как и в случае реакций с основаниями, с основными оксидами кислоты образуют соль и воду. Соль содержит кислотный остаток той кислоты, которая использовалась в реакции нейтрализации. Например, фосфорную кислоту используют для очистки железа от ржавчины (оксидов железа). Фосфорная кислота, убирая с поверхности металла его оксид, с самим железом реагирует очень медленно. Оксид железа превращается в растворимую соль Fe. PO 4, которую смывают водой вместе с остатками кислоты. 4. Взаимодействие кислот с металлами. Для взаимодействия кислот с металлом должны выполняться некоторые условия (в отличие от реакций кислот с основаниями и основными оксидами, которые идут практически всегда).
НАСКОЛЬКО ЛЕГКО КИСЛОТА ОТДАЕТ ПРОТОНЫ МОЛЕКУЛАМ ДАННОГО РАСТВОРИТЕЛЯ. 1. Действие растворов кислот на индикаторы. Практически все кислоты (кроме кремниевой) хорошо растворимы в воде. Растворы кислот в воде изменяют окраску специальных веществ - индикаторов. По окраске индикаторов определяют присутствие кислоты. Индикатор лакмус окрашивается растворами кислот в красный цвет, индикатор метиловый оранжевый - тоже в красный цвет. 2. Взаимодействие кислот с основаниями. Эта реакция, как вы уже знаете, называется реакцией нейтрализации. Кислота реагируют с основанием с образованием соли, в которой всегда в неизменном виде обнаруживается кислотный остаток. Вторым продуктом реакции нейтрализации обязательно является вода. Например: H 2 SO 4 + Ca(OH)2 = Ca. SO 4 + 2 H 2 O Для реакций нейтрализации достаточно, чтобы хотя бы одно из реагирующих веществ было растворимо в воде. Поскольку практически все кислоты растворимы в воде, они вступают в реакции нейтрализации не только с растворимыми, но и с нерастворимыми основаниями. Исключением является кремниевая кислота, которая плохо растворима в воде и поэтому может реагировать только с растворимыми основаниями - такими как Na. OH и KOH: H 2 Si. O 3 + 2 Na. OH = Na 2 Si. O 3 + 2 H 2 O 3. Взаимодействие кислот с основными оксидами. Поскольку основные оксиды - ближайшие родственники оснований - с ними кислоты также вступают в реакции нейтрализации: 2 HCl + Ca. O = Ca. Cl 2 + H 2 O Как и в случае реакций с основаниями, с основными оксидами кислоты образуют соль и воду. Соль содержит кислотный остаток той кислоты, которая использовалась в реакции нейтрализации. Например, фосфорную кислоту используют для очистки железа от ржавчины (оксидов железа). Фосфорная кислота, убирая с поверхности металла его оксид, с самим железом реагирует очень медленно. Оксид железа превращается в растворимую соль Fe. PO 4, которую смывают водой вместе с остатками кислоты. 4. Взаимодействие кислот с металлами. Для взаимодействия кислот с металлом должны выполняться некоторые условия (в отличие от реакций кислот с основаниями и основными оксидами, которые идут практически всегда).
 СВЯЗЫВАЕТ ОТ МОЛЕКУЛ ДАННОГО РАСТВОРИТЕЛЯ. Основания - это нейтральные молекулы или ионы, способные присоединять протон. Существует также основание, в котором гидрокси-группа присоединена не к металлу, а к иону NH 4+ (катиону аммония). Это основание называется гидроксидом аммония и имеет формулу NH 4 OH. Гидроксид аммония образуется в рекции присоединения воды к аммиаку, когда аммиак растворяют в воде: NH 3 + H 2 O = NH 4 OH (гидроксид аммония). Основания бывают растворимыми и нерастворимыми. Растворимые основания называются щелочами. Растворы щелочей скользкие на ощупь ("мыльные") и довольно едкие. Они разъедают кожу, ткани, бумагу, очень опасны (как и кислоты) при попадании в глаза. Поэтому при работе со щелочами и кислотами необходимо пользоваться защитными очками. Если раствор щелочи все-таки попал в лицо, необходимо промыть глаза большим количеством воды, а затем разбавленным раствором слабой кислоты (например, уксусной). Этот способ медицинской помощи основан на уже известной нам реакции нейтрализации. Na. OH + уксусная кислота (разб. ) = соль + вода Лишь небольшую часть всех оснований называют щелочами. Это, например, KOH – гидроксид калия (едкое кали), Na. OH – гидроксид натрия, Li. OH – гидроксид лития, Ca(OH)2 – гидроксид кальция (его раствор называется известковой водой), Ba(OH)2 – гидроксид бария. Большинство других оснований в воде нерастворимы и щелочами их не называют.
СВЯЗЫВАЕТ ОТ МОЛЕКУЛ ДАННОГО РАСТВОРИТЕЛЯ. Основания - это нейтральные молекулы или ионы, способные присоединять протон. Существует также основание, в котором гидрокси-группа присоединена не к металлу, а к иону NH 4+ (катиону аммония). Это основание называется гидроксидом аммония и имеет формулу NH 4 OH. Гидроксид аммония образуется в рекции присоединения воды к аммиаку, когда аммиак растворяют в воде: NH 3 + H 2 O = NH 4 OH (гидроксид аммония). Основания бывают растворимыми и нерастворимыми. Растворимые основания называются щелочами. Растворы щелочей скользкие на ощупь ("мыльные") и довольно едкие. Они разъедают кожу, ткани, бумагу, очень опасны (как и кислоты) при попадании в глаза. Поэтому при работе со щелочами и кислотами необходимо пользоваться защитными очками. Если раствор щелочи все-таки попал в лицо, необходимо промыть глаза большим количеством воды, а затем разбавленным раствором слабой кислоты (например, уксусной). Этот способ медицинской помощи основан на уже известной нам реакции нейтрализации. Na. OH + уксусная кислота (разб. ) = соль + вода Лишь небольшую часть всех оснований называют щелочами. Это, например, KOH – гидроксид калия (едкое кали), Na. OH – гидроксид натрия, Li. OH – гидроксид лития, Ca(OH)2 – гидроксид кальция (его раствор называется известковой водой), Ba(OH)2 – гидроксид бария. Большинство других оснований в воде нерастворимы и щелочами их не называют.
 КЛАССИФИКАЦИЯ КИСЛОТ И ОСНОВАНИЙ. Классификация кислот. 1. Нейтральные кислоты. 2. Катионные кислоты. 3. Анионные кислоты. Классификация оснований. 1. Нейтральные основания. 2. Анионные основания. 3. Катионные основания: продукты неполного протонирования оснований.
КЛАССИФИКАЦИЯ КИСЛОТ И ОСНОВАНИЙ. Классификация кислот. 1. Нейтральные кислоты. 2. Катионные кислоты. 3. Анионные кислоты. Классификация оснований. 1. Нейтральные основания. 2. Анионные основания. 3. Катионные основания: продукты неполного протонирования оснований.
 РАСТВОР СИЛЬНОЙ КИСЛОТЫ Пусть HA - сильная одноосновная кислота, тогда в растворе существуют следующие равновесия: [indent]HA + H 2 O → H 3 O+ + A 2 H 2 O ↔ H 3 O+ + OH-[/indent] Запишем уравнение электронейтральности для данной равновесной системы [indent][H 3 O+] = [A-] + [OH-][/indent] Если молярная концентрация сильной одноосновной кислоты больше ~106 моль/л, то вкладом ионов H 3 O+, образующихся при автопротолизе воды, можно пренебречь. Так концентрация последних равна концентрации OH--ионов, то уравнение электронейтральности принимает вид: [indent][H 3 O+] = [A-][/indent] Запишем уравнение материального баланса [indent]CHA = [A-] + [HA][/indent] Так как одноосновная кислота HA является сильной, то равновесная концентрация [HA] ~ 0. Таким образом, уравнение материального баланса принимает вид: [indent]CHA = [A-][/indent] и, следовательно, [indent][H 3 O+] = CHA; p. H = -lg. CHA[/indent] Если молярная концентрация сильной одноосновной кислоты меньше ~106 моль/л, то вкладом ионов H 3 O+, образующихся при автопротолизе воды, пренебречь нельзя. Так как CHA = [A-] и [OH-] = Kw / [H 3 O+], то уравнение электронейтральности принимает вид: [indent][H 3 O+] = CHA + Kw / [H 3 O+], [/indent] отсюда [indent][H 3 O+]2 - CHA[H 3 O+] - Kw = 0[/indent]
РАСТВОР СИЛЬНОЙ КИСЛОТЫ Пусть HA - сильная одноосновная кислота, тогда в растворе существуют следующие равновесия: [indent]HA + H 2 O → H 3 O+ + A 2 H 2 O ↔ H 3 O+ + OH-[/indent] Запишем уравнение электронейтральности для данной равновесной системы [indent][H 3 O+] = [A-] + [OH-][/indent] Если молярная концентрация сильной одноосновной кислоты больше ~106 моль/л, то вкладом ионов H 3 O+, образующихся при автопротолизе воды, можно пренебречь. Так концентрация последних равна концентрации OH--ионов, то уравнение электронейтральности принимает вид: [indent][H 3 O+] = [A-][/indent] Запишем уравнение материального баланса [indent]CHA = [A-] + [HA][/indent] Так как одноосновная кислота HA является сильной, то равновесная концентрация [HA] ~ 0. Таким образом, уравнение материального баланса принимает вид: [indent]CHA = [A-][/indent] и, следовательно, [indent][H 3 O+] = CHA; p. H = -lg. CHA[/indent] Если молярная концентрация сильной одноосновной кислоты меньше ~106 моль/л, то вкладом ионов H 3 O+, образующихся при автопротолизе воды, пренебречь нельзя. Так как CHA = [A-] и [OH-] = Kw / [H 3 O+], то уравнение электронейтральности принимает вид: [indent][H 3 O+] = CHA + Kw / [H 3 O+], [/indent] отсюда [indent][H 3 O+]2 - CHA[H 3 O+] - Kw = 0[/indent]
 РАСТВОР СИЛЬНОГО ОСНОВАНИЯ. Пусть B - сильное однокислотное основание, тогда в растворе существуют следующие равновесия: [indent]B + H 2 O → OH- + BH+ 2 H 2 O ↔ H 3 O+ + OH-[/indent] Запишем уравнение электронейтральности для данной равновесной системы [indent][OH-] = [BH+] + [H 3 O+][/indent] Если молярная концентрация сильного однокислотного основания больше ~106 моль/л, то вкладом OH--ионов, образующихся при автопротолизе воды, можно пренебречь. Так концентрация последних равна концентрации ионов H 3 O+, то уравнение электронейтральности принимает вид: [indent][OH-] = [BH+][/indent] Запишем уравнение материального баланса [indent]CB = [BH+] + [B][/indent] Так как однокислотное основание B является сильным, то равновесная концентрация [B] ~ 0. Таким образом, уравнение материального баланса принимает вид: [indent]CB = [BH+][/indent] и, следовательно, [indent][OH-] = CB[/indent] Так как шкалу кислотности принято выражать в единицах p. H, а [OH-] = Kw / [H 3 O+], то [indent][H 3 O+] = Kw / CB; p. H = p. Kw + lg. CB[/indent] Если молярная концентрация сильного однокислотного основания меньше ~106 моль/л, то вкладом OH--ионов, образующихся при автопротолизе воды, пренебречь нельзя. Так как CB = [BH+] и [OH-] = Kw / [H 3 O+], то уравнение электронейтральности принимает вид: [indent]Kw / [H 3 O+] = CB + [H 3 O+], [/indent] отсюда [indent][H 3 O+]2 + CB[H 3 O+] - Kw = 0[/indent]
РАСТВОР СИЛЬНОГО ОСНОВАНИЯ. Пусть B - сильное однокислотное основание, тогда в растворе существуют следующие равновесия: [indent]B + H 2 O → OH- + BH+ 2 H 2 O ↔ H 3 O+ + OH-[/indent] Запишем уравнение электронейтральности для данной равновесной системы [indent][OH-] = [BH+] + [H 3 O+][/indent] Если молярная концентрация сильного однокислотного основания больше ~106 моль/л, то вкладом OH--ионов, образующихся при автопротолизе воды, можно пренебречь. Так концентрация последних равна концентрации ионов H 3 O+, то уравнение электронейтральности принимает вид: [indent][OH-] = [BH+][/indent] Запишем уравнение материального баланса [indent]CB = [BH+] + [B][/indent] Так как однокислотное основание B является сильным, то равновесная концентрация [B] ~ 0. Таким образом, уравнение материального баланса принимает вид: [indent]CB = [BH+][/indent] и, следовательно, [indent][OH-] = CB[/indent] Так как шкалу кислотности принято выражать в единицах p. H, а [OH-] = Kw / [H 3 O+], то [indent][H 3 O+] = Kw / CB; p. H = p. Kw + lg. CB[/indent] Если молярная концентрация сильного однокислотного основания меньше ~106 моль/л, то вкладом OH--ионов, образующихся при автопротолизе воды, пренебречь нельзя. Так как CB = [BH+] и [OH-] = Kw / [H 3 O+], то уравнение электронейтральности принимает вид: [indent]Kw / [H 3 O+] = CB + [H 3 O+], [/indent] отсюда [indent][H 3 O+]2 + CB[H 3 O+] - Kw = 0[/indent]
 РАСТВОР СЛАБОЙ КИСЛОТЫ Пусть HA - слабая одноосновная кислота, тогда в растворе существует следующее равновесие (автопротолиз воды мы пока учитывать не будем): [indent]HA + H 2 O ↔ H 3 O+ + AKa = [H 3 O+][A-] / [HA] - константа кислотности[/indent] Так как в данной системе единственным источником H 3 O+ и ионов A- является молекула HA, то уравнение электронейтральности принимает вид: [indent][H 3 O+] = [A-][/indent] Запишем уравнение материального баланса [indent]СHA = [HA] + [A-][/indent] Из уравнения материального баланса видно, что равновесная концентрация молекулярной формы слабой кислоты равна разности между общей концентрацией растворенной кислоты CHA и концентрацией анионной формы. Таким образом, [indent][HA] = CHA - [A-] = CHA - [H 3 O+][/indent] Подставив эти выражения в уравнение для константы кислотности [indent]Ka = [H 3 O+][A-] / [HA] = [H 3 O+]2 / (CHA - [H 3 O+])[/indent] и проведя соответствующее преобразование, получаем квадратное уравнение: [indent][H 3 O+]2 + Ka[H 3 O+] - Ka. CHA = 0[/indent] Такой ход вычислений применим к любым растворам слабых кислот, за исключением очень разбавленных растворов с концентрацией растворенного вещества ниже 10 -6 моль/л. Однако во многих случаях эту формулу можно упростить. Если степень протолиза (α = [H 3 O+] / CHA) кислоты меньше 5% *, можно считать, что [HA] ~ CHA. А так как в данной системе единственным источником ионов H 3 O+ и A- является слабая кислота HA, то [H 3 O+] = [A-]. С учетом всех этих допущений [indent]Ka = [H 3 O+][A-] / [HA] = [H 3 O+]2 / CHA[/indent] Решение этого уравнения относительно ионов H 3 O+ приводит к значению [indent][H 3 O+] = (Ka. CHA)1/2[/indent] или в логарифмической форме [indent]p. H = 1/2 (p. Ka - lg. CHA)[/indent]
РАСТВОР СЛАБОЙ КИСЛОТЫ Пусть HA - слабая одноосновная кислота, тогда в растворе существует следующее равновесие (автопротолиз воды мы пока учитывать не будем): [indent]HA + H 2 O ↔ H 3 O+ + AKa = [H 3 O+][A-] / [HA] - константа кислотности[/indent] Так как в данной системе единственным источником H 3 O+ и ионов A- является молекула HA, то уравнение электронейтральности принимает вид: [indent][H 3 O+] = [A-][/indent] Запишем уравнение материального баланса [indent]СHA = [HA] + [A-][/indent] Из уравнения материального баланса видно, что равновесная концентрация молекулярной формы слабой кислоты равна разности между общей концентрацией растворенной кислоты CHA и концентрацией анионной формы. Таким образом, [indent][HA] = CHA - [A-] = CHA - [H 3 O+][/indent] Подставив эти выражения в уравнение для константы кислотности [indent]Ka = [H 3 O+][A-] / [HA] = [H 3 O+]2 / (CHA - [H 3 O+])[/indent] и проведя соответствующее преобразование, получаем квадратное уравнение: [indent][H 3 O+]2 + Ka[H 3 O+] - Ka. CHA = 0[/indent] Такой ход вычислений применим к любым растворам слабых кислот, за исключением очень разбавленных растворов с концентрацией растворенного вещества ниже 10 -6 моль/л. Однако во многих случаях эту формулу можно упростить. Если степень протолиза (α = [H 3 O+] / CHA) кислоты меньше 5% *, можно считать, что [HA] ~ CHA. А так как в данной системе единственным источником ионов H 3 O+ и A- является слабая кислота HA, то [H 3 O+] = [A-]. С учетом всех этих допущений [indent]Ka = [H 3 O+][A-] / [HA] = [H 3 O+]2 / CHA[/indent] Решение этого уравнения относительно ионов H 3 O+ приводит к значению [indent][H 3 O+] = (Ka. CHA)1/2[/indent] или в логарифмической форме [indent]p. H = 1/2 (p. Ka - lg. CHA)[/indent]
 РАСТВОР СЛАБОГО ОСНОВАНИЯ Пусть В - слабое однокислотное основание, тогда в растворе существует следующее равновесие (автопротолиз воды мы пока учитывать не будем): [indent]B + H 2 O ↔ BH+ + OHKb = [BH+][OH-] / [B] - константа основности[/indent] Так как шкалу кислотности принято выражать в единицах p. H, а в выражение константы основности равновесная концентрация протонов не входит в явном виде, то удобнее будет воспользоваться выражением константы кислотности сопряженной кислоты (KBH+ или Ka). [indent]BH+ + H 2 O ↔ B + H 3 O+ KBH+ = [B][H 3 O+] / [BH+] - константа кислотности сопряженной кислоты[/indent] Так как в системе единственным источником OH- и ионов BH+ является молекула B, то уравнение электронейтральности принимает вид: [indent][BH+] = [OH-][/indent] Запишем уравнение материального баланса [indent]СB = [B] + [BH+][/indent] Из уравнения материального баланса видно, что равновесная концентрация молекулярной формы слабого основания равна разности между общей концентрацией растворенного основания CB и концентрацией катионной формы. Таким образом, [indent][B] = CB - [BH+] = CB - [OH-] = CB - Kw / [H 3 O+][/indent] Подставив эти выражения в уравнение константы кислотности сопряженной кислоты [indent]KBH+ = (CB - Kw / [H 3 O+])[H 3 O+] / (Kw / [H 3 O+])[/indent] и проведя соответствующее преобразование, получаем квадратное уравнение: [indent]CB[H 3 O+]2 - Kw[H 3 O+] - Kw. KBH+ = 0[/indent] Такой ход вычислений применим к любым растворам слабых однокислотных оснований, за исключением очень разбавленных растворов с концентрацией растворенного вещества ниже 10 -6 моль/л. Однако во многих случаях эту формулу можно упростить. Если степень протолиза (α = [OH-] / CB = Kw / ([H 3 O+]CB)) основания меньше 5% *, можно считать, что [B] ~ CB. А так как в данной системе единственным источником ионов OH- и BH+ является слабое основание B, то [OH-] = [BH+]. С учетом всех этих допущений [indent]KBH+ = [B][H 3 O+] / [BH+] = CB[H 3 O+]2 / Kw[/indent] Решение этого уравнения относительно ионов H 3 O+ приводит к значению [indent][H 3 O+] = (Kw. KBH+ / CB)1/2[/indent] или в логарифмической форме [indent]p. H = 1/2 (p. Kw + p. KBH+ + lg. CB)[/indent]
РАСТВОР СЛАБОГО ОСНОВАНИЯ Пусть В - слабое однокислотное основание, тогда в растворе существует следующее равновесие (автопротолиз воды мы пока учитывать не будем): [indent]B + H 2 O ↔ BH+ + OHKb = [BH+][OH-] / [B] - константа основности[/indent] Так как шкалу кислотности принято выражать в единицах p. H, а в выражение константы основности равновесная концентрация протонов не входит в явном виде, то удобнее будет воспользоваться выражением константы кислотности сопряженной кислоты (KBH+ или Ka). [indent]BH+ + H 2 O ↔ B + H 3 O+ KBH+ = [B][H 3 O+] / [BH+] - константа кислотности сопряженной кислоты[/indent] Так как в системе единственным источником OH- и ионов BH+ является молекула B, то уравнение электронейтральности принимает вид: [indent][BH+] = [OH-][/indent] Запишем уравнение материального баланса [indent]СB = [B] + [BH+][/indent] Из уравнения материального баланса видно, что равновесная концентрация молекулярной формы слабого основания равна разности между общей концентрацией растворенного основания CB и концентрацией катионной формы. Таким образом, [indent][B] = CB - [BH+] = CB - [OH-] = CB - Kw / [H 3 O+][/indent] Подставив эти выражения в уравнение константы кислотности сопряженной кислоты [indent]KBH+ = (CB - Kw / [H 3 O+])[H 3 O+] / (Kw / [H 3 O+])[/indent] и проведя соответствующее преобразование, получаем квадратное уравнение: [indent]CB[H 3 O+]2 - Kw[H 3 O+] - Kw. KBH+ = 0[/indent] Такой ход вычислений применим к любым растворам слабых однокислотных оснований, за исключением очень разбавленных растворов с концентрацией растворенного вещества ниже 10 -6 моль/л. Однако во многих случаях эту формулу можно упростить. Если степень протолиза (α = [OH-] / CB = Kw / ([H 3 O+]CB)) основания меньше 5% *, можно считать, что [B] ~ CB. А так как в данной системе единственным источником ионов OH- и BH+ является слабое основание B, то [OH-] = [BH+]. С учетом всех этих допущений [indent]KBH+ = [B][H 3 O+] / [BH+] = CB[H 3 O+]2 / Kw[/indent] Решение этого уравнения относительно ионов H 3 O+ приводит к значению [indent][H 3 O+] = (Kw. KBH+ / CB)1/2[/indent] или в логарифмической форме [indent]p. H = 1/2 (p. Kw + p. KBH+ + lg. CB)[/indent]
 ГИДРОЛИЗА. • Гидро лиз (от др. -греч. ὕδωρ — вода + λύσις — разложение) — один из видов химических реакций сольволиза, где при взаимодействии веществ с водой происходит разложение исходного вещества с образованием новых соединений. Механизм гидролиза соединений различных классов: соли, углеводы, белки, сложные эфиры, жиры и другие имеют существенные различия. • Степень гидролиза. Под степенью гидролиза подразумевается отношение части соли, подвергающейся гидролизу, к общей концентрации её ионов в растворе. Обозначается α (или hгидр); α = (cгидр/cобщ)· 100 % где cгидр — число молей гидролизованной соли, cобщ — общее число молей растворённой соли. Степень гидролиза соли тем выше, чем слабее кислота или основание, её образующие. Является количественной характеристикой гидролиза. • Константа гидролиза — константа равновесия гидролитической реакции. Так константа гидролиза соли равна отношению произведения равновесных концентраций продуктов реакции гидролиза к равновесной концентрации соли с
ГИДРОЛИЗА. • Гидро лиз (от др. -греч. ὕδωρ — вода + λύσις — разложение) — один из видов химических реакций сольволиза, где при взаимодействии веществ с водой происходит разложение исходного вещества с образованием новых соединений. Механизм гидролиза соединений различных классов: соли, углеводы, белки, сложные эфиры, жиры и другие имеют существенные различия. • Степень гидролиза. Под степенью гидролиза подразумевается отношение части соли, подвергающейся гидролизу, к общей концентрации её ионов в растворе. Обозначается α (или hгидр); α = (cгидр/cобщ)· 100 % где cгидр — число молей гидролизованной соли, cобщ — общее число молей растворённой соли. Степень гидролиза соли тем выше, чем слабее кислота или основание, её образующие. Является количественной характеристикой гидролиза. • Константа гидролиза — константа равновесия гидролитической реакции. Так константа гидролиза соли равна отношению произведения равновесных концентраций продуктов реакции гидролиза к равновесной концентрации соли с
 ВЫЧИСЛЕНИЕ ЗНАЧЕНИЙ РН РАСТВОРОВ СОЛЕЙ, ПОДВЕРГАЮЩИХСЯ ГИДРОЛИЗУ Вычисление p. H растворов солей В качестве примера возьмем гидролиз ацетата натрия: CH 3 COONa+HOH<—>CH 3 COOH+Na. OH Ионное уравнение: CH 3 COO-+HOH<—>CH 3 COOH+OHКонстанта равновесия этой реакции. K=[CH 3 COOH] • [OH-]/[CH 3 COO- ] • [HOH] так концентрация воды практически остается постоянной, ее можно объединить с константой равновесия: Kг=K • [H 2 O]=[CH 3 COOH] • [OH-]/[CH 3 COO-] где Кг - константа гидролиза. Выразим [OH-] через ионное произведение воды [OH-] =Kв / [H+] и подставив эту величину в уравнение Кг получаем Kг=K • Kв =[CH 3 COOH] • [OH-]/[CH 3 COO-] • [H+] =Kв/Kk где Kk - константа диссоциации слабой кислоты. В общем случае, если исходную концентрацию аниона слабой кислоты А- обозначить через С моль/л, то Ch моль/л – это концентрация той части аниона А-, которая подверглась гидролизу и образовала Ch моль/л слабой кислоты HA и Ch моль/л гидроксильных ионов : A-+HOH<—>HA+OH-C-Ch Ch Chгде: h – степень гидролиза, т. е доля молекул соли, подвергающихся гидролизу. Константа гидролиза соли: При малом значении h: Kг=Сh 2 откуда . Так как [HA]=[OH-]=C , то Kг=[OH- ]2 /C; [H+]=Kв/[OH- ]=Kв/Kк , p. H=-lg[H+]. Аналогично соотношение можно получить и при рассмотрении гидролиза соли слабого основания и сильной кислоты: Kг=[OH- ]2 /C; [H+]=Kв/[OH- ]=Kв/Kосн
ВЫЧИСЛЕНИЕ ЗНАЧЕНИЙ РН РАСТВОРОВ СОЛЕЙ, ПОДВЕРГАЮЩИХСЯ ГИДРОЛИЗУ Вычисление p. H растворов солей В качестве примера возьмем гидролиз ацетата натрия: CH 3 COONa+HOH<—>CH 3 COOH+Na. OH Ионное уравнение: CH 3 COO-+HOH<—>CH 3 COOH+OHКонстанта равновесия этой реакции. K=[CH 3 COOH] • [OH-]/[CH 3 COO- ] • [HOH] так концентрация воды практически остается постоянной, ее можно объединить с константой равновесия: Kг=K • [H 2 O]=[CH 3 COOH] • [OH-]/[CH 3 COO-] где Кг - константа гидролиза. Выразим [OH-] через ионное произведение воды [OH-] =Kв / [H+] и подставив эту величину в уравнение Кг получаем Kг=K • Kв =[CH 3 COOH] • [OH-]/[CH 3 COO-] • [H+] =Kв/Kk где Kk - константа диссоциации слабой кислоты. В общем случае, если исходную концентрацию аниона слабой кислоты А- обозначить через С моль/л, то Ch моль/л – это концентрация той части аниона А-, которая подверглась гидролизу и образовала Ch моль/л слабой кислоты HA и Ch моль/л гидроксильных ионов : A-+HOH<—>HA+OH-C-Ch Ch Chгде: h – степень гидролиза, т. е доля молекул соли, подвергающихся гидролизу. Константа гидролиза соли: При малом значении h: Kг=Сh 2 откуда . Так как [HA]=[OH-]=C , то Kг=[OH- ]2 /C; [H+]=Kв/[OH- ]=Kв/Kк , p. H=-lg[H+]. Аналогично соотношение можно получить и при рассмотрении гидролиза соли слабого основания и сильной кислоты: Kг=[OH- ]2 /C; [H+]=Kв/[OH- ]=Kв/Kосн
 БУФЕРНЫЕ СИСТЕМЫ (РАСТВОРЫ). Буферными называют растворы, р. Н которых практически на изменяется от добавления к ним небольших количеств сильной кислоты или щелочи, а также при разведении. Простейший буферный раствор – это смесь слабой кислоты и соли, имеющей с этой кислотой общий анион (например, смесь уксусной кислоты СН 3 СООН и ацетата натрия СН 3 СООNa), либо смесь слабого основания и соли, имеющей с этим основанием общий катион (например, смесь гидроксида аммония NH 4 OH с хлоридом аммония NH 4 Cl). С точки зрения протонной теории 1 буферное действие растворов обусловлено наличием кислотноосновного равновесия общего типа: Воснование + Н+ Û ВН+сопряженная кислота НАкислота Û Н+ + А-сопряженное основание Сопряженные кислотно-основные пары В /ВН+ и А- /НА называют буферными системами. Буферные растворы играют большую роль в жизнедеятельности. К числу исключительных свойств живых организмов относится их способность поддерживать постоянство р. Н биологических жидкостей, тканей и органов – кислотно-основной гомеостаз. Это постоянство обусловлено наличием нескольких буферных систем, входящих в состав этих тканей. Классификация буферных систем: 1. Кислотные. Состоят из слабой кислоты и соли этой кислоты. Например, ацетатная буферная система (CH 3 COOH+ СН 3 СООNa ), гидрокарбонатная буферная система (H 2 CO 3 +Na. HCO 3 ). 2. Основные. Состоят из слабого основания и его соли. Например, аммиачная буферная система (NH 3 H 2 O + NH 4 Cl). 3. Солевые. Состоят из кислой и средней соли или двух кислых солей. Например, карбонатная буферная система (Na. HCO 3+Na 2 CO 3 ), фосфатная буферная система (КН 2 PO 4 + К 2 НPO 4). 4. ^ Аминокислотные и белковые. Если суммарный заряд молекулы аминокислоты или белка равен нулю (изоэлектрическое состояние), то растворы этих соединений не являются буферными. Их буферное действие начинает проявляться тогда, когда к ним добавляют некоторое количество кислоты или щелочи. Тогда часть белка (аминокислоты) переходит из изоэлектрического состояния в форму “белок-кислота” или соответственно в форму “белок-основание”. Образуется смесь двух форм белка: а) слабая “белок-кислота” + соль этой слабой кислоты; б) слабое “белок- основание” + соль этого слабого основания.
БУФЕРНЫЕ СИСТЕМЫ (РАСТВОРЫ). Буферными называют растворы, р. Н которых практически на изменяется от добавления к ним небольших количеств сильной кислоты или щелочи, а также при разведении. Простейший буферный раствор – это смесь слабой кислоты и соли, имеющей с этой кислотой общий анион (например, смесь уксусной кислоты СН 3 СООН и ацетата натрия СН 3 СООNa), либо смесь слабого основания и соли, имеющей с этим основанием общий катион (например, смесь гидроксида аммония NH 4 OH с хлоридом аммония NH 4 Cl). С точки зрения протонной теории 1 буферное действие растворов обусловлено наличием кислотноосновного равновесия общего типа: Воснование + Н+ Û ВН+сопряженная кислота НАкислота Û Н+ + А-сопряженное основание Сопряженные кислотно-основные пары В /ВН+ и А- /НА называют буферными системами. Буферные растворы играют большую роль в жизнедеятельности. К числу исключительных свойств живых организмов относится их способность поддерживать постоянство р. Н биологических жидкостей, тканей и органов – кислотно-основной гомеостаз. Это постоянство обусловлено наличием нескольких буферных систем, входящих в состав этих тканей. Классификация буферных систем: 1. Кислотные. Состоят из слабой кислоты и соли этой кислоты. Например, ацетатная буферная система (CH 3 COOH+ СН 3 СООNa ), гидрокарбонатная буферная система (H 2 CO 3 +Na. HCO 3 ). 2. Основные. Состоят из слабого основания и его соли. Например, аммиачная буферная система (NH 3 H 2 O + NH 4 Cl). 3. Солевые. Состоят из кислой и средней соли или двух кислых солей. Например, карбонатная буферная система (Na. HCO 3+Na 2 CO 3 ), фосфатная буферная система (КН 2 PO 4 + К 2 НPO 4). 4. ^ Аминокислотные и белковые. Если суммарный заряд молекулы аминокислоты или белка равен нулю (изоэлектрическое состояние), то растворы этих соединений не являются буферными. Их буферное действие начинает проявляться тогда, когда к ним добавляют некоторое количество кислоты или щелочи. Тогда часть белка (аминокислоты) переходит из изоэлектрического состояния в форму “белок-кислота” или соответственно в форму “белок-основание”. Образуется смесь двух форм белка: а) слабая “белок-кислота” + соль этой слабой кислоты; б) слабое “белок- основание” + соль этого слабого основания.
 БУФЕРНАЯ ЕМКОСТЬ. Буферная емкость. Способность буферных систем противодействовать резкому изменению р. Н при добавлении к ним сильной кислоты или основания является ограниченной. Буферная смесь поддерживает р. Н постоянным только при условии, что количество вносимых в раствор сильной кислоты или щелочи не превышает определенной величины. В противном случае наблюдается резкое изменение р. Н, т. е. буферное действие раствора прекращается. Это связано с тем, что в результате протекающей реакции изменяется соотношение молярных концентраций компонентов буферной системы: Скислоты/Ссоли или Соснования/Ссоли. При этом концентрация компонента, реагирующего с добавленной кислотой или щелочью, уменьшается, а концентрация второго компонента возрастает, т. к. он дополнительно образуется в ходе реакции. Количественно буферное действие раствора характеризуется с помощью буферной емкости (В). При этом различают буферную емкость по кислоте (Вк. ) и буферную емкость по основанию или щелочи (Во. ). Буферной емкостью по кислоте является то количество химического эквивалента сильной кислоты, которое нужно добавить к 1 литру (1 дм 3) буферной системы, чтобы уменьшить её р. Н на единицу. Ее можно рассчитать по следующей формуле: где n(1/z HA) - число молей химического эквивалента сильной кислоты, добавленное к 1 литру буферной системы; р. Н 1 - водородный показатель системы до добавления сильной кислоты; р. Н 2 - водородный показатель системы после добавления сильной кислоты. Буферной емкостью по основанию является то количество химического эквивалента сильного основания (щелочи), которое нужно добавить к 1 литру (1 дм 3) буферной системы, чтобы вызвать увеличение ее р. Н на единицу: где n(1/z В) - число молей химического эквивалента основания, которое добавили к 1 литру буферного раствора; р. Н 1 - водородный показатель раствора до добавления основания; р. Н 2 - водородный показатель раствора после добавления основания. В более общем случае (если брать не 1 литр буферной системы, а любой другой ее объем) формула для подсчета буферной емкости по основанию примет следующий вид: где С(1/z В) - молярная концентрация химического эквивалента основания в добавляемом растворе; V(В) - объем (л) добавленного раствора сильного основания; V(буферной системы) - объем буферного раствора (л), к которому добавляют раствор сильного основания.
БУФЕРНАЯ ЕМКОСТЬ. Буферная емкость. Способность буферных систем противодействовать резкому изменению р. Н при добавлении к ним сильной кислоты или основания является ограниченной. Буферная смесь поддерживает р. Н постоянным только при условии, что количество вносимых в раствор сильной кислоты или щелочи не превышает определенной величины. В противном случае наблюдается резкое изменение р. Н, т. е. буферное действие раствора прекращается. Это связано с тем, что в результате протекающей реакции изменяется соотношение молярных концентраций компонентов буферной системы: Скислоты/Ссоли или Соснования/Ссоли. При этом концентрация компонента, реагирующего с добавленной кислотой или щелочью, уменьшается, а концентрация второго компонента возрастает, т. к. он дополнительно образуется в ходе реакции. Количественно буферное действие раствора характеризуется с помощью буферной емкости (В). При этом различают буферную емкость по кислоте (Вк. ) и буферную емкость по основанию или щелочи (Во. ). Буферной емкостью по кислоте является то количество химического эквивалента сильной кислоты, которое нужно добавить к 1 литру (1 дм 3) буферной системы, чтобы уменьшить её р. Н на единицу. Ее можно рассчитать по следующей формуле: где n(1/z HA) - число молей химического эквивалента сильной кислоты, добавленное к 1 литру буферной системы; р. Н 1 - водородный показатель системы до добавления сильной кислоты; р. Н 2 - водородный показатель системы после добавления сильной кислоты. Буферной емкостью по основанию является то количество химического эквивалента сильного основания (щелочи), которое нужно добавить к 1 литру (1 дм 3) буферной системы, чтобы вызвать увеличение ее р. Н на единицу: где n(1/z В) - число молей химического эквивалента основания, которое добавили к 1 литру буферного раствора; р. Н 1 - водородный показатель раствора до добавления основания; р. Н 2 - водородный показатель раствора после добавления основания. В более общем случае (если брать не 1 литр буферной системы, а любой другой ее объем) формула для подсчета буферной емкости по основанию примет следующий вид: где С(1/z В) - молярная концентрация химического эквивалента основания в добавляемом растворе; V(В) - объем (л) добавленного раствора сильного основания; V(буферной системы) - объем буферного раствора (л), к которому добавляют раствор сильного основания.
 БУФЕРНОЕ ДЕЙСТВИЕ. Многие реакции в растворе протекают в нужном направлении только при определенной концентрации ионов Н+. Изменение её в ту или иную сторону от соответствующего оптимального значения приводит к появлению новых, часто нежелательных продуктов. В связи с этим, поддержание постоянного значения р. Н на протяжении всего времени осуществления реакции часто является важным условием ее успешного завершения. Особенно актуально это для биохимических процессов, протекающих в живых организмах. Большинство из них катализируется различными ферментами или гормонами, проявляющими свою биологическую активность только в строго определенном и достаточно узком интервале значений р. Н. Растворы, способные сохранять постоянной концентрацию ионов Н+ при добавлении к ним небольших количеств сильной кислоты или щелочи, а также при разбавлении, называются буферными растворами или буферными системами. Свойство данных растворов сохранять неизменным присущее им значение р. Н при вышеперечисленных обстоятельствах, называется иначе буферным действием.
БУФЕРНОЕ ДЕЙСТВИЕ. Многие реакции в растворе протекают в нужном направлении только при определенной концентрации ионов Н+. Изменение её в ту или иную сторону от соответствующего оптимального значения приводит к появлению новых, часто нежелательных продуктов. В связи с этим, поддержание постоянного значения р. Н на протяжении всего времени осуществления реакции часто является важным условием ее успешного завершения. Особенно актуально это для биохимических процессов, протекающих в живых организмах. Большинство из них катализируется различными ферментами или гормонами, проявляющими свою биологическую активность только в строго определенном и достаточно узком интервале значений р. Н. Растворы, способные сохранять постоянной концентрацию ионов Н+ при добавлении к ним небольших количеств сильной кислоты или щелочи, а также при разбавлении, называются буферными растворами или буферными системами. Свойство данных растворов сохранять неизменным присущее им значение р. Н при вышеперечисленных обстоятельствах, называется иначе буферным действием.
![ЗНАЧЕНИЯ РН БУФЕРНЫХ РАСТВОРОВ. В чистой воде при 25 °C концентрации ионов водорода ([H+]) ЗНАЧЕНИЯ РН БУФЕРНЫХ РАСТВОРОВ. В чистой воде при 25 °C концентрации ионов водорода ([H+])](https://present5.com/presentation/208984867_428487904/image-39.jpg) ЗНАЧЕНИЯ РН БУФЕРНЫХ РАСТВОРОВ. В чистой воде при 25 °C концентрации ионов водорода ([H+]) и гидроксид-ионов ([OH−]) одинаковы и составляют 10− 7 моль/л, это напрямую следует из определения ионного произведения воды, которое равно [H+] · [OH−] и составляет 10− 14 моль²/л² (при 25 °C). Когда концентрации обоих видов ионов в растворе одинаковы, говорят, что раствор имеет нейтральную реакцию. При добавлении к воде кислоты концентрация ионов водорода увеличивается, а концентрация гидроксид-ионов соответственно уменьшается, при добавлении основания — наоборот, повышается содержание гидроксид-ионов, а концентрация ионов водорода падает. Когда [H+] > [OH−] говорят, что раствор является кислым, а при [OH−] > [H+] — щелочным. Для удобства представления, чтобы избавиться от отрицательного показателя степени, вместо концентраций ионов водорода пользуются их десятичным логарифмом, взятым с обратным знаком, который собственно и является водородным показателем — p. H.
ЗНАЧЕНИЯ РН БУФЕРНЫХ РАСТВОРОВ. В чистой воде при 25 °C концентрации ионов водорода ([H+]) и гидроксид-ионов ([OH−]) одинаковы и составляют 10− 7 моль/л, это напрямую следует из определения ионного произведения воды, которое равно [H+] · [OH−] и составляет 10− 14 моль²/л² (при 25 °C). Когда концентрации обоих видов ионов в растворе одинаковы, говорят, что раствор имеет нейтральную реакцию. При добавлении к воде кислоты концентрация ионов водорода увеличивается, а концентрация гидроксид-ионов соответственно уменьшается, при добавлении основания — наоборот, повышается содержание гидроксид-ионов, а концентрация ионов водорода падает. Когда [H+] > [OH−] говорят, что раствор является кислым, а при [OH−] > [H+] — щелочным. Для удобства представления, чтобы избавиться от отрицательного показателя степени, вместо концентраций ионов водорода пользуются их десятичным логарифмом, взятым с обратным знаком, который собственно и является водородным показателем — p. H.
 ХИМИЧЕСКОМ АНАЛИЗЕ. Буферные растворы широко применяют в химическом анализе в тех случаях, когда по условиям опыта химическая реакция должна протекать при соблюдении точного значения , не меняющегося при разбавлении раствора или при добавлении к нему других реагентов. Например, при проведении реакций окисления—восстановления, при осаждении сульфидов, гидроокисей, карбонатов, хроматов, фосфатов и другие. Приведем некоторые случаи использования их в целях анализа. Ацетатный буферный раствор применяют при осаждении осадков, не осаждаемых в кислых или щелочных растворах. Вредное влияние кислот подавляет ацетат натрия, который вступает в реакцию с сильной кислотой. Например: или в ионной форме; Вредное влияние оснований подавляет уксусная кислота, которая вступает в реакцию с сильным основанием: Например, -ионы образуют с хромат-ионами в уксуснокислой среде в присутствии и -ионов осадок , при этом остаются в растворе. Для достижения полноты осаждения добавляют к исследуемому раствору ацетатную буферную смесь, оказывающую буферное действие в отношении сильных кислот и сильных оснований. Разделение ионов, осаждаемых в виде гидроокисей и оксиацетатов , от ионов, не осаждаемых в виде указанных соединений, также ведут в ацетатцо-буферной среде. Ацетатно-буферную смесь применяют и для селективного окисления — восстановления в присутствии. Аммиачноаммонийный буферный раствор применяют при осаждении карбонатов бария, стронция, кальция и отделения их от ионов магния ; при осаждении сульфидов никеля, кобальта, цинка, марганца, железа, а также при выделении гидроокисей алюминия, хрома, бериллия, титана, циркония, железа. Формиатный буферный раствор применяют при отделении ионов цинка, осаждаемых в виде в присутствии ионов кобальта, никеля, марганца, железа, алюминия и хрома. Фосфатный буферный раствор используют при проведении многих реакций окисления — восстановления. Для успешного применения буферных смесей в целях анализа необходимо помнить о том, что не всякая смесь пригодна для данного анализа. Буферную смесь выбирают в зависимости от ее назначения. Она должна удовлетвррять определенному качественному составу, а ее компоненты
ХИМИЧЕСКОМ АНАЛИЗЕ. Буферные растворы широко применяют в химическом анализе в тех случаях, когда по условиям опыта химическая реакция должна протекать при соблюдении точного значения , не меняющегося при разбавлении раствора или при добавлении к нему других реагентов. Например, при проведении реакций окисления—восстановления, при осаждении сульфидов, гидроокисей, карбонатов, хроматов, фосфатов и другие. Приведем некоторые случаи использования их в целях анализа. Ацетатный буферный раствор применяют при осаждении осадков, не осаждаемых в кислых или щелочных растворах. Вредное влияние кислот подавляет ацетат натрия, который вступает в реакцию с сильной кислотой. Например: или в ионной форме; Вредное влияние оснований подавляет уксусная кислота, которая вступает в реакцию с сильным основанием: Например, -ионы образуют с хромат-ионами в уксуснокислой среде в присутствии и -ионов осадок , при этом остаются в растворе. Для достижения полноты осаждения добавляют к исследуемому раствору ацетатную буферную смесь, оказывающую буферное действие в отношении сильных кислот и сильных оснований. Разделение ионов, осаждаемых в виде гидроокисей и оксиацетатов , от ионов, не осаждаемых в виде указанных соединений, также ведут в ацетатцо-буферной среде. Ацетатно-буферную смесь применяют и для селективного окисления — восстановления в присутствии. Аммиачноаммонийный буферный раствор применяют при осаждении карбонатов бария, стронция, кальция и отделения их от ионов магния ; при осаждении сульфидов никеля, кобальта, цинка, марганца, железа, а также при выделении гидроокисей алюминия, хрома, бериллия, титана, циркония, железа. Формиатный буферный раствор применяют при отделении ионов цинка, осаждаемых в виде в присутствии ионов кобальта, никеля, марганца, железа, алюминия и хрома. Фосфатный буферный раствор используют при проведении многих реакций окисления — восстановления. Для успешного применения буферных смесей в целях анализа необходимо помнить о том, что не всякая смесь пригодна для данного анализа. Буферную смесь выбирают в зависимости от ее назначения. Она должна удовлетвррять определенному качественному составу, а ее компоненты
 СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ. 1. Харитонов Ю. Я. Аналитическая химия. Аналитика. В двух книгах. 3 е издание. М. : Высш. шк. , 2005. 2. . Лурье Ю. Ю. Справочник по аналитической химии. М. : Химия, 1989. 3. http: //yandex. ru/ 4. http: //ru. wikipedia. org
СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ. 1. Харитонов Ю. Я. Аналитическая химия. Аналитика. В двух книгах. 3 е издание. М. : Высш. шк. , 2005. 2. . Лурье Ю. Ю. Справочник по аналитической химии. М. : Химия, 1989. 3. http: //yandex. ru/ 4. http: //ru. wikipedia. org


