Кислотно-основное равновесие.ppt
- Количество слайдов: 39
 Кислотно-основное равновесие 16. 02. 12
Кислотно-основное равновесие 16. 02. 12
 Теория Аррениуса Основана на его теории электролитической диссоциации (является частным следствием этой теории): 1. Кислота – вещество, отщепляющее при ионизации протон. HNO 3 ↔ H+ + NO 3 - и HNO 2 ↔ H+ + NO 22. Основание – вещество, отщепляющее при ионизации гидроксид-ион. Na. OH ↔ Na+ + OH- и NH 3 + H 2 O ↔ NH 4+ + OH-
Теория Аррениуса Основана на его теории электролитической диссоциации (является частным следствием этой теории): 1. Кислота – вещество, отщепляющее при ионизации протон. HNO 3 ↔ H+ + NO 3 - и HNO 2 ↔ H+ + NO 22. Основание – вещество, отщепляющее при ионизации гидроксид-ион. Na. OH ↔ Na+ + OH- и NH 3 + H 2 O ↔ NH 4+ + OH-
 Кислоты и основания, для которых степень распада на ионы (степень электролитической диссоциации) имеет значение, близкое к единице, были названы Аррениусом сильными (HNO 3, Na. OH), а все остальные – слабыми (HNO 2, NH 3 *H 2 O).
Кислоты и основания, для которых степень распада на ионы (степень электролитической диссоциации) имеет значение, близкое к единице, были названы Аррениусом сильными (HNO 3, Na. OH), а все остальные – слабыми (HNO 2, NH 3 *H 2 O).
 Слабые кислоты можно было сравнить по силе, используя закон действующих масс – по значениям констант кислотной диссоциации KДК Слабые основания – по значениям констант оснóвной диссоциации KДО. Чем выше значение KД, тем более сильным считался слабый электролит-кислота или слабый электролит-основание.
Слабые кислоты можно было сравнить по силе, используя закон действующих масс – по значениям констант кислотной диссоциации KДК Слабые основания – по значениям констант оснóвной диссоциации KДО. Чем выше значение KД, тем более сильным считался слабый электролит-кислота или слабый электролит-основание.
 Для многооснóвных кислот (например, H 2 CO 3 или H 3 PO 4) и многокислотных оснований типа Ca(OH)2 и La(OH)3 идет ступенчатая диссоциация – последовательный отрыв каждого катиона H+ или аниона OH-: H 2 CO 3 ↔ H+ + HCO 3 -, HCO 3 - ↔ H+ + CO 32 Ca(OH)2 ↔ Ca. OH+ + OH-, Ca. OH+ ↔ Ca 2+ + OH-
Для многооснóвных кислот (например, H 2 CO 3 или H 3 PO 4) и многокислотных оснований типа Ca(OH)2 и La(OH)3 идет ступенчатая диссоциация – последовательный отрыв каждого катиона H+ или аниона OH-: H 2 CO 3 ↔ H+ + HCO 3 -, HCO 3 - ↔ H+ + CO 32 Ca(OH)2 ↔ Ca. OH+ + OH-, Ca. OH+ ↔ Ca 2+ + OH-
 Недостатки теории Аррениуса: 1. Эксперименты показали, что растворимость и степень диссоциации никак между собой не связаны: и хорошо, и плохо растворимый электролит может оказаться и сильным, и слабым.
Недостатки теории Аррениуса: 1. Эксперименты показали, что растворимость и степень диссоциации никак между собой не связаны: и хорошо, и плохо растворимый электролит может оказаться и сильным, и слабым.
 Указанные экспериментальные факты были объяснены в 1888 году В. Оствальдом, который сформулировал закон разбавления, устанавливающий математическую зависимость между степенью диссоциации α и аналитической (по приготовлению) концентрацией вещества в растворе С, а именно: KД = α 2 С/(1 – α) = Const
Указанные экспериментальные факты были объяснены в 1888 году В. Оствальдом, который сформулировал закон разбавления, устанавливающий математическую зависимость между степенью диссоциации α и аналитической (по приготовлению) концентрацией вещества в растворе С, а именно: KД = α 2 С/(1 – α) = Const
 2. По идее Аррениуса, вода является лишь растворителем (средой) и химически не участвует в реакциях диссоциации кислот и оснований. Однако известно, что это не всегда так (физико-химическая теория растворов Менделеева).
2. По идее Аррениуса, вода является лишь растворителем (средой) и химически не участвует в реакциях диссоциации кислот и оснований. Однако известно, что это не всегда так (физико-химическая теория растворов Менделеева).
 3. По идее Аррениуса, кислые соли должны диссоциировать в воде так же ступенчато, как многоосновные кислоты: Na. HSO 4 ↔ Na+ + HSO 4 -, HSO 4 - ↔ H+ + SO 42 Na. HCO 3 ↔ Na+ + HCO 3 -, HCO 3 - ↔ H+ + CO 32 При этом они должны создавать в растворе кислотную среду, обусловленную избытком ионов H+. Однако экспериментальные данные показывают, что, например, в растворе Na. HSO 4 среда кислотная, а в растворе Na. HCO 3 – наоборот, щелочная, хотя избыточное содержание гидроксид-ионов OH- в рамках теории Аррениуса объяснить невозможно.
3. По идее Аррениуса, кислые соли должны диссоциировать в воде так же ступенчато, как многоосновные кислоты: Na. HSO 4 ↔ Na+ + HSO 4 -, HSO 4 - ↔ H+ + SO 42 Na. HCO 3 ↔ Na+ + HCO 3 -, HCO 3 - ↔ H+ + CO 32 При этом они должны создавать в растворе кислотную среду, обусловленную избытком ионов H+. Однако экспериментальные данные показывают, что, например, в растворе Na. HSO 4 среда кислотная, а в растворе Na. HCO 3 – наоборот, щелочная, хотя избыточное содержание гидроксид-ионов OH- в рамках теории Аррениуса объяснить невозможно.
 4. В рамки определений Аррениуса не укладывались реакции гидролиза солей, образованных слабыми кислотами или слабыми основаниями, например: Al. Cl 3 + H 2 O ↔ (Al. OH)Cl 2 + HCl, Al 3+ + H 2 O ↔ Al. OH 2+ + H+ Na 2 CO 3 + H 2 O ↔ Na. HCO 3 + Na. OH, CO 32 - + H 2 O ↔ HCO 3 -+ OHНесмотря на то, что подобные соли создают в растворе кислотную или щелочную среду, кислотами или основаниями по Аррениусу они не являются. Поскольку вода входит в уравнения гидролиза уже как полноценный реагент, такие реакции, согласно представлениям Аррениуса, считались особым видом обменных реакций в водном растворе, а состояние равновесия характеризовали константами гидролиза, вычисляемыми по сложными правилам, различным для солей разных типов.
4. В рамки определений Аррениуса не укладывались реакции гидролиза солей, образованных слабыми кислотами или слабыми основаниями, например: Al. Cl 3 + H 2 O ↔ (Al. OH)Cl 2 + HCl, Al 3+ + H 2 O ↔ Al. OH 2+ + H+ Na 2 CO 3 + H 2 O ↔ Na. HCO 3 + Na. OH, CO 32 - + H 2 O ↔ HCO 3 -+ OHНесмотря на то, что подобные соли создают в растворе кислотную или щелочную среду, кислотами или основаниями по Аррениусу они не являются. Поскольку вода входит в уравнения гидролиза уже как полноценный реагент, такие реакции, согласно представлениям Аррениуса, считались особым видом обменных реакций в водном растворе, а состояние равновесия характеризовали константами гидролиза, вычисляемыми по сложными правилам, различным для солей разных типов.
 5. В-пятых, невозможно описать кислотноосновное равновесие в неводных растворителях.
5. В-пятых, невозможно описать кислотноосновное равновесие в неводных растворителях.
 Теория Бренстеда-Лоури Кислота – это водородсодержащая частица вещества (молекула или ион), способная быть донором протона Основание – это частица вещества, способная быть акцептором протона. Кислоты и основания как вещества, теряющие и приобретающие протоны, называются протолитами, передача протона от кислоты к основанию именуется протолизом, а химическая реакция между ними – протолитической реакцией.
Теория Бренстеда-Лоури Кислота – это водородсодержащая частица вещества (молекула или ион), способная быть донором протона Основание – это частица вещества, способная быть акцептором протона. Кислоты и основания как вещества, теряющие и приобретающие протоны, называются протолитами, передача протона от кислоты к основанию именуется протолизом, а химическая реакция между ними – протолитической реакцией.
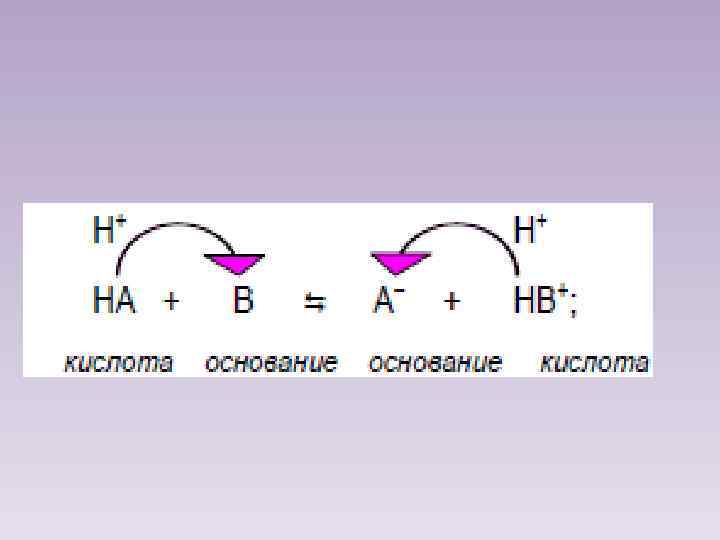
 В протолитической реакции всегда имеются две сопряженные пары «кислота» / «основание» НA/A- и HB+/B. Например, в реакции HNO 3 + NH 3 ↔ NO 3 - + NH 4+ сопряженными парами будут HNO 3/ NO 3 - и NH 4+ / NH 3.
В протолитической реакции всегда имеются две сопряженные пары «кислота» / «основание» НA/A- и HB+/B. Например, в реакции HNO 3 + NH 3 ↔ NO 3 - + NH 4+ сопряженными парами будут HNO 3/ NO 3 - и NH 4+ / NH 3.
 Т. о. основные положения протолитической теории сводятся к следующим моментам: 1 Каждой кислоте соответствует основание, которое возникает при потере кислотой протона. Таким образом, вводится понятие сопряженной пары: кислоту и основание, относящиеся к одной паре, называют сопряженными. 2 Вещество не может реагировать как кислота, если нет акцептора протона. Таким образом, должна быть другая сопряженная пара, борьба между этими парами. 3 Сила кислоты характеризуется количеством переданных протонов, сила основания – числом принятых протонов. 4 Направление процесса: в сторону более слабых кислот и оснований.
Т. о. основные положения протолитической теории сводятся к следующим моментам: 1 Каждой кислоте соответствует основание, которое возникает при потере кислотой протона. Таким образом, вводится понятие сопряженной пары: кислоту и основание, относящиеся к одной паре, называют сопряженными. 2 Вещество не может реагировать как кислота, если нет акцептора протона. Таким образом, должна быть другая сопряженная пара, борьба между этими парами. 3 Сила кислоты характеризуется количеством переданных протонов, сила основания – числом принятых протонов. 4 Направление процесса: в сторону более слабых кислот и оснований.
 Примеры кислотно-основных равновесий А 1 + В 2 ↔ А 2 + В 1 Примечание HCl + NH 3 ↔ NH 4+ + Cl- Нейтрализаци я H 2 O + H 2 O ↔ H 3 O+ + OHNH 3 + NH 3 ↔ NH 4+ + NH 2 - Автоионизаци я (автопротолиз ) Диссоциация CH 3 COOH + H 2 O ↔ H 3 O+ + CH 3 COO+ в различных H 2 SO 4 + CH 3 COOH ↔ CH 3 COOH 2 + HSO 4 растворителях + H 2 O + NH 3 ↔ NH 4 + OH Гидролиз H 2 O + S 2 - ↔ HS- + OH 3+ Al(H 2 O)6 + H 2 O ↔ H 3 O+ + [Al(H 2 O)5(OH)]2+
Примеры кислотно-основных равновесий А 1 + В 2 ↔ А 2 + В 1 Примечание HCl + NH 3 ↔ NH 4+ + Cl- Нейтрализаци я H 2 O + H 2 O ↔ H 3 O+ + OHNH 3 + NH 3 ↔ NH 4+ + NH 2 - Автоионизаци я (автопротолиз ) Диссоциация CH 3 COOH + H 2 O ↔ H 3 O+ + CH 3 COO+ в различных H 2 SO 4 + CH 3 COOH ↔ CH 3 COOH 2 + HSO 4 растворителях + H 2 O + NH 3 ↔ NH 4 + OH Гидролиз H 2 O + S 2 - ↔ HS- + OH 3+ Al(H 2 O)6 + H 2 O ↔ H 3 O+ + [Al(H 2 O)5(OH)]2+
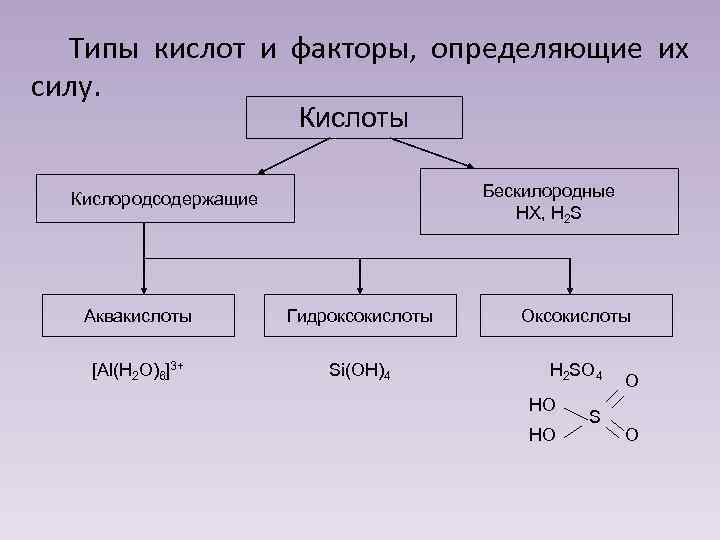 Типы кислот и факторы, определяющие их силу. Кислоты Бескилородные HX, H 2 S Кислородсодержащие Аквакислоты Гидроксокислоты Оксокислоты [Al(H 2 O)6]3+ Si(OH)4 H 2 SO 4 HO HO S O O
Типы кислот и факторы, определяющие их силу. Кислоты Бескилородные HX, H 2 S Кислородсодержащие Аквакислоты Гидроксокислоты Оксокислоты [Al(H 2 O)6]3+ Si(OH)4 H 2 SO 4 HO HO S O O
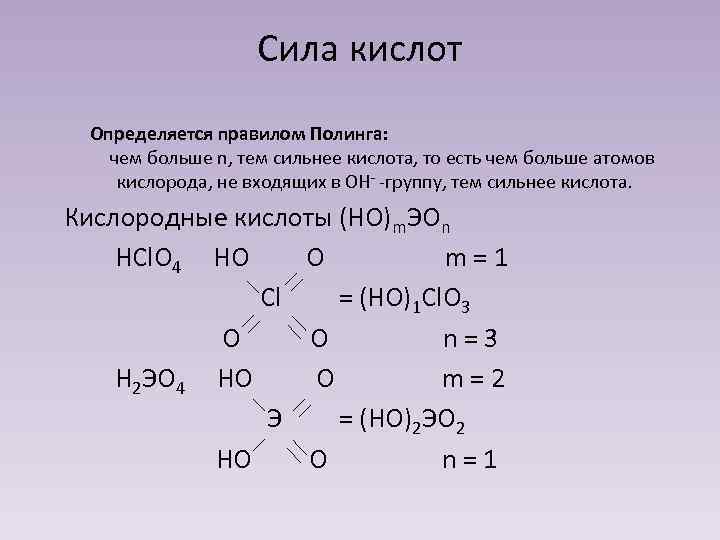 Сила кислот Определяется правилом Полинга: чем больше n, тем сильнее кислота, то есть чем больше атомов кислорода, не входящих в OH- -группу, тем сильнее кислота. Кислородные кислоты (НО)m. ЭОn HCl. O 4 HO O m=1 Cl = (HO)1 Cl. O 3 O O n=3 H 2 ЭO 4 HO O m=2 Э = (НО)2 ЭО 2 НО О n=1
Сила кислот Определяется правилом Полинга: чем больше n, тем сильнее кислота, то есть чем больше атомов кислорода, не входящих в OH- -группу, тем сильнее кислота. Кислородные кислоты (НО)m. ЭОn HCl. O 4 HO O m=1 Cl = (HO)1 Cl. O 3 O O n=3 H 2 ЭO 4 HO O m=2 Э = (НО)2 ЭО 2 НО О n=1
 Протонные растворители и их автопротолиз Протонные растворители Кислотные Основные Амфотерные
Протонные растворители и их автопротолиз Протонные растворители Кислотные Основные Амфотерные
 Кислотные и основные растворители Кислотные и оснόвные растворители проявляют названную функцию по отношению к большинству растворенных в них протолитов, заставляя последние быть соответственно или только основаниями, или только кислотами. Поэтому в среде кислотных и оснόвных растворителей весьма немного протолитов с одноименной функцией (кислотной и оснόвной соответственно), а протолитов с противоположной функцией – численно много, причем их сила примерно одинакова (сглажена) вследствие высокой кислотности или основности самого растворителя. Такое сглаживание называют нивелирующим действием растворителя. Примерами кислотных растворителей являются вещества HCl. O 4, HF, H 2 SO 4, HNO 3 и CH 3 COOH, а примерами оснόвных растворителей – вещества NH 3, N 2 H 4, C 5 H 5 N (пиридин) и др.
Кислотные и основные растворители Кислотные и оснόвные растворители проявляют названную функцию по отношению к большинству растворенных в них протолитов, заставляя последние быть соответственно или только основаниями, или только кислотами. Поэтому в среде кислотных и оснόвных растворителей весьма немного протолитов с одноименной функцией (кислотной и оснόвной соответственно), а протолитов с противоположной функцией – численно много, причем их сила примерно одинакова (сглажена) вследствие высокой кислотности или основности самого растворителя. Такое сглаживание называют нивелирующим действием растворителя. Примерами кислотных растворителей являются вещества HCl. O 4, HF, H 2 SO 4, HNO 3 и CH 3 COOH, а примерами оснόвных растворителей – вещества NH 3, N 2 H 4, C 5 H 5 N (пиридин) и др.
 Амфотерные растворители способны проявлять по отношению к одному большому набору протолитов кислотные свойства, а к другому большому набору протолитов – оснόвные свойства. Амфотерные растворители оказывают обладают весьма сильным дифференцирующим действием, а именно: увеличивают различие в силе большого числа кислот и большого числа оснований. Это дает возможность изучать и сравнивать в среде амфотерных растворителей кислотно-оснόвные свойства широкого круга веществ.
Амфотерные растворители способны проявлять по отношению к одному большому набору протолитов кислотные свойства, а к другому большому набору протолитов – оснόвные свойства. Амфотерные растворители оказывают обладают весьма сильным дифференцирующим действием, а именно: увеличивают различие в силе большого числа кислот и большого числа оснований. Это дает возможность изучать и сравнивать в среде амфотерных растворителей кислотно-оснόвные свойства широкого круга веществ.
 Ионное произведение растворителя. Каждый протонный растворитель HL является амфолитом по отношению к самому себе и вступает в реакцию автопротолиза: HL + HL = L- + H 2 L+ Выражение для константы равновесия реакции автопротолиза HL Степень протолиза очень мала и, следовательно, равновесная молярная концентрация непротолизованных молекул растворителя [HL] практически равна исходной концентрации этого растворителя CHL: [HL] = CHL
Ионное произведение растворителя. Каждый протонный растворитель HL является амфолитом по отношению к самому себе и вступает в реакцию автопротолиза: HL + HL = L- + H 2 L+ Выражение для константы равновесия реакции автопротолиза HL Степень протолиза очень мала и, следовательно, равновесная молярная концентрация непротолизованных молекул растворителя [HL] практически равна исходной концентрации этого растворителя CHL: [HL] = CHL
 Значение аналитической концентрации химически чистого вещества CHL (т. е. отношение количества этого вещества к собственному объему) – это константа данного вещества. Объединяя в выражении для KC постоянные KC и [HL]2 в одну константу KC*[HL]2 и обозначая ее KS, получим выражение: KS = [L-]*[H 2 L+] = Const Величина KS – ионное произведение растворителя. Значение KS служит количественной характеристикой реакции автопротолиза данного растворителя.
Значение аналитической концентрации химически чистого вещества CHL (т. е. отношение количества этого вещества к собственному объему) – это константа данного вещества. Объединяя в выражении для KC постоянные KC и [HL]2 в одну константу KC*[HL]2 и обозначая ее KS, получим выражение: KS = [L-]*[H 2 L+] = Const Величина KS – ионное произведение растворителя. Значение KS служит количественной характеристикой реакции автопротолиза данного растворителя.
 Ионное произведение воды обозначается иначе – KB: H 2 O + H 2 O ↔ OH- + H 3 O+; KB = 1, 0 · 1014 (25°C)
Ионное произведение воды обозначается иначе – KB: H 2 O + H 2 O ↔ OH- + H 3 O+; KB = 1, 0 · 1014 (25°C)
 Слабые кислоты и основания. Константа кислотности Пусть протолит HA является слабой кислотой по отношению к HL: HA +HL ↔ A- + H 2 L+ Выражение для константы равновесия этой реакции
Слабые кислоты и основания. Константа кислотности Пусть протолит HA является слабой кислотой по отношению к HL: HA +HL ↔ A- + H 2 L+ Выражение для константы равновесия этой реакции
![KC*[HL] = KK Поэтому: р. Н раствора слабой кислоты: р. Н = 0, 5(р. KC*[HL] = KK Поэтому: р. Н раствора слабой кислоты: р. Н = 0, 5(р.](https://present5.com/presentation/3/9354683_184434798.pdf-img/9354683_184434798.pdf-26.jpg) KC*[HL] = KK Поэтому: р. Н раствора слабой кислоты: р. Н = 0, 5(р. КК - lg. CК)
KC*[HL] = KK Поэтому: р. Н раствора слабой кислоты: р. Н = 0, 5(р. КК - lg. CК)
 Величина KK – это константа кислотности. Она является количественной характеристикой состояния протолитического равновесия обратимой реакции между кислотой HA и основанием HL. Чем больше значение KK, тем более сильной кислотой считается протолит HA в данном растворителе HL.
Величина KK – это константа кислотности. Она является количественной характеристикой состояния протолитического равновесия обратимой реакции между кислотой HA и основанием HL. Чем больше значение KK, тем более сильной кислотой считается протолит HA в данном растворителе HL.
 Аналогично выводится константа основности. р. Н раствора слабого оснвоания: р. Н = 14 – 0, 5(р. КО - lg. CО) КО – константа основности СО – концентрация основания
Аналогично выводится константа основности. р. Н раствора слабого оснвоания: р. Н = 14 – 0, 5(р. КО - lg. CО) КО – константа основности СО – концентрация основания
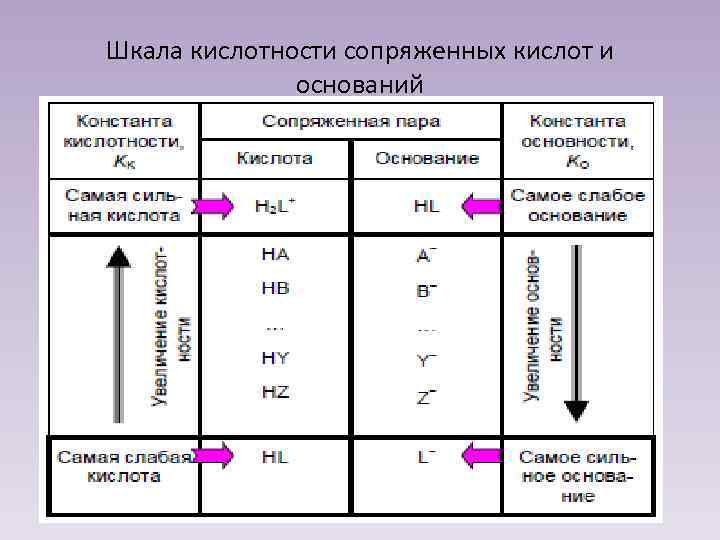 Шкала кислотности сопряженных кислот и оснований
Шкала кислотности сопряженных кислот и оснований
 Гидролиз Сольволиз (гидролиз) – обменная химическая реакция между растворителем (водой) и растворенным веществом. Сольватация (гидратация) – реакция комплексообразования, т. е. присоединение молекул растворителя (воды) к ионам растворенного вещества по донорно-акцепторному механизму.
Гидролиз Сольволиз (гидролиз) – обменная химическая реакция между растворителем (водой) и растворенным веществом. Сольватация (гидратация) – реакция комплексообразования, т. е. присоединение молекул растворителя (воды) к ионам растворенного вещества по донорно-акцепторному механизму.
 Гидролизу подвергаются соли: 1) Образованные катионом слабого основания и анионом сильной кислоты, например, Al. Cl 3: Al 3+ катион слабого основания Al(OH)3; Cl- - анион сильной кислоты HCl; 2) Образованные катионом сильного основания и анионом слабой кислоты, например, Na 2 S: Na+ катион сильного основания Na. OH; S-2 – анион слабой кислоты H 2 S; 3) Образованные катионом слабого основания и анионом слабой кислоты, например, NH 4 S: NH 4+ катион слабого основания NH 4 OH; S-2 – анион слабой кислоты H 2 S.
Гидролизу подвергаются соли: 1) Образованные катионом слабого основания и анионом сильной кислоты, например, Al. Cl 3: Al 3+ катион слабого основания Al(OH)3; Cl- - анион сильной кислоты HCl; 2) Образованные катионом сильного основания и анионом слабой кислоты, например, Na 2 S: Na+ катион сильного основания Na. OH; S-2 – анион слабой кислоты H 2 S; 3) Образованные катионом слабого основания и анионом слабой кислоты, например, NH 4 S: NH 4+ катион слабого основания NH 4 OH; S-2 – анион слабой кислоты H 2 S.
 В результате гидролиза всегда образуется малодиссоциирующий (слабый) электролит, представляющий собой слабую кислоту или слабое основание!!!
В результате гидролиза всегда образуется малодиссоциирующий (слабый) электролит, представляющий собой слабую кислоту или слабое основание!!!
 Количественная характеристика процесса гидролиза 1. Степень гидролиза – отношение количества гидролизовавшихся молекул к общему количеству молекул. 2. Константа гидролиза – константа, описывающая состояние гидролитического процесса.
Количественная характеристика процесса гидролиза 1. Степень гидролиза – отношение количества гидролизовавшихся молекул к общему количеству молекул. 2. Константа гидролиза – константа, описывающая состояние гидролитического процесса.
 Соль, гидролизующаяся по катиону А) Диссоциация соли: Al. Cl 3 ↔ Al 3+ + 3 Cl. Б) Взаимодействие с молекулой воды: Составной компонент (Al 3+) слабого электролита (Al(OH)3) «отрывает» от молекулы воды недостающую часть для образования этого слабого электролита: Al 3+ + H 2 O = Al. OH 2+ + Н+ Как правило, гидролиз протекает только по первой ступени (для многозарядных ионов). Константа гидролиза:
Соль, гидролизующаяся по катиону А) Диссоциация соли: Al. Cl 3 ↔ Al 3+ + 3 Cl. Б) Взаимодействие с молекулой воды: Составной компонент (Al 3+) слабого электролита (Al(OH)3) «отрывает» от молекулы воды недостающую часть для образования этого слабого электролита: Al 3+ + H 2 O = Al. OH 2+ + Н+ Как правило, гидролиз протекает только по первой ступени (для многозарядных ионов). Константа гидролиза:
 Аналогичный процесс происходит при гидролизе соли, содержащей анион слабой кислоты, однако в этом случае в раствор будут выделяться гидроксид ионы. При гидролизе катиона слабого основания в раствор выделяются протоны водорода! р. Н < 7 При гидролизе аниона слабой кислоты в раствор выделяются гидкроксид-ионы! р. Н > 7
Аналогичный процесс происходит при гидролизе соли, содержащей анион слабой кислоты, однако в этом случае в раствор будут выделяться гидроксид ионы. При гидролизе катиона слабого основания в раствор выделяются протоны водорода! р. Н < 7 При гидролизе аниона слабой кислоты в раствор выделяются гидкроксид-ионы! р. Н > 7
 Смещение протолитических равновесий Смещение протолитического равновесия, как любого другого химического равновесия, подчиняется принципу Ле-Шателье.
Смещение протолитических равновесий Смещение протолитического равновесия, как любого другого химического равновесия, подчиняется принципу Ле-Шателье.
 Влияние температуры определяется эндотермичностью реакций протолиза: Cr 3+·H 2 O + H 2 O ↔ Cr. OH 2+ + H 3 O+ ; ΔH = +52 к. Дж HF + H 2 O ↔ F- + H 3 O+ ; ΔH = +273 к. Дж SO 32 - + H 2 O ↔ HSO 3 - + OH- ; ΔH = +66 к. Дж При охлаждении раствора протолитические равновесия сдвигаются влево (в сторону реагентов), а при нагревании – вправо (в сторону продуктов). Последнее часто используется на практике для увеличения полноты протекания реакций протолиза. Иногда это приводит даже к полному разрушению равновесия: Fe 3+·H 2 O + 4 H 2 O = Fe. O(OH)(т) + 3 H 3 O+
Влияние температуры определяется эндотермичностью реакций протолиза: Cr 3+·H 2 O + H 2 O ↔ Cr. OH 2+ + H 3 O+ ; ΔH = +52 к. Дж HF + H 2 O ↔ F- + H 3 O+ ; ΔH = +273 к. Дж SO 32 - + H 2 O ↔ HSO 3 - + OH- ; ΔH = +66 к. Дж При охлаждении раствора протолитические равновесия сдвигаются влево (в сторону реагентов), а при нагревании – вправо (в сторону продуктов). Последнее часто используется на практике для увеличения полноты протекания реакций протолиза. Иногда это приводит даже к полному разрушению равновесия: Fe 3+·H 2 O + 4 H 2 O = Fe. O(OH)(т) + 3 H 3 O+
 Влияние концентрации растворенного вещества определяется тем, что вода – полноправный реагент протолитических реакций. При разбавлении раствора (уменьшении концентрации вещества) степень протолиза увеличивается, при концентрировании раствора – уменьшается. Иногда в сильно разбавленных растворах протолитическое равновесие разрушается: Bi 3+·H 2 O + 5 H 2 O(избыток) = Bi(OH)3(т) + 3 H 3 O+
Влияние концентрации растворенного вещества определяется тем, что вода – полноправный реагент протолитических реакций. При разбавлении раствора (уменьшении концентрации вещества) степень протолиза увеличивается, при концентрировании раствора – уменьшается. Иногда в сильно разбавленных растворах протолитическое равновесие разрушается: Bi 3+·H 2 O + 5 H 2 O(избыток) = Bi(OH)3(т) + 3 H 3 O+
 Влияние одноименного иона среды протолиза осуществляется введением избытка ионов H 3 O+ (при протолизе кислот) или OH- (при протолизе оснований). Это смещает протолитическое равновесие влево (избыток H 3 O+ создается прибавлением сильной кислоты HB, а избыток ионов OH- – прибавлением щелочи MOH): Fe 3+·H 2 O + H 2 O ↔ Fe. OH 2+ + H 3 O+ Бесцвет. желтый H 2 SO 4 + 2 H 2 O = SO 42 - + 2 H 3 O+
Влияние одноименного иона среды протолиза осуществляется введением избытка ионов H 3 O+ (при протолизе кислот) или OH- (при протолизе оснований). Это смещает протолитическое равновесие влево (избыток H 3 O+ создается прибавлением сильной кислоты HB, а избыток ионов OH- – прибавлением щелочи MOH): Fe 3+·H 2 O + H 2 O ↔ Fe. OH 2+ + H 3 O+ Бесцвет. желтый H 2 SO 4 + 2 H 2 O = SO 42 - + 2 H 3 O+


