7.Гидрокси.ppt
- Количество слайдов: 35
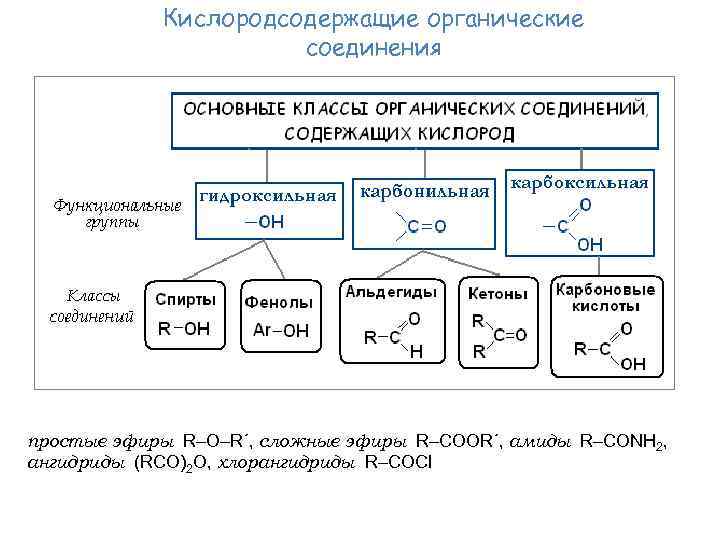 Кислородсодержащие органические соединения простые эфиры R O R´, сложные эфиры R COOR´, амиды R CONH 2, ангидриды (RCO)2 O, хлорангидриды R COCl
Кислородсодержащие органические соединения простые эфиры R O R´, сложные эфиры R COOR´, амиды R CONH 2, ангидриды (RCO)2 O, хлорангидриды R COCl
 К органическим гидроксисоединениям относятся соединения, содержащие одну или более гидроксильных групп –ОН, связанных с углеводородным радикалом. Классификация 1. В зависимости от гибридизации углеродного атома, с которым связана гидроксильная группа, эти соединения подразделяют на: спирты R–OH - соединения, содержащие одну или несколько гидроксильных групп, которые связаны с sp 3–гибридизованным углеродным атомом фенолы Ar–OH – соединения, в молекулах которых ОН-группы непосредственно связаны с ароматическим ядром 2. По числу гидроксильных групп гидроксисоединения подразделяются на: одноатомные (одна группа ОН), многоатомные (две и более групп ОН). Двухатомные вицинальные спирты (ОН-группы у соседних С-атомов) называют гликолями
К органическим гидроксисоединениям относятся соединения, содержащие одну или более гидроксильных групп –ОН, связанных с углеводородным радикалом. Классификация 1. В зависимости от гибридизации углеродного атома, с которым связана гидроксильная группа, эти соединения подразделяют на: спирты R–OH - соединения, содержащие одну или несколько гидроксильных групп, которые связаны с sp 3–гибридизованным углеродным атомом фенолы Ar–OH – соединения, в молекулах которых ОН-группы непосредственно связаны с ароматическим ядром 2. По числу гидроксильных групп гидроксисоединения подразделяются на: одноатомные (одна группа ОН), многоатомные (две и более групп ОН). Двухатомные вицинальные спирты (ОН-группы у соседних С-атомов) называют гликолями
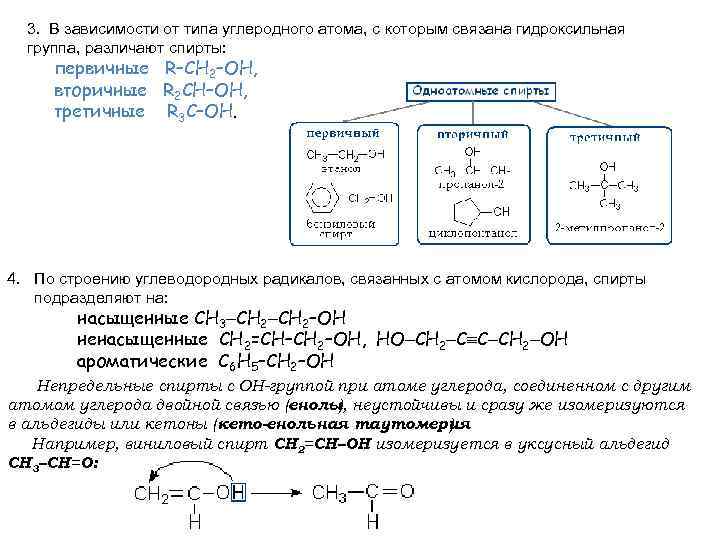 3. В зависимости от типа углеродного атома, с которым связана гидроксильная группа, различают спирты: первичные R–CH 2–OH, вторичные R 2 CH–OH, третичные R 3 C–OH. 4. По строению углеводородных радикалов, связанных с атомом кислорода, спирты подразделяют на: насыщенные СH 3 CH 2–OH ненасыщенные CH 2=CH–CH 2–OH, НО СН 2 С С СН 2 ОН ароматические C 6 H 5–CH 2–OH Непредельные спирты с ОН-группой при атоме углерода, соединенном с другим атомом углерода двойной связью (енолы неустойчивы и сразу же изомеризуются ), в альдегиды или кетоны (кето-енольная таутомерия ). Например, виниловый спирт CH 2=CH–OH изомеризуется в уксусный альдегид CH 3–CH=O:
3. В зависимости от типа углеродного атома, с которым связана гидроксильная группа, различают спирты: первичные R–CH 2–OH, вторичные R 2 CH–OH, третичные R 3 C–OH. 4. По строению углеводородных радикалов, связанных с атомом кислорода, спирты подразделяют на: насыщенные СH 3 CH 2–OH ненасыщенные CH 2=CH–CH 2–OH, НО СН 2 С С СН 2 ОН ароматические C 6 H 5–CH 2–OH Непредельные спирты с ОН-группой при атоме углерода, соединенном с другим атомом углерода двойной связью (енолы неустойчивы и сразу же изомеризуются ), в альдегиды или кетоны (кето-енольная таутомерия ). Например, виниловый спирт CH 2=CH–OH изомеризуется в уксусный альдегид CH 3–CH=O:
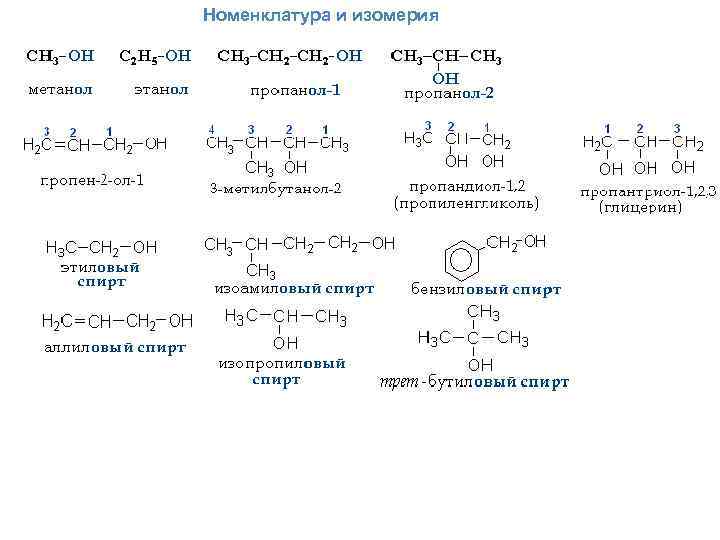 Номенклатура и изомерия
Номенклатура и изомерия

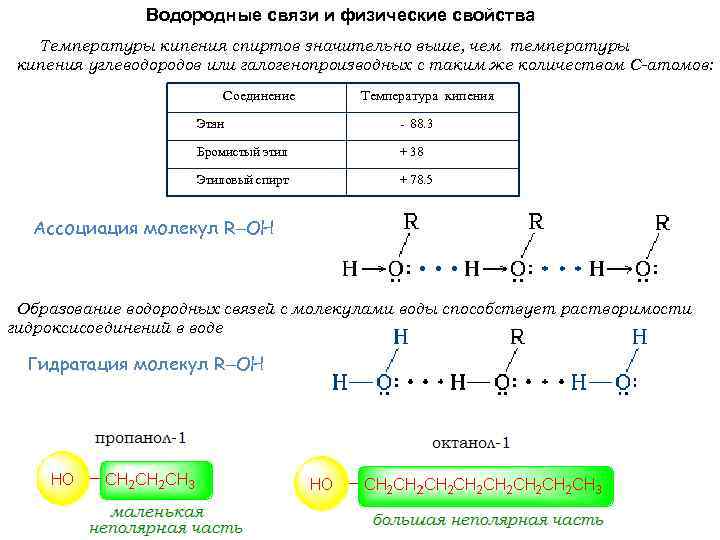 Водородные связи и физические свойства Температуры кипения спиртов значительно выше, чем температуры кипения углеводородов или галогенопроизводных с таким же количеством С-атомов: Соединение Температура кипения Этан - 88. 3 Бромистый этил + 38 Этиловый спирт + 78. 5 Ассоциация молекул R OH Образование водородных связей с молекулами воды способствует растворимости гидроксисоединений в воде Гидратация молекул R OH
Водородные связи и физические свойства Температуры кипения спиртов значительно выше, чем температуры кипения углеводородов или галогенопроизводных с таким же количеством С-атомов: Соединение Температура кипения Этан - 88. 3 Бромистый этил + 38 Этиловый спирт + 78. 5 Ассоциация молекул R OH Образование водородных связей с молекулами воды способствует растворимости гидроксисоединений в воде Гидратация молекул R OH
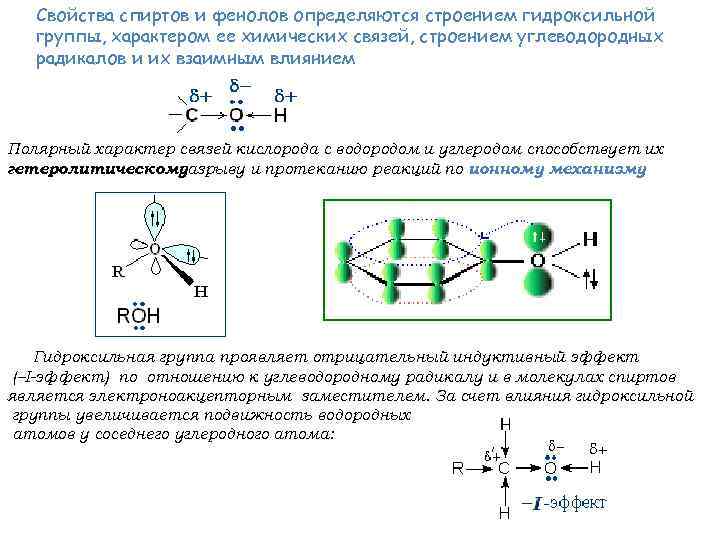 Свойства спиртов и фенолов определяются строением гидроксильной группы, характером ее химических связей, строением углеводородных радикалов и их взаимным влиянием Полярный характер связей кислорода с водородом и углеродом способствует их гетеролитическому разрыву и протеканию реакций по ионному механизму. Гидроксильная группа проявляет отрицательный индуктивный эффект ( I-эффект) по отношению к углеводородному радикалу и в молекулах спиртов является электроноакцепторным заместителем. За счет влияния гидроксильной группы увеличивается подвижность водородных атомов у соседнего углеродного атома:
Свойства спиртов и фенолов определяются строением гидроксильной группы, характером ее химических связей, строением углеводородных радикалов и их взаимным влиянием Полярный характер связей кислорода с водородом и углеродом способствует их гетеролитическому разрыву и протеканию реакций по ионному механизму. Гидроксильная группа проявляет отрицательный индуктивный эффект ( I-эффект) по отношению к углеводородному радикалу и в молекулах спиртов является электроноакцепторным заместителем. За счет влияния гидроксильной группы увеличивается подвижность водородных атомов у соседнего углеродного атома:
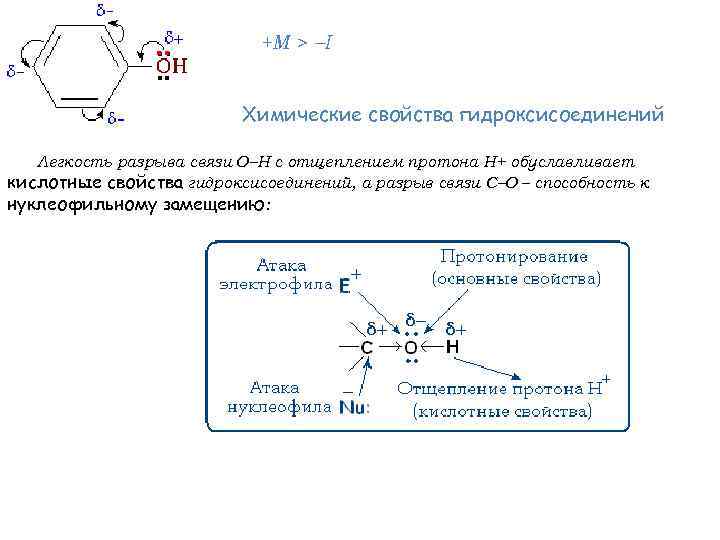 +M > I Химические свойства гидроксисоединений Легкость разрыва связи О–Н с отщеплением протона Н+ обуславливает кислотные свойства гидроксисоединений, а разрыв связи С–О – способность к нуклеофильному замещению:
+M > I Химические свойства гидроксисоединений Легкость разрыва связи О–Н с отщеплением протона Н+ обуславливает кислотные свойства гидроксисоединений, а разрыв связи С–О – способность к нуклеофильному замещению:
 Реакции с разрывом связи О–Н • реакции замещения атома водорода (протона) на металл (кислотные свойства); • реакции замещения атома водорода (протона) на остаток кислоты (ацилирование, образование сложных эфиров); • реакции отщепления водорода от кислорода и углерода (окисление и дегидрирование). 1. Кислотные свойства гидроксисоединений Одноатомные спирты реагируют с щелочными и щелочноземельными металлами, образуя соли алкоголяты (алкоксиды): С щелочами спирты алкоголятов не образуют! Кислотность одноатомных спиртов убывает в ряду: CH 3 OH > первичный > вторичный > третичный.
Реакции с разрывом связи О–Н • реакции замещения атома водорода (протона) на металл (кислотные свойства); • реакции замещения атома водорода (протона) на остаток кислоты (ацилирование, образование сложных эфиров); • реакции отщепления водорода от кислорода и углерода (окисление и дегидрирование). 1. Кислотные свойства гидроксисоединений Одноатомные спирты реагируют с щелочными и щелочноземельными металлами, образуя соли алкоголяты (алкоксиды): С щелочами спирты алкоголятов не образуют! Кислотность одноатомных спиртов убывает в ряду: CH 3 OH > первичный > вторичный > третичный.
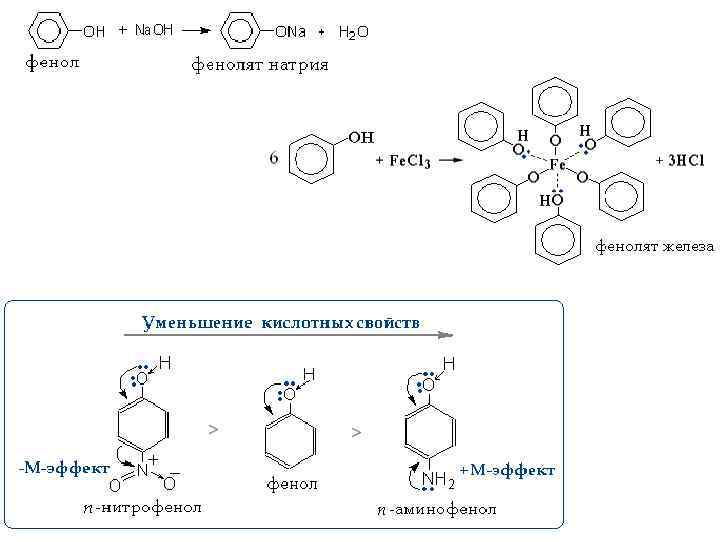
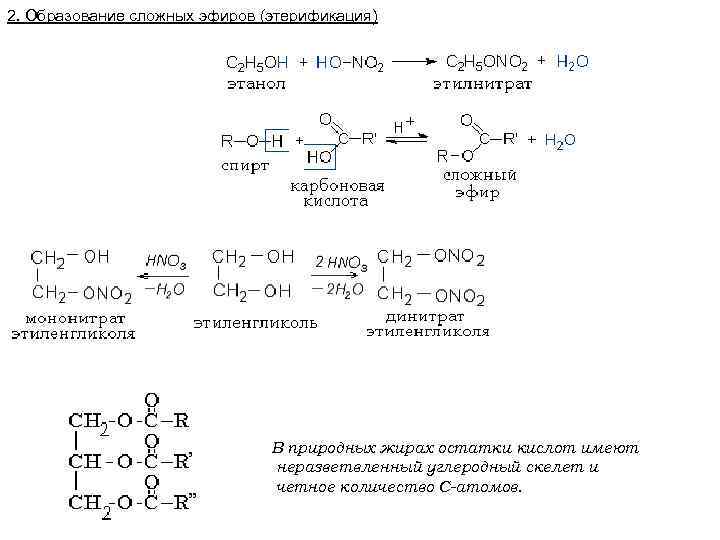 2. Образование сложных эфиров (этерификация) В природных жирах остатки кислот имеют неразветвленный углеродный скелет и четное количество С-атомов.
2. Образование сложных эфиров (этерификация) В природных жирах остатки кислот имеют неразветвленный углеродный скелет и четное количество С-атомов.
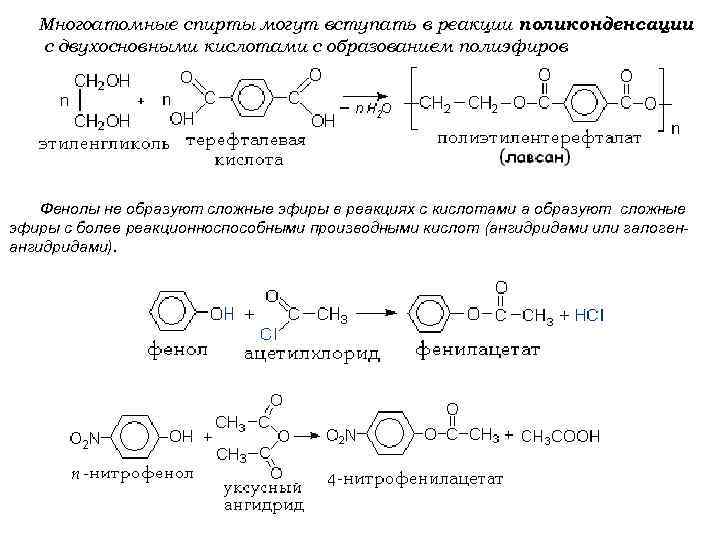 Многоатомные спирты могут вступать в реакции поликонденсации с двухосновными кислотами с образованием полиэфиров Фенолы не образуют сложные эфиры в реакциях с кислотами а образуют сложные эфиры с более реакционноспособными производными кислот (ангидридами или галогенангидридами).
Многоатомные спирты могут вступать в реакции поликонденсации с двухосновными кислотами с образованием полиэфиров Фенолы не образуют сложные эфиры в реакциях с кислотами а образуют сложные эфиры с более реакционноспособными производными кислот (ангидридами или галогенангидридами).
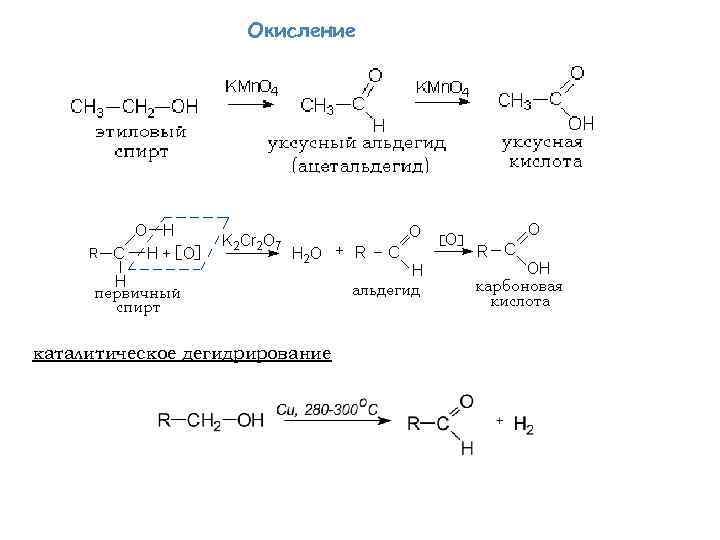 Окисление каталитическое дегидрирование
Окисление каталитическое дегидрирование
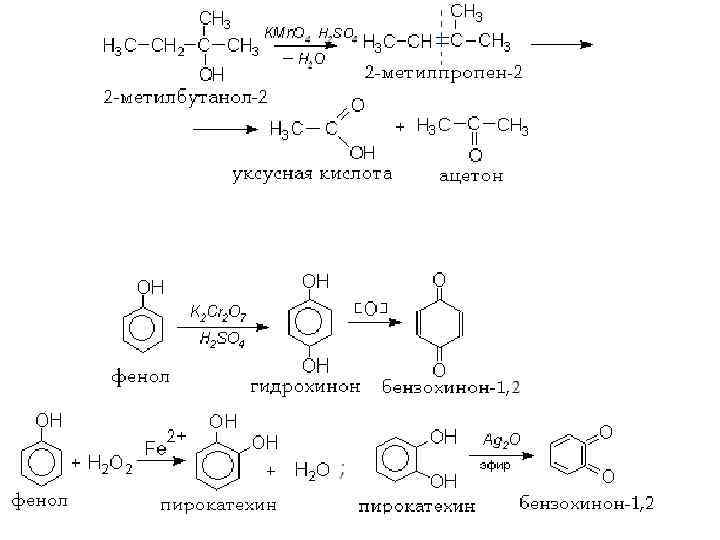
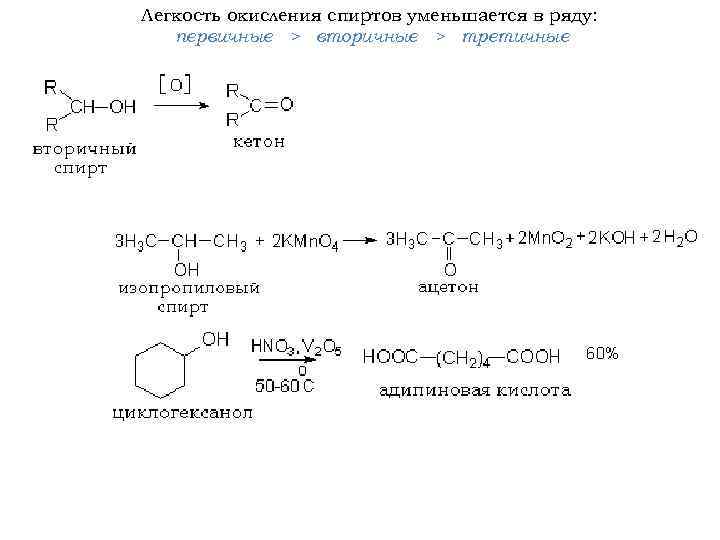 Легкость окисления спиртов уменьшается в ряду: первичные > вторичные > третичные
Легкость окисления спиртов уменьшается в ряду: первичные > вторичные > третичные
 Реакции с разрывом связи С–О • реакция замещения OH-группы на галоген или другую нуклеофильную группу (RO-, NH 2 - и т. п. ), идущая по механизму нуклеофильного замещения SN; • реакция отщепления (элиминирования) ОН и Н от соседних атомов углерода (внутримолекулярная дегидратация спиртов – образование алкенов); • реакция замещения группы ОН при разрыве связи С–О в одной молекуле и замещения атома Н с разрывом связи О–Н - в другой молекуле гидроксисоединения (межмолекулярная дегидратация – образование простых эфиров). Для фенолов реакции этого типа не характерны, поскольку атом кислорода прочно связан с атомом углерода бензольного кольца за счет сопряжения неподеленной электронной пары атома кислорода с ароматическим ядром (+М-эффект).
Реакции с разрывом связи С–О • реакция замещения OH-группы на галоген или другую нуклеофильную группу (RO-, NH 2 - и т. п. ), идущая по механизму нуклеофильного замещения SN; • реакция отщепления (элиминирования) ОН и Н от соседних атомов углерода (внутримолекулярная дегидратация спиртов – образование алкенов); • реакция замещения группы ОН при разрыве связи С–О в одной молекуле и замещения атома Н с разрывом связи О–Н - в другой молекуле гидроксисоединения (межмолекулярная дегидратация – образование простых эфиров). Для фенолов реакции этого типа не характерны, поскольку атом кислорода прочно связан с атомом углерода бензольного кольца за счет сопряжения неподеленной электронной пары атома кислорода с ароматическим ядром (+М-эффект).
 Реакции замещения ОН-группы - SN 1. Образование галогеноуглеводородов а) Реакции с галогеноводородами: Бензиловый спирт аллиловый спирт третичный спирт > > вторичный спирт > первичный спирт HI > HBr > HCl HF
Реакции замещения ОН-группы - SN 1. Образование галогеноуглеводородов а) Реакции с галогеноводородами: Бензиловый спирт аллиловый спирт третичный спирт > > вторичный спирт > первичный спирт HI > HBr > HCl HF
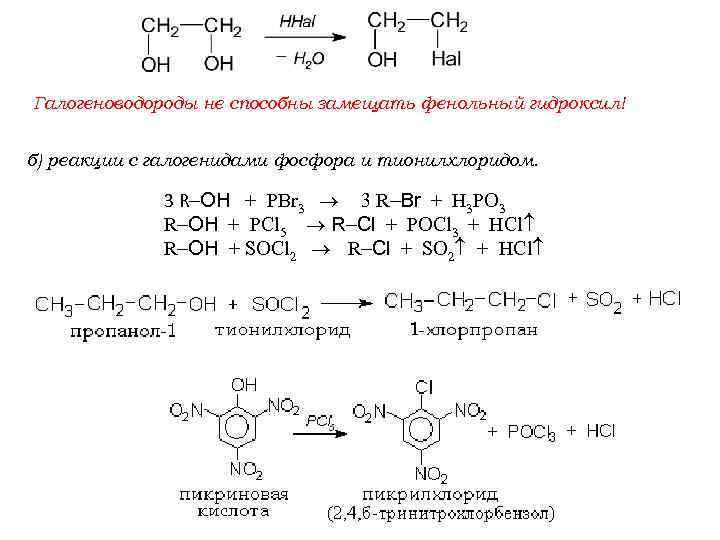 Галогеноводороды не способны замещать фенольный гидроксил! б) реакции с галогенидами фосфора и тионилхлоридом. 3 R OH + PBr 3 3 R Br + H 3 PO 3 R OH + PCl 5 R Cl + POCl 3 + HCl R OH + SOCl 2 R Cl + SO 2 + HСl
Галогеноводороды не способны замещать фенольный гидроксил! б) реакции с галогенидами фосфора и тионилхлоридом. 3 R OH + PBr 3 3 R Br + H 3 PO 3 R OH + PCl 5 R Cl + POCl 3 + HCl R OH + SOCl 2 R Cl + SO 2 + HСl
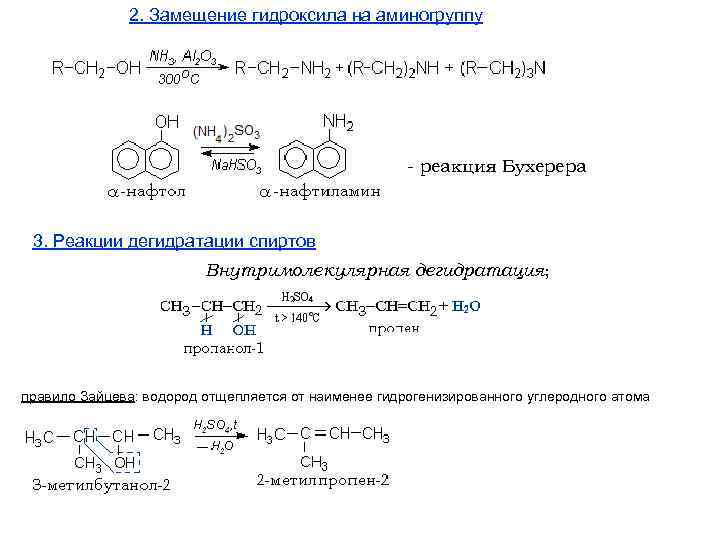 2. Замещение гидроксила на аминогруппу - реакция Бухерера 3. Реакции дегидратации спиртов Внутримолекулярная дегидратация; правило Зайцева: водород отщепляется от наименее гидрогенизированного углеродного атома
2. Замещение гидроксила на аминогруппу - реакция Бухерера 3. Реакции дегидратации спиртов Внутримолекулярная дегидратация; правило Зайцева: водород отщепляется от наименее гидрогенизированного углеродного атома
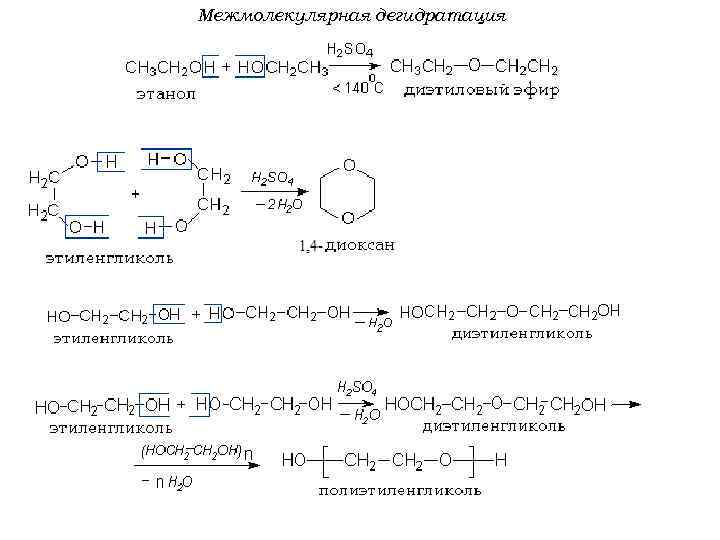 Межмолекулярная дегидратация
Межмолекулярная дегидратация
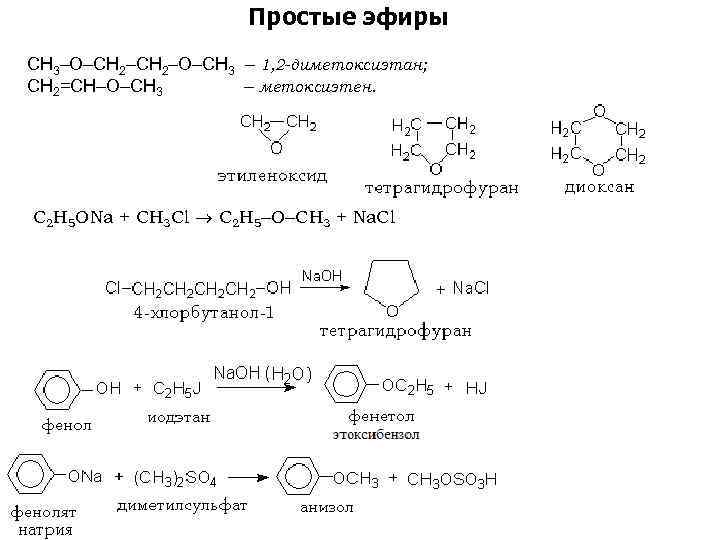 Простые эфиры СН 3 О СН 2 О СН 3 – 1, 2 -диметоксиэтан; СН 2=СН О СН 3 – метоксиэтен. C 2 H 5 ONa + CH 3 Cl C 2 H 5 O CH 3 + Na. Cl
Простые эфиры СН 3 О СН 2 О СН 3 – 1, 2 -диметоксиэтан; СН 2=СН О СН 3 – метоксиэтен. C 2 H 5 ONa + CH 3 Cl C 2 H 5 O CH 3 + Na. Cl
 Кислотное расщепление простых эфиров: Направление расщепления. Кислотное расщепление происходит селективно: если эфир содержит первичную и вторичную группу, то образуется вторичный спирт и первичный галогеналкан:
Кислотное расщепление простых эфиров: Направление расщепления. Кислотное расщепление происходит селективно: если эфир содержит первичную и вторичную группу, то образуется вторичный спирт и первичный галогеналкан:
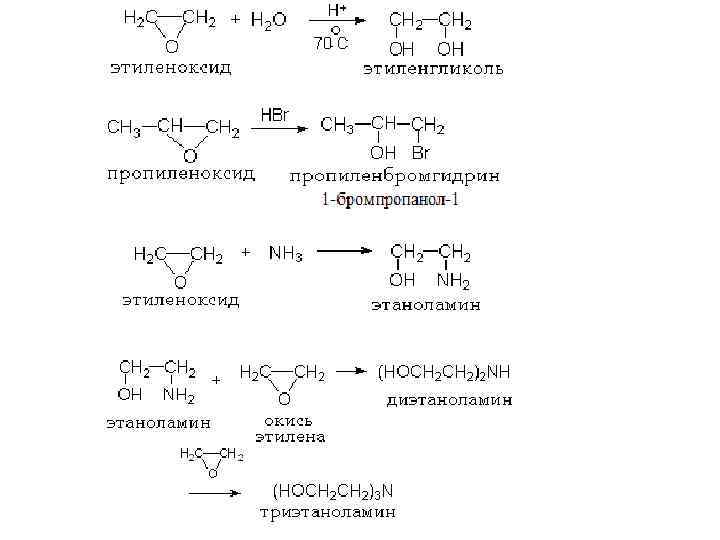
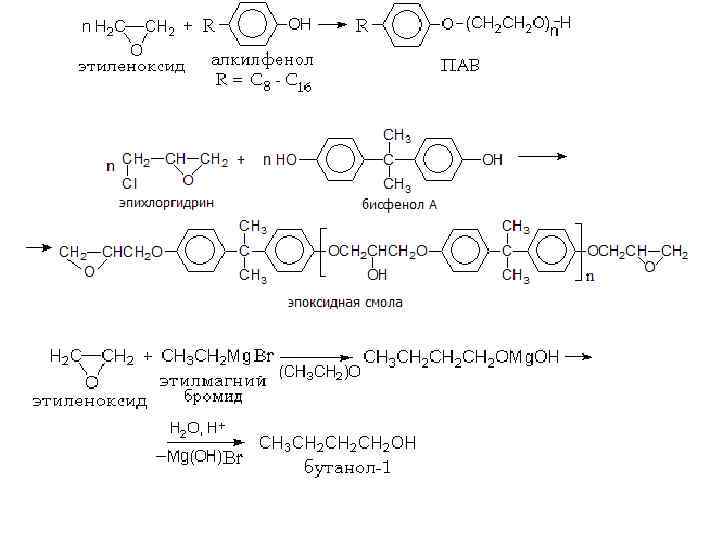
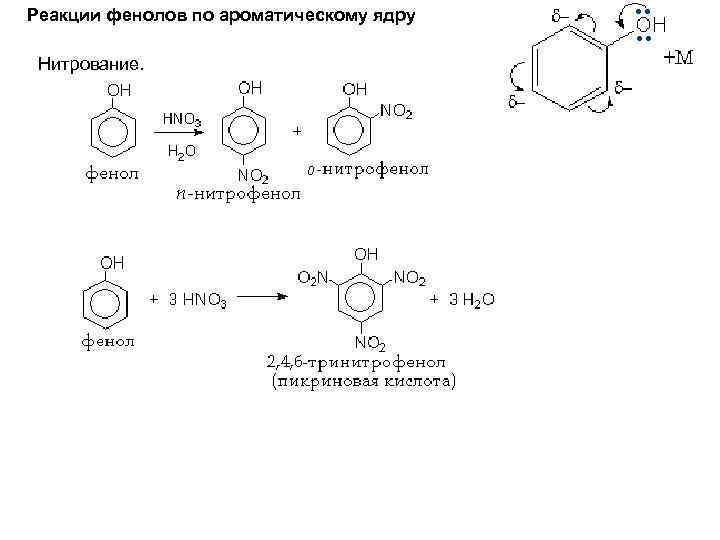 Реакции фенолов по ароматическому ядру Нитрование.
Реакции фенолов по ароматическому ядру Нитрование.
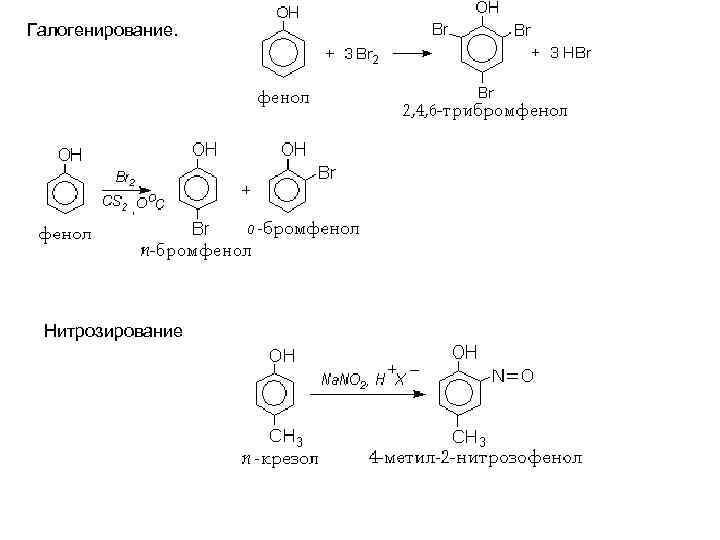 Галогенирование. Нитрозирование
Галогенирование. Нитрозирование
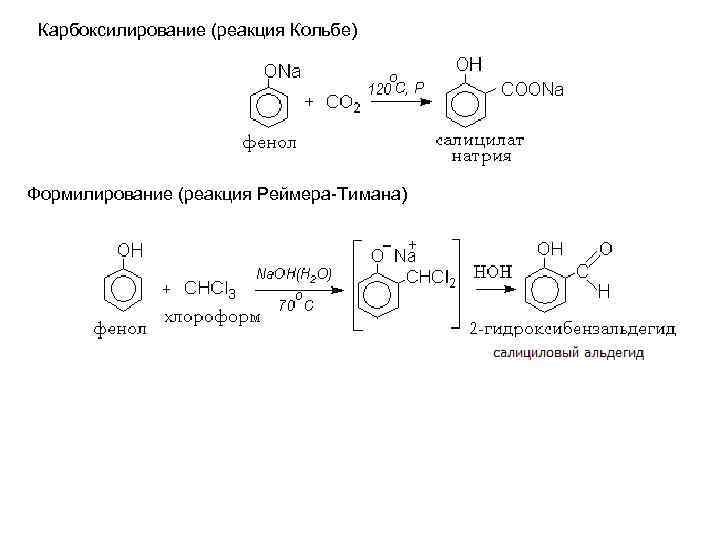 Карбоксилирование (реакция Кольбе) Формилирование (реакция Реймера-Тимана)
Карбоксилирование (реакция Кольбе) Формилирование (реакция Реймера-Тимана)
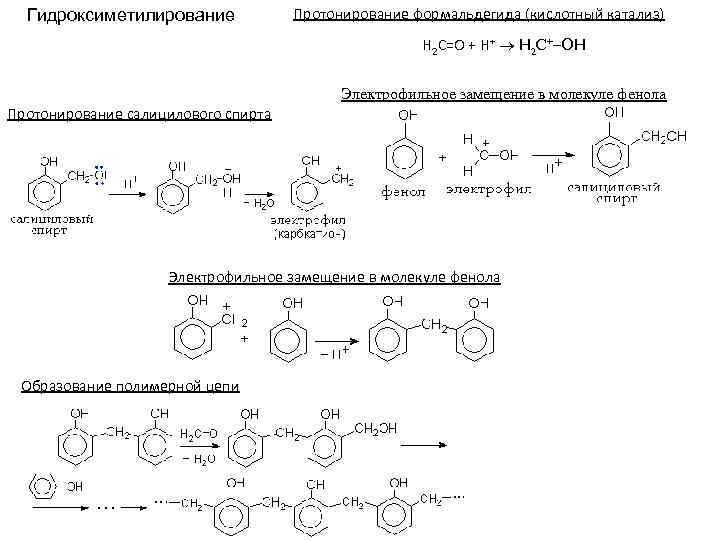 Гидроксиметилирование Протонирование формальдегида (кислотный катализ) Н 2 С=О + Н+ Н 2 С+ ОН Электрофильное замещение в молекуле фенола Протонирование салицилового спирта Электрофильное замещение в молекуле фенола Образование полимерной цепи
Гидроксиметилирование Протонирование формальдегида (кислотный катализ) Н 2 С=О + Н+ Н 2 С+ ОН Электрофильное замещение в молекуле фенола Протонирование салицилового спирта Электрофильное замещение в молекуле фенола Образование полимерной цепи
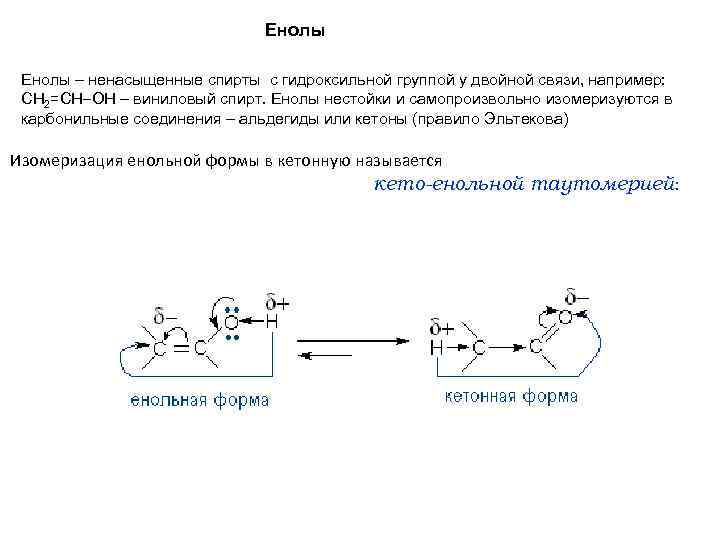 Енолы – ненасыщенные спирты с гидроксильной группой у двойной связи, например: СН 2=СН ОН – виниловый спирт. Енолы нестойки и самопроизвольно изомеризуются в карбонильные соединения – альдегиды или кетоны (правило Эльтекова) Изомеризация енольной формы в кетонную называется кето-енольной таутомерией:
Енолы – ненасыщенные спирты с гидроксильной группой у двойной связи, например: СН 2=СН ОН – виниловый спирт. Енолы нестойки и самопроизвольно изомеризуются в карбонильные соединения – альдегиды или кетоны (правило Эльтекова) Изомеризация енольной формы в кетонную называется кето-енольной таутомерией:
 Получение спиртов и фенолов 1. Щелочной гидролиз галогеноуглеводородов: 2. Гидратация алкенов (промышленный метод получения спиртов): Присоединение воды к несимметричным алкенам идет по правилу Марковникова с образованием вторичных или третичных спиртов:
Получение спиртов и фенолов 1. Щелочной гидролиз галогеноуглеводородов: 2. Гидратация алкенов (промышленный метод получения спиртов): Присоединение воды к несимметричным алкенам идет по правилу Марковникова с образованием вторичных или третичных спиртов:
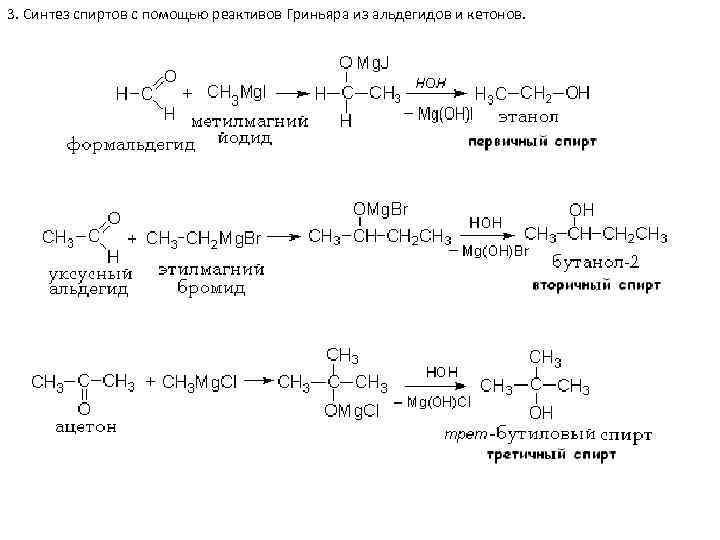 3. Синтез спиртов с помощью реактивов Гриньяра из альдегидов и кетонов.
3. Синтез спиртов с помощью реактивов Гриньяра из альдегидов и кетонов.
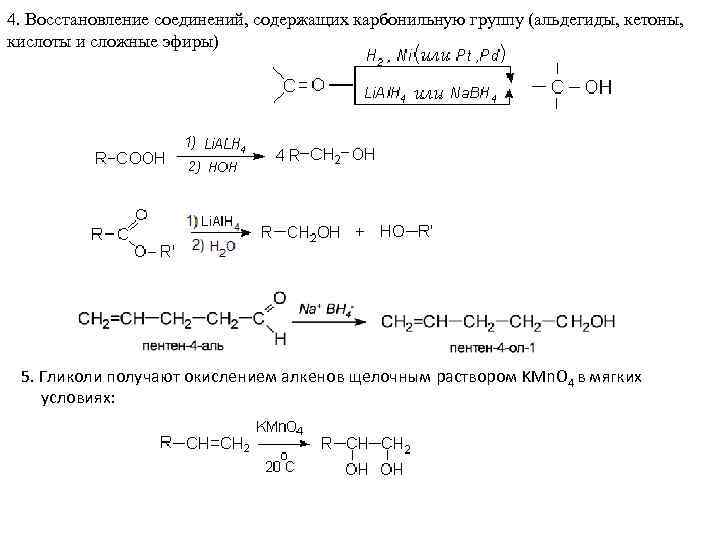 4. Восстановление соединений, содержащих карбонильную группу (альдегиды, кетоны, кислоты и сложные эфиры) 5. Гликоли получают окислением алкенов щелочным раствором KMn. O 4 в мягких условиях:
4. Восстановление соединений, содержащих карбонильную группу (альдегиды, кетоны, кислоты и сложные эфиры) 5. Гликоли получают окислением алкенов щелочным раствором KMn. O 4 в мягких условиях:
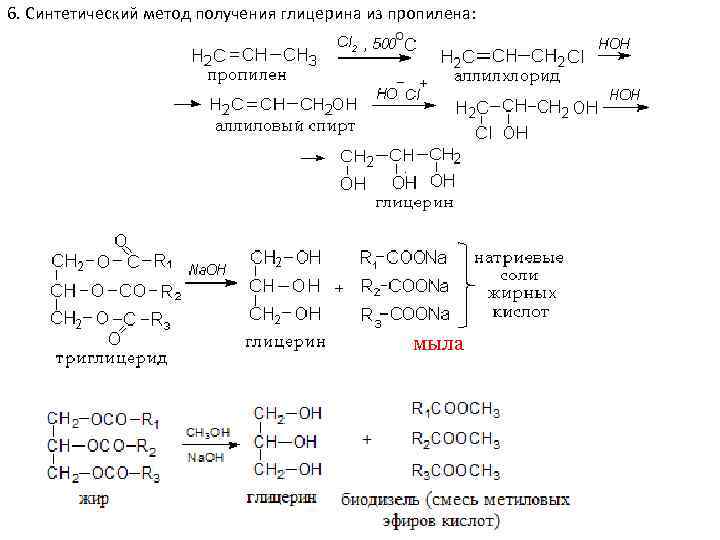 6. Синтетический метод получения глицерина из пропилена: мыла
6. Синтетический метод получения глицерина из пропилена: мыла
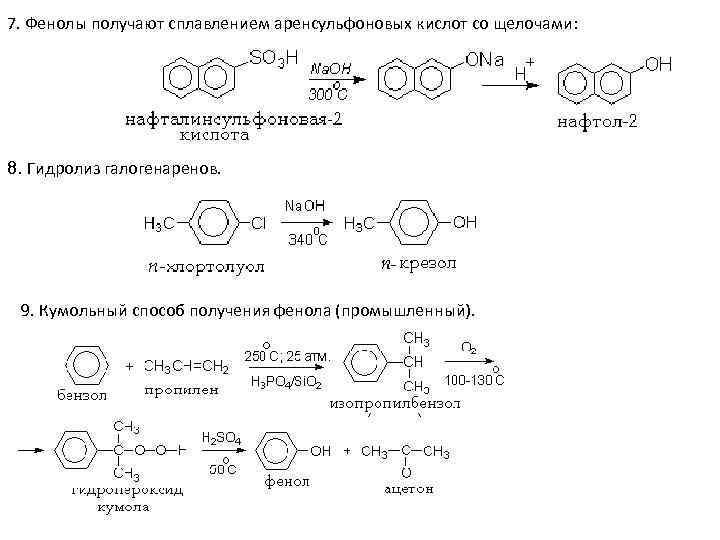 7. Фенолы получают сплавлением аренсульфоновых кислот со щелочами: 8. Гидролиз галогенаренов. 9. Кумольный способ получения фенола (промышленный).
7. Фенолы получают сплавлением аренсульфоновых кислот со щелочами: 8. Гидролиз галогенаренов. 9. Кумольный способ получения фенола (промышленный).



