кислород гаманькова 1.ppt
- Количество слайдов: 24
 Кислород Химия 9 класс Гаманькова ВА 1
Кислород Химия 9 класс Гаманькова ВА 1
 Открытие кислорода В 1771 году шведский химик и аптекарь Карл Вильгельм Шееле (1742 -1786) при нагреве Mn. O 2 с концентрированной серной кислотой наблюдал выделение "виртольного воздуха" – кислорода (O 2), который он также получил при прокаливании селитры. l В 1772 -1774 годах английский физик, философ и священник Джозеф Пристли (1733– 1804) получил кислород, независимо от Шееле, при прокаливании оксида ртути (Hg. O). l К таким же результатам пришел естествоиспытатель Байен. l В 1777 году французский химик Антуан Лоран Лавуазье (1743– 1794) объяснил процессы дыхания и горения и дал название кислороду – Oxygenium. l
Открытие кислорода В 1771 году шведский химик и аптекарь Карл Вильгельм Шееле (1742 -1786) при нагреве Mn. O 2 с концентрированной серной кислотой наблюдал выделение "виртольного воздуха" – кислорода (O 2), который он также получил при прокаливании селитры. l В 1772 -1774 годах английский физик, философ и священник Джозеф Пристли (1733– 1804) получил кислород, независимо от Шееле, при прокаливании оксида ртути (Hg. O). l К таким же результатам пришел естествоиспытатель Байен. l В 1777 году французский химик Антуан Лоран Лавуазье (1743– 1794) объяснил процессы дыхания и горения и дал название кислороду – Oxygenium. l
 Кислород как элемент. 1. Элемент кислород находится в VI группе, главной подгруппе, II периоде, порядковый номер № 8, Ar = 16. 2. Строение атома: +8 О ) ) 26 1 S 2 S 2 2 P 4 валентность II, степень окисления -2, 0 (редко +2; +1; -1). 3. Входит в состав оксидов, оснований, солей, кислот, органических веществ, в том числе живых организмов. 01. 02. 2018 3
Кислород как элемент. 1. Элемент кислород находится в VI группе, главной подгруппе, II периоде, порядковый номер № 8, Ar = 16. 2. Строение атома: +8 О ) ) 26 1 S 2 S 2 2 P 4 валентность II, степень окисления -2, 0 (редко +2; +1; -1). 3. Входит в состав оксидов, оснований, солей, кислот, органических веществ, в том числе живых организмов. 01. 02. 2018 3
 Кислород как элемент (продолжение). 4. В земной коре его 49%, в воде – 89%. 5. В составе воздуха (в виде простого вещества) – 20 -21% по объёму. Состав воздуха: О 2 – 20 -21 %; N 2 – 78%; CO 2 – 0, 03%, остальное приходится на инертные газы, пары воды, примеси. Кислород имеет три устойчивых изотопа: 16, 17 и 18 Дополнительно … Кислород является самым распространённым элементом нашей планеты. По весу на его долю приходится примерно половина общей массы всех элементов земной коры. 01. 02. 2018 4
Кислород как элемент (продолжение). 4. В земной коре его 49%, в воде – 89%. 5. В составе воздуха (в виде простого вещества) – 20 -21% по объёму. Состав воздуха: О 2 – 20 -21 %; N 2 – 78%; CO 2 – 0, 03%, остальное приходится на инертные газы, пары воды, примеси. Кислород имеет три устойчивых изотопа: 16, 17 и 18 Дополнительно … Кислород является самым распространённым элементом нашей планеты. По весу на его долю приходится примерно половина общей массы всех элементов земной коры. 01. 02. 2018 4
 Кислород как простое вещество l молекула О 2 двухатомная l Химическая связь ковалентная неполярная, двойная (сигма и пи связь) l Молекула неполярная
Кислород как простое вещество l молекула О 2 двухатомная l Химическая связь ковалентная неполярная, двойная (сигма и пи связь) l Молекула неполярная
 Способы получения и собирания Кислород в природе образуется в кислорода. процессе фотосинтеза. В промышленности его получают перегонкой сжиженного воздуха при t = - 200 С. Кислород t кипения = - 1830 С. Азот t кипения = - 1950 С. В лаборатории кислород получают реакциями разложения: а) воды под действием электрического тока (электролиз): 2 H 2 O → 2 H 2 + O 2 б) пероксида водорода под действием Mn. O 2 : Mn. O 2 01. 02. 2018 2 Н 2 О 2 → 2 Н 2 О + О 2 6
Способы получения и собирания Кислород в природе образуется в кислорода. процессе фотосинтеза. В промышленности его получают перегонкой сжиженного воздуха при t = - 200 С. Кислород t кипения = - 1830 С. Азот t кипения = - 1950 С. В лаборатории кислород получают реакциями разложения: а) воды под действием электрического тока (электролиз): 2 H 2 O → 2 H 2 + O 2 б) пероксида водорода под действием Mn. O 2 : Mn. O 2 01. 02. 2018 2 Н 2 О 2 → 2 Н 2 О + О 2 6
 ! Катализатор – вещество, изменяющее скорость реакции, но само при этом не расходующееся. разложение перманганата калия 2 KMn. O 4 → K 2 Mn. O 4 + Mn. O 2 + O 2 условие (200° C) l разложение бертолетовой соли 2 KCl. O 3 → 2 KCl + 3 O 2 , условия(150° C, Mn. O 2) l l KCl. O 4 → KCl + 2 O 2 , l 2 KNO 3 → 2 KNO 2 + O 2 , условие(500° C) условие(t ) Подумайте … Как проверить, собрался ли кислород в сосуде? 01. 02. 2018 7
! Катализатор – вещество, изменяющее скорость реакции, но само при этом не расходующееся. разложение перманганата калия 2 KMn. O 4 → K 2 Mn. O 4 + Mn. O 2 + O 2 условие (200° C) l разложение бертолетовой соли 2 KCl. O 3 → 2 KCl + 3 O 2 , условия(150° C, Mn. O 2) l l KCl. O 4 → KCl + 2 O 2 , l 2 KNO 3 → 2 KNO 2 + O 2 , условие(500° C) условие(t ) Подумайте … Как проверить, собрался ли кислород в сосуде? 01. 02. 2018 7
 Опыты получения кислорода. 01. 02. 2018 8
Опыты получения кислорода. 01. 02. 2018 8
 Проверка собравшегося кислорода 01. 02. 2018 9
Проверка собравшегося кислорода 01. 02. 2018 9
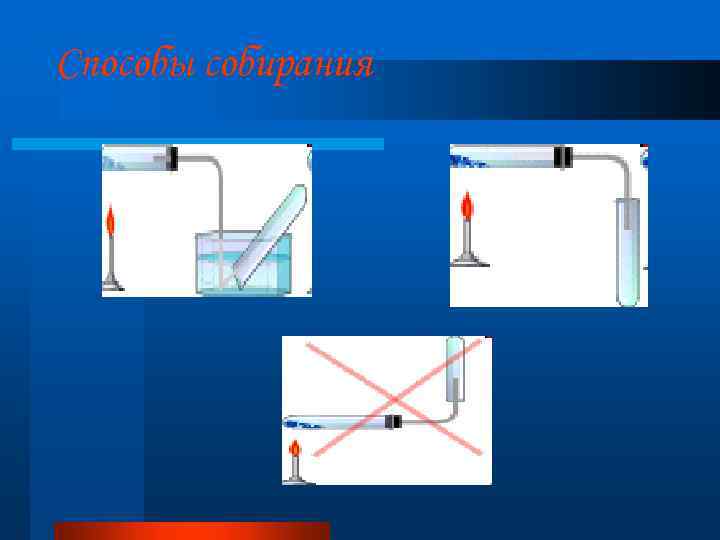 Способы собирания
Способы собирания
 Физические свойства кислорода. • газ без цвета и запаха • в свободном виде встречается в виде двух аллотропных модификаций О 2 ( «обычный» кислород) и О 3 (озон). • Температура кипения жидкого кислорода (жидкость имеет голубой цвет) равна – 182, 9°C • Малорастворим в воде • Тяжелее воздуха 01. 02. 2018 11
Физические свойства кислорода. • газ без цвета и запаха • в свободном виде встречается в виде двух аллотропных модификаций О 2 ( «обычный» кислород) и О 3 (озон). • Температура кипения жидкого кислорода (жидкость имеет голубой цвет) равна – 182, 9°C • Малорастворим в воде • Тяжелее воздуха 01. 02. 2018 11
 Химические свойства кислорода l Высокая прочность химической связи между атомами в молекуле О 2 приводит к тому, что при комнатной температуре кислород химически довольно малоактивен. l обладает высокой электроотрицательностью; l в реакциях выступает окислителем; l поддерживает процессы горения и медленного окисления, к которым относится, например, дыхание. Подумайте … Горение – это окисление, идущее с выделением тепла и света. Каковы условия горения? 01. 02. 2018 12
Химические свойства кислорода l Высокая прочность химической связи между атомами в молекуле О 2 приводит к тому, что при комнатной температуре кислород химически довольно малоактивен. l обладает высокой электроотрицательностью; l в реакциях выступает окислителем; l поддерживает процессы горения и медленного окисления, к которым относится, например, дыхание. Подумайте … Горение – это окисление, идущее с выделением тепла и света. Каковы условия горения? 01. 02. 2018 12
 Со многими веществами кислород вступает во взаимодействие без нагревания, например, со щелочными и щелочноземельными металлами (образуются соответствующие оксиды типа Li 2 O, Ca. O и др. , l пероксиды типа Na 2 O 2, Ba. O 2 и др. и супероксиды типа КО 2, Rb. O 2 и др. ), l вызывает образование ржавчины на поверхности стальных изделий. l l 4 Fe + 3 O 2 = 2 Fe 2 O 3 3 Fe + 2 O 2 = Fe 3 O 4 (или Fe. O× Fe 2 O 3) Железная окалина l 2 Cu + O 2 = 2 Cu. O l l Не взаимодействует с золотом и платиной
Со многими веществами кислород вступает во взаимодействие без нагревания, например, со щелочными и щелочноземельными металлами (образуются соответствующие оксиды типа Li 2 O, Ca. O и др. , l пероксиды типа Na 2 O 2, Ba. O 2 и др. и супероксиды типа КО 2, Rb. O 2 и др. ), l вызывает образование ржавчины на поверхности стальных изделий. l l 4 Fe + 3 O 2 = 2 Fe 2 O 3 3 Fe + 2 O 2 = Fe 3 O 4 (или Fe. O× Fe 2 O 3) Железная окалина l 2 Cu + O 2 = 2 Cu. O l l Не взаимодействует с золотом и платиной
 Известно, что железо на воздухе ржавеет, особенно в воде, при высокой влажности. Эта реакция родственна горению железа в кислороде, хотя протекает гораздо медленнее: l 4 Fe + 3 O 2 + 2 n. H 2 O = 2 Fe 2 O 3× n. H 2 O (ржавчина – гидрат оксида железа III) l Ржавление металлов называется коррозией. Коррозия причиняет колоссальный вред человеческой цивилизации. l
Известно, что железо на воздухе ржавеет, особенно в воде, при высокой влажности. Эта реакция родственна горению железа в кислороде, хотя протекает гораздо медленнее: l 4 Fe + 3 O 2 + 2 n. H 2 O = 2 Fe 2 O 3× n. H 2 O (ржавчина – гидрат оксида железа III) l Ржавление металлов называется коррозией. Коррозия причиняет колоссальный вред человеческой цивилизации. l
 l l l l l Взаимодействие с неметаллами при горении неметаллов образуются оксиды, как правило, высших степеней окисления, при сгорании в недостатке кислорода – оксиды низших степеней окисления. S + O 2 = SO 2. 250°С 4 Р + 5 О 2 = 2 Р 2 О 5 60 ° С белый фосфор без нагревания С + О 2 = СО 2. 700 -800 °С 2 Н 2 + О 2 = 2 Н 2 О. 300 °С N 2 + O 2 = 2 NO (около 1500 -2000°C) Из неметаллов кислород напрямую ни при каких условиях не взаимодействует с галогенами
l l l l l Взаимодействие с неметаллами при горении неметаллов образуются оксиды, как правило, высших степеней окисления, при сгорании в недостатке кислорода – оксиды низших степеней окисления. S + O 2 = SO 2. 250°С 4 Р + 5 О 2 = 2 Р 2 О 5 60 ° С белый фосфор без нагревания С + О 2 = СО 2. 700 -800 °С 2 Н 2 + О 2 = 2 Н 2 О. 300 °С N 2 + O 2 = 2 NO (около 1500 -2000°C) Из неметаллов кислород напрямую ни при каких условиях не взаимодействует с галогенами
 Взаимодействие со сложными веществами l В этом случае образуются оксиды элементов, из которых состоит молекула сложного вещества. l l 4 NH 3 + 3 O 2 = 2 N 2 + 6 H 2 O; NH 3 + O 2 = NO + H 2 O ( с катализатором) l l PH 3 + O 2 = P 2 O 5 + H 2 O 2 H 2 S + 3 O 2 = 2 H 2 O + 2 SO 2 l 2 Cu. S + 3 O 2 = 2 Cu. O + 2 SO 2; l СН 4 + 2 О 2 = СО 2 + 2 Н 2 О. l 4 Fe. S 2 + 11 O 2 = 2 Fe 2 O 3 + 8 SO 2 пирит
Взаимодействие со сложными веществами l В этом случае образуются оксиды элементов, из которых состоит молекула сложного вещества. l l 4 NH 3 + 3 O 2 = 2 N 2 + 6 H 2 O; NH 3 + O 2 = NO + H 2 O ( с катализатором) l l PH 3 + O 2 = P 2 O 5 + H 2 O 2 H 2 S + 3 O 2 = 2 H 2 O + 2 SO 2 l 2 Cu. S + 3 O 2 = 2 Cu. O + 2 SO 2; l СН 4 + 2 О 2 = СО 2 + 2 Н 2 О. l 4 Fe. S 2 + 11 O 2 = 2 Fe 2 O 3 + 8 SO 2 пирит
 Доокисление сложных веществ l P 2 O 3 + O 2 = P 2 O 5 l O 2 + 4 Fe(OH)2 + 2 H 2 O = 4 Fe(OH)3, l O 2 + 4 Cr(OH)2 + 2 H 2 O = 4 Cr(OH)3. l 2 NO + О 2 = 2 NO 2 l 2 SO 2 + O 2 = 2 SO 3 l 2 Na 2 SO 3 + O 2 = 2 Na 2 SO 4 l Только, если окисляемый элемент находится в средней степени окисления
Доокисление сложных веществ l P 2 O 3 + O 2 = P 2 O 5 l O 2 + 4 Fe(OH)2 + 2 H 2 O = 4 Fe(OH)3, l O 2 + 4 Cr(OH)2 + 2 H 2 O = 4 Cr(OH)3. l 2 NO + О 2 = 2 NO 2 l 2 SO 2 + O 2 = 2 SO 3 l 2 Na 2 SO 3 + O 2 = 2 Na 2 SO 4 l Только, если окисляемый элемент находится в средней степени окисления
 Применение кислорода: l l l 01. 02. 2018 Находит широкое применение в медицине и промышленности. При высотных полётах лётчиков снабжают специальными приборами с кислородом. При многих лёгочных и сердечных заболеваниях, а также при операциях дают вдыхать кислород из кислородных подушек. Кислородом в баллонах снабжают подводные лодки. Горение рыхлого горючего материала, пропитанного жидким кислородом, сопровождается взрывом, что даёт возможность применять кислород при взрывных работах. Жидкий кислород применяют в реактивных двигателях, в автогенной сварке и резке металлов, даже под водой. его смеси с угольным порошком, древесной мукой или другими горючими веществами называются оксиликвитами и обладают большой взрывной силой. 18
Применение кислорода: l l l 01. 02. 2018 Находит широкое применение в медицине и промышленности. При высотных полётах лётчиков снабжают специальными приборами с кислородом. При многих лёгочных и сердечных заболеваниях, а также при операциях дают вдыхать кислород из кислородных подушек. Кислородом в баллонах снабжают подводные лодки. Горение рыхлого горючего материала, пропитанного жидким кислородом, сопровождается взрывом, что даёт возможность применять кислород при взрывных работах. Жидкий кислород применяют в реактивных двигателях, в автогенной сварке и резке металлов, даже под водой. его смеси с угольным порошком, древесной мукой или другими горючими веществами называются оксиликвитами и обладают большой взрывной силой. 18
 Озон (O 3). l В 1840 году немецкий химик Кристиан Фридрих Шенбейн (1799 -1868) открыл озон. l l Озон образуется в атмосфере при электрических разрядах. Озоновый слой в стратосфере толщиной в несколько сантиметров поглощает ультрафиолетовое излучение. l Физические свойства озона. Озон представляет собой газ светло-синего цвета, с характерным резким запахом, растворимый в воде. Жидкий озон имеет темно-фиолетовый цвет, а твердый сине-черный. Ядовит. l Применение озона. Озон применяют для дезинфекции воды и в медицине, для отбеливания тканей и очистки некоторых соединений, для идентификации соединений.
Озон (O 3). l В 1840 году немецкий химик Кристиан Фридрих Шенбейн (1799 -1868) открыл озон. l l Озон образуется в атмосфере при электрических разрядах. Озоновый слой в стратосфере толщиной в несколько сантиметров поглощает ультрафиолетовое излучение. l Физические свойства озона. Озон представляет собой газ светло-синего цвета, с характерным резким запахом, растворимый в воде. Жидкий озон имеет темно-фиолетовый цвет, а твердый сине-черный. Ядовит. l Применение озона. Озон применяют для дезинфекции воды и в медицине, для отбеливания тканей и очистки некоторых соединений, для идентификации соединений.
 l 1. Озон является сильнейшим окислителем, окисляет даже золото и платину, и уступает только фтору и фториду кислорода. l 2 KI + O 3 + H 2 O = l Pb. S + 2 O 3 = Pb. SO 4 + O 2. I 2 + 2 KOH + O 2. При приливании к озону аммиака образуется белый дым нитрита аммония. l Озон способен чернить серебро, переводя металл в оксид. l l 3 SO 2 + O 3 = 3 SO 3, l Na 2 S + O 3 = Na 2 SO 3.
l 1. Озон является сильнейшим окислителем, окисляет даже золото и платину, и уступает только фтору и фториду кислорода. l 2 KI + O 3 + H 2 O = l Pb. S + 2 O 3 = Pb. SO 4 + O 2. I 2 + 2 KOH + O 2. При приливании к озону аммиака образуется белый дым нитрита аммония. l Озон способен чернить серебро, переводя металл в оксид. l l 3 SO 2 + O 3 = 3 SO 3, l Na 2 S + O 3 = Na 2 SO 3.
 Интересные факты Токсичность озона (О 3) проявляется в результате его действия на дыхательную систему человека и животных. Озон обладает высокой химической активностью, для проявления его токсического действия достаточно минимальных концентраций. Он является почти идеальным боевым отравляющим веществом, и только по причине трудности его получения он не оказался в числе примененных боевых газов в период Первой мировой войны. l К числу его недостатков военные относят резкий запах. l
Интересные факты Токсичность озона (О 3) проявляется в результате его действия на дыхательную систему человека и животных. Озон обладает высокой химической активностью, для проявления его токсического действия достаточно минимальных концентраций. Он является почти идеальным боевым отравляющим веществом, и только по причине трудности его получения он не оказался в числе примененных боевых газов в период Первой мировой войны. l К числу его недостатков военные относят резкий запах. l
 Допиши химические реакции: Ca + O 2 → Na + O 2 → Al + O 2 → S + O 2 → Cu. O + O 2 → Fe. O + O 2 → 01. 02. 2018 22
Допиши химические реакции: Ca + O 2 → Na + O 2 → Al + O 2 → S + O 2 → Cu. O + O 2 → Fe. O + O 2 → 01. 02. 2018 22
 l Как погасить горящую древесину? l Загоревшуюся на человеке одежду? l Горящую на поверхности воды нефть? 01. 02. 2018 23
l Как погасить горящую древесину? l Загоревшуюся на человеке одежду? l Горящую на поверхности воды нефть? 01. 02. 2018 23
 Нельзя тушить водой горючие жидкости и легковоспламеняющиеся жидкости, электроустановки под напряжением, разливы нефтепродуктов химические вещества, которые вступают в реакцию при взаимодействии с водой. l Для тушения ЛВЖ и ГЖ, горящих нефтепродуктов применяют огнетушители - порошковые, пенные, углекислотные, в зависимости от горящего продукта, песок. Электроустановки тушат кошмой (асбестовым одеялом). l водой заливать нельзя вещества которые реагируют с водой, например карбид кальция( т. к. при взаимодействии с водой выделяет горючий газ) l Все вещества, которые легче воды (например, нефть). Поскольку горение - это химическая реакция с участием кислорода (воздуха), их гасят, лишая доступ воздуха (обычно с помощью пены) l
Нельзя тушить водой горючие жидкости и легковоспламеняющиеся жидкости, электроустановки под напряжением, разливы нефтепродуктов химические вещества, которые вступают в реакцию при взаимодействии с водой. l Для тушения ЛВЖ и ГЖ, горящих нефтепродуктов применяют огнетушители - порошковые, пенные, углекислотные, в зависимости от горящего продукта, песок. Электроустановки тушат кошмой (асбестовым одеялом). l водой заливать нельзя вещества которые реагируют с водой, например карбид кальция( т. к. при взаимодействии с водой выделяет горючий газ) l Все вещества, которые легче воды (например, нефть). Поскольку горение - это химическая реакция с участием кислорода (воздуха), их гасят, лишая доступ воздуха (обычно с помощью пены) l


