Общие пути обмена аминокислот 17.ppt
- Количество слайдов: 56

Кировский государственный медицинский университет ОБЩИЕ ПУТИ ОБМЕНА АМИНОКИСЛОТ. КОНЕЧНЫЕ ПРОДУКТЫ АЗОТИСТОГО ОБМЕНА.

Значение белков. Функции. • • Ферментативная Гормональная (инсулин) Рецепторная Транспортная Структурная (мембраны) Опорная (коллаген, эластин) Трофическая (овоальбумин) Энергетическая (17. 1 к. Дж – 1 г)

Значение белков. Функции • • Механохимическая (актин, миозин) Электроосмотическая (Na, K-АТФ-аза) Энерготрансформаторная (АТФ-синтаза) Когенетическая Генно-регуляторная Иммунологическая Обезвреживающая Гемостатическая (фибриноген и белки сверт. крови)

Источники и пути использования аминокислот • Аминокислоты - 30 г. • В крови - 35 - 65 мг/дл. • Белки - 15 кг

Питание
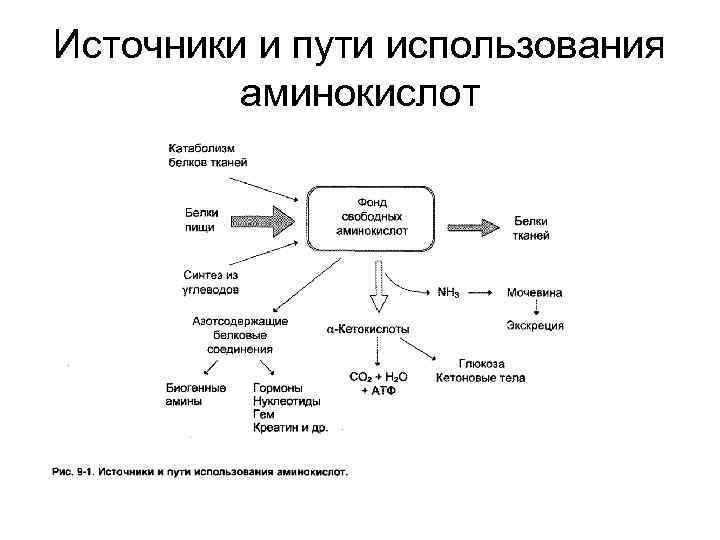
Источники и пути использования аминокислот
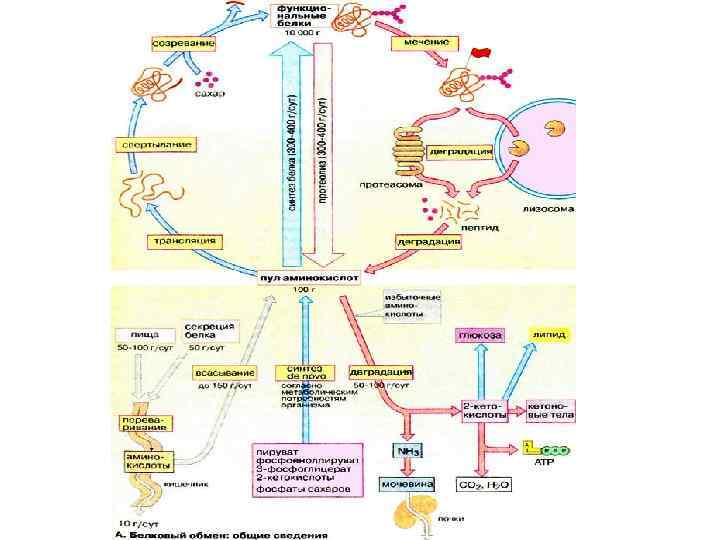

Азотистый баланс Метаболизм азота связан с обменом АК и в норме сбалансирован. Азотистое равновесие - количества поступающего и выделяемого белкового N 2 равны. Положительный баланс – выделяется только часть вновь поступающего N 2 (рост организма). Отрицательный баланс - выделяется N 2 больше, чем поступает (следствие заболеваний).

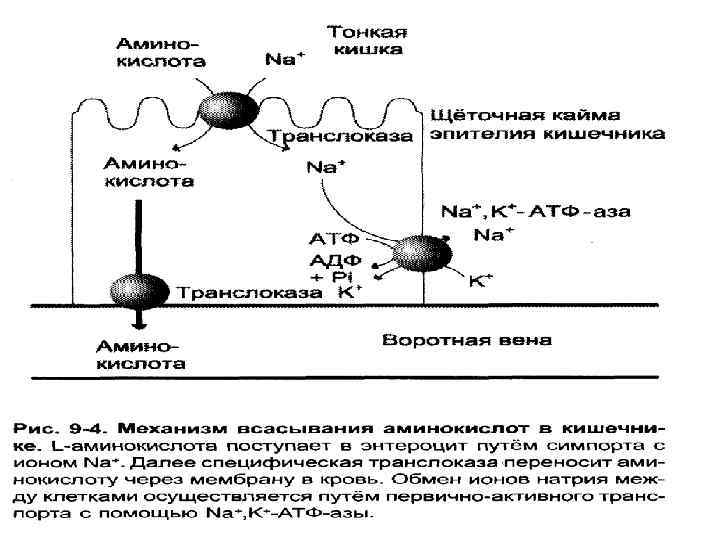
• Полученные с пищей белки подвергаются полному гидролизу в ЖКТ до АК, которые всасываются и распределяются в организме. • 8 из 20 протеиногенных АК у человека незаменимые АК.

НЕЗАМЕНИМЫЕ АК Val, Leu, Ile, Tre, Lys, Met, Phe, Trp

Общие пути обмена АК • • ДЕЗАМИНИРОВАНИЕ ТРАНСАМИНИРОВАНИЕ ДЕКАРБОКСИЛИРОВАНИЕ БИОСИНТЕЗ ЗАМЕНИМЫХ АМИНОКИСЛОТ

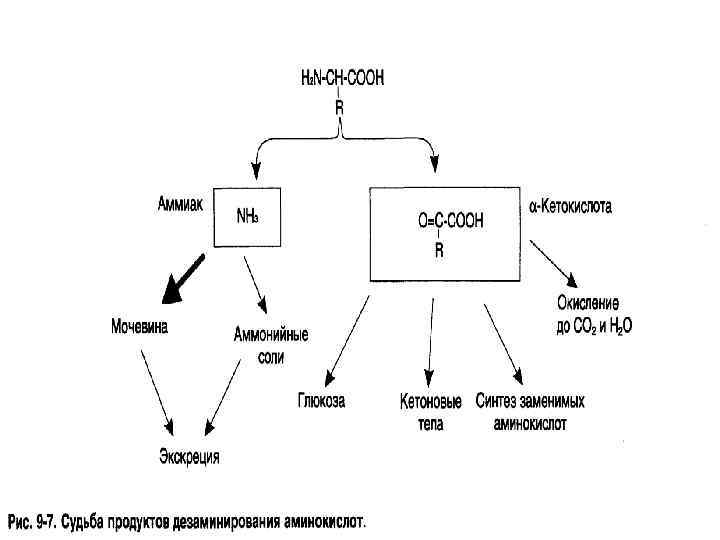
ДЕЗАМИНИРОВАНИЕ • Элиминация от АК NH 2 -группы в виде аммиака. Реакция протекает по различным механизмам.

• • • 4 вида дезаминирования: - ВОССТАНОВИТЕЛЬНОЕ - ГИДРОЛИТИЧЕСКОЕ - ОКИСЛИТЕЛЬНОЕ - ВНУТРИМОЛЕКУЛЯРНОЕ (ЭЛИМИНИРУЮЩЕЕ).

Химизм окислительного дезаминирования • Окислительное дезаминирование. Аминогруппа вначале окисляется до иминогруппы (водороды переносятся на НАД+). На второй стадии происходит гидролитическое отщепление иминогруппы и образуется 2 -кетокислота.
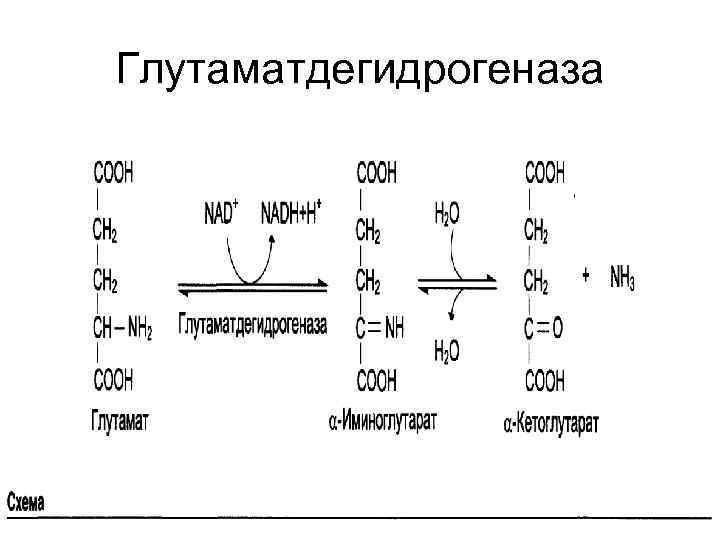
Глутаматдегидрогеназа

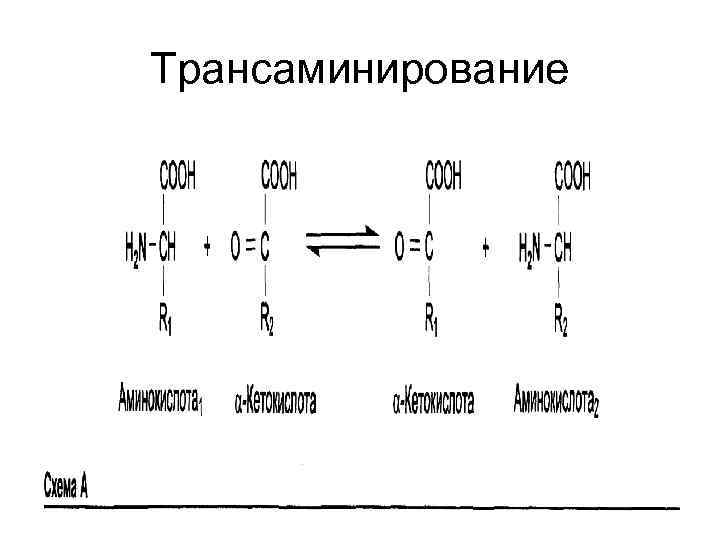
ТРАНСАМИНИРОВАНИЕ • А. Е. Браунштейн • М. Г. Крицман (1937)

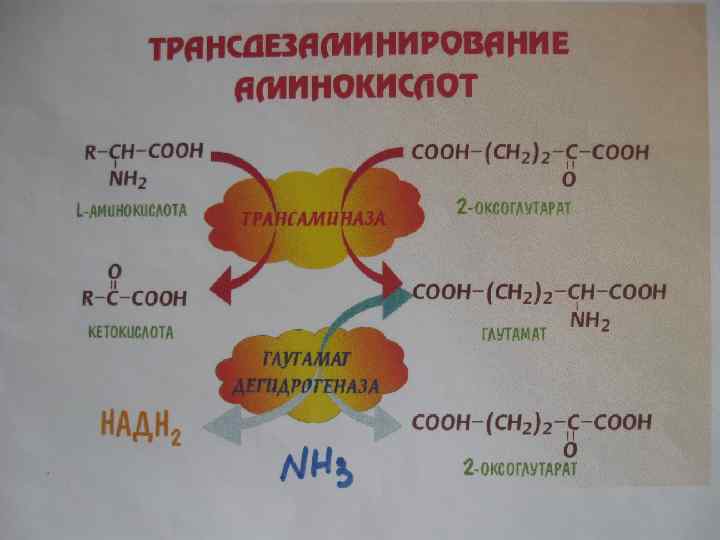
Трансаминирование • Перенос аминогруппы с любой АК на альфа-кетокислоту без промежуточного образования аммиака. • АК + кетокислота Новая АК + новая кетокислота • Глу + ПВК альфа-КГ + Ала
Трансаминирование

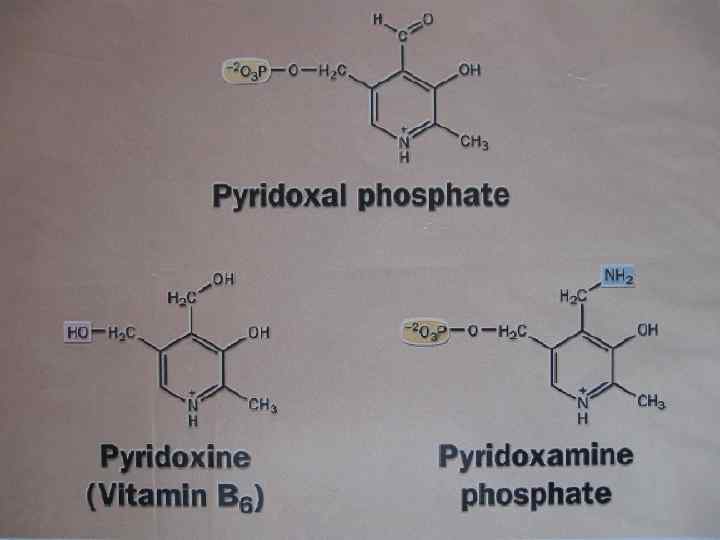
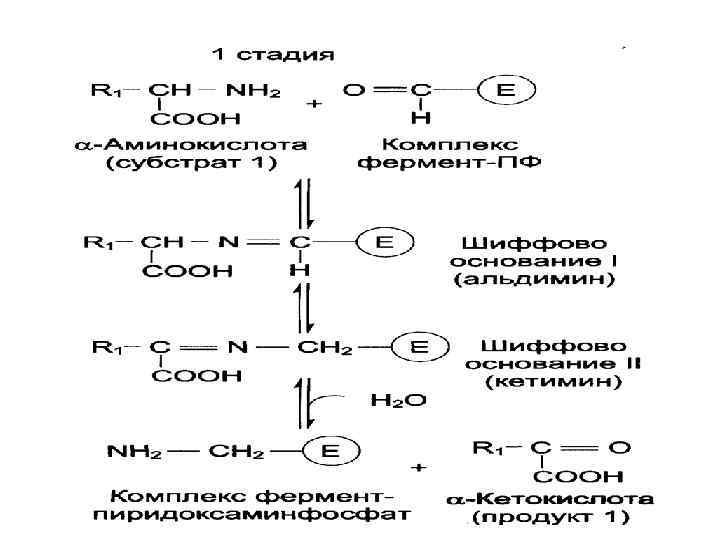
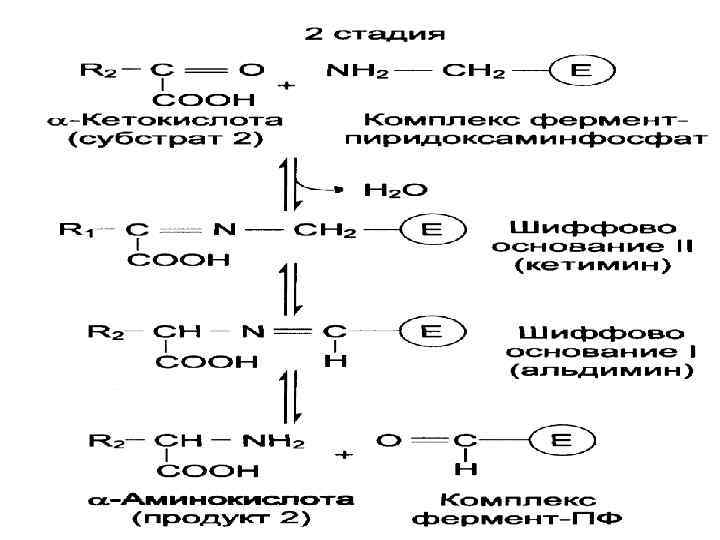
Аминотрансферазы • Трансаминирование катализируют аминотрансферазы. Переносимая NH 2 -группа временно присоединяется к связанному с ферментом пиридоксальфосфату, который переходит в пиридоксаминофосфат.

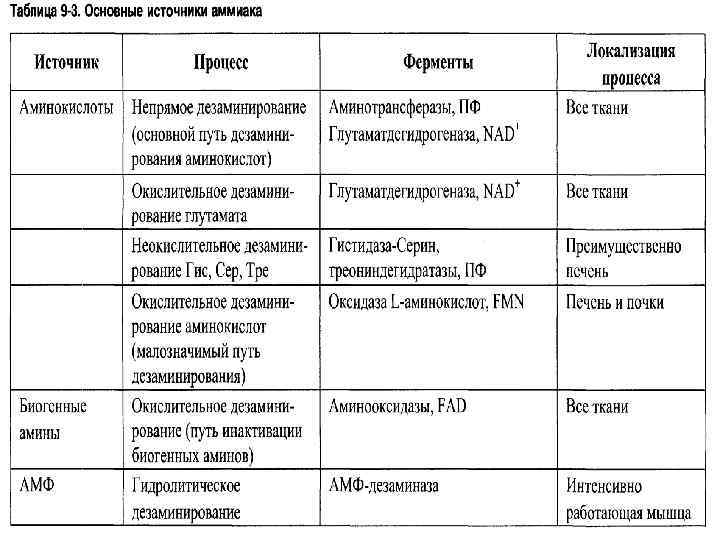
КОНЕЧНЫЕ ПРОДУКТЫ АЗОТИСТОГО ОБМЕНА

АММИАК • При дезаминировании АК, при распаде пуринов и пиримидинов освобождается аммиак.

ТОКСИЧНОСТЬ АММИАКА • Аммиак - NH 3 - клеточный яд, при высоких конц. повреждает нервные клетки (гепатаргическая кома). • В норме распад 70 г АК в сутки – конц. NH 3 в крови 60 мкмоль/л.

Токсичность аммиака • В опытах на кроликах концентрация NH 3 3 ммоль/л вызывала смерть! • Причины токсичности: 1. при р. Н крови в виде NH 4+, проникает через плазм. и МХ мембраны с большим трудом.

• Нейтр. мол. своб. NH 3 легко проходят эти мембраны. • При р. Н 7, 4 только 1% NH 3 от общего количества аммиака проникает в клетки мозга и МХ.

Причины токсичности NH 3 + альфа-КГ + НАДФН 2 - Глу + НАДФ+ Н 2 О Отток альфа- КГ из ЦТК (снижение скорости окисления глюкозы)

Механизмы детоксикации аммиака • 1. Синтез глутамина: Глн, аспарагина: Асн. • 2. Синтез мочевины. • 3. Аминирование а-КГ --> Глу. • 4. Амидирование белков.

Механизмы детоксикации аммиака • 5. Синтез пурин. и пиримид. структур. • 6. Нейтрализация в почках кислотами и выделение с мочой аммонийных солей.

Восстановительное аминирование • Реутилизация аммиака за счет глутаматдегидрогеназной реакции
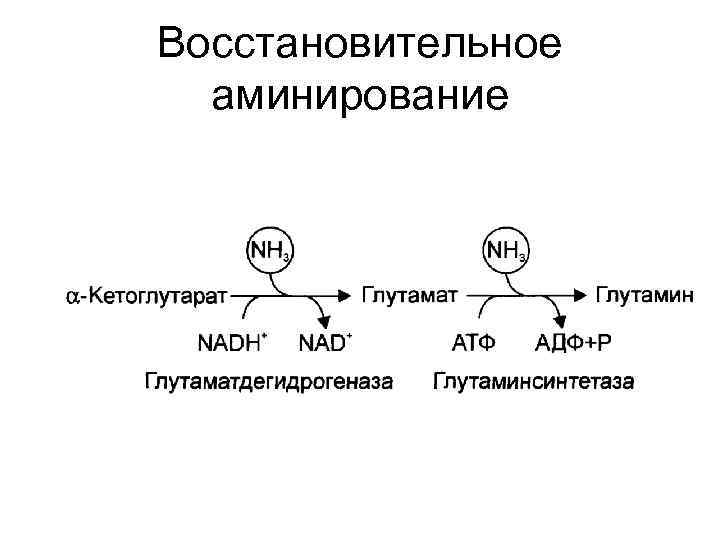
Восстановительное аминирование

Биосинтез глутамина

Глутаминаза


МОЧЕВИНА • У человека инактивация NH 3 осуществляется за счет синтеза мочевины, часть NH 3 выводится почками.

СТАДИИ СИНТЕЗА МОЧЕВИНЫ • Мочевина образуется в результате циклической последовательности реакций, протекающих в печени.

Первая стадия • Из гидрокарбоната (НСО 3 -) и аммиака с потреблением 2 молекул АТФ образуется карбамоилфосфат.

Синтез карбамоилфосфата

Вторая стадия • Карбамоильный остаток переносится на орнитин с образованием цитруллина.

Синтез цитруллина

Третья стадия • Вторая аминогруппа для мочевины поставляется за счет реакции аспартата с цитруллином.

Синтез аргининосукцината

Четвертая стадия Отщепление фумарата от аргининосукцината приводит к аргинину.
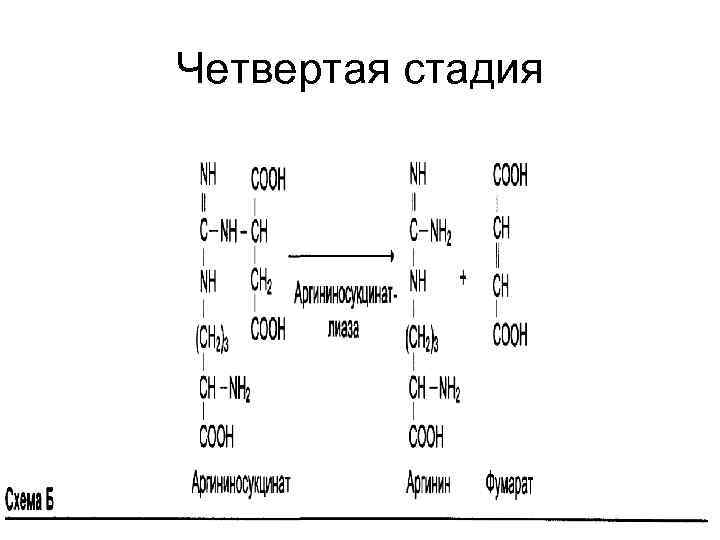
Четвертая стадия

Пятая стадия В результате гидролиза аргинина образуется мочевина. Остающийся орнитин вновь включается в цикл мочевины.
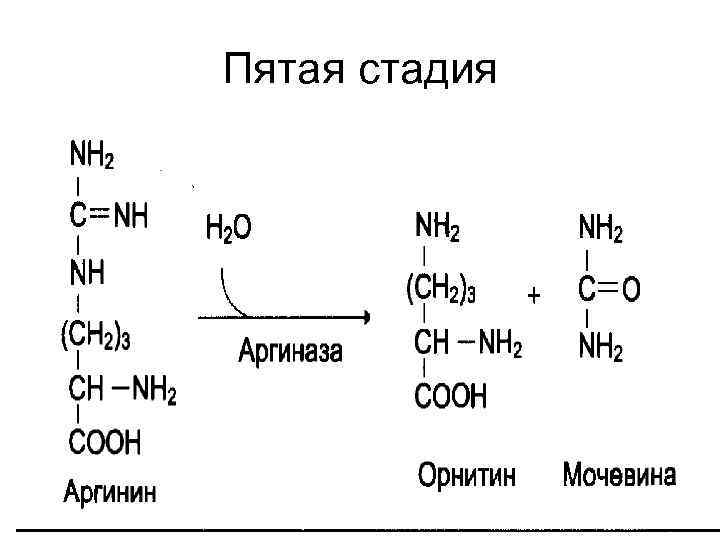
Пятая стадия

Взаимосвязь цикла мочевинообразования и ЦТК

ЭНЕРГОЗАВИСИМЫЙ ПРОЦЕСС • Биосинтез мочевины требует затрат энергии за счет расщепления четырех высокоэнергетических связей: двух при синтезе карбамоилфосфата и двух (!) при образовании аргининосукцината (АТФ → АМФ + PPi, РРi → 2 Pi).

Наследственные нарушения орнитинового цикла и их симптомы
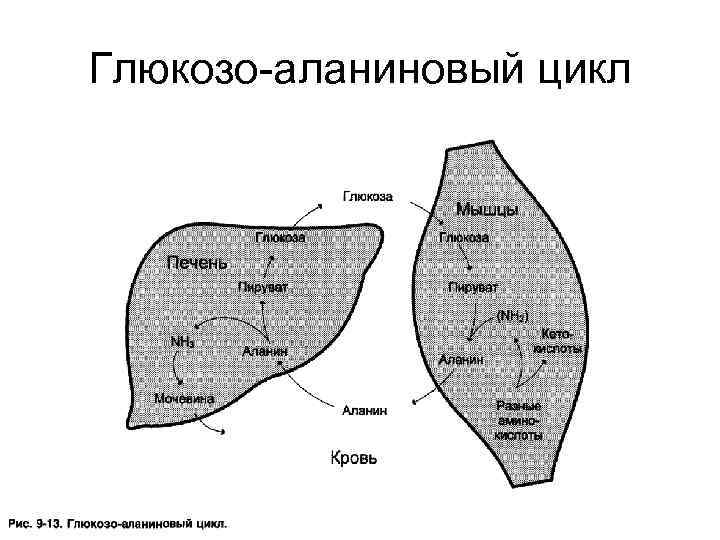
Глюкозо-аланиновый цикл

• БЛАГОДАРЮ ЗА ВНИМАНИЕ!
Общие пути обмена аминокислот 17.ppt