Метаболизм белков.ppt
- Количество слайдов: 48

Кировская государственная медицинская академия Кафедра химии Лекция: Метаболизм белков Заведующий кафедрой доктор медицинских наук, профессор Цапок Петр Иванович

ОБЩИЕ ПУТИ ОБМЕНА АМИНОКИСЛОТ • • Значение белков. Функции. Роль белков в питании. Нормы белка. Биологическая ценность белков. Источники и пути использования аминокислот. Переваривание белков в ЖКТ. Протеолиз Общие и специфические пути обмена аминокислот Дезаминирование и трансаминирование Биосинтез аминокислот

Значение белков. Функции. • • Ферментативная Гормональная – инсулин Рецепторная Транспортная – ЛПНВ Структурная – МХ, мембраны Опорная – коллаген Трофическая – овоальбумин Энергетическая – 17. 1 к. Дж – 1 г.

Значение белков. Функции • • Механохимическая – актин, миозин Электроосмотическая – Na, K-АТФ-аза Энерготрансформаторная – АТФ-синтетаза Когенетическая Генно-регуляторная Иммунологическая Обезвреживающая Гемостатическая - фибриноген

Нормы белка. Биологическая ценность белков. • • Общее количество поступающего белка Перевариваемость белка Аминокислотный состав Общая калорийность поступающих продуктов питания О, 7 г/кг – день Новорожденным – 4 г/кг Дети – 2 г/кг 5 лет – 1 г/кг

Минимальная норма белка Ежедневно необходимо получать с пищей не менее 30 г белка.

Источники и пути использования аминокислот • Аминокислоты - 30 г. • В крови - 35 - 65 мг/дл. • Белки - 15 кг Пища аминокислоты углеводы белки тканей
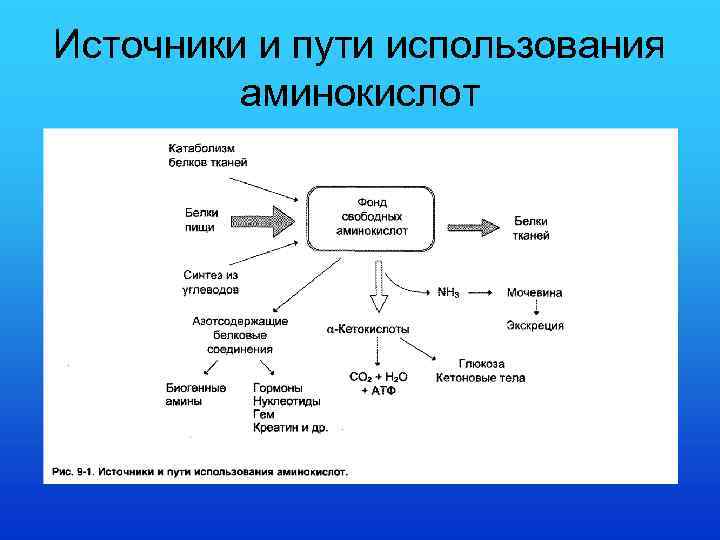
Источники и пути использования аминокислот
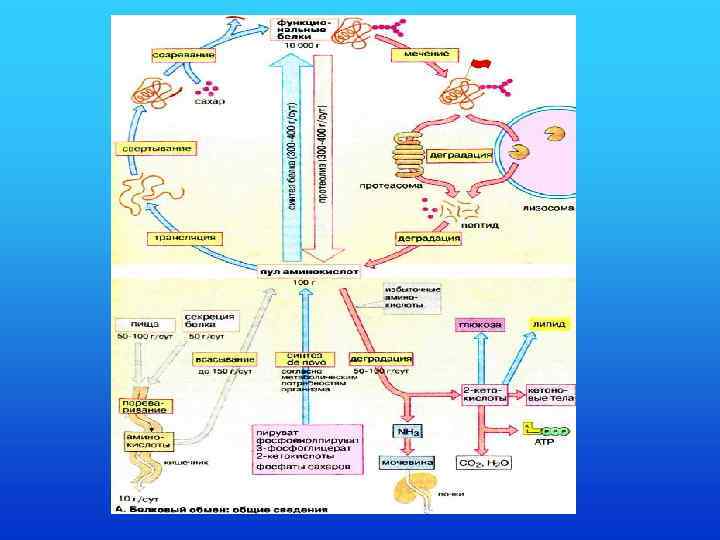

• Аминокислоты не запасаются в организме, в печени окисляется или используется до 100 г аминокислот в сутки. Содержащийся в них азот превращается в мочевину и выделяется с мочой, а углеродный скелет используется в синтезе углеводов, липидов или окисляется с образованием АТФ.

• В организме взрослого человека ежедневно разрушается до аминокислот 300 -400 г белка (протеолиз). Примерно то же самое количество аминокислот включается во вновь образованные молекулы белков (белковый биосинтез).

Азотистый баланс • В организме человека массой 70 кг содержится около 15 кг белка, большая его часть локализована в мышцах. Баланс азота в организме определяется метаболизмом белков. Окисление аминокислот поставляет 10 - 15 % метаболической энергии.

Азотистый баланс • В организме взрослого человека метаболизм азота в целом сбалансирован, т. е. количества поступающего и выделяемого белкового азота примерно равны. Если выделяется только часть вновь поступающего азота, баланс положителен. Это наблюдается, например, при росте организма. Отрицательный баланс встречается редко, главным образом как следствие заболеваний.

ПРОТЕОЛИЗ • Расщепление белков до свободных аминокислот осуществляют ферменты: протеиназы и пептидазы. • По месту атаки молекулы субстрата протеолитические ферменты делятся на эндопептидазы и экзопептидазы.

• Эндопептидазы, или протеиназы, расщепляют пептидную связь внутри пептидной цепи. • Для полного расщепления белков до свободных аминокислот необходимо несколько ферментов с различной специфичностью.
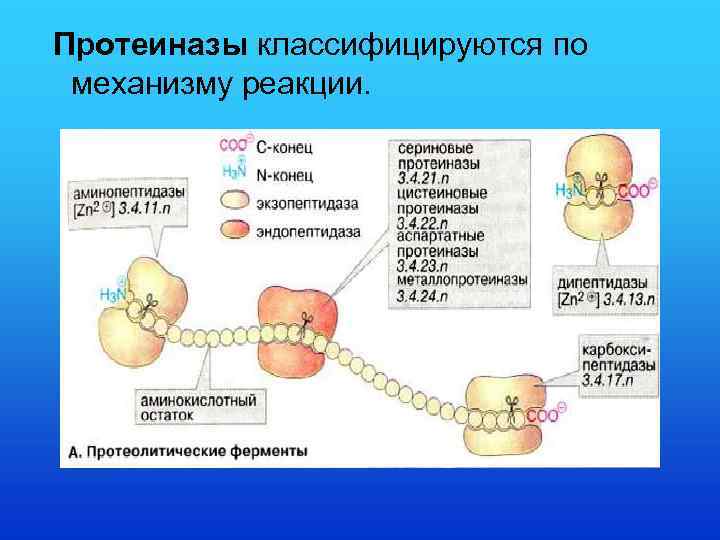
Протеиназы классифицируются по механизму реакции.

• Сериновые протеиназы содержат в активном центре остаток серина, в цистеиновых протеиназах таким является остаток цистеина. • Экзопептидазы гидролизуют пептиды с конца цепи: • аминопептидазы — с N-конца, карбоксипептидазы — с С-конца. Дипептидазы расщепляют только дипептиды.

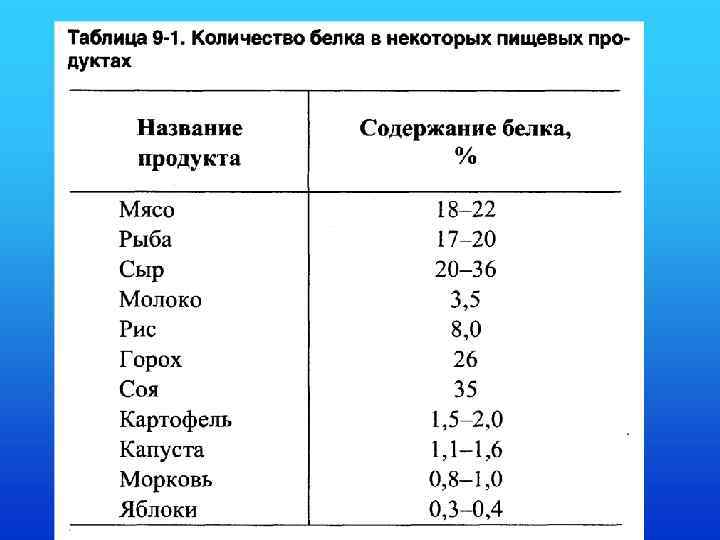
• Полученные с пищей белки подвергаются полному гидролизу в ЖКТ до АК, которые всасываются и кровотоком распределяются в организме. • 8 из 20 белковых АК не могут синтезироваться в организме человека ( незаменимые аминокислоты) должны поступать с пищей.

Секреция соляной кислоты в желудке
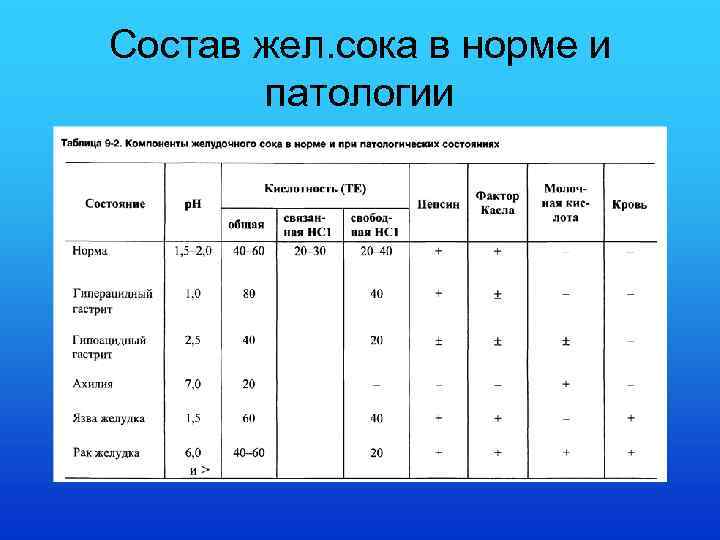
Состав жел. сока в норме и патологии

Активация химотрипсиногена


Глутамильный цикл

Общие пути обмена АК • • ДЕЗАМИНИРОВАНИЕ ТРАНСАМИНИРОВАНИЕ ДЕКАРБОКСИЛИРОВАНИЕ БИОСИНТЕЗ ЗАМЕНИМЫХ АМИНОКИСЛОТ

ДЕЗАМИНИРОВАНИЕ • Освобождение NH 2 -группы в виде аммиака. Отщепление NH 3 с образованием двойной связи (элиминирующее дезаминирование).

• • • Известны 4 вида дезаминирования: - ВОССТАНОВИТЕЛЬНОЕ - ГИДРОЛИТИЧЕСКОЕ - ОКИСЛИТЕЛЬНОЕ - ВНУТРИМОЛЕКУЛЯРНОЕ
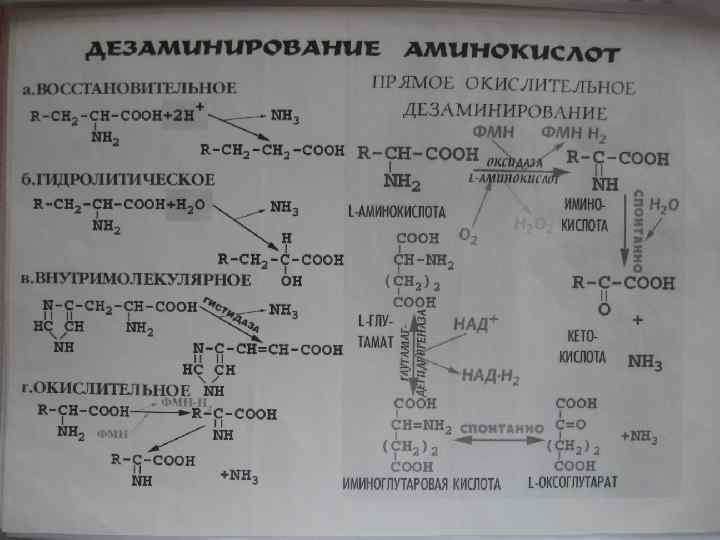

Химизм окислительного дезаминирования • Окислительное дезаминирование. Аминогруппа вначале окисляется до иминогруппы, при этом водороды переносятся на НАД+ или НАДФ+. На второй стадии происходит гидролитическое отщепление иминогруппы и образуется 2 кетокислота.
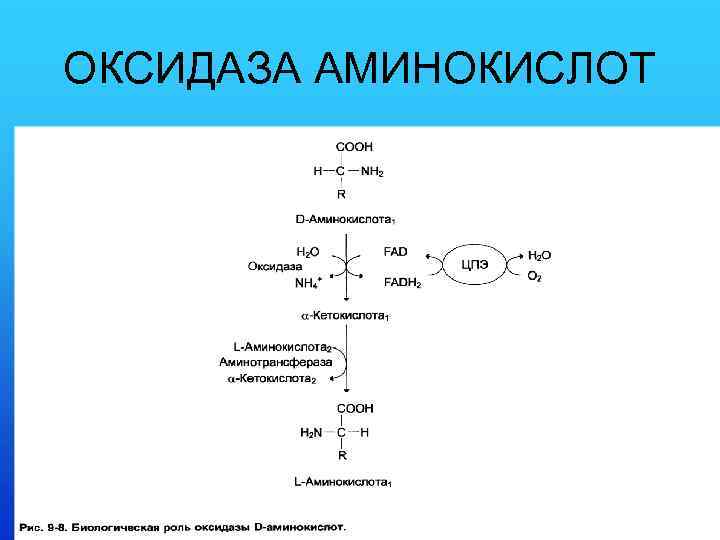
ОКСИДАЗА АМИНОКИСЛОТ
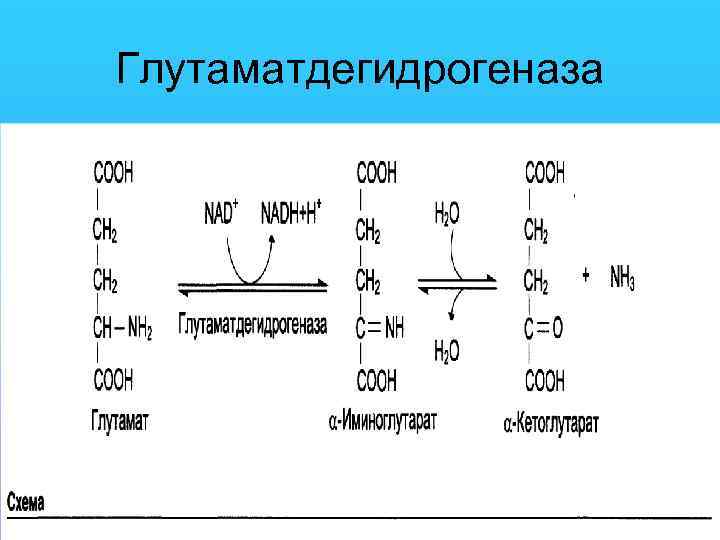
Глутаматдегидрогеназа


ТРАНСАМИНИРОВАНИЕ • А. Е. Браунштейн • М. Г. Крицман (1937)

Определение • Перенос аминогруппы с любой АК на альфа-кетокислоту без промежуточного образования аммиака. • АК + кетокислота Новая АК + новая кетокислота • Глу + ПВК альфа-КГ + Ала

Трансаминирование
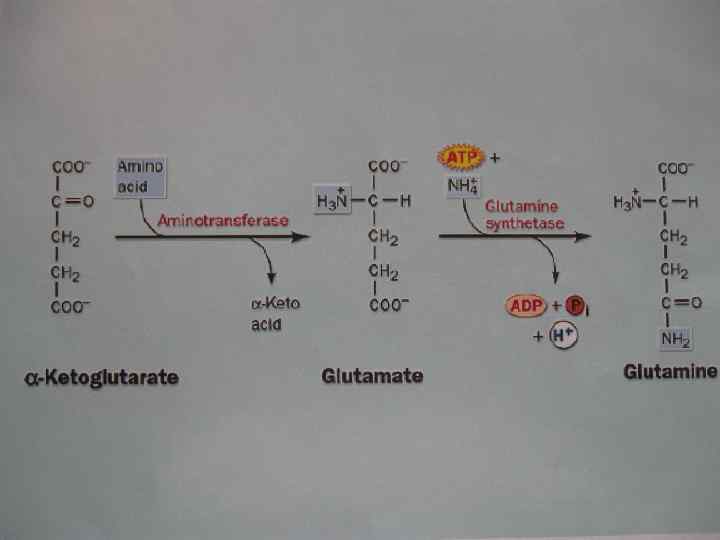
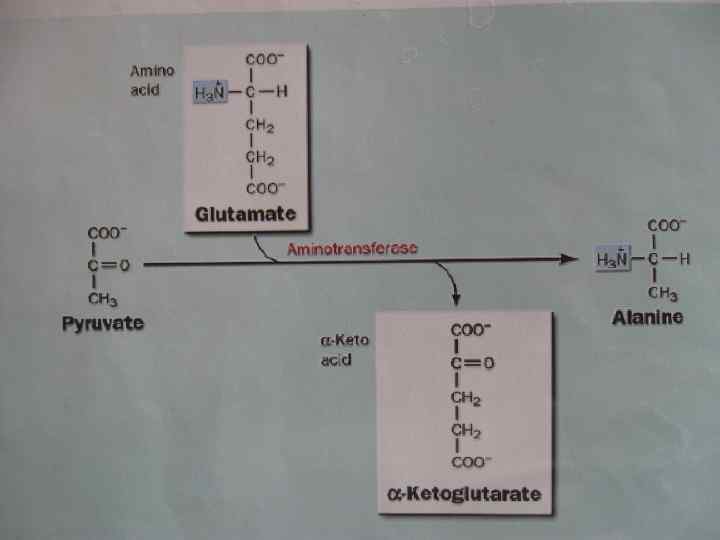

• Трансаминирование – это процесс, когда аминогруппа аминокислоты ( АК 1) переносится на альфа-кетокислоту (кеток-та 1). Из АК при этом образуется новая альфа-кетокислота, а из первоначальной кетокислоты — новая АК.

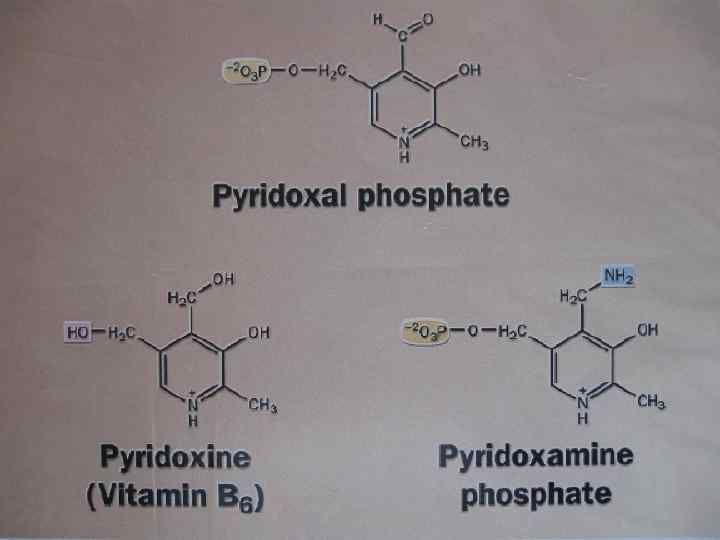
Аминотрансферазы • Реакции трансаминирования катализируются аминотрансферазами. Переносимая NH 2 -группа временно присоединяется к связанному с ферментом пиридоксальфосфату, который переходит в пиридоксаминофосфат.
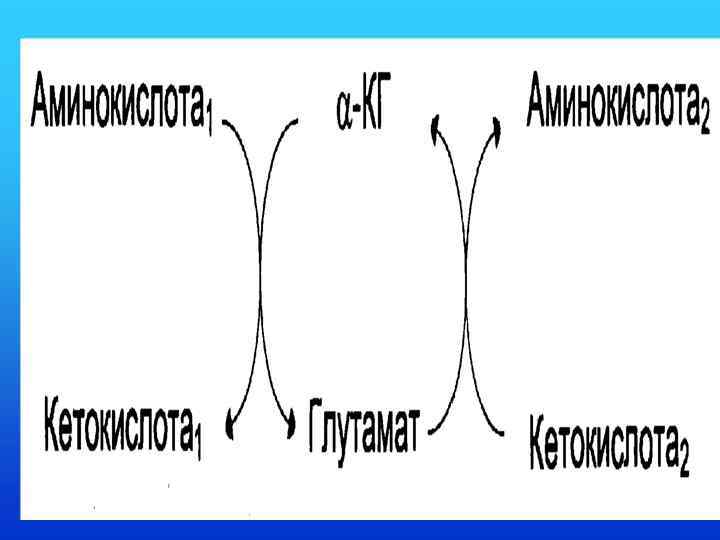
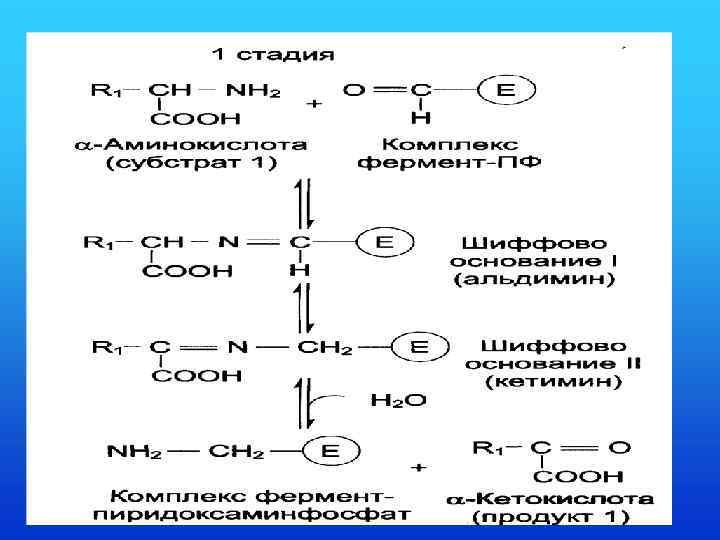
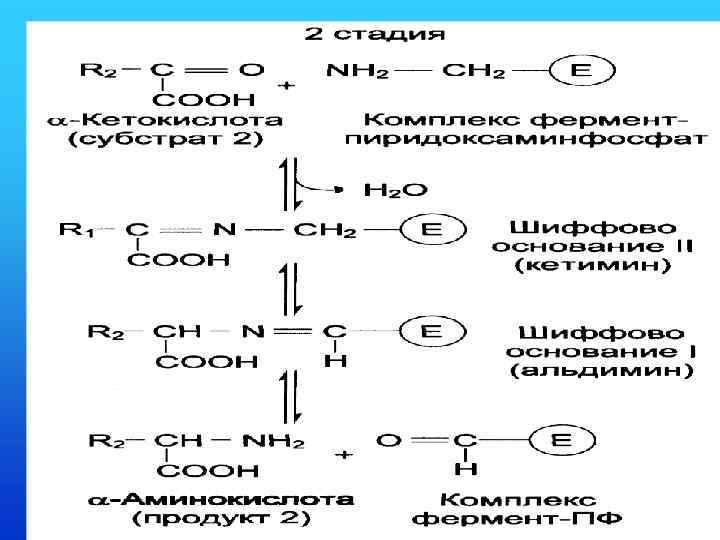


Аланинаминотрансфераза (АЛТ)
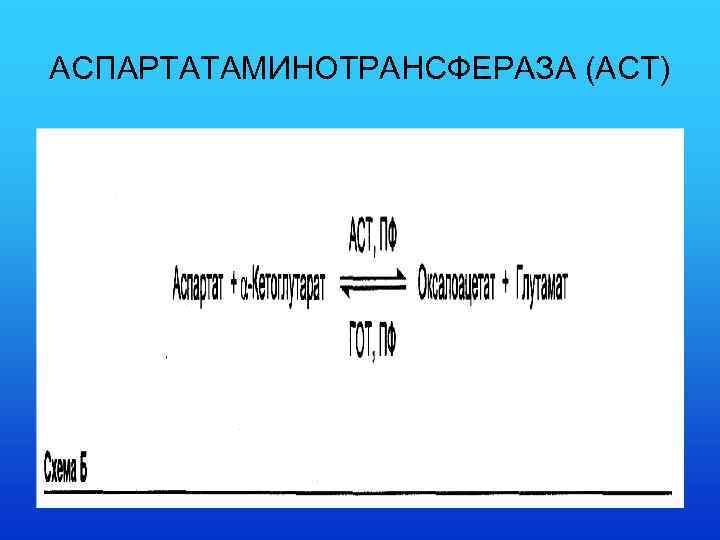
АСПАРТАТАМИНОТРАНСФЕРАЗА (АСТ)
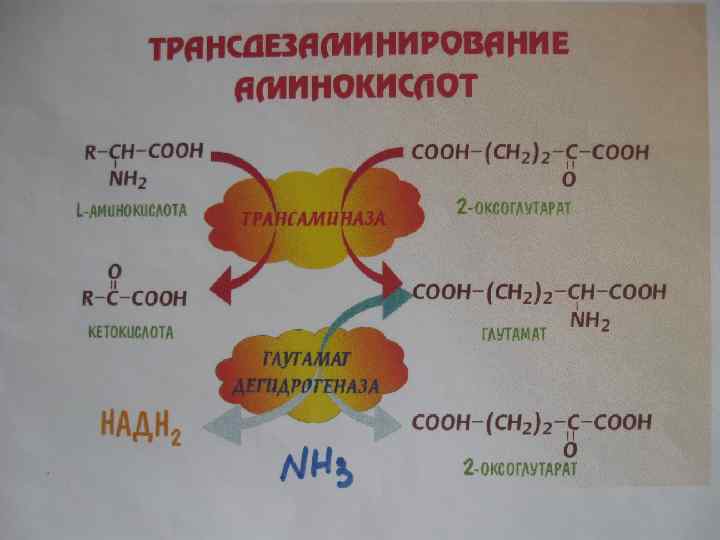

Коллекторная роль Глу
Метаболизм белков.ppt