Презентация Трансляция генетической информации.ppt
- Количество слайдов: 42

Кировская государственная медицинская академия Кафедра биологической химии Лекция: Трансляция генетической информации Заведующий кафедрой: доктор медицинских наук, профессор Цапок Петр Иванович

ТРАНСЛЯЦИЯ • Конечной целью реализации генетической информации в живой клетке является синтез белков, которые и осуществляют все биологические функции клетки, необходимые для ее жизнедеятельности, развития и адаптации к меняющимся внешним условиям. Однако генетическая информация в нуклеиновых кислотах записана последовательностью нуклеотидов. Поэтому ее необходимо перевести на язык аминокислотных остатков. Этот процесс перевода генетической информации с языка нуклеотидов на язык аминокислот и называется трансляцией генетической информации.

Факторы • Синтез белка - самый сложный из биосинтетических процессов. Он требует очень большого числа ферментов и других специфических макромолекул. В эукариотических клетках в белковом синтезе принимают участие свыше 70 рибосомальных белков, не менее 20 ферментов, необходимых для активации аминокислот-предшественников, более десятка вспомогательных ферментов и особых факторов для собственно белкового синтеза и не менее 100 дополнительных ферментов, участвующих в процессе созревания белков. Также в синтезе белка участвуют более 70 видов транспортных РНК и рибосомных РНК. Многие из этих макромолекул организованы в сложные трехмерные структуры рибосом, в которых по мере синтеза полипептидной цепи происходит перемещение (транслокация) м. РНК.

ЭТАПЫ • Сегодня мы знаем, что процесс белкового синтеза протекает в пять основных этапов. • Этап 1: активация аминокислот • На этом этапе, который протекает не в рибосоме, а в цитозоле, каждая из 20 аминокислот ковалентно присоединяется к определенной т. РНК, используя для этого энергию АТР. Эти реакции катализируются группой требующих присутствия ионов Mg 2+ активирующих ферментов, каждый из которых является специфическим по отношению к одной из аминокислот и к соответствующей этой аминокислоте т. РНК.

Этап 2: инициация полипептидной цепи • На этом этапе м. РНК, содержащая информацию о данном полипептиде, связывается с малой субчастицей рибосомы, а затем и с инициирующей аминокислотой, прикрепленной к соответствующей т. РНК; в результате образуется инициирующий комплекс. т. РНК, несущая инициирующую аминокислоту, взаимодействует по принципу комплементарности с находящимся в составе м. РНК особым триплетом, или кодоном, который сигнализирует о начале полипептидной цепи. • Осуществлению этого процесса, который требует участия гуанозинтрифосфата (GTP), способствуют три специфических белка, присутствующие в цитозоле и называемые факторами инициации.

Этап 3: элонгация • Далее полипептидная цепь удлиняется за счет последовательного ковалентного присоединения аминокислот, каждая из которых доставляется к рибосоме и встраивается в определенное положение с помощью соответствующей т. РНК, образующей комплементарные пары с отвечающим ей кодоном в м. РНК. Элонгация осуществляется при помощи белков цитозоля, называемых факторами элонгации. Для связывания каждой поступающей аминоацил-т. РНК и для перемещения рибосомы вдоль м. РНК на один кодон, т. е. для удлинения растущего полипептида на одно звено, затрачивается энергия, получаемая при гидролизе двух молекул GTP.

Этап 4: терминация и высвобождение полипептида • После завершения синтеза полипептидной цепи, о котором сигнализирует терминирующий кодон м. РНК, происходит высвобождение полипептида из рибосомы при участии особых «рилизинг» -факторов (от англ, release - высвобождать), или факторов терминации.

Этап 5: сворачивание полипептидной цепи и процессинг • Чтобы принять свою нативную биологически активную форму, полипептид должен свернуться, образуя при этом определенную пространственную конфигурацию. До или после сворачивания новосинтезированный полипептид может претерпевать процессинг, осуществляемый ферментами и заключающийся в удалении инициирующих аминокислот, в отщеплении лишних аминокислотных остатков, во введении в определенные аминокислотные остатки фосфатных, метильных, карбоксильных и других групп, а также в присоединении олигосахаридов или простетических групп.

Генетический код • Информация о последовательности аминокислотных остатков в белке записана в кодирующей этот белок м. РНК в виде последовательности тринуклеотидных фрагментов — кодонов. Необходимость как минимум трех нуклеотидных остатков для кодирования каждого из аминокислотных остатков связана с тем, что 20 незаменимых аминокислот нельзя закодировать двухнуклеотидными фрагментами (всего 16 возможных комбинаций). Из соотношения числа кодируемых аминокислот (20) и числа возможных комбинаций тринуклеотидов (64) следует, что генетический код должен быть вырожденным, т. е. одной аминокислоте должно соответствовать несколько кодонов.
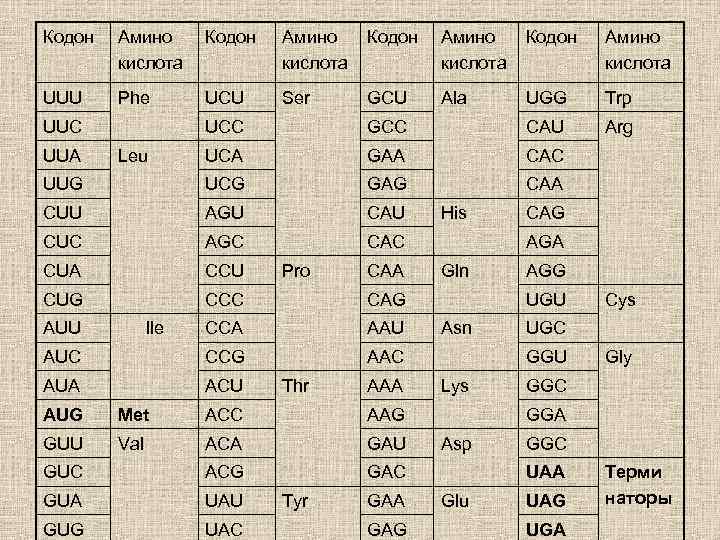
Кодон Амино Кодон кислота Амино кислота UUU Phe Ser Ala UGG Trp Arg UUC UCU GCU UCC GCC CAU UCA GAA CAC UUG UCG GAG CAA CUU AGU CAU CUC AGC CAC CUA CCU CUG CCC CAG CCA AAU AUC CCG AAC AUA ACU UUA Leu AUU Ile Pro Thr CAA AUG Met ACC Val ACA GAU GUC ACG UAU GUG UAC Gln Tyr GAA GAG AGG UGU Asn Lys Cys UGC GGU GAC GUA CAG AGA AAG GUU His Gly GGC GGA Asp GGC UAA Glu UAG UGA Терми наторы

КОДОНЫ • Как видно из таблицы распределение кодонов по аминокислотным остаткам весьма неравномерно. Три кодона — UAA, UAG и UGA — не соответствуют ни одной из аминокислот. Они являются сигналами прекращения синтеза полипептидной цепи (кодоны-терминаторы). Кодон AUG представляет собой инициирующий кодон, во внутренних положениях он кодирует метионин.

СВОЙСТВА КОДОНОВ • При рассмотрении последовательностей кодонов выявляется интересная закономерность: комплементарность кодона данной аминокислоте определяется первыми двумя нуклеотидами, третья же буква может отличаться.

Транспортные РНК • Прежде, чем аминокислота будет присоединена к растущей полипептидной цепи, необходимо активировать ее карбоксильную группу и затем поместить в конец растущей белковой цепи именно ту активированную аминокислоту, которая соответствует очередному кодону м. РНК. В обоих этих процессах непосредственное участие принимают транспортные РНК (т. РНК). т. РНК — это короткая РНК, обладающая специфичной структурой.

АКТИВАЦИЯ АМИНОКИСЛОТ • Необходимость активации аминокислоты вызвана тем, что прямое взаимодействие аниона кислоты с концевой аминогруппой растущей цепи полипептида энергетически невыгодно. В таких случаях кислоту обычно предварительно превращают в высоко активный сложный эфир, который и вводят во взаимодействие с аминогруппой. Точно так же поступает и клетка. На этом этапе каждая из 20 аминокислот ковалентно присоединяется к определенной т. РНК. Эти реакции катализируются 20 ферментами, называемыми аминоацил-т. РНКсинтетазами, каждая из которых специфична по отношению к какой-то одной аминокислоте и соответствующей т. РНК, при этом используется энергия АТР.

АКТИВАЦИЯ АМИНОКИСЛОТ • Общий вид катализируемой ими реакции имеет вид:

СТАДИИ АКТИВАЦИИ АМИНОКИСЛОТ • Процесс состоит из двух стадий. На первой стадии в активном центре фермента в результате взаимодействия АТР и аминокислоты образуется связанное с ферментом промежуточное соединение — аминоациладенилат.
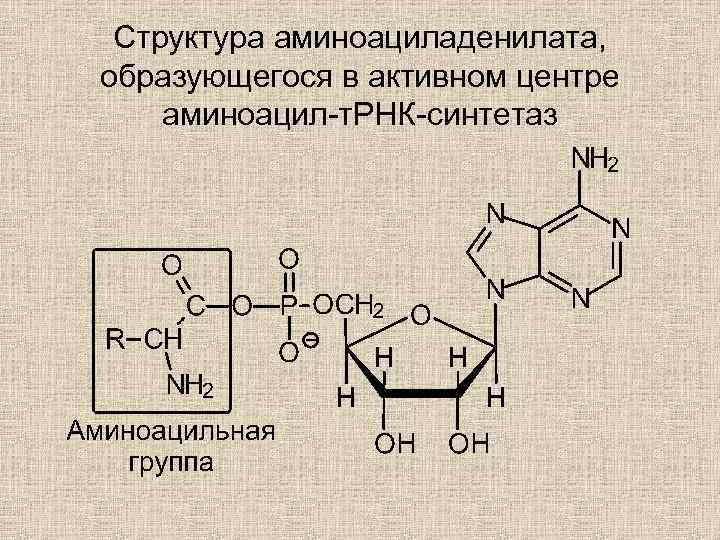
Структура аминоациладенилата, образующегося в активном центре аминоацил-т. РНК-синтетаз

Вторая стадия • На второй стадии аминоацильный остаток переносится с аминоациладенилата на соответствующую специфическую т. РНК, при этом аминоацильный остаток связывается со свободной 2'- или 3'гидроксигруппой концевого остатка аденозина в молекуле т. РНК.

СПЕЦИФИЧНОСТЬ ФЕРМЕНТОВ • Аминоацил-т. РНК-синтетазы очень специфичны по отношению как т. РНК, так и по отношению к соответствующей ей аминокислоте. Частота ошибок не превышает трех на 10000. После присоединения к соответствующей т. РНК аминокислота уже не участвует в определении специфичности аминоацилт. РНК, ибо сама по себе аминоацильная группа не узнается ни рибосомой, ни т. РНК. Специфичность аминоацил-т. РНК обеспечивается исключительно структурой т. РНК за счет уотсон-криковской комплементарности антикодонового триплета кодоновому триплету м. РНК.

Число т. РНК • Можно было бы ожидать, что общее число т. РНК будет в точности соответствовать числу кодонов (61 кодон; 3 кодона терминирующие), т. е. для каждого кодона будет существовать отдельная т. РНК. Однако число различных т. РНК существенно меньше числа кодонов.
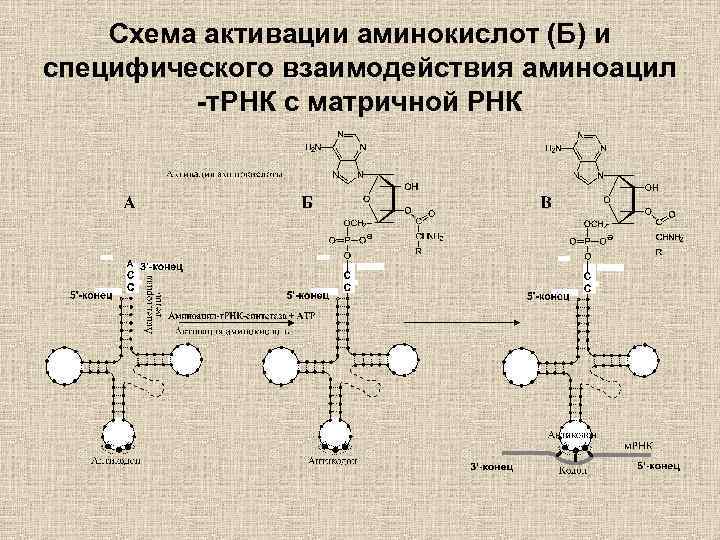
Схема активации аминокислот (Б) и специфического взаимодействия аминоацил -т. РНК с матричной РНК

КОМПЛЕМЕНТАРНОСТЬ КОДОНА • Комплементарность кодона данной аминокислоте определяется первыми двумя нуклеотидами, третья же буква может отличаться. Для объяснения это явление Фрэнсис Крик предложил гипотезу «качания» . Суть гипотезы состоит в следующем: • 1. Два первых основания кодона всегда образуют прочные уотсон-криковские пары. • 2. Третье основание кодона и первое основание антикодона, как привило, образуют менее прочную «качающуюся» пару. Если первое основание антикодона C или А, то такой антикодон способен «читать» только один кодон; если U или G, то такой антикодон может прочитать два разных кодона. Наконец, если первое основание гипоксантин (основание нуклеозида инозина (I), то антикодон может прочитать три антикодона
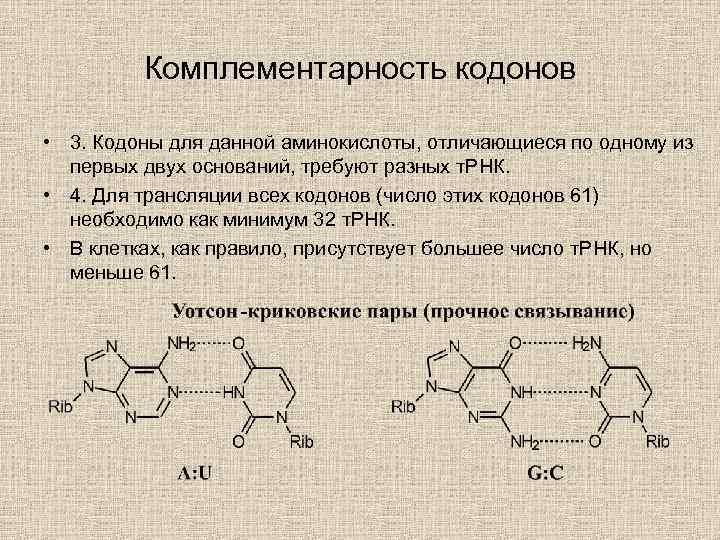
Комплементарность кодонов • 3. Кодоны для данной аминокислоты, отличающиеся по одному из первых двух оснований, требуют разных т. РНК. • 4. Для трансляции всех кодонов (число этих кодонов 61) необходимо как минимум 32 т. РНК. • В клетках, как правило, присутствует большее число т. РНК, но меньше 61.
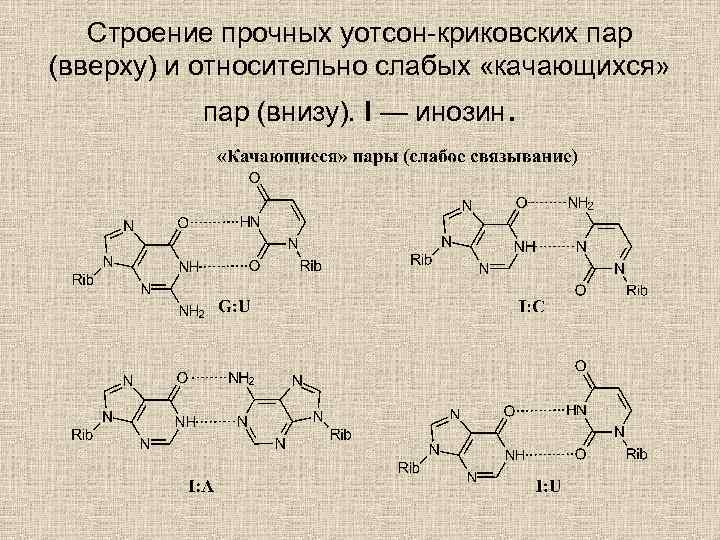
Строение прочных уотсон-криковских пар (вверху) и относительно слабых «качающихся» пар (внизу). I — инозин.

Синтез белка на рибосоме • Собственно синтез полипептидных цепей происходит на рибосоме. Рибосома представляет собой очень сложный белок-нуклеиновый комплекс. Каждая рибосома состоит из двух неравных по размеру субчастиц, которые в свою очередь состоят из белков и рибосомальных РНК (р. РНК).
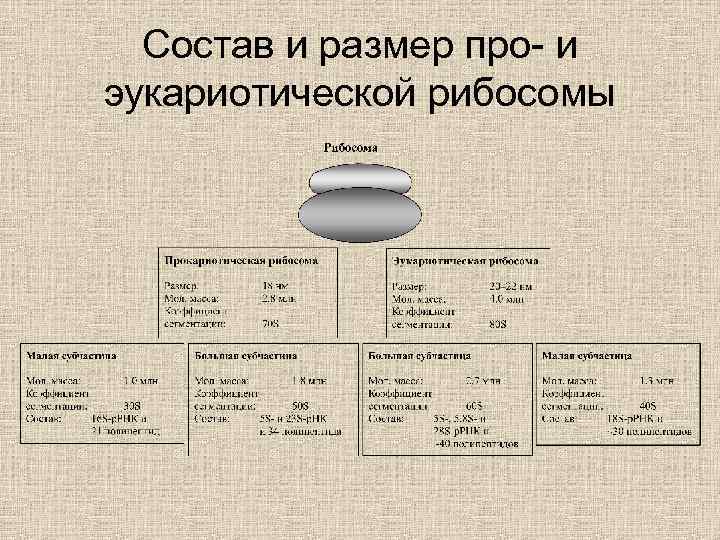
Состав и размер про- и эукариотической рибосомы

СТРОЕНИЕ • Хотя обычно рибосомы изображают в виде симметричной структуры, в действительности субчастицы расположены не симметрично и имеют совершенно неправильную форму. Две замысловатой формы субчастицы пригнаны друг к другу, причем между ними остается щель. Через эту щель проходит молекула м. РНК, вдоль которой в процессе трансляции движется рибосома. Из этой же щели появляется новосинтезированная полипептидная цепь.
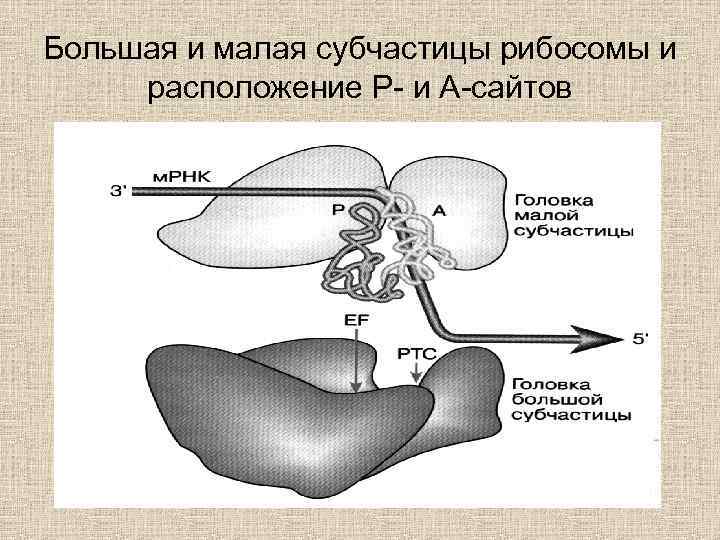
Большая и малая субчастицы рибосомы и расположение Р- и А-сайтов

• В процессе трансляции рибосома движется от 5'- к 3'-концу м. РНК, а синтез полипептида начинается с N-конца протекает от N- к Сконцу. В процессе трансляции рибосомы должны одновременно взаимодействовать с м. РНК и двумя молекулами т. РНК, одна из которых несет на 3'-конце пептидный фрагмент, а другая — аминоацильный. Участки рибосомы, на которых связываются эти т. РНК, называют Р-сайтом и А-сайтом, соответственно. В обоих участках т. РНК связаны с соответствующими кодонами.

Инициация синтеза полипептидной цепи • Инициация синтеза полипептидной цепи - реакция между двумя аминоацил-т. РНК, несущими остатки, соответствующие первой и второй аминокислоте создаваемого белка. При этом первой аминокислотой, как правило, является метионин. В тех преобладающих случаях, когда N-концевая аминокислота зрелого белка отличается от метионина, последний удаляется в ходе процессинга синтезируемого полипептида. При этом в стадии инициации участвует специальная метиониновая т. РНК, которая называется инициаторной и обозначается т. РНКi. Met.

• Наряду с ней у всех живых организмов существует другая специфичная к метионину т. РНК, элонгаторная т. РНКе. Met. У прокариот метионин, связанный с инициаторной т. РНК, формилируется по a-аминогруппе. Для образования инициирующего комплекса необходимы три белка, называемые факторами инициации (IF-1, IF-2 и IF-3).

• Инициирующая т. РНКi. Met может связываться только с Р-сайтом, однако это исключение: все остальные вновь поступающие аминоацил-т. РНК присоединяются к А-участку, тогда как Р -участок — это такое место рибосомы, с которого уходят «пустые» т. РНК.

Элонгация синтеза полипептидной цепи • Реакция образования новых пептидных связей на рибосомах на стадии элонгации представляет собой перенос растущей пептидной цепи длиной г звеньев, связанной сложноэфирной связью с одной из гидроксигрупп 3'концевого нуклеотида т. РНК, специфичной к i-й аминокислоте, на aаминогруппу (i + 1)-й аминокислоты, связанной со специфичной к ней т. РНК.

Участок декодирования • В процессе трансляции рибосомы должны одновременно взаимодействовать с м. РНК и двумя молекулами т. РНК, одна из которых несет на 3'-конце пептидный фрагмент (связана в Р-участке), а другая — аминоацильный (связана в А-участке). В обоих участках т. РНК связаны с соответствующими кодонами. Область рибосомы, с которой в А-участке взаимодействуют кодон и антикодон, называют участком декодирования.

• После отбора аминоацил-т. РНК происходит перенос пептидного фрагмента на a-аминогруппу аминоацил-т. РНК. Участок рибосомы, на котором происходит этот процесс и который, следовательно, содержит каталитический центр для переноса пептида, называется пептидилтрансферазным участком.

• Поскольку расстояние между 3'-концом т. РНК и антикодоновой петлей порядка 8 нм, пептидилтрансферазный и декодирующий участки на рибосоме удалены друг от друга. Известно, что они вообще находятся на разных субъединицах рибосом: декодирующий — на малой, а пептидилтрансферазный — на большой субъединице. Молекулы т. РНК располагаются на рибосоме таким образом, что взаимодействуют с обеими субъединицами, причем на большой субъединице в районе пептидилтрансферазного центра сближены их 3'-концевые Ср. А фрагменты, а на малой субъединице вблизи декодирующего участка — их антикодоновые петли.

• После переноса пептидного остатка аминоацилт. РНК, находящаяся в А-участке, превращается в пептидил-т. РНК. За этим следует транслокация, перемещающая ее в Р-участок, при этом перемещается и связанный с ней кодон (и, естественно, вся молекула м. РНК). • В процессе элонгации участвуют два белковых фактора EF-1 и EF-2. Происходящее при элонгации «продергивание» м. РНК через рибосому (или движение рибосомы по м. РНК) требует затраты энергии. Для этого используется энергия гидролиза трифосфатной связи GTP.

Терминация синтеза полипептидной цепи • Терминация происходит на специальных кодонах-терминаторах Up. A, Up. Ap. G и Up. Gp. A. Когда в участок, на котором на рибосоме проходит отбор мономера, попадает такой кодон, связывания какой-либо аминоацил-т. РНК не происходит и синтез полипептидной цепи прекращается. При этом проходит гидролиз сложноэфирной связи, соединяющей синтезированный полипептид с т. РНК, т. е. освобождение полипептида.

• Каждая молекула информационной РНК (м. РНК) помимо полирибонуклеотидной последовательности, программирующей некоторую последовательность аминокислот, содержит дополнительные нетранслируемые области как с 3'-, так и с 5'-конца. У прокариотических м. РНК непосредственно перед инициаторным кодоном находится специальная олигопуриновая последовательность из шести нуклеотидов, комплементарная 3'-концевому фрагменту рибосомной РНК малой субъединицы (последовательность Шайна-Дельгарно).

• Образование комплекса между этими олигорибонуклеотидными фрагментами играет важную роль в обеспечении фиксации инициаторного кодона в декодирующем участке активного центра рибосомы. У многих эукариотических м. РНК на 5'-конце имеется специфическая структура, называемая кэпом (от англ, cap — шапочка).

• На 3'-конце многих эукариотических м. РНК имеется довольно протяженный фрагмент, состоящий только из остатков адениловой кислоты. Этот поли(А)-фрагмент не входит в состав первичного транскрипта, т. е. не запрограммирован непосредственно в гене, а присоединяется с помощью специального фермента — полинуклеотидаденилилтрансферазы.

СПАСИБО ЗА ВНИМАНИЕ!
Презентация Трансляция генетической информации.ppt