Кинетика химических реакций Химическая кинетика – учение о









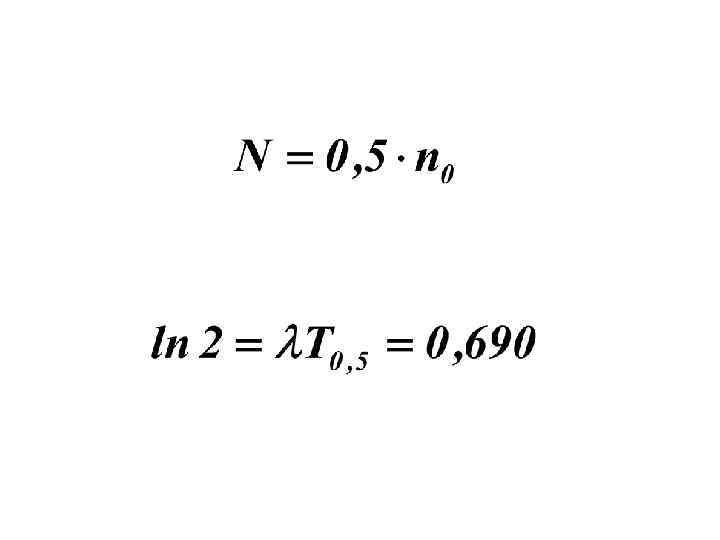


























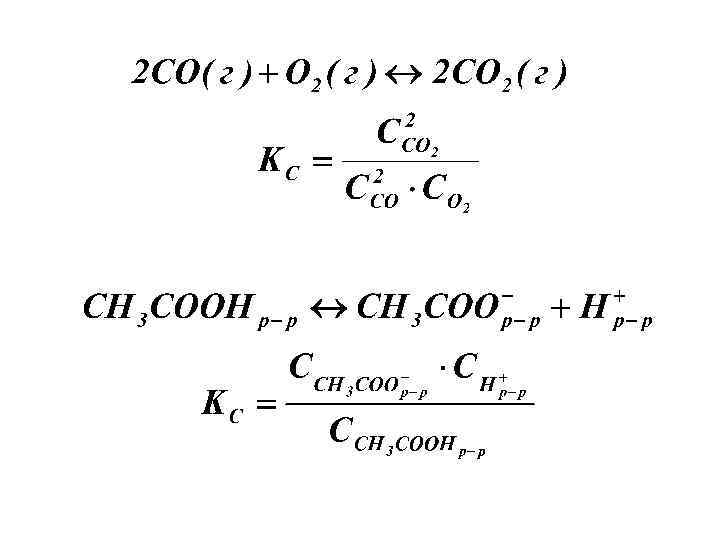





Лекция 3 Кинетика и равновесие.ppt
- Количество слайдов: 46
 Кинетика химических реакций Химическая кинетика – учение о химическом процессе, его механизме и закономерностях развития во времени.
Кинетика химических реакций Химическая кинетика – учение о химическом процессе, его механизме и закономерностях развития во времени.
 Термодинамически наиболее вероятны реакции, у которых значение нормального сродства наиболее отрицательны. Пример: N 2+O 2=2 NO r. G 298= + 176 к. Дж С+О 2=СО 2 r. G 298= -395 к. Дж
Термодинамически наиболее вероятны реакции, у которых значение нормального сродства наиболее отрицательны. Пример: N 2+O 2=2 NO r. G 298= + 176 к. Дж С+О 2=СО 2 r. G 298= -395 к. Дж
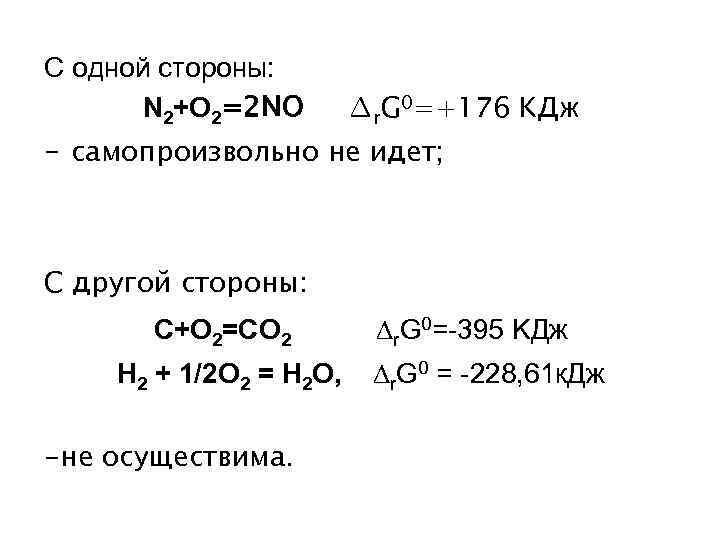
 С одной стороны: N 2+O 2=2 NO ∆r. G 0=+176 KДж - самопроизвольно не идет; С другой стороны: С+О 2=СО 2 ∆r. G 0=-395 KДж Н 2 + 1/2 О 2 = Н 2 О, r. G 0 = -228, 61 к. Дж -не осуществима.
С одной стороны: N 2+O 2=2 NO ∆r. G 0=+176 KДж - самопроизвольно не идет; С другой стороны: С+О 2=СО 2 ∆r. G 0=-395 KДж Н 2 + 1/2 О 2 = Н 2 О, r. G 0 = -228, 61 к. Дж -не осуществима.
 Реакционная способность химической системы при заданных условиях характеризуется скоростью и возможной глубиной химической реакции. (пример реакции)
Реакционная способность химической системы при заданных условиях характеризуется скоростью и возможной глубиной химической реакции. (пример реакции)
 Дифференциальное уравнение скорости химической реакции. Скорость реакции – кинетический критерий • ni = порядок реакции • n = 0, дробные и целые числа, (в основном 1, 2, не более 3)
Дифференциальное уравнение скорости химической реакции. Скорость реакции – кинетический критерий • ni = порядок реакции • n = 0, дробные и целые числа, (в основном 1, 2, не более 3)
 Простые кинетические уравнения для элементарных реакций I и II порядков Ед. изм Дифференциальное константы Время уравнение скорости полупревращения I C-1 II
Простые кинетические уравнения для элементарных реакций I и II порядков Ед. изм Дифференциальное константы Время уравнение скорости полупревращения I C-1 II
 Кинетика радиоактивного распада Где - кинетическая константа, называемая постоянной распада и зависящая только от природы радионуклида.
Кинетика радиоактивного распада Где - кинетическая константа, называемая постоянной распада и зависящая только от природы радионуклида.
 • где N 0 - есть число атомов радионуклида к моменту времени t = 0; • N - число атомов радионуклидов к моменту времени . • t = Т 1/2 время, за которое распадается половина первоначального кол-ва атомов радионуклида N 0
• где N 0 - есть число атомов радионуклида к моменту времени t = 0; • N - число атомов радионуклидов к моменту времени . • t = Т 1/2 время, за которое распадается половина первоначального кол-ва атомов радионуклида N 0
 Число молекул реагентов, участвующих в простой одностадийной реакции, состоящей из одного элементарного акта – молекулярность реакции. Мономолекулярная реакция: I 2 = 2 I (газ) (I) Бимолекулярная реакция: 2 NO = N 2 O 2 Тримолекулярные реакции: 2 NO + O 2 = 2 NO 2 H+O 2+M=HO 2+M*
Число молекул реагентов, участвующих в простой одностадийной реакции, состоящей из одного элементарного акта – молекулярность реакции. Мономолекулярная реакция: I 2 = 2 I (газ) (I) Бимолекулярная реакция: 2 NO = N 2 O 2 Тримолекулярные реакции: 2 NO + O 2 = 2 NO 2 H+O 2+M=HO 2+M*
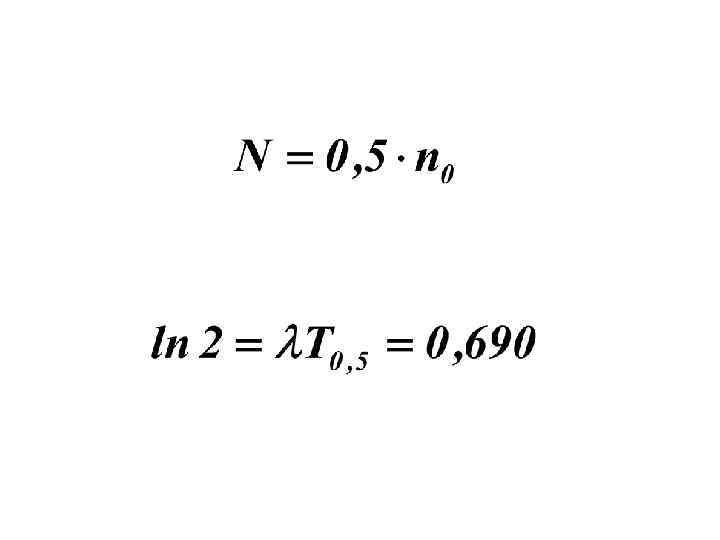 HIO 3 + 3 H 2 SO 3 = HI + 3 H 2 SO 4, медленная стадия HIO 3 + H 2 SO 3 = HIO 2 + H 2 SO 4, быстрые стадии HIO 2 + H 2 SO 3 = HIO + H 2 SO 4, HIO + H 2 SO 3 = HI + H 2 SO 4. ν=k[HIO 3]·[H 2 SO 3]
HIO 3 + 3 H 2 SO 3 = HI + 3 H 2 SO 4, медленная стадия HIO 3 + H 2 SO 3 = HIO 2 + H 2 SO 4, быстрые стадии HIO 2 + H 2 SO 3 = HIO + H 2 SO 4, HIO + H 2 SO 3 = HI + H 2 SO 4. ν=k[HIO 3]·[H 2 SO 3]
 Зависимость скорости реакции от температуры С повышением температуры скорость реакции возрастает. Согласно правилу Вант-Гоффа при повышении температуры процесса на 100 С скорость реакции в области умеренных температур увеличивается в 2 -4 раза.
Зависимость скорости реакции от температуры С повышением температуры скорость реакции возрастает. Согласно правилу Вант-Гоффа при повышении температуры процесса на 100 С скорость реакции в области умеренных температур увеличивается в 2 -4 раза.
 • Уравнение Вант-Гоффа • Уравнение Аррениуса
• Уравнение Вант-Гоффа • Уравнение Аррениуса
 • Еа – энергия активации реакции – избыточная энергия, которой должны обладать молекулы во время столкновения, чтобы произошло взаимодействие.
• Еа – энергия активации реакции – избыточная энергия, которой должны обладать молекулы во время столкновения, чтобы произошло взаимодействие.
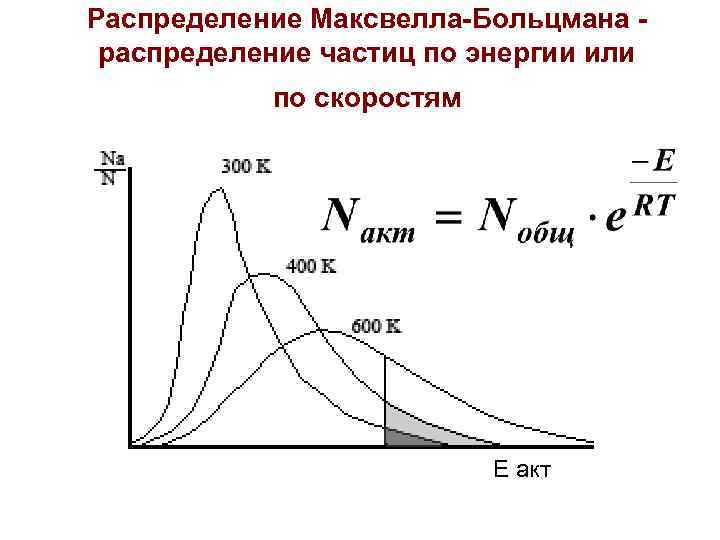
 Распределение Максвелла-Больцмана - распределение частиц по энергии или по скоростям Е акт
Распределение Максвелла-Больцмана - распределение частиц по энергии или по скоростям Е акт
 Eакт >o Положительное значение энергии активации показывает, что на пути от исходных веществ к продуктам имеется энергетический барьер, который не позволяет немедленно осуществляться всем термодинамически возможным реакциям.
Eакт >o Положительное значение энергии активации показывает, что на пути от исходных веществ к продуктам имеется энергетический барьер, который не позволяет немедленно осуществляться всем термодинамически возможным реакциям.
 • Из уравнения Аррениуса:
• Из уравнения Аррениуса:
 • Величины Еа и А в уравнении Аррениуса мало изменяются с температурой. • В подавляющем большинстве случаев Еа>0, однако имеются реакции Еа 0 и даже меньше нуля.
• Величины Еа и А в уравнении Аррениуса мало изменяются с температурой. • В подавляющем большинстве случаев Еа>0, однако имеются реакции Еа 0 и даже меньше нуля.
 Механизм химической реакции • Последовательные - реакции с промежуточными стадиями, когда продукт предыдущей стадии служит исходным веществом для последующей:
Механизм химической реакции • Последовательные - реакции с промежуточными стадиями, когда продукт предыдущей стадии служит исходным веществом для последующей:
 Параллельные реакции • Реакции, в которых исходные вещества способны образовывать разные продукты реакции или одно вещество одновременно способно реагировать с несколькими веществами.
Параллельные реакции • Реакции, в которых исходные вещества способны образовывать разные продукты реакции или одно вещество одновременно способно реагировать с несколькими веществами.
 Сопряженные (одна реакция идет в присутствии другой) 1. HBr. O 3 + 3 H 2 SO 3 = HBr + 3 H 2 SO 4; 2. HBr. O 3 + 3 H 3 As. O 3 = HBr + 3 H 3 As. O 4. Вторая реакция идет только в присутствии первой, так как H 2 SO 3 более сильный восстановитель, чем H 3 As. O 3, и в системе протекают реакции 1) HBr. O 3 + H 2 SO 3 = HBr. O 2 + H 2 SO 4 HBr. O 2– HBr. O 2 более сильный окислитель, чем H 3 As. O 3. ⇒ 2) HBr. O 2 + 2 H 3 As. O 3 = HBr + 2 H 3 As. O 4.
Сопряженные (одна реакция идет в присутствии другой) 1. HBr. O 3 + 3 H 2 SO 3 = HBr + 3 H 2 SO 4; 2. HBr. O 3 + 3 H 3 As. O 3 = HBr + 3 H 3 As. O 4. Вторая реакция идет только в присутствии первой, так как H 2 SO 3 более сильный восстановитель, чем H 3 As. O 3, и в системе протекают реакции 1) HBr. O 3 + H 2 SO 3 = HBr. O 2 + H 2 SO 4 HBr. O 2– HBr. O 2 более сильный окислитель, чем H 3 As. O 3. ⇒ 2) HBr. O 2 + 2 H 3 As. O 3 = HBr + 2 H 3 As. O 4.
 Цепные реакции H 2 + Cl 2 = 2 HCl Cl 2 + h = 2 Cl • зарождение цепи; Cl • + H 2 = HCl + H • продолжение цепи; H • + Cl 2 = HCl + Cl • продолжение цепи; H • + H • = H 2 обрыв цепи; Cl • +Cl • = Cl 2 обрыв цепи.
Цепные реакции H 2 + Cl 2 = 2 HCl Cl 2 + h = 2 Cl • зарождение цепи; Cl • + H 2 = HCl + H • продолжение цепи; H • + Cl 2 = HCl + Cl • продолжение цепи; H • + H • = H 2 обрыв цепи; Cl • +Cl • = Cl 2 обрыв цепи.
 • КОЛЕБАТЕЛЬНЫЕ РЕАКЦИИ – класс окислительно-восстановительных периодических реакций. - Катализатор - Ингибитор
• КОЛЕБАТЕЛЬНЫЕ РЕАКЦИИ – класс окислительно-восстановительных периодических реакций. - Катализатор - Ингибитор
 Реакция Белоусова - Жаботинского «Химические часы» - тонкий слой - волны от бесцветного (Ce+3) к жёлтому (Ce+4) и обратно.
Реакция Белоусова - Жаботинского «Химические часы» - тонкий слой - волны от бесцветного (Ce+3) к жёлтому (Ce+4) и обратно.
 Катализ – это явление изменения скорости реакции, происходящее под действием некоторых веществ (катализаторов).
Катализ – это явление изменения скорости реакции, происходящее под действием некоторых веществ (катализаторов).
 Катализатор – вещество, изменяющее скорость химической реакции за счет участия в промежуточном химическом взаимодействии с компонентами химической реакции, но восстанавливающее после каждого цикла промежуточного взаимодействия свой химический состав.
Катализатор – вещество, изменяющее скорость химической реакции за счет участия в промежуточном химическом взаимодействии с компонентами химической реакции, но восстанавливающее после каждого цикла промежуточного взаимодействия свой химический состав.
 Ингибиторы – это вещества, замедляющие реакцию и входящие в состав продукта реакции.
Ингибиторы – это вещества, замедляющие реакцию и входящие в состав продукта реакции.
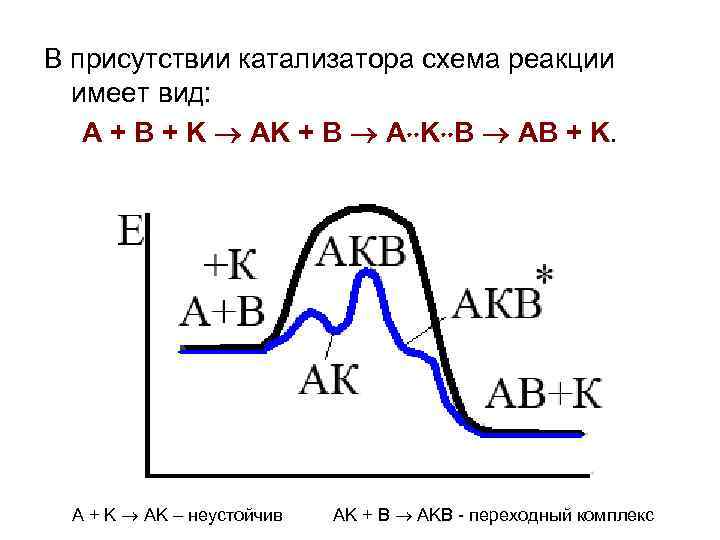
 В присутствии катализатора схема реакции имеет вид: A + B + K AK + B A K B AB + K. A + K AK – неустойчив AK + B AKB - переходный комплекс
В присутствии катализатора схема реакции имеет вид: A + B + K AK + B A K B AB + K. A + K AK – неустойчив AK + B AKB - переходный комплекс
 ХИМИЧЕСКОЕ РАВНОВЕСИЕ
ХИМИЧЕСКОЕ РАВНОВЕСИЕ
 Состояние равновесия - состояние системы, при котором в ней не наблюдается никаких изменений при неизменных условиях.
Состояние равновесия - состояние системы, при котором в ней не наблюдается никаких изменений при неизменных условиях.
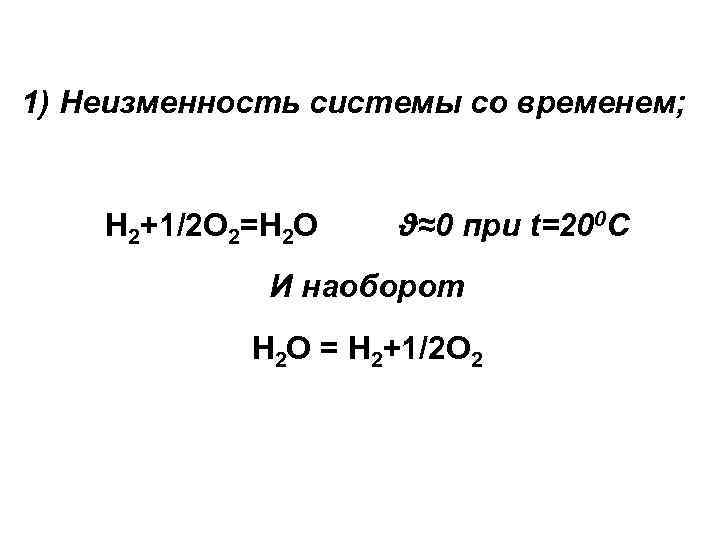
 1) Неизменность системы со временем; Н 2+1/2 О 2=Н 2 О ϑ≈0 при t=200 С И наоборот Н 2 О = Н 2+1/2 О 2
1) Неизменность системы со временем; Н 2+1/2 О 2=Н 2 О ϑ≈0 при t=200 С И наоборот Н 2 О = Н 2+1/2 О 2
 2) независимость состояния равновесия от того, каким путем оно достигнуто; При комнатной температуре и р=1 атм Н 2+О 2=1/2 Н 2 О Н 2 О= 1/2 Н 2+О 2 Воды не образуется вода не разлагается
2) независимость состояния равновесия от того, каким путем оно достигнуто; При комнатной температуре и р=1 атм Н 2+О 2=1/2 Н 2 О Н 2 О= 1/2 Н 2+О 2 Воды не образуется вода не разлагается
 3) Зависимость от внешних условий Н 2+О 2=1/2 Н 2 О – состояние ложного равновесия переход в другое состояние – скачкообразный Синтез воды при достижении критической температуры происходит со взрывом Электролиз 1/2 Н 2 О = Н 2+О 2
3) Зависимость от внешних условий Н 2+О 2=1/2 Н 2 О – состояние ложного равновесия переход в другое состояние – скачкообразный Синтез воды при достижении критической температуры происходит со взрывом Электролиз 1/2 Н 2 О = Н 2+О 2
 Обратимые реакции • Карбонатная буферная система Мирового океана
Обратимые реакции • Карбонатная буферная система Мирового океана
 Практически необратимые реакции 1) сжигание органического топлива; 2) реакции осаждения тяжелых металлов в сточных водах; 3) реакции известкования почвы и воды
Практически необратимые реакции 1) сжигание органического топлива; 2) реакции осаждения тяжелых металлов в сточных водах; 3) реакции известкования почвы и воды
 Основные законы состояния истинного равновесия Принцип Ле Шателье-Брауна: если в равновесной системе изменить внешние условия, то равновесие смешается так, чтобы эффект внешнего воздействия уменьшался. N 2 + 3 H 2 2 NH 3
Основные законы состояния истинного равновесия Принцип Ле Шателье-Брауна: если в равновесной системе изменить внешние условия, то равновесие смешается так, чтобы эффект внешнего воздействия уменьшался. N 2 + 3 H 2 2 NH 3
 Закон действующих масс Кинетическое представление – Гульдберг и Ваге, 1867; Термодинамический вывод Вант-Гофф, 1885.
Закон действующих масс Кинетическое представление – Гульдберг и Ваге, 1867; Термодинамический вывод Вант-Гофф, 1885.
 Для гомогенных равновесных систем
Для гомогенных равновесных систем
 Для гетерогенных систем
Для гетерогенных систем
 Направление химических реакций
Направление химических реакций
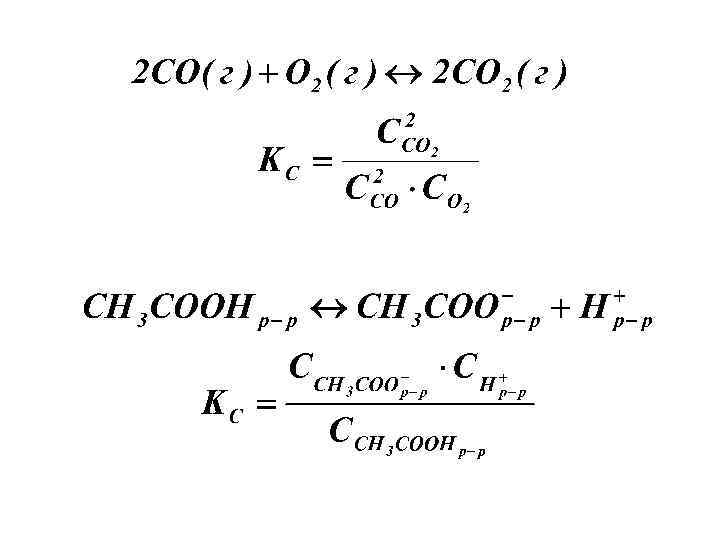 КТ 1 и КТ 2 -константы равновесия химической реакции при температурах Т 1 и Т 2 соответственно.
КТ 1 и КТ 2 -константы равновесия химической реакции при температурах Т 1 и Т 2 соответственно.
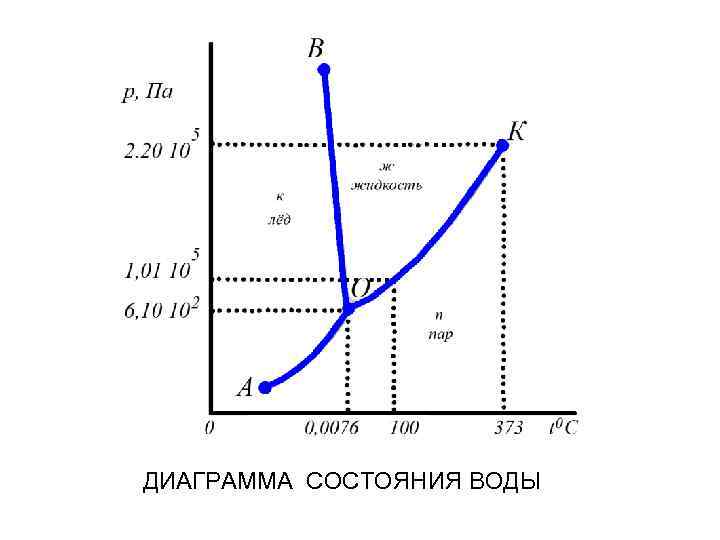
 ДИАГРАММА СОСТОЯНИЯ ВОДЫ
ДИАГРАММА СОСТОЯНИЯ ВОДЫ
 ПРАВИЛО ФАЗ ГИББСА С+Ф=К+2 Фаза Ф Число компонентов К К=s-n-m Число степеней свободы С
ПРАВИЛО ФАЗ ГИББСА С+Ф=К+2 Фаза Ф Число компонентов К К=s-n-m Число степеней свободы С





