 Кинетика химических реакций
Кинетика химических реакций
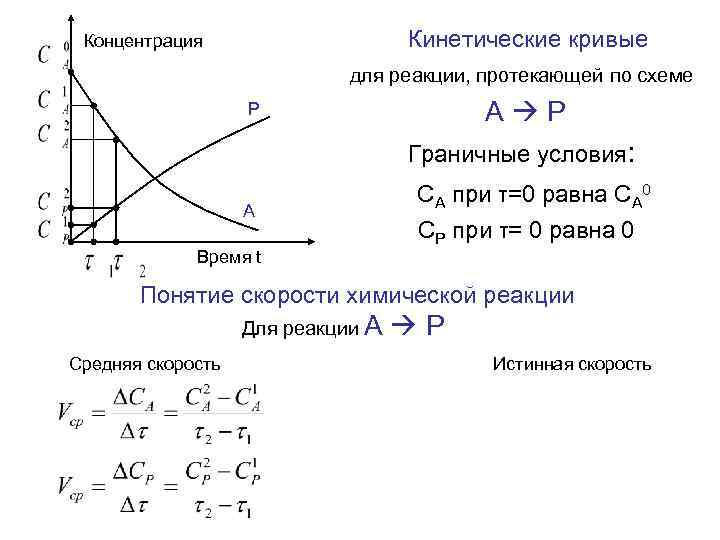 Концентрация Кинетические кривые для реакции, протекающей по схеме P А Р Граничные условия: СА при τ=0 равна СА 0 A CР при τ= 0 равна 0 Время t Понятие скорости химической реакции Для реакции А Р Средняя скорость Истинная скорость
Концентрация Кинетические кривые для реакции, протекающей по схеме P А Р Граничные условия: СА при τ=0 равна СА 0 A CР при τ= 0 равна 0 Время t Понятие скорости химической реакции Для реакции А Р Средняя скорость Истинная скорость
 Порядок химической реакции Для элементарной химической реакции, протекающей по схеме k а 1 А 1+а 2 А 2+…+аi. Ai+… p 1 P 1+p 2 P 2+…+pj. Pj+… i=1, …n j=1, …m Порядок химической реакции по i-тому компоненту ni = ai Суммарный порядок химической реакции n∑ = n 1 + n 2 + … + ni = ∑ ni i =1
Порядок химической реакции Для элементарной химической реакции, протекающей по схеме k а 1 А 1+а 2 А 2+…+аi. Ai+… p 1 P 1+p 2 P 2+…+pj. Pj+… i=1, …n j=1, …m Порядок химической реакции по i-тому компоненту ni = ai Суммарный порядок химической реакции n∑ = n 1 + n 2 + … + ni = ∑ ni i =1
 Молекулярность химической реакции • Молекулярность химической реакции – число частиц, участвующих в единичном акте этой реакции. • Молекулярность всей химической реакции определяется молекулярностью самой медленной стадии. Примеры реакций с различной молекулярностью Мономолекулярная реакция N 2 O 5 NO 2 + NO + O 2 Бимолекулярная реакция Тримолекулярная реакция N 2 O 3 + N 2 O 5 4 NO 2 Редкий случай, на практике, как правило, не реализуется. Примеры тримолекулярных реакций с Внешне бимолекулярная реакция участием NO: в действительности является 2 NO + Cl 2 2 NOCl мономолекулярной: 2 NO + Br 2 2 NOBr 2 N 2 O 5 4 NO 2 + O 2 2 NO + H 2 N 2 O + H 2 O Тримолекулярной является ре- N 2 O 5 N 2 O 3 + O 2 (медленно) акция образования озона в страто- сфере N 2 O 3 + N 2 O 5 4 NO 2 (быстро) O 2 + O + M O 3 + M *
Молекулярность химической реакции • Молекулярность химической реакции – число частиц, участвующих в единичном акте этой реакции. • Молекулярность всей химической реакции определяется молекулярностью самой медленной стадии. Примеры реакций с различной молекулярностью Мономолекулярная реакция N 2 O 5 NO 2 + NO + O 2 Бимолекулярная реакция Тримолекулярная реакция N 2 O 3 + N 2 O 5 4 NO 2 Редкий случай, на практике, как правило, не реализуется. Примеры тримолекулярных реакций с Внешне бимолекулярная реакция участием NO: в действительности является 2 NO + Cl 2 2 NOCl мономолекулярной: 2 NO + Br 2 2 NOBr 2 N 2 O 5 4 NO 2 + O 2 2 NO + H 2 N 2 O + H 2 O Тримолекулярной является ре- N 2 O 5 N 2 O 3 + O 2 (медленно) акция образования озона в страто- сфере N 2 O 3 + N 2 O 5 4 NO 2 (быстро) O 2 + O + M O 3 + M *
 Факторы, влияющие на скорость химической реакции Концентрация реагирующих веществ для химической реакции а 1 А 1+а 2 А 2+…+аn. An продукты Основной закон химической кинетики – закон действующих масс. «Скорость химической реакции (k) прямопропорциональна произведению концентраций реагирующих веществ в степенях, соответствующих стехиометрическим коэффициентам» . (Гульберг, Вааге, 1867 г. ) k – коэффициент пропорциональности – константа скорости химической реакции
Факторы, влияющие на скорость химической реакции Концентрация реагирующих веществ для химической реакции а 1 А 1+а 2 А 2+…+аn. An продукты Основной закон химической кинетики – закон действующих масс. «Скорость химической реакции (k) прямопропорциональна произведению концентраций реагирующих веществ в степенях, соответствующих стехиометрическим коэффициентам» . (Гульберг, Вааге, 1867 г. ) k – коэффициент пропорциональности – константа скорости химической реакции
 Факторы, влияющие на скорость химической реакции Температура • Правило Вакт-Гоффа: при увеличении температуры на 100 скорость химической реакции возрастает в 2 -4 раза - температурный коэффициент или - скорость реакции при температуре t 2 и t 1 - продолжительность реакции при температуре t 2 и t 1 • Уравнение Аррениуса или ΔЕ – энергия активации [Дж/моль]
Факторы, влияющие на скорость химической реакции Температура • Правило Вакт-Гоффа: при увеличении температуры на 100 скорость химической реакции возрастает в 2 -4 раза - температурный коэффициент или - скорость реакции при температуре t 2 и t 1 - продолжительность реакции при температуре t 2 и t 1 • Уравнение Аррениуса или ΔЕ – энергия активации [Дж/моль]
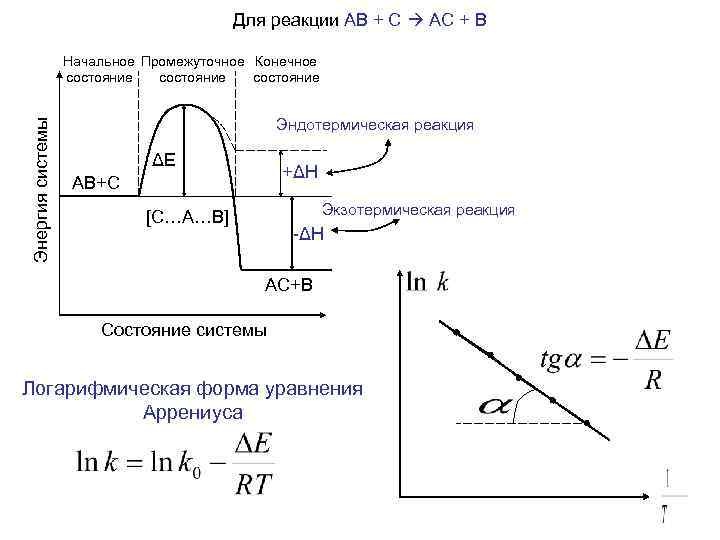 Для реакции АВ + С АС + В Начальное Промежуточное Конечное состояние Эндотермическая реакция Энергия системы ΔE +ΔH AB+C [C…A…B] Экзотермическая реакция -ΔH AC+B Состояние системы Логарифмическая форма уравнения Аррениуса
Для реакции АВ + С АС + В Начальное Промежуточное Конечное состояние Эндотермическая реакция Энергия системы ΔE +ΔH AB+C [C…A…B] Экзотермическая реакция -ΔH AC+B Состояние системы Логарифмическая форма уравнения Аррениуса
 Кинетическая классификация химических реакций Концентрация Необратимая реакция первого порядка B A Время Концентрация Необратимая реакция второго порядка С D A B Время
Кинетическая классификация химических реакций Концентрация Необратимая реакция первого порядка B A Время Концентрация Необратимая реакция второго порядка С D A B Время
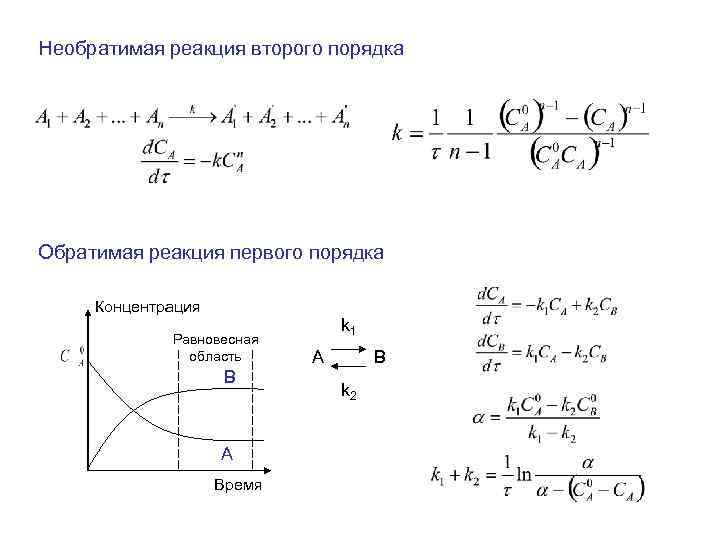 Необратимая реакция второго порядка Обратимая реакция первого порядка Концентрация k 1 Равновесная область A B k 2 A Время
Необратимая реакция второго порядка Обратимая реакция первого порядка Концентрация k 1 Равновесная область A B k 2 A Время
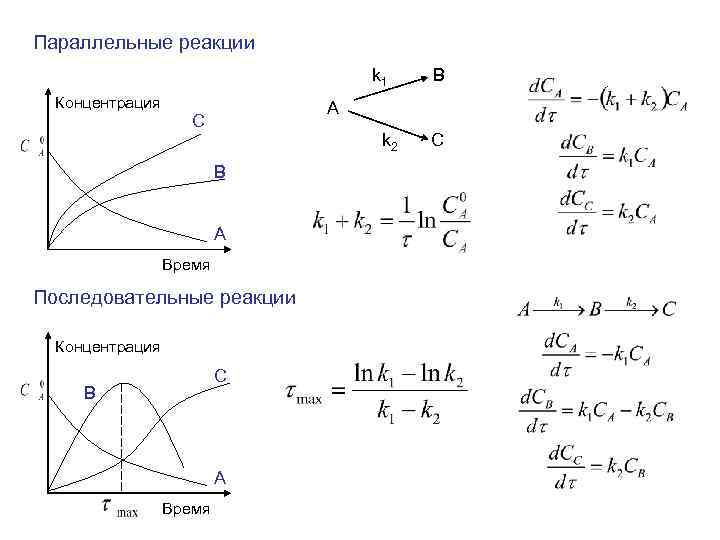 Параллельные реакции k 1 B Концентрация A С k 2 C B A Время Последовательные реакции Концентрация С B A Время
Параллельные реакции k 1 B Концентрация A С k 2 C B A Время Последовательные реакции Концентрация С B A Время





















