КИНЕТИКА ХИМИЧЕСКИХ ПРОЦЕССОВ ОСНОВНЫЕ ПОНЯТИЯ















![Путь реакции [начальное] [переходное] [конечное] активированный Путь реакции [начальное] [переходное] [конечное] активированный](https://present5.com/presentation/3/52606873_265453301.pdf-img/52606873_265453301.pdf-16.jpg)






КИНЕТИКА ХИМИЧЕСКИХ ПРОЦЕССОВ.ppt
- Количество слайдов: 25
 КИНЕТИКА ХИМИЧЕСКИХ ПРОЦЕССОВ
КИНЕТИКА ХИМИЧЕСКИХ ПРОЦЕССОВ
 ОСНОВНЫЕ ПОНЯТИЯ В КИНЕТИКЕ: • Система - вещество или совокупность веществ, реально или мысленно отделённых от окружающей среды. • Фаза - часть системы отделённая от других её частей поверхностью раздела при переходе через которую свойства изменяются скачкаобразно. • Гомогенная система - система, состоящая из одной фазы (воздух, состоящий из кислорода, азота, и др. веществ) • Гетерогенная система - система, состоящая из нескольких фаз (нефть - смесь углеводородов и воды)
ОСНОВНЫЕ ПОНЯТИЯ В КИНЕТИКЕ: • Система - вещество или совокупность веществ, реально или мысленно отделённых от окружающей среды. • Фаза - часть системы отделённая от других её частей поверхностью раздела при переходе через которую свойства изменяются скачкаобразно. • Гомогенная система - система, состоящая из одной фазы (воздух, состоящий из кислорода, азота, и др. веществ) • Гетерогенная система - система, состоящая из нескольких фаз (нефть - смесь углеводородов и воды)
 • Скорость гомогенной реакции – количество вещества, вступающего в реакцию или образующегося при реакции за единицу времени в единице объёма системы ∆n – изменение количества вещества, ∆τ – время реакции, V – объём системы.
• Скорость гомогенной реакции – количество вещества, вступающего в реакцию или образующегося при реакции за единицу времени в единице объёма системы ∆n – изменение количества вещества, ∆τ – время реакции, V – объём системы.
 • Скорость гетерогенной реакции – количество вещества, вступающего в реакцию или образующегося при реакции за единицу времени на единице площади раздела фаз: S – площадь раздела фаз
• Скорость гетерогенной реакции – количество вещества, вступающего в реакцию или образующегося при реакции за единицу времени на единице площади раздела фаз: S – площадь раздела фаз
 Скорость химической реакции зависит от: • концентрации реагирующих веществ • температуры системы • природы реагирующих веществ Зависимость скорости реакции от концентрации реагирующих веществ сформулирована в законе действующих масс «при постоянной температуре, скорость химической реакции пропорциональна произведению концентрации реагирующих веществ в степенях соответствующих их стехиометрическим коэффициентам
Скорость химической реакции зависит от: • концентрации реагирующих веществ • температуры системы • природы реагирующих веществ Зависимость скорости реакции от концентрации реагирующих веществ сформулирована в законе действующих масс «при постоянной температуре, скорость химической реакции пропорциональна произведению концентрации реагирующих веществ в степенях соответствующих их стехиометрическим коэффициентам
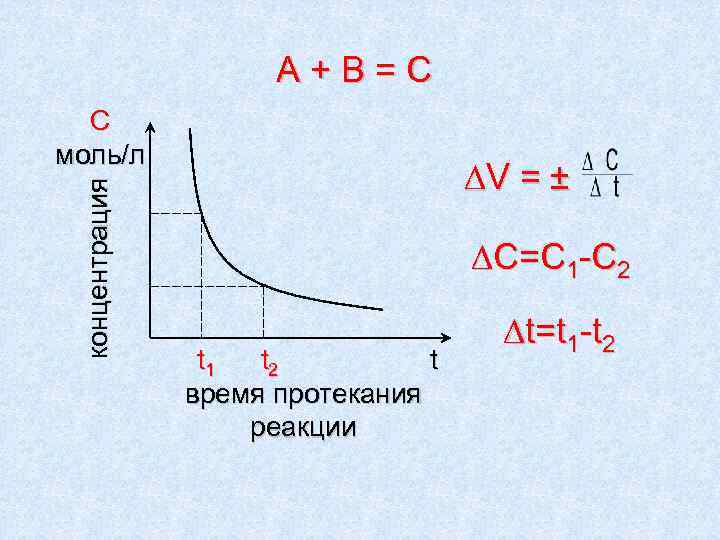
 A+В=С С моль/л ∆V = ± концентрация ∆C=C 1 -C 2 ∆t=t 1 -t 2 t 1 t 2 t время протекания реакции
A+В=С С моль/л ∆V = ± концентрация ∆C=C 1 -C 2 ∆t=t 1 -t 2 t 1 t 2 t время протекания реакции
 Для реакции: m. A + n. B → продукты Скорость реакции запишется: k – константа скорости, [A], [B] – концентрации веществ А и В m, n – стехиометрические коэффициенты
Для реакции: m. A + n. B → продукты Скорость реакции запишется: k – константа скорости, [A], [B] – концентрации веществ А и В m, n – стехиометрические коэффициенты
 Говорят, что реакция имеет порядок “m” по реагенту A и порядок “n” по реагенту В. Закон действующих масс справедлив для простейших реакций (общий порядок до 3) Физический смысл константы в том, что при [A]=[B]=1 моль, V=k, т. е. константа скорости – скорость реакции при концентрации реагирующих веществ равных единице. Константа скорости зависит от природы реагирующих веществ и от температуры.
Говорят, что реакция имеет порядок “m” по реагенту A и порядок “n” по реагенту В. Закон действующих масс справедлив для простейших реакций (общий порядок до 3) Физический смысл константы в том, что при [A]=[B]=1 моль, V=k, т. е. константа скорости – скорость реакции при концентрации реагирующих веществ равных единице. Константа скорости зависит от природы реагирующих веществ и от температуры.
 Например: для реакции: • Зависимость скорости реакции от концентрации /кинетическое уравнение/ запишется: • Для гетерогенных систем в кинетическое уравнение входят концентрации только тех веществ, которые находятся в растворе или в газообразной фазе.
Например: для реакции: • Зависимость скорости реакции от концентрации /кинетическое уравнение/ запишется: • Для гетерогенных систем в кинетическое уравнение входят концентрации только тех веществ, которые находятся в растворе или в газообразной фазе.
 Например: Для реакции Кинетическое уравнение запишется: но так как для твёрдых веществ концентрация веществ на поверхности остаётся постоянной, следует: Где kэф – эффективная константа скорости
Например: Для реакции Кинетическое уравнение запишется: но так как для твёрдых веществ концентрация веществ на поверхности остаётся постоянной, следует: Где kэф – эффективная константа скорости
 • Повышение температуры приводит к увеличению скорости реакции, так как увеличивается скорость движения молекул и возрастает число столкновений между молекулами. • Возрастание скорости реакции при нагревании в первом приближении подчиняется следующему правилу “при повышении температуры на 10 градусов, скорость химической реакции возрастает на величину температурного коэффициента:
• Повышение температуры приводит к увеличению скорости реакции, так как увеличивается скорость движения молекул и возрастает число столкновений между молекулами. • Возрастание скорости реакции при нагревании в первом приближении подчиняется следующему правилу “при повышении температуры на 10 градусов, скорость химической реакции возрастает на величину температурного коэффициента:
 Зависимость скорости реакции от температуры в этом случае выражается уравнением Вант-Гоффа: Vt 2 – cкорость реакции при температуре t 2 Vt 1 – cкорость реакции при температуре t 1 γ – температурный коэффициент
Зависимость скорости реакции от температуры в этом случае выражается уравнением Вант-Гоффа: Vt 2 – cкорость реакции при температуре t 2 Vt 1 – cкорость реакции при температуре t 1 γ – температурный коэффициент
 Например: Температурный коэффициент реакции равен 2. Температура системы повысилась на 30°. Скорость реакции возросла:
Например: Температурный коэффициент реакции равен 2. Температура системы повысилась на 30°. Скорость реакции возросла:
 Молекулы, обладающие необходимым запасом энергии называется активированными молекулами. Избыточная энергия называется энергией активации(Еа) Зависимость скорости реакции от температуры выражается уравнением Аррениуса.
Молекулы, обладающие необходимым запасом энергии называется активированными молекулами. Избыточная энергия называется энергией активации(Еа) Зависимость скорости реакции от температуры выражается уравнением Аррениуса.
 Уравнение Аррениуса K – константа скорости реакции, Еа – энергия активации, R – газовая постоянная, Т – температура, °К, е – основание натурального логарифма.
Уравнение Аррениуса K – константа скорости реакции, Еа – энергия активации, R – газовая постоянная, Т – температура, °К, е – основание натурального логарифма.
![> Путь реакции [начальное] [переходное] [конечное] активированный > Путь реакции [начальное] [переходное] [конечное] активированный](https://present5.com/presentation/3/52606873_265453301.pdf-img/52606873_265453301.pdf-16.jpg) Путь реакции [начальное] [переходное] [конечное] активированный состояние комплекс состояние A 2 + B 2 = 2 AB ∆G<0 A–A A -|- A A + ¦ ¦ + B–B B -|- B B начальное переходное конечное (активированный комплекс)
Путь реакции [начальное] [переходное] [конечное] активированный состояние комплекс состояние A 2 + B 2 = 2 AB ∆G<0 A–A A -|- A A + ¦ ¦ + B–B B -|- B B начальное переходное конечное (активированный комплекс)
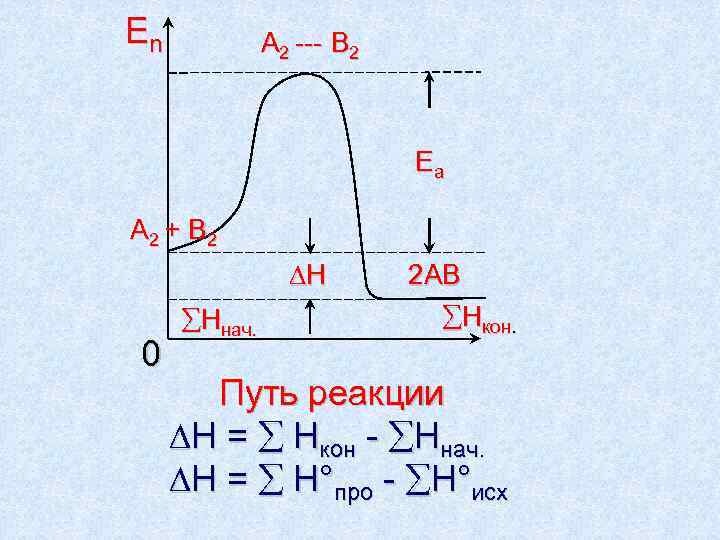
 En A 2 --- B 2 Ea A 2 + B 2 ∆H 2 AB Hнач. Hкон. 0 Путь реакции ∆H = Hкон - Hнач. ∆H = H°про - H°исх
En A 2 --- B 2 Ea A 2 + B 2 ∆H 2 AB Hнач. Hкон. 0 Путь реакции ∆H = Hкон - Hнач. ∆H = H°про - H°исх
 Уравнение связывающие константу скорости с энергией активации и энтропией активации
Уравнение связывающие константу скорости с энергией активации и энтропией активации
 Катализаторы – это вещества, изменяющие скорость химической реакции за счёт проведения её через ряд промежуточных циклов
Катализаторы – это вещества, изменяющие скорость химической реакции за счёт проведения её через ряд промежуточных циклов
 Отрицательные катализаторы (ингибиторы) замедляют скорость химической реакции за счёт подавления одного из возможных путей реакции. Положительные катализаторы увеличивают скорость химической реакции за счет проведения её по новому пути с меньшей энергией активации.
Отрицательные катализаторы (ингибиторы) замедляют скорость химической реакции за счёт подавления одного из возможных путей реакции. Положительные катализаторы увеличивают скорость химической реакции за счет проведения её по новому пути с меньшей энергией активации.
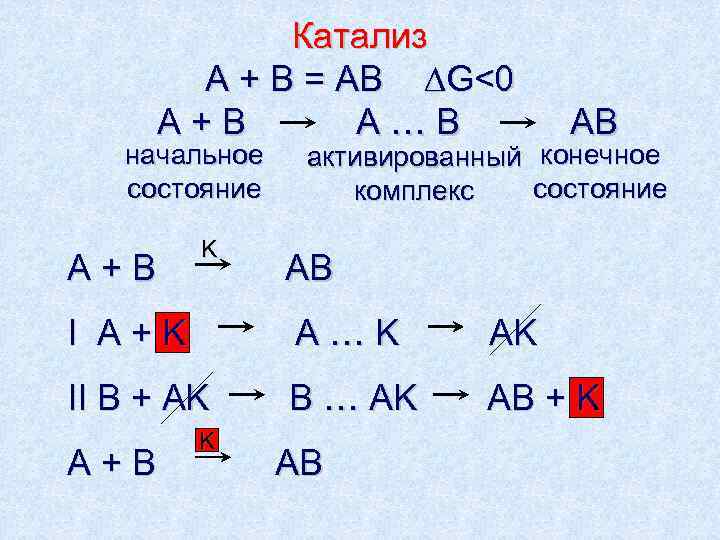
 Катализ A + В = АВ ∆G<0 A+B A…B AB начальное активированный конечное состояние комплекс состояние K A+B AB I A+K A…K AK II B + AK B … AK AB + K K A+B AB
Катализ A + В = АВ ∆G<0 A+B A…B AB начальное активированный конечное состояние комплекс состояние K A+B AB I A+K A…K AK II B + AK B … AK AB + K K A+B AB
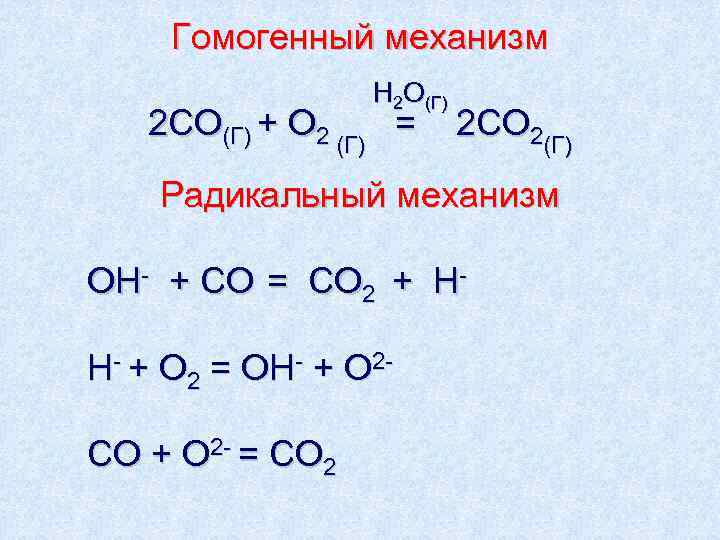
 Гомогенный механизм H 2 O (Г ) 2 СO(Г) + О 2 (Г) = 2 С O 2 (Г ) Радикальный механизм OH- + CO = CO 2 + H- H- + O 2 = OH- + O 2 - CO + O 2 - = CO 2
Гомогенный механизм H 2 O (Г ) 2 СO(Г) + О 2 (Г) = 2 С O 2 (Г ) Радикальный механизм OH- + CO = CO 2 + H- H- + O 2 = OH- + O 2 - CO + O 2 - = CO 2
 Молекулярный механизм NO(Г) 2 SO 2(Г)+ О 2 (Г) = 2 SO 3(Г) – гомоген. I NO + 1/2 + O 2 = NO 2 II NO 2 + SO 2 = SO 3 + NO
Молекулярный механизм NO(Г) 2 SO 2(Г)+ О 2 (Г) = 2 SO 3(Г) – гомоген. I NO + 1/2 + O 2 = NO 2 II NO 2 + SO 2 = SO 3 + NO
 Гетерогенный V 2 O 5 2 SO 2(Г)+ О 2 (Г) = (тв) 2 SO 3(Г) 5 стадий 1. транспорт вещества к поверхности катализатора 2. адсорбция 3. реакция на поверхности катализатора 4. десорбция 5. транспорт вещества с поверхности катализатора
Гетерогенный V 2 O 5 2 SO 2(Г)+ О 2 (Г) = (тв) 2 SO 3(Г) 5 стадий 1. транспорт вещества к поверхности катализатора 2. адсорбция 3. реакция на поверхности катализатора 4. десорбция 5. транспорт вещества с поверхности катализатора
 Для реальных процессов энергия активации в пределах 44 -120 к. Дж/моль. Для процессов с Еа<40 к. Дж/моль скорость реакции характеризуется взрывом, процессы Еа>120 к. Дж/моль практически не идут.
Для реальных процессов энергия активации в пределах 44 -120 к. Дж/моль. Для процессов с Еа<40 к. Дж/моль скорость реакции характеризуется взрывом, процессы Еа>120 к. Дж/моль практически не идут.

