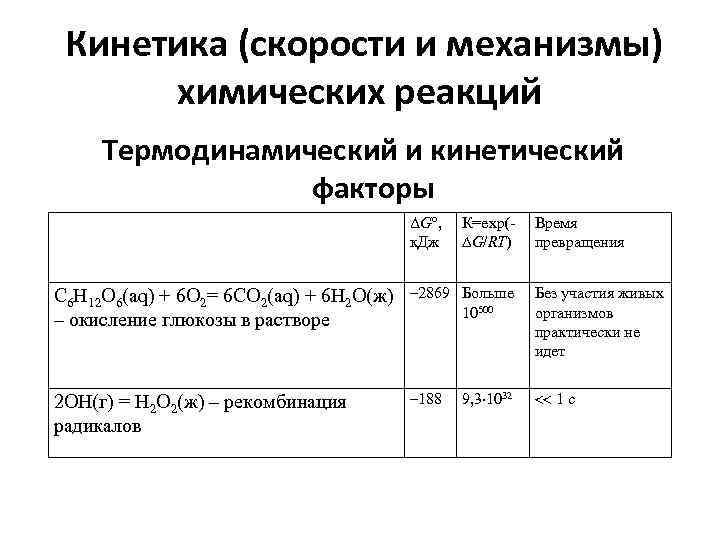
 Кинетика (скорости и механизмы) химических реакций Термодинамический и кинетический факторы ΔG , к. Дж К=exp( G/RT) Время превращения С 6 Н 12 О 6(aq) + 6 О 2= 6 СО 2(aq) + 6 Н 2 О(ж) – окисление глюкозы в растворе 2869 Больше 10500 Без участия живых организмов практически не идет 2 ОН(г) = Н 2 О 2(ж) – рекомбинация радикалов 188 1 с 9, 3 1032
Кинетика (скорости и механизмы) химических реакций Термодинамический и кинетический факторы ΔG , к. Дж К=exp( G/RT) Время превращения С 6 Н 12 О 6(aq) + 6 О 2= 6 СО 2(aq) + 6 Н 2 О(ж) – окисление глюкозы в растворе 2869 Больше 10500 Без участия живых организмов практически не идет 2 ОН(г) = Н 2 О 2(ж) – рекомбинация радикалов 188 1 с 9, 3 1032
 Молекулярность химической реакции – число частиц в единичном столкновении реакции МОНОМОЛЕКУЛЯРНЫЕ J 2 ↔ 2 J Ca. CO 3 → Ca. O + CO 2 • БИМОЛЕКУЛЯРНЫЕ • H 2 + J 2 ↔ 2 HJ • ТРИМОЛЕКУЛЯРНЫЕ H 2 + 2 NO → N 2 O + H 2 O • ? • 4 NH 3 + 5 O 2 → 4 NO + 6 H 2 O
Молекулярность химической реакции – число частиц в единичном столкновении реакции МОНОМОЛЕКУЛЯРНЫЕ J 2 ↔ 2 J Ca. CO 3 → Ca. O + CO 2 • БИМОЛЕКУЛЯРНЫЕ • H 2 + J 2 ↔ 2 HJ • ТРИМОЛЕКУЛЯРНЫЕ H 2 + 2 NO → N 2 O + H 2 O • ? • 4 NH 3 + 5 O 2 → 4 NO + 6 H 2 O
 Классификация реакций • простые реакции - осуществляются посредством однотипных элементарных актов • сложные реакции осуществляются посредством разнотипных элементарных актов (последовательных, параллельных, последовательно-параллельных, цепных, сопряженных и т. д. ) • лимитирующая стадия реакции – элементарный акт, определяющий скорость реакции в целом: для строго последовательных реакций – это самая медленная стадия; для строго параллельных реакций – самая быстрая.
Классификация реакций • простые реакции - осуществляются посредством однотипных элементарных актов • сложные реакции осуществляются посредством разнотипных элементарных актов (последовательных, параллельных, последовательно-параллельных, цепных, сопряженных и т. д. ) • лимитирующая стадия реакции – элементарный акт, определяющий скорость реакции в целом: для строго последовательных реакций – это самая медленная стадия; для строго параллельных реакций – самая быстрая.
 Скорость реакции (Vr) • Скорость реакции (Vr) – изменение количества исходных веществ или продуктов реакции, происходящие в единицу времени (τ) в единице объема (для гомогенных реакций) • или на единице площади поверхности (для гетерогенных реакций).
Скорость реакции (Vr) • Скорость реакции (Vr) – изменение количества исходных веществ или продуктов реакции, происходящие в единицу времени (τ) в единице объема (для гомогенных реакций) • или на единице площади поверхности (для гетерогенных реакций).
 Скорость реакции • • • зависит от факторов: природы реагирующих веществ; концентрации реагирующих веществ; температуры; наличия катализатора; величины поверхности раздела фаз (для гетерогенных реакций);
Скорость реакции • • • зависит от факторов: природы реагирующих веществ; концентрации реагирующих веществ; температуры; наличия катализатора; величины поверхности раздела фаз (для гетерогенных реакций);
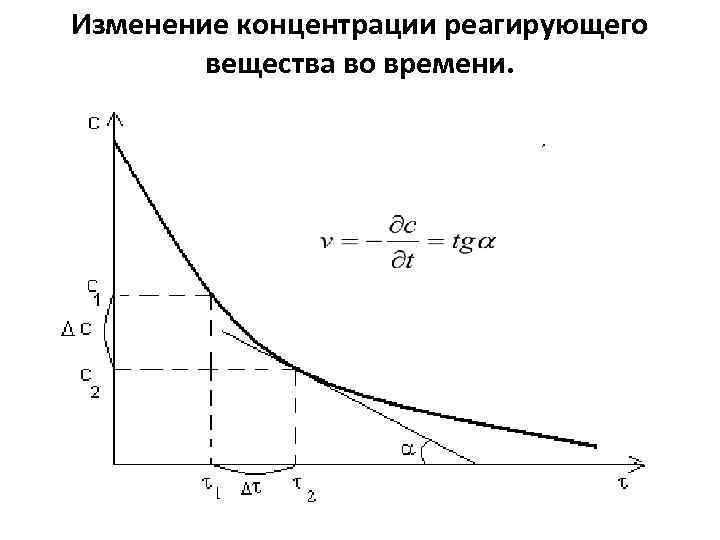 Изменение концентрации реагирующего вещества во времени.
Изменение концентрации реагирующего вещества во времени.
 Зависимость скорости реакции от концентрации реагирующих веществ • Средняя скорость реакции • Истинная скорость реакции
Зависимость скорости реакции от концентрации реагирующих веществ • Средняя скорость реакции • Истинная скорость реакции
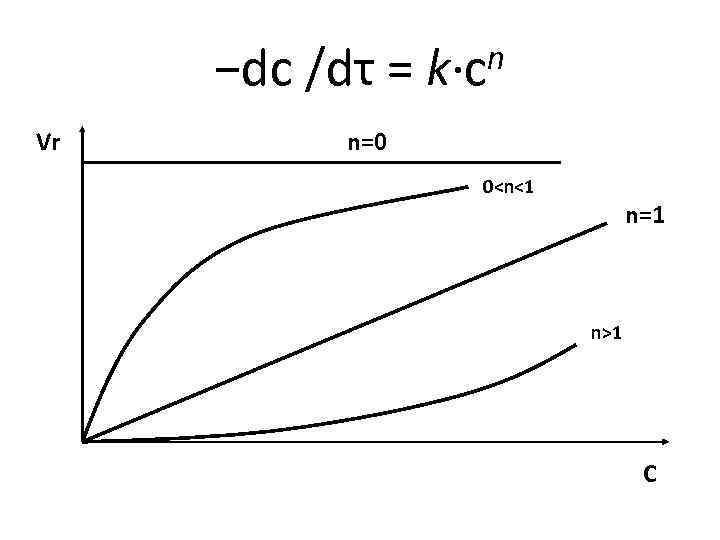 n −dc /dτ = k·c Vr n=0 01 C
n −dc /dτ = k·c Vr n=0 01 C
 Дифференциальные и интегральные уравнения для реакций различного порядка Дифференциальное Интегральное кинетическое уравнение Период полупревращени я (τ0, 5) n 1 2 0 −dc /dτ = k·c lnco/cτ = k·τ τ0, 5= ln 2/k −dc /dτ =k·c 2 1/cτ− 1/co = k·τ τ0, 5=1/k·co −dc /dτ = k co − cτ = k·τ τ0, 5= co/2 k
Дифференциальные и интегральные уравнения для реакций различного порядка Дифференциальное Интегральное кинетическое уравнение Период полупревращени я (τ0, 5) n 1 2 0 −dc /dτ = k·c lnco/cτ = k·τ τ0, 5= ln 2/k −dc /dτ =k·c 2 1/cτ− 1/co = k·τ τ0, 5=1/k·co −dc /dτ = k co − cτ = k·τ τ0, 5= co/2 k
 «частный порядок» реакции a. А + b. В → d. D v = −dc(А) /dτ = −dc(В) /dτ p·c(B)q = k·c(A) c(A), c(B) – концентрации реагентов, моль/л; k – константа скорости реакции, равная скорости при концентрациях реагирующих веществ 1 моль/л; p – порядок реакции по реагенту А; q – порядок реакции по реагенту В.
«частный порядок» реакции a. А + b. В → d. D v = −dc(А) /dτ = −dc(В) /dτ p·c(B)q = k·c(A) c(A), c(B) – концентрации реагентов, моль/л; k – константа скорости реакции, равная скорости при концентрациях реагирующих веществ 1 моль/л; p – порядок реакции по реагенту А; q – порядок реакции по реагенту В.
 Молекулярность и порядок реакции COCl 2 CO + Cl 2 реакция сложная и обратимая в данных условиях n = 1, 5
Молекулярность и порядок реакции COCl 2 CO + Cl 2 реакция сложная и обратимая в данных условиях n = 1, 5
 Молекулярность и порядок реакции 2 NO 2 N 2 + 2 O 2 - реакция простая n = 2 и не обратима в данных условиях.
Молекулярность и порядок реакции 2 NO 2 N 2 + 2 O 2 - реакция простая n = 2 и не обратима в данных условиях.
 Истинная и экспериментальная константа H 2 O 2 + 2 I + 2 H+ I 2 + 2 H 2 O I 2 + 2 S 2 O 32 - 2 I- + S 4 O 62 С(I-) = const, C(H+) = const V = K(ист)· С(I-)· C(H+)· C(H 2 O 2 ) K(эксп) =K(ист)· С(I-)· C(H+) V = K(эксп) ·C(H 2 O 2)
Истинная и экспериментальная константа H 2 O 2 + 2 I + 2 H+ I 2 + 2 H 2 O I 2 + 2 S 2 O 32 - 2 I- + S 4 O 62 С(I-) = const, C(H+) = const V = K(ист)· С(I-)· C(H+)· C(H 2 O 2 ) K(эксп) =K(ист)· С(I-)· C(H+) V = K(эксп) ·C(H 2 O 2)
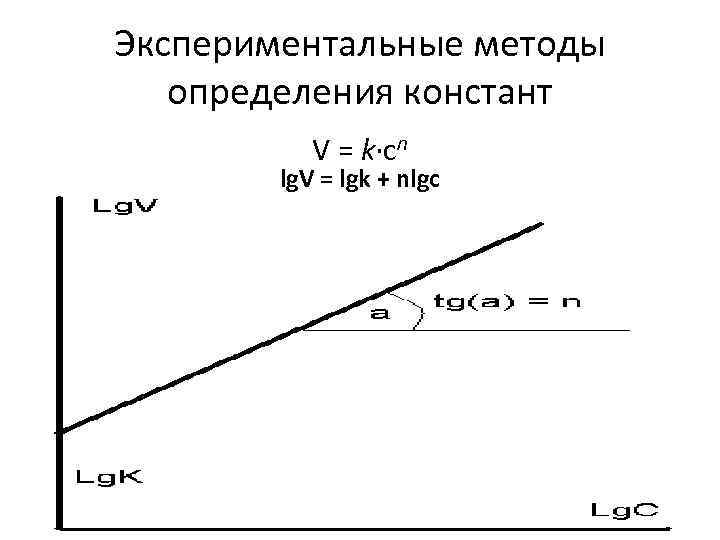 Экспериментальные методы определения констант V = k·cn lg. V = lgk + nlgc
Экспериментальные методы определения констант V = k·cn lg. V = lgk + nlgc