2. Энергия активации.ppt
- Количество слайдов: 8
 Кинетика процессов горения Энергия активации Тепловой эффект реакции
Кинетика процессов горения Энергия активации Тепловой эффект реакции
 Энергия активации Согласно молекулярно-кинетической теории химическая реакция представляет собой процесс разрушения старых молекулярных связей вещества и создание новых. l В любом выделенном объёме, имеющем постоянную температуру, отдельные молекулы вещества двигаются с различными скоростями, т. е. имеют разные кинетические энергии. Химическая реакция может протекать только в том случае, если соударение молекул произойдёт с энергией, достаточной для разрушения старых внутримолекулярных связей. l Многие, даже очень быстрые реакции, при простом соприкосновении реагентов не идут. Например, смесь водорода с кислородом может очень долго находиться при комнатной температуре, не вступая в реакцию друг с другом. Но стоит только поднести к ней горящую спичку, как реакция начинает протекать очень быстро, часто со взрывом (поэтому смесь водорода с кислородом в объемном отношении 2: 1 даже называют "гремучим газом"). l
Энергия активации Согласно молекулярно-кинетической теории химическая реакция представляет собой процесс разрушения старых молекулярных связей вещества и создание новых. l В любом выделенном объёме, имеющем постоянную температуру, отдельные молекулы вещества двигаются с различными скоростями, т. е. имеют разные кинетические энергии. Химическая реакция может протекать только в том случае, если соударение молекул произойдёт с энергией, достаточной для разрушения старых внутримолекулярных связей. l Многие, даже очень быстрые реакции, при простом соприкосновении реагентов не идут. Например, смесь водорода с кислородом может очень долго находиться при комнатной температуре, не вступая в реакцию друг с другом. Но стоит только поднести к ней горящую спичку, как реакция начинает протекать очень быстро, часто со взрывом (поэтому смесь водорода с кислородом в объемном отношении 2: 1 даже называют "гремучим газом"). l
 В чем же причина? Как уже отмечалось, не любые соударения молекул или других химических частиц приводят к их взаимодействию, а только эффективные, то есть те соударения частиц, суммарная энергия которых больше какого-то определенного значения. l Эта "пороговая" энергия или минимальная энергия, которую нужно сообщить молекуле, чтобы преодолеть внутримолекулярные силы сцепления, называется энергией активации ЕА данной реакции. l После получения такой энергии внутренние связи в молекуле разрушаются, и она (молекула) становится готовой к образованию нового вещества. l Таким образом, энергию активации можно рассматривать как своего рода энергетический барьер, который необходимо преодолеть, прежде чем произойдёт реакция. l
В чем же причина? Как уже отмечалось, не любые соударения молекул или других химических частиц приводят к их взаимодействию, а только эффективные, то есть те соударения частиц, суммарная энергия которых больше какого-то определенного значения. l Эта "пороговая" энергия или минимальная энергия, которую нужно сообщить молекуле, чтобы преодолеть внутримолекулярные силы сцепления, называется энергией активации ЕА данной реакции. l После получения такой энергии внутренние связи в молекуле разрушаются, и она (молекула) становится готовой к образованию нового вещества. l Таким образом, энергию активации можно рассматривать как своего рода энергетический барьер, который необходимо преодолеть, прежде чем произойдёт реакция. l
 Энергия активации ЕА
Энергия активации ЕА
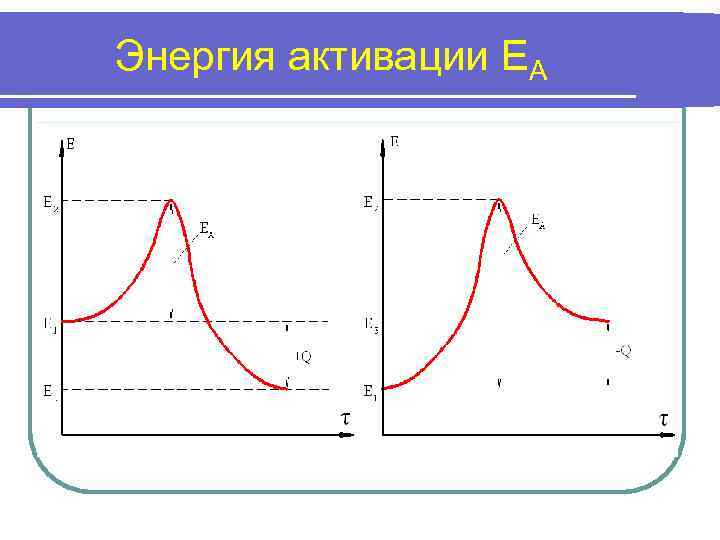
 Тепловой эффект реакции l l l В состоянии (1) молекулы исходных веществ имеют запас внутренней энергии Е 1, недостаточный для разрушения внутримолекулярных связей при их столкновении. Для осуществления прямой реакции к системе необходимо подвести некоторое количество энергии ЕА. Она и является энергией активации прямой реакции. При этом молекулы переходят в состояние (2) с внутренней энергией E 2 = E 1 + EA. В состоянии (2) молекулы при столкновении вступают в химическую реакцию с образованием продуктов реакции и выделением теплоты. После охлаждения продуктов реакции до начальной температуры (точка 3) внутренняя энергия продуктов сгорания (если речь идёт о реакции горения) будет равна Е 3, а количество выделяемой энергии Е 2 – E 3. Разность между выделившейся энергией и энергией активации ЕА , поглощаемой в процессе активизации молекул, представляет собой тепловой эффект реакции Q = E 2 – E 1. Если эта разность положительна (рис. 1 а), т. е. Q > 0 , то реакция экзотермическая, если – отрицательная (рис. 1 б), т. е. Q < 0 , то реакция эндотермическая.
Тепловой эффект реакции l l l В состоянии (1) молекулы исходных веществ имеют запас внутренней энергии Е 1, недостаточный для разрушения внутримолекулярных связей при их столкновении. Для осуществления прямой реакции к системе необходимо подвести некоторое количество энергии ЕА. Она и является энергией активации прямой реакции. При этом молекулы переходят в состояние (2) с внутренней энергией E 2 = E 1 + EA. В состоянии (2) молекулы при столкновении вступают в химическую реакцию с образованием продуктов реакции и выделением теплоты. После охлаждения продуктов реакции до начальной температуры (точка 3) внутренняя энергия продуктов сгорания (если речь идёт о реакции горения) будет равна Е 3, а количество выделяемой энергии Е 2 – E 3. Разность между выделившейся энергией и энергией активации ЕА , поглощаемой в процессе активизации молекул, представляет собой тепловой эффект реакции Q = E 2 – E 1. Если эта разность положительна (рис. 1 а), т. е. Q > 0 , то реакция экзотермическая, если – отрицательная (рис. 1 б), т. е. Q < 0 , то реакция эндотермическая.
 Энергия активации l Очевидно, что если прямая реакция является экзотермической, то обратная будет эндотермической. l Чем выше ЕА, тем труднее осуществить реакцию. C + О 2 = CО 2 ЕА = (25, 6 – 40) ккал/г-моль = (107000 – 167000) к. Дж/кмоль l При высоких температурах возможна реакция восстановления двуокиси углерода у раскалённой поверхности углерода СО 2 + C = 2 CО EА = (32 – 51, 4) ккал/г-моль = (134000 – 215000) к. Дж/кмоль
Энергия активации l Очевидно, что если прямая реакция является экзотермической, то обратная будет эндотермической. l Чем выше ЕА, тем труднее осуществить реакцию. C + О 2 = CО 2 ЕА = (25, 6 – 40) ккал/г-моль = (107000 – 167000) к. Дж/кмоль l При высоких температурах возможна реакция восстановления двуокиси углерода у раскалённой поверхности углерода СО 2 + C = 2 CО EА = (32 – 51, 4) ккал/г-моль = (134000 – 215000) к. Дж/кмоль
 Энергия активации Влияние температуры При повышении температуры увеличивается кинетическая энергия молекул исходных веществ, соответственно уменьшается количество энергии, необходимое для доведения молекул до активного состояния. l Если ЕА невелика, то в исходных веществах всегда найдутся молекулы, которые смогут преодолеть “энергетический барьер” и превратиться в молекулы продуктов реакции. l Если же ЕА велика, то таких молекул в реакторе может и не оказаться. l Таким образом, скорость реакции прочих равных условиях тем больше, чем меньше ее энергия активации. l
Энергия активации Влияние температуры При повышении температуры увеличивается кинетическая энергия молекул исходных веществ, соответственно уменьшается количество энергии, необходимое для доведения молекул до активного состояния. l Если ЕА невелика, то в исходных веществах всегда найдутся молекулы, которые смогут преодолеть “энергетический барьер” и превратиться в молекулы продуктов реакции. l Если же ЕА велика, то таких молекул в реакторе может и не оказаться. l Таким образом, скорость реакции прочих равных условиях тем больше, чем меньше ее энергия активации. l
 Катализаторы На практике часто встречаются случаи, когда необходимо осуществить реакцию, энергия активации которой очень велика. l Скорость такой реакции, естественно, очень мала или практически равна нулю. l Если при этом сильно нагреть реакционную смесь нельзя (например, исходное вещество при таком нагревании разлагается, или равновесие смещается в сторону исходного вещества), то для получения нужного вещества приходится идти "обходным путем", применяя катализаторы. l
Катализаторы На практике часто встречаются случаи, когда необходимо осуществить реакцию, энергия активации которой очень велика. l Скорость такой реакции, естественно, очень мала или практически равна нулю. l Если при этом сильно нагреть реакционную смесь нельзя (например, исходное вещество при таком нагревании разлагается, или равновесие смещается в сторону исходного вещества), то для получения нужного вещества приходится идти "обходным путем", применяя катализаторы. l


