Lecture_2_2014.ppt
- Количество слайдов: 27
 КИНЕТИКА Инженерная химия каталитических процессов
КИНЕТИКА Инженерная химия каталитических процессов
 От молекулярного уровня – до промышленной реализации Изучая новый процесс в лабораторных условиях, исследователь должен быть уверен, что его экспериментальные результаты будут пригодны для экстраполяции к промышленным условиям. 1. В реакторе протекают сильно нелинейные процессы каталитических превращений, которые осложнены процессами переноса тепла и массы в зерне катализатора и объеме реактора, характеризующимися многообразием связей. Взаимное влияние каталитических реакций и процессов тепло- и массопереноса и, соответственно, результаты процесса сильно зависят от размера и типа реактора 2. При создании каталитических реакторов необходим учет процессов массо- и теплопереноса. Если в лабораторном реакторе, при определении каталитических свойств, мы стараемся исключить их влияние, то в промышленном реакторе они имеют определяющее значение. Выбор конструктивных элементов реактора сильно зависит от этого. Как выполнить масштабный переход? 2
От молекулярного уровня – до промышленной реализации Изучая новый процесс в лабораторных условиях, исследователь должен быть уверен, что его экспериментальные результаты будут пригодны для экстраполяции к промышленным условиям. 1. В реакторе протекают сильно нелинейные процессы каталитических превращений, которые осложнены процессами переноса тепла и массы в зерне катализатора и объеме реактора, характеризующимися многообразием связей. Взаимное влияние каталитических реакций и процессов тепло- и массопереноса и, соответственно, результаты процесса сильно зависят от размера и типа реактора 2. При создании каталитических реакторов необходим учет процессов массо- и теплопереноса. Если в лабораторном реакторе, при определении каталитических свойств, мы стараемся исключить их влияние, то в промышленном реакторе они имеют определяющее значение. Выбор конструктивных элементов реактора сильно зависит от этого. Как выполнить масштабный переход? 2
 Как перейти от лабораторного реактора к промышленному ? В реакторе протекают сильно нелинейные процессы каталитических превращений и процессы массо- и теплопереноса. Взаимное влияние химических и физических процессов, и результаты процесса зависят от типа и размера реактора. Разработка реакторов в начале XX века – 99% искусства на основе опыта и инженерной интуиции, 1 % науки. Физическое моделирование - 30 -50 годы XX века Изучение процесса на основе теории подобия. Метод оставался основным методом разработки каталитических реакторов до конца 50 -х годов XX века. Метод “черного ящика” - последовательность пилотных установок, увеличивая размеры, т. о. заполняется дистанция между лабораторным и промышленным масштабом. Математическое моделирование Изучение процесса на математических моделях c целью предсказания их протекания в аппаратах заданной конструкции, т. е. в реальном реакторе. В настоящее время этот метод является теоретической основой промышленного катализа, так как позволяет решать проблемы масштабного перехода. 3
Как перейти от лабораторного реактора к промышленному ? В реакторе протекают сильно нелинейные процессы каталитических превращений и процессы массо- и теплопереноса. Взаимное влияние химических и физических процессов, и результаты процесса зависят от типа и размера реактора. Разработка реакторов в начале XX века – 99% искусства на основе опыта и инженерной интуиции, 1 % науки. Физическое моделирование - 30 -50 годы XX века Изучение процесса на основе теории подобия. Метод оставался основным методом разработки каталитических реакторов до конца 50 -х годов XX века. Метод “черного ящика” - последовательность пилотных установок, увеличивая размеры, т. о. заполняется дистанция между лабораторным и промышленным масштабом. Математическое моделирование Изучение процесса на математических моделях c целью предсказания их протекания в аппаратах заданной конструкции, т. е. в реальном реакторе. В настоящее время этот метод является теоретической основой промышленного катализа, так как позволяет решать проблемы масштабного перехода. 3
 Как перейти от лабораторного реактора к промышленному ? Основы математического моделирования Для корректного использования при масштабировании реактора модель должна адекватно отражать химические превращения и процессы переноса вещества и тепла. Масштабный переход возможен в том случае, когда выделенные составляющие процесса инвариантны к размеру реактора. Это выполнимо, если используется иерархическая структура модели процесса. Иерархия моделей – последовательность все более сложных моделей, отражающих все большее число свойств оригинала. При таком построении модели выделяются масштабные уровни процесса, не зависящие от размера реактора, на каждом из них определяются его составляющие и их взаимное влияние. Процесс на одном масштабном уровне входит как составляющая на следующем. Результаты на одном масштабном уровне не зависят от данных, характеризующих вышестоящий уровень. Такая модель адекватно отражает скорости реакции и явления переноса тепла и массы. 4
Как перейти от лабораторного реактора к промышленному ? Основы математического моделирования Для корректного использования при масштабировании реактора модель должна адекватно отражать химические превращения и процессы переноса вещества и тепла. Масштабный переход возможен в том случае, когда выделенные составляющие процесса инвариантны к размеру реактора. Это выполнимо, если используется иерархическая структура модели процесса. Иерархия моделей – последовательность все более сложных моделей, отражающих все большее число свойств оригинала. При таком построении модели выделяются масштабные уровни процесса, не зависящие от размера реактора, на каждом из них определяются его составляющие и их взаимное влияние. Процесс на одном масштабном уровне входит как составляющая на следующем. Результаты на одном масштабном уровне не зависят от данных, характеризующих вышестоящий уровень. Такая модель адекватно отражает скорости реакции и явления переноса тепла и массы. 4
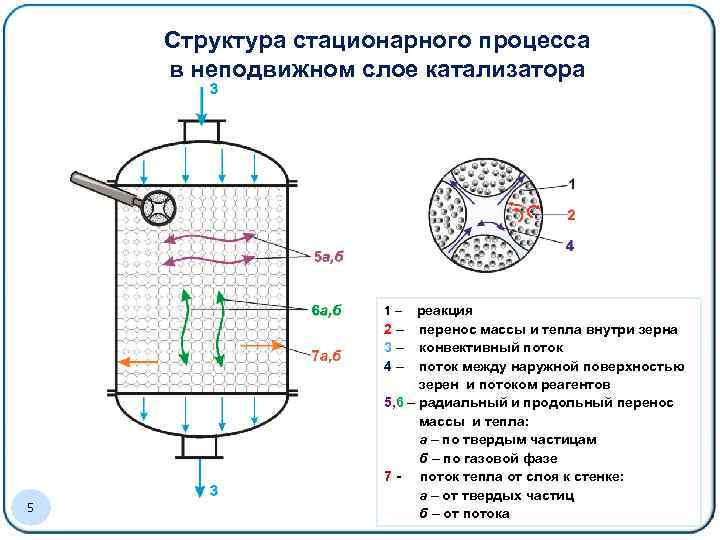 Структура стационарного процесса в неподвижном слое катализатора реакция 2 – перенос массы и тепла внутри зерна 3 – конвективный поток 4 – поток между наружной поверхностью зерен и потоком реагентов 5, 6 – радиальный и продольный перенос массы и тепла: а – по твердым частицам б – по газовой фазе 7 - поток тепла от слоя к стенке: а – от твердых частиц б – от потока 1– 5
Структура стационарного процесса в неподвижном слое катализатора реакция 2 – перенос массы и тепла внутри зерна 3 – конвективный поток 4 – поток между наружной поверхностью зерен и потоком реагентов 5, 6 – радиальный и продольный перенос массы и тепла: а – по твердым частицам б – по газовой фазе 7 - поток тепла от слоя к стенке: а – от твердых частиц б – от потока 1– 5
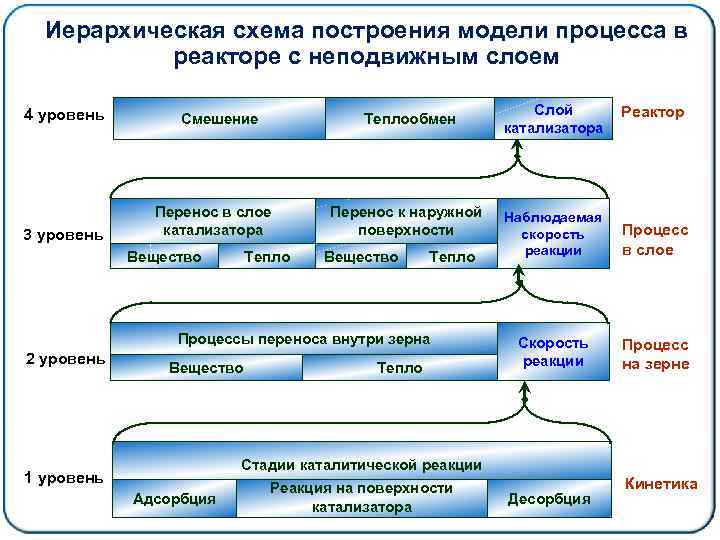 Иерархическая схема построения модели процесса в реакторе с неподвижным слоем 4 уровень 3 уровень Смешение Теплообмен Перенос в слое катализатора Вещество Тепло Перенос к наружной поверхности Вещество Тепло Процессы переноса внутри зерна 2 уровень Вещество Тепло Слой катализатора Реактор Наблюдаемая скорость реакции Процесс в слое Скорость реакции Процесс на зерне Стадии каталитической реакции 1 уровень Адсорбция Реакция на поверхности катализатора Десорбция Кинетика
Иерархическая схема построения модели процесса в реакторе с неподвижным слоем 4 уровень 3 уровень Смешение Теплообмен Перенос в слое катализатора Вещество Тепло Перенос к наружной поверхности Вещество Тепло Процессы переноса внутри зерна 2 уровень Вещество Тепло Слой катализатора Реактор Наблюдаемая скорость реакции Процесс в слое Скорость реакции Процесс на зерне Стадии каталитической реакции 1 уровень Адсорбция Реакция на поверхности катализатора Десорбция Кинетика
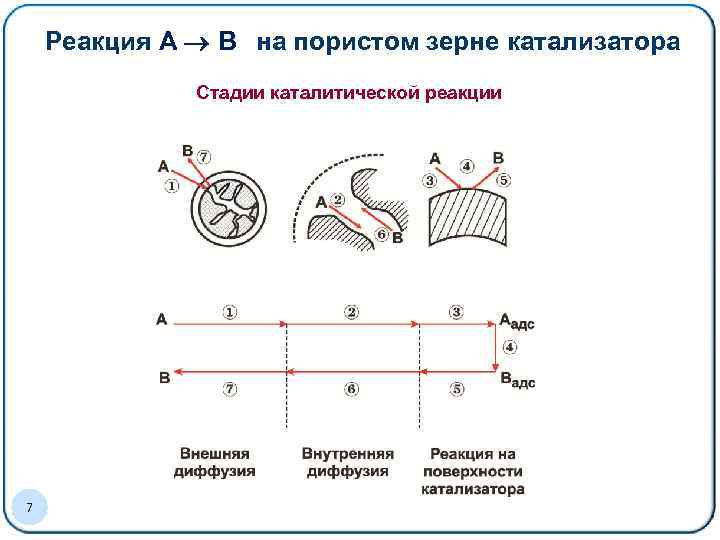 Реакция A B на пористом зерне катализатора Стадии каталитической реакции 7
Реакция A B на пористом зерне катализатора Стадии каталитической реакции 7
 Кинетика каталитической реакции для расчета реактора При расчете слоя катализатора в реакторе нужно вычислить скорости реакций в каждом элементе слоя. Для этого нужна кинетическая модель в виде выражений для скоростей реакции, отражающих зависимость от рабочих условий - температуры, давления, концентраций реагентов. Кинетическая модель – система уравнений, описывающая скорости реакции в условиях, где отсутствует сопротивление массо- и теплопереносу скоростей реакции в зависимости от: а) концентраций реагирующих веществ в газовой фазе и на поверхности катализатора, б) температуры, в) давления, изменяющихся во всей области параметров, которые встречаются при практической реализации процесса. 8
Кинетика каталитической реакции для расчета реактора При расчете слоя катализатора в реакторе нужно вычислить скорости реакций в каждом элементе слоя. Для этого нужна кинетическая модель в виде выражений для скоростей реакции, отражающих зависимость от рабочих условий - температуры, давления, концентраций реагентов. Кинетическая модель – система уравнений, описывающая скорости реакции в условиях, где отсутствует сопротивление массо- и теплопереносу скоростей реакции в зависимости от: а) концентраций реагирующих веществ в газовой фазе и на поверхности катализатора, б) температуры, в) давления, изменяющихся во всей области параметров, которые встречаются при практической реализации процесса. 8
 Общий вид кинетической модели Кинетические исследования включают: а) Экспериментальное определение скоростей реакций при отсутствии влияния процессов массо- и теплопереноса б) Вывод и отбор адекватных кинетических уравнений в) Решение обратной задачи - определение констант и энергий активаций Кинетические модели для стационарных условий: 9
Общий вид кинетической модели Кинетические исследования включают: а) Экспериментальное определение скоростей реакций при отсутствии влияния процессов массо- и теплопереноса б) Вывод и отбор адекватных кинетических уравнений в) Решение обратной задачи - определение констант и энергий активаций Кинетические модели для стационарных условий: 9
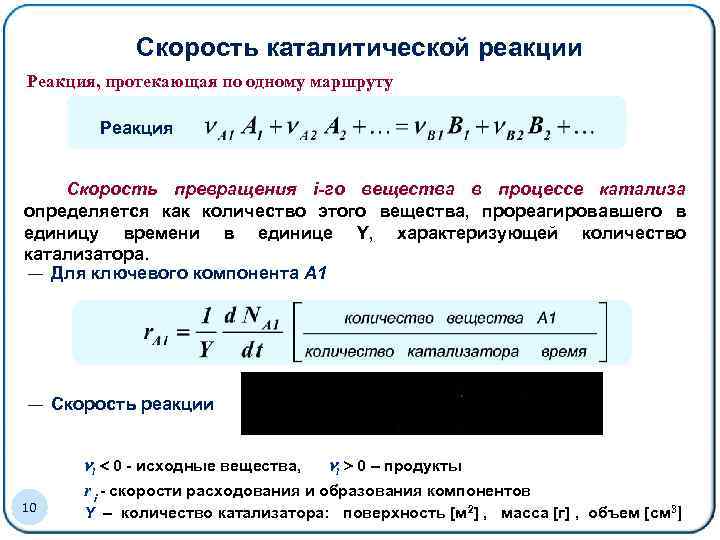 Скорость каталитической реакции Реакция, протекающая по одному маршруту Реакция Скорость превращения i-го вещества в процессе катализа определяется как количество этого вещества, прореагировавшего в единицу времени в единице Y, характеризующей количество катализатора. ― Для ключевого компонента А 1 ― Скорость реакции i 0 - исходные вещества, 10 i 0 – продукты r i - скорости расходования и образования компонентов Y – количество катализатора: поверхность [м 2] , масса [г] , объем [см 3]
Скорость каталитической реакции Реакция, протекающая по одному маршруту Реакция Скорость превращения i-го вещества в процессе катализа определяется как количество этого вещества, прореагировавшего в единицу времени в единице Y, характеризующей количество катализатора. ― Для ключевого компонента А 1 ― Скорость реакции i 0 - исходные вещества, 10 i 0 – продукты r i - скорости расходования и образования компонентов Y – количество катализатора: поверхность [м 2] , масса [г] , объем [см 3]
 Скорость каталитической реакции Реакция Ø Ø 11 Скорость реакции в общем виде: Без изменения объема газовой фазы: Ø Размерности Y – поверхность [м 2], вес [г] или объем катализатора [см 3], V - объем системы, см 3, ci - концентрации компонентов, моль/см 3
Скорость каталитической реакции Реакция Ø Ø 11 Скорость реакции в общем виде: Без изменения объема газовой фазы: Ø Размерности Y – поверхность [м 2], вес [г] или объем катализатора [см 3], V - объем системы, см 3, ci - концентрации компонентов, моль/см 3
 Кинетические модели для стационарных условий 1. Экспериментальное определение скоростей каталитической реакции в отсутствии влияния процессов массо- и теплопереноса 2. Вывод кинетических уравнений скоростей реакции • с использованием феноменологического подхода • на основе данных о механизме реакции 3. Решение обратной задачи – определение параметров 4. Дискриминация и выбор кинетических уравнений 12 Цикл повторяется несколько раз - скрининг, простейшие уравнения на основе феноменологического подхода, кинетическая модель для дизайна каталитического реактора, полученная на основе механизма реакции
Кинетические модели для стационарных условий 1. Экспериментальное определение скоростей каталитической реакции в отсутствии влияния процессов массо- и теплопереноса 2. Вывод кинетических уравнений скоростей реакции • с использованием феноменологического подхода • на основе данных о механизме реакции 3. Решение обратной задачи – определение параметров 4. Дискриминация и выбор кинетических уравнений 12 Цикл повторяется несколько раз - скрининг, простейшие уравнения на основе феноменологического подхода, кинетическая модель для дизайна каталитического реактора, полученная на основе механизма реакции
 Кинетические модели для стационарных условий Экспериментальное определение скоростей каталитической реакции § Проведение экспериментов в лабораторных реакторах в отсутствии влияния внешней и внутренней диффузии при T = const § Расчет скоростей реакции, используя величины измеренных концентраций (конверсий) реагентов и продуктов и данные о рабочих условиях – загрузке катализатора, скорости подачи реакционной смеси, температуре и т. д. Область рабочих условий должна охватывать всю область параметров, которые встречаются при практической реализации процесса 13
Кинетические модели для стационарных условий Экспериментальное определение скоростей каталитической реакции § Проведение экспериментов в лабораторных реакторах в отсутствии влияния внешней и внутренней диффузии при T = const § Расчет скоростей реакции, используя величины измеренных концентраций (конверсий) реагентов и продуктов и данные о рабочих условиях – загрузке катализатора, скорости подачи реакционной смеси, температуре и т. д. Область рабочих условий должна охватывать всю область параметров, которые встречаются при практической реализации процесса 13
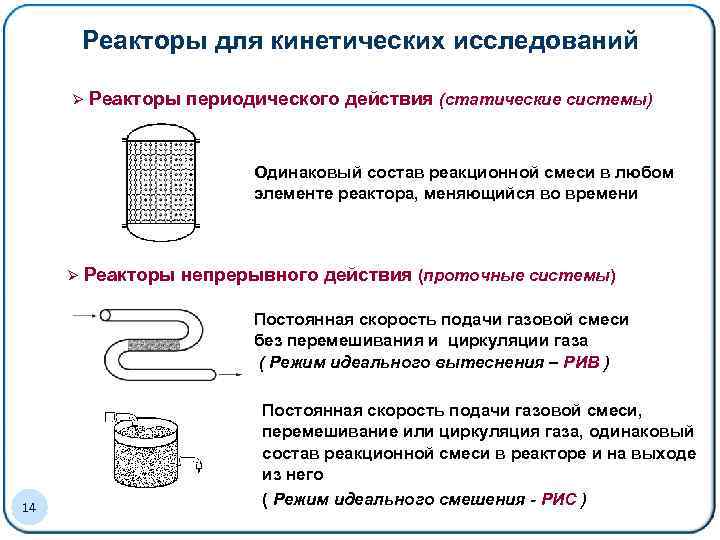 Реакторы для кинетических исследований Ø Реакторы периодического действия (статические системы) Одинаковый состав реакционной смеси в любом элементе реактора, меняющийся во времени Ø Реакторы непрерывного действия (проточные системы) Постоянная скорость подачи газовой смеси без перемешивания и циркуляции газа ( Режим идеального вытеснения – РИВ ) 14 Постоянная скорость подачи газовой смеси, перемешивание или циркуляция газа, одинаковый состав реакционной смеси в реакторе и на выходе из него ( Режим идеального смешения - РИС )
Реакторы для кинетических исследований Ø Реакторы периодического действия (статические системы) Одинаковый состав реакционной смеси в любом элементе реактора, меняющийся во времени Ø Реакторы непрерывного действия (проточные системы) Постоянная скорость подачи газовой смеси без перемешивания и циркуляции газа ( Режим идеального вытеснения – РИВ ) 14 Постоянная скорость подачи газовой смеси, перемешивание или циркуляция газа, одинаковый состав реакционной смеси в реакторе и на выходе из него ( Режим идеального смешения - РИС )
 Проточные реакторы Режим идеального вытеснения (РИВ) Реакционная газовая смесь подается с постоянной скоростью, перемешивание либо циркуляция газа отсутствует. Эксперименты выполняются при постоянной температуре. Экспериментальные условия: Ø Ø Ø Ø Размер частиц катализатора ~ 1 - 2 мм Диаметр реактора ~ 0. 5 -1 см Объем катализатора ~ 1 - 10 см 3 Высота слоя катализатора ~ 3 - 10 см Скорость реакционного потока ~ 10 - 20 л/ч Температура ~ 250 - 500 o. C Давление – 1 атм Отношение высоты слоя к диаметру 15 10
Проточные реакторы Режим идеального вытеснения (РИВ) Реакционная газовая смесь подается с постоянной скоростью, перемешивание либо циркуляция газа отсутствует. Эксперименты выполняются при постоянной температуре. Экспериментальные условия: Ø Ø Ø Ø Размер частиц катализатора ~ 1 - 2 мм Диаметр реактора ~ 0. 5 -1 см Объем катализатора ~ 1 - 10 см 3 Высота слоя катализатора ~ 3 - 10 см Скорость реакционного потока ~ 10 - 20 л/ч Температура ~ 250 - 500 o. C Давление – 1 атм Отношение высоты слоя к диаметру 15 10
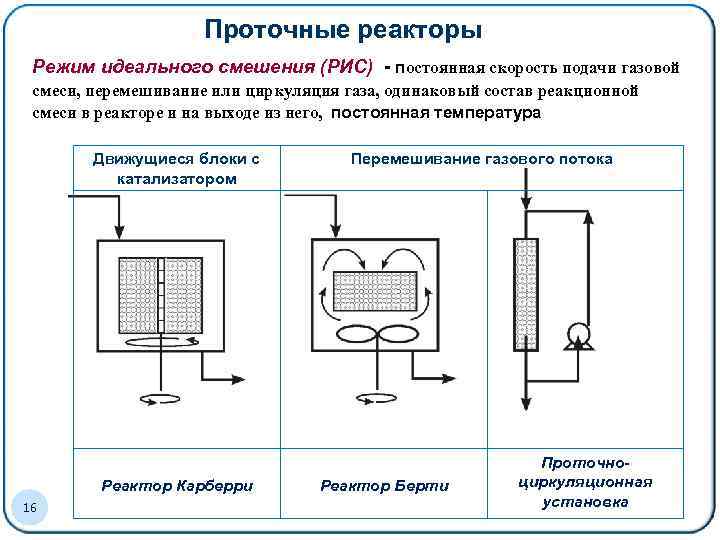 Проточные реакторы Режим идеального смешения (РИС) - постоянная скорость подачи газовой смеси, перемешивание или циркуляция газа, одинаковый состав реакционной смеси в реакторе и на выходе из него, постоянная температура Движущиеся блоки с катализатором Реактор Карберри 16 Перемешивание газового потока Реактор Берти Проточноциркуляционная установка
Проточные реакторы Режим идеального смешения (РИС) - постоянная скорость подачи газовой смеси, перемешивание или циркуляция газа, одинаковый состав реакционной смеси в реакторе и на выходе из него, постоянная температура Движущиеся блоки с катализатором Реактор Карберри 16 Перемешивание газового потока Реактор Берти Проточноциркуляционная установка
 Математические модели лабораторных реакторов T = const • Реакторы периодического действия (batch reactor) • Реакторы идеального вытеснения (plug flow reactor) • Реактор идеального смешения (continious stirred tank reactor) 17
Математические модели лабораторных реакторов T = const • Реакторы периодического действия (batch reactor) • Реакторы идеального вытеснения (plug flow reactor) • Реактор идеального смешения (continious stirred tank reactor) 17
 Скрининг катализаторов • Основные характеристики : - активность - селективность - стабильность • Характеристики активности - x - степень превращения исходного реагента при одинаковых реакционных условиях - - время контакта при постоянных составе реакционной смеси и степени превращения исходного реагента; - k - константа скорости реакции РИВ: РИC: 18 r =kc
Скрининг катализаторов • Основные характеристики : - активность - селективность - стабильность • Характеристики активности - x - степень превращения исходного реагента при одинаковых реакционных условиях - - время контакта при постоянных составе реакционной смеси и степени превращения исходного реагента; - k - константа скорости реакции РИВ: РИC: 18 r =kc
 Кинетические модели для стационарных условий Вывод кинетических уравнений Ø Феноменологический подход - формально- кинетический метод; - использование типичных видов кинетических уравнений, адекватно описывающих весь набор экспериментальных данных Ø Физико-химический подход - определение предполагаемого механизма реакции в виде совокупности каталитических стадий на основе имеющейся информации - данных релаксационных методов, знаний о состоянии поверхности катализатора, полученных с помощью физметодов и т. д. ; - определение лимитирующих, быстрых и равновесных стадий; - вывод кинетических уравнений для скоростей реакции, содержащих концентрации исходных веществ и продуктов реакции, предполагая выражения для кинетических закономерностей отдельных стадий (обычно, на основе закона действующих поверхностей). 19
Кинетические модели для стационарных условий Вывод кинетических уравнений Ø Феноменологический подход - формально- кинетический метод; - использование типичных видов кинетических уравнений, адекватно описывающих весь набор экспериментальных данных Ø Физико-химический подход - определение предполагаемого механизма реакции в виде совокупности каталитических стадий на основе имеющейся информации - данных релаксационных методов, знаний о состоянии поверхности катализатора, полученных с помощью физметодов и т. д. ; - определение лимитирующих, быстрых и равновесных стадий; - вывод кинетических уравнений для скоростей реакции, содержащих концентрации исходных веществ и продуктов реакции, предполагая выражения для кинетических закономерностей отдельных стадий (обычно, на основе закона действующих поверхностей). 19
 Кинетические модели для стационарных условий Вывод кинетических уравнений Требования § Выполнение закона сохранения вещества § Плавный переход модели в тривиальные решения: § Непрерывность по концентрациям § Экстраполяция в рамках условий эксперимента c 0, r 0; Типичный вид кинетических уравнений: а) степенные зависимости - на основе закона действующих масс б) зависимости типа Лэнгмюра - Хиншельвуда 20
Кинетические модели для стационарных условий Вывод кинетических уравнений Требования § Выполнение закона сохранения вещества § Плавный переход модели в тривиальные решения: § Непрерывность по концентрациям § Экстраполяция в рамках условий эксперимента c 0, r 0; Типичный вид кинетических уравнений: а) степенные зависимости - на основе закона действующих масс б) зависимости типа Лэнгмюра - Хиншельвуда 20
 Кинетические модели для стационарных условий Реакция А В Механизм реакции 1. A + [ Z ] [ AZ ] r 1 = k 1 c. A Z ; 2. [ AZ ] B + [ Z ] r 2 = k 2 AZ ; r-1 = k-1 AZ + Z = const Условие постоянства количества активных центров Кинетическое уравнение A. r 1 = r-1 r 2 B. r 1, r-1, r 2 - сопоставимы 21 k 1 c. A (1 - ) = k-1 + k 2 AZ
Кинетические модели для стационарных условий Реакция А В Механизм реакции 1. A + [ Z ] [ AZ ] r 1 = k 1 c. A Z ; 2. [ AZ ] B + [ Z ] r 2 = k 2 AZ ; r-1 = k-1 AZ + Z = const Условие постоянства количества активных центров Кинетическое уравнение A. r 1 = r-1 r 2 B. r 1, r-1, r 2 - сопоставимы 21 k 1 c. A (1 - ) = k-1 + k 2 AZ
 Кинетические модели для стационарных условий Решение обратной задачи § расчет скоростей реакции на основе кинетических выражений и начальных приближений для постоянных параметров; § сопоставление расчетных и экспериментальных величин скоростей, минимизация отклонений; § определение неизвестных постоянных параметров в кинетических § выражениях скоростей реакции: констант и энергий активаций. Дискриминация кинетических выражений § решение обратной задачи для нескольких видов кинетических выражений; § выбор уравнений, для которых отклонение расчетных и экспериментальных величин минимально. 22 Цикл повторяется несколько раз - скрининг, простейшие уравнения, использование феноменологического подхода, кинетическая модель для дизайна каталитического реактора, полученная на основе механизма реакции
Кинетические модели для стационарных условий Решение обратной задачи § расчет скоростей реакции на основе кинетических выражений и начальных приближений для постоянных параметров; § сопоставление расчетных и экспериментальных величин скоростей, минимизация отклонений; § определение неизвестных постоянных параметров в кинетических § выражениях скоростей реакции: констант и энергий активаций. Дискриминация кинетических выражений § решение обратной задачи для нескольких видов кинетических выражений; § выбор уравнений, для которых отклонение расчетных и экспериментальных величин минимально. 22 Цикл повторяется несколько раз - скрининг, простейшие уравнения, использование феноменологического подхода, кинетическая модель для дизайна каталитического реактора, полученная на основе механизма реакции
 Кинетические уравнения каталитических процессов Процесс 1. Окислительное дегидрирование бутилена 2. Окисление метанола Катализатор Оксидный, Fe-Sb Оксидный, Fe–Mo 3. Окисление этилена Ag / Al 2 O 3 4. Окисление пропилена в акролеин Оксидный многокомпонентный 5. Окисление HCl 23 (Cu. Cl 2 + Na. Cl) / Al 2 O 3 Кинетическое уравнение
Кинетические уравнения каталитических процессов Процесс 1. Окислительное дегидрирование бутилена 2. Окисление метанола Катализатор Оксидный, Fe-Sb Оксидный, Fe–Mo 3. Окисление этилена Ag / Al 2 O 3 4. Окисление пропилена в акролеин Оксидный многокомпонентный 5. Окисление HCl 23 (Cu. Cl 2 + Na. Cl) / Al 2 O 3 Кинетическое уравнение
 Кинетические уравнения каталитических процессов с учетом неоднородной поверхности для обратимых реакций Процесс Синтез аммиака (ур-ие Темкина – Пыжева) Катализатор Fe (промот) Окисление SO 2 Конверсия СО 24 Pt Fe 2 O 3 Кинетическое уравнение
Кинетические уравнения каталитических процессов с учетом неоднородной поверхности для обратимых реакций Процесс Синтез аммиака (ур-ие Темкина – Пыжева) Катализатор Fe (промот) Окисление SO 2 Конверсия СО 24 Pt Fe 2 O 3 Кинетическое уравнение
 Учебная литература Основная 1. Левеншпиль О. Инженерное оформление химических процессов. - М. , Химия, 1969. 2. Боресков Г. К. Гетерогенный катализ. - Новосибирск, Наука, 1986. 3. Франк-Каменецкий Д. А. Диффузия и теплопередача в химической кинетике. - М. , Наука, 1987. 4. Катализ в промышленности/под ред. Б. Рич. / - М. , Мир, 1986. 5. Справочник азотчика, т. 1 и 2. - М. , Химия, 1986. 6. Арис Р. Анализ процессов в химических реакторах. - Л. , Химия, 1989. 7. Бесков В. С. , Флокк В. Моделирование каталитических процессов и реакторов. - М. , Химия, 1991. 8. Бесков В. С. , Общая химическая технология. - М. , Академкнига, 2005. 25
Учебная литература Основная 1. Левеншпиль О. Инженерное оформление химических процессов. - М. , Химия, 1969. 2. Боресков Г. К. Гетерогенный катализ. - Новосибирск, Наука, 1986. 3. Франк-Каменецкий Д. А. Диффузия и теплопередача в химической кинетике. - М. , Наука, 1987. 4. Катализ в промышленности/под ред. Б. Рич. / - М. , Мир, 1986. 5. Справочник азотчика, т. 1 и 2. - М. , Химия, 1986. 6. Арис Р. Анализ процессов в химических реакторах. - Л. , Химия, 1989. 7. Бесков В. С. , Флокк В. Моделирование каталитических процессов и реакторов. - М. , Химия, 1991. 8. Бесков В. С. , Общая химическая технология. - М. , Академкнига, 2005. 25
 Учебная литература Основная 9. Hayes R. E. Introduction to Chemical Reactor Analysis. - Amsterdam, Gordon and Breach Science Publishers, 2001 (University of Alberta, Canada) 10. Слинько М. Г. Основы и принципы математического моделирования каталитических процессов. – Новосибирск, БИК, 2004 11. А. С. Носков “Промышленные каталитические реакторы и их особенности”, в кн. “Промышленный катализ в лекциях”, выпуск 4, 2006. - Москва, “Калвис”, 2006. 12. Слинько М. Г. Общие вопросы теории химических процессов и реакторов, том 1 и 2. – Новосибирск, БИК, 2008 26
Учебная литература Основная 9. Hayes R. E. Introduction to Chemical Reactor Analysis. - Amsterdam, Gordon and Breach Science Publishers, 2001 (University of Alberta, Canada) 10. Слинько М. Г. Основы и принципы математического моделирования каталитических процессов. – Новосибирск, БИК, 2004 11. А. С. Носков “Промышленные каталитические реакторы и их особенности”, в кн. “Промышленный катализ в лекциях”, выпуск 4, 2006. - Москва, “Калвис”, 2006. 12. Слинько М. Г. Общие вопросы теории химических процессов и реакторов, том 1 и 2. – Новосибирск, БИК, 2008 26
 Учебная литература Дополнительная 1. Levenshpiel O. Тhe Сhemical Reactor Omnibook. - Oregon State 2. University, Corvallis, Oregon, 1993. 2. Handbook of Heterogeneous Catalysis, Vol. 3, VCH Verlagsgesellschaft mb. H, Weinheim (Germany), 1997. 3. R. Aris. Ends and beginnings in the mathematical modeling of chemical engineering systems, Chemical Engineering Science, Vol. 48, N. 14, pp. 2507 -2517, 1993. 4. J. -C. Charpentier. Four main objectives for the future of chemical and process engineering…. , Chemical Engineering Journal, Vol. 103, N. 1 - 3, pp. 3 -19, 2005. 27
Учебная литература Дополнительная 1. Levenshpiel O. Тhe Сhemical Reactor Omnibook. - Oregon State 2. University, Corvallis, Oregon, 1993. 2. Handbook of Heterogeneous Catalysis, Vol. 3, VCH Verlagsgesellschaft mb. H, Weinheim (Germany), 1997. 3. R. Aris. Ends and beginnings in the mathematical modeling of chemical engineering systems, Chemical Engineering Science, Vol. 48, N. 14, pp. 2507 -2517, 1993. 4. J. -C. Charpentier. Four main objectives for the future of chemical and process engineering…. , Chemical Engineering Journal, Vol. 103, N. 1 - 3, pp. 3 -19, 2005. 27


