Кинетика электрохимической коррозии Лекция 4.ppt
- Количество слайдов: 12
 Кинетика электрохимической коррозии Плетнев Михаил Андреевич
Кинетика электрохимической коррозии Плетнев Михаил Андреевич
 Поляризация электродов (перенапряжение) ΔЕк = Ек – Е 0 к < 0 (катодная поляризация) ΔЕа = Еа – Е 0 а > 0 (анодная поляризация) ƞk и ƞa - перенапряжение катодного и анодного процессов ΔЕk ≡ ƞk= Еk – Е 0 k 0 ΔЕа ≡ ƞa= Еа – Е 0 а
Поляризация электродов (перенапряжение) ΔЕк = Ек – Е 0 к < 0 (катодная поляризация) ΔЕа = Еа – Е 0 а > 0 (анодная поляризация) ƞk и ƞa - перенапряжение катодного и анодного процессов ΔЕk ≡ ƞk= Еk – Е 0 k 0 ΔЕа ≡ ƞa= Еа – Е 0 а
 Причины электродной поляризации Электрохимический процесс включает следующие стадии: 1) подвод реагирующих веществ к электроду; 2) процесс электрохимического превращения на поверхности электрода (собственно электрохимическая реакция), который может сопровождаться дополнительными химическими реакциями; 3) отвод продуктов реакции от электрода.
Причины электродной поляризации Электрохимический процесс включает следующие стадии: 1) подвод реагирующих веществ к электроду; 2) процесс электрохимического превращения на поверхности электрода (собственно электрохимическая реакция), который может сопровождаться дополнительными химическими реакциями; 3) отвод продуктов реакции от электрода.
 Деполяризация электродов Анодная деполяризация заключается в снижении поляризации анода – электрода, на котором происходит окисление, происходящее при пропускании через электрохимическую систему электрического тока. Деполяризационные процессы: 1. Анодное растворение металла: Me - ne → Men+ 2. Перемешивание электролита – уменьшается концентрационная поляризация. 3. Введение депассиваторов. Cl- - уменьшает анодную пассивацию; 4. Введение комплексообразователей: например, молекулы аммиака NH 3 снижают концентрацию ионов металла (Zn 2+, Cu 2+) в прианодном пространстве: Cu 2+ +4 NH 3 → [Cu(NH 3)]42+
Деполяризация электродов Анодная деполяризация заключается в снижении поляризации анода – электрода, на котором происходит окисление, происходящее при пропускании через электрохимическую систему электрического тока. Деполяризационные процессы: 1. Анодное растворение металла: Me - ne → Men+ 2. Перемешивание электролита – уменьшается концентрационная поляризация. 3. Введение депассиваторов. Cl- - уменьшает анодную пассивацию; 4. Введение комплексообразователей: например, молекулы аммиака NH 3 снижают концентрацию ионов металла (Zn 2+, Cu 2+) в прианодном пространстве: Cu 2+ +4 NH 3 → [Cu(NH 3)]42+
 Деполяризация электродов Катодная деполяризация заключается в снижении поляризации катода – электрода, на котором происходит восстановление, происходящей при пропускании через электрохимическую систему электрического тока. Процессы катодной деполяризации (поглощения электронов): 1. Восстановление ионов металла. Men+ + ne → Mes 2. Восстановление ионов водорода (водородная деполяризация). H+ + e →½ H 2 3. Восстановление молекулярного кислорода (кислородная деполяризация). O 2 + 2 H 2 O + 4 e → 4 OH-
Деполяризация электродов Катодная деполяризация заключается в снижении поляризации катода – электрода, на котором происходит восстановление, происходящей при пропускании через электрохимическую систему электрического тока. Процессы катодной деполяризации (поглощения электронов): 1. Восстановление ионов металла. Men+ + ne → Mes 2. Восстановление ионов водорода (водородная деполяризация). H+ + e →½ H 2 3. Восстановление молекулярного кислорода (кислородная деполяризация). O 2 + 2 H 2 O + 4 e → 4 OH-
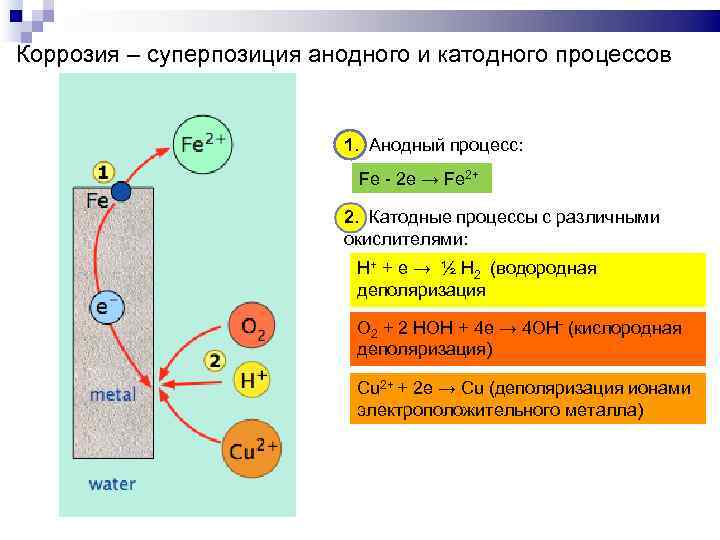 Коррозия – суперпозиция анодного и катодного процессов 1. Анодный процесс: Fe - 2 e → Fe 2+ 2. Катодные процессы с различными окислителями: H+ + e → ½ H 2 (водородная деполяризация O 2 + 2 HOH + 4 e → 4 OH- (кислородная деполяризация) Cu 2+ + 2 e → Cu (деполяризация ионами электроположительного металла)
Коррозия – суперпозиция анодного и катодного процессов 1. Анодный процесс: Fe - 2 e → Fe 2+ 2. Катодные процессы с различными окислителями: H+ + e → ½ H 2 (водородная деполяризация O 2 + 2 HOH + 4 e → 4 OH- (кислородная деполяризация) Cu 2+ + 2 e → Cu (деполяризация ионами электроположительного металла)
 Скорость электрохимической реакции (1) где Z – количество электронов, участвующих в реакции; F – число Фарадея; k – const скорости; (2) Сox, Cred – концентрация окислительной и восстановленной форм реагентов; ∆GK – энергия активации катодного процесса; ∆GA – энергия активации анодного процесса. ∆ Gk = ZFE α (3) ∆ GA = ZFE(1 – α), (4) где α - коэффициент переноса С учетом (3) и (4) уравнения (1) и (2) преобразуются в (5) (6)
Скорость электрохимической реакции (1) где Z – количество электронов, участвующих в реакции; F – число Фарадея; k – const скорости; (2) Сox, Cred – концентрация окислительной и восстановленной форм реагентов; ∆GK – энергия активации катодного процесса; ∆GA – энергия активации анодного процесса. ∆ Gk = ZFE α (3) ∆ GA = ZFE(1 – α), (4) где α - коэффициент переноса С учетом (3) и (4) уравнения (1) и (2) преобразуются в (5) (6)
 Скорость электрохимической реакции С учетом того, что i = i a – ik Получаем (7) (8) Вводим ток обмена: И с учетом (7), (8) и (9), получаем с учетом того, что ∆E = ƞ, т. е. перенапряжению электрохимической реакции: ia = i 0 CRed exp[(1 -α)Fƞa/RT] (10) ik = i 0 COx exp[-αFƞk/RT] (11) Логарифмируем и решаем относительно ƞ (перенапряжения), при этом 1–α=β
Скорость электрохимической реакции С учетом того, что i = i a – ik Получаем (7) (8) Вводим ток обмена: И с учетом (7), (8) и (9), получаем с учетом того, что ∆E = ƞ, т. е. перенапряжению электрохимической реакции: ia = i 0 CRed exp[(1 -α)Fƞa/RT] (10) ik = i 0 COx exp[-αFƞk/RT] (11) Логарифмируем и решаем относительно ƞ (перенапряжения), при этом 1–α=β
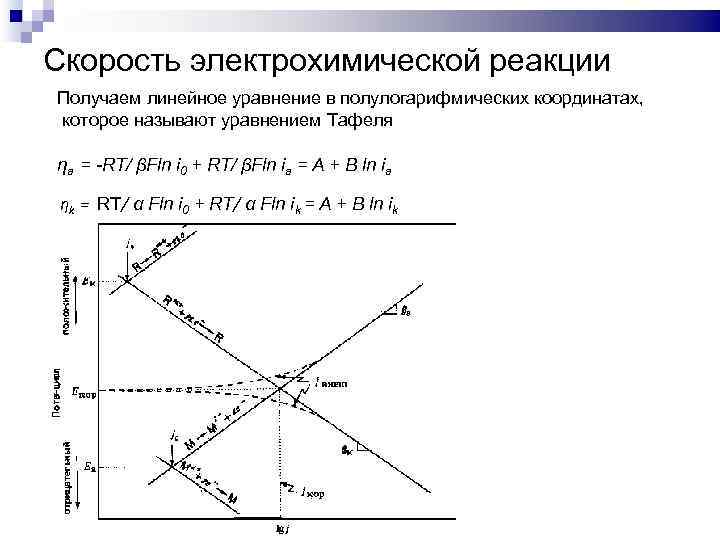 Скорость электрохимической реакции Получаем линейное уравнение в полулогарифмических координатах, которое называют уравнением Тафеля ƞa = -RT/ βFln i 0 + RT/ βFln ia = A + B ln ia ƞk = RT/ α Fln i 0 + RT/ α Fln ik = A + B ln ik
Скорость электрохимической реакции Получаем линейное уравнение в полулогарифмических координатах, которое называют уравнением Тафеля ƞa = -RT/ βFln i 0 + RT/ βFln ia = A + B ln ia ƞk = RT/ α Fln i 0 + RT/ α Fln ik = A + B ln ik
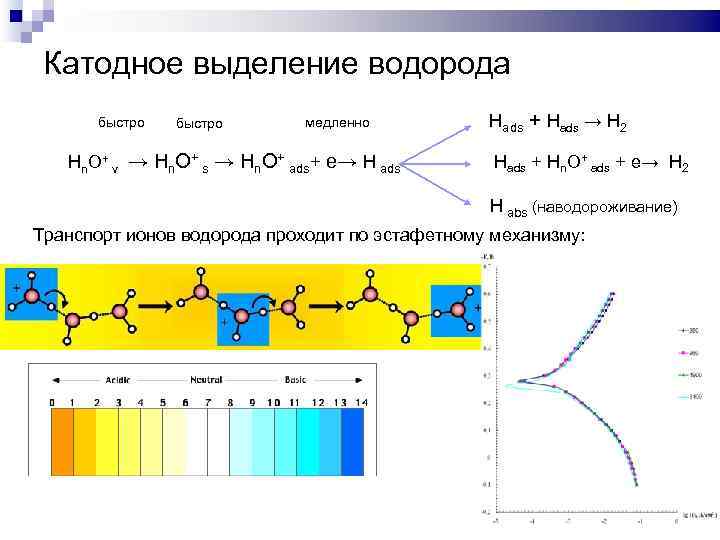 Катодное выделение водорода быстро медленно Hn. O+ v → Hn. O+ s → Hn. O+ ads+ e→ H ads Hads + Hads → H 2 Hads + Hn. O+ ads + e→ H 2 H abs (наводороживание) Транспорт ионов водорода проходит по эстафетному механизму:
Катодное выделение водорода быстро медленно Hn. O+ v → Hn. O+ s → Hn. O+ ads+ e→ H ads Hads + Hads → H 2 Hads + Hn. O+ ads + e→ H 2 H abs (наводороживание) Транспорт ионов водорода проходит по эстафетному механизму:
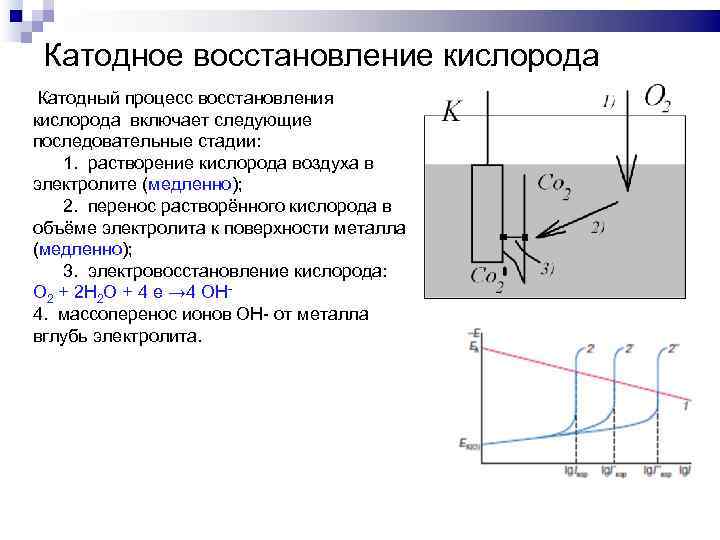 Катодное восстановление кислорода Катодный процесс восстановления кислорода включает следующие последовательные стадии: 1. растворение кислорода воздуха в электролите (медленно); 2. перенос растворённого кислорода в объёме электролита к поверхности металла (медленно); 3. электровосстановление кислорода: O 2 + 2 H 2 O + 4 e → 4 OH 4. массоперенос ионов OH- от металла вглубь электролита.
Катодное восстановление кислорода Катодный процесс восстановления кислорода включает следующие последовательные стадии: 1. растворение кислорода воздуха в электролите (медленно); 2. перенос растворённого кислорода в объёме электролита к поверхности металла (медленно); 3. электровосстановление кислорода: O 2 + 2 H 2 O + 4 e → 4 OH 4. массоперенос ионов OH- от металла вглубь электролита.
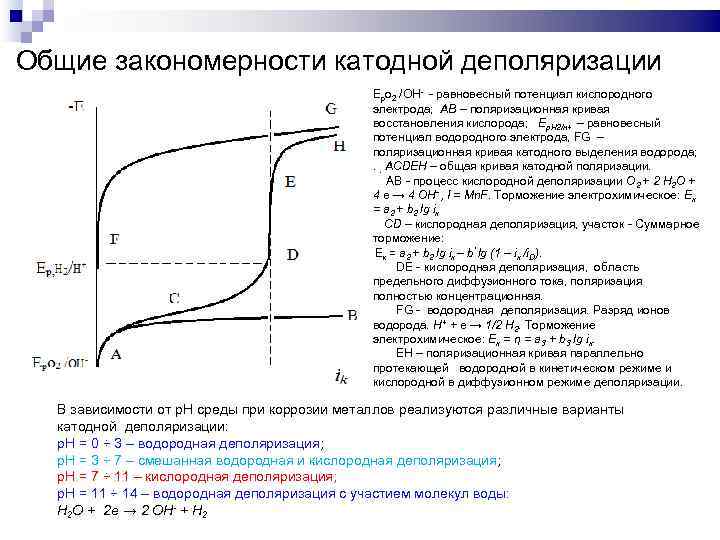 Общие закономерности катодной деполяризации Eрo 2 /OH- - равновесный потенциал кислородного электрода; AB – поляризационная кривая восстановления кислорода; Eр. H 2/н+ – равновесный потенциал водородного электрода, FG – поляризационная кривая катодного выделения водорода; . . ACDEН – общая кривая катодной поляризации. AB - процесс кислородной деполяризации O 2 + 2 H 2 O + 4 e → 4 OH- , I = Mn. F. Торможение электрохимическое: Eк = a 2 + b 2 lg iк CD – кислородная деполяризация, участок - Суммарное торможение: Eк = a 2 + b 2 lg iк – b’ lg (1 – iк /i. D). DE - кислородная деполяризация, область предельного диффузионного тока, поляризация полностью концентрационная. FG - водородная деполяризация. Разряд ионов водорода. H+ + e → 1/2 H 2. Торможение электрохимическое: Eк = η = a 3 + b 3 lg iк. EH – поляризационная кривая параллельно протекающей водородной в кинетическом режиме и кислородной в диффузионном режиме деполяризации. В зависимости от р. Н среды при коррозии металлов реализуются различные варианты катодной деполяризации: р. Н = 0 ÷ 3 – водородная деполяризация; р. Н = 3 ÷ 7 – смешанная водородная и кислородная деполяризация; р. Н = 7 ÷ 11 – кислородная деполяризация; р. Н = 11 ÷ 14 – водородная деполяризация с участием молекул воды: H 2 O + 2 e → 2 OH- + H 2
Общие закономерности катодной деполяризации Eрo 2 /OH- - равновесный потенциал кислородного электрода; AB – поляризационная кривая восстановления кислорода; Eр. H 2/н+ – равновесный потенциал водородного электрода, FG – поляризационная кривая катодного выделения водорода; . . ACDEН – общая кривая катодной поляризации. AB - процесс кислородной деполяризации O 2 + 2 H 2 O + 4 e → 4 OH- , I = Mn. F. Торможение электрохимическое: Eк = a 2 + b 2 lg iк CD – кислородная деполяризация, участок - Суммарное торможение: Eк = a 2 + b 2 lg iк – b’ lg (1 – iк /i. D). DE - кислородная деполяризация, область предельного диффузионного тока, поляризация полностью концентрационная. FG - водородная деполяризация. Разряд ионов водорода. H+ + e → 1/2 H 2. Торможение электрохимическое: Eк = η = a 3 + b 3 lg iк. EH – поляризационная кривая параллельно протекающей водородной в кинетическом режиме и кислородной в диффузионном режиме деполяризации. В зависимости от р. Н среды при коррозии металлов реализуются различные варианты катодной деполяризации: р. Н = 0 ÷ 3 – водородная деполяризация; р. Н = 3 ÷ 7 – смешанная водородная и кислородная деполяризация; р. Н = 7 ÷ 11 – кислородная деполяризация; р. Н = 11 ÷ 14 – водородная деполяризация с участием молекул воды: H 2 O + 2 e → 2 OH- + H 2


