Spektroskopichni_metodi_analizu.ppt
- Количество слайдов: 25
 Київський національний університет імені Тараса Шевченка Хімічний факультет Спектроскопічні методи аналізу Лекція для студентів 2 курсу 2014/2015 н. р. 1
Київський національний університет імені Тараса Шевченка Хімічний факультет Спектроскопічні методи аналізу Лекція для студентів 2 курсу 2014/2015 н. р. 1
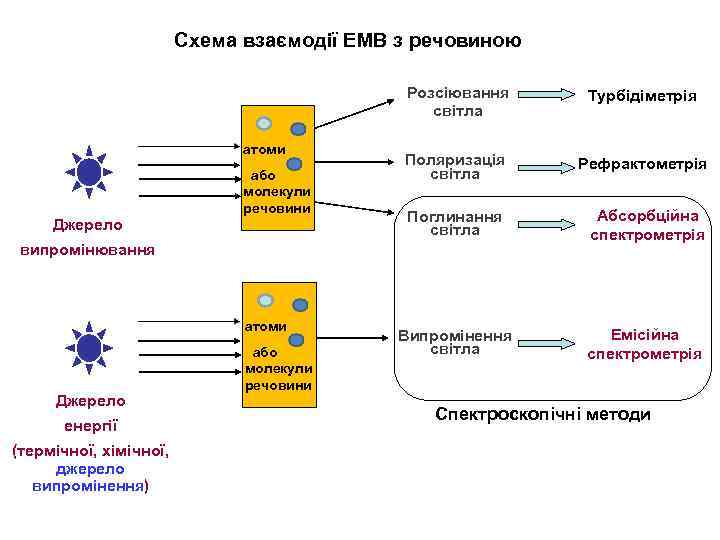 Схема взаємодії ЕМВ з речовиною Розсіювання світла атоми Джерело або молекули речовини Турбідіметрія Поляризація світла Рефрактометрія Поглинання світла Абсорбційна спектрометрія Випромінення світла Емісійна спектрометрія випромінювання атоми Джерело енергії (термічної, хімічної, джерело випромінення) або молекули речовини Спектроскопічні методи
Схема взаємодії ЕМВ з речовиною Розсіювання світла атоми Джерело або молекули речовини Турбідіметрія Поляризація світла Рефрактометрія Поглинання світла Абсорбційна спектрометрія Випромінення світла Емісійна спектрометрія випромінювання атоми Джерело енергії (термічної, хімічної, джерело випромінення) або молекули речовини Спектроскопічні методи
 Загальна характеристика спектроскопічних методів аналізу Спектроскопічні методи • грунтуються на взаємодії ЕМВ з речовиною • використовуються як для якісного (ідентифікація), так і для кількісного аналізу • придатні для визначення речовин у широкому концентраційному діапазоні • більш селективні, ніж методи “мокрої хімії” Коротко про суть спектрометричних методів (для лінивих : ) • Атоми (молекули) здатні взаємодіяти з ЕМВ – поглинати або випромінювати світло • Взаємодія є характерною для даного роду атомів (молекул) • Кількість поглинутого або випроміненого світла є пропорційною концентрації атомів (молекул)
Загальна характеристика спектроскопічних методів аналізу Спектроскопічні методи • грунтуються на взаємодії ЕМВ з речовиною • використовуються як для якісного (ідентифікація), так і для кількісного аналізу • придатні для визначення речовин у широкому концентраційному діапазоні • більш селективні, ніж методи “мокрої хімії” Коротко про суть спектрометричних методів (для лінивих : ) • Атоми (молекули) здатні взаємодіяти з ЕМВ – поглинати або випромінювати світло • Взаємодія є характерною для даного роду атомів (молекул) • Кількість поглинутого або випроміненого світла є пропорційною концентрації атомів (молекул)
 Електромагнітна хвиля Характеристики електромагнітної хвилі: -частота, - кількість разів у секунду, коли магнітне поле досягає максимального значення (1 Гц = 1 с-1) -довжина хвилі, - відстань, що проходить хвиля за час одного повного коливання (м) =с/ -Хвильове число, с=2, 9979. 108 м/с) см-1 ЕМВ випромінюється не безперевно, а квантами (фотонами) – певними неподільними порціями електромагнітної енергії Рівняння Планка стала Планка h=6, 626. 10– 34 Дж. с
Електромагнітна хвиля Характеристики електромагнітної хвилі: -частота, - кількість разів у секунду, коли магнітне поле досягає максимального значення (1 Гц = 1 с-1) -довжина хвилі, - відстань, що проходить хвиля за час одного повного коливання (м) =с/ -Хвильове число, с=2, 9979. 108 м/с) см-1 ЕМВ випромінюється не безперевно, а квантами (фотонами) – певними неподільними порціями електромагнітної енергії Рівняння Планка стала Планка h=6, 626. 10– 34 Дж. с
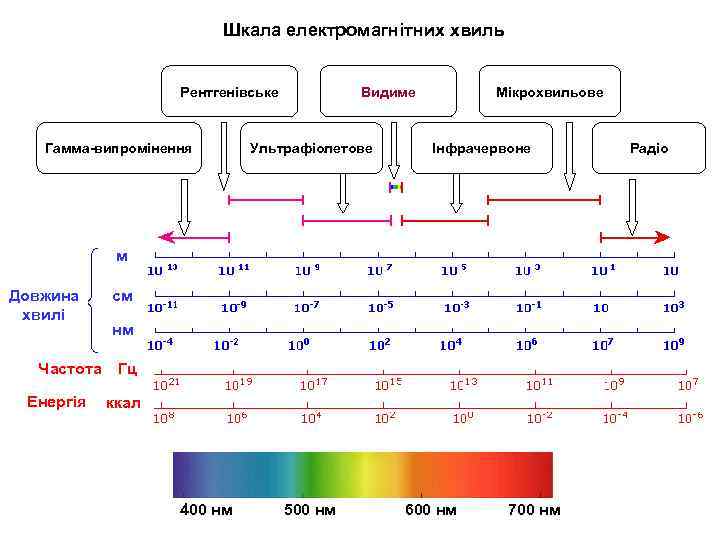 Шкала електромагнітних хвиль Рентгенівське Гамма-випромінення Видиме Ультрафіолетове Мікрохвильове Інфрачервоне м Довжина хвилі Частота Енергія см нм Гц ккал 400 нм 500 нм 600 нм 700 нм Радіо
Шкала електромагнітних хвиль Рентгенівське Гамма-випромінення Видиме Ультрафіолетове Мікрохвильове Інфрачервоне м Довжина хвилі Частота Енергія см нм Гц ккал 400 нм 500 нм 600 нм 700 нм Радіо
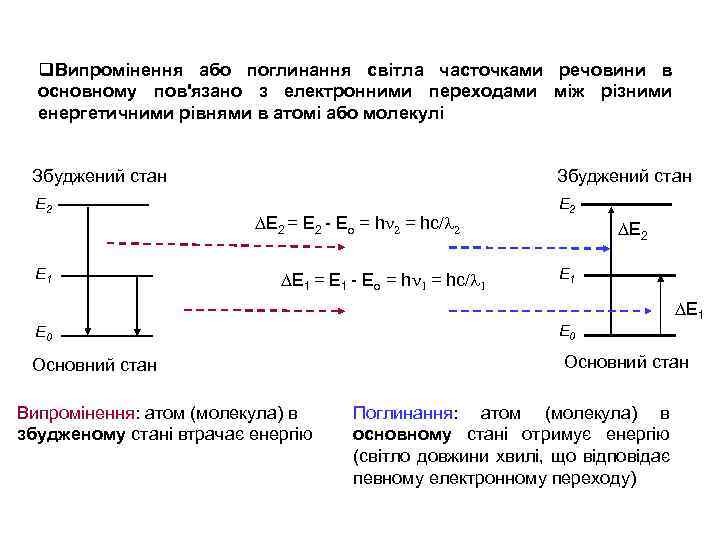 q. Випромінення або поглинання світла часточками речовини в основному пов'язано з електронними переходами між різними енергетичними рівнями в атомі або молекулі Збуджений стан E 2 E 1 DE 2 = E 2 - Eo = hn 2 = hc/l 2 DE 1 = E 1 - Eo = hn 1 = hc/l 1 DE 2 E 1 DE 1 E 0 Основний стан Випромінення: атом (молекула) в збудженому стані втрачає енергію E 0 Основний стан Поглинання: атом (молекула) в основному стані отримує енергію (світло довжини хвилі, що відповідає певному електронному переходу)
q. Випромінення або поглинання світла часточками речовини в основному пов'язано з електронними переходами між різними енергетичними рівнями в атомі або молекулі Збуджений стан E 2 E 1 DE 2 = E 2 - Eo = hn 2 = hc/l 2 DE 1 = E 1 - Eo = hn 1 = hc/l 1 DE 2 E 1 DE 1 E 0 Основний стан Випромінення: атом (молекула) в збудженому стані втрачає енергію E 0 Основний стан Поглинання: атом (молекула) в основному стані отримує енергію (світло довжини хвилі, що відповідає певному електронному переходу)
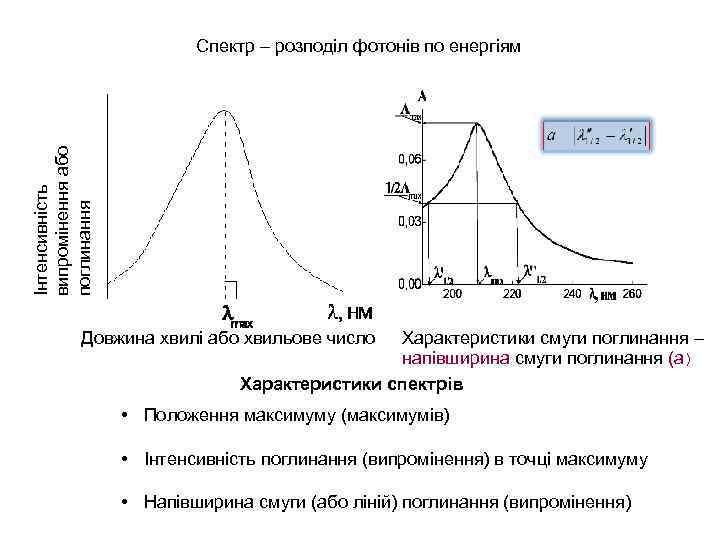 Інтенсивність випромінення або поглинання Спектр – розподіл фотонів по енергіям Довжина хвилі або хвильове число Характеристики смуги поглинання – напівширина смуги поглинання (а) Характеристики спектрів • Положення максимуму (максимумів) • Інтенсивність поглинання (випромінення) в точці максимуму • Напівширина смуги (або ліній) поглинання (випромінення)
Інтенсивність випромінення або поглинання Спектр – розподіл фотонів по енергіям Довжина хвилі або хвильове число Характеристики смуги поглинання – напівширина смуги поглинання (а) Характеристики спектрів • Положення максимуму (максимумів) • Інтенсивність поглинання (випромінення) в точці максимуму • Напівширина смуги (або ліній) поглинання (випромінення)
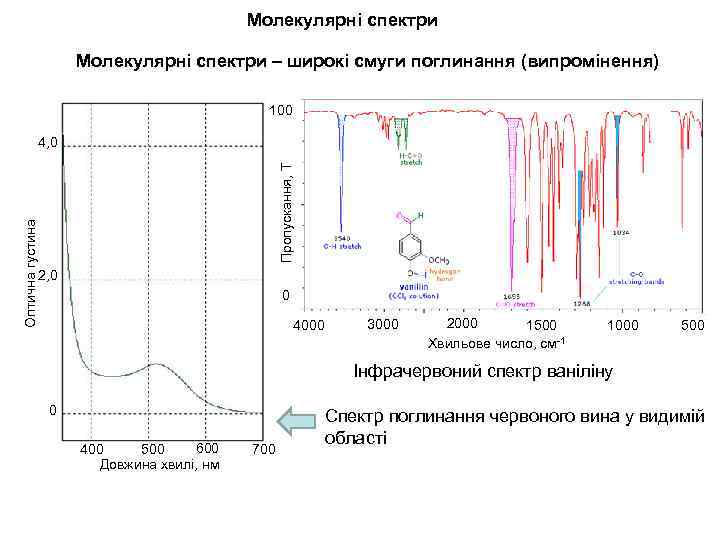 Молекулярні спектри – широкі смуги поглинання (випромінення) 100 Пропускання, Т Оптична густина 4, 0 2, 0 0 4000 3000 2000 1500 Хвильове число, см-1 1000 500 Інфрачервоний спектр ваніліну 0 600 400 500 Довжина хвилі, нм 700 Спектр поглинання червоного вина у видимій області
Молекулярні спектри – широкі смуги поглинання (випромінення) 100 Пропускання, Т Оптична густина 4, 0 2, 0 0 4000 3000 2000 1500 Хвильове число, см-1 1000 500 Інфрачервоний спектр ваніліну 0 600 400 500 Довжина хвилі, нм 700 Спектр поглинання червоного вина у видимій області
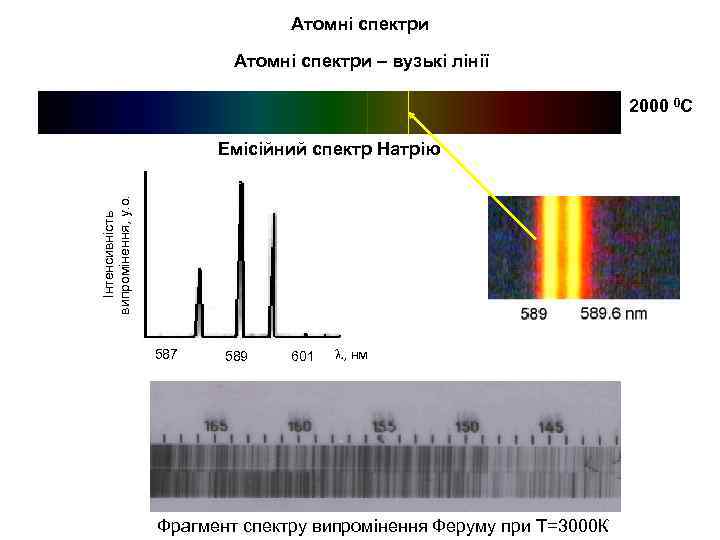 Атомні спектри – вузькі лінії 2000 0 С Інтенсивність випромінення, у. о. Емісійний спектр Натрію 587 589 601 l, нм Фрагмент спектру випромінення Феруму при Т=3000 К
Атомні спектри – вузькі лінії 2000 0 С Інтенсивність випромінення, у. о. Емісійний спектр Натрію 587 589 601 l, нм Фрагмент спектру випромінення Феруму при Т=3000 К
 Методи оптичної спектрометрії: Поділяються на І. Атомні üАтомно-абсорбційний метод üАтомно-емісійний метод ІІ. Молекулярні üМолекулярно-абсорбційний метод üмолекулярно-емісійний метод 10
Методи оптичної спектрометрії: Поділяються на І. Атомні üАтомно-абсорбційний метод üАтомно-емісійний метод ІІ. Молекулярні üМолекулярно-абсорбційний метод üмолекулярно-емісійний метод 10
 Методи атомної спектрометрії • Виключно елементний аналіз • Висока чутливість (межа виявлення від 1 до 100 мкг/л) • Достатньо висока селективність
Методи атомної спектрометрії • Виключно елементний аналіз • Висока чутливість (межа виявлення від 1 до 100 мкг/л) • Достатньо висока селективність
 Атомно-абсорбційна спектрометрія ü Усі атоми можуть поглинати світло üСвітло поглинають атоми у основному енергетичному стані ü Довжина хвилі при якій атом поглинає світло є специфічною для кожного елементу ü Кількість поглинутого атомами світла збільшується пропорційно концентрації поглинаючих атомів у одиниці об'єму. Теоретичні основи методу розроблені австралійським спектроскопістом Аланом Уолшем (1914 -1998) в 50 -х роках ХХ сторіччя
Атомно-абсорбційна спектрометрія ü Усі атоми можуть поглинати світло üСвітло поглинають атоми у основному енергетичному стані ü Довжина хвилі при якій атом поглинає світло є специфічною для кожного елементу ü Кількість поглинутого атомами світла збільшується пропорційно концентрації поглинаючих атомів у одиниці об'єму. Теоретичні основи методу розроблені австралійським спектроскопістом Аланом Уолшем (1914 -1998) в 50 -х роках ХХ сторіччя
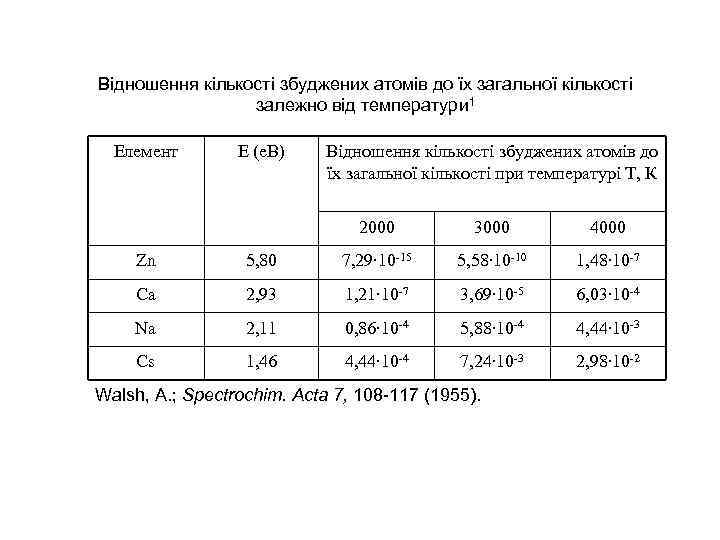 Відношення кількості збуджених атомів до їх загальної кількості залежно від температури 1 Елемент Е (е. В) Відношення кількості збуджених атомів до їх загальної кількості при температурі Т, К 2000 3000 4000 Zn 5, 80 7, 29∙ 10 -15 5, 58∙ 10 -10 1, 48∙ 10 -7 Ca 2, 93 1, 21∙ 10 -7 3, 69∙ 10 -5 6, 03∙ 10 -4 Na 2, 11 0, 86∙ 10 -4 5, 88∙ 10 -4 4, 44∙ 10 -3 Cs 1, 46 4, 44∙ 10 -4 7, 24∙ 10 -3 2, 98∙ 10 -2 Walsh, A. ; Spectrochim. Acta 7, 108 -117 (1955).
Відношення кількості збуджених атомів до їх загальної кількості залежно від температури 1 Елемент Е (е. В) Відношення кількості збуджених атомів до їх загальної кількості при температурі Т, К 2000 3000 4000 Zn 5, 80 7, 29∙ 10 -15 5, 58∙ 10 -10 1, 48∙ 10 -7 Ca 2, 93 1, 21∙ 10 -7 3, 69∙ 10 -5 6, 03∙ 10 -4 Na 2, 11 0, 86∙ 10 -4 5, 88∙ 10 -4 4, 44∙ 10 -3 Cs 1, 46 4, 44∙ 10 -4 7, 24∙ 10 -3 2, 98∙ 10 -2 Walsh, A. ; Spectrochim. Acta 7, 108 -117 (1955).
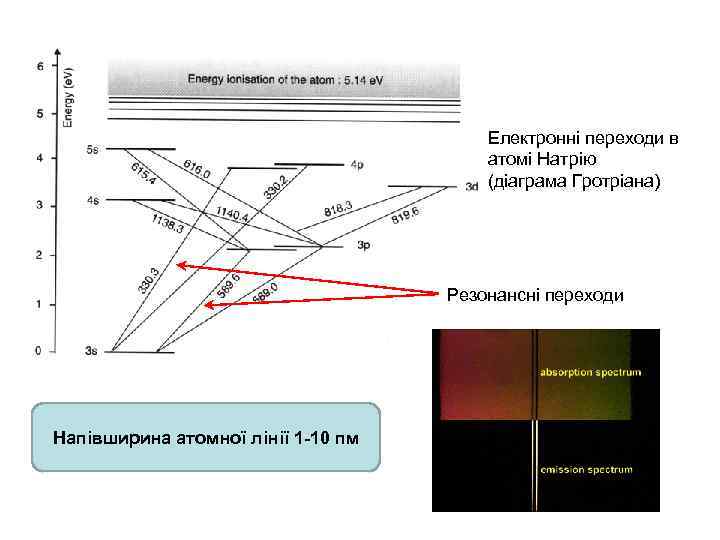 Електронні переходи в атомі Натрію (діаграма Гротріана) Резонансні переходи Напівширина атомної лінії 1 -10 пм
Електронні переходи в атомі Натрію (діаграма Гротріана) Резонансні переходи Напівширина атомної лінії 1 -10 пм
 Особливості методу атомно-абсорбційної спектрометрії 1. Практично всі атоми знаходяться в основному енергетичному стані 2. Електронні переходи відбуваються виключно з основного стану 3. Електронні переходи відбуваються внаслідок поглинання світла певної частоти 3. Спектр - відносно мала кількість дуже тонких ліній 4. Ступінь поглинання залежить від: • ймовірності електронного переходу • кількості атомів, що здатні поглинати
Особливості методу атомно-абсорбційної спектрометрії 1. Практично всі атоми знаходяться в основному енергетичному стані 2. Електронні переходи відбуваються виключно з основного стану 3. Електронні переходи відбуваються внаслідок поглинання світла певної частоти 3. Спектр - відносно мала кількість дуже тонких ліній 4. Ступінь поглинання залежить від: • ймовірності електронного переходу • кількості атомів, що здатні поглинати
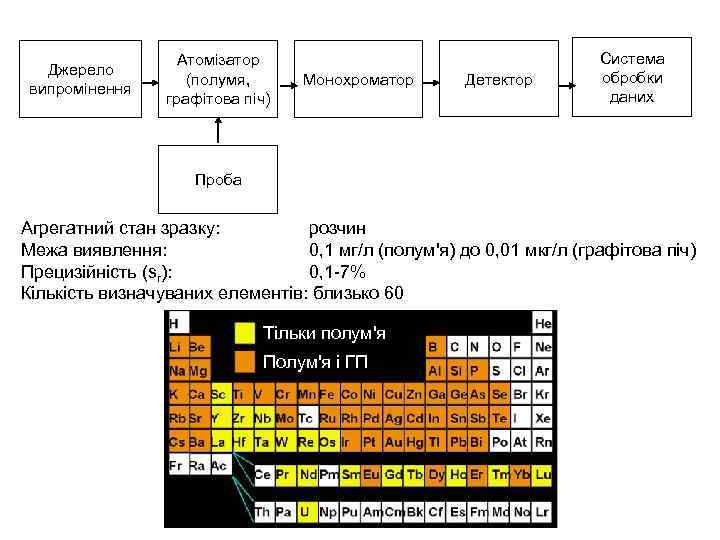 Джерело випромінення Атомізатор (полумя, графітова піч) Монохроматор Детектор Система обробки даних Проба Агрегатний стан зразку: розчин Межа виявлення: 0, 1 мг/л (полум'я) до 0, 01 мкг/л (графітова піч) Прецизійність (sr): 0, 1 -7% Кількість визначуваних елементів: близько 60 Тільки полум'я Полум'я і ГП
Джерело випромінення Атомізатор (полумя, графітова піч) Монохроматор Детектор Система обробки даних Проба Агрегатний стан зразку: розчин Межа виявлення: 0, 1 мг/л (полум'я) до 0, 01 мкг/л (графітова піч) Прецизійність (sr): 0, 1 -7% Кількість визначуваних елементів: близько 60 Тільки полум'я Полум'я і ГП
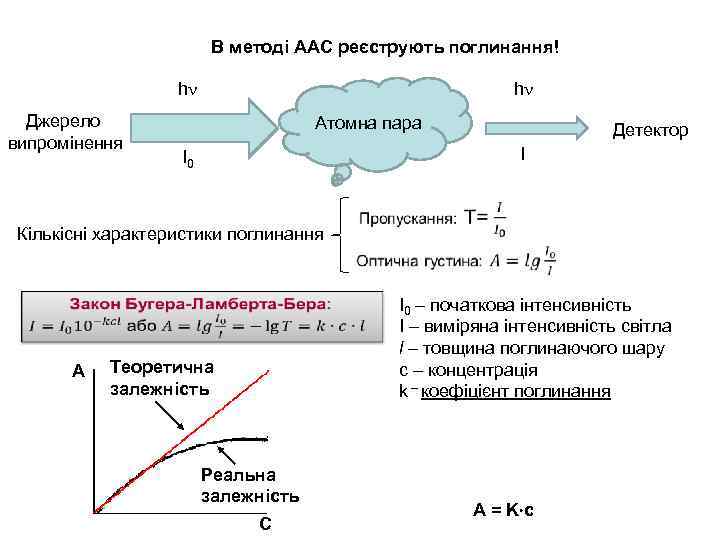 В методі ААС реєструють поглинання! hn Джерело випромінення hn Атомна пара Детектор I I 0 Кількісні характеристики поглинання А І0 – початкова інтенсивність І – виміряна інтенсивність світла l – товщина поглинаючого шару c – концентрація k – коефіцієнт поглинання Теоретична залежність Реальна залежність С A = K c
В методі ААС реєструють поглинання! hn Джерело випромінення hn Атомна пара Детектор I I 0 Кількісні характеристики поглинання А І0 – початкова інтенсивність І – виміряна інтенсивність світла l – товщина поглинаючого шару c – концентрація k – коефіцієнт поглинання Теоретична залежність Реальна залежність С A = K c
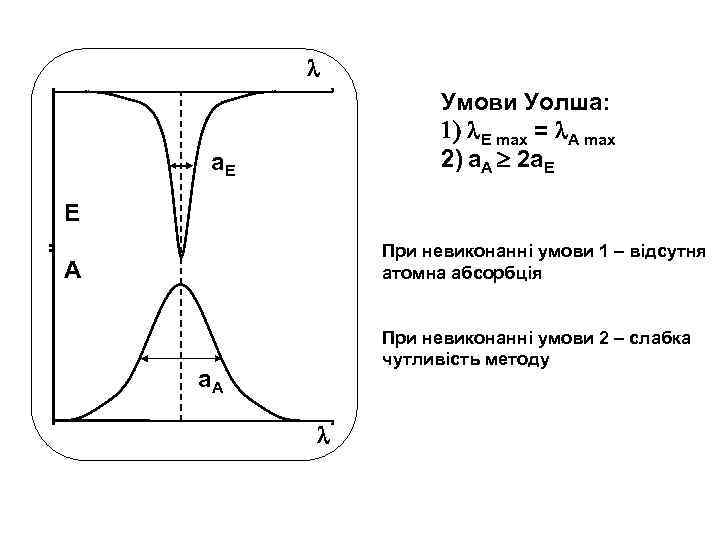 Умови Уолша: 1) E max = A max 2) a. A 2 a. E E При невиконанні умови 1 – відсутня атомна абсорбція А При невиконанні умови 2 – слабка чутливість методу a. A
Умови Уолша: 1) E max = A max 2) a. A 2 a. E E При невиконанні умови 1 – відсутня атомна абсорбція А При невиконанні умови 2 – слабка чутливість методу a. A
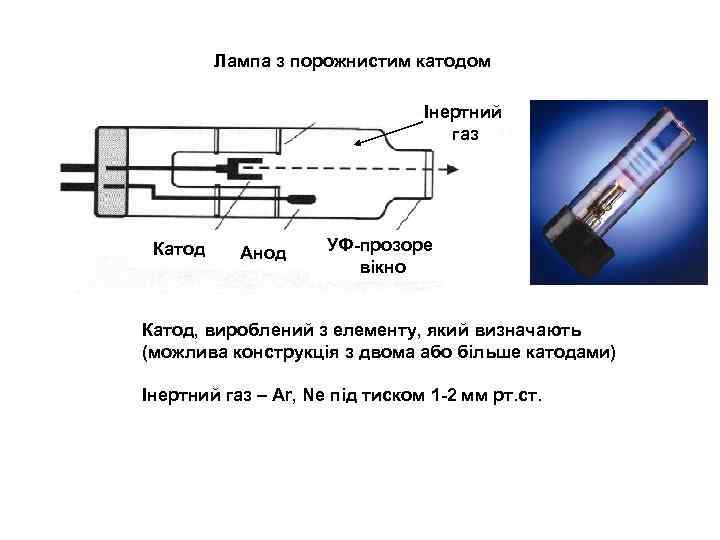 Лампа з порожнистим катодом Інертний газ Катод Анод УФ-прозоре вікно Катод, вироблений з елементу, який визначають (можлива конструкція з двома або більше катодами) Інертний газ – Ar, Ne під тиском 1 -2 мм рт. ст.
Лампа з порожнистим катодом Інертний газ Катод Анод УФ-прозоре вікно Катод, вироблений з елементу, який визначають (можлива конструкція з двома або більше катодами) Інертний газ – Ar, Ne під тиском 1 -2 мм рт. ст.
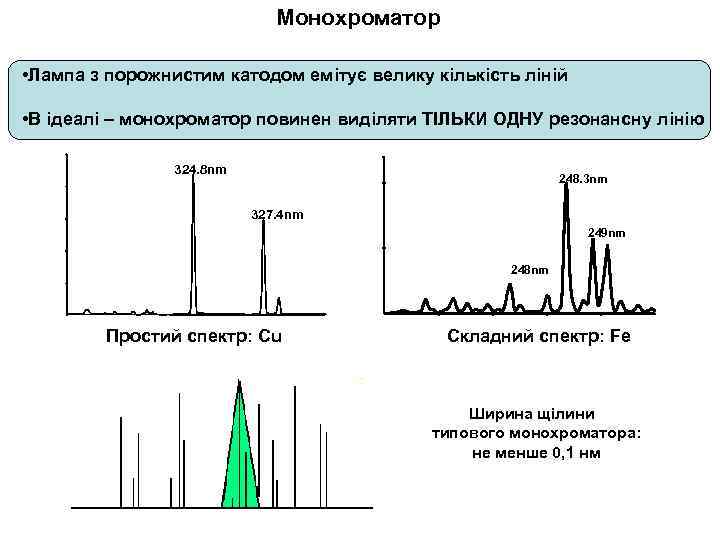 Монохроматор • Лампа з порожнистим катодом емітує велику кількість ліній • В ідеалі – монохроматор повинен виділяти ТІЛЬКИ ОДНУ резонансну лінію 324. 8 nm 248. 3 nm 327. 4 nm 249 nm 248 nm Простий спектр: Cu Складний спектр: Fe Ширина щілини типового монохроматора: не менше 0, 1 нм
Монохроматор • Лампа з порожнистим катодом емітує велику кількість ліній • В ідеалі – монохроматор повинен виділяти ТІЛЬКИ ОДНУ резонансну лінію 324. 8 nm 248. 3 nm 327. 4 nm 249 nm 248 nm Простий спектр: Cu Складний спектр: Fe Ширина щілини типового монохроматора: не менше 0, 1 нм
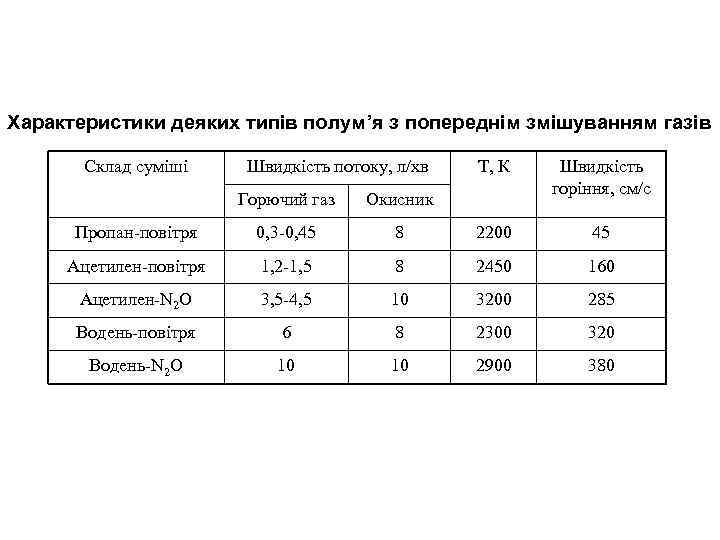 Характеристики деяких типів полум’я з попереднім змішуванням газів Склад суміші Швидкість потоку, л/хв Т, К Швидкість горіння, см/с Горючий газ Окисник Пропан-повітря 0, 3 -0, 45 8 2200 45 Ацетилен-повітря 1, 2 -1, 5 8 2450 160 Ацетилен-N 2 O 3, 5 -4, 5 10 3200 285 Водень-повітря 6 8 2300 320 Водень-N 2 O 10 10 2900 380
Характеристики деяких типів полум’я з попереднім змішуванням газів Склад суміші Швидкість потоку, л/хв Т, К Швидкість горіння, см/с Горючий газ Окисник Пропан-повітря 0, 3 -0, 45 8 2200 45 Ацетилен-повітря 1, 2 -1, 5 8 2450 160 Ацетилен-N 2 O 3, 5 -4, 5 10 3200 285 Водень-повітря 6 8 2300 320 Водень-N 2 O 10 10 2900 380
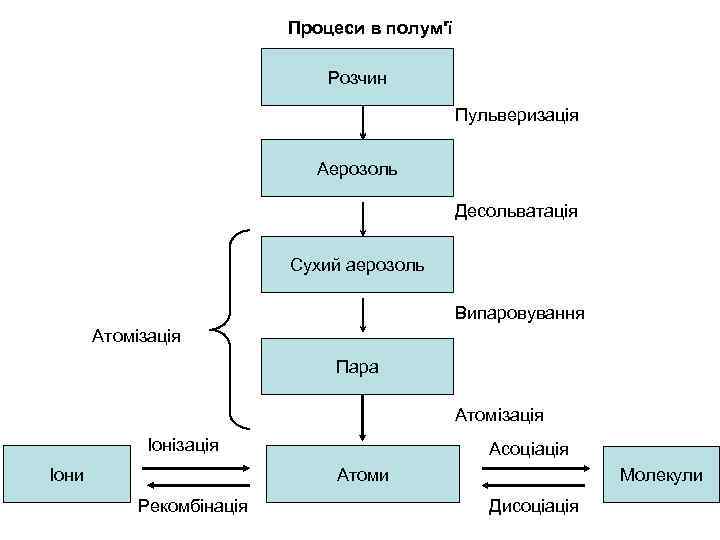 Процеси в полум'ї Розчин Пульверизація Аерозоль Десольватація Сухий аерозоль Випаровування Атомізація Пара Атомізація Іони Асоціація Атоми Рекомбінація Молекули Дисоціація
Процеси в полум'ї Розчин Пульверизація Аерозоль Десольватація Сухий аерозоль Випаровування Атомізація Пара Атомізація Іони Асоціація Атоми Рекомбінація Молекули Дисоціація
 Переваги і недоліки атомізації у полум’ї Переваги: • Стабільність роботи атомізатора • Висока відтворюваність результатів: Sr = 1 -3% • Експресність визначення (~5 секунд на пробу) • Невисока вартість обладнання • Слабкі ефекти матриці Недоліки: • Тільки аналіз розчинів • Вибухонебезпечність газів • Іонізація • Розбавлення проби газом • Невисока ефективність - >90% проби йде у злив! • Час життя вільного атома у полум’ї – 10 -4 с Чутливість – 1/100 від теоретичної
Переваги і недоліки атомізації у полум’ї Переваги: • Стабільність роботи атомізатора • Висока відтворюваність результатів: Sr = 1 -3% • Експресність визначення (~5 секунд на пробу) • Невисока вартість обладнання • Слабкі ефекти матриці Недоліки: • Тільки аналіз розчинів • Вибухонебезпечність газів • Іонізація • Розбавлення проби газом • Невисока ефективність - >90% проби йде у злив! • Час життя вільного атома у полум’ї – 10 -4 с Чутливість – 1/100 від теоретичної
 Взаємодія ЕМВ з речовиною
Взаємодія ЕМВ з речовиною
 Взаємодія ЕМВ з речовиною
Взаємодія ЕМВ з речовиною


