Vitamin.pptx
- Количество слайдов: 30
 КИЇВСЬКИЙ НАЦІОНАЛЬНИЙ УНІВЕРСИТЕТ ІМ. ТАРАСА ШЕВЧЕНКА Визначення вітаміну Е у харчових продуктах Виконала: студентка І курсу магістратури Кафедри аналітичної хімії Дячук Анна
КИЇВСЬКИЙ НАЦІОНАЛЬНИЙ УНІВЕРСИТЕТ ІМ. ТАРАСА ШЕВЧЕНКА Визначення вітаміну Е у харчових продуктах Виконала: студентка І курсу магістратури Кафедри аналітичної хімії Дячук Анна
 ЗАГАЛЬНА ІНФОРМАЦІЯ Вітаміни (від лат. Vita – життя) – низькомолекулярні органічні сполуки різної хімічної природи, що є необхідні для здійснення життєво важливих біохімічних та фізіологічних процесів у живих організмах. Організм людини та тварини не синтезує вітаміни або не у достатніх кількостях, тому від повинен отримувати їх у готовому вигляді з продуктів харчування.
ЗАГАЛЬНА ІНФОРМАЦІЯ Вітаміни (від лат. Vita – життя) – низькомолекулярні органічні сполуки різної хімічної природи, що є необхідні для здійснення життєво важливих біохімічних та фізіологічних процесів у живих організмах. Організм людини та тварини не синтезує вітаміни або не у достатніх кількостях, тому від повинен отримувати їх у готовому вигляді з продуктів харчування.
 ЗАГАЛЬНА ІНФОРМАЦІЯ Основні групи продуктів харчування для збагачення вітамінами: q борошно і хлібобулочні вироби - вітаміни групи В; q продукти дитячого харчування - всі вітаміни; q напої, в тому числі сухі концентрати - всі вітаміни, окрім А, Д; q молочні продукти - вітаміни А, Д, Е, К q фруктові соки - всі вітаміни, окрім А, Д. При виробництві продуктів харчування контроль за вмістом вітамінів передбачені в продуктах, де вони додаються або де необхідно гарантувати їх певний зміст. Додані та контрольовані вітамінами в плодоовочевих консервах є вітамін С і каротин, вітаміни В 1 і В 2 визначають при встановленні харчової цінності продукту.
ЗАГАЛЬНА ІНФОРМАЦІЯ Основні групи продуктів харчування для збагачення вітамінами: q борошно і хлібобулочні вироби - вітаміни групи В; q продукти дитячого харчування - всі вітаміни; q напої, в тому числі сухі концентрати - всі вітаміни, окрім А, Д; q молочні продукти - вітаміни А, Д, Е, К q фруктові соки - всі вітаміни, окрім А, Д. При виробництві продуктів харчування контроль за вмістом вітамінів передбачені в продуктах, де вони додаються або де необхідно гарантувати їх певний зміст. Додані та контрольовані вітамінами в плодоовочевих консервах є вітамін С і каротин, вітаміни В 1 і В 2 визначають при встановленні харчової цінності продукту.
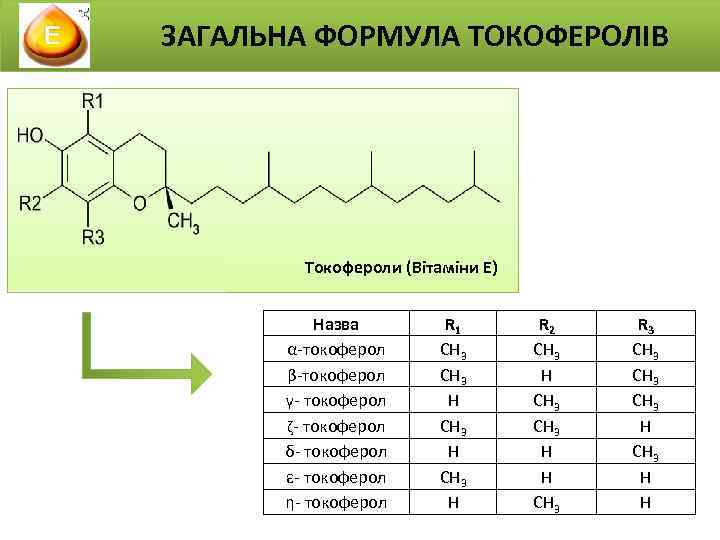 ЗАГАЛЬНА ФОРМУЛА ТОКОФЕРОЛІВ Токофероли (Вітаміни Е) Назва α-токоферол β-токоферол γ- токоферол ζ- токоферол δ- токоферол ε- токоферол η- токоферол R 1 СН 3 Н R 2 СН 3 Н Н СН 3 R 3 СН 3 Н Н
ЗАГАЛЬНА ФОРМУЛА ТОКОФЕРОЛІВ Токофероли (Вітаміни Е) Назва α-токоферол β-токоферол γ- токоферол ζ- токоферол δ- токоферол ε- токоферол η- токоферол R 1 СН 3 Н R 2 СН 3 Н Н СН 3 R 3 СН 3 Н Н
 ВМІСТ ВІТАМІНІВ У ХАРЧОВИХ ПРОДУКТАХ Значення для організму: v Є головною поживною речовиною – антиоксидантом. v Уповільнює процес старіння клітин унаслідок окислення. v Покращує живлення клітин. v Зміцнює стінки кровоносних судин. v Запобігає утворенню тромбів і сприяє їх розсмоктуванню. В якості харчової добавки позначається як E 306 (суміш токоферолів), E 307 (αтокоферол), E 308 (γ-токоферол) та E 309 (δ-токоферол).
ВМІСТ ВІТАМІНІВ У ХАРЧОВИХ ПРОДУКТАХ Значення для організму: v Є головною поживною речовиною – антиоксидантом. v Уповільнює процес старіння клітин унаслідок окислення. v Покращує живлення клітин. v Зміцнює стінки кровоносних судин. v Запобігає утворенню тромбів і сприяє їх розсмоктуванню. В якості харчової добавки позначається як E 306 (суміш токоферолів), E 307 (αтокоферол), E 308 (γ-токоферол) та E 309 (δ-токоферол).
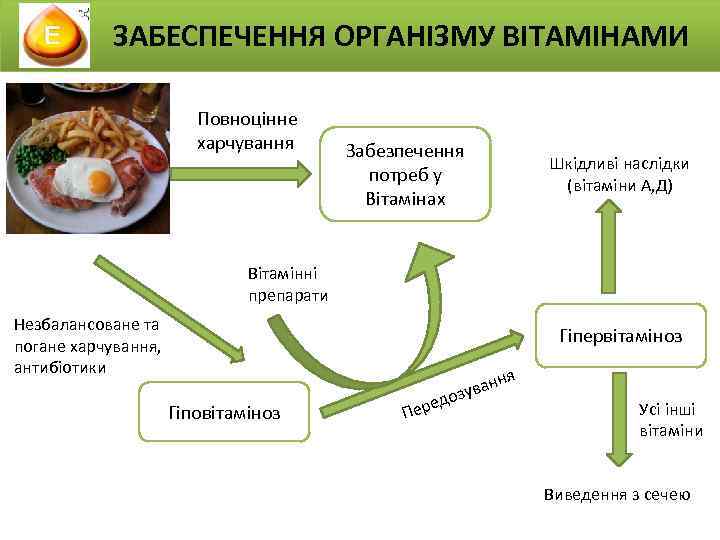 ЗАБЕСПЕЧЕННЯ ОРГАНІЗМУ ВІТАМІНАМИ Повноцінне харчування Забезпечення потреб у Вітамінах Шкідливі наслідки (вітаміни А, Д) Вітамінні препарати Незбалансоване та погане харчування, антибіотики Гіпервітаміноз Гіповітаміноз Пе ня ван зу едо р Усі інші вітаміни Виведення з сечею
ЗАБЕСПЕЧЕННЯ ОРГАНІЗМУ ВІТАМІНАМИ Повноцінне харчування Забезпечення потреб у Вітамінах Шкідливі наслідки (вітаміни А, Д) Вітамінні препарати Незбалансоване та погане харчування, антибіотики Гіпервітаміноз Гіповітаміноз Пе ня ван зу едо р Усі інші вітаміни Виведення з сечею
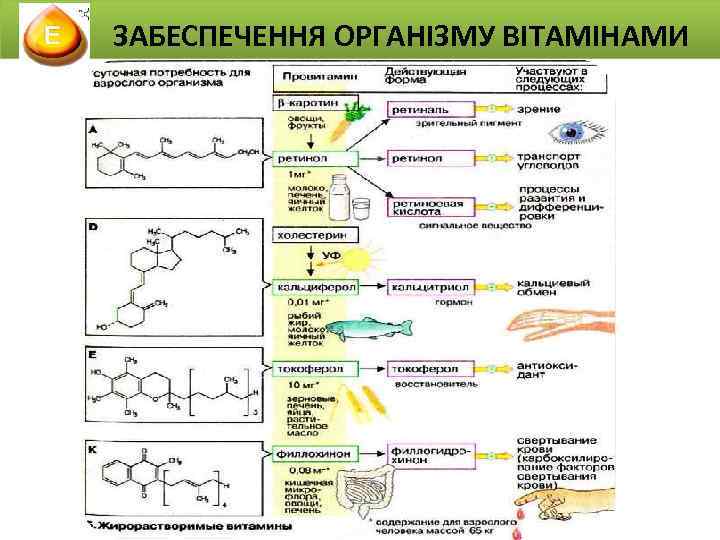 ЗАБЕСПЕЧЕННЯ ОРГАНІЗМУ ВІТАМІНАМИ
ЗАБЕСПЕЧЕННЯ ОРГАНІЗМУ ВІТАМІНАМИ
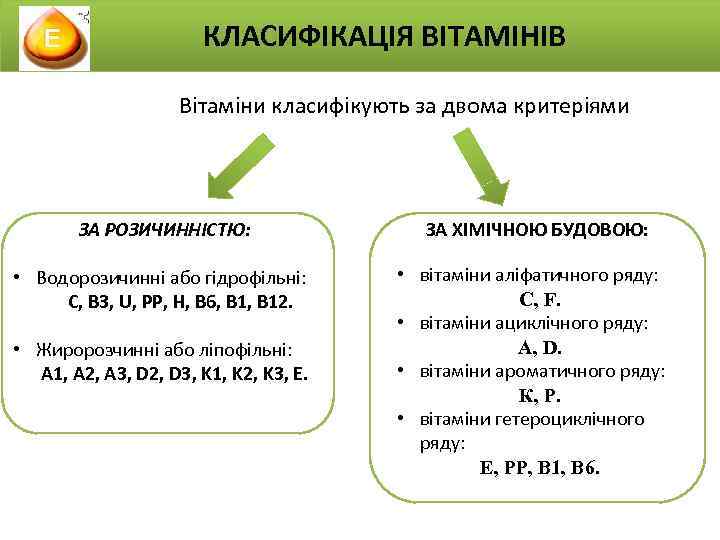 КЛАСИФІКАЦІЯ ВІТАМІНІВ Вітаміни класифікують за двома критеріями ЗА РОЗИЧИННІСТЮ: • Водорозичинні або гідрофільні: С, В 3, U, РР, Н, В 6, В 12. • Жиророзчинні або ліпофільні: А 1, А 2, А 3, D 2, D 3, K 1, K 2, K 3, E. ЗА ХІМІЧНОЮ БУДОВОЮ: • вітаміни аліфатичного ряду: С, F. • вітаміни ациклічного ряду: А, D. • вітаміни ароматичного ряду: К, Р. • вітаміни гетероциклічного ряду: Е, РР, В 1, В 6.
КЛАСИФІКАЦІЯ ВІТАМІНІВ Вітаміни класифікують за двома критеріями ЗА РОЗИЧИННІСТЮ: • Водорозичинні або гідрофільні: С, В 3, U, РР, Н, В 6, В 12. • Жиророзчинні або ліпофільні: А 1, А 2, А 3, D 2, D 3, K 1, K 2, K 3, E. ЗА ХІМІЧНОЮ БУДОВОЮ: • вітаміни аліфатичного ряду: С, F. • вітаміни ациклічного ряду: А, D. • вітаміни ароматичного ряду: К, Р. • вітаміни гетероциклічного ряду: Е, РР, В 1, В 6.
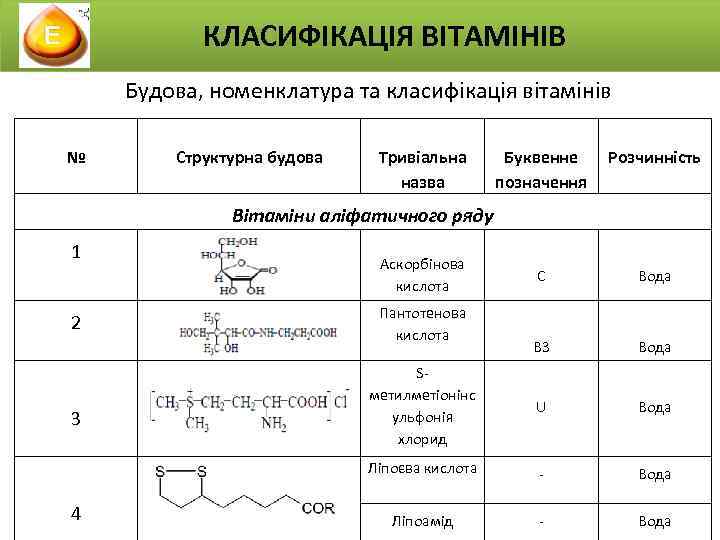 КЛАСИФІКАЦІЯ ВІТАМІНІВ Будова, номенклатура та класифікація вітамінів № Структурна будова Тривіальна назва Буквенне позначення Розчинність Вітаміни аліфатичного ряду 1 2 3 4 Аскорбінова кислота Пантотенова кислота С Вода В 3 Вода Sметилметіонінс ульфонія хлорид U Вода Ліпоєва кислота - Вода Ліпоамід - Вода
КЛАСИФІКАЦІЯ ВІТАМІНІВ Будова, номенклатура та класифікація вітамінів № Структурна будова Тривіальна назва Буквенне позначення Розчинність Вітаміни аліфатичного ряду 1 2 3 4 Аскорбінова кислота Пантотенова кислота С Вода В 3 Вода Sметилметіонінс ульфонія хлорид U Вода Ліпоєва кислота - Вода Ліпоамід - Вода
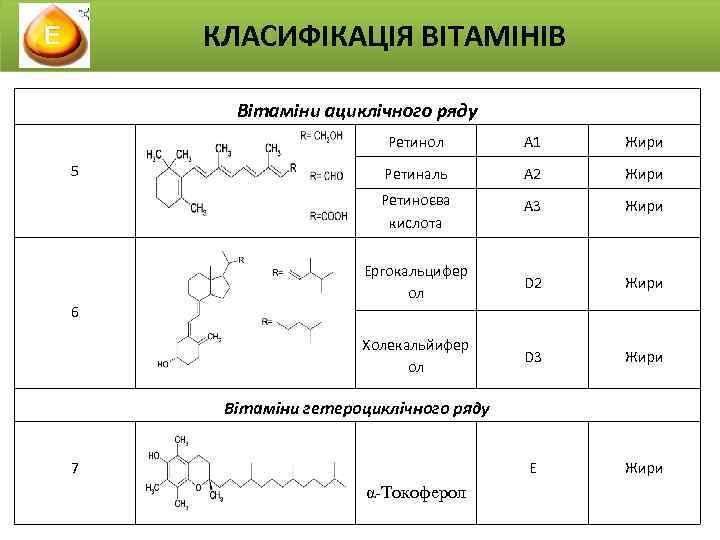 КЛАСИФІКАЦІЯ ВІТАМІНІВ Вітаміни ациклічного ряду Ретинол А 1 Жири 5 Ретиналь А 2 Жири Ретиноєва кислота А 3 Жири Ергокальцифер ол D 2 Жири D 3 Жири E Жири 6 Холекальйифер ол Вітаміни гетероциклічного ряду 7 α-Токоферол
КЛАСИФІКАЦІЯ ВІТАМІНІВ Вітаміни ациклічного ряду Ретинол А 1 Жири 5 Ретиналь А 2 Жири Ретиноєва кислота А 3 Жири Ергокальцифер ол D 2 Жири D 3 Жири E Жири 6 Холекальйифер ол Вітаміни гетероциклічного ряду 7 α-Токоферол
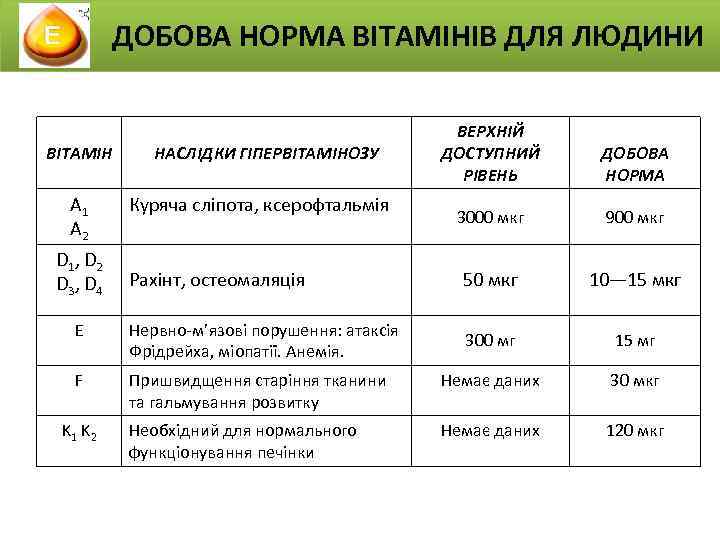 ДОБОВА НОРМА ВІТАМІНІВ ДЛЯ ЛЮДИНИ ВЕРХНІЙ ДОСТУПНИЙ РІВЕНЬ ДОБОВА НОРМА 3000 мкг 900 мкг Рахінт, остеомаляція 50 мкг 10— 15 мкг Е Нервно-м’язові порушення: атаксія Фрідрейха, міопатії. Анемія. 300 мг 15 мг F Пришвидщення старіння тканини та гальмування розвитку Немає даних 30 мкг Необхідний для нормального функціонування печінки Немає даних 120 мкг ВІТАМІН A 1 А 2 D 1, D 2 D 3, D 4 K 1 K 2 НАСЛІДКИ ГІПЕРВІТАМІНОЗУ Куряча сліпота, ксерофтальмія
ДОБОВА НОРМА ВІТАМІНІВ ДЛЯ ЛЮДИНИ ВЕРХНІЙ ДОСТУПНИЙ РІВЕНЬ ДОБОВА НОРМА 3000 мкг 900 мкг Рахінт, остеомаляція 50 мкг 10— 15 мкг Е Нервно-м’язові порушення: атаксія Фрідрейха, міопатії. Анемія. 300 мг 15 мг F Пришвидщення старіння тканини та гальмування розвитку Немає даних 30 мкг Необхідний для нормального функціонування печінки Немає даних 120 мкг ВІТАМІН A 1 А 2 D 1, D 2 D 3, D 4 K 1 K 2 НАСЛІДКИ ГІПЕРВІТАМІНОЗУ Куряча сліпота, ксерофтальмія
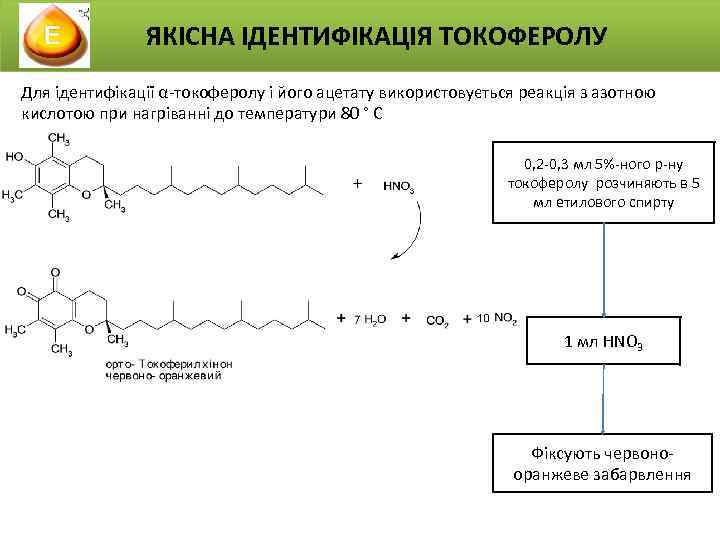 ЯКІСНА ІДЕНТИФІКАЦІЯ ТОКОФЕРОЛУ Для ідентифікації α-токоферолу і його ацетату використовується реакція з азотною кислотою при нагріванні до температури 80 ° С 0, 2 -0, 3 мл 5%-ного р-ну токоферолу розчиняють в 5 мл етилового спирту 1 мл HNO 3 Фіксують червонооранжеве забарвлення
ЯКІСНА ІДЕНТИФІКАЦІЯ ТОКОФЕРОЛУ Для ідентифікації α-токоферолу і його ацетату використовується реакція з азотною кислотою при нагріванні до температури 80 ° С 0, 2 -0, 3 мл 5%-ного р-ну токоферолу розчиняють в 5 мл етилового спирту 1 мл HNO 3 Фіксують червонооранжеве забарвлення
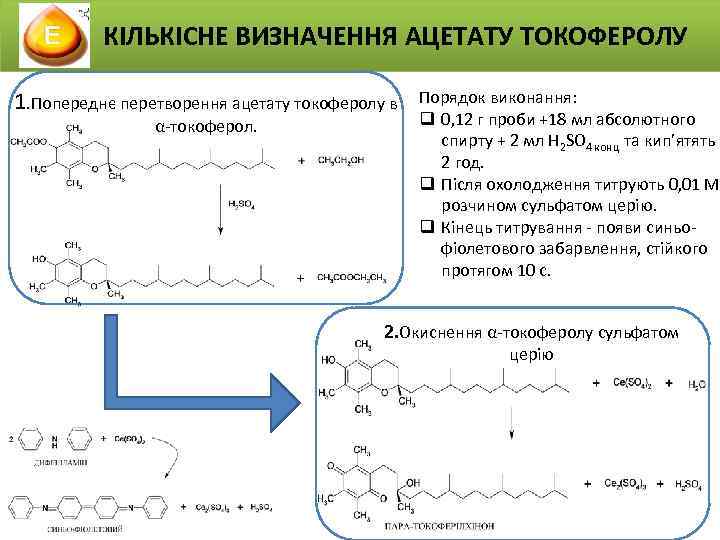 КІЛЬКІСНЕ ВИЗНАЧЕННЯ АЦЕТАТУ ТОКОФЕРОЛУ 1. Попереднє перетворення ацетату токоферолу в α-токоферол. Порядок виконання: q 0, 12 г проби +18 мл абсолютного спирту + 2 мл H 2 SO 4 конц та кип’ятять 2 год. q Після охолодження титрують 0, 01 М розчином сульфатом церію. q Кінець титрування - появи синьофіолетового забарвлення, стійкого протягом 10 с. 2. Окиснення α-токоферолу сульфатом церію
КІЛЬКІСНЕ ВИЗНАЧЕННЯ АЦЕТАТУ ТОКОФЕРОЛУ 1. Попереднє перетворення ацетату токоферолу в α-токоферол. Порядок виконання: q 0, 12 г проби +18 мл абсолютного спирту + 2 мл H 2 SO 4 конц та кип’ятять 2 год. q Після охолодження титрують 0, 01 М розчином сульфатом церію. q Кінець титрування - появи синьофіолетового забарвлення, стійкого протягом 10 с. 2. Окиснення α-токоферолу сульфатом церію
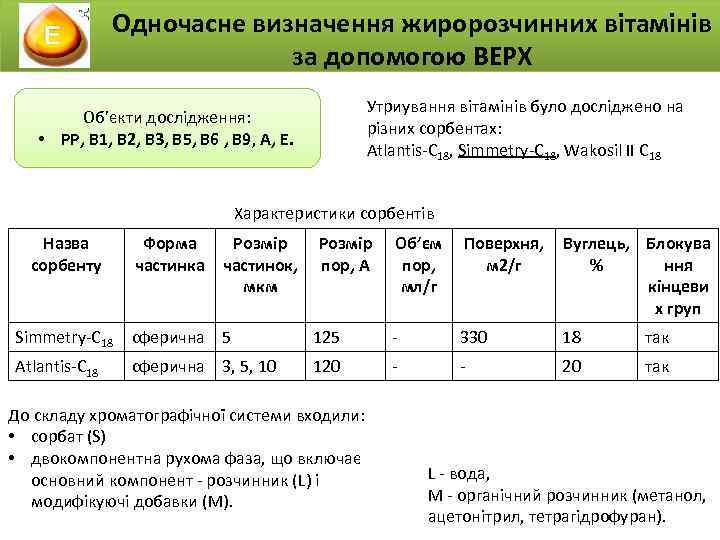 Одночасне визначення жиророзчинних вітамінів за допомогою ВЕРХ Утриування вітамінів було досліджено на різних сорбентах: Atlantis-C 18, Simmetry-C 18, Wakosil II C 18 Об’єкти дослідження: • PP, B 1, B 2, B 3, B 5, B 6 , B 9, A, E. Характеристики сорбентів Назва сорбенту Форма частинка Розмір частинок, пор, А мкм Об’єм Поверхня, Вуглець, Блокува пор, м 2/г % ння мл/г кінцеви х груп Simmetry-C 18 сферична 5 125 - 330 18 так Atlantis-C 18 сферична 3, 5, 10 120 - - 20 так До складу хроматографічної системи входили: • сорбат (S) • двокомпонентна рухома фаза, що включає основний компонент - розчинник (L) і модифікуючі добавки (M). L - вода, M - органічний розчинник (метанол, ацетонітрил, тетрагідрофуран).
Одночасне визначення жиророзчинних вітамінів за допомогою ВЕРХ Утриування вітамінів було досліджено на різних сорбентах: Atlantis-C 18, Simmetry-C 18, Wakosil II C 18 Об’єкти дослідження: • PP, B 1, B 2, B 3, B 5, B 6 , B 9, A, E. Характеристики сорбентів Назва сорбенту Форма частинка Розмір частинок, пор, А мкм Об’єм Поверхня, Вуглець, Блокува пор, м 2/г % ння мл/г кінцеви х груп Simmetry-C 18 сферична 5 125 - 330 18 так Atlantis-C 18 сферична 3, 5, 10 120 - - 20 так До складу хроматографічної системи входили: • сорбат (S) • двокомпонентна рухома фаза, що включає основний компонент - розчинник (L) і модифікуючі добавки (M). L - вода, M - органічний розчинник (метанол, ацетонітрил, тетрагідрофуран).
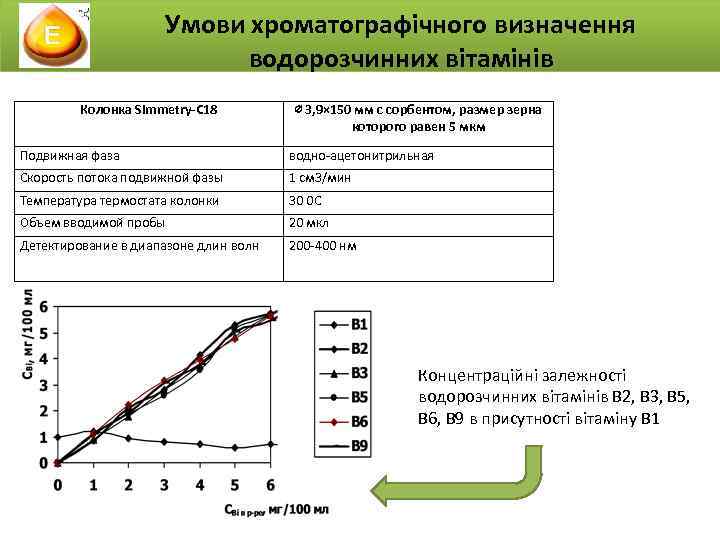 Умови хроматографічного визначення водорозчинних вітамінів Колонка Simmetry-C 18 ∅ 3, 9× 150 мм с сорбентом, размер зерна которого равен 5 мкм Подвижная фаза водно-ацетонитрильная Скорость потока подвижной фазы 1 см 3/мин Температура термостата колонки 30 0 С Объем вводимой пробы 20 мкл Детектирование в диапазоне длин волн 200 -400 нм Концентраційні залежності водорозчинних вітамінів В 2, В 3, В 5, В 6, В 9 в присутності вітаміну В 1
Умови хроматографічного визначення водорозчинних вітамінів Колонка Simmetry-C 18 ∅ 3, 9× 150 мм с сорбентом, размер зерна которого равен 5 мкм Подвижная фаза водно-ацетонитрильная Скорость потока подвижной фазы 1 см 3/мин Температура термостата колонки 30 0 С Объем вводимой пробы 20 мкл Детектирование в диапазоне длин волн 200 -400 нм Концентраційні залежності водорозчинних вітамінів В 2, В 3, В 5, В 6, В 9 в присутності вітаміну В 1
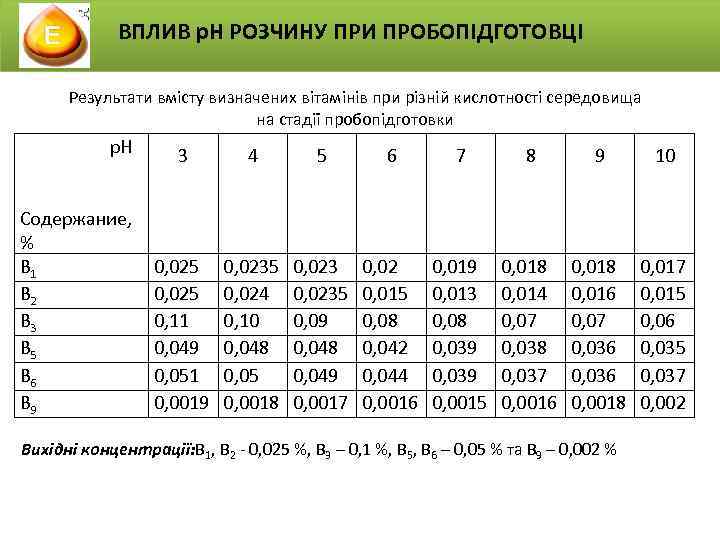 ВПЛИВ р. Н РОЗЧИНУ ПРИ ПРОБОПІДГОТОВЦІ Результати вмісту визначених вітамінів при різній кислотності середовища на стадії пробопідготовки р. Н 3 Содержание, % В 1 0, 025 В 2 0, 025 В 3 0, 11 В 5 0, 049 В 6 0, 051 В 9 0, 0019 4 5 6 7 8 9 10 0, 0235 0, 024 0, 10 0, 048 0, 05 0, 0018 0, 0235 0, 09 0, 048 0, 049 0, 0017 0, 02 0, 015 0, 08 0, 042 0, 044 0, 0016 0, 019 0, 013 0, 08 0, 039 0, 0015 0, 018 0, 014 0, 07 0, 038 0, 037 0, 0016 0, 018 0, 016 0, 07 0, 036 0, 0018 0, 017 0, 015 0, 06 0, 035 0, 037 0, 002 Вихідні концентрації: В 1, В 2 - 0, 025 %, В 3 – 0, 1 %, В 5, В 6 – 0, 05 % та В 9 – 0, 002 %
ВПЛИВ р. Н РОЗЧИНУ ПРИ ПРОБОПІДГОТОВЦІ Результати вмісту визначених вітамінів при різній кислотності середовища на стадії пробопідготовки р. Н 3 Содержание, % В 1 0, 025 В 2 0, 025 В 3 0, 11 В 5 0, 049 В 6 0, 051 В 9 0, 0019 4 5 6 7 8 9 10 0, 0235 0, 024 0, 10 0, 048 0, 05 0, 0018 0, 0235 0, 09 0, 048 0, 049 0, 0017 0, 02 0, 015 0, 08 0, 042 0, 044 0, 0016 0, 019 0, 013 0, 08 0, 039 0, 0015 0, 018 0, 014 0, 07 0, 038 0, 037 0, 0016 0, 018 0, 016 0, 07 0, 036 0, 0018 0, 017 0, 015 0, 06 0, 035 0, 037 0, 002 Вихідні концентрації: В 1, В 2 - 0, 025 %, В 3 – 0, 1 %, В 5, В 6 – 0, 05 % та В 9 – 0, 002 %
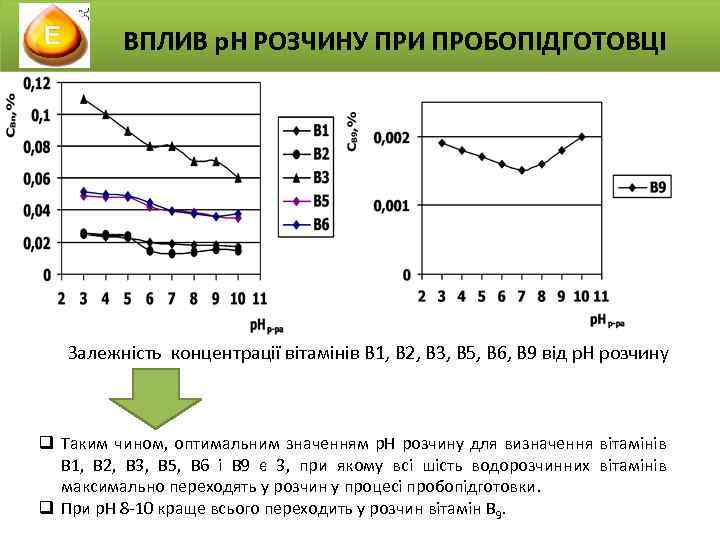 ВПЛИВ р. Н РОЗЧИНУ ПРИ ПРОБОПІДГОТОВЦІ Залежність концентрації вітамінів В 1, В 2, В 3, В 5, В 6, В 9 від р. Н розчину q Таким чином, оптимальним значенням р. Н розчину для визначення вітамінів В 1, В 2, В 3, В 5, В 6 і В 9 є 3, при якому всі шість водорозчинних вітамінів максимально переходять у розчин у процесі пробопідготовки. q При р. Н 8 -10 краще всього переходить у розчин вітамін В 9.
ВПЛИВ р. Н РОЗЧИНУ ПРИ ПРОБОПІДГОТОВЦІ Залежність концентрації вітамінів В 1, В 2, В 3, В 5, В 6, В 9 від р. Н розчину q Таким чином, оптимальним значенням р. Н розчину для визначення вітамінів В 1, В 2, В 3, В 5, В 6 і В 9 є 3, при якому всі шість водорозчинних вітамінів максимально переходять у розчин у процесі пробопідготовки. q При р. Н 8 -10 краще всього переходить у розчин вітамін В 9.
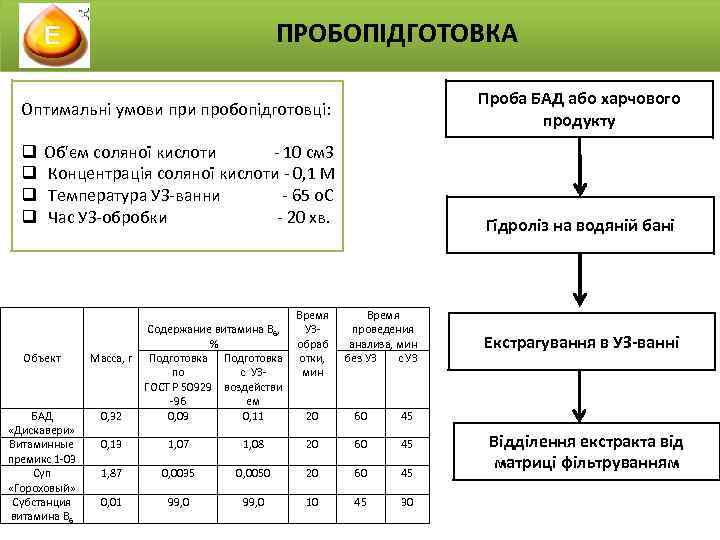 ПРОБОПІДГОТОВКА Проба БАД або харчового продукту Оптимальні умови пробопідготовці: q q Об'єм соляної кислоти - 10 см 3 Концентрація соляної кислоти - 0, 1 М Температура УЗ-ванни - 65 о. С Час УЗ-обробки - 20 хв. Объект Масса, г БАД «Дискавери» Витаминные премикс 1 -03 Суп «Гороховый» Субстанция витамина В 6 0, 32 Содержание витамина В 6, % Подготовка по с УЗГОСТ Р 50929 воздействи -96 ем 0, 09 0, 11 Гідроліз на водяній бані Время УЗпроведения обраб анализа, мин с УЗ отки, без УЗ мин 20 60 Екстрагування в УЗ-ванні 45 0, 13 1, 07 1, 08 20 60 45 1, 87 0, 0035 0, 0050 20 60 45 0, 01 99, 0 10 45 30 Відділення екстракта від матриці фільтруванням
ПРОБОПІДГОТОВКА Проба БАД або харчового продукту Оптимальні умови пробопідготовці: q q Об'єм соляної кислоти - 10 см 3 Концентрація соляної кислоти - 0, 1 М Температура УЗ-ванни - 65 о. С Час УЗ-обробки - 20 хв. Объект Масса, г БАД «Дискавери» Витаминные премикс 1 -03 Суп «Гороховый» Субстанция витамина В 6 0, 32 Содержание витамина В 6, % Подготовка по с УЗГОСТ Р 50929 воздействи -96 ем 0, 09 0, 11 Гідроліз на водяній бані Время УЗпроведения обраб анализа, мин с УЗ отки, без УЗ мин 20 60 Екстрагування в УЗ-ванні 45 0, 13 1, 07 1, 08 20 60 45 1, 87 0, 0035 0, 0050 20 60 45 0, 01 99, 0 10 45 30 Відділення екстракта від матриці фільтруванням
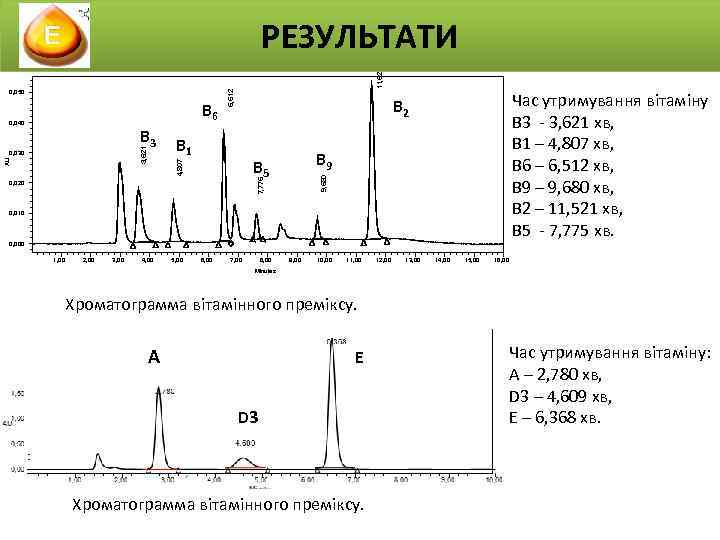 В 6 В 9 В 5 7, 775 AU В 1 4, 807 3, 621 В 3 0, 030 Час утримування вітаміну В 3 - 3, 621 хв, В 1 – 4, 807 хв, В 6 – 6, 512 хв, В 9 – 9, 680 хв, В 2 – 11, 521 хв, В 5 - 7, 775 хв. В 2 9, 680 0, 040 6, 512 0, 050 11, 521 РЕЗУЛЬТАТИ 0, 020 0, 010 0, 000 1, 00 2, 00 3, 00 4, 00 5, 00 6, 00 7, 00 8, 00 9, 00 10, 00 11, 00 12, 00 13, 00 14, 00 15, 00 16, 00 Minutes Хроматограмма вітамінного преміксу. А Е D 3 Хроматограмма вітамінного преміксу. Час утримування вітаміну: А – 2, 780 хв, D 3 – 4, 609 хв, Е – 6, 368 хв.
В 6 В 9 В 5 7, 775 AU В 1 4, 807 3, 621 В 3 0, 030 Час утримування вітаміну В 3 - 3, 621 хв, В 1 – 4, 807 хв, В 6 – 6, 512 хв, В 9 – 9, 680 хв, В 2 – 11, 521 хв, В 5 - 7, 775 хв. В 2 9, 680 0, 040 6, 512 0, 050 11, 521 РЕЗУЛЬТАТИ 0, 020 0, 010 0, 000 1, 00 2, 00 3, 00 4, 00 5, 00 6, 00 7, 00 8, 00 9, 00 10, 00 11, 00 12, 00 13, 00 14, 00 15, 00 16, 00 Minutes Хроматограмма вітамінного преміксу. А Е D 3 Хроматограмма вітамінного преміксу. Час утримування вітаміну: А – 2, 780 хв, D 3 – 4, 609 хв, Е – 6, 368 хв.
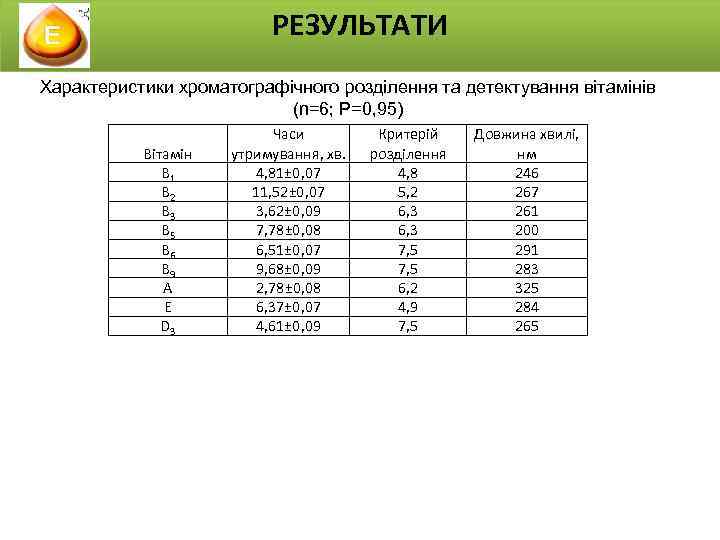 РЕЗУЛЬТАТИ Характеристики хроматографічного розділення та детектування вітамінів (n=6; Р=0, 95) Вітамін В 1 В 2 В 3 В 5 В 6 В 9 А Е D 3 Часи утримування, хв. 4, 81± 0, 07 11, 52± 0, 07 3, 62± 0, 09 7, 78± 0, 08 6, 51± 0, 07 9, 68± 0, 09 2, 78± 0, 08 6, 37± 0, 07 4, 61± 0, 09 Критерій розділення 4, 8 5, 2 6, 3 7, 5 6, 2 4, 9 7, 5 Довжина хвилі, нм 246 267 261 200 291 283 325 284 265
РЕЗУЛЬТАТИ Характеристики хроматографічного розділення та детектування вітамінів (n=6; Р=0, 95) Вітамін В 1 В 2 В 3 В 5 В 6 В 9 А Е D 3 Часи утримування, хв. 4, 81± 0, 07 11, 52± 0, 07 3, 62± 0, 09 7, 78± 0, 08 6, 51± 0, 07 9, 68± 0, 09 2, 78± 0, 08 6, 37± 0, 07 4, 61± 0, 09 Критерій розділення 4, 8 5, 2 6, 3 7, 5 6, 2 4, 9 7, 5 Довжина хвилі, нм 246 267 261 200 291 283 325 284 265
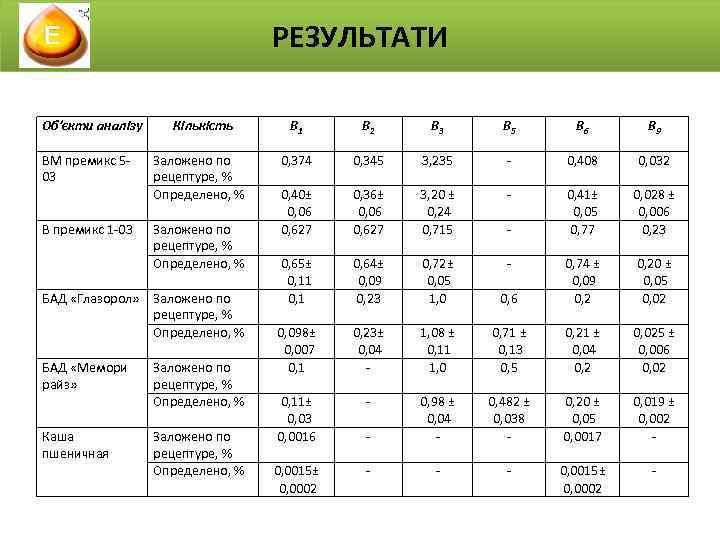 РЕЗУЛЬТАТИ Об’єкти аналізу ВМ премикс 503 В премикс 1 -03 Кількість Заложено по рецептуре, % Определено, % БАД «Глазорол» Заложено по рецептуре, % Определено, % БАД «Мемори райз» Каша пшеничная Заложено по рецептуре, % Определено, % В 1 В 2 В 3 В 5 В 6 В 9 0, 374 0, 345 3, 235 - 0, 408 0, 032 0, 40± 0, 06 0, 627 0, 36± 0, 06 0, 627 3, 20 ± 0, 24 0, 715 - 0, 41± 0, 05 0, 77 0, 028 ± 0, 006 0, 23 0, 65± 0, 11 0, 64± 0, 09 0, 23 0, 72± 0, 05 1, 0 0, 6 0, 74 ± 0, 09 0, 20 ± 0, 05 0, 02 0, 098± 0, 007 0, 1 0, 23± 0, 04 - 1, 08 ± 0, 11 1, 0 0, 71 ± 0, 13 0, 5 0, 21 ± 0, 04 0, 2 0, 025 ± 0, 006 0, 02 0, 11± 0, 03 0, 0016 - 0, 98 ± 0, 04 - 0, 482 ± 0, 038 - 0, 20 ± 0, 05 0, 0017 0, 019 ± 0, 002 - 0, 0015± 0, 0002 - -
РЕЗУЛЬТАТИ Об’єкти аналізу ВМ премикс 503 В премикс 1 -03 Кількість Заложено по рецептуре, % Определено, % БАД «Глазорол» Заложено по рецептуре, % Определено, % БАД «Мемори райз» Каша пшеничная Заложено по рецептуре, % Определено, % В 1 В 2 В 3 В 5 В 6 В 9 0, 374 0, 345 3, 235 - 0, 408 0, 032 0, 40± 0, 06 0, 627 0, 36± 0, 06 0, 627 3, 20 ± 0, 24 0, 715 - 0, 41± 0, 05 0, 77 0, 028 ± 0, 006 0, 23 0, 65± 0, 11 0, 64± 0, 09 0, 23 0, 72± 0, 05 1, 0 0, 6 0, 74 ± 0, 09 0, 20 ± 0, 05 0, 02 0, 098± 0, 007 0, 1 0, 23± 0, 04 - 1, 08 ± 0, 11 1, 0 0, 71 ± 0, 13 0, 5 0, 21 ± 0, 04 0, 2 0, 025 ± 0, 006 0, 02 0, 11± 0, 03 0, 0016 - 0, 98 ± 0, 04 - 0, 482 ± 0, 038 - 0, 20 ± 0, 05 0, 0017 0, 019 ± 0, 002 - 0, 0015± 0, 0002 - -
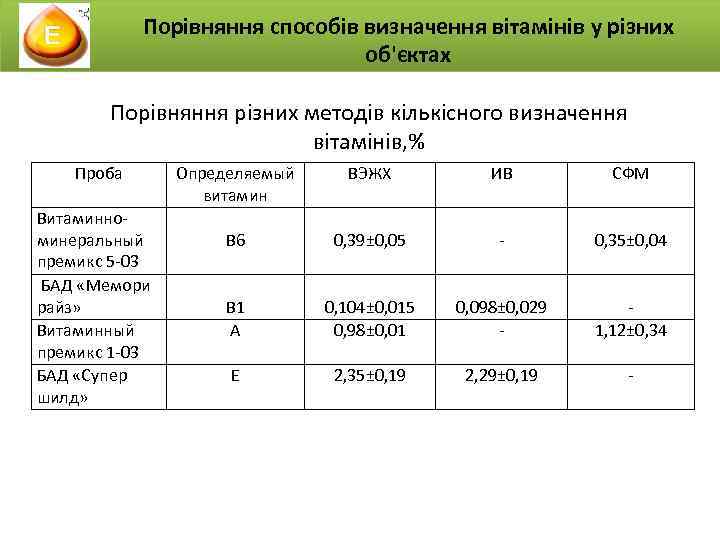 Порівняння способів визначення вітамінів у різних об'єктах Порівняння різних методів кількісного визначення вітамінів, % Проба Витаминноминеральный премикс 5 -03 БАД «Мемори райз» Витаминный премикс 1 -03 БАД «Супер шилд» Определяемый витамин В 6 ВЭЖХ ИВ СФМ 0, 39± 0, 05 - 0, 35± 0, 04 В 1 А 0, 104± 0, 015 0, 98± 0, 01 0, 098± 0, 029 - 1, 12± 0, 34 Е 2, 35± 0, 19 2, 29± 0, 19 -
Порівняння способів визначення вітамінів у різних об'єктах Порівняння різних методів кількісного визначення вітамінів, % Проба Витаминноминеральный премикс 5 -03 БАД «Мемори райз» Витаминный премикс 1 -03 БАД «Супер шилд» Определяемый витамин В 6 ВЭЖХ ИВ СФМ 0, 39± 0, 05 - 0, 35± 0, 04 В 1 А 0, 104± 0, 015 0, 98± 0, 01 0, 098± 0, 029 - 1, 12± 0, 34 Е 2, 35± 0, 19 2, 29± 0, 19 -
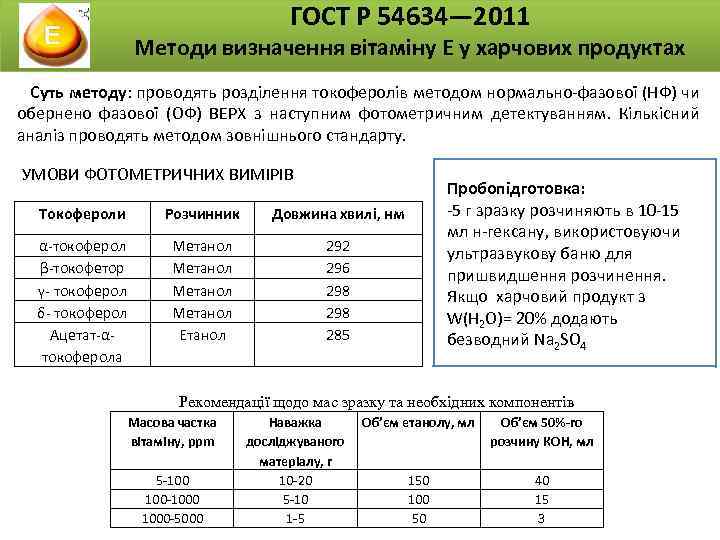 ГОСТ Р 54634— 2011 Методи визначення вітаміну Е у харчових продуктах Суть методу: проводять розділення токоферолів методом нормально-фазової (НФ) чи обернено фазової (ОФ) ВЕРХ з наступним фотометричним детектуванням. Кількісний аналіз проводять методом зовнішнього стандарту. УМОВИ ФОТОМЕТРИЧНИХ ВИМІРІВ Токофероли Розчинник Довжина хвилі, нм α-токоферол β-токофетор γ- токоферол δ- токоферол Ацетат-αтокоферола Метанол Етанол Пробопідготовка: -5 г зразку розчиняють в 10 -15 мл н-гексану, використовуючи ультразвукову баню для пришвидшення розчинення. Якщо харчовий продукт з W(H 2 O)= 20% додають безводний Na 2 SO 4 292 296 298 285 Рекомендації щодо мас зразку та необхідних компонентів Масова частка вітаміну, ppm 5 -100 100 -1000 -5000 Наважка досліджуваного матеріалу, г 10 -20 5 -10 1 -5 Об’єм етанолу, мл Об’єм 50%-го розчину КОН, мл 150 100 50 40 15 3
ГОСТ Р 54634— 2011 Методи визначення вітаміну Е у харчових продуктах Суть методу: проводять розділення токоферолів методом нормально-фазової (НФ) чи обернено фазової (ОФ) ВЕРХ з наступним фотометричним детектуванням. Кількісний аналіз проводять методом зовнішнього стандарту. УМОВИ ФОТОМЕТРИЧНИХ ВИМІРІВ Токофероли Розчинник Довжина хвилі, нм α-токоферол β-токофетор γ- токоферол δ- токоферол Ацетат-αтокоферола Метанол Етанол Пробопідготовка: -5 г зразку розчиняють в 10 -15 мл н-гексану, використовуючи ультразвукову баню для пришвидшення розчинення. Якщо харчовий продукт з W(H 2 O)= 20% додають безводний Na 2 SO 4 292 296 298 285 Рекомендації щодо мас зразку та необхідних компонентів Масова частка вітаміну, ppm 5 -100 100 -1000 -5000 Наважка досліджуваного матеріалу, г 10 -20 5 -10 1 -5 Об’єм етанолу, мл Об’єм 50%-го розчину КОН, мл 150 100 50 40 15 3
 Визначення вітаміну Е в рослинній олії за допомогою ВЕРХ з використанням УФ-детектора Пробопідготовка: § Розчинення досліджуваного зразку у гексані (1: 10). § До 20 мл отриманого р-ну + 60 мл СН 3 ОН + 20 мл внутрішнього стандарту (С= 30 мг/л). § Отриманий р-н центрифугували протягом 5 хв (3000 об. /хв. ) § Рочин відфільтрували через фільтр (розмір пор 0, 45 мм). § Відфільтрований розчин аналізували. * Даний розчин можна зберігати у темному місці при 22 С не більше 7 днів. Умови хроматографування: • Об’єм введеної проби 50 мл. • Рухома фаза - метанол-вода (96: 4). • Швидкість потоку 2 мл/хв. • Температура колонки 45 С. • Ідентифікація проводилась при довжині хвилі 292 нм.
Визначення вітаміну Е в рослинній олії за допомогою ВЕРХ з використанням УФ-детектора Пробопідготовка: § Розчинення досліджуваного зразку у гексані (1: 10). § До 20 мл отриманого р-ну + 60 мл СН 3 ОН + 20 мл внутрішнього стандарту (С= 30 мг/л). § Отриманий р-н центрифугували протягом 5 хв (3000 об. /хв. ) § Рочин відфільтрували через фільтр (розмір пор 0, 45 мм). § Відфільтрований розчин аналізували. * Даний розчин можна зберігати у темному місці при 22 С не більше 7 днів. Умови хроматографування: • Об’єм введеної проби 50 мл. • Рухома фаза - метанол-вода (96: 4). • Швидкість потоку 2 мл/хв. • Температура колонки 45 С. • Ідентифікація проводилась при довжині хвилі 292 нм.
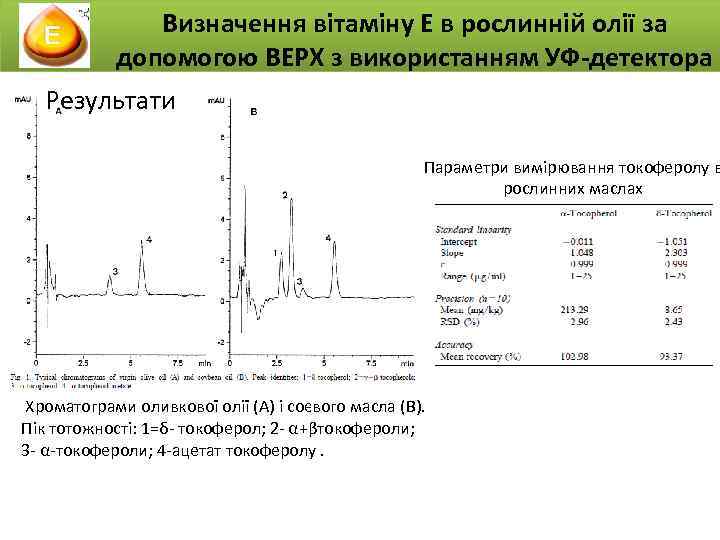 Визначення вітаміну Е в рослинній олії за допомогою ВЕРХ з використанням УФ-детектора Результати Параметри вимірювання токоферолу в рослинних маслах Хроматограми оливкової олії (A) і соєвого масла (B). Пік тотожності: 1=δ- токоферол; 2 - α+βтокофероли; 3 - α-токофероли; 4 -ацетат токоферолу.
Визначення вітаміну Е в рослинній олії за допомогою ВЕРХ з використанням УФ-детектора Результати Параметри вимірювання токоферолу в рослинних маслах Хроматограми оливкової олії (A) і соєвого масла (B). Пік тотожності: 1=δ- токоферол; 2 - α+βтокофероли; 3 - α-токофероли; 4 -ацетат токоферолу.
 Визначення вітаміну Е в рослинній сировиніза допомогою ВЕРХ з використанням МАС-детектора Під час аналізу на вміст вітаміну Е, робочі розчини повинні бути захищені від світла і кисню для того, щоб кількісно його ідентифікувати. Його можна безпосередньо проаналізувати в олії після розведення зразків з гексаном, або провести гаряче омилення, умови якого повинні бути ретельно збалансовані для уникнення втрат. Пробопідготовка: Пробопідготовка 1. Наважку ківі (2 г ) + 3 г бутилгідрокситолуол + 1 г Na 2 SO 4 → розчинили у гексані. 2. Отриманий розчин відцентрифугували, обережно декантували та пропустили крізь фільтр.
Визначення вітаміну Е в рослинній сировиніза допомогою ВЕРХ з використанням МАС-детектора Під час аналізу на вміст вітаміну Е, робочі розчини повинні бути захищені від світла і кисню для того, щоб кількісно його ідентифікувати. Його можна безпосередньо проаналізувати в олії після розведення зразків з гексаном, або провести гаряче омилення, умови якого повинні бути ретельно збалансовані для уникнення втрат. Пробопідготовка: Пробопідготовка 1. Наважку ківі (2 г ) + 3 г бутилгідрокситолуол + 1 г Na 2 SO 4 → розчинили у гексані. 2. Отриманий розчин відцентрифугували, обережно декантували та пропустили крізь фільтр.
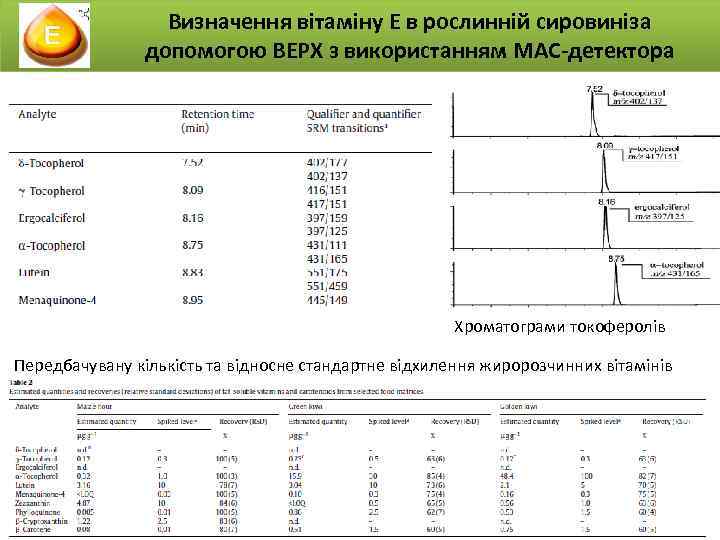 Визначення вітаміну Е в рослинній сировиніза допомогою ВЕРХ з використанням МАС-детектора Хроматограми токоферолів Передбачувану кількість та відносне стандартне відхилення жиророзчинних вітамінів
Визначення вітаміну Е в рослинній сировиніза допомогою ВЕРХ з використанням МАС-детектора Хроматограми токоферолів Передбачувану кількість та відносне стандартне відхилення жиророзчинних вітамінів
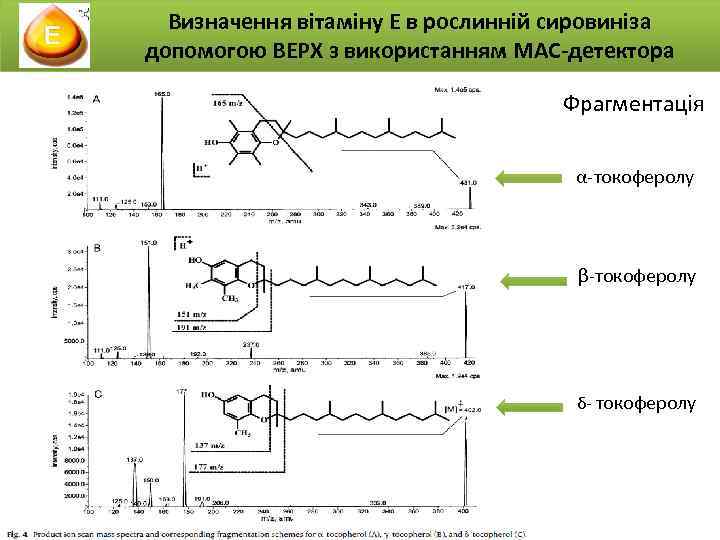 Визначення вітаміну Е в рослинній сировиніза допомогою ВЕРХ з використанням МАС-детектора Фрагментація α-токоферолу β-токоферолу δ- токоферолу
Визначення вітаміну Е в рослинній сировиніза допомогою ВЕРХ з використанням МАС-детектора Фрагментація α-токоферолу β-токоферолу δ- токоферолу
 Список використаної літератури 1. ГОСТ Р 54634— 2011 Продукты пищевые функциональные. Методы определение витамина Е. 2. E. Gimeno, A. I. Castellote, R. M. Lamuela-Ravento´s, M. C. de la Torre, M. C. Lo´pez-Sabater// Rapid determination of vitamin E in vegetable oils by reversedphase high-performance liquid chromatography// Journal of Chromatography A, 881 (2000) 251– 254. 3. В. И. Аньшаков, И. С. Алпеева, Г. Д. Брыкина, Е. Лазарева// ОПРЕДЕЛЕНИЕ ВИТАМИНА Е МЕТОДОМ ВЫСОКОЭФФЕКТИВНОЙ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ С КОСВЕННЫМ СПЕКТРОФОТОМЕТРИЧЕСКИМ ДЕТЕКТИРОВАНИЕМ, ВЕСТН. МОСК. УН-ТА. СЕР. 2. ХИМИЯ. 2000. Т. 41. № 4. 4. A. K. Hewavitharanaa, ∗, M. C. Lanaria, C. Becub// Simultaneous determination of Vitamin E homologs in chicken meat by liquid chromatography with fluorescence detection, Journal of Chromatography A, 1025 (2004) 313– 317. 5. Anna Rizzolo, Stefano Polesello// Chromatographic determination of vitamins in foods, Journal of Chromatography A, Volume 624, Issues 1– 2, 30 October 1992, Pages 103– 152. 6. http: //kust-blog. info/? p=464 7. http: //ru. wikipedia. org/wiki/%D 0%92%D 0%B 8%D 1%82%D 0%B 0%D 0%BC%D 0%B 8%D 0%BD_E. 8. Alessandra Gentili ∗, Fulvia Caretti// Evaluation of a method based on liquid chromatography–diode arraydetector–tandem mass spectrometry for a rapid and comprehensive characterization of the fatsoluble vitamin and carotenoid profile of selected plant foods, Journal of Chromatography A, 1218 (2011) 684– 697
Список використаної літератури 1. ГОСТ Р 54634— 2011 Продукты пищевые функциональные. Методы определение витамина Е. 2. E. Gimeno, A. I. Castellote, R. M. Lamuela-Ravento´s, M. C. de la Torre, M. C. Lo´pez-Sabater// Rapid determination of vitamin E in vegetable oils by reversedphase high-performance liquid chromatography// Journal of Chromatography A, 881 (2000) 251– 254. 3. В. И. Аньшаков, И. С. Алпеева, Г. Д. Брыкина, Е. Лазарева// ОПРЕДЕЛЕНИЕ ВИТАМИНА Е МЕТОДОМ ВЫСОКОЭФФЕКТИВНОЙ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ С КОСВЕННЫМ СПЕКТРОФОТОМЕТРИЧЕСКИМ ДЕТЕКТИРОВАНИЕМ, ВЕСТН. МОСК. УН-ТА. СЕР. 2. ХИМИЯ. 2000. Т. 41. № 4. 4. A. K. Hewavitharanaa, ∗, M. C. Lanaria, C. Becub// Simultaneous determination of Vitamin E homologs in chicken meat by liquid chromatography with fluorescence detection, Journal of Chromatography A, 1025 (2004) 313– 317. 5. Anna Rizzolo, Stefano Polesello// Chromatographic determination of vitamins in foods, Journal of Chromatography A, Volume 624, Issues 1– 2, 30 October 1992, Pages 103– 152. 6. http: //kust-blog. info/? p=464 7. http: //ru. wikipedia. org/wiki/%D 0%92%D 0%B 8%D 1%82%D 0%B 0%D 0%BC%D 0%B 8%D 0%BD_E. 8. Alessandra Gentili ∗, Fulvia Caretti// Evaluation of a method based on liquid chromatography–diode arraydetector–tandem mass spectrometry for a rapid and comprehensive characterization of the fatsoluble vitamin and carotenoid profile of selected plant foods, Journal of Chromatography A, 1218 (2011) 684– 697
 Дякую за увагу
Дякую за увагу


