кинетика первый порядок.ppt
- Количество слайдов: 23
 КАЗАНСКИЙ (ПРИВОЛЖСКИЙ) ФЕДЕРАЛЬНЫЙ УНИВЕРСИТЕТ Энергетический механизм ферментативных и неферментативных реакций. Реакции нулевого, первого, второго, третьего порядка Романова Нина LOGO Казань, 2013 Галиева Адиля Галиева Айсылу Кашинская Дания Маятина Ольга
КАЗАНСКИЙ (ПРИВОЛЖСКИЙ) ФЕДЕРАЛЬНЫЙ УНИВЕРСИТЕТ Энергетический механизм ферментативных и неферментативных реакций. Реакции нулевого, первого, второго, третьего порядка Романова Нина LOGO Казань, 2013 Галиева Адиля Галиева Айсылу Кашинская Дания Маятина Ольга
 ПЛАН v Энергетический механизм ферментативных и неферментативных реакций v Порядок реакции v Реакция нулевого порядка v Реакция первого порядка v Реакция второго порядка v Реакция третьего порядка 2
ПЛАН v Энергетический механизм ферментативных и неферментативных реакций v Порядок реакции v Реакция нулевого порядка v Реакция первого порядка v Реакция второго порядка v Реакция третьего порядка 2
 Энергетический механизм ферментативных и неферментативных реакций v. Н 2 СО 3 → Н 2 О + СО 2 Угольная кислота слабая; реакция её разложения пойдёт при обычных условиях, если молекулы угольной кислоты имеют энергию, превышающую определённый уровень, называемый энергией активации Еа Е а Н 2 СО 3 Чем больше молекул обладает энергией, превышающей уровень Еа , тем выше скорость химической реакции. Повысить скорость химической реакции можно нагреванием. При этом увеличивается энергия реагирующих молекул. 3
Энергетический механизм ферментативных и неферментативных реакций v. Н 2 СО 3 → Н 2 О + СО 2 Угольная кислота слабая; реакция её разложения пойдёт при обычных условиях, если молекулы угольной кислоты имеют энергию, превышающую определённый уровень, называемый энергией активации Еа Е а Н 2 СО 3 Чем больше молекул обладает энергией, превышающей уровень Еа , тем выше скорость химической реакции. Повысить скорость химической реакции можно нагреванием. При этом увеличивается энергия реагирующих молекул. 3
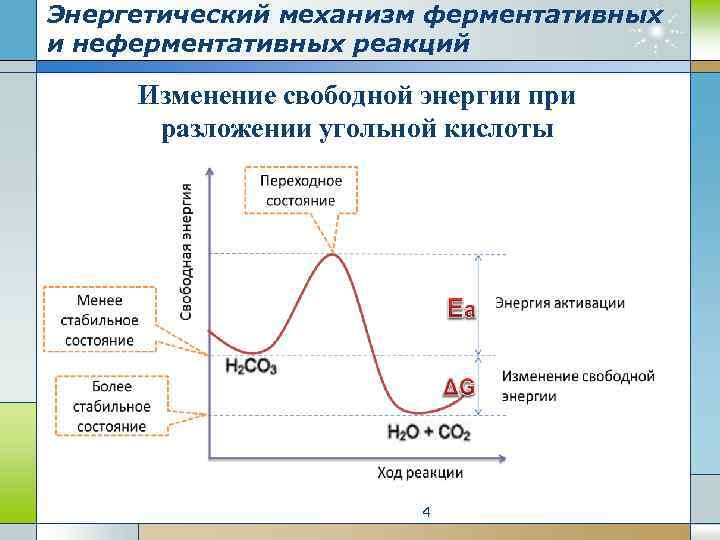 Энергетический механизм ферментативных и неферментативных реакций Изменение свободной энергии при разложении угольной кислоты 4
Энергетический механизм ферментативных и неферментативных реакций Изменение свободной энергии при разложении угольной кислоты 4
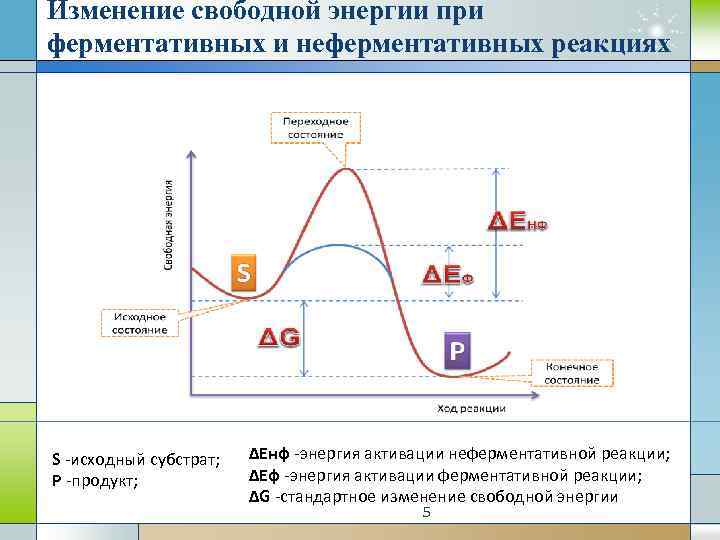 Изменение свободной энергии при ферментативных и неферментативных реакциях S -исходный субстрат; Р -продукт; ΔЕнф -энергия активации неферментативной реакции; ΔЕф -энергия активации ферментативной реакции; ΔG -стандартное изменение свободной энергии 5
Изменение свободной энергии при ферментативных и неферментативных реакциях S -исходный субстрат; Р -продукт; ΔЕнф -энергия активации неферментативной реакции; ΔЕф -энергия активации ферментативной реакции; ΔG -стандартное изменение свободной энергии 5
 Представим ситуацию из м/ф Шрек * Что бы было, если бы Шрек пошел спасать Фиону без осла (фермента): Шрек подходит к башне, а там дракон, они борется с драконихой и у него на это уходит ооочень много энергии * Что бы было, если бы Шрек пошел спасать Фиону с ослом (с ферментом): Шрек с ослом подходят к башне, навстречу им – дракониха, осел завораживает ее, она, ослепленная любовью, забывает про Шрека и не трогает его, Шрек тратит на спасение Фионы очень небольшое количество энергии. 6
Представим ситуацию из м/ф Шрек * Что бы было, если бы Шрек пошел спасать Фиону без осла (фермента): Шрек подходит к башне, а там дракон, они борется с драконихой и у него на это уходит ооочень много энергии * Что бы было, если бы Шрек пошел спасать Фиону с ослом (с ферментом): Шрек с ослом подходят к башне, навстречу им – дракониха, осел завораживает ее, она, ослепленная любовью, забывает про Шрека и не трогает его, Шрек тратит на спасение Фионы очень небольшое количество энергии. 6
 ! Ферменты, с термодинамической точки зрения, ускоряют химические реакции за счет снижения энергии активации путем увеличения числа активированных молекул, которые становятся реакционноспособными на более низком энергетическом уровне 7
! Ферменты, с термодинамической точки зрения, ускоряют химические реакции за счет снижения энергии активации путем увеличения числа активированных молекул, которые становятся реакционноспособными на более низком энергетическом уровне 7
 Порядок реакции v Порядок реакции – это эмпирическая величина, равная сумме показателей степеней, с которыми концентрации реагентов входят в выражение для скорости реакции. Так, для реакции v a. A + b. B m. M + n. N v скорость уменьшения концентрации С реагента А можно представить в виде, где СА и СВ – концентрации исходных веществ А и В соответственно. Порядок реакции в этом случае равен а + b. Коэффициент пропорциональности k, входящий в уравнение, называется константой скорости. Он равен скорости реакции при единичной концентрации реагентов. 8
Порядок реакции v Порядок реакции – это эмпирическая величина, равная сумме показателей степеней, с которыми концентрации реагентов входят в выражение для скорости реакции. Так, для реакции v a. A + b. B m. M + n. N v скорость уменьшения концентрации С реагента А можно представить в виде, где СА и СВ – концентрации исходных веществ А и В соответственно. Порядок реакции в этом случае равен а + b. Коэффициент пропорциональности k, входящий в уравнение, называется константой скорости. Он равен скорости реакции при единичной концентрации реагентов. 8
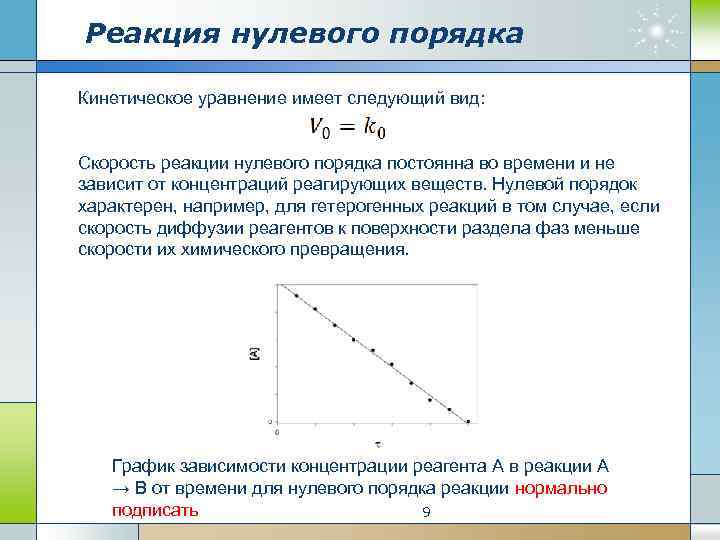 Реакция нулевого порядка Кинетическое уравнение имеет следующий вид: Скорость реакции нулевого порядка постоянна во времени и не зависит от концентраций реагирующих веществ. Нулевой порядок характерен, например, для гетерогенных реакций в том случае, если скорость диффузии реагентов к поверхности раздела фаз меньше скорости их химического превращения. График зависимости концентрации реагента A в реакции A → B от времени для нулевого порядка реакции нормально подписать 9
Реакция нулевого порядка Кинетическое уравнение имеет следующий вид: Скорость реакции нулевого порядка постоянна во времени и не зависит от концентраций реагирующих веществ. Нулевой порядок характерен, например, для гетерогенных реакций в том случае, если скорость диффузии реагентов к поверхности раздела фаз меньше скорости их химического превращения. График зависимости концентрации реагента A в реакции A → B от времени для нулевого порядка реакции нормально подписать 9
 Реакция нулевого порядка • –d. C/dt = k dx/dt = k x = kt + C Значению x = 0 соответствует t = 0, откуда константа С = 0 и x = kt В величину k могут входить различные константы, например интенсивность света, концентрация насыщенного раствора или пара. k –константа скорости реакции, размерность k – моль/(л*с). С – концентрация t- время 10
Реакция нулевого порядка • –d. C/dt = k dx/dt = k x = kt + C Значению x = 0 соответствует t = 0, откуда константа С = 0 и x = kt В величину k могут входить различные константы, например интенсивность света, концентрация насыщенного раствора или пара. k –константа скорости реакции, размерность k – моль/(л*с). С – концентрация t- время 10
 v Осел – с v Любовь фионы – скорость реакции v любовь не зависит от осла, она постоянна во времени v С ослом шрек или без осла, ей пофиг 11
v Осел – с v Любовь фионы – скорость реакции v любовь не зависит от осла, она постоянна во времени v С ослом шрек или без осла, ей пофиг 11
 Реакция первого порядка Если скорость реакции зависит от концентрации только одного реагента в первой степени, то выражение для скорости принимает вид: 12
Реакция первого порядка Если скорость реакции зависит от концентрации только одного реагента в первой степени, то выражение для скорости принимает вид: 12
 Реакция первого порядка Определение константы скорости k 1 = rt /Ct Тангенс угла наклона прямой, построенной по экспериментальным данным, будет равен k 1. 13
Реакция первого порядка Определение константы скорости k 1 = rt /Ct Тангенс угла наклона прямой, построенной по экспериментальным данным, будет равен k 1. 13
 Период полураспада . Время, за которое количество вещества уменьшается вдвое, не зависит от его количества в момент начала реакции и в любой данный момент реакции. 14
Период полураспада . Время, за которое количество вещества уменьшается вдвое, не зависит от его количества в момент начала реакции и в любой данный момент реакции. 14
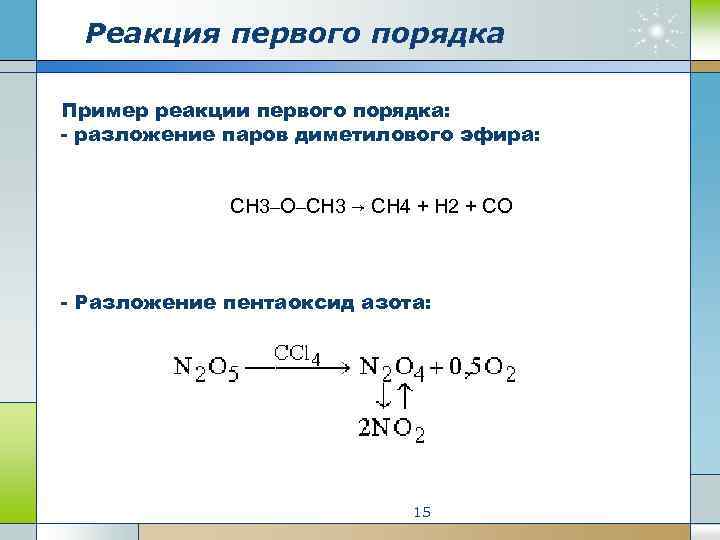 Реакция первого порядка Пример реакции первого порядка: - разложение паров диметилового эфира: СH 3–O–CH 3 → CH 4 + H 2 + CO - Разложение пентаоксид азота: 15
Реакция первого порядка Пример реакции первого порядка: - разложение паров диметилового эфира: СH 3–O–CH 3 → CH 4 + H 2 + CO - Разложение пентаоксид азота: 15
 Реакция второго порядка Реакции второго порядка. Когда скорость реакции пропорциональна квадрату концентрации отдельного реагента или концентрациям каждого из двух реагирующих веществ в первой степени, мы имеем дело с реакцией второго порядка. В дифференциальной форме выражения для скорости такой реакции имеют вид И Пусть a – начальная молярная концентрация реагента А, x – число его молей в 1 л, прореагировавшее за время t; тогда скорость реакции будет равна dx/dt = k(a – x)2 или dx/(a – x)2 = kdt Проинтегрировав, получим 1/(a – x) = kt + C Поскольку x = 0 при t = 0, константа С = 1/а. Отсюда И 16
Реакция второго порядка Реакции второго порядка. Когда скорость реакции пропорциональна квадрату концентрации отдельного реагента или концентрациям каждого из двух реагирующих веществ в первой степени, мы имеем дело с реакцией второго порядка. В дифференциальной форме выражения для скорости такой реакции имеют вид И Пусть a – начальная молярная концентрация реагента А, x – число его молей в 1 л, прореагировавшее за время t; тогда скорость реакции будет равна dx/dt = k(a – x)2 или dx/(a – x)2 = kdt Проинтегрировав, получим 1/(a – x) = kt + C Поскольку x = 0 при t = 0, константа С = 1/а. Отсюда И 16
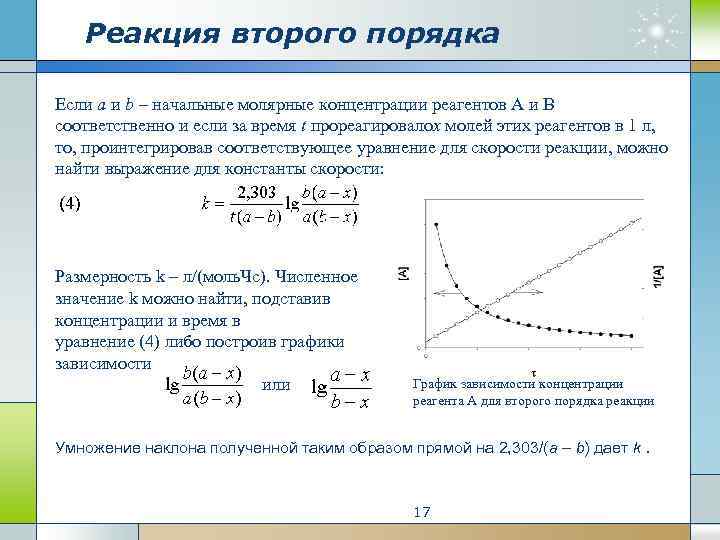 Реакция второго порядка Если а и b – начальные молярные концентрации реагентов А и В соответственно и если за время t прореагировалоx молей этих реагентов в 1 л, то, проинтегрировав соответствующее уравнение для скорости реакции, можно найти выражение для константы скорости: Размерность k – л/(моль. Чс). Численное значение k можно найти, подставив концентрации и время в уравнение (4) либо построив графики зависимости или График зависимости концентрации реагента A для второго порядка реакции Умножение наклона полученной таким образом прямой на 2, 303/(a – b) дает k. 17
Реакция второго порядка Если а и b – начальные молярные концентрации реагентов А и В соответственно и если за время t прореагировалоx молей этих реагентов в 1 л, то, проинтегрировав соответствующее уравнение для скорости реакции, можно найти выражение для константы скорости: Размерность k – л/(моль. Чс). Численное значение k можно найти, подставив концентрации и время в уравнение (4) либо построив графики зависимости или График зависимости концентрации реагента A для второго порядка реакции Умножение наклона полученной таким образом прямой на 2, 303/(a – b) дает k. 17
 Реакция третьего порядка Скорость реакции третьего порядка может зависеть от концентрации одного реагента в третьей степени, либо концентрации одного реагента во второй степени и второго реагента в первой степени, либо от концентрации каждого из трех реагентов в первой степени. Так, или dx/dt = k(a – x)3 Разделение переменных и интегрирование дают Или Здесь размерность k – л 2/(моль2 Чс). 18
Реакция третьего порядка Скорость реакции третьего порядка может зависеть от концентрации одного реагента в третьей степени, либо концентрации одного реагента во второй степени и второго реагента в первой степени, либо от концентрации каждого из трех реагентов в первой степени. Так, или dx/dt = k(a – x)3 Разделение переменных и интегрирование дают Или Здесь размерность k – л 2/(моль2 Чс). 18
 выводы v Бойцовский клуб v Первое правило Бойцовского клуба: не упоминать о Бойцовском клубе. v Второе правило Бойцовского клуба: не упоминать нигде о Бойцовском клубе. v Третье правило Бойцовского клуба: боец крикнул «стоп» , выдохся, отключился — бой окончен. v Четвертое: в бою участвуют лишь двое. v Пятое: бои идут один за другим. v Шестое: снимать обувь и рубашки. v Седьмое: бой продолжается столько, сколько нужно. v Восьмое и последнее: тот, кто впервые пришёл в клуб — примет бой. 19
выводы v Бойцовский клуб v Первое правило Бойцовского клуба: не упоминать о Бойцовском клубе. v Второе правило Бойцовского клуба: не упоминать нигде о Бойцовском клубе. v Третье правило Бойцовского клуба: боец крикнул «стоп» , выдохся, отключился — бой окончен. v Четвертое: в бою участвуют лишь двое. v Пятое: бои идут один за другим. v Шестое: снимать обувь и рубашки. v Седьмое: бой продолжается столько, сколько нужно. v Восьмое и последнее: тот, кто впервые пришёл в клуб — примет бой. 19
 Задание 20
Задание 20
 Глоссарий • • • Энергией активации называют дополнительное количество кинетической энергии, необходимое молекулам вещества, чтобы они вступили в реакцию. Свободной энергии реакции ΔG - разница энергии между исходным реагентом и конечными соединениями. Кинетическое уравнение – выражает зависимость скорости химической реакции от концентраций компонентов реакционной смеси. Частный порядок реакции - показатель степени при концентрации каждого из реагирующих веществ в кинетическом уравнении химической реакции. Общий порядок реакции - сумма показателей степени в кинетическом уравнении химической реакции (x + y + z). Гетерогенные реакции - химические реакции с участием веществ, находящихся в различных фазах и составляющих в совокупности гетерогенную систему. Период полупревращения – время, за которое концентрация исходного вещества уменьшается вдвое по сравнению с исходной. 21
Глоссарий • • • Энергией активации называют дополнительное количество кинетической энергии, необходимое молекулам вещества, чтобы они вступили в реакцию. Свободной энергии реакции ΔG - разница энергии между исходным реагентом и конечными соединениями. Кинетическое уравнение – выражает зависимость скорости химической реакции от концентраций компонентов реакционной смеси. Частный порядок реакции - показатель степени при концентрации каждого из реагирующих веществ в кинетическом уравнении химической реакции. Общий порядок реакции - сумма показателей степени в кинетическом уравнении химической реакции (x + y + z). Гетерогенные реакции - химические реакции с участием веществ, находящихся в различных фазах и составляющих в совокупности гетерогенную систему. Период полупревращения – время, за которое концентрация исходного вещества уменьшается вдвое по сравнению с исходной. 21
 Ссылки v http: //www. distedu. ru/edu 3/map. php v http: //www. bigpi. biysk. ru/encicl/articles/43/1004364 F. htm v http: //ru. wikipedia. org/wiki/%D 0%A 5%D 0%B 8%D 0%BC%D 0%B 8%D 1%87%D 0 %B 5%D 1%81%D 0%BA%D 0%B 0%D 1%8 F_%D 0%BA%D 0%B 8%D 0%BD%D 0%B 5 %D 1%82%D 0%B 8%D 0%BA%D 0%B 0#. D 0. A 0. D 0. B 5. D 0. B 0. D 0. BA. D 1. 86. D 0. B 8. D 1. 8 F_. D 0. BD. D 1. 83. D 0. BB. D 0. B 5. D 0. B 2. D 0. BE. D 0. B 3. D 0. BE_. D 0. BF. D 0. BE. D 1. 8 0. D 1. 8 F. D 0. B 4. D 0. BA. D 0. B 0 v http: //www. physchem. chimfak. rsu. ru/Source/PCC/Kinetics_2. htm v http: //chemistry. ru/course/content/chapter 5/section/paragraph 3/theory. html v http: //www. biochemistry. ru/biohimija_severina/B 5873 Part 16 -92. html v http: //www. ngpedia. ru/id 154182 p 3. html 22
Ссылки v http: //www. distedu. ru/edu 3/map. php v http: //www. bigpi. biysk. ru/encicl/articles/43/1004364 F. htm v http: //ru. wikipedia. org/wiki/%D 0%A 5%D 0%B 8%D 0%BC%D 0%B 8%D 1%87%D 0 %B 5%D 1%81%D 0%BA%D 0%B 0%D 1%8 F_%D 0%BA%D 0%B 8%D 0%BD%D 0%B 5 %D 1%82%D 0%B 8%D 0%BA%D 0%B 0#. D 0. A 0. D 0. B 5. D 0. B 0. D 0. BA. D 1. 86. D 0. B 8. D 1. 8 F_. D 0. BD. D 1. 83. D 0. BB. D 0. B 5. D 0. B 2. D 0. BE. D 0. B 3. D 0. BE_. D 0. BF. D 0. BE. D 1. 8 0. D 1. 8 F. D 0. B 4. D 0. BA. D 0. B 0 v http: //www. physchem. chimfak. rsu. ru/Source/PCC/Kinetics_2. htm v http: //chemistry. ru/course/content/chapter 5/section/paragraph 3/theory. html v http: //www. biochemistry. ru/biohimija_severina/B 5873 Part 16 -92. html v http: //www. ngpedia. ru/id 154182 p 3. html 22
 LOGO
LOGO


