Баранский М.В. 4301-51.pptx
- Количество слайдов: 12
 Казанский Национальный Исследовательский Технологический Университет СРС ПО ДИСЦИПЛИНЕ «РЕАКЦИОННАЯ СПОСОБНОСТЬ ХИМИЧЕСКИХ СОЕДИНЕНИЙ» НА ТЕМУ: «ОПРЕДЕЛЕНИЕ РЕАКЦИОННОЙ СПОСОБНОСТИ, ЕЕ КОЛИЧЕСТВЕННАЯ ОЦЕНКА, РЕАКЦИОННЫЕ СЕРИИ, ТИПИЧНЫЕ РЕАКЦИОННЫЕ СЕРИИ, КВАНТОВО-МЕХАНИЧЕСКАЯ ТЕОРИЯ РЕАКЦИОННОЙ СПОСОБНОСТИ, ВЛИЯНИЕ СРЕДЫ НА РЕАКЦИОННУЮ СПОСОБНОСТЬ. » Казань 2012 г. Выполнил: студент гр. 4301 -51 Баранский М. В. Проверила: Исхакова И. О
Казанский Национальный Исследовательский Технологический Университет СРС ПО ДИСЦИПЛИНЕ «РЕАКЦИОННАЯ СПОСОБНОСТЬ ХИМИЧЕСКИХ СОЕДИНЕНИЙ» НА ТЕМУ: «ОПРЕДЕЛЕНИЕ РЕАКЦИОННОЙ СПОСОБНОСТИ, ЕЕ КОЛИЧЕСТВЕННАЯ ОЦЕНКА, РЕАКЦИОННЫЕ СЕРИИ, ТИПИЧНЫЕ РЕАКЦИОННЫЕ СЕРИИ, КВАНТОВО-МЕХАНИЧЕСКАЯ ТЕОРИЯ РЕАКЦИОННОЙ СПОСОБНОСТИ, ВЛИЯНИЕ СРЕДЫ НА РЕАКЦИОННУЮ СПОСОБНОСТЬ. » Казань 2012 г. Выполнил: студент гр. 4301 -51 Баранский М. В. Проверила: Исхакова И. О
 Введение: Реакционная способность - характеристика химической активности веществ, учитывающая как разнообразие реакций, возможных для данного вещества, так и их скорость. Например, благородные металлы (Au, Pt) и инертные газы (Не, Ar, Kr, Xe) химически инертны, то есть у них низкая реакционная способность; щелочные металлы (Li, Na, К, Cs) и галогены (F, Cl, Вг, I) химически активны, то есть обладают высокой реакционной способностью. В органической химии насыщение углеводороды характеризуются низкой Р. с. , для них возможны немногочисленные реакции (радикальное галогенирование и нитрование, дегидрирование, деструкция с разрывом С —С-связей и некоторые др. ), происходящие в жёстких условиях (высокая температура, ультрафиолетовое облучение). Для галогенопроизводных насыщенных углеводородов уже возможны, кроме того, реакции дегидрогалогенирования, нуклеофильного замещения галогена, образования магнийорганических соединений и др. , происходящие в мягких условиях. Наличие в молекуле двойных и тройных связей, функциональных групп (гидроксильной —ОН, карбоксильной —СООН, аминогруппы — NH 2 и др. ) приводит к дальнейшему увеличению Р. с. Количественно Р. с. выражают константами скоростей реакций или константами равновесия в случае обратимых процессов.
Введение: Реакционная способность - характеристика химической активности веществ, учитывающая как разнообразие реакций, возможных для данного вещества, так и их скорость. Например, благородные металлы (Au, Pt) и инертные газы (Не, Ar, Kr, Xe) химически инертны, то есть у них низкая реакционная способность; щелочные металлы (Li, Na, К, Cs) и галогены (F, Cl, Вг, I) химически активны, то есть обладают высокой реакционной способностью. В органической химии насыщение углеводороды характеризуются низкой Р. с. , для них возможны немногочисленные реакции (радикальное галогенирование и нитрование, дегидрирование, деструкция с разрывом С —С-связей и некоторые др. ), происходящие в жёстких условиях (высокая температура, ультрафиолетовое облучение). Для галогенопроизводных насыщенных углеводородов уже возможны, кроме того, реакции дегидрогалогенирования, нуклеофильного замещения галогена, образования магнийорганических соединений и др. , происходящие в мягких условиях. Наличие в молекуле двойных и тройных связей, функциональных групп (гидроксильной —ОН, карбоксильной —СООН, аминогруппы — NH 2 и др. ) приводит к дальнейшему увеличению Р. с. Количественно Р. с. выражают константами скоростей реакций или константами равновесия в случае обратимых процессов.
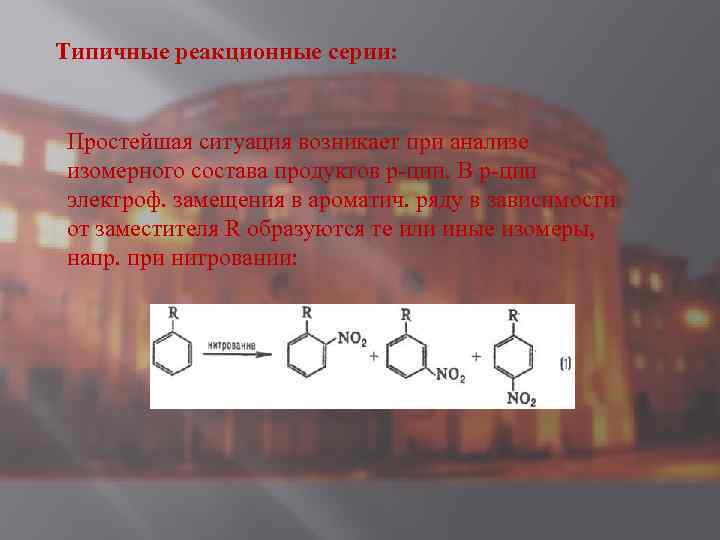 Типичные реакционные серии: Простейшая ситуация возникает при анализе изомерного состава продуктов р-ции. В р-ции электроф. замещения в ароматич. ряду в зависимости от заместителя R образуются те или иные изомеры, напр. при нитровании:
Типичные реакционные серии: Простейшая ситуация возникает при анализе изомерного состава продуктов р-ции. В р-ции электроф. замещения в ароматич. ряду в зависимости от заместителя R образуются те или иные изомеры, напр. при нитровании:
![Электронодонорные заместители [R=СН 3, ОСН 3, N(CH 3)2] стимулируют образование орто- и пара-продук-тов, а Электронодонорные заместители [R=СН 3, ОСН 3, N(CH 3)2] стимулируют образование орто- и пара-продук-тов, а](https://present5.com/presentation/19308556_136761433/image-4.jpg) Электронодонорные заместители [R=СН 3, ОСН 3, N(CH 3)2] стимулируют образование орто- и пара-продук-тов, а электроноакцепторные (R = СООН, SO 3 H, NO 2)-мета-продуктов, причем в первом случае р-ция идет легче, чем с незамещенным бензолом (R = Н), а во втором-труднее. Эти закономерности наз. правилами ориентации в ароматическом ряду. При нуклеоф. замещении правилами ориентации обращаются. Стереохим. направленность перипиклич. р-ций определяется Вудворда-Хофмаиа правилами, напр. :
Электронодонорные заместители [R=СН 3, ОСН 3, N(CH 3)2] стимулируют образование орто- и пара-продук-тов, а электроноакцепторные (R = СООН, SO 3 H, NO 2)-мета-продуктов, причем в первом случае р-ция идет легче, чем с незамещенным бензолом (R = Н), а во втором-труднее. Эти закономерности наз. правилами ориентации в ароматическом ряду. При нуклеоф. замещении правилами ориентации обращаются. Стереохим. направленность перипиклич. р-ций определяется Вудворда-Хофмаиа правилами, напр. :
 При дисротаторном пути р-ции заместители R и R' в продукте будут расположены по одну сторону плоскости цикла, при конротаторном пути-по разные стороны. Эксперимент показывает, что термич. циклизация производных бутадиена происходит по конротаторному пути, а фотохим. циклизация-по дисротаторному пути. В примерах (1) и (2) нет необходимости в количеств. кинетич. измерениях, реакционная способность определяется по относит. выходу изомеров. Пример широкой реакц. серии-рции радикального присоединения по двойной связи:
При дисротаторном пути р-ции заместители R и R' в продукте будут расположены по одну сторону плоскости цикла, при конротаторном пути-по разные стороны. Эксперимент показывает, что термич. циклизация производных бутадиена происходит по конротаторному пути, а фотохим. циклизация-по дисротаторному пути. В примерах (1) и (2) нет необходимости в количеств. кинетич. измерениях, реакционная способность определяется по относит. выходу изомеров. Пример широкой реакц. серии-рции радикального присоединения по двойной связи:
 Реакционная способность характеризуется отношением константы скорости k к константе скорости k 0 р-ции с этиленом (R, R' = Н) (см. табл. ). Аналогичные кинетич. измерения сделаны для р-ций присоединения метильного радикала к ароматич. молекулам и для р-ций присоединения др. радикалов.
Реакционная способность характеризуется отношением константы скорости k к константе скорости k 0 р-ции с этиленом (R, R' = Н) (см. табл. ). Аналогичные кинетич. измерения сделаны для р-ций присоединения метильного радикала к ароматич. молекулам и для р-ций присоединения др. радикалов.
 Квантовохимическая теория реакционной способности: Современная теоретическая химия позволяет непосредственно рассчитать абс. константы скорости только для несложных хим. систем. В теории реакционной способности качеств. закономерности м. б. выявлены для объектов любой сложности. При этом используют разл. подходы. При эмпирич. подходе классифицируют влияние заместителей по неск. типам (эффекты сопряжения, полярные, пространственные и др. ) и применяют корреляционные соотношения. Традиц. квантовохим. подход основан на активированного комплекса теории; при этом предполагается, что для всех р-ций, составляющих реакц. серию (без пространств. и соль-ватац. эффектов), остается примерно постоянным пред-экспоненц. множитель А в Аррениуса уравнении для константы скорости k = Aexp(-E. /RT) (R-газовая постоянная, Т-абс. т-ра). Поэтому характеристикой реакционной способности служит энергия активации рции E. , к-рая практически совпадает с высотой потенц. барьера на поверхности потенциальной энергии (ППЭ).
Квантовохимическая теория реакционной способности: Современная теоретическая химия позволяет непосредственно рассчитать абс. константы скорости только для несложных хим. систем. В теории реакционной способности качеств. закономерности м. б. выявлены для объектов любой сложности. При этом используют разл. подходы. При эмпирич. подходе классифицируют влияние заместителей по неск. типам (эффекты сопряжения, полярные, пространственные и др. ) и применяют корреляционные соотношения. Традиц. квантовохим. подход основан на активированного комплекса теории; при этом предполагается, что для всех р-ций, составляющих реакц. серию (без пространств. и соль-ватац. эффектов), остается примерно постоянным пред-экспоненц. множитель А в Аррениуса уравнении для константы скорости k = Aexp(-E. /RT) (R-газовая постоянная, Т-абс. т-ра). Поэтому характеристикой реакционной способности служит энергия активации рции E. , к-рая практически совпадает с высотой потенц. барьера на поверхности потенциальной энергии (ППЭ).
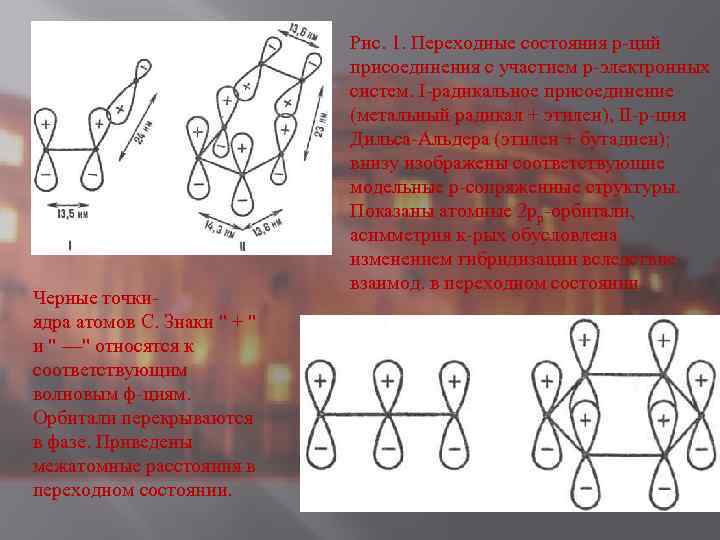 Черные точкиядра атомов С. Знаки " + " и " —" относятся к соответствующим волновым ф-циям. Орбитали перекрываются в фазе. Приведены межатомные расстояния в переходном состоянии. Рис. 1. Переходные состояния р-ций присоединения с участием p-электронных систем. I-радикальное присоединение (метальный радикал + этилен), II-р-ция Дильса-Альдера (этилен + бутадиен); внизу изображены соответствующие модельные p-сопряженные структуры. Показаны атомные 2 pp-орбитали, асимметрия к-рых обусловлена изменением гибридизации вследствие взаимод. в переходном состоянии.
Черные точкиядра атомов С. Знаки " + " и " —" относятся к соответствующим волновым ф-циям. Орбитали перекрываются в фазе. Приведены межатомные расстояния в переходном состоянии. Рис. 1. Переходные состояния р-ций присоединения с участием p-электронных систем. I-радикальное присоединение (метальный радикал + этилен), II-р-ция Дильса-Альдера (этилен + бутадиен); внизу изображены соответствующие модельные p-сопряженные структуры. Показаны атомные 2 pp-орбитали, асимметрия к-рых обусловлена изменением гибридизации вследствие взаимод. в переходном состоянии.
 Энергия стабилизации. Для относит. оценки E. в реакц. сериях важна концепция делокализации электронов в переходном состоянии (активир. комплексе) р-ции (М. Эванс, 1939). Согласно этой концепции, электронное строение мн. реакц. центров подобно строению сопряженных открытых и циклических я-электронных систем (рис. 1). Открытое переходное состояние радикальной р-ции типа (3) подобно p-электронной системе аллильного радикала (рис. 1, I), а "циклическое" переходное состояние согласованной р-ции Дильса-Альдера (этилен + бутадиен) по строению напоминает бензол (рис. 1, И). p-Электроны заместителей R и R' включаются в общую делокализованную систему электронов. Относит. мерой энергии активации р-ции, а следовательно и реакционной способности, может служить энергия стабилизации переходного состояния (энергия делокализации), т. е. разность между энергией сопряженной системы p-электронов переходного состояния и энергией p-электронов в изолир. реагентах. Энергию стабилизации можно рассчитать полуэмпирическими методами квантовой химии, напр. методом Хюккеля. Вычисляя энергию стабилизации, можно предсказывать реакционную способность хим. соединения во мн. р-циях (иллюстрации см. на рис. 2).
Энергия стабилизации. Для относит. оценки E. в реакц. сериях важна концепция делокализации электронов в переходном состоянии (активир. комплексе) р-ции (М. Эванс, 1939). Согласно этой концепции, электронное строение мн. реакц. центров подобно строению сопряженных открытых и циклических я-электронных систем (рис. 1). Открытое переходное состояние радикальной р-ции типа (3) подобно p-электронной системе аллильного радикала (рис. 1, I), а "циклическое" переходное состояние согласованной р-ции Дильса-Альдера (этилен + бутадиен) по строению напоминает бензол (рис. 1, И). p-Электроны заместителей R и R' включаются в общую делокализованную систему электронов. Относит. мерой энергии активации р-ции, а следовательно и реакционной способности, может служить энергия стабилизации переходного состояния (энергия делокализации), т. е. разность между энергией сопряженной системы p-электронов переходного состояния и энергией p-электронов в изолир. реагентах. Энергию стабилизации можно рассчитать полуэмпирическими методами квантовой химии, напр. методом Хюккеля. Вычисляя энергию стабилизации, можно предсказывать реакционную способность хим. соединения во мн. р-циях (иллюстрации см. на рис. 2).
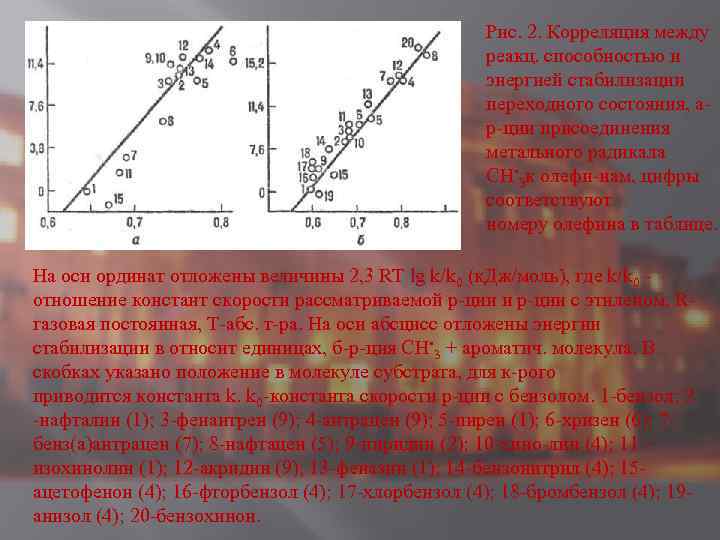 Рис. 2. Корреляция между реакц. способностью и энергией стабилизации переходного состояния, ар-ции присоединения метального радикала СН • 3 к олефи-нам, цифры соответствуют номеру олефина в таблице. На оси ординат отложены величины 2, 3 RТ lg k/k 0 (к. Дж/моль), где k/k 0 - отношение констант скорости рассматриваемой р-ции и р-ции с этиленом, Rгазовая постоянная, Т-абс. т-ра. На оси абсцисс отложены энергии стабилизации в относит единицах, б-р-ция СН • 3 + ароматич. молекула. В скобках указано положение в молекуле субстрата, для к-рого приводится константа k. k 0 -константа скорости р-ции с бензолом. 1 -бензол; 2 -нафталин (1); 3 -фенантрен (9); 4 -антрацен (9); 5 -пирен (1); 6 -хризен (6); 7 бенз(а)антрацен (7); 8 -нафтацен (5); 9 -пиридин (2); 10 -хино-лин (4); 11 изохинолин (1); 12 -акридин (9); 13 -феназин (1); 14 -бензонитрил (4); 15 ацетофенон (4); 16 -фторбензол (4); 17 -хлорбензол (4); 18 -бромбензол (4); 19 анизол (4); 20 -бензохинон.
Рис. 2. Корреляция между реакц. способностью и энергией стабилизации переходного состояния, ар-ции присоединения метального радикала СН • 3 к олефи-нам, цифры соответствуют номеру олефина в таблице. На оси ординат отложены величины 2, 3 RТ lg k/k 0 (к. Дж/моль), где k/k 0 - отношение констант скорости рассматриваемой р-ции и р-ции с этиленом, Rгазовая постоянная, Т-абс. т-ра. На оси абсцисс отложены энергии стабилизации в относит единицах, б-р-ция СН • 3 + ароматич. молекула. В скобках указано положение в молекуле субстрата, для к-рого приводится константа k. k 0 -константа скорости р-ции с бензолом. 1 -бензол; 2 -нафталин (1); 3 -фенантрен (9); 4 -антрацен (9); 5 -пирен (1); 6 -хризен (6); 7 бенз(а)антрацен (7); 8 -нафтацен (5); 9 -пиридин (2); 10 -хино-лин (4); 11 изохинолин (1); 12 -акридин (9); 13 -феназин (1); 14 -бензонитрил (4); 15 ацетофенон (4); 16 -фторбензол (4); 17 -хлорбензол (4); 18 -бромбензол (4); 19 анизол (4); 20 -бензохинон.
 Концепция граничных орбиталей. Оценки реакционной способности особенно просты, если использовать возмущений теорию. В распространенном варианте теории возмущений энергия стабилизации представляется в виде суммы вкладов от взаимод. между мол. орбиталями реагентов. Наиб. вклад в сумму дают, как правило, взаимод. граничных орбиталей, т. е. высших заполненных электронами и низших незаполненных орбиталей; согласно К. Фукуи (1952), существенны только эти вклады (см. Граничных орбиталей теория). Концепцию граничных орбиталей часто применяют в качестве основы для обсуждения реакционной способности. Альтернантные системы. Качеств. подход, не обязательно использующий теорию возмущений, сформулирован для класса сопряженных систем, наз. альтернант-ными. Они образованы из одинаковых атомов (обычно углерода) и не содержат нечетных циклов (см. Альтернантные углеводороды). Для таких систем в рамках Хюккеля метода можно без всяких вычислений выявить нек-рые общие закономерности. Так, введение полярного заместителя приводит к чередованию положит. и отрицат. изменений электронной плотности в сопряженной углеродной цепи относительно незамещенного углеводородного соед. (закон альтернирующей полярности, Ч. Коул-сон, Г. Лонге-Хиггинс, 1947). Этот вывод теории позволяет объяснить правила ориентации в ароматич. ряду (р-ция 1).
Концепция граничных орбиталей. Оценки реакционной способности особенно просты, если использовать возмущений теорию. В распространенном варианте теории возмущений энергия стабилизации представляется в виде суммы вкладов от взаимод. между мол. орбиталями реагентов. Наиб. вклад в сумму дают, как правило, взаимод. граничных орбиталей, т. е. высших заполненных электронами и низших незаполненных орбиталей; согласно К. Фукуи (1952), существенны только эти вклады (см. Граничных орбиталей теория). Концепцию граничных орбиталей часто применяют в качестве основы для обсуждения реакционной способности. Альтернантные системы. Качеств. подход, не обязательно использующий теорию возмущений, сформулирован для класса сопряженных систем, наз. альтернант-ными. Они образованы из одинаковых атомов (обычно углерода) и не содержат нечетных циклов (см. Альтернантные углеводороды). Для таких систем в рамках Хюккеля метода можно без всяких вычислений выявить нек-рые общие закономерности. Так, введение полярного заместителя приводит к чередованию положит. и отрицат. изменений электронной плотности в сопряженной углеродной цепи относительно незамещенного углеводородного соед. (закон альтернирующей полярности, Ч. Коул-сон, Г. Лонге-Хиггинс, 1947). Этот вывод теории позволяет объяснить правила ориентации в ароматич. ряду (р-ция 1).
 Спасибо за внимание!
Спасибо за внимание!


