Intro.ppt
- Количество слайдов: 35
 Катионная полимеризация – ионная полимеризация, при которой концевое звено растущей цепи несет полный или частичный положительный заряд (т. о. активными центрами реакции являются карбкатионы). Карбкатионы в органической химии R 3 C+ CH 5+
Катионная полимеризация – ионная полимеризация, при которой концевое звено растущей цепи несет полный или частичный положительный заряд (т. о. активными центрами реакции являются карбкатионы). Карбкатионы в органической химии R 3 C+ CH 5+
 Катионная полимеризация Z – электронодонорный заместитель, который стабилизирует образующийся карбокатион Карбокатионы – заряженные частицы, которые содержат атом углерода с вокантной орбиралью.
Катионная полимеризация Z – электронодонорный заместитель, который стабилизирует образующийся карбокатион Карбокатионы – заряженные частицы, которые содержат атом углерода с вокантной орбиралью.
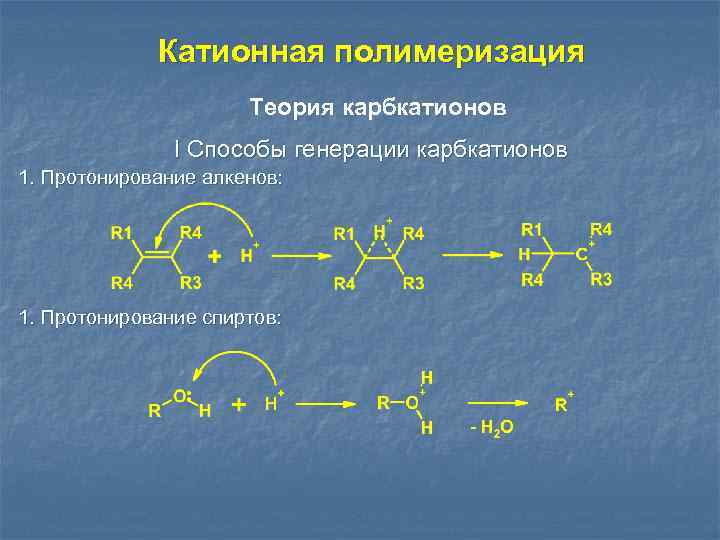 Катионная полимеризация Теория карбкатионов I Способы генерации карбкатионов 1. Протонирование алкенов: 1. Протонирование спиртов:
Катионная полимеризация Теория карбкатионов I Способы генерации карбкатионов 1. Протонирование алкенов: 1. Протонирование спиртов:
 Катионная полимеризация Теория карбкатионов I Способы генерации карбкатионов 3. Протонирование алканов суперкислотами: 4. Разложение солей диазония:
Катионная полимеризация Теория карбкатионов I Способы генерации карбкатионов 3. Протонирование алканов суперкислотами: 4. Разложение солей диазония:
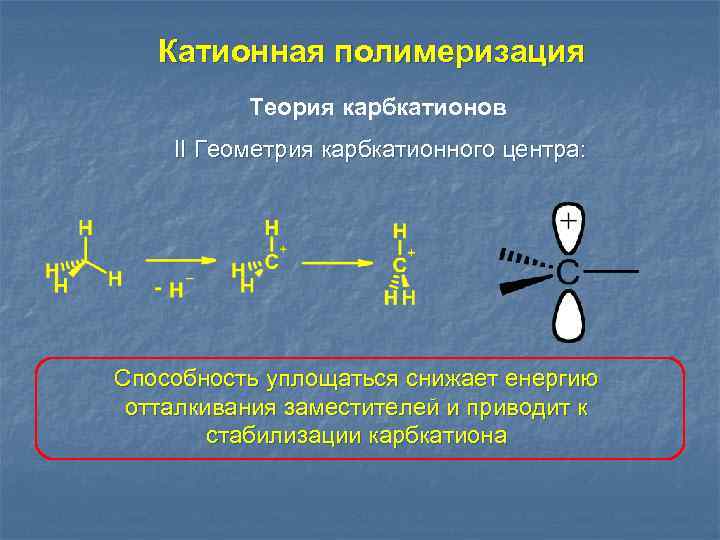 Катионная полимеризация Теория карбкатионов II Геометрия карбкатионного центра: Способность уплощаться снижает енергию отталкивания заместителей и приводит к стабилизации карбкатиона
Катионная полимеризация Теория карбкатионов II Геометрия карбкатионного центра: Способность уплощаться снижает енергию отталкивания заместителей и приводит к стабилизации карбкатиона
 Катионная полимеризация Теория карбокатионов III Факторы, стабилизирующие карбкатионный центр: Карбокатионный центр является электронодефицитным 1 Влияние индуктивного эффекта заместителей: Заместители с +I эффектом стабилизируют карбокатионный центр, с –I - дестабилизируют
Катионная полимеризация Теория карбокатионов III Факторы, стабилизирующие карбкатионный центр: Карбокатионный центр является электронодефицитным 1 Влияние индуктивного эффекта заместителей: Заместители с +I эффектом стабилизируют карбокатионный центр, с –I - дестабилизируют
 Катионная полимеризация Теория карбокатионов III Факторы, стабилизирующие карбокатионный центр: 2 Влияние мезомерного эффекта заместителей: Заместители с +М эффектом стабилизируют карбокатионный центр, с –М - дестабилизируют
Катионная полимеризация Теория карбокатионов III Факторы, стабилизирующие карбокатионный центр: 2 Влияние мезомерного эффекта заместителей: Заместители с +М эффектом стабилизируют карбокатионный центр, с –М - дестабилизируют
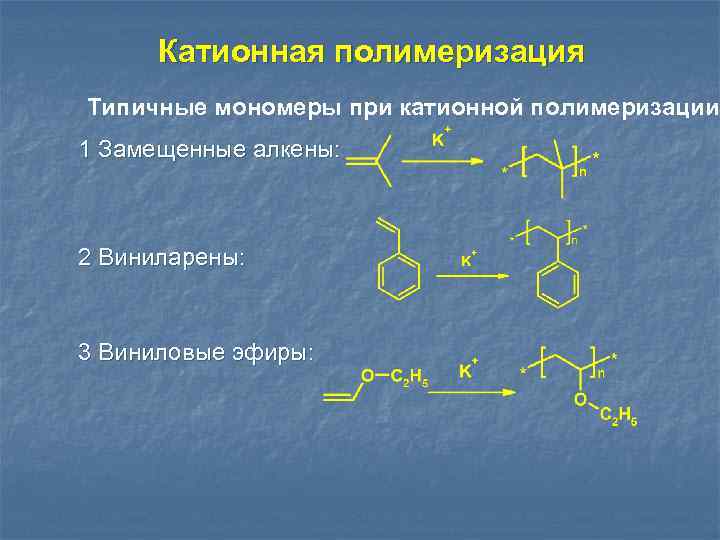 Катионная полимеризация Типичные мономеры при катионной полимеризации 1 Замещенные алкены: 2 Виниларены: 3 Виниловые эфиры:
Катионная полимеризация Типичные мономеры при катионной полимеризации 1 Замещенные алкены: 2 Виниларены: 3 Виниловые эфиры:
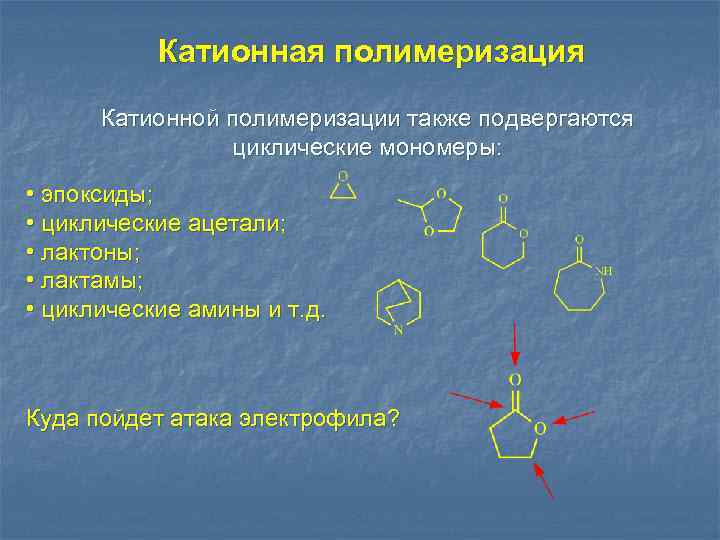 Катионная полимеризация Катионной полимеризации также подвергаются циклические мономеры: • эпоксиды; • циклические ацетали; • лактоны; • лактамы; • циклические амины и т. д. Куда пойдет атака электрофила?
Катионная полимеризация Катионной полимеризации также подвергаются циклические мономеры: • эпоксиды; • циклические ацетали; • лактоны; • лактамы; • циклические амины и т. д. Куда пойдет атака электрофила?
 Катионная полимеризация Чтобы определить место атаки катиона, необходимо сравнить стабильность образующихся продуктов. Это поможет определить строение получающегося полимера
Катионная полимеризация Чтобы определить место атаки катиона, необходимо сравнить стабильность образующихся продуктов. Это поможет определить строение получающегося полимера
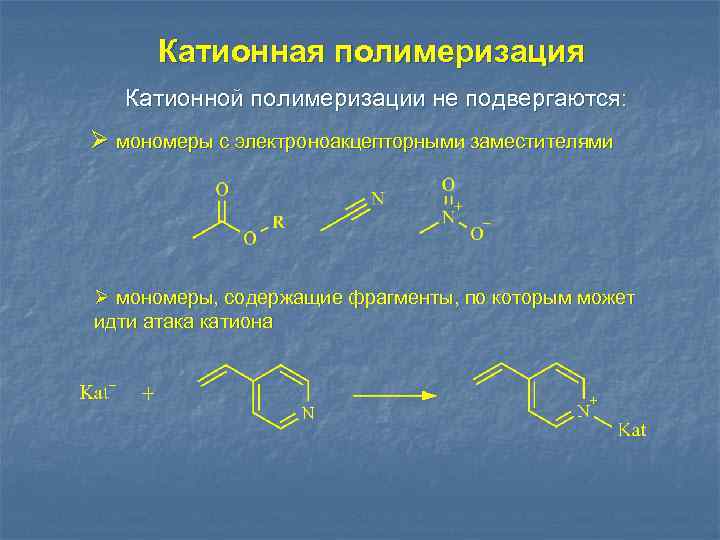 Катионная полимеризация Катионной полимеризации не подвергаются: Ø мономеры с электроноакцепторными заместителями Ø мономеры, содержащие фрагменты, по которым может идти атака катиона
Катионная полимеризация Катионной полимеризации не подвергаются: Ø мономеры с электроноакцепторными заместителями Ø мономеры, содержащие фрагменты, по которым может идти атака катиона
 Катионная полимеризация Инициаторы Ø кислоты Бренстеда H 2 SO 4, H 3 PO 4, CF 3 COOH, HCl. O 4 и др. Ø кислоты Льюиса BF 3 , Al. Cl 3 , Al. Br 3 , Sn. Cl 4 , Zn. Cl 2 и др. Ø галогены и интергалогениды I 2 , IBr , ICl и др. Ø оксониевые соли R 3 O + X -
Катионная полимеризация Инициаторы Ø кислоты Бренстеда H 2 SO 4, H 3 PO 4, CF 3 COOH, HCl. O 4 и др. Ø кислоты Льюиса BF 3 , Al. Cl 3 , Al. Br 3 , Sn. Cl 4 , Zn. Cl 2 и др. Ø галогены и интергалогениды I 2 , IBr , ICl и др. Ø оксониевые соли R 3 O + X -
 Катионная полимеризация Особенность инициирования I Протонные кислоты Критерием, по которому сравнивают влияние различных кислот на ход процесса, является эффективное отношение константы роста к константе обрыва Значения эффективного отношения константы роста к константе обрыва для различных кислот Кислота HBr HSO 3 F H 2 SO 4 HCl. O 4 kp/ko 30 500 800 20000
Катионная полимеризация Особенность инициирования I Протонные кислоты Критерием, по которому сравнивают влияние различных кислот на ход процесса, является эффективное отношение константы роста к константе обрыва Значения эффективного отношения константы роста к константе обрыва для различных кислот Кислота HBr HSO 3 F H 2 SO 4 HCl. O 4 kp/ko 30 500 800 20000
 Катионная полимеризация Особенность инициирования I Протонные кислоты
Катионная полимеризация Особенность инициирования I Протонные кислоты
 Катионная полимеризация Особенность инициирования I Протонные кислоты Ø С увеличением силы кислоты или с уменьшением нуклеофильности аниона вероятность обрыва цепи значительно снижается Ø Проведение катионной полимеризации в растворителях, которые хорошо сольватируют анионы, уменьшает вероятность обрыва цепи
Катионная полимеризация Особенность инициирования I Протонные кислоты Ø С увеличением силы кислоты или с уменьшением нуклеофильности аниона вероятность обрыва цепи значительно снижается Ø Проведение катионной полимеризации в растворителях, которые хорошо сольватируют анионы, уменьшает вероятность обрыва цепи
 Катионная полимеризация Особенность инициирования II Кислоты Льюиса (Al. Cl 3, BF 3, Sn. Cl 4, Ti. Cl 4 и др. ) становятся каталитически активными в присутствии протонодонорных соединений, галогеналканов или этеров, называемых сокатализаторами. Каталитические комплексы, непосредственно инициирующие полимеризацию, образуются при взаимодействии кислот Льюиса с сокатализаторами. v = k [M] [I]
Катионная полимеризация Особенность инициирования II Кислоты Льюиса (Al. Cl 3, BF 3, Sn. Cl 4, Ti. Cl 4 и др. ) становятся каталитически активными в присутствии протонодонорных соединений, галогеналканов или этеров, называемых сокатализаторами. Каталитические комплексы, непосредственно инициирующие полимеризацию, образуются при взаимодействии кислот Льюиса с сокатализаторами. v = k [M] [I]
 Катионная полимеризация Особенность инициирования II Кислоты Льюиса Особенности полимеризации в присутствии Al. Br 3 и Al. I 3 Возможна активация полимеризации без сокатализаторов v = k [M] [I]2
Катионная полимеризация Особенность инициирования II Кислоты Льюиса Особенности полимеризации в присутствии Al. Br 3 и Al. I 3 Возможна активация полимеризации без сокатализаторов v = k [M] [I]2
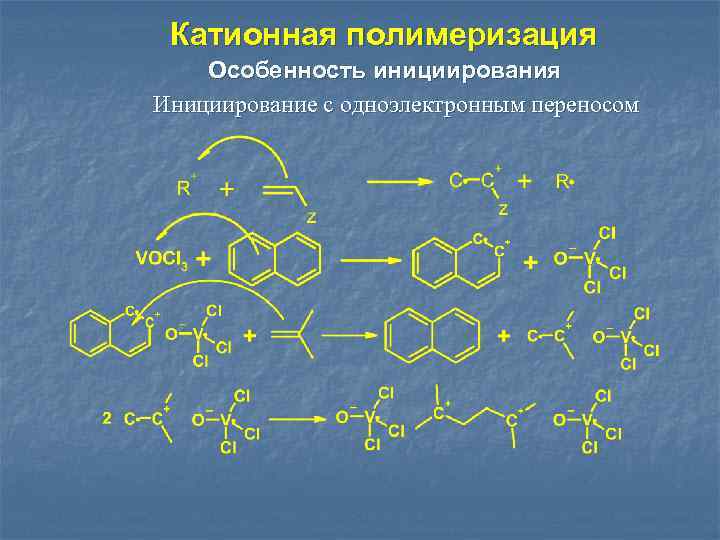 Катионная полимеризация Особенность инициирования Инициирование с одноэлектронным переносом
Катионная полимеризация Особенность инициирования Инициирование с одноэлектронным переносом
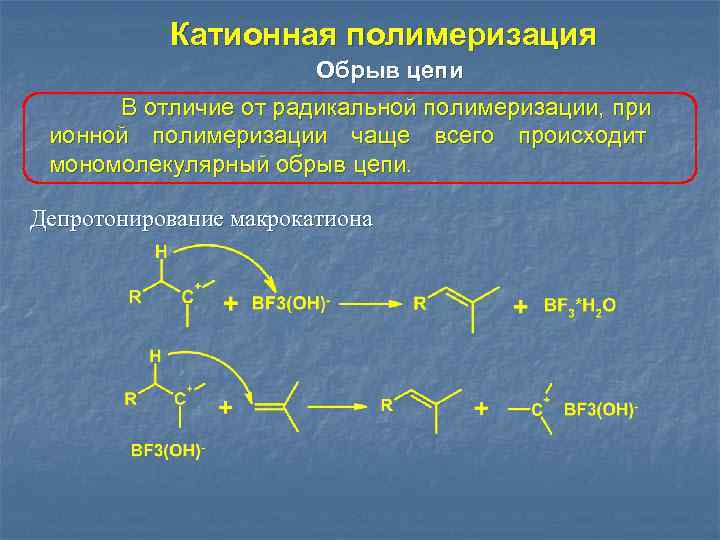 Катионная полимеризация Обрыв цепи В отличие от радикальной полимеризации, при ионной полимеризации чаще всего происходит мономолекулярный обрыв цепи. Депротонирование макрокатиона
Катионная полимеризация Обрыв цепи В отличие от радикальной полимеризации, при ионной полимеризации чаще всего происходит мономолекулярный обрыв цепи. Депротонирование макрокатиона
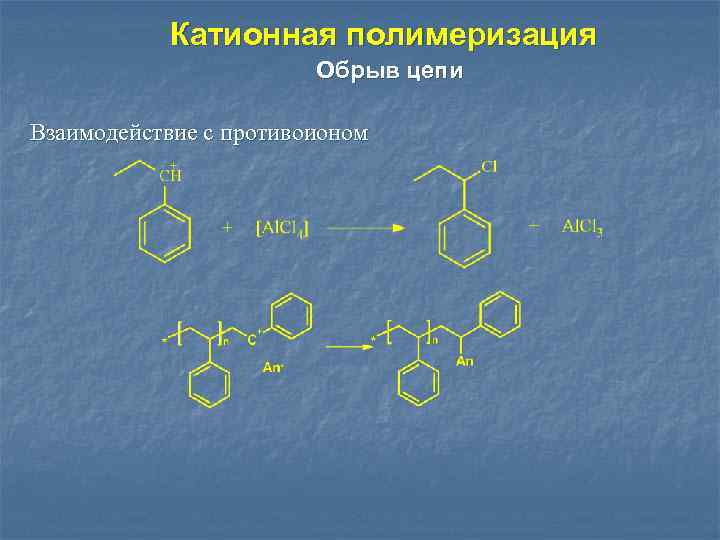 Катионная полимеризация Обрыв цепи Взаимодействие с противоионом
Катионная полимеризация Обрыв цепи Взаимодействие с противоионом
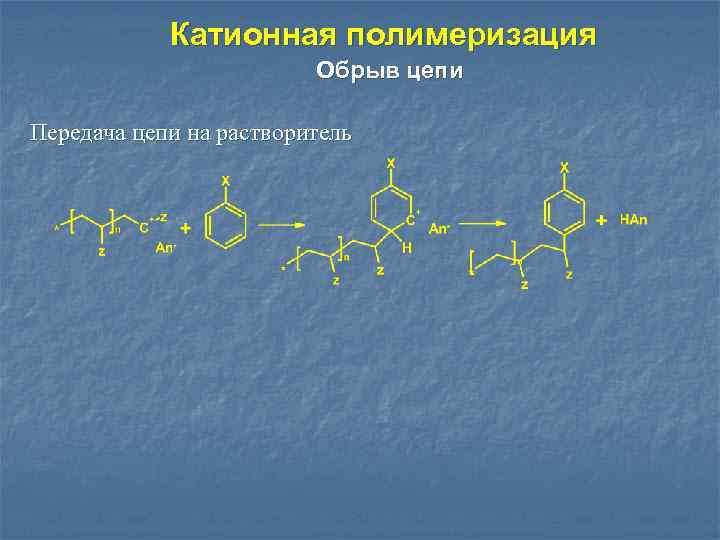 Катионная полимеризация Обрыв цепи Передача цепи на растворитель
Катионная полимеризация Обрыв цепи Передача цепи на растворитель
 Катионная полимеризация Кинетика катионной полимеризации Скорость инициирования зависит от концентрации инициатора: vи = kи [I] Скорость роста цепи пропорциональна концентрации активного карбокатиона и мономера: vр = kр[Pn+][M] Обрыв цепи описывается уравнением мономолекулярной реакции по отношению к концентрации активного центра vоб = kоб[Pn+]
Катионная полимеризация Кинетика катионной полимеризации Скорость инициирования зависит от концентрации инициатора: vи = kи [I] Скорость роста цепи пропорциональна концентрации активного карбокатиона и мономера: vр = kр[Pn+][M] Обрыв цепи описывается уравнением мономолекулярной реакции по отношению к концентрации активного центра vоб = kоб[Pn+]
 Катионная полимеризация Кинетика катионной полимеризации В стационарном режиме полимеризации скорость обрыва можно принять равной скорости инициирования (vо = vи ) Тогда выражение для скорости полимеризации будет иметь следующий вид: kи kр vп = [M] [I] kо Степень полимеризации v k [M] Рп = р vо + vп ko + kп[M] Степень полимеризации не зависит от концентрации инициатора
Катионная полимеризация Кинетика катионной полимеризации В стационарном режиме полимеризации скорость обрыва можно принять равной скорости инициирования (vо = vи ) Тогда выражение для скорости полимеризации будет иметь следующий вид: kи kр vп = [M] [I] kо Степень полимеризации v k [M] Рп = р vо + vп ko + kп[M] Степень полимеризации не зависит от концентрации инициатора
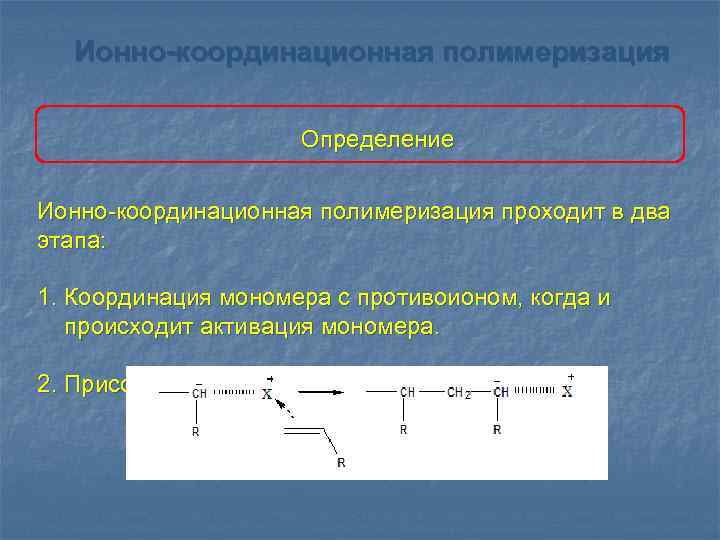 Ионно-координационная полимеризация Определение Ионно-координационная полимеризация проходит в два этапа: 1. Координация мономера с противоионом, когда и происходит активация мономера. 2. Присоединение мономера.
Ионно-координационная полимеризация Определение Ионно-координационная полимеризация проходит в два этапа: 1. Координация мономера с противоионом, когда и происходит активация мономера. 2. Присоединение мономера.
 Ионно-координационная полимеризация Катализаторы Циглера-Натта Карл Циглер (1898 - 1973) Джулио Натта (1903 - 1979) Нобелевская премия по химии «за открытия в области химии и технологии высокомолекулярных соединений»
Ионно-координационная полимеризация Катализаторы Циглера-Натта Карл Циглер (1898 - 1973) Джулио Натта (1903 - 1979) Нобелевская премия по химии «за открытия в области химии и технологии высокомолекулярных соединений»
 Ионно-координационная полимеризация Катализаторы Циглера-Натта Первые попытки использования катализаторов, содержащих алюминий (Циглер): Полимеризация этилена (Циглер): Вклад Натта: − первый пример изотактического кристаллического полимера
Ионно-координационная полимеризация Катализаторы Циглера-Натта Первые попытки использования катализаторов, содержащих алюминий (Циглер): Полимеризация этилена (Циглер): Вклад Натта: − первый пример изотактического кристаллического полимера
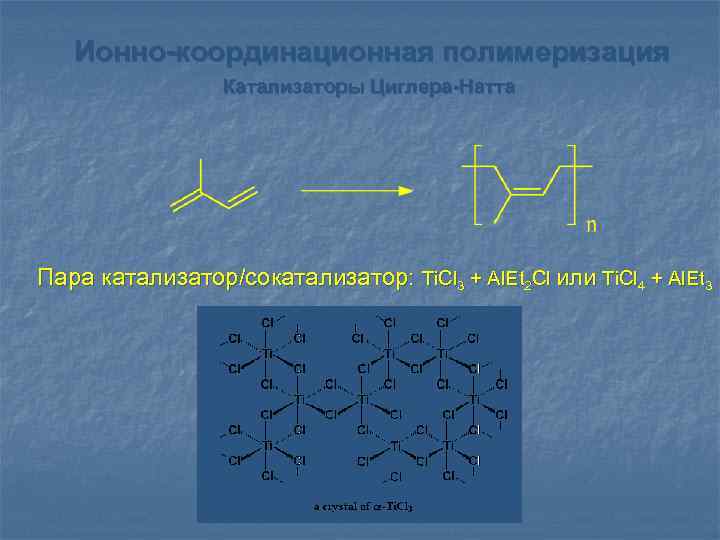 Ионно-координационная полимеризация Катализаторы Циглера-Натта Пара катализатор/сокатализатор: Ti. Cl 3 + Al. Et 2 Cl или Ti. Cl 4 + Al. Et 3
Ионно-координационная полимеризация Катализаторы Циглера-Натта Пара катализатор/сокатализатор: Ti. Cl 3 + Al. Et 2 Cl или Ti. Cl 4 + Al. Et 3
 Ионно-координационная полимеризация Катализаторы Циглера-Натта
Ионно-координационная полимеризация Катализаторы Циглера-Натта
 Ионно-координационная полимеризация Катализаторы Циглера-Натта
Ионно-координационная полимеризация Катализаторы Циглера-Натта
 Ионно-координационная полимеризация Катализаторы Циглера-Натта
Ионно-координационная полимеризация Катализаторы Циглера-Натта
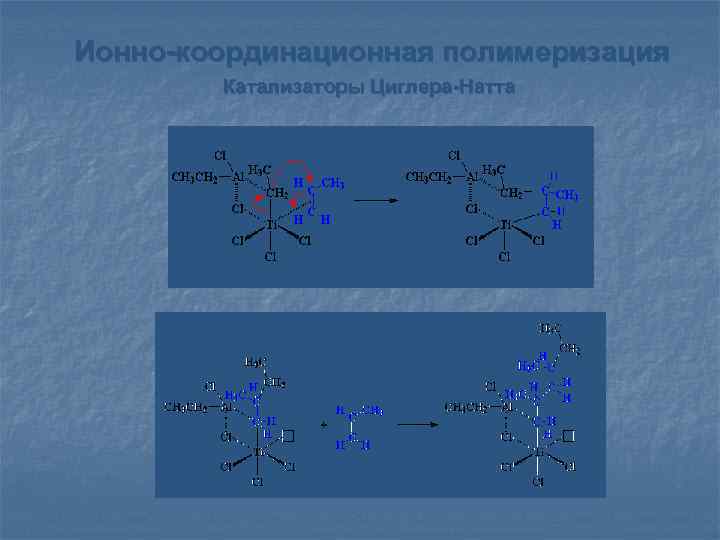 Ионно-координационная полимеризация Катализаторы Циглера-Натта
Ионно-координационная полимеризация Катализаторы Циглера-Натта
 Ионно-координационная полимеризация Катализаторы Циглера-Натта
Ионно-координационная полимеризация Катализаторы Циглера-Натта
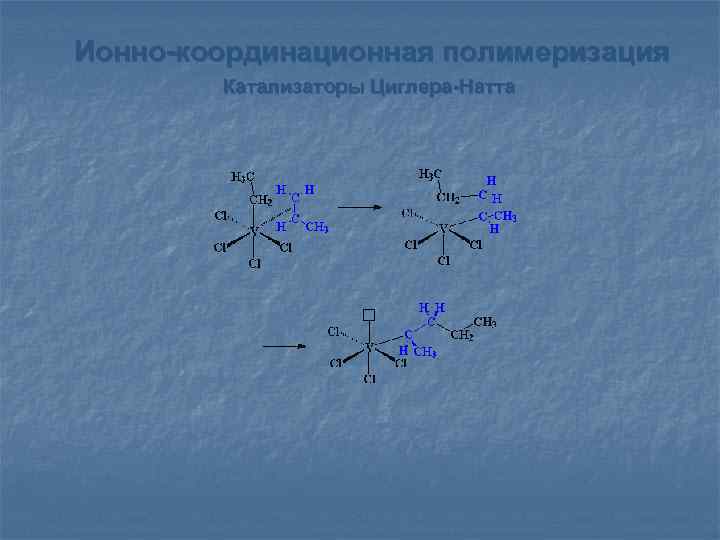 Ионно-координационная полимеризация Катализаторы Циглера-Натта
Ионно-координационная полимеризация Катализаторы Циглера-Натта
 Ионно-координационная полимеризация Катализаторы Циглера-Натта
Ионно-координационная полимеризация Катализаторы Циглера-Натта
 Ионно-координационная полимеризация Катализаторы Циглера-Натта Карл Циглер последний Alхимик, потому что «… он превратил алюминий в золото» .
Ионно-координационная полимеризация Катализаторы Циглера-Натта Карл Циглер последний Alхимик, потому что «… он превратил алюминий в золото» .


