11_Catalysis.ppt
- Количество слайдов: 37
 Каталіз
Каталіз
 Класифікація • Гомогенний каталіз • Гетерогенний каталіз • Ензиматичний каталіз Каталізатори зазвичай використовуються для: • Підвищення швидкості реакцій • Зміни температурного інтервалу перебігу реакцій • Впливу на розподіл продуктів
Класифікація • Гомогенний каталіз • Гетерогенний каталіз • Ензиматичний каталіз Каталізатори зазвичай використовуються для: • Підвищення швидкості реакцій • Зміни температурного інтервалу перебігу реакцій • Впливу на розподіл продуктів
 Найважливіші характеристики каталізаторів • активність – досягнення прийнятної швидкості реакції • селективність – мінімізація утворення побічних продуктів • час життя – часта заміна каталізатору значно підвищує вартість • вартість – прийнятна вартість визначається часом життя каталізатора та ціною продукту
Найважливіші характеристики каталізаторів • активність – досягнення прийнятної швидкості реакції • селективність – мінімізація утворення побічних продуктів • час життя – часта заміна каталізатору значно підвищує вартість • вартість – прийнятна вартість визначається часом життя каталізатора та ціною продукту
 Промотор: добавка, що не має притаманних даному каталізатору каталітичних властивостей, але підвищує активність каталізатору Введення промотору призводить до: • Збільшення доступної площини поверхні • Стабілізації каталізатору по відношенню до небажаних процесів зросту кристалів та спікання • Поліпшення механічної міцності Приклади: оксид алюмінію, азбест
Промотор: добавка, що не має притаманних даному каталізатору каталітичних властивостей, але підвищує активність каталізатору Введення промотору призводить до: • Збільшення доступної площини поверхні • Стабілізації каталізатору по відношенню до небажаних процесів зросту кристалів та спікання • Поліпшення механічної міцності Приклади: оксид алюмінію, азбест
 Носій: слугує головним чином як платформа, на яку наноситься каталізатор – зазвичай, не виявляє власної каталітичної активності Використання носія призводить до: • Збільшення доступної площини поверхні за рахунок високопористої природи носія • Підвищення стабільності • Поліпшення характеристик процесу теплопередачі Приклади: оксид алюмінію, азбест, карборунд, оксид заліза(ІІІ), манган, активоване вугілля, оксид цинку
Носій: слугує головним чином як платформа, на яку наноситься каталізатор – зазвичай, не виявляє власної каталітичної активності Використання носія призводить до: • Збільшення доступної площини поверхні за рахунок високопористої природи носія • Підвищення стабільності • Поліпшення характеристик процесу теплопередачі Приклади: оксид алюмінію, азбест, карборунд, оксид заліза(ІІІ), манган, активоване вугілля, оксид цинку
 Акселератори: речовини, які можуть додаватися до реакційної системи з метою підтримки активності каталізатора за рахунок мінімізації ефектів каталітичних отрут Отрути: речовини, які понижують активність каталізатора. Вони не додаються навмисно, проте наносяться на каталізатор під час реакції Приклади: сірка, свинець, іони деяких металів (Hg, Pd, Bi, Sn, Cu, Fe та ін. )
Акселератори: речовини, які можуть додаватися до реакційної системи з метою підтримки активності каталізатора за рахунок мінімізації ефектів каталітичних отрут Отрути: речовини, які понижують активність каталізатора. Вони не додаються навмисно, проте наносяться на каталізатор під час реакції Приклади: сірка, свинець, іони деяких металів (Hg, Pd, Bi, Sn, Cu, Fe та ін. )
 Інгібітор: речовина, що додається до каталізатору під час його виробництва з метою зменшення активності останнього
Інгібітор: речовина, що додається до каталізатору під час його виробництва з метою зменшення активності останнього
 Активність каталізатору залежить від текстури та електронної будови. Активність каталізатору пояснюється впливом наступних факторів: • Активні центри на поверхні каталізатору • Геометрія поверхні • Електронна будова • Утворення поверхневих інтермедіатів Ефективність каталізатору залежить від: активності, селективності та часу життя
Активність каталізатору залежить від текстури та електронної будови. Активність каталізатору пояснюється впливом наступних факторів: • Активні центри на поверхні каталізатору • Геометрія поверхні • Електронна будова • Утворення поверхневих інтермедіатів Ефективність каталізатору залежить від: активності, селективності та часу життя
 Активний центр: невеличка ділянка (точка) на поверхні каталізатора, що може утворювати міцні хімічні зв'язки з адсорбованими атомами або молекулами. Активні центри формуються ненасиченими атомами на поверхні, що утворюються внаслідок: • неоднорідності поверхні • дислокацій • наявності граней кристалів • розламів вздовж границь зерен
Активний центр: невеличка ділянка (точка) на поверхні каталізатора, що може утворювати міцні хімічні зв'язки з адсорбованими атомами або молекулами. Активні центри формуються ненасиченими атомами на поверхні, що утворюються внаслідок: • неоднорідності поверхні • дислокацій • наявності граней кристалів • розламів вздовж границь зерен
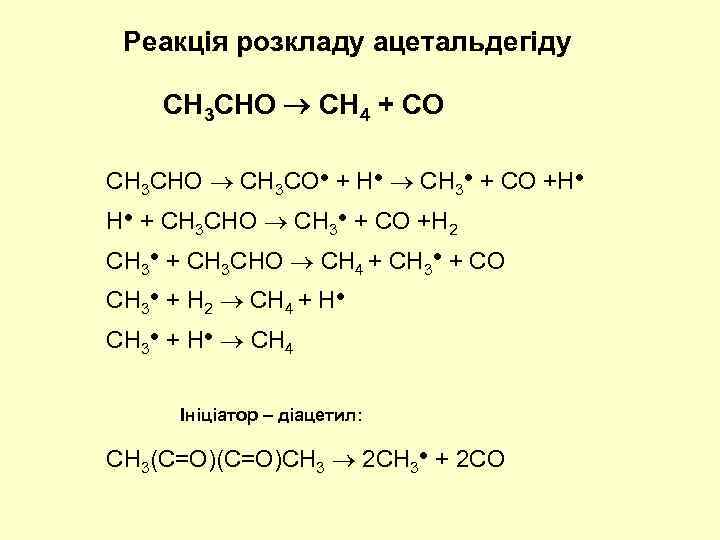 Реакція розкладу ацетальдегіду CH 3 CHO CH 4 + CO CH 3 CHO CH 3 CO● + H● CH 3● + CO +H● H● + CH 3 CHO CH 3● + CO +H 2 CH 3● + CH 3 CHO CH 4 + CH 3● + CO CH 3● + H 2 CH 4 + H● CH 3● + H● CH 4 Ініціатор – діацетил: CH 3(С=O)CH 3 2 CH 3● + 2 CO
Реакція розкладу ацетальдегіду CH 3 CHO CH 4 + CO CH 3 CHO CH 3 CO● + H● CH 3● + CO +H● H● + CH 3 CHO CH 3● + CO +H 2 CH 3● + CH 3 CHO CH 4 + CH 3● + CO CH 3● + H 2 CH 4 + H● CH 3● + H● CH 4 Ініціатор – діацетил: CH 3(С=O)CH 3 2 CH 3● + 2 CO
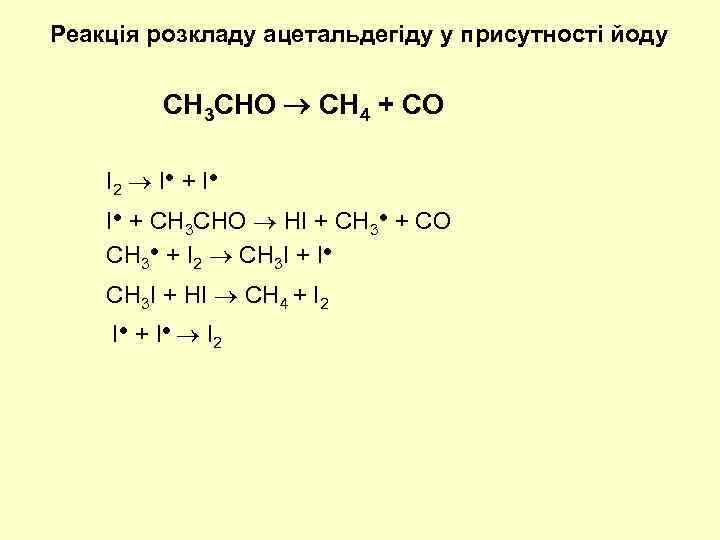 Реакція розкладу ацетальдегіду у присутності йоду CH 3 CHO CH 4 + CO I 2 I● + I● I● + CH 3 CHO HI + CH 3● + CO CH 3● + I 2 CH 3 I + I● CH 3 I + HI CH 4 + I 2 I● + I● I 2
Реакція розкладу ацетальдегіду у присутності йоду CH 3 CHO CH 4 + CO I 2 I● + I● I● + CH 3 CHO HI + CH 3● + CO CH 3● + I 2 CH 3 I + I● CH 3 I + HI CH 4 + I 2 I● + I● I 2
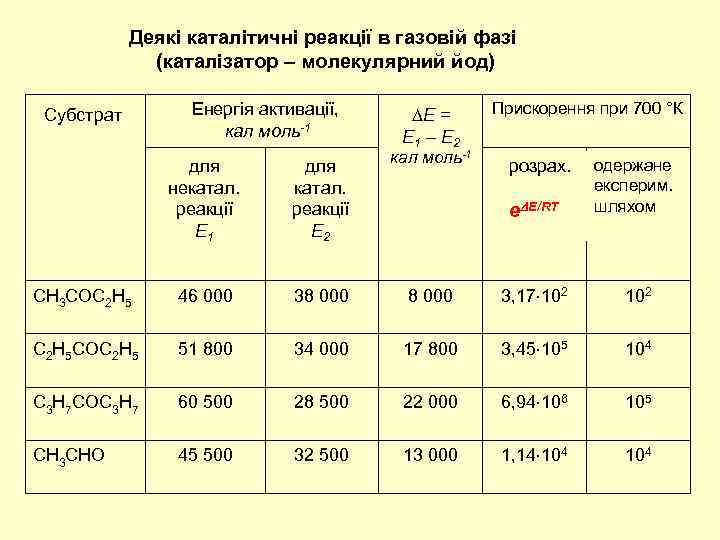 Деякі каталітичні реакції в газовій фазі (каталізатор – молекулярний йод) Субстрат Енергія активації, кал моль-1 Е = Е 1 – Е 2 для некатал. реакції Е 1 для катал. реакції Е 2 кал моль-1 CH 3 COC 2 H 5 46 000 38 000 C 2 H 5 COC 2 H 5 51 800 C 3 H 7 COC 3 H 7 CH 3 CHO Прискорення при 700 °К е Е/RT одержане експерим. шляхом 8 000 3, 17 102 34 000 17 800 3, 45 104 60 500 28 500 22 000 6, 94 106 105 45 500 32 500 13 000 1, 14 104 розрах.
Деякі каталітичні реакції в газовій фазі (каталізатор – молекулярний йод) Субстрат Енергія активації, кал моль-1 Е = Е 1 – Е 2 для некатал. реакції Е 1 для катал. реакції Е 2 кал моль-1 CH 3 COC 2 H 5 46 000 38 000 C 2 H 5 COC 2 H 5 51 800 C 3 H 7 COC 3 H 7 CH 3 CHO Прискорення при 700 °К е Е/RT одержане експерим. шляхом 8 000 3, 17 102 34 000 17 800 3, 45 104 60 500 28 500 22 000 6, 94 106 105 45 500 32 500 13 000 1, 14 104 розрах.
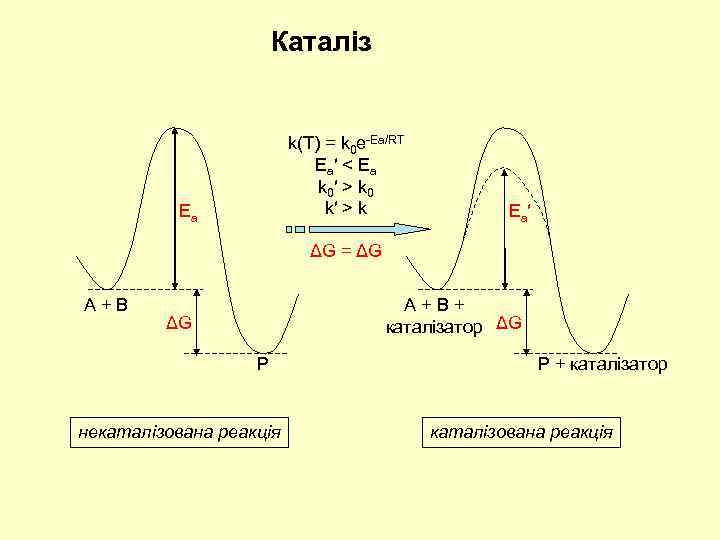 Каталіз k(T) = k 0 e-Ea/RT Ea′ < Ea k 0′ > k 0 k′ > k Ea Ea′ ΔG = ΔG A + B + каталізатор ΔG ΔG P некаталізована реакція P + каталізатор каталізована реакція
Каталіз k(T) = k 0 e-Ea/RT Ea′ < Ea k 0′ > k 0 k′ > k Ea Ea′ ΔG = ΔG A + B + каталізатор ΔG ΔG P некаталізована реакція P + каталізатор каталізована реакція
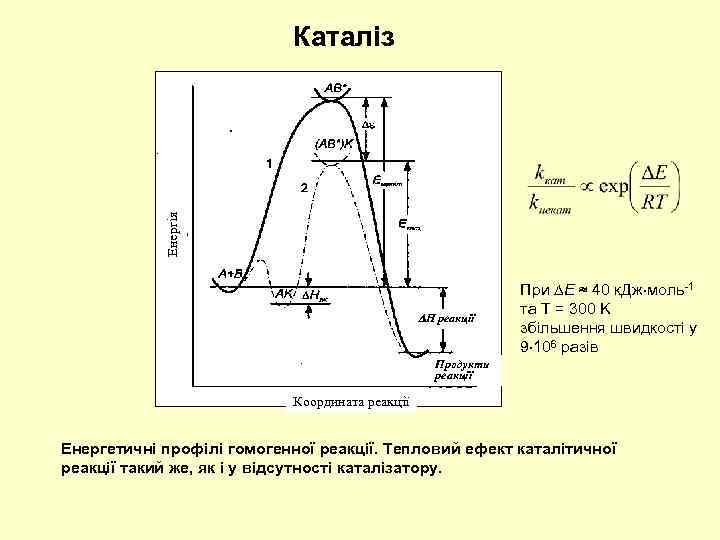 Енергія Каталіз H реакції При E ≈ 40 к. Дж моль-1 та T = 300 K збільшення швидкості у 9 106 разів Продукти реакції Координата реакції Енергетичні профілі гомогенної реакції. Тепловий ефект каталітичної реакції такий же, як і у відсутності каталізатору.
Енергія Каталіз H реакції При E ≈ 40 к. Дж моль-1 та T = 300 K збільшення швидкості у 9 106 разів Продукти реакції Координата реакції Енергетичні профілі гомогенної реакції. Тепловий ефект каталітичної реакції такий же, як і у відсутності каталізатору.
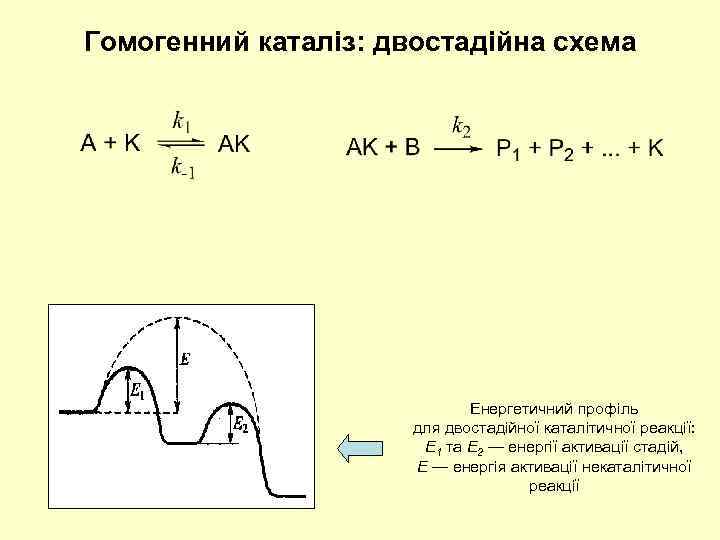 Гомогенний каталіз: двостадійна схема Енергетичний профіль для двостадійної каталітичної реакції: Е 1 та Е 2 — енергії активації стадій, Е — енергія активації некаталітичної реакції
Гомогенний каталіз: двостадійна схема Енергетичний профіль для двостадійної каталітичної реакції: Е 1 та Е 2 — енергії активації стадій, Е — енергія активації некаталітичної реакції
 Гомогенний каталіз: двостадійна схема
Гомогенний каталіз: двостадійна схема
 Типові форми кінетичних рівнянь для деяких гомогенно-каталітичних реакцій
Типові форми кінетичних рівнянь для деяких гомогенно-каталітичних реакцій
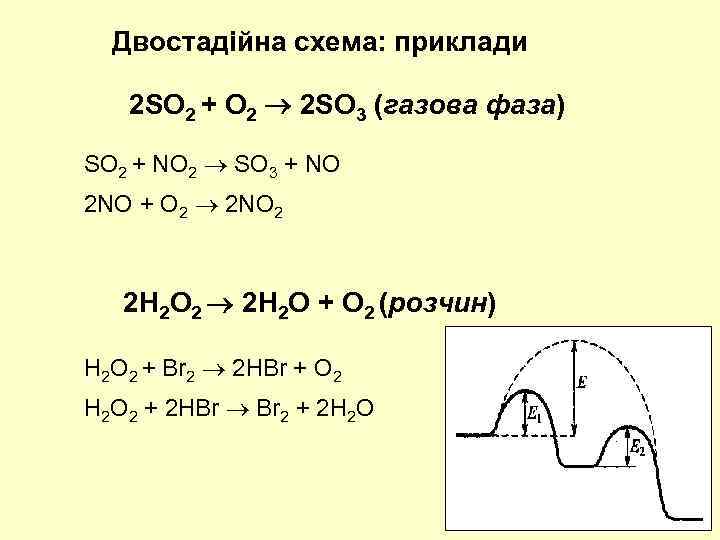 Двостадійна схема: приклади 2 SO 2 + O 2 2 SO 3 (газова фаза) SO 2 + NO 2 SO 3 + NO 2 NO + O 2 2 NO 2 2 H 2 O 2 2 H 2 O + O 2 (розчин) H 2 O 2 + Br 2 2 HBr + O 2 H 2 O 2 + 2 HBr Br 2 + 2 H 2 O
Двостадійна схема: приклади 2 SO 2 + O 2 2 SO 3 (газова фаза) SO 2 + NO 2 SO 3 + NO 2 NO + O 2 2 NO 2 2 H 2 O 2 2 H 2 O + O 2 (розчин) H 2 O 2 + Br 2 2 HBr + O 2 H 2 O 2 + 2 HBr Br 2 + 2 H 2 O
 Окисно-відновний каталіз 2 H 2 O 2 2 H 2 O + O 2 Fe 2+ + H 2 O 2 Fe 3+ + OH● + OHFe 3+ + H 2 O 2 Fe 2+ + H 2 O 2●+ H 2 O 2+ + OH- H 2 O + HO 2● Fe 2+ + OH● Fe 3+ + OHFe 3+ + HO 2● Fe 2+ + HO 2+ + OH- H 2 O + O 2
Окисно-відновний каталіз 2 H 2 O 2 2 H 2 O + O 2 Fe 2+ + H 2 O 2 Fe 3+ + OH● + OHFe 3+ + H 2 O 2 Fe 2+ + H 2 O 2●+ H 2 O 2+ + OH- H 2 O + HO 2● Fe 2+ + OH● Fe 3+ + OHFe 3+ + HO 2● Fe 2+ + HO 2+ + OH- H 2 O + O 2
 Автокаталітичні реакції Mn 2+ 5 C 2 O 42 - + 2 Mn. O 4 - + 16 H+ 2 Mn 2+ + 10 CO 2 + 8 H 2 O Некаталітичний процес: a – початкова концентрація реагенту, d – початкова концентрація каталізатора, а-x – поточна концентрація реагенту Початкові умови: x = 0 за t =0
Автокаталітичні реакції Mn 2+ 5 C 2 O 42 - + 2 Mn. O 4 - + 16 H+ 2 Mn 2+ + 10 CO 2 + 8 H 2 O Некаталітичний процес: a – початкова концентрація реагенту, d – початкова концентрація каталізатора, а-x – поточна концентрація реагенту Початкові умови: x = 0 за t =0
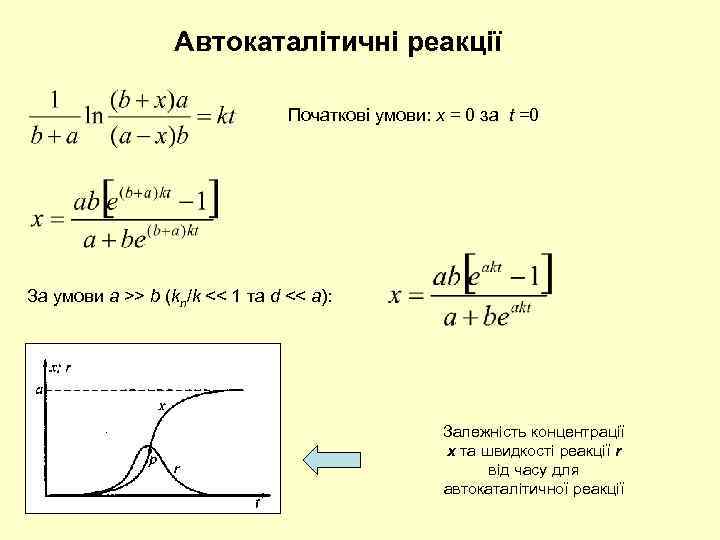 Автокаталітичні реакції Початкові умови: x = 0 за t =0 За умови a >> b (kn/k << 1 та d << a): Залежність концентрації x та швидкості реакції r від часу для автокаталітичної реакції
Автокаталітичні реакції Початкові умови: x = 0 за t =0 За умови a >> b (kn/k << 1 та d << a): Залежність концентрації x та швидкості реакції r від часу для автокаталітичної реакції
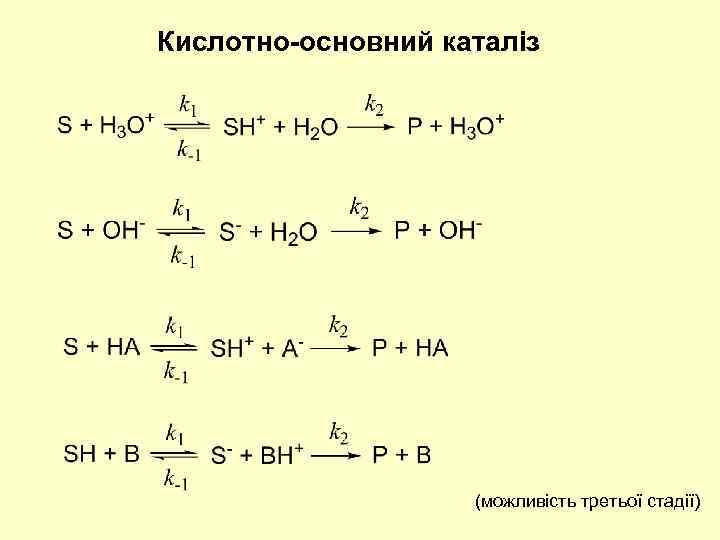 Кислотно-основний каталіз (можливість третьої стадії)
Кислотно-основний каталіз (можливість третьої стадії)
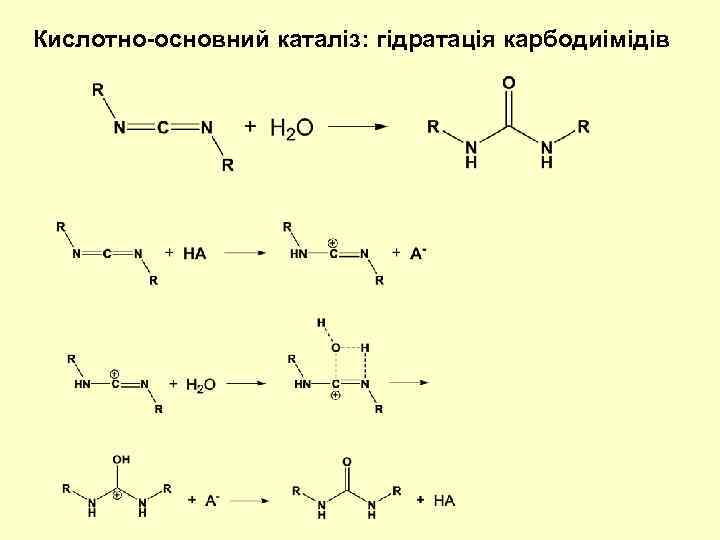 Кислотно-основний каталіз: гідратація карбодиімідів
Кислотно-основний каталіз: гідратація карбодиімідів
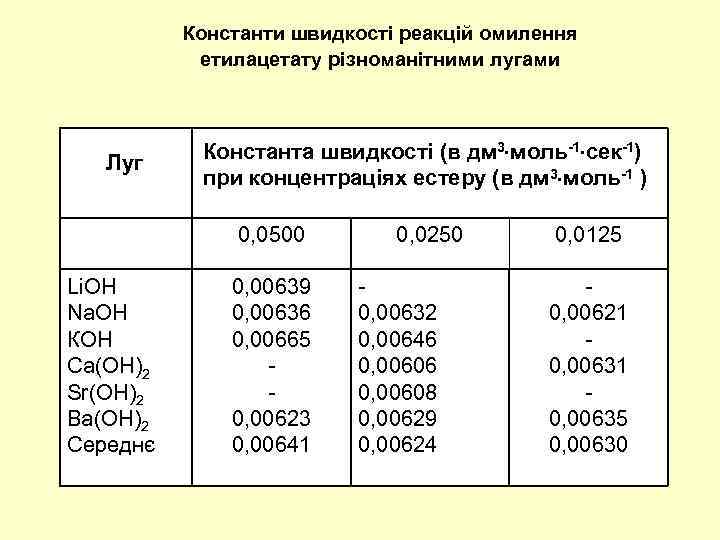 Константи швидкості реакцій омилення етилацетату різноманітними лугами Луг Константа швидкості (в дм 3 моль-1 сек-1) при концентраціях естеру (в дм 3 моль-1 ) 0, 0500 Li. OH Na. OH КОН Са(ОН)2 Sr(OH)2 Ва(ОН)2 Середнє 0, 00639 0, 00636 0, 00665 0, 00623 0, 00641 0, 0250 0, 00632 0, 00646 0, 00608 0, 00629 0, 00624 0, 0125 0, 00621 0, 00635 0, 00630
Константи швидкості реакцій омилення етилацетату різноманітними лугами Луг Константа швидкості (в дм 3 моль-1 сек-1) при концентраціях естеру (в дм 3 моль-1 ) 0, 0500 Li. OH Na. OH КОН Са(ОН)2 Sr(OH)2 Ва(ОН)2 Середнє 0, 00639 0, 00636 0, 00665 0, 00623 0, 00641 0, 0250 0, 00632 0, 00646 0, 00608 0, 00629 0, 00624 0, 0125 0, 00621 0, 00635 0, 00630
 Кислотно-основний каталіз
Кислотно-основний каталіз
 Специфічний кислотно-основний каталіз Для водних розчинів:
Специфічний кислотно-основний каталіз Для водних розчинів:
 Специфічний кислотний каталіз первинний сольовий ефект
Специфічний кислотний каталіз первинний сольовий ефект
 Специфічний кислотний каталіз Вимірюючи константу швидкості у розчинах з різною кислотністю, можна визначити значення k 2 та Kb
Специфічний кислотний каталіз Вимірюючи константу швидкості у розчинах з різною кислотністю, можна визначити значення k 2 та Kb
 Загальний кислотно-основний каталіз
Загальний кислотно-основний каталіз
 Загальний кислотно-основний каталіз Загальний кислотний каталіз Загальний основний каталіз Кореляційні співвідношення Бренстеда вторинний сольовий ефект
Загальний кислотно-основний каталіз Загальний кислотний каталіз Загальний основний каталіз Кореляційні співвідношення Бренстеда вторинний сольовий ефект
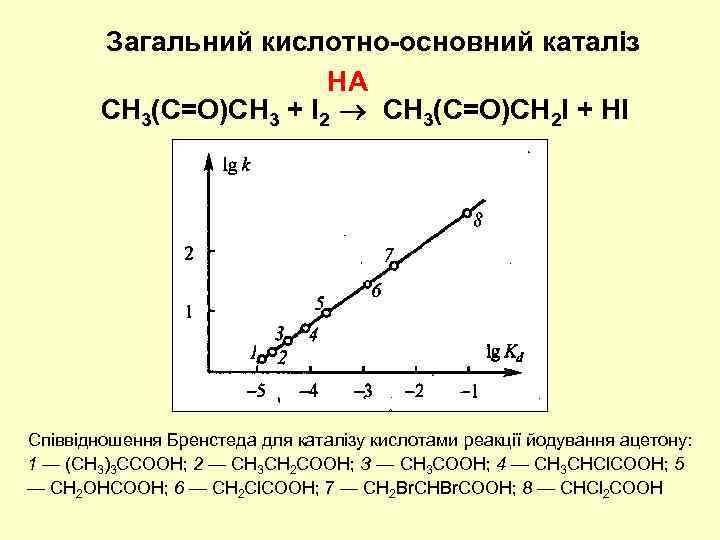 Загальний кислотно-основний каталіз HA CH 3(C=O)CH 3 + I 2 CH 3(C=O)CH 2 I + HI Співвідношення Бренстеда для каталізу кислотами реакції йодування ацетону: 1 — (СН 3)3 ССООН; 2 — СН 3 СН 2 СООН; З — СН 3 СООН; 4 — СН 3 СНСl. СООН; 5 — СН 2 ОНСООН; 6 — СН 2 Сl. СООН; 7 — СН 2 Вr. СНВr. СООН; 8 — СНСl 2 СООН
Загальний кислотно-основний каталіз HA CH 3(C=O)CH 3 + I 2 CH 3(C=O)CH 2 I + HI Співвідношення Бренстеда для каталізу кислотами реакції йодування ацетону: 1 — (СН 3)3 ССООН; 2 — СН 3 СН 2 СООН; З — СН 3 СООН; 4 — СН 3 СНСl. СООН; 5 — СН 2 ОНСООН; 6 — СН 2 Сl. СООН; 7 — СН 2 Вr. СНВr. СООН; 8 — СНСl 2 СООН
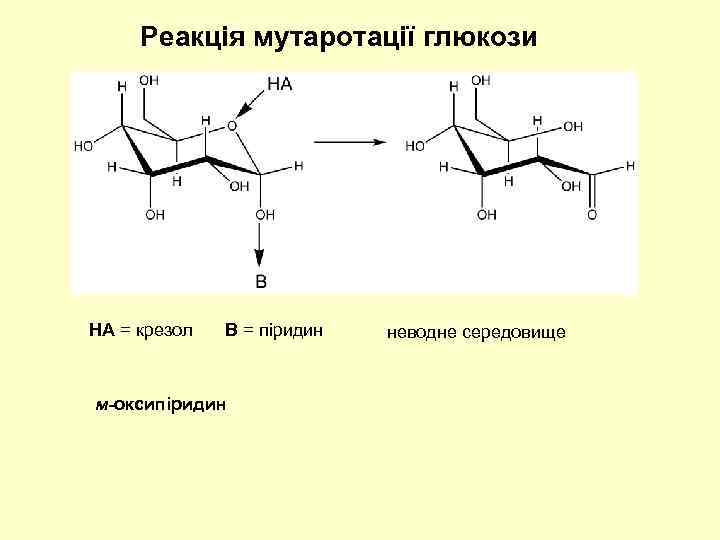 Реакція мутаротації глюкози HA = крезол B = піридин м-оксипіридин неводне середовище
Реакція мутаротації глюкози HA = крезол B = піридин м-оксипіридин неводне середовище
 Додаткові слайди
Додаткові слайди
 Catalytic steps in homogeneous reactions Most catalytic process can be built up from a small number of different types of step – Association / dissociation of a ligand » requires labile complexes – Insertion and elimination reactions – Nucleophilic attack on a coordinated ligand – Oxidation and reduction of a metal center – Oxidative addition / reductive elimination
Catalytic steps in homogeneous reactions Most catalytic process can be built up from a small number of different types of step – Association / dissociation of a ligand » requires labile complexes – Insertion and elimination reactions – Nucleophilic attack on a coordinated ligand – Oxidation and reduction of a metal center – Oxidative addition / reductive elimination
 • Coking/Fouling: deposition of carbonaceous material on the surface of the catalyst - Common to reactions involving hydrocarbons
• Coking/Fouling: deposition of carbonaceous material on the surface of the catalyst - Common to reactions involving hydrocarbons
 Типові форми кінетичних рівнянь для деяких гомогенно-каталітичних реакцій Механизм Кинетическое уравнение Предельные условия A 4 -B —v Продукты Л + К^ АК* d[A] dt ft, АК* + В -^ К + АВ ї^ї АВК* ft, А +В+К d[A] dt Аз. А, [A] [B] fti + K. IA] 1 Л| ft 3 ft, IAJ ГВ] r„, "Ai+*il. A][Bl 114 fti [A]>AS - ^Г- - а 3 [В] [К] АіГАІР]» *, ft 3>Ai [A] -i. H^[A]IB]|ia fts» ft, [A][BJ -^--^-ІАЦВПй АВК* —V К + АВ А + К-^>АК* +B- dt A 3 A, [A] [B] ft, [A] + ft» [B] L ' ft, [AJ>ft» IB] —^--МВ][К 1 a [A] dt feft, [A] [B] fts 4 -fti [А] [В] 1 Л] A, [A][B]» ft 3 ^v. K + AB А + В 4 - К -^*- АВК*-^* К 4 - АВ MB] > ft: [A] -■^--MAJIKI ft, > ft, [A] IB] - ^§~ - Ai [A] [B] IK] АВ —> Г [родукты к, AB 4 -K^=t АК* 4 -В ft, d[A] ■ ft 3 ft, [АВ] f. АВ 4 -К^±АВК* к, АВК* -^*- А 4 - В 4 - К dt d[AB dt MB]» ft, [AB] d[A] ft, [ABl , „, " df - ft 2 ' [BJ ll 4 ft 2 [BJ 4 - *, [ABJ IUJ АВ 4 -К-^-АК* +В АК*^- ft, [AB]>ft 2[B] АК* -Ь- К 4 - А К+А АВ 4 -К-Д-АВК* ^> А + В 4 - К ft 3 ft, [AB] ft. + ft. JABJ l. M A, [AB]» ftt d t. AJ ~ ь ft 3» ft, [AB] гк-i —Цр- " A, [AB] [K]
Типові форми кінетичних рівнянь для деяких гомогенно-каталітичних реакцій Механизм Кинетическое уравнение Предельные условия A 4 -B —v Продукты Л + К^ АК* d[A] dt ft, АК* + В -^ К + АВ ї^ї АВК* ft, А +В+К d[A] dt Аз. А, [A] [B] fti + K. IA] 1 Л| ft 3 ft, IAJ ГВ] r„, "Ai+*il. A][Bl 114 fti [A]>AS - ^Г- - а 3 [В] [К] АіГАІР]» *, ft 3>Ai [A] -i. H^[A]IB]|ia fts» ft, [A][BJ -^--^-ІАЦВПй АВК* —V К + АВ А + К-^>АК* +B- dt A 3 A, [A] [B] ft, [A] + ft» [B] L ' ft, [AJ>ft» IB] —^--МВ][К 1 a [A] dt feft, [A] [B] fts 4 -fti [А] [В] 1 Л] A, [A][B]» ft 3 ^v. K + AB А + В 4 - К -^*- АВК*-^* К 4 - АВ MB] > ft: [A] -■^--MAJIKI ft, > ft, [A] IB] - ^§~ - Ai [A] [B] IK] АВ —> Г [родукты к, AB 4 -K^=t АК* 4 -В ft, d[A] ■ ft 3 ft, [АВ] f. АВ 4 -К^±АВК* к, АВК* -^*- А 4 - В 4 - К dt d[AB dt MB]» ft, [AB] d[A] ft, [ABl , „, " df - ft 2 ' [BJ ll 4 ft 2 [BJ 4 - *, [ABJ IUJ АВ 4 -К-^-АК* +В АК*^- ft, [AB]>ft 2[B] АК* -Ь- К 4 - А К+А АВ 4 -К-Д-АВК* ^> А + В 4 - К ft 3 ft, [AB] ft. + ft. JABJ l. M A, [AB]» ftt d t. AJ ~ ь ft 3» ft, [AB] гк-i —Цр- " A, [AB] [K]
 Вирази Kp через Тип реакції A 2 B Вигляд рівняння Тип реакції 2 A 3 B A B + C 2 A B + 2 C A + B C + D 2 A + B C A + 3/2 B C + D 3 A + B 2 C 2 A + B 2 C A + B 2 C A + 2 B C + D A + B 3 C 2 A B + C Вигляд рівняння
Вирази Kp через Тип реакції A 2 B Вигляд рівняння Тип реакції 2 A 3 B A B + C 2 A B + 2 C A + B C + D 2 A + B C A + 3/2 B C + D 3 A + B 2 C 2 A + B 2 C A + B 2 C A + 2 B C + D A + B 3 C 2 A B + C Вигляд рівняння


