 Катализ
Катализ
 Что такое катализатор? • Свойства: - Селективность. Катализаторы сами не вызывают химическую реакцию, а только ускоряют реакцию, которая протекает и без них. - Не влияют на энергетический итог реакции. - В обратимых реакциях катализаторы ускоряют как прямую, так и обратную реакцию, причем в одинаковой степени. - Каталитические яды
Что такое катализатор? • Свойства: - Селективность. Катализаторы сами не вызывают химическую реакцию, а только ускоряют реакцию, которая протекает и без них. - Не влияют на энергетический итог реакции. - В обратимых реакциях катализаторы ускоряют как прямую, так и обратную реакцию, причем в одинаковой степени. - Каталитические яды
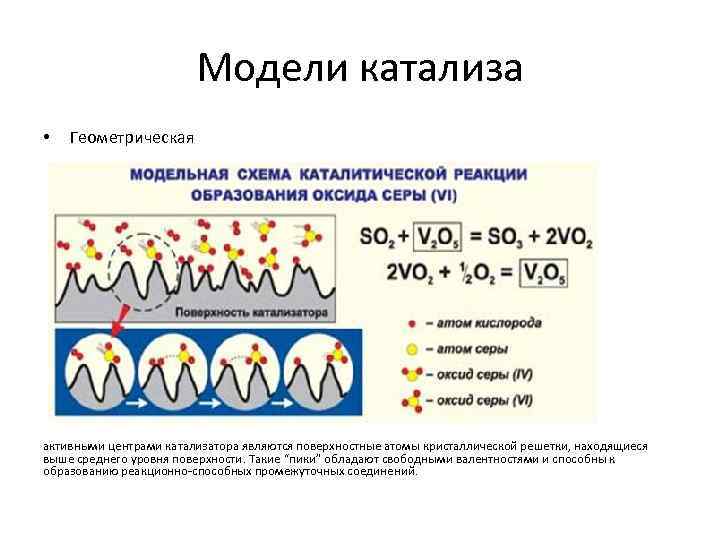 Модели катализа • Геометрическая активными центрами катализатора являются поверхностные атомы кристаллической решетки, находящиеся выше среднего уровня поверхности. Такие “пики” обладают свободными валентностями и способны к образованию реакционно-способных промежуточных соединений.
Модели катализа • Геометрическая активными центрами катализатора являются поверхностные атомы кристаллической решетки, находящиеся выше среднего уровня поверхности. Такие “пики” обладают свободными валентностями и способны к образованию реакционно-способных промежуточных соединений.
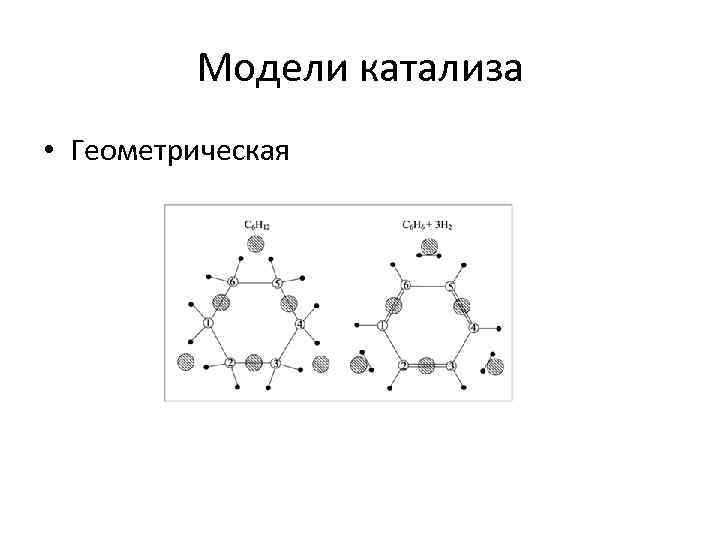 Модели катализа • Геометрическая
Модели катализа • Геометрическая
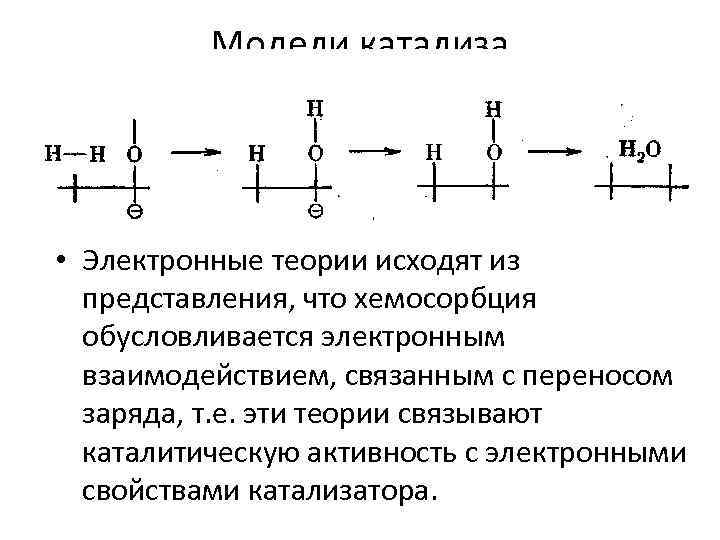 Модели катализа • Электронные теории исходят из представления, что хемосорбция обусловливается электронным взаимодействием, связанным с переносом заряда, т. е. эти теории связывают каталитическую активность с электронными свойствами катализатора.
Модели катализа • Электронные теории исходят из представления, что хемосорбция обусловливается электронным взаимодействием, связанным с переносом заряда, т. е. эти теории связывают каталитическую активность с электронными свойствами катализатора.
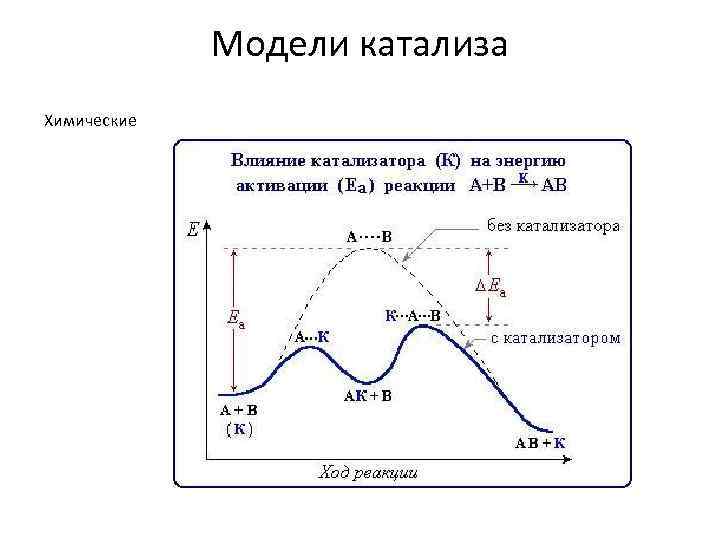 Модели катализа Химические
Модели катализа Химические
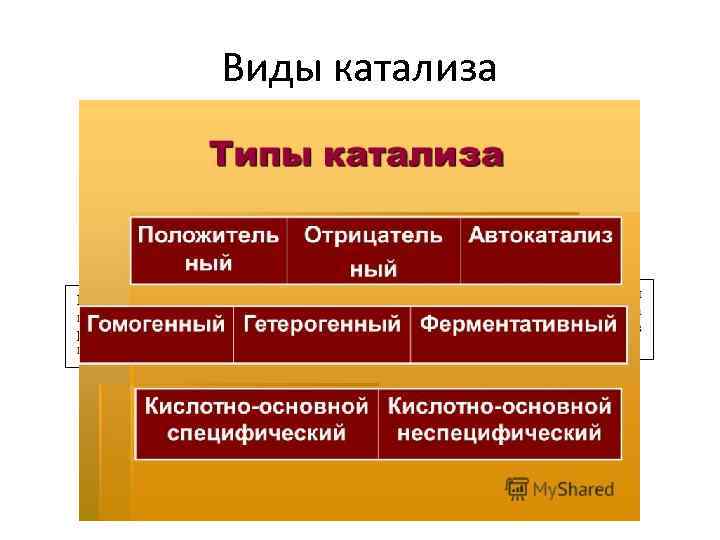 Виды катализа
Виды катализа
 Сложный катализатор 1. Отрыв NO 2 групп 2. Окисление углерода и водородосодержащие продукты, восстановление до окиси азота 3. Сажа адсорбирует окиси азота 4. Свинец катализует окисление C 5. Медь катализует окисление CO Pb. O Cu. O
Сложный катализатор 1. Отрыв NO 2 групп 2. Окисление углерода и водородосодержащие продукты, восстановление до окиси азота 3. Сажа адсорбирует окиси азота 4. Свинец катализует окисление C 5. Медь катализует окисление CO Pb. O Cu. O
 Катализатор на подложке Для получения катализаторов с развитой пористой структурой применяют специальные методы их приготовления. Высокоразвитой структурой обладают некоторые природные либо искусственные высокопористые адсорбенты, такие как алюмосиликаты, цеолиты, силикагель, алюмогель, активированный уголь. Эти вещества также используют в качестве носителей для металлосодержащих компонентов каталитических систем.
Катализатор на подложке Для получения катализаторов с развитой пористой структурой применяют специальные методы их приготовления. Высокоразвитой структурой обладают некоторые природные либо искусственные высокопористые адсорбенты, такие как алюмосиликаты, цеолиты, силикагель, алюмогель, активированный уголь. Эти вещества также используют в качестве носителей для металлосодержащих компонентов каталитических систем.
 Катализатор на подложке
Катализатор на подложке