Катализ. Цепные реакции Лекция 12 по курсу «Общая


Катализ. Цепные реакции Лекция 12 по курсу «Общая химия»

Что такое катализатор? • Вещество, ускоряющее химическую реакцию, но само при этом не расходующееся • ***Это не значит, что катализатор не участвует в реакции!*** Участвует, и еще как! • Кроме положительного катализа (ускорение), существует отрицательный (ингибирование) • Катализ бывает гомогенный (катализатор в одной фазе с реагентами) и гетерогенный (катализатор и реагенты в разных фазах)
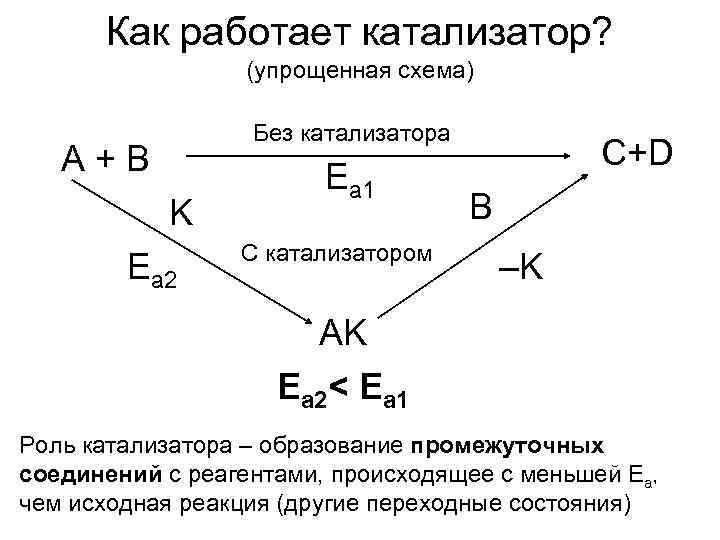
Как работает катализатор? (упрощенная схема) Без катализатора A+B С+D Ea 1 K B С катализатором Ea 2 –K AK Ea 2< Ea 1 Роль катализатора – образование промежуточных соединений с реагентами, происходящее с меньшей Ea, чем исходная реакция (другие переходные состояния)
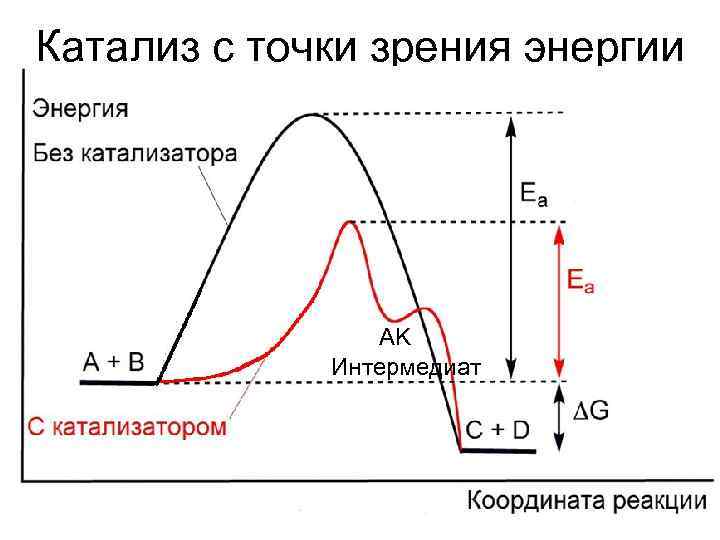
Катализ с точки зрения энергии AK Интермедиат

Важные замечания • Катализатор одинаково ускоряет как прямую, так и обратную реакцию. Поэтому он не смещает химического равновесия, а лишь ускоряет его достижение. • Тепловой эффект каталитической реакции такой же, как без катализатора! • Каталитические яды отравляют катализатор (лишают его активности), образуя более прочные соединения с ним, чем исходные вещества

Гомогенный катализ 2 H 2 O 2 = 2 H 2 O + O 2 Катализируется йодид-ионами 1. H 2 O 2 + I- = IO- + H 2 O Исходное Катали- Интер- Продукт вещество затор медиат 2. H 2 O 2 + IO- = H 2 O + O 2 + I- Исходное Интер- Катали- Продукт вещество медиат затор Если 1 – лимитирующая стадия, то: v = k. C(H 2 O 2)C(I–)
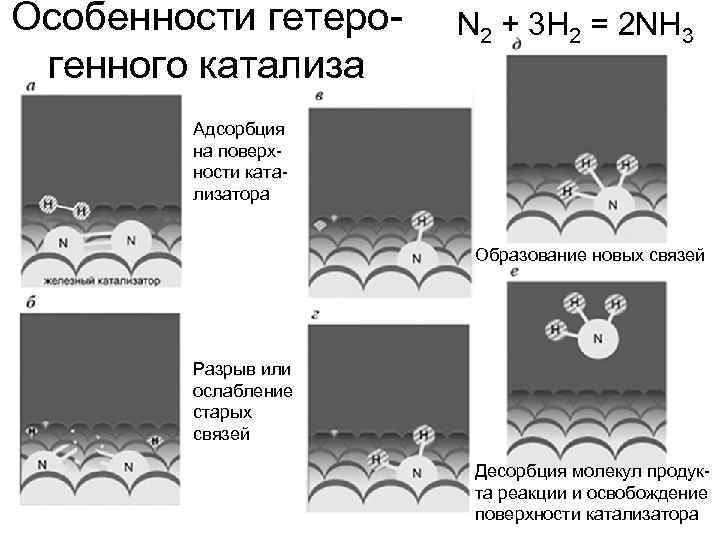
Особенности гетеро- N 2 + 3 H 2 = 2 NH 3 генного катализа Адсорбция на поверх- ности ката- лизатора Образование новых связей Разрыв или ослабление старых связей Десорбция молекул продук- та реакции и освобождение поверхности катализатора
Ферменты По химической природе – белки Особенности ферментативного катализа • Высочайшая селективность • Очень мягкие условия и высокая скорость • Скорость вначале растет с температурой, но затем начинает падать Причина? Денатурация белка!
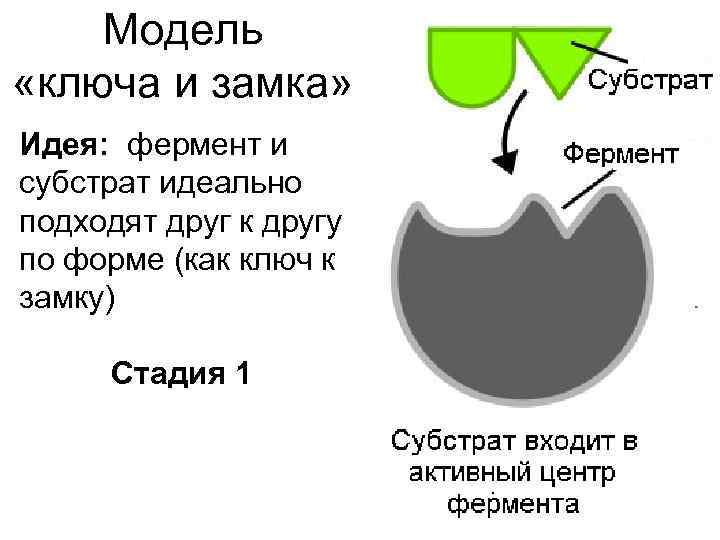
Модель «ключа и замка» Идея: фермент и субстрат идеально подходят друг к другу по форме (как ключ к замку) Стадия 1

Модель «ключа и замка» Взаимодействие в комплексе фермент- субстрат происходит за счет: Водородных связей Электростатического притяжения И т. д. Стадия 2

Модель «ключа и замка» Продукты реакции слабее удерживаются в комплексе с ферментом, чем исходные вещества Стадия 3

Модель «ключа и замка» После удаления продуктов активный центр восстанавливает исходную форму и снова готов к повторению стадии 1 Стадия 4

Автокатализ Автокаталитическая реакция: в качестве катализатора выступает один из продуктов 2 Mn. O 4− + 5 H 2 C 2 O 4 + 6 H+ = 2 Mn 2+ + 10 CO 2 + 8 H 2 O катализатор C C(Mn. O 4–) упала, скорость низкая Зависимость концентрации C(Mn 2+) больше, продуктов от скорость больше времени при автокатализе C(Mn 2+) низкая, скорость низкая t

Цепные реакции • Изучены Н. Семеновым и Р. Хиншелвудом в 30 -е годы ХХ века на примере окисления паров белого фосфора • Особенности – одна активная частица вызывает целый каскад (цепочку) превращений – скорость реакций зависит от формы сосуда и наличия инертных примесей – при очень высоких концентрациях скорость падает • Большинство реакций горения – цепные
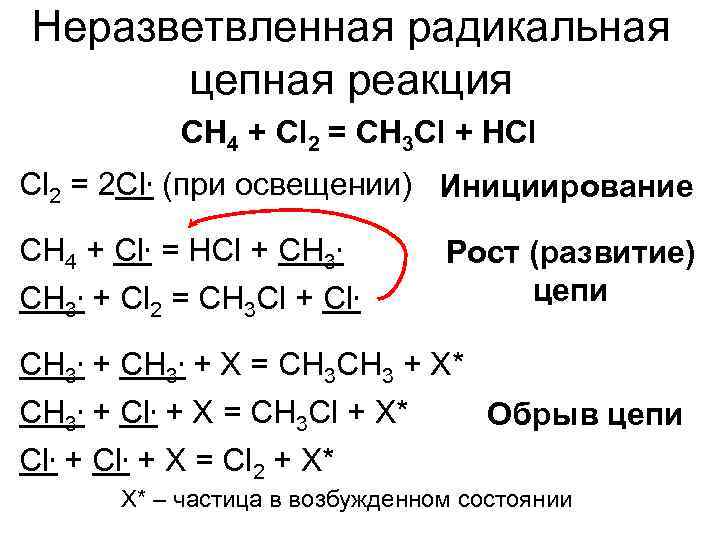
Неразветвленная радикальная цепная реакция CH 4 + Cl 2 = CH 3 Cl + HCl Cl 2 = 2 Cl∙ (при освещении) Инициирование CH 4 + Cl∙ = HCl + CH 3∙ Рост (развитие) CH 3∙ + Cl 2 = CH 3 Cl + Cl∙ цепи CH 3∙ + X = CH 3 + X* CH 3∙ + Cl∙ + X = CH 3 Cl + X* Обрыв цепи Cl∙ + X = Cl 2 + X* – частица в возбужденном состоянии

Разветвленная радикальная цепная реакция 2 H 2 + O 2 = 2 H 2 O O 2 = O 2* (при нагревании) Инициирование H 2 + O 2* = HOO∙ + H∙ H∙ + O 2 = HOO∙ Рост (развитие) HOO∙ + H 2 = H 2 O 2 + H∙ цепи H 2 O 2 = 2 HO∙ + H 2 = H 2 O + H∙ Обрыв цепи HO∙ + H∙ + X = H 2 O + X* (пример)
12_Катализ и цепные реакции.ppt
- Количество слайдов: 16

