катализ 1 - 2014.pptx
- Количество слайдов: 44
 Катализ 1. Основные понятия.
Катализ 1. Основные понятия.
 Определение катализа проф. Г. К. Боресков (1907 -1984) Катализ – изменение скорости химической реакции под влиянием веществ – катализаторов, многократно вступающий в катализаторов промежуточное химическое взаимодействие с участниками реакции и восстанавливающих свой химический состав после каждого цикла взаимодействия.
Определение катализа проф. Г. К. Боресков (1907 -1984) Катализ – изменение скорости химической реакции под влиянием веществ – катализаторов, многократно вступающий в катализаторов промежуточное химическое взаимодействие с участниками реакции и восстанавливающих свой химический состав после каждого цикла взаимодействия.
 Определение катализа ИЮПАК Катализатор – это вещество, увеличивающее скорость реакции, но не изменяющее суммарной стандартной энергии Гиббса Явление называется катализом, реакции каталитическими. «Катализ» и «катализатор» не следует применять при замедлении скорости реакции. В этом случае пользуются термином «ингибитор» а
Определение катализа ИЮПАК Катализатор – это вещество, увеличивающее скорость реакции, но не изменяющее суммарной стандартной энергии Гиббса Явление называется катализом, реакции каталитическими. «Катализ» и «катализатор» не следует применять при замедлении скорости реакции. В этом случае пользуются термином «ингибитор» а
 Термодинамический аспект катализа 1. Катализатор не влияет на значение изменения энергии Гиббса реакции Следствие: Присутствие катализатора не может вызвать протекание реакции, запрещеной термодинамически ( ) 2 H 2 O H 2 + O 2 V = Const T = 25 0 C
Термодинамический аспект катализа 1. Катализатор не влияет на значение изменения энергии Гиббса реакции Следствие: Присутствие катализатора не может вызвать протекание реакции, запрещеной термодинамически ( ) 2 H 2 O H 2 + O 2 V = Const T = 25 0 C
 Термодинамический аспект катализа 2. Катализатор не смещает химическое равновесие. Следствия: а) Ка остается строго постоянной только в случае гетерогенного катализатора (а тв = 1). б) катализатор ускоряет как прямую, так и обратную реакцию, причем в одинаковое количество раз. в) катализатор не меняет равновесный состав смеси*. *Следует иметь ввиду возможность изменения коэффициентов активности в различных растворителях, приводящую к изменению Кс без изменения Ка
Термодинамический аспект катализа 2. Катализатор не смещает химическое равновесие. Следствия: а) Ка остается строго постоянной только в случае гетерогенного катализатора (а тв = 1). б) катализатор ускоряет как прямую, так и обратную реакцию, причем в одинаковое количество раз. в) катализатор не меняет равновесный состав смеси*. *Следует иметь ввиду возможность изменения коэффициентов активности в различных растворителях, приводящую к изменению Кс без изменения Ка
 N 2 + 3 H 2 2 NH 3 Проблема: При низкой температуре процесс очень медленный При высокой температуре равновесие смещено влево Т, С Выход, % 10 атм 100 атм 300 атм 400 3, 8 25 47 500 1, 3 10, 6 26 600 0, 5 4 14 Реальный процесс: 200 -300 атм; ~ 400 C; Fe, K 2 O, Ca. O
N 2 + 3 H 2 2 NH 3 Проблема: При низкой температуре процесс очень медленный При высокой температуре равновесие смещено влево Т, С Выход, % 10 атм 100 атм 300 атм 400 3, 8 25 47 500 1, 3 10, 6 26 600 0, 5 4 14 Реальный процесс: 200 -300 атм; ~ 400 C; Fe, K 2 O, Ca. O
 Термодинамический аспект катализа 3. Катализатор вступает в химическое взаимодействие с веществами, участвующими в реакции. Без катализатора: С катализатором: –> возникает новый путь реакции
Термодинамический аспект катализа 3. Катализатор вступает в химическое взаимодействие с веществами, участвующими в реакции. Без катализатора: С катализатором: –> возникает новый путь реакции
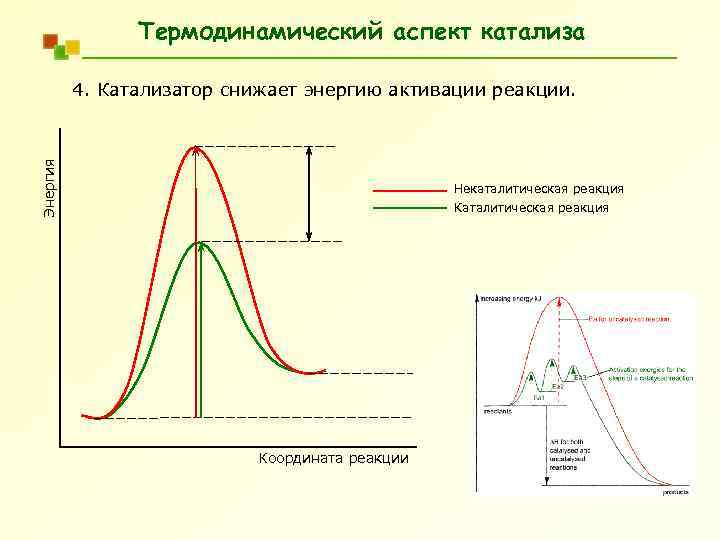 Термодинамический аспект катализа Энергия 4. Катализатор снижает энергию активации реакции. Некаталитическая реакция Координата реакции
Термодинамический аспект катализа Энергия 4. Катализатор снижает энергию активации реакции. Некаталитическая реакция Координата реакции
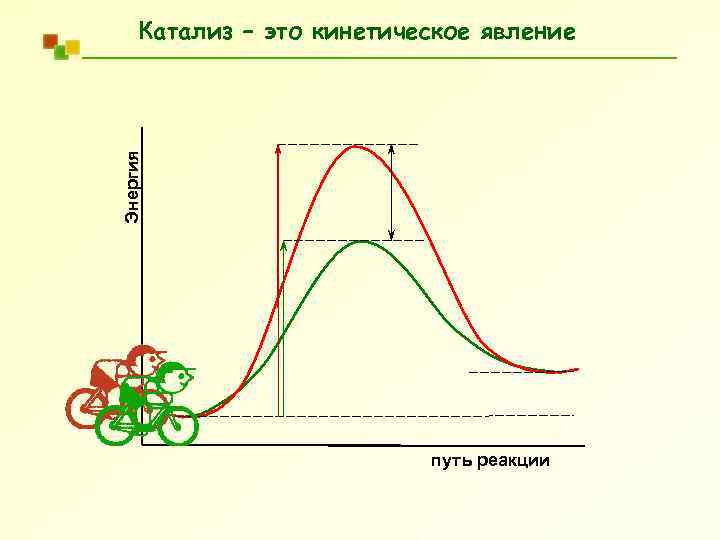 Энергия Катализ – это кинетическое явление путь реакции
Энергия Катализ – это кинетическое явление путь реакции
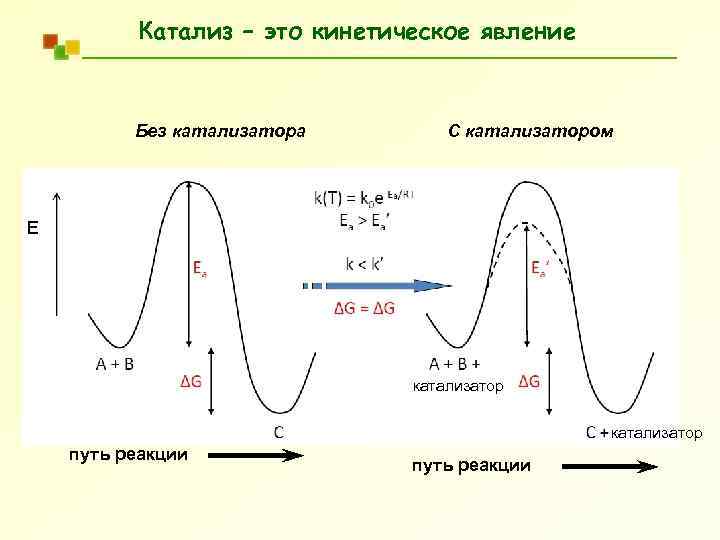 Катализ – это кинетическое явление Без катализатора С катализатором E катализатор путь реакции
Катализ – это кинетическое явление Без катализатора С катализатором E катализатор путь реакции
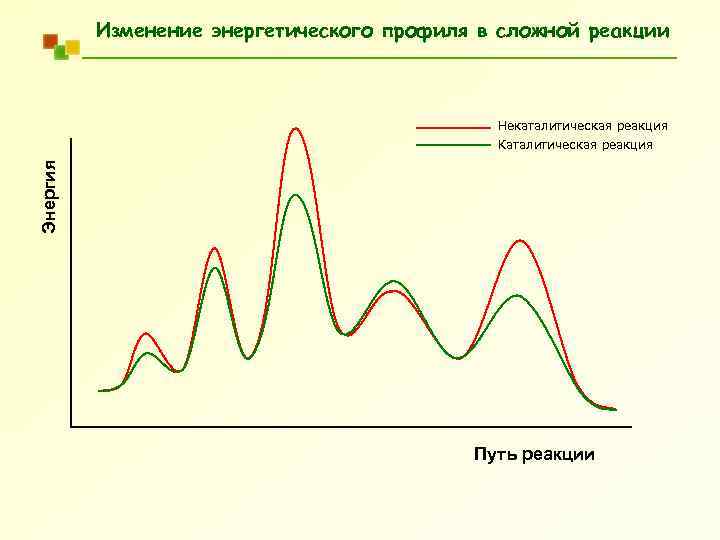 Изменение энергетического профиля в сложной реакции Некаталитическая реакция Энергия Каталитическая реакция Путь реакции
Изменение энергетического профиля в сложной реакции Некаталитическая реакция Энергия Каталитическая реакция Путь реакции
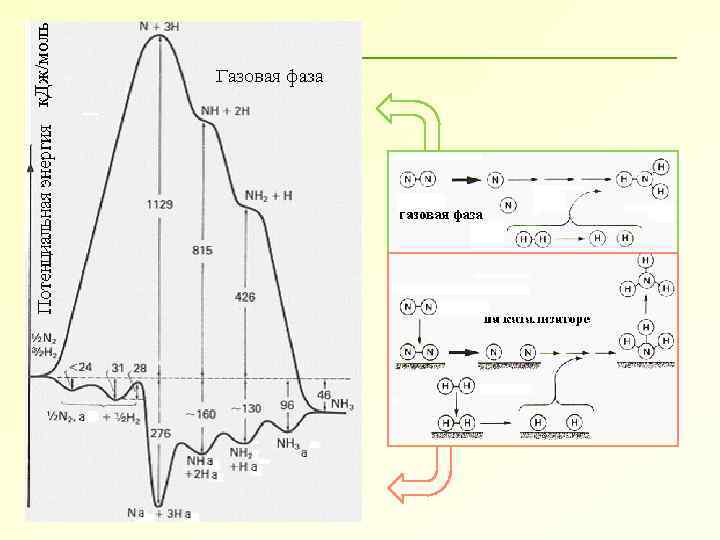 к. Дж/моль
к. Дж/моль
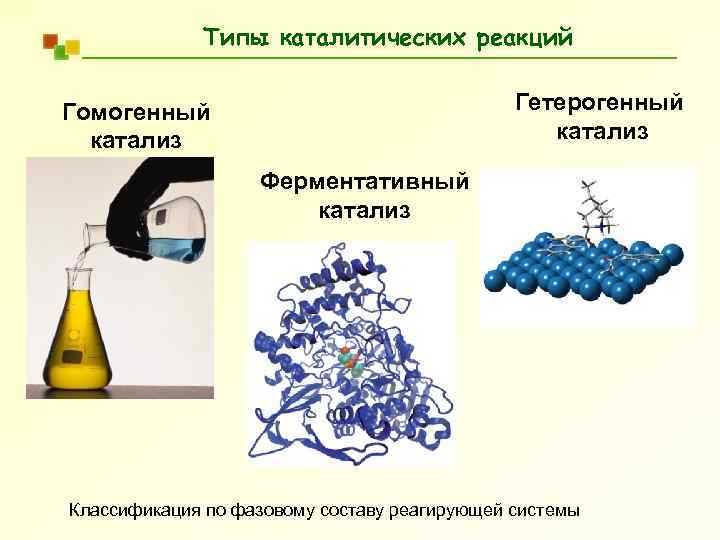 Типы каталитических реакций Гетерогенный катализ Гомогенный катализ Ферментативный катализ Классификация по фазовому составу реагирующей системы
Типы каталитических реакций Гетерогенный катализ Гомогенный катализ Ферментативный катализ Классификация по фазовому составу реагирующей системы
 Активный центр катализатора (АЦ) – это химическое соединение (изолированное или агрегированное с другими молекулами или атомами), имеющее состав и структуру, обеспечивающие его реакционную способность в образовании промежуточных веществ (интермедиатов), необходимых для превращения субстратов в продукты. В активные центры катализаторов может быть вовлечена как ничтожная часть массы катализатора (~ 10 -6%), так и практически весь катализатор (~ 100%). 3. По строению АЦ - массивный - нанесенный - закрепленный
Активный центр катализатора (АЦ) – это химическое соединение (изолированное или агрегированное с другими молекулами или атомами), имеющее состав и структуру, обеспечивающие его реакционную способность в образовании промежуточных веществ (интермедиатов), необходимых для превращения субстратов в продукты. В активные центры катализаторов может быть вовлечена как ничтожная часть массы катализатора (~ 10 -6%), так и практически весь катализатор (~ 100%). 3. По строению АЦ - массивный - нанесенный - закрепленный
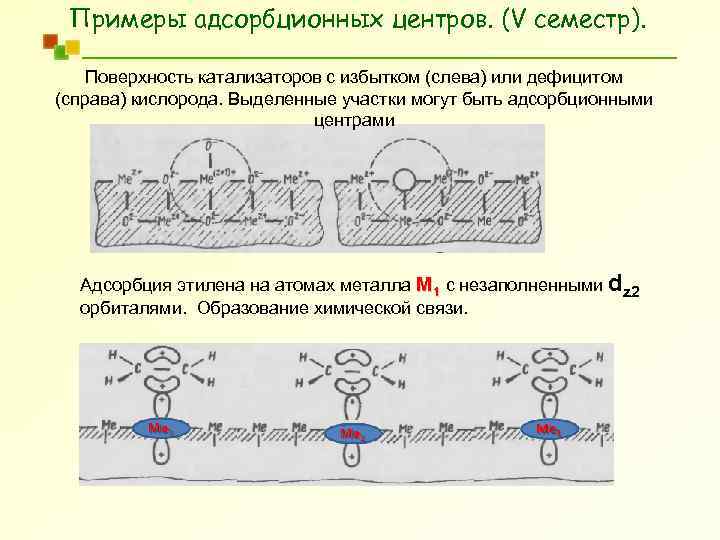 Примеры адсорбционных центров. (V семестр). Поверхность катализаторов с избытком (слева) или дефицитом (справа) кислорода. Выделенные участки могут быть адсорбционными центрами Адсорбция этилена на атомах металла М 1 с незаполненными dz 2 орбиталями. Образование химической связи.
Примеры адсорбционных центров. (V семестр). Поверхность катализаторов с избытком (слева) или дефицитом (справа) кислорода. Выделенные участки могут быть адсорбционными центрами Адсорбция этилена на атомах металла М 1 с незаполненными dz 2 орбиталями. Образование химической связи.
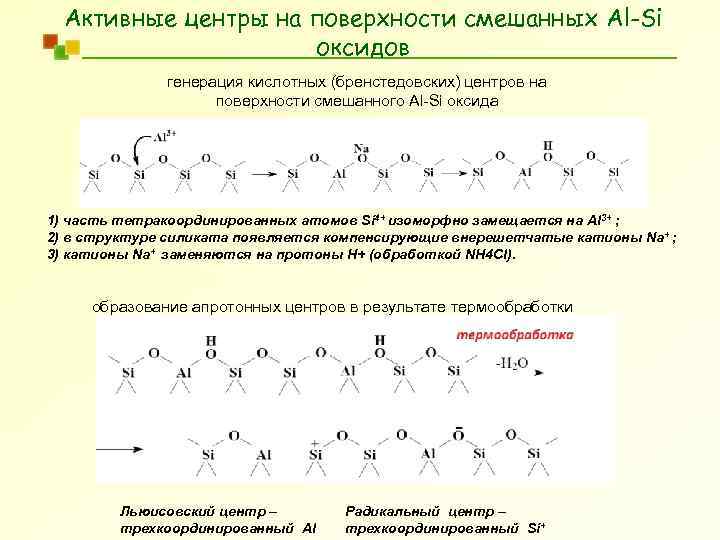 Активные центры на поверхности смешанных Al-Si оксидов генерация кислотных (бренстедовских) центров на поверхности смешанного Al-Si оксида 1) часть тетракоординированных атомов Si 4+ изоморфно замещается на Al 3+ ; 2) в структуре силиката появляется компенсирующие внерешетчатые катионы Na + ; 3) катионы Na+ заменяются на протоны Н+ (обработкой NH 4 Cl). образование апротонных центров в результате термообработки Льюисовский центр – трехкоординированный Al Радикальный центр – трехкоординированный Si+
Активные центры на поверхности смешанных Al-Si оксидов генерация кислотных (бренстедовских) центров на поверхности смешанного Al-Si оксида 1) часть тетракоординированных атомов Si 4+ изоморфно замещается на Al 3+ ; 2) в структуре силиката появляется компенсирующие внерешетчатые катионы Na + ; 3) катионы Na+ заменяются на протоны Н+ (обработкой NH 4 Cl). образование апротонных центров в результате термообработки Льюисовский центр – трехкоординированный Al Радикальный центр – трехкоординированный Si+
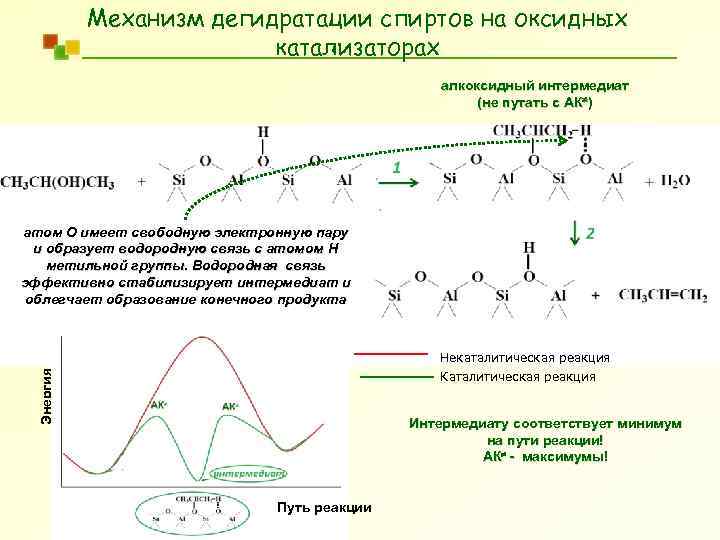 Механизм дегидратации спиртов на оксидных катализаторах алкоксидный интермедиат (не путать с АК ) атом О имеет свободную электронную пару и образует водородную связь с атомом Н метильной группы. Водородная связь эффективно стабилизирует интермедиат и облегчает образование конечного продукта Энергия Некаталитическая реакция Каталитическая реакция Интермедиату соответствует минимум на пути реакции! АК - максимумы! Путь реакции
Механизм дегидратации спиртов на оксидных катализаторах алкоксидный интермедиат (не путать с АК ) атом О имеет свободную электронную пару и образует водородную связь с атомом Н метильной группы. Водородная связь эффективно стабилизирует интермедиат и облегчает образование конечного продукта Энергия Некаталитическая реакция Каталитическая реакция Интермедиату соответствует минимум на пути реакции! АК - максимумы! Путь реакции
 Характеристики каталитического процесса Интегральная селективность nц. п – количество образующегося целевого продукта ni – количество образующегося i-продукта Дифференциальная селективность (мгновенная) rц. п – скорость образования целевого продукта ri – скорость образования i-продукта
Характеристики каталитического процесса Интегральная селективность nц. п – количество образующегося целевого продукта ni – количество образующегося i-продукта Дифференциальная селективность (мгновенная) rц. п – скорость образования целевого продукта ri – скорость образования i-продукта
 Активность катализатора A = rk – БОРЕСКОВ ro (1 - ) - степень заполнения реактора скорость реакции с катализатором Гомогенный катализ скорость реакции без катализатора [Ckат] = [молькат/лреакционной среды] Гетерогенный катализ Отнесение активности к единице площади поверхности катализатора ИЮПАК Отнесение активности к единице массы катализатора Количество продукта, образующегося в единицу времени на одном активном центре
Активность катализатора A = rk – БОРЕСКОВ ro (1 - ) - степень заполнения реактора скорость реакции с катализатором Гомогенный катализ скорость реакции без катализатора [Ckат] = [молькат/лреакционной среды] Гетерогенный катализ Отнесение активности к единице площади поверхности катализатора ИЮПАК Отнесение активности к единице массы катализатора Количество продукта, образующегося в единицу времени на одном активном центре
 Активный центр катализатора (АЦ) – это химическое соединение (изолированное или агрегированное с другими молекулами или атомами), имеющее состав и структуру, обеспечивающие его реакционную способность в образовании промежуточных веществ (интермедиатов), необходимых для превращения субстратов в продукты. В активные центры катализаторов может быть вовлечена как ничтожная часть массы катализатора (~ 10 -6%), так и практически весь катализатор (~ 100%). 3. По строению АЦ - массивный - нанесенный - закрепленный
Активный центр катализатора (АЦ) – это химическое соединение (изолированное или агрегированное с другими молекулами или атомами), имеющее состав и структуру, обеспечивающие его реакционную способность в образовании промежуточных веществ (интермедиатов), необходимых для превращения субстратов в продукты. В активные центры катализаторов может быть вовлечена как ничтожная часть массы катализатора (~ 10 -6%), так и практически весь катализатор (~ 100%). 3. По строению АЦ - массивный - нанесенный - закрепленный
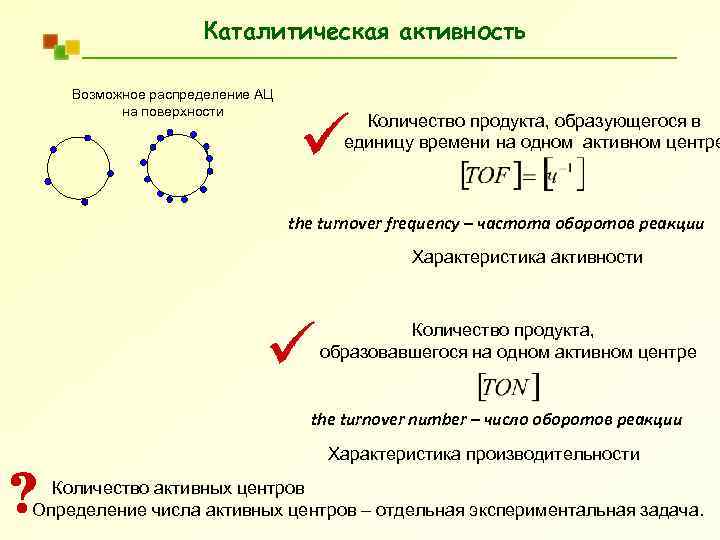 Каталитическая активность Возможное распределение АЦ на поверхности Количество продукта, образующегося в единицу времени на одном активном центре the turnover frequency – частота оборотов реакции Характеристика активности Количество продукта, образовавшегося на одном активном центре the turnover number – число оборотов реакции Характеристика производительности Количество активных центров Определение числа активных центров – отдельная экспериментальная задача.
Каталитическая активность Возможное распределение АЦ на поверхности Количество продукта, образующегося в единицу времени на одном активном центре the turnover frequency – частота оборотов реакции Характеристика активности Количество продукта, образовавшегося на одном активном центре the turnover number – число оборотов реакции Характеристика производительности Количество активных центров Определение числа активных центров – отдельная экспериментальная задача.
 Катализ 2. Гомогенный катализ. Общий и специфический кислотный катализ.
Катализ 2. Гомогенный катализ. Общий и специфический кислотный катализ.
 Гидратация карбодиимидов Медленно идет в нейтральных растворах, т. к. требует атаки слабого нуклеофила (воды) на слабый электрофил (углерод). В кислых растворах протонирование азота повышает электрофильность углерода и гидратация резко ускоряется
Гидратация карбодиимидов Медленно идет в нейтральных растворах, т. к. требует атаки слабого нуклеофила (воды) на слабый электрофил (углерод). В кислых растворах протонирование азота повышает электрофильность углерода и гидратация резко ускоряется
 Декарбонилирование бензоилмуравьиной кислоты Самая медленная стадия – превращение протонированного субстрата
Декарбонилирование бензоилмуравьиной кислоты Самая медленная стадия – превращение протонированного субстрата
 Специфический кислотный катализ • Первая стадия – квазиравновесная Константа связывания (binding) субстрата • Вторая стадия - медленная специфический кислотный катализ – скорость реакции зависит от
Специфический кислотный катализ • Первая стадия – квазиравновесная Константа связывания (binding) субстрата • Вторая стадия - медленная специфический кислотный катализ – скорость реакции зависит от
 Специфический кислотный катализ
Специфический кислотный катализ
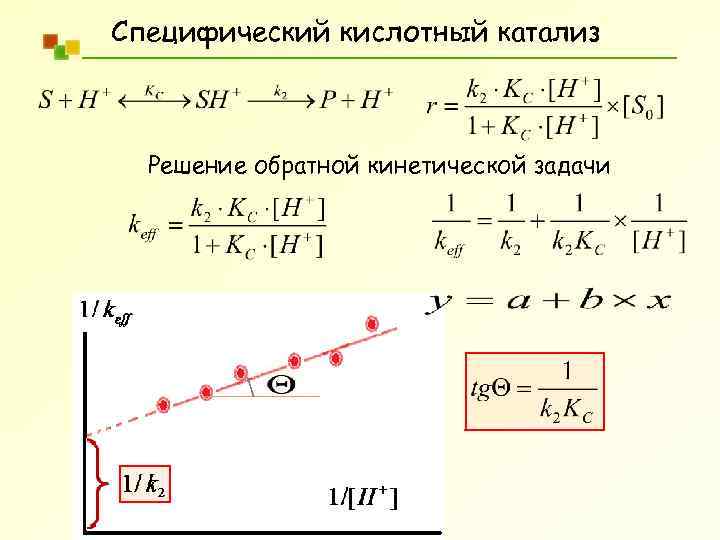 Специфический кислотный катализ Решение обратной кинетической задачи
Специфический кислотный катализ Решение обратной кинетической задачи
 Специфический кислотный катализ Реальные растворы и неводные растворители надо знать! индикаторная шкала кислотности ионизация индикатора В, константа основности В Кислотность Функция кислотности Гаммета
Специфический кислотный катализ Реальные растворы и неводные растворители надо знать! индикаторная шкала кислотности ионизация индикатора В, константа основности В Кислотность Функция кислотности Гаммета
 Специфический кислотный катализ Индикаторная шкала кислотности. 1 Кислотность – характеризует способность среды передавать протон субстрату В Функция кислотности Гаммета
Специфический кислотный катализ Индикаторная шкала кислотности. 1 Кислотность – характеризует способность среды передавать протон субстрату В Функция кислотности Гаммета
 Специфический кислотный катализ Индикаторная шкала кислотности. 2 ионизация индикатора В, константа основности В диссоциация протонированного индикатора ВН+, константа диссоциации ВН+ измеряемая величина (индикаторы В и его протонированная форма имеют разную окраску) константа диссоциации известна из справочных данных можно определить , добавив в среду индикатор В
Специфический кислотный катализ Индикаторная шкала кислотности. 2 ионизация индикатора В, константа основности В диссоциация протонированного индикатора ВН+, константа диссоциации ВН+ измеряемая величина (индикаторы В и его протонированная форма имеют разную окраску) константа диссоциации известна из справочных данных можно определить , добавив в среду индикатор В
 Специфический кислотный катализ Индикаторная шкала кислотности. 3 мало зависит от природы В, но определяется растворителем. в одной среде, с одной добавив в среду индикатор В и определив кислотность знаем
Специфический кислотный катализ Индикаторная шкала кислотности. 3 мало зависит от природы В, но определяется растворителем. в одной среде, с одной добавив в среду индикатор В и определив кислотность знаем
 Специфический кислотный катализ Индикаторная шкала кислотности. 4 Константа диссоциации SH+ Константа связывания субстрата и H+
Специфический кислотный катализ Индикаторная шкала кислотности. 4 Константа диссоциации SH+ Константа связывания субстрата и H+
 Специфический кислотный катализ
Специфический кислотный катализ
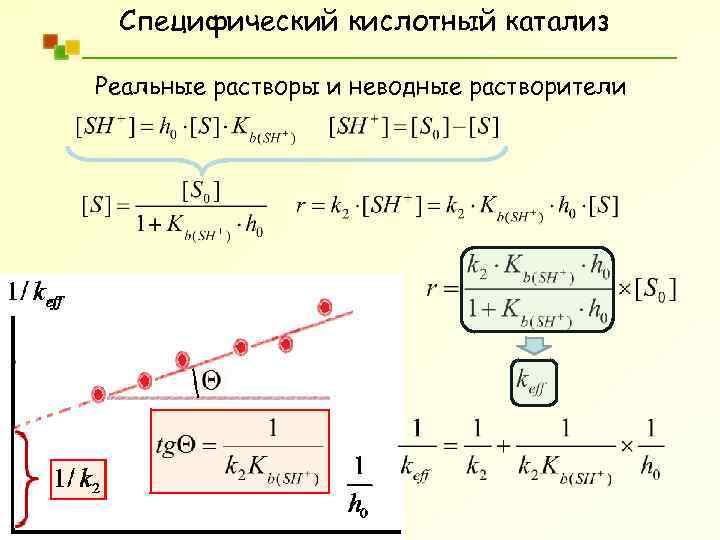 Специфический кислотный катализ Реальные растворы и неводные растворители
Специфический кислотный катализ Реальные растворы и неводные растворители
 Специфический кислотный катализ Реальные растворы и неводные растворители. Разбавленные растворы.
Специфический кислотный катализ Реальные растворы и неводные растворители. Разбавленные растворы.
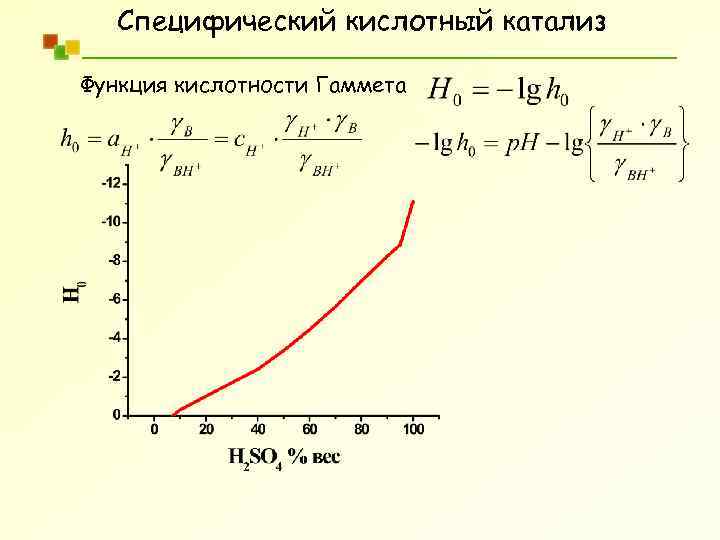 Специфический кислотный катализ Функция кислотности Гаммета
Специфический кислотный катализ Функция кислотности Гаммета
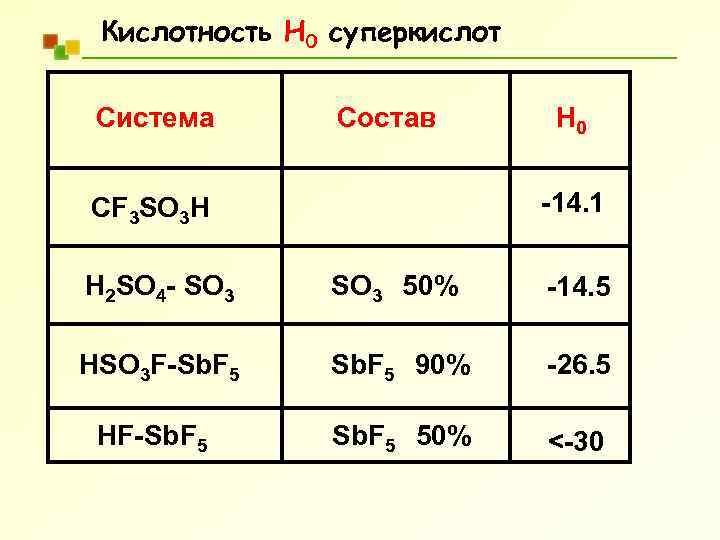 Кислотность Н 0 суперкислот Система Состав H 0 -14. 1 CF 3 SO 3 H H 2 SO 4 - SO 3 50% -14. 5 HSO 3 F-Sb. F 5 90% -26. 5 HF-Sb. F 5 50% <-30
Кислотность Н 0 суперкислот Система Состав H 0 -14. 1 CF 3 SO 3 H H 2 SO 4 - SO 3 50% -14. 5 HSO 3 F-Sb. F 5 90% -26. 5 HF-Sb. F 5 50% <-30
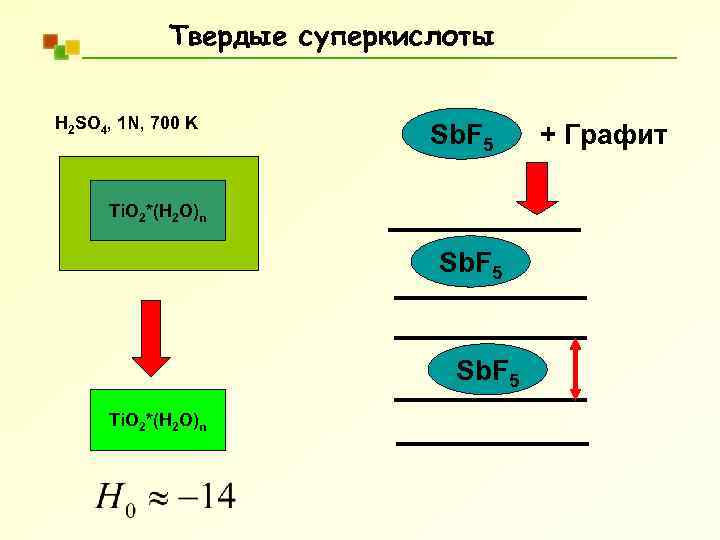 Твердые суперкислоты H 2 SO 4, 1 N, 700 K Sb. F 5 Ti. O 2*(H 2 O)n + Графит
Твердые суперкислоты H 2 SO 4, 1 N, 700 K Sb. F 5 Ti. O 2*(H 2 O)n + Графит
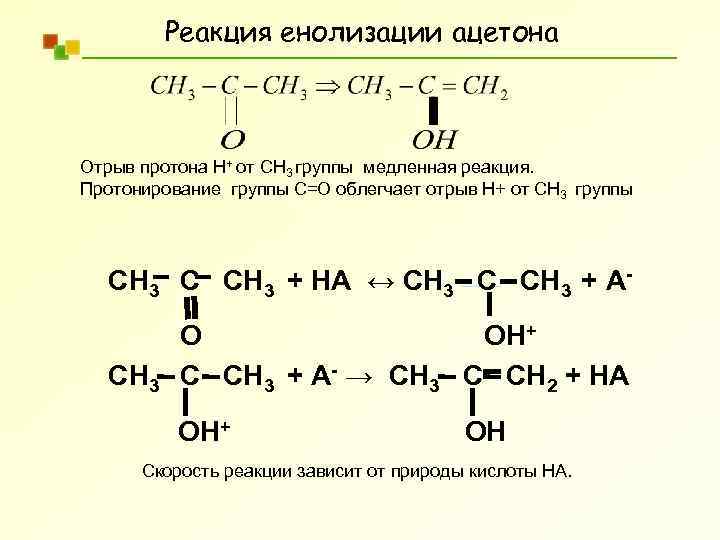 Реакция енолизации ацетона Отрыв протона Н+ от СН 3 группы медленная реакция. Протонирование группы С=О облегчает отрыв Н+ от СН 3 группы СH 3 C CH 3 + HA ↔ СH 3 C CH 3 + AСH 3 O OH+ C CH 3 + A- → СH 3 C CH 2 + НA OH+ OH Скорость реакции зависит от природы кислоты НА.
Реакция енолизации ацетона Отрыв протона Н+ от СН 3 группы медленная реакция. Протонирование группы С=О облегчает отрыв Н+ от СН 3 группы СH 3 C CH 3 + HA ↔ СH 3 C CH 3 + AСH 3 O OH+ C CH 3 + A- → СH 3 C CH 2 + НA OH+ OH Скорость реакции зависит от природы кислоты НА.
 Общий кислотный катализ • Кислота (катализатор) не только переводит субстрат в активную форму, но и участвует в его дальнейшем превращении. Скорость реакции зависит от природы кислоты. Лимитирующая стадия –протонирование субстрата
Общий кислотный катализ • Кислота (катализатор) не только переводит субстрат в активную форму, но и участвует в его дальнейшем превращении. Скорость реакции зависит от природы кислоты. Лимитирующая стадия –протонирование субстрата
 Общий кислотный катализ Н 3 О+ и Н 2 О также оказывают каталитическое действие
Общий кислотный катализ Н 3 О+ и Н 2 О также оказывают каталитическое действие
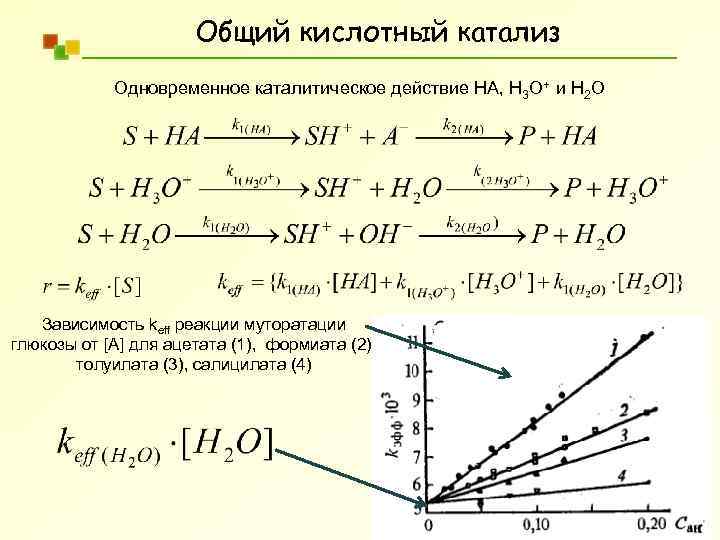 Общий кислотный катализ Одновременное каталитическое действие НА, Н 3 О+ и Н 2 О Зависимость keff реакции муторатации глюкозы от [A] для ацетата (1), формиата (2), толуилата (3), салицилата (4)
Общий кислотный катализ Одновременное каталитическое действие НА, Н 3 О+ и Н 2 О Зависимость keff реакции муторатации глюкозы от [A] для ацетата (1), формиата (2), толуилата (3), салицилата (4)
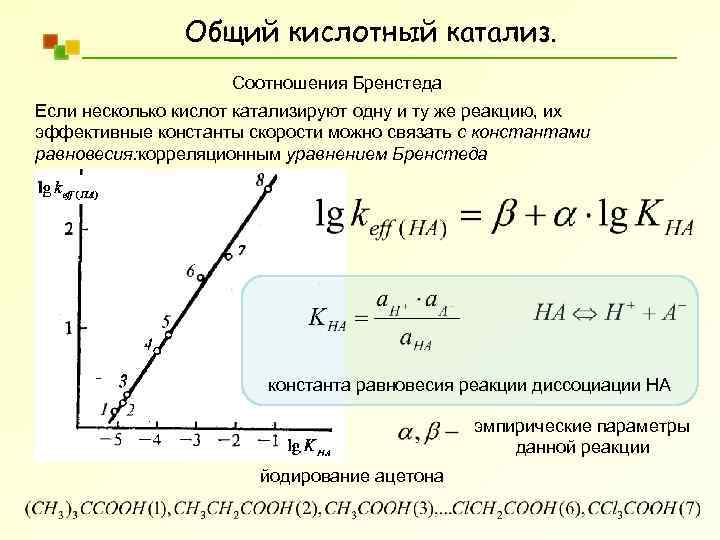 Общий кислотный катализ. Соотношения Бренстеда Если несколько кислот катализируют одну и ту же реакцию, их эффективные константы скорости можно связать с константами равновесия: корреляционным уравнением Бренстеда константа равновесия реакции диссоциации НА эмпирические параметры данной реакции йодирование ацетона
Общий кислотный катализ. Соотношения Бренстеда Если несколько кислот катализируют одну и ту же реакцию, их эффективные константы скорости можно связать с константами равновесия: корреляционным уравнением Бренстеда константа равновесия реакции диссоциации НА эмпирические параметры данной реакции йодирование ацетона
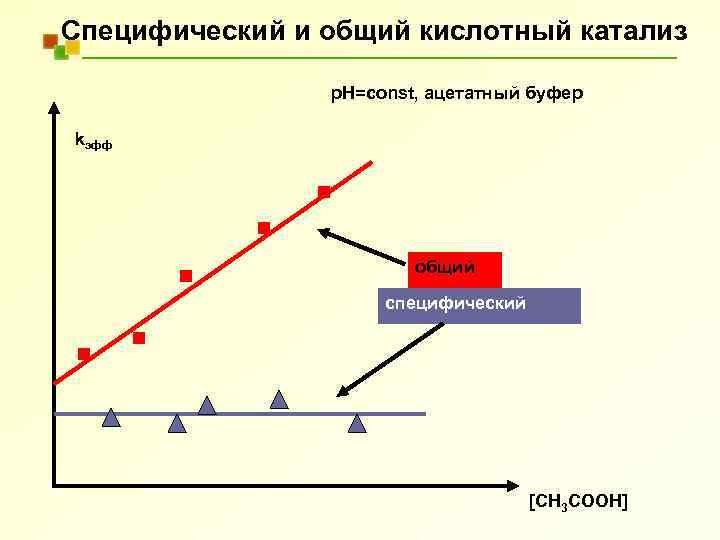 Специфический и общий кислотный катализ p. H=const, ацетатный буфер kэфф общий специфический [CH 3 COOH]
Специфический и общий кислотный катализ p. H=const, ацетатный буфер kэфф общий специфический [CH 3 COOH]


