ОХТ ЛК 9.ppt
- Количество слайдов: 16
 Каталитические процессы Гетерогеннокаталитические процессы Кинетика гетерогеннокаталитических процессов Реакторы для гетерогеннокаталитических процессов
Каталитические процессы Гетерогеннокаталитические процессы Кинетика гетерогеннокаталитических процессов Реакторы для гетерогеннокаталитических процессов
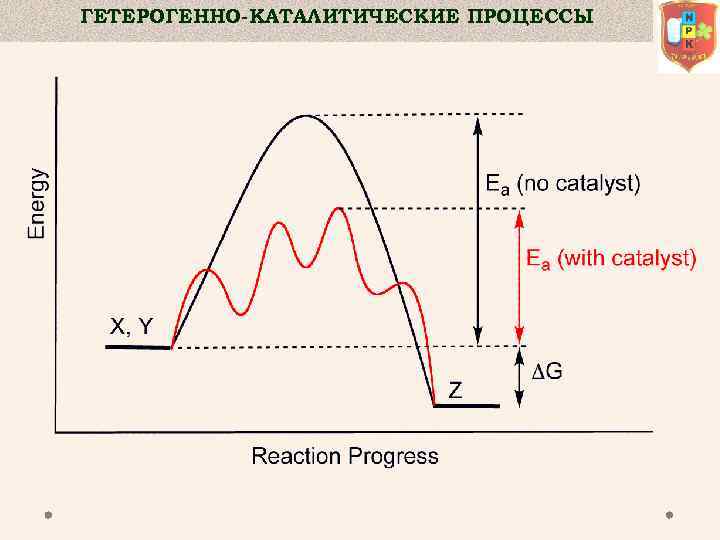
 ГЕТЕРОГЕННО–КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ Катализом называют изменение скорости химических реакций в результате воздействия веществ — катализаторов, которые участвуют в реакции, вступая в промежуточное химическое взаимодействие с реагентами, но восстанавливают свой химический состав по окончании каталитического акта. По фазовому состоянию реагентов и катализатора каталитические процессы разделяют на две основные группы: - гомогенные - гетерогенные.
ГЕТЕРОГЕННО–КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ Катализом называют изменение скорости химических реакций в результате воздействия веществ — катализаторов, которые участвуют в реакции, вступая в промежуточное химическое взаимодействие с реагентами, но восстанавливают свой химический состав по окончании каталитического акта. По фазовому состоянию реагентов и катализатора каталитические процессы разделяют на две основные группы: - гомогенные - гетерогенные.
 ГЕТЕРОГЕННО-КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ
ГЕТЕРОГЕННО-КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ
 ГЕТЕРОГЕННО -КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ Все каталитические реакции по типу взаимодействия между реагентами и катализатором делят на окислительновосстановительные и кислотно-основные. Основные требования к катализаторам Активность катализатора — это мера ускоряющего действия его на данную реакцию. Наиболее часто активность выражают разностью или соотношением скоростей каталитической и некаталитической реакций, степенью превращения исходного реагента или выходом целевого продукта при определенном технологическом режиме. Иногда активность представляют соотношением констант скоростей каталитической и некаталитической реакций или отношением энергий активации. Избирательность (селективность) действия катализаторов важна для большинства каталитических процессов органической технологии, в которых термодинамически возможен ряд параллельных и последовательных реакций. Избирательность некоторых катализаторов позволяет сильно ускорять только одну реакцию из ряда возможных, проводить процесс при такой температуре, при которой подавляются другие реакции.
ГЕТЕРОГЕННО -КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ Все каталитические реакции по типу взаимодействия между реагентами и катализатором делят на окислительновосстановительные и кислотно-основные. Основные требования к катализаторам Активность катализатора — это мера ускоряющего действия его на данную реакцию. Наиболее часто активность выражают разностью или соотношением скоростей каталитической и некаталитической реакций, степенью превращения исходного реагента или выходом целевого продукта при определенном технологическом режиме. Иногда активность представляют соотношением констант скоростей каталитической и некаталитической реакций или отношением энергий активации. Избирательность (селективность) действия катализаторов важна для большинства каталитических процессов органической технологии, в которых термодинамически возможен ряд параллельных и последовательных реакций. Избирательность некоторых катализаторов позволяет сильно ускорять только одну реакцию из ряда возможных, проводить процесс при такой температуре, при которой подавляются другие реакции.
 ГЕТЕРОГЕННО-КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ Температура зажигания — это минимальная температура, при которой процесс начинает идти с достаточной для практических целей скоростью. Термостойкость катализаторов определяет возможность стабильной работы при высоких температурах. Стойкость катализатора к действию контактных ядов — важнейшая характеристика, определяющая возможность отравления катализатора. Отравление катализатора — это частичная или полная потеря активности под действием небольшого количества веществ, называемых контактными ядами. Теплопроводность катализатора является важной характеристикой, т. к. способствует выравниванию температуры в слое контактной массы. Прочность зерен катализатора. Данное свойство должно обеспечивать эксплуатацию катализатора в течение длительного времени.
ГЕТЕРОГЕННО-КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ Температура зажигания — это минимальная температура, при которой процесс начинает идти с достаточной для практических целей скоростью. Термостойкость катализаторов определяет возможность стабильной работы при высоких температурах. Стойкость катализатора к действию контактных ядов — важнейшая характеристика, определяющая возможность отравления катализатора. Отравление катализатора — это частичная или полная потеря активности под действием небольшого количества веществ, называемых контактными ядами. Теплопроводность катализатора является важной характеристикой, т. к. способствует выравниванию температуры в слое контактной массы. Прочность зерен катализатора. Данное свойство должно обеспечивать эксплуатацию катализатора в течение длительного времени.
 КИНЕТИКА ГЕТЕРОГЕННО–КАТАЛИТИЧЕСКИХ ПРОЦЕССОВ Для кинетического моделирования этого сложного превращения его необходимо представить как результат суперпозиции нескольких элементарных процессов: ü Диффузия реагента из объёма к поверхности катализатора (массоперенос). ü Адсорбция реагента на поверхности катализатора. ü Разрыв связей адсорбированных молекул. Химическое превращение реагента в продукт на поверхности катализатора. ü Создание новых связей, формирование адсорбированных молекул продукта. ü Десорбция продукта с поверхности катализатора. Диффузия продукта от поверхности катализатора в объём (массоперенос).
КИНЕТИКА ГЕТЕРОГЕННО–КАТАЛИТИЧЕСКИХ ПРОЦЕССОВ Для кинетического моделирования этого сложного превращения его необходимо представить как результат суперпозиции нескольких элементарных процессов: ü Диффузия реагента из объёма к поверхности катализатора (массоперенос). ü Адсорбция реагента на поверхности катализатора. ü Разрыв связей адсорбированных молекул. Химическое превращение реагента в продукт на поверхности катализатора. ü Создание новых связей, формирование адсорбированных молекул продукта. ü Десорбция продукта с поверхности катализатора. Диффузия продукта от поверхности катализатора в объём (массоперенос).
 КИНЕТИКА ГЕТЕРОГЕННО- КАТАЛИТИЧЕСКИХ ПРОЦЕССОВ Каталитические процессы как частный случай гетерогенных ХТП в зависимости от технологических условий диффузионных и кинетических областях. могут протекать в В присутствии катализатора К бимолекулярная гомогенная реакция А + В = С + … протекает по следующей схеме: 1) образование промежуточного соединения АК А + К = АК; 2) образование активированного комплекса АК + В = (АВ')К; 3) образование конечных продуктов и регенерация катализатора (АВ')К = К + С + …. Если переход от активированного комплекса в отсутствие катализатора к активированному комплексу, возникающему в ходе каталитического процесса, является экзотермическим, т. е. АВ' + К = (АВ')К, Н < 0,
КИНЕТИКА ГЕТЕРОГЕННО- КАТАЛИТИЧЕСКИХ ПРОЦЕССОВ Каталитические процессы как частный случай гетерогенных ХТП в зависимости от технологических условий диффузионных и кинетических областях. могут протекать в В присутствии катализатора К бимолекулярная гомогенная реакция А + В = С + … протекает по следующей схеме: 1) образование промежуточного соединения АК А + К = АК; 2) образование активированного комплекса АК + В = (АВ')К; 3) образование конечных продуктов и регенерация катализатора (АВ')К = К + С + …. Если переход от активированного комплекса в отсутствие катализатора к активированному комплексу, возникающему в ходе каталитического процесса, является экзотермическим, т. е. АВ' + К = (АВ')К, Н < 0,
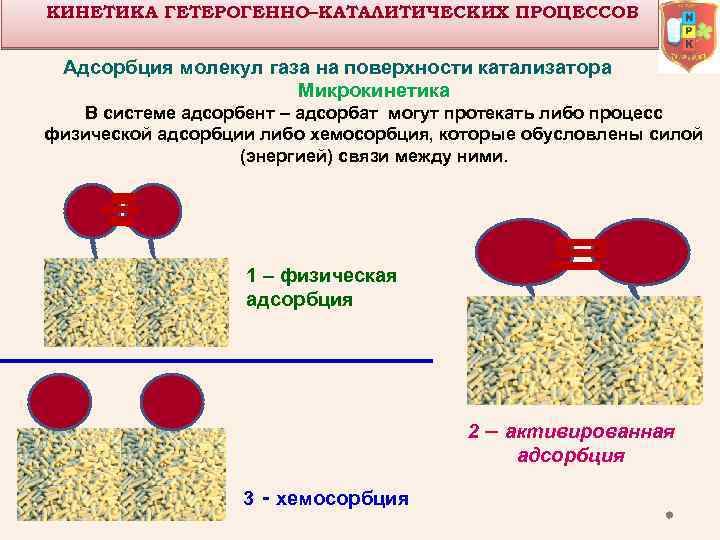 КИНЕТИКА ГЕТЕРОГЕННО–КАТАЛИТИЧЕСКИХ ПРОЦЕССОВ Адсорбция молекул газа на поверхности катализатора Микрокинетика В системе адсорбент – адсорбат могут протекать либо процесс физической адсорбции либо хемосорбция, которые обусловлены силой (энергией) связи между ними. 1 – физическая адсорбция 2 – активированная адсорбция 3 - хемосорбция
КИНЕТИКА ГЕТЕРОГЕННО–КАТАЛИТИЧЕСКИХ ПРОЦЕССОВ Адсорбция молекул газа на поверхности катализатора Микрокинетика В системе адсорбент – адсорбат могут протекать либо процесс физической адсорбции либо хемосорбция, которые обусловлены силой (энергией) связи между ними. 1 – физическая адсорбция 2 – активированная адсорбция 3 - хемосорбция
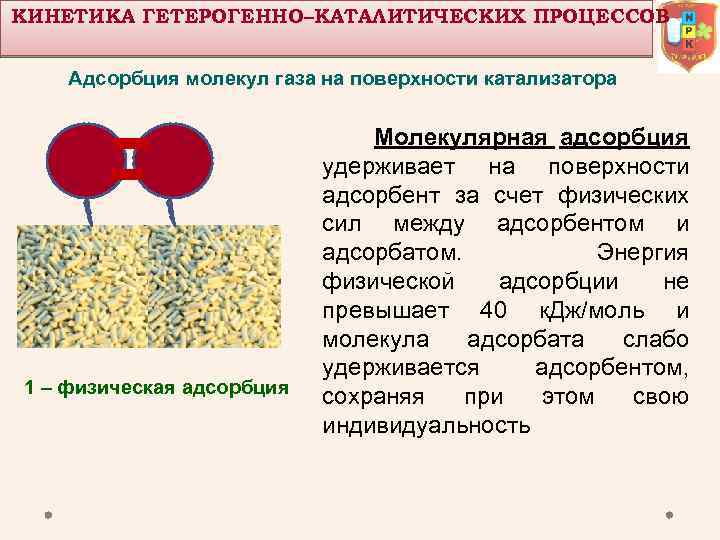 КИНЕТИКА ГЕТЕРОГЕННО–КАТАЛИТИЧЕСКИХ ПРОЦЕССОВ Адсорбция молекул газа на поверхности катализатора Молекулярная 1 – физическая адсорбция удерживает на поверхности адсорбент за счет физических сил между адсорбентом и адсорбатом. Энергия физической адсорбции не превышает 40 к. Дж/моль и молекула адсорбата слабо удерживается адсорбентом, сохраняя при этом свою индивидуальность
КИНЕТИКА ГЕТЕРОГЕННО–КАТАЛИТИЧЕСКИХ ПРОЦЕССОВ Адсорбция молекул газа на поверхности катализатора Молекулярная 1 – физическая адсорбция удерживает на поверхности адсорбент за счет физических сил между адсорбентом и адсорбатом. Энергия физической адсорбции не превышает 40 к. Дж/моль и молекула адсорбата слабо удерживается адсорбентом, сохраняя при этом свою индивидуальность
 КИНЕТИКА ГЕТЕРОГЕННО–КАТАЛИТИЧЕСКИХ ПРОЦЕССОВ Адсорбция молекул газа на поверхности катализатора 2 – активированная адсорбция Активированная адсорбция – адсорбция, которая характеризуется наличием химического взаимодействия между адсорбентом и адсорбатом. Энергия связи – свыше 80 к. Дж/моль. Под воздействием поверхности адсорбента (катализатора) – активного центра – в молекуле газа-адсорбата происходят некоторые изменения, в частности, меняется геометрия молекулы, увеличивается длина связей между атомами, изменяются углы. Молекула ещё сохраняет свою индивидуальность, но за счет изменения геометрии меняются её свойства и она становится реакционоспособной.
КИНЕТИКА ГЕТЕРОГЕННО–КАТАЛИТИЧЕСКИХ ПРОЦЕССОВ Адсорбция молекул газа на поверхности катализатора 2 – активированная адсорбция Активированная адсорбция – адсорбция, которая характеризуется наличием химического взаимодействия между адсорбентом и адсорбатом. Энергия связи – свыше 80 к. Дж/моль. Под воздействием поверхности адсорбента (катализатора) – активного центра – в молекуле газа-адсорбата происходят некоторые изменения, в частности, меняется геометрия молекулы, увеличивается длина связей между атомами, изменяются углы. Молекула ещё сохраняет свою индивидуальность, но за счет изменения геометрии меняются её свойства и она становится реакционоспособной.
 КИНЕТИКА ГЕТЕРОГЕННО–КАТАЛИТИЧЕСКИХ ПРОЦЕССОВ Адсорбция молекул газа на поверхности катализатора 3 - хемосорбция Хемосорбция – образование прочных химических связей между поверхностью адсорбента и адсорбатом. Энергия связи – свыше 100 к. Дж/моль. За счет взаимодействия с поверхностью адсорбента образуются стабильные химические соединения. При этом активность катализатора снижается, т. е. происходит отравление катализатора
КИНЕТИКА ГЕТЕРОГЕННО–КАТАЛИТИЧЕСКИХ ПРОЦЕССОВ Адсорбция молекул газа на поверхности катализатора 3 - хемосорбция Хемосорбция – образование прочных химических связей между поверхностью адсорбента и адсорбатом. Энергия связи – свыше 100 к. Дж/моль. За счет взаимодействия с поверхностью адсорбента образуются стабильные химические соединения. При этом активность катализатора снижается, т. е. происходит отравление катализатора
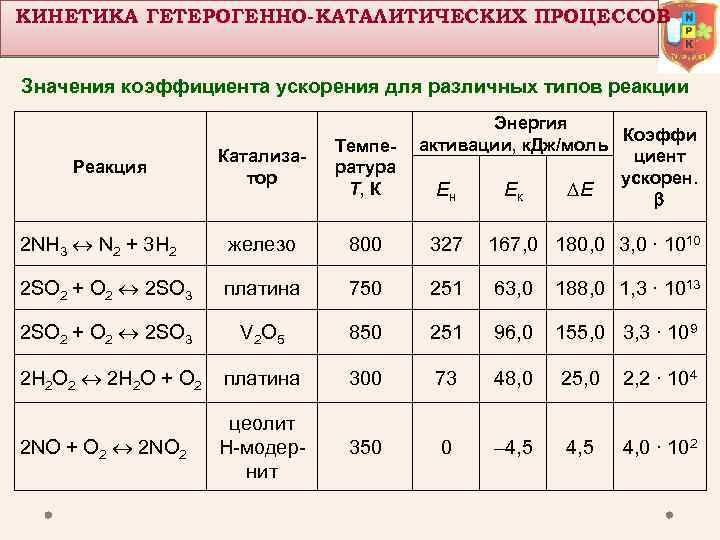 КИНЕТИКА ГЕТЕРОГЕННО-КАТАЛИТИЧЕСКИХ ПРОЦЕССОВ Значения коэффициента ускорения для различных типов реакции Энергия Коэффи активации, к. Дж/моль циент ускорен. Ен Ек Е Катализатор Температура Т, К 2 NH 3 N 2 + 3 H 2 железо 800 327 167, 0 180, 0 3, 0 ∙ 1010 2 SO 2 + O 2 2 SO 3 платина 750 251 63, 0 188, 0 1, 3 ∙ 1013 2 SO 2 + O 2 2 SO 3 V 2 О 5 850 251 96, 0 155, 0 3, 3 ∙ 109 2 H 2 O 2 2 H 2 O + О 2 платина 300 73 48, 0 25, 0 2, 2 ∙ 104 2 NO + O 2 2 NO 2 цеолит Н-модернит 350 0 – 4, 5 4, 0 ∙ 102 Реакция
КИНЕТИКА ГЕТЕРОГЕННО-КАТАЛИТИЧЕСКИХ ПРОЦЕССОВ Значения коэффициента ускорения для различных типов реакции Энергия Коэффи активации, к. Дж/моль циент ускорен. Ен Ек Е Катализатор Температура Т, К 2 NH 3 N 2 + 3 H 2 железо 800 327 167, 0 180, 0 3, 0 ∙ 1010 2 SO 2 + O 2 2 SO 3 платина 750 251 63, 0 188, 0 1, 3 ∙ 1013 2 SO 2 + O 2 2 SO 3 V 2 О 5 850 251 96, 0 155, 0 3, 3 ∙ 109 2 H 2 O 2 2 H 2 O + О 2 платина 300 73 48, 0 25, 0 2, 2 ∙ 104 2 NO + O 2 2 NO 2 цеолит Н-модернит 350 0 – 4, 5 4, 0 ∙ 102 Реакция
 ГЕТЕРОГЕННО-КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ При разработке катализаторов стремятся обеспечить высокую активность путем увеличения как каталитической активности единицы поверхности, так и самой удельной поверхности. Повышение активности единицы поверхности достигается путем правильного выбора состава катализаторов или, как их часто называют, контактных масс. Контактные массы обычно не являются индивидуальными веществами, а представляют смесь собственно каталитически активных соединений с активаторами, тем или иным способом нанесенную на, носители. Активаторы, или промоторы — это вещества, повышающие активность основного вещества-катализатора. При этом сами активаторы могут не обладать каталитическими свойствами. Носители (трегеры) — инертные вещества, на которые наносят каталитически активные соединения или промоторы. Как правило, это пористые вещества с достаточно высокой термостойкостью.
ГЕТЕРОГЕННО-КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ При разработке катализаторов стремятся обеспечить высокую активность путем увеличения как каталитической активности единицы поверхности, так и самой удельной поверхности. Повышение активности единицы поверхности достигается путем правильного выбора состава катализаторов или, как их часто называют, контактных масс. Контактные массы обычно не являются индивидуальными веществами, а представляют смесь собственно каталитически активных соединений с активаторами, тем или иным способом нанесенную на, носители. Активаторы, или промоторы — это вещества, повышающие активность основного вещества-катализатора. При этом сами активаторы могут не обладать каталитическими свойствами. Носители (трегеры) — инертные вещества, на которые наносят каталитически активные соединения или промоторы. Как правило, это пористые вещества с достаточно высокой термостойкостью.
 ГЕТЕРОГЕННО-КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ Основные методы изготовления катализаторов: ü Осаждение гидроксидов или карбонатов из растворов их солей с последующим формованием и термообработкой контактной массы (осажденные катализаторы). ü Смешение порошкообразных каталитически активных веществ, промоторов, носителей и связующих с последующим прессованием и термообработкой (смешанные катализаторы). ü Сплавление нескольких оксидов с последующим восстановлением металлов из оксидов (плавленые катализаторы). Иногда после сплавления одно из веществ удаляют путем выщелачивания (скелетные катализаторы). ü Пропитка пористого носителя раствором, содержащим соли активных элементов, с их последующей сушкой и термообработкой (нанесенные катализаторы). Катализаторы выпускают в виде таблеток, колец, шариков, цилиндрических гранул, сеток и др.
ГЕТЕРОГЕННО-КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ Основные методы изготовления катализаторов: ü Осаждение гидроксидов или карбонатов из растворов их солей с последующим формованием и термообработкой контактной массы (осажденные катализаторы). ü Смешение порошкообразных каталитически активных веществ, промоторов, носителей и связующих с последующим прессованием и термообработкой (смешанные катализаторы). ü Сплавление нескольких оксидов с последующим восстановлением металлов из оксидов (плавленые катализаторы). Иногда после сплавления одно из веществ удаляют путем выщелачивания (скелетные катализаторы). ü Пропитка пористого носителя раствором, содержащим соли активных элементов, с их последующей сушкой и термообработкой (нанесенные катализаторы). Катализаторы выпускают в виде таблеток, колец, шариков, цилиндрических гранул, сеток и др.
 ГЕТЕРОГЕННО–КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ Катализатор процесса окисления орто-ксилола во фталевый ангидрид Катализатор разложения аммиака Катализаторы для процессов: риформинга, изомеризации, гидрокрекинга, гидрирования, гидродеалкилирования
ГЕТЕРОГЕННО–КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ Катализатор процесса окисления орто-ксилола во фталевый ангидрид Катализатор разложения аммиака Катализаторы для процессов: риформинга, изомеризации, гидрокрекинга, гидрирования, гидродеалкилирования
 ГЕТЕРОГЕННО–КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ
ГЕТЕРОГЕННО–КАТАЛИТИЧЕСКИЕ ПРОЦЕССЫ


